Уротелиальный эпителий что это
Обновлено: 25.04.2024
Уротелиальный рак (карцинома) — это злокачественная опухоль, которая развивается из уротелия (эпителия, который покрывает мочевыводящие пути). Данное заболевание может развиваться на уровне чашечно-лоханочной системы почки, мочеточника, мочевого пузыря и уретры. Именно в этих отделах присутствует уротелий. Обычно опухоль возникает у людей от 50 до 80 лет. Мужчины заболевают чаще чем женщины. В 90-95% случаев поражается мочевой пузырь.
Этиология
Риск развития уротелиального рака возрастает в следующих случаях:
- Воздействие ароматических аминов. Данные вещества являются канцерогенными и образуются в различных производственных процессах. К ним относится нефтяная, лакокрасочная, химическая и угольная промышленность. Как правило, уротелиальный рак развивается при длительном контакте с данными канцерогенами.
- Курение. Сигаретный дым повышает риск развития опухоли по различным данным до семи раз.
- Прием некоторых лекарственных препаратов. Имеются основания полагать, что длительный прием некоторых обезболивающих средств и цитостатического препарата — циклофосфамида может вызвать уротелиаальный рак.
- Облучение мочевыделительной системы с целью лечения опухолей другой локализации. Заболевание развивается спустя много лет после воздействия на человека поражающего фактора.
В некоторых странах мира (Судан, Египет) распространены гельминты (шистосомы), которые проникают в мочевыделительную систему, вызывая ее повреждения. Это может способствовать онкологическому перерождению уротелия. Однако Россия не является страной, эндемичной по данному паразитическому заболеванию, поэтому этот механизм не актуален.
Клиническая картина
Чаще всего уротелиальный рак проявляется безболезненной макро- или микрогематурией, то есть кровью в моче в больших или малых количествах. В некоторых случаях может наблюдаться учащенное мочеиспускание, императивные (неотложные, сильные) позывы, боль и жжение при опорожнении мочевого пузыря. Если опухоль находится в области мочеточника или лоханки почки, может отмечаться пальпироваться одностороннее опухолевидное образование в области поясницы, сопровождающееся болью в боку.
Помимо местных симптомов, указывающих на поражение мочевыделительной системы, у пациентов могут возникать системные признаки, общие для многих онкологических заболеваний. К ним относят потерю массы тела, слабость вялость, тошноту, лихорадку. Данные проявления развиваются обычно на поздних стадиях рака.
Классификация
Существуют несколько основных подходов к классификации уротелиального рака. Всемирная организация здравоохранения разделяет данное заболевание на три степени, в зависимости от уровня злокачественности.
В клинической практике наиболее распространена система TNM, которая учитывает характеристики первичной опухоли, состояние лимфоузлов и отдаленные метастазы. На основании этой системы выделяют четыре стадии заболевания.
Также существует морфологическая классификация рака, в которой выделяют следующие формы:
- Высокодифференцированная папиллярная уротелиальная карцинома.
- Низкодифференцированная папиллярная уротелиальная карцинома.
- Плоская неинвазивная уротелиальная карцинома.
- Инвазивная уротелиальная карцинома.
Также существуют редкие морфологические типы уротелиального рака. К ним относятся: гнездный, лимфоэпителиомоподобный и микропапиллярный варианты.
Диагностика
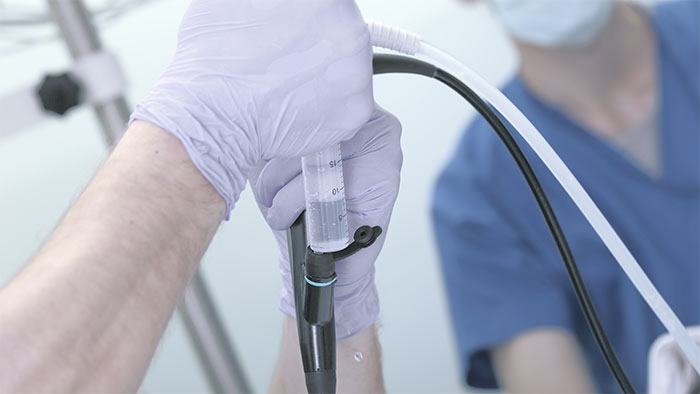
Для диагностики уротелиального рака рекомендуется проводить следующие лабораторно-инструментальные методы исследования:
- Цистоскопия с биопсией.
- Цитологическое исследование мочи.
- Ультразвуковое исследование мочевого пузыря.
- Мультидетекторная компьютерная урография.
- Магниторезонансная томография (МРТ).
- Уретеропиелоскопия с биопсией — эндоскопическое исследование просвета мочеточника и лоханки почки с взятием образца тканей для гистологического исследования.
- Дополнительно выполняется общий анализ крови, мочи, биохимический анализ крови, коагулограмма.
При необходимости, в план обследования могут быть включены и другие методы, а также назначены консультации профильных специалистов. Диагностический этап является чрезвычайно важным, так как он позволяет определить точную форму рака, определить стадию и подобрать эффективное лечение.
Как лечить заболевание
Лечение уротелиального рака зависит от его расположения, стадии и вида. В случае небольших высокодифференцированных опухолей мочевого пузыря золотым стандартом является трансуретральная резекция. Это эндоскопическое вмешательство в полость органа с доступом через уретру. Операция малотравматична. Также возможно лазерное удаление опухолевой ткани. После проведения данных операций пациенту необходимо регулярно проводить цитологическое исследование мочи и цистоскопию. Низкодифференцированный инвазивный рак требует более радикального метода — резекции мочевого пузыря или цистэктомии. При частых рецидивах используется введение в полость органа бацилл Кальмета-Герена (БЦЖ), которые вызывают разрушение опухолевых клеток.

Если опухоль располагается в районе верхних мочевых путей, то выполняется радикальная нефруретерэктомия. Данная операция подразумевает резекцию мочеточника совместно с мочевым пузырем. Кроме того, как правило, хирург удаляет лимфатические узлы.
По показаниям назначается до- и послеоперационная терапия цитостатическими препаратами, содержащими платину. Лучевая терапия также может применяется в сочетании с хирургическим лечением.
Медицинское наблюдение после лечения и прогноз
После лечения уротелиального рака требуется контроль за состоянием пациента с целью раннего выявления возможного рецидива. Пациенту необходимо регулярно проводить цистоскопию и цитологическое исследование мочи. При необходимости назначают и другие методы диагностики, например, УЗИ мочевого пузыря. Точный план наблюдения составляет лечащий врач.
Выживаемость пациентов, в первую очередь, определяется стадией процесса и степенью дифференцировки клеток уротелиального рака. При инвазивной опухоли на последних стадиях пятилетняя выживаемость составляет около 10-50%. Еще одним фактором, влияющим на последующий прогноз, является возраст. Пожилые люди имеют худшие показатели выживаемости по сравнению с молодыми. Наилучших результатов можно добиться при выявлении начальной стадии уротелиальной карциномы и хорошем ответе на проводимое лечение. В такой ситуации зачастую удается достичь длительной ремиссии.

Цель исследования – диагностика потенциально чрезвычайно опасных, угрожающих жизни опухолей уринарного тракта высокой степени злокачественности (HGUC). Цитологическое исследование введено в мировую медицинскую практику в 1945 году Дж. Папаниколау.
Уринарный тракт – это анатомические структуры, выполняющие функцию мочевыделения. Он состоит из почечных лоханок, мочеточников, мочевого пузыря и уретры. Переходный эпителий или уротелий, покрывающий уринарный тракт при определённых обстоятельствах становится источником новообразований, которые весьма разнообразны, как по морфологическому строению, так и по степени злокачественности. Первичные злокачественные опухоли почечной лоханки и мочеточника составляют всего 5-6% от всех опухолей уротелия, так что, основная доля угрожающей жизни патологии приходится на опухоли мочевого пузыря (МЗ РБ ГУ РНПЦ ОМР им. Н.Н. Александрова. «Алгоритмы диагностики и лечения злокачественных новообразований», 2012).

Ежегодно в РБ выявляют 1000-1200 новых случаев рака мочевого пузыря на различных стадиях развития. Страдает преимущественно мужское население. В Европейских странах, в структуре общей онкологической заболеваемости, рак мочевого пузыря занимает 4-е место у мужчин и 14-е – у женщин. В подавляющем числе случаев – это уротелиальная карцинома высокой степени злокачественности (HGUC), которая проявляет себя клинически гематурией, т.е. появлением крови в моче. За последние 20 лет в нашей стране заболеваемость выросла почти в 2 раза. Относительно высокий показатель отношения смертности к заболеваемости, который составляет 0.33, означает, что каждый третий пациент погибает, а это, без сомнений, свидетельствует об отсутствии эффективных неинвазивных методов ранней диагностики.
Каковы же основные причины возникновения рака мочевого пузыря? В настоящее время рассматривают несколько причин злокачественного перерождения уротелия. В Европе, среди этиологических факторов доминируют промышленные химические соединения, а среди них наибольшим канцерогенным действием обладают продукты переработки углеводородов. В странах с высоким уровнем заболеваемости шистосоматозом (Египет), паразитарный агент является основной причиной того, что рак мочевого пузыря занимает по распространённости первое место среди всех онкологических заболеваний (A.S.Felix, A.S. Soliman, H.Khaled (et al.) – 2008. -Vol.19-P.421-429). И, кроме того, более высокий уровень заболеваемости злокачественными заболеваниями уротелиального тракта выявляют среди курильщиков.

В последние годы учёные рассматривают возможность вирусной природы рака мочевого пузыря. Полиомавирус человека 1, более известный, как полиома-BK-вирус, уже многие годы притягивает к себе внимание исследователей в данной области, как потенциально опасный фактор развития неопластических процессов мочевыводящей системы. Этот вирус широко распространён среди всей популяции человека. Можно сказать, что им инфицировано до 90% взрослого населения нашей планеты. Впервые, штамм человеческого полиомавируса был выделен из мочи ещё в 1971 году. В названии этого штамма заглавные латинские буквы BK соответствуют инициалам того пациента, у которого его обнаружили. И за последние два десятилетия, наши представления о роли этого вируса серьёзно эволюционировали. Неоспоримым является тот факт, что при снижении иммунологической защиты, а именно при проведении цитостатической терапии у пациентов с аллографт трансплантацией почек, полиома-BK-вирус является основной причиной BKV аллографт нефропатии, уретрального стеноза и геморрагического цистита (Drachenberg CB, Hirsch HH, Ramos E, Papadimitriou JC (2005). Hum. Pathol. 36: 1245-1255).
Вирус проникает в организм человека через верхние дыхательные пути и долгое время бессимптомно персистирует преимущественно в уротелии, а также в костном мозге, вызывая латентное инфицирование. Здоровая иммунная система контролирует бессимптомное пребывание вируса в организме человека. Однако, при нарушеннии иммунного надзора, возникающего по тем или иным причинам, вследствие угнетения функции иммунитета, происходит активация BKV-вируса. А морфологическим отражением перехода из латентного состояния в активное, является появление специфических клеток. В уротелиальном эпителии вирусные частицы образуют внутриядерные включения, в результате чего, клетка приобретает очень характерные морфологические черты. Первое описание таких клеток с включениями вирусных частиц дал доктор Koss LG 40 лет назад, обнаружив их в моче пациента после проведенной трансплантации почки. Он назвал их Decoy-клетки. Они могут быть 4-х типов и до последнего времени, среди цитопатологов доминируют представления, что эти инфицированные клетки нельзя относить к злокачественным. Но их появление в моче пациента с аллографт трансплантацией, является самым ранним признаком угрозы BKV аллографт нефропатии. На данных рисунках представлены 4 морфологических типа Decoy-клеток.

Иными словами, Decoy- клетки – самые ранние предвестники отторжения трансплантата. Но только с внедрением в практику жидкостных технологий приготовления препарата из свежевыпущенной мочи или из смыва мочевого пузыря, с окраской по Папаниколау, стало возможным обнаруживать эти клетки, и с высокой чувствительностью и специфичностью отличать их от злокачественных. В настоящее время обнаружение Decoy-клеток в моче является скрининговым тестом BKV нефропатии. Кроме того, у пациентов, перенесших трансплантацию почки, наряду с Decoy-клетками, часто обнаруживают клетки уротелия, с признаками выраженной клеточной атипии, соответствующими цитоморфологическим характеристикам уротелиальной карциномы высокой степени злокачественности, а также клетки, которые несут в себе одновременно черты, присущие и Decoy-клеткам, и клеткам HGUC. Эти клетки не только имеют смешанные черты Decoy-клеток и злокачественных, но и несут в себе протеины (SV-40 T) полиома-BK-вируса (Galed-Placed I, Valbuena-Ruvira L. Diagn Cytopathol.2011 Dec;39(12):933-7). Многие из клинических случаев, описанных в литературе, свидетельствуют о возможной онкогенной роли полиома-BK-вируса в возникновении уротелиальной карциномы (Hassan S, Alirhayim Z, Ahmed S, Amer S. Case Rep Nephrol.2013; 2013:858139). Протеины BKV оказывают повреждающее действие на синтез белков-супрессоров опухолевого роста (р53), что приводит к нарушению процесcов восстановления ДНК. Этот патогенетический механизм лежит в основе возникновения генетически нестабильных изменений, приводящих к трансформации нормального уротелия сначала в диспластичный, а затем в уротелиальную карциному высокой степени злокачественности (HGUC). HGUC характеризуется высокой частотой рецидивов и прогрессии до мышечно-инвазивных стадий Т2,Т3,Т4 с метастазами в лимфатические узлы. в 95% случаев всех смертельных исходов от рака мочевого пузыря устанавливают диагноз HGUC.

Итак, достоинства цитологического исследования уротелиального тракта:
- Неинвазивность процедуры (анализ из «баночки»);
- Высокая специфичность диагностики HGUC, приближающаяся к 100%;
- Высокая чувствительность диагностики HGUC ~ 80%;
- ~30-70% пациентов с HGUC выживают;
- ~5-15% случаев HGUС прогрессируют; статистика США.
- 535 000 пациентов с раком мочевого пузыря выжили.

Предпочтительной технологией приготовления цитологического препарата мочи является жидкостная осаждением (BD SurePath), которую мы используем в нашей лаборатории. Тонкослойные мазки позволяют проводить дальнейшую диагностику с использованием всего арсенала молекулярно-генетических методов ( иммуноцитохимия, FISH, и т.д.).
Цитологический диагноз HGUC объединяет в себе все генетически нестабильные злокачественные опухоли уротелия, гистологически весьма разнообразные. С целью оптимизации подходов к интерпретации уринарной цитопатологии и стандартизации критериев диагностики, на международном конгрессе в Париже, в 2013 году была принята новая цитологическая система классификации. Она во многом напоминает систему Bethesda для цитологического анализа патологии щитовидной железы и цервикального канала.
Итак, цитологическое исследование мочи с применением жидкостных технологий приготовления мазка и использованием диагностических критериев Парижской классификации 2014 года, является основным неинвазивным методом диагностики и мониторирования уротелиальной карциномы высокой степени злокачественности.
Выделяют отдельную группу заболеваний мочевого пузыря, которые могут быть результатом острого или хронического воспаления. К ним относятся уротелиальная гиперплазия, реактивные и метапластические изменения уротелия. Гиперплазия уротелия и плоскоклеточная метаплазия характерны для мочепузырного треугольника. Эпителиальная гиперплазия – это доброкачественная пролиферация уротелия в ответ на воспаление или раздражение, характеризуется гистологически нормальным уротелием и увеличением числа слоев клеток уротелия. Реактивные изменения уротелия всегда связываются с острым или хроническим воспламенением в собственной пластинке слизистой и вызываются бактериями, травмой, химическими или токсическими агентами. Клетки уротелия при этом теряют полярность, их размеры и форма не меняются, испытывают недостаток в ядерном хроматине, повреждается ядерная мембрана. Пациенты с реактивными изменениями уротелия не находятся в группе риска перерождения в уротелиальную неоплазию.
Плоскоклеточная метаплазия – это доброкачественное пролиферативное и метапластическое образование, в котором нормальный уротелий замещен неороговевающим плоским эпителием. Она наиболее часто проявляется в виде белесых округлых участков в области треугольника мочевого пузыря у женщин. Является вариантом нормы. При цистоскопии участки плоскоклеточной метаплазии без ороговения выглядят как бледные серовато-белые островки с неровными контурами, чаще всего локализуются в области треугольника и иногда окружены зоной гиперемии. Другой вариант плоскоклеточной метаплазии уротелия характеризуется выраженными признаками ороговения и является лейкоплакией. Лейкоплакия мочевого пузыря обычно развивается как защитная реакция на хроническое воспаление или длительное воздействие повреждающих факторов (конкрементов, катетеров, дренажных трубок). По международной классификации лейкоплакию относят к неопухолевым изменениям эпителия. Тем не менее многие исследователи склонны считать плоскоклеточную метаплазию с ороговением «фоновым процессом для карциномы мочевого пузыря». При лейкоплакии риск развития рака возрастает при условии развития акантоза и дисплазии уротелия. Цистоскопическая картина сформировавшихся очагов лейкоплакии характеризуется наличием серовато-белых или желтого цвета бляшек, возвышающихся над уровнем слизистой оболочки. Применяемые методы оперативного лечения хронического цистита с лейкоплакией мочевого пузыря – трансуретральная резекция, электрокоагуляция, вапоризация.
Практически неотличимые от рака мочевого пузыря по цистоскопической картине изменения могут быть обусловлены так называемой нефрогенной метаплазией уротелия. Речь идет о процессе, морфологическим отражением которого является формирование в стенке мочевого пузыря очагов, напоминающих при микроскопическом исследовании дистальные извитые канальцы почки. Развитие нефрогенной метаплазии принято связывать с травмой мочевыводящих путей, хирургическими вмешательствами на органах таза, проведением внутрипузырной химиотерапии и иммунотерапии (тиофосфамид, вакцина BCG). Клинически нефрогенная метаплазия может протекать бессимптомно или проявляться гематурией и дизурией. Единственным методом исследования, позволяющим достоверно диагностировать нефрогенную метаплазию и отличить ее от опухоли, является биопсия пораженного участка стенки мочевого пузыря. При бессимптомном течении рекомендует ограничиться наблюдением с ежегодным цистоскопическим контролем и цитологическим исследованием мочи, при наличии клинических проявлений выполняют трансуретральную резекцию.
Несмотря на то, что изучению хронического цистита посвящено множество исследований, эпидемиология заболевания свидетельствует об актуальности проблемы. Существует настоятельная необходимость углубленного изучения симптомов, клинических проявлений воспалительных заболеваний мочевого пузыря для усовершенствования диагностики больных хроническим циститом. Выявление корреляции клинических и морфологических проявлений воспалительных заболеваний мочевого пузыря позволит оценить гистоморфологические изменения стенки мочевого пузыря в зависимости от вида воспалительного процесса. Необходимо определить прогностическую значимость биопсии мочевого пузыря у больных неспецифическим циститом и хронической тазовой болью. Понимание патогенеза и клинических проявлений воспалительных заболеваний мочевого пузыря невозможно без детального изучения морфологических изменений.
Переходноклеточный рак — это злокачественная опухоль, которая развивается из клеток переходного эпителия, локализующегося преимущественно в органах мочевыделительной системы. Другое название данного вида опухоли — уротелиальный рак.
Причины возникновения и факторы риска
- Наличие производственных вредностей, в частности контакт с ароматическими аминами и их производными. Переходноклеточный рак может возникнуть через 20 лет после контакта с химическими канцерогенами.
- Курение табака. Табачный дым в 2,5-7 раз увеличивает вероятность развития переходноклеточного рака.
- Хронический цистит, вызванный шистосомозом — эндемичным заболеванием, распространенным в северной Африке.
- Хронические бактериальные инфекции верхних мочевыводящих путей и мочевого пузыря.
- Мочекаменная болезнь.
- Длительный прием некоторых лекарственных препаратов, в частности анальгетиков.
Симптоматика
Как правило, самым первым симптомом переходноклеточного рака является гематурия — примесь крови в моче. Если ее мало, моча может не менять цвет или приобретать розовый оттенок. При выраженной гематурии моча будет красной, в ряде случаев со сгустками крови. При обильных кровотечениях может развиться тампонада мочевого пузыря с острой задержкой мочи.
Хронические кровотечения приводят к развитию анемии. Это сопровождается бледностью кожных покровов, слабостью, ухудшением качества ногтей и волос, снижением уровня гемоглобина в общем анализе крови.
По мере разрастания опухоли, больных начинают беспокоить явления дизурии: учащенное мочеиспускание, императивные позывы, чувство неполного опорожнения мочевого пузыря. Вскоре возникает боль. Сначала она присутствует при наполненном мочевом пузыре и во время мочеиспускания, но затем становится постоянной и локализуется над лонной костью, в области поясницы или промежности.
При раке мочеточника может возникнуть задержка оттока мочи с развитием гидронефроза. Это может приводить к отекам, симптомам интоксикации, развитию артериальной гипертензии и хронической почечной недостаточности.
Классификация
Переходноклеточный рак классифицируют по степени злокачественности. Здесь выделяют 4 группы:
- Высокодифференцированный переходноклеточный рак.
- Умереннодифференцированный переходноклеточный рак.
- Низкодифференцированный рак.
- Недифференцированный рак.
Соответственно увеличение злокачественности идет по нарастающей. Наиболее благоприятный прогноз — при опухолях высокой степени дифференцировки, и, соответственно, наиболее агрессивным течением отличаются недифференцированные формы переходноклеточного рака.
Диагностика
Для диагностики переходноклеточного рака применяют следующие методы:
Лечение
Радикальное излечение переходноклеточного рака может быть достигнуто только с помощью хирургического вмешательства, объем которого зависит от степени инвазии опухоли. Если это немышечноинвазивное новообразование, выполняют резекцию пораженного фрагмента органа, например, трансуретральную резекцию мочевого пузыря или мочеточника.
При мышечноинвазивной опухоли мочевого пузыря необходимо полное удаление пораженного органа с окружающими тканями: удаляют сам пузырь, околопузырную клетчатку, простату, матку с придатками, лимфатические узлы и, при необходимости, часть уретры. При поражении мочеточника удаляется почка, сам мочеточник и частично мочевой пузырь (зависит от локализации). При удалении мочевого пузыря производятся различные виды пластических операций по формированию ортотопического мочевого пузыря.
Если новообразование нерезектабельно, или проведено нерадикально, проводят паллиативные операции. Например, выводят на кожу уретерокутанеостому (мочеточники) или нефростому. В этом случае моча будет отводиться в специальный контейнер или мешок, крепящийся к стоме.

Химиотерапия
При переходноклеточном раке может применяться локальная или системная химиотерапия. Локальная предполагает инстилляции химиотерапевтических препаратов в мочевой пузырь и мочеточник. Ее обязательно проводят после органосохраняющих операций. В дальнейшем, по показаниям инстилляции могут повторяться. Системная химиотерапия показана после нерадикального лечения, а также при высоких рисках развития рецидивов и образования микрометастазов.
Иммунотерапия
В рамках иммунотерапии при переходноклеточном раке используются инстилляции вакцины БЦЖ. Изначально она разрабатывалась и применялась для профилактики туберкулеза. Но была показана ее эффективность и для стимуляции противоопухолевого иммунитета при терапии переходноклеточного рака.
Лучевая терапия
Лучевая терапия может применяться в рамках радикального лечения, адъювантной и неоадъювантной терапии.
Восстановление
Период восстановления после лечения рака мочевыводящих путей занимает несколько месяцев. В это время заживают послеоперационные раны, пациент учится ухаживать за стомой или опорожнять неоцистис (искусственный мочевой пузырь). Более подробные рекомендации даст лечащий доктор с учетом особенностей проведенного лечения.
Осложнения
При отсутствии лечения переходноклеточного рака развиваются следующие осложнения:
- Сдавление опухолью стенки мочеточника, нарушение оттока мочи и гидронефроз. В тяжелых случаях развивается почечная недостаточность вплоть до уремии — отравления организма продуктами обмена белка, которые в норме должны выводиться с мочой.
- Опухоли больших размеров склонны к распаду, что приводит к кровотечениям и присоединению инфекции. В результате развиваются циститы и пиелонефриты. Моча приобретает гнойных характер.
- В ряде случаев опухоль прорастает в тазовые органы — матку, прямую кишку, влагалище. В результате образуются свищи, сопровождаемые характерной симптоматикой, например, выделением мочи из влагалища, хроническими вагинитами и др.
Прогноз
Прогноз при раке мочевыводящих путей зависит от инвазивности опухоли, степени ее дифференцировки и общего состояния на момент первичного лечения. В случае неинвазивных опухолей, излечения удается достичь в 80-85% случаев. При инвазивном раке этот процент колеблется в пределах 15-20. Химиотерапия хоть и не дает возможности устранить злокачественный процесс, но позволит его стабилизировать на какое-то время.
Профилактика
Профилактика рака мочевыводящих путей заключается в применении следующих мероприятий:
- Отказ от курения.
- Использование средств защиты при работе с профессиональными вредностями и бытовой химией.
- Своевременное лечение заболеваний мочевыделительной системы.
- Использование чистой питьевой воды.
Кроме того, для профилактики переходноклеточного рака стоит соблюдать принципы здорового питания, а также поддерживать физическую активность на должном уровне.
Онкологи называют рак мочеточника уротелиальным раком верхних мочевыводящих путей. Уротелиальный потому что рак развивается из клеток эпителия, выстилающего выводящие мочу органы. Верхние мочевыводящие пути — это почечная лоханка и мочеточник. К нижним путям относят мочевой пузырь.
Внутренняя поверхность органов выстлана многослойным переходным — уротелиальным – эпителием. Под раком почки подразумевается поражение только почечной паренхимы, а выработанная тканью почки моча собирается в другой части почки — почечной лоханке, затем проходит мочеточником и до времени скапливается в мочевом пузыре.

В мочеточнике образуются и эпидермоидный рак, и аденокарциномы, но очень-очень редко — в 1% всех злокачественных опухолей мочеточника. Самый частый уротелиальный рак, конечно, рак мочевого пузыря, на него приходится до 90%, на втором месте по частоте — рак почечной лоханки, а после — рак мочеточника. Вместе на лоханку и мочеточник приходится где-то 5–10% или 1–2 случая на 100 тысяч населения. Поскольку эпителий, выстилающий мочевыводящие пути, одинаковый, рак может возникать сразу в нескольких местах и органах. На такое сочетанное поражение мочевого пузыря, мочеточника или лоханки приходится чуть более 12%.
При любом раке после радикальной операции возможен рецидив, причем при раке верхних мочевыводящих путей почти у половины больных опухоль возникает в дотоле не задействованном в опухолевом процессе мочевом пузыре. У 5% рецидив может развиться в эпителии противоположной больному мочеточнику почечной лоханке. Поэтому рак мочеточника называют уротелиальным раком верхних мочевыводящих путей или коротко УРВМП.
Факторы риска рака мочеточника
Все уротелиальные раки вместе занимают четвёртое место в структуре злокачественных опухолей. Рак мочеточника — далеко не болезнь молодых, основную когорту составляют пожилые люди, перешагнувшие 70-летие, преимущественно мужчины, женщины болеют им в три раза реже. Видимо, скоро статистика по полу изменится, потому что фактором риска рака мочеточника является курение, мужское курение снижается, тогда как женское неуклонно растёт. Вот уже женщины часто стали болеть раком лёгкого, теперь на очереди рак уротелия — мочевого пузыря и мочеточника. Табак увеличивает вероятность УРВМП в семь раз.
Ещё в ХVIII веке было замечено, что красильщики слишком часто болеют раком мочевого пузыря, про рак мочеточника тогда тоже догадывались, но диагностика была слабовата. Сегодня рак мочеточника - профессиональное заболевание для работников лакокрасочной, текстильной, химической промышленности, нефтяников и шахтёров. На здоровье оказывают влияние два, абсолютно вредных, и даже запрещённых вещества: бензидин и нафталин. Достаточно семилетнего контакта по работе с этими канцерогенами, чтобы через полтора-два десятилетия попасть на приём онкоуролога и провести с ним остаток своей жизни.
Прогноз
Эпителиальная выстилка мочевого пузыря и мочеточника одинаковая, только стенка мочеточника много тоньше, поэтому опухоль довольно быстро её прорастает, что означает уже переход в другую — не раннюю стадию и распространение на другие органы и ткани. В мочевом пузыре мощный мышечный слой, поэтому в нём не так часто, как в мочеточнике выявляют опухоль, перешедшую в третью стадию, то есть проросшую мышцу, 15% против 60% при УРВМП. Отсюда и много худший прогноз в отношении продолжительности жизни: при II–III стадии рака мочеточника меньше половины больных живут больше 5 лет, при выходе рака за всю стенку мочеточника на этот срок жизни может надеяться только каждый десятый. Половая принадлежность не отражается на прогнозе, как не считалось раньше, но возраст оказывает влияние, чем старше, тем хуже перспективы. И совсем не потому, что есть ограничения в лечении пожилых людей.
Классификация
Классификация и морфологическая структура рака мочеточника похожа на таковые при раке мочевого пузыря. Также развиваются плоские опухоли или рак in situ, когда злокачественные клетки ещё не вышли за пределы «малой родины», не имеют собственных сосудов, то есть рак в зачатке. Следующий этап развития — неинвазивный рак, злокачественный потенциал которого невысокий. И далее инвазивный рак, внедряющийся в ткани.
Стадирование по TNM не учитывает размер опухолевого узла, а только прорастание стенки мочеточника. Вся стенка мочеточника — три жиденьких слоя.
- Первый уровень или Т1 — преодоление клетками, возникшими в слизистой оболочке, подслизистой соединительнотканной основы.
- Второй или Т2 — вовлечение в опухолевый процесс мышечного слоя.
- Третий или Т3 — рак продвинулся в окружающую мочеточник жировую клетчатку.
- Четвёртый уровень распространения или Т4, когда рак мочеточника прошёл в соседние органы. Но это всё ещё местное распространение, даже с поражёнными метастазами лимфатическими узлами, цепочки которых рассыпаны от почек до малого таза. Четвёртая стадия рака мочеточника — это метастазы в отдалённых органах.

Клиническая симптоматика
Главная и единственная функция мочеточника — проведение мочи от почки в мочевой пузырь. Растущая опухоль перекрывает просвет трубки, а он всего около 12 мм, нарушая отток мочи. При блокировке тока мочи по мочеточнику почечная лоханка раздувается от мочи — гидронефроз. Переполненная мочой лоханка вынуждает почку прекратить выработку мочи. Почки в принципе не болят, поэтому всё это проходит незаметно для владельца до тех пор, пока не вспыхнет инфекция. Вот тогда температура, боль в пояснице, мутная моча. Тогда говорят, что на фоне гидронефротической трансформации почки развилось воспаление или пиелонефрит.
Боли появляются при прорастании опухолью соседних структур, когда уже через брюшную стенку неполного пациента можно прощупать опухоль. Ранним признаком рака служит появление в моче эритроцитов, если мочу сдать на анализ по другому поводу или при диспансеризации. Окрашивание мочи кровью свидетельствует о немаленькой опухоли. Если у больного на фоне выраженного недомогания снижается вес, то стоит думать о метастатическом распространении опухолевого процесса по организму.
Обследование
Недавно самым важным методом диагностики опухоли мочеточника было рентгенологическое исследование — экскреторная урография, когда в вену водили контрастное вещество и под рентгеном смотрели его выделение почками, делая снимки в определённые фазы исследования. После снимки смотрели и находили нарушение выделения контраста по мочевыводящим путям. Это обследование урологи не доверяли даже рентгенологам, важно было отследить весь процесс, от этапа к этапу.
Сегодня «золотым» стандартом стала мультидетекторная компьютерная урография, которая почти стопроцентно выявляет опухоли мочеточника больше 5 мм, и даже менее 3 мм, но уже не с таким результатом. Она позволяет оценить всю стенку мочеточника. Чуть менее чувствительна МРТ. Прекрасно показала себя в диагностике уретероскопия — эндоскопическое исследование мочеточника, при которой можно взять кусочек опухоли на гистологическое исследование. Ну, а на первом этапе можно взять мочу на цитологическое исследование, если под микроскопом найдут раковые клетки, то высока вероятность прорастания раком мышечной стенки мочеточника. При этом надо наверняка быть уверенным, что в мочевом пузыре полный порядок и нет рака.

Лечение
При всех злокачественных опухолях, кроме опухолей кроветворной и лимфатической тканей, один радикальный путь спасения — операция. Вне зависимости от уровня поражения мочеточника, достигающего более 30 см, выполняется радикальная нефроуретерэктомия: удаление почки, мочеточника и части мочевого пузыря одним блоком. Естественно, что опухоль должна быть удаляемой, то есть не прорастает в соседние структуры. Обязательно резецируют часть мочевого пузыря во избежание развития рецидивной опухоли. Отмечено, что операция с отсрочкой в полтора месяца после выявления опухоли значительно ухудшает результат лечения.
С лапароскопическими операциями ещё не определились окончательно, есть вопросы по безопасности в отношении рассеивания раковых клеток. Также не определились, какие лимфатические узлы надо удалять профилактически, но удаляются все поражённые опухолью. Сегодня с ограничениями выполняют органосохраняющую резекцию мочеточника по сегментам, потому что при большой опухоли радикальность такой операции сомнительна. Для сегментарной резекции должны быть показания, к примеру, поражение опухолью мочеточника единственной почки или почечная недостаточность, когда удаление одной почки только ухудшит состояние и укоротит жизнь.
При больших опухолях и сомнительной радикальности операции подключают лучевую терапию, при неоперабельном раке возможно сочетание лучевой и химиотерапии.
Кажется, что такой простой орган с одной-единственной функцией, а как сложно протекает и лечится. Но всё преодолимо, и врачи «Евроонко» готовы помочь.
Читайте также:

