Витамин а при лечении папиллом
Обновлено: 27.04.2024
Помимо ярко выраженного антибактериального эффекта витамин D также оказывает противовирусное действие. Увеличивая экспрессию интерферона альфа, кателицидина, дефенсина и противовирусных микроРНК, витамин D активирует различные механизмы врожденного противовирусного иммунитета. Результаты фундаментальных и клинических исследований показывают необходимость компенсации дефицита витамина D для успешной терапии вирусных гепатитов, респираторной и папилломавирусной инфекций. Противовирусные эффекты витамина D также важны для повышения эффективности профилактики и терапии опухолевых заболеваний шейки матки.
- КЛЮЧЕВЫЕ СЛОВА: рак шейки матки, вирус папилломы человека, инфекции, заболевания кишечника, артрит, дерматит, Аквадетрим
Помимо ярко выраженного антибактериального эффекта витамин D также оказывает противовирусное действие. Увеличивая экспрессию интерферона альфа, кателицидина, дефенсина и противовирусных микроРНК, витамин D активирует различные механизмы врожденного противовирусного иммунитета. Результаты фундаментальных и клинических исследований показывают необходимость компенсации дефицита витамина D для успешной терапии вирусных гепатитов, респираторной и папилломавирусной инфекций. Противовирусные эффекты витамина D также важны для повышения эффективности профилактики и терапии опухолевых заболеваний шейки матки.
Рис. 1. Экспрессия вирусной РНК Con1-1b и J6/JFH-1 в культурах гепатоцитов под воздействием 1,25(OH)2D. Клетки обрабатывали 1,25(OH)2D в концентрациях от 0 до 0,4 мкМ в течение 48 часов, после чего их собирали и экстрагировали РНК. Уровни вирусной РНК изм
Рис. 3. Гистопатология поражений кожи, вызванных ДМБА, у мышей с делецией VDR(-/-). Участки опухолей кожи, окрашенные гематоксилином/эозином, получены от мышей с делецией VDR(-/-) через шесть месяцев после воздействия ДМБА:
Рис. 4. Результат воздействия канцерогена ДМБА на пролиферативный маркер BrdU у мышей с делецией VDR(-/-).
Рис. 5. Количественная оценка толщины эпидермиса (А) и клеток с маркером BrdU (Б) у мышей VDR(+/+) и VDR(-/-), обработанных ДМБА
Витамин D – комплексный регулятор врожденного и приобретенного иммунитета, поэтому недостаточность этого витамина снижает антибактериальный и противовирусный иммунитет, стимулирует развитие патологий, ассоциированных с хроническим системным воспалением (атопического дерматита, ревматоидного артрита, воспалительных заболеваний кишечника, аутоиммунных заболеваний щитовидной железы и сепсиса). Результаты фундаментальных и клинических исследований показали, что возникающие на фоне недостаточности витамина D хроническое воспаление и нарушения врожденного иммунитета значительно снижают резистентность организма к туберкулезу, хроническому бронхиту, вирусным заболеваниям (вирусному гепатиту, острому респираторному заболеванию, папилломавирусной инфекции) [1, 2]. Таким образом, обеспеченность витамином D может существенно влиять на иммунитет, в том числе на противовирусную защиту организма.
Противодействие инфекционным заболеваниям играет важную роль в акушерско-гинекологической практике. В частности, вирусные и бактериальные заболевания на фоне недостаточного уровня витамина D повышают риск развития опухолей эндометрия, яичников и шейки матки [3]. Кроме того, иммуномодулирующее, антипролиферативное, проапоптотическое, антиангиогенное, противовоспалительное и противоопухолевое действие витамина D, обнаруженное в фундаментальных и клинических исследованиях, – еще один аргумент в пользу назначения витамина D для профилактики и терапии различных «гинекологических» опухолей, в том числе рака шейки матки [4].
В настоящей статье последовательно рассмотрены молекулярные основы противовирусного действия витамина D, результаты фундаментальных и клинических исследований, указывающие на действие витамина D против вирусов гепатита, Эпштейна – Барр, папилломы человека (ВПЧ), респираторно-синцитиального вируса и др. Показана целесообразность применения витамина D в профилактике и терапии опухолевых заболеваний шейки матки.
О молекулярных механизмах противовирусного действия витамина D
Витамин-D-индуцированные механизмы, связанные с противовирусной активностью, включают корректировку врожденного иммунного ответа (интерфероны), повышение уровней кателицидина (LL-37) и дефенсина, а также активацию специфических противовирусных микроРНК. Витамин D усиливает эффект интерферона, уменьшая синтез вирусных белков в зараженных вирусами клетках. Например, при инфицировании гепатоцитов в культуре вирусом гепатита С воздействие витамина D в форме 1,25(OH)2D активирует гены, связанные с аутофагией вирусных частиц (рецептор 37 G-белков (GPR37), фактор, индуцируемый гипоксией 1-альфа (HIF-1-альфа), хемокиновый лиганд 20 (CCL20)), и подавляет интенсивность репликации вируса (рис. 1) [5].
Одна из основ противовирусного действия витамина D – повышение экспрессии антимикробных пептидов кателицидина и бета-дефенсина 2 [6], которые проявляют не только микробицидную, но и противогрибковую и противовирусную активность [7].
Антимикробный пептид кателицидин – неотъемлемый компонент витамин-D-зависимого врожденного антимикробного иммунитета. Антимикробные пептиды встраиваются в цитоплазматическую мембрану бактерий и белковые оболочки вирусов и, приводя к образованию пор, нарушают целостность бактерий и вирусов. Кроме того, проникая внутрь бактерий и вирусов, положительно заряженные антимикробные пептиды связываются с отрицательно заряженными ДНК и РНК, что также стимулирует гибель бактерий и вирусов.
Обработка моноцитов в культуре посредством биологически активной формы витамина D (1,25(OH)2D) дозозависимо повышала экспрессию мРНК антимикробного пептида кателицидина в 48–140 раз, причем увеличение экспрессии гена кателицидина коррелировало с повышенной экспрессией белка кателицидина [8]. В клиническом исследовании установлена корреляция между уровнями 25(OH)D и кателицидина в плазме крови (фактор корреляции 0,45, р = 0,05) [9]. Более высокая концентрация кателицидина в плазме существенно (в 3,7 раза) снижала риск смерти от инфекции у пациентов с диализом [10].
Витамин D повышает экспрессию определенных микроРНК, которые проявляют противовирусные и онкопротективные свойства. Напомним, что микроРНК представляют собой короткие специфические фрагменты РНК, которые ассоциируются с матричной РНК для синтеза того или иного белка и осуществляют тонкую настройку экспрессии этого белка. Иначе говоря, посредством микроРНК синтезируется столько молекул белка, сколько нужно для потребностей клетки. Как недостаточный, так и избыточный синтез белков может приводить к развитию опухолей.
Витамин D и активированные им микроРНК (в частности, miR-155 и miR-146) тормозят экспрессию целевых специфических белков, ассоциированных с формированием избыточного воспаления: толл-подобных рецепторов 2 и 4, фактора некроза опухоли альфа, интерлейкинов 1-бета и 6, транскрипционного фактора NF-kB, киназного комплекса IkB (IKK), супрессора сигналинга цитокинов 1 (SOCS1) [11]. Активная форма витамина 1,25(OH)2D потенцирует ингибирующее действие miR-130а при репликации вируса гепатита C [5], повышающего риск опухолевых процессов в печени в десятки раз. Фундаментальные исследования показали, что воздействие витамина D на иммунитет также осуществляется посредством регуляции деления Т-хелперных лимфоцитов, дифференцирования В-клеток, секреции интерферона и других цитокинов, что способствует снижению избыточного воспаления [1].
Витамин D против вирусного гепатита
25(OH)D подавляет продукцию вируса гепатита С. Клетки HuH-7 в культуре были инфицированы вирусом гепатита С в присутствии или в отсутствие витамина D. 25(OH)D дозозависимо уменьшал вне- и внутриклеточный уровни основного антигена вируса гепатита С. Ингибирующее действие 25(OH)D осуществлялось на стадии сборки инфицирующего вирусного комплекса [12].
25(OH)D подавляет репликацию вируса гепатита С и способствует более быстрому вирусологическому ответу организма. Выживаемость клеток и нагрузка вирусом наблюдались в линиях клеток Con1-1b и J6/JFH-2a в культуре, обработанных различными дозами 25(OH)D. Вирусная нагрузка клеток Con1-1b дозозависимо снижалась на 69, 80 и 86% после обработки 1, 5 и 10 мкМ 25(OH)D соответственно (р 3+ - и CD 4+ -T-лимфоцитов и отношение CD 4+ /CD 8+ значительно увеличивались (p 30 нг/мл (ОР 1,57, 95% ДИ 1,12–2,2), особенно у пациентов, получавших витамин D (ОР 4,59, 95% ДИ 1,67–12,63). Важно отметить, что противовирусный эффект витамина D не зависел от генотипа вируса гепатита С [16].
Витамин D против других вирусов
Респираторно-синцитиальная вирусная инфекция ослабляет противовирусную и противоопухолевую защиту организма путем негативного воздействия на метаболизм витамина D. При заражении клеток респираторно-синцитиальные вирусы уменьшают экспрессию рецептора витамина D (Vitamin D Receptor – VDR) и увеличивают экспрессию фермента 1-бета-гидроксилазы, которая инактивирует витамин D [19].
Витамин D способствует усилению противовирусной защиты бронхиальных эпителиальных клеток при участии противовирусного и антибактериального пептида кателицидина и активации сигнальных путей интерферона [20]. Поддерживая противовирусный иммунитет, витамин D также снижает вызываемую респираторно-синцитиальным вирусом активацию провоспалительного фактора NF-kB и соответствующих цитокинов в эпителии дыхательных путей. Витамин D индуцирует белок IkBa, ингибитор фактора NF-kB, и снижает вызываемую респираторно-синцитиальным вирусом активацию провоспалительных генов, управляемых NF-kB (интерферон бета, CXCL10 и др.). Ингибирование NF-kB посредством аденовирусных частиц, содержащих IkBa, имитировало эффекты витамина D. Таким образом, витамин D уменьшал воспалительную реакцию в ответ на вирусные инфекции, не снижая при этом противовирусного действия [21].
Метаанализ 25 рандомизированных исследований (n = 10 933), проведенный с использованием данных об индивидуальных пациентах, показал, что дотации витамина D способствовали снижению риска инфицирования острым респираторным заболеванием в среднем на 12% (ОР 0,88, 95% ДИ 0,81–0,96, p 30 нг/мл) [28]. В среднем риск инфицирования ВПЧ увеличивался на 14% при снижении уровня в сыворотке 25(ОН)D на каждые 10 нг/мл (ОР 1,14, 95% ДИ 1,02–1,27) (рис. 2).
Был опубликован клинический случай, который продемонстрировал эффективность местного применения витамина D у пациентки с папилломой на правом указательном пальце [29]. Так, пациентка А., 41 год, с врожденным заболеванием почек перенесла трансплантацию почки от умершего донора и находилась на терапии иммунодепрессантами (такролимус, микофенолата мофетил). Через 19 месяцев после трансплантации у пациентки образовалась папиллома на правом указательном пальце, которая вырастала вновь и вновь, несмотря на многократную криотерапию и электрокоагуляцию. Местное лечение папилломы с использованием раствора 1,25(OH)2D (0,5 мкг/сут) привело к полному излечению через три месяца.
Витамин D как нутриентная основа профилактики и терапии опухолевых заболеваний шейки матки
1,25(OH)2D ингибирует пролиферацию опухолевых клеток шейки матки путем подавления экспрессии онкогена рака шейки матки (HCCR-1) и увеличения экспрессии проапоптотического белка р21. Опухолевые клетки шейки матки (линия HeLaS3) культивировали в средах с различными концентрациями 1,25(OH)2D, которые индуцировали остановку клеточного цикла на фазе G1. 1,25(OH)2D дозозависимо уменьшал экспрессию белка HCCR-1 посредством транскрипционной регуляции экспрессии гена HCCR-1 и повышенной экспрессии белка p21 и промоторной активности [30].
1,25(OH)2D увеличивает экспрессию онкопротективных микроРНК в клетках рака шейки матки (линия SiHa). МикроРНК влияют на экспрессию многочисленных белков деления клетки, поэтому поддержание функции микроРНК играет важную роль в торможении возникновения и развития опухолей. Показано, что 1,25(OH)2D регулирует экспрессию онкозащитных микроРНК miR-22, miR-296-3p и miR-498 [31].
Иммуногистохимический анализ показал, что уровни экспрессии VDR при цервикальной карциноме повышены по сравнению с нормальной тканью шейки матки. Окрашивание на VDR было однородным, без визуальных различий между отдельными опухолевыми клетками. Умеренно-сильное окрашивание на VDR было обнаружено в 16 из 21 биопсии рака шейки матки независимо от того, экспрессировали эти опухоли цитокератин 10 или трансглутаминазу К. Повышенная экспрессия VDR – один из аспектов иммунного ответа организма на ВПЧ [32].
Делеция рецептора витамина D в эксперименте сенсибилизирует эпителий к химически индуцированному опухолегенезу. Данный эффект вполне понятен, так как 1,25(OH)2D – мощный регулятор клеточной пролиферации, дифференцировки и апоптоза в различных типах клеток, включая кератиноциты. У мышей, гомозиготных по делеции рецептора витамина D (VDR(-/-)), пероральное введение канцерогена 7,12-диметилбензатрацена (ДМБА) вызывало развитие папиллом на всех участках тела со средней опухолевой нагрузкой в 5,3 папиллом/мышь. Никаких папиллом или каких-либо других поражений кожи не наблюдалось у мышей соответствующего возраста и пола без делеции рецептора витамина D (VDR (+/+)) [33].
У мышей линии VDR(-/-) начиная с семинедельного возраста отмечалась гиперпролиферация клеток кожи, которая резко усиливалась после воздействия ДМБА. Без воздействия канцерогена у мышей VDR(-/-) образования опухолей не наблюдалось, но имел место прогрессирующий фенотип кожи, характеризующийся утолщенной морщинистой кожей, дермоидными кистами и длинными вьющимися когтями. Усиленная чувствительность мышей VDR(-/-) к химически индуцированному канцерогенезу кожи убедительно доказывает, что нарушение сигнализации VDR предрасполагает к неоплазиям, вызываемым ВПЧ [33].
Согласно гистопатологическому анализу поражений кожи, у мышей VDR(-/-) обнаружены 94 опухоли на коже, которые были классифицированы по гистологическим подтипам (рис. 3). Большинство всех опухолей (40%) были сальными папилломами (рис. 3А) – доброкачественными поражениями, которые связаны с волосяными фолликулами, сальными железами и межфолликулярной дермой. Кроме того, встречались плоскоклеточные папилломы (25% поражений, рис. 3Б) и фолликулярные папилломы (15% поражений, рис. 3В). Такие виды поражений, как базально-клеточная карцинома (рис. 3Г) и гемангиома (рис. 3Д), выявлялись гораздо реже. Пигментированные поражения, классифицированные как меланотические очаги, которые обычно отсутствуют в мышиной коже, наблюдались у мышей с делецией VDR(-/-) (11% поражений). Меланотические очаги (рис. 3Е) состояли из агрегатов сильно пигментированных клеток с плохо выраженными цитоплазматическими признаками [33].
Витамин D оказывает антипролиферативное и продифференцирующее действие на кератиноциты, поэтому были исследованы биопсии кожи мышей VDR(-/-) посредством количественного определения пролиферативного маркера BrdU. Во всех опухолях мышей VDR(-/-) уровни BrdU были выше, чем рядом в здоровой коже (рис. 4 и 5). В большинстве опухолей пролиферация клеток ограничивалась одним слоем. В других случаях (особенно при плоских папилломах) BrdU-положительные клетки были сгруппированы в несколько слоев. Данные показывают, что расширение опухоли связано с дальнейшим усилением пролиферации эпидермальных клеток у мышей с делецией гена рецептора витамина D [33].
В клинико-эпидемиологическом исследовании более высокое потребление кальция и витамина D ассоциировалось с уменьшением риска развития неоплазии шейки матки (n = 2430, в том числе 405 случаев цервикальной неоплазии). По сравнению с самым низким квартилем потребления кальция риск заболевания дозозависимо понижался в двух верхних квартилях на 14% (ОШ 0,86, 95% ДИ 0,63–1,17) и 50% (ОШ 0,50, 95% ДИ 0,34–0,73) соответственно (p = 0,004). Более высокое потребление витамина D независимо снижало риск заболевания на 20% в третьем (ОР 0,80, 95% ДИ 0,56–1,15) и 36% в четвертом квартиле (ОР 0,64, 95% ДИ 0,43–0,94, p = 0,013) [34].
Таким образом, противовирусное и противоопухолевое действие витамина D позволяет предположить, что повышение обеспеченности этим витамином улучшит результаты терапии опухолевых заболеваний шейки матки. Действительно, в рандомизированном плацебоконтролируемом исследовании долгосрочное применение витамина D индуцировало регрессию цервикальной интраэпителиальной неоплазии [35].
При папилломавирусной инфекции, как и при других хронических заболеваниях с длительной персистенцией вируса, развиваются иммунодефицитные состояния (ИДС), обусловленные недостаточностью различных звеньев иммунной системы, поэтому для повышения эффективности лечения в схемы терапии необходимо включать кроме противовирусных (системно и местно) и иммунокорригирующие препараты, а также патогенетические средства (системная энзимотерапия, антиоксиданты, про- и пребиотики), которые облегчают состояние пациента и способствуют более действенному применению используемых лекарств. При сочетании ПВИ с другими возбудителями проводится комплексное лечение с использованием этиотропных препаратов в отношении конкретных возбудителей в стандартных дозировках. Показано, что современное лечение не позволяет избежать рецидивирования ПВИ в 20-30% случаев (Беляковский В. Н., 2003; Ван Крог Д. и др., 2002).
В последнее время стали известны особенности иммунного ответа организма человека в случае инфицирования вирусами папилломы. Известно, что вирусами папилломы не инфицируются антиген-презентирующие клетки (АПК), избегая тем самым прямого пути активации иммунитета. Ранние вирусные белки ВПЧ локализуются в основном в ядре инфицированных клеток, и у больных с ВПЧ-индуцированной дисплазией регистрируется очень слабый иммунный ответ на эти белки. В то же время ранние белки ВПЧ синтезируются активно и индуцируют процессы малигнизации инфицированных клеток. Поздние гены ВПЧ содержат кодоны, которые очень редко используются млекопитающими. За счет этого синтез капсидных белков ВПЧ протекает медленно и в малых количествах, тормозя развитие противовирусного иммунитета. Таким образом, в процессе эволюции сложился механизм, при котором вирусная инфекция на молекулярном уровне защищается от системного воздействия иммунитета хозяина (Schwarts S., 2000). У больных ПВИ отмечается снижение показателей Т-клеточного звена иммунитета, иммунорегуляторного индекса (CD4/CD8), количества клеток Лангерганса и иммунного ответа цервикальных лимфоцитов. Снижена функциональная активность натуральных киллеров (NK), уровень основных сывороточных иммуноглобулинов. Содержание ЦИК в периферической крови увеличено, что коррелировало с распространенностью и тяжестью процесса. Дисбаланс иммунной системы обосновывает использование в комплексной терапии ПВИ иммунокорригирующих препаратов. Предполагается, что чувствительность ВПЧ к отдельным химиопрепаратам обусловлена прежде всего генетически запрограммированными особенностями иммунного ответа при этой патологии. Длительное использование для лечения ВПЧ-ассоциированных заболеваний препаратов ИФН-а2 более чем у 50% пролеченных пациентов не приводит к клиническому улучшению в связи с резистентностью инфицированных клеток к ИФН. Оказалось, что это явление напрямую связано с уровнем синтеза онкобелка Е7, который нейтрализует противовирусную и противоопухолевую активность ИФН-а2 за счет избирательного блокирования большинства генов, индуцируемых интерфероном, существенно снижая эффективность интерферонотерапии (Nees M. и соавт., 2001). Установлена также способность белка Е7 внутриклеточно инактивировать фактор регуляции активности интерферона (IRF), являющегося фактором транскрипции и активирующегося в клетках под воздействием на них ИФН-а и ИФН-b, и, в свою очередь, включает транскрипцию генов, кодирующих синтез противовирусных белков. Онкобелок Е7 является мощным иммуносупрессором, значительно снижающим эффективность иммунокорригирующей терапии. Иными словами, причиной неудач терапии ВПЧ-инфекции препаратами интерферона является определяемая онкобелком Е7 устойчивость зараженных клеток в процессе лечения, из чего следуют важные выводы для клинической практики (Киселев В. И., 2004):
- местная интерферонотерапия остается важным методом лечения ВПЧ-ассоциированных заболеваний;
- измерение содержания белка Е7 ВПЧ является необходимым условием для назначения терапии и прогнозирования ее эффективности;
- в случае высокого содержания Е7 необходимы мероприятия по его снижению, что сделает опухолевые клетки более воспримчи-выми к интерферону.
Таким образом, лечение ПВИ остается довольно трудной задачей, несмотря на значительный арсенал средств и методов терапии. Поскольку полного излечения к настоящему времени достичь невозможно, считают, что целью проводимых лечебных манипуляций должна быть не элиминация возбудителя, а перевод инфекции в стадию устойчивой ремиссии (клинического выздоровления). В связи с этим предлагается следующая тактика ведения пациентов с ВПЧ-инфекцией (Беляковский В. Н., 2003):
1) разрушение папилломатозных очагов; 2) стимуляция противовирусного иммунитета, т. е. коррекция общего и местного иммунитета; 3) сочетание этих подходов, устранение факторов, способствующих рецидивам болезни. Важно помнить, что методы лечения, направленные на удаление поверхностного слоя эпидермиса без санации клеток базального слоя, неэффективны и сопровождаются рецидивом заболевания. Возможность реактивации инфекции диктует необходимость применения комбинированных методов лечения: деструкции видимых проявлений и использование (системно и местно) препаратов с противовирусной и иммуномодулирующей активностью (табл. 7, 8).
Таблица 7. Местные методы терапии остроконечных кандилом
| Деструктивные методы | Цитотоксические препараты | |
| Физические | Хирургическое иссечение | Подофиллин |
| Электрохирургические методы | Подофиллотоксин | |
| Криотерапия | 5-фторурацил | |
| Лазеротерапия | ||
| Химические | Азотная кислота | |
| Трихлоруксусная кислота | ||
| Солкодерм (уксусная + щавелевая + молочная + азотная кислоты + ионы металлов) | ||
| Ферезол | ||
Таблица 8. Принципы терапии кондилом
| Методы терапии | Средства для лечения |
| Противовирусные препараты | Мазь бонафтона 0,5-1-2% и риодоксола — 0,25 и 0,5%. Наносить 5-6 раз в день, 2-3 нед. Мазь 2% бонафтона + 0,5% риодоксола Бонафтон внутрь по 0,2 г 3 р. в день, 10 дней. 3% мазь оксолиновая, 2-3 нед. Индинол, по 2 капсулы 2 раза в день натощак, за 10 минут до еды в течение 3 месяцев |
| Цитотоксические препараты, местно | Подофиллин в виде 10-25% раствора, 1-2 р.в нед., 5 недель. Подофиллотоксин (кондилин) 2 раза в сутки в течение 3 дней с 4-дневным перерывом, повторять до 4 раз. 20% мазь подофиллотоксина. 5-фторурацил в виде 5% крема 1 раз на ночь 7 дней, или 1 раз в неделю в течение 10 недель |
| Деструктивные методы | Физические (криодеструкция, лазеротерапия, диатермокоагуляция). |
| Хирургические методы | Химические (80-90% трихлоруксусная кислота, ферезол — 1 раз в нед., солкодерм — излечение 80-90%) В т. ч. и электрохирургическое иссечение |
| Иммунологические методы | а-, b-, y-интерфероны, индукторы ИНФ, рекомбинантные ин-терлейкины (ИЛ-2, ронколейкин). Изопринозин (табл. 0,5) по 1,0 г 3 р./день, 2-4 нед. как основное лечение. Либо лазеротерапия+изопринозин по 2 табл. 5 дней, 3 курса с интервалом 1 мес. Ликопид табл. по 10 мг/день, 6 дней. 3 курса с интервалом в 2 нед. Галавит в/м., 1-й д. — 200 мг, 2-й день — 100 мг, с 111 дня — по 100 мг через день, № 10-15. 12,5% циклоферон в/м по 2 мл (250 мг) по схеме 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23-й дни лечения. Местно аппликации 5% линимента циклоферона, либо гидрогель алломедина 3-4 раза в день. Изопринозином по 2 таблетки (1000 мг) 3 р/д в течение 14-28 дней в сочетании с в/м введением циклоферона по 4 мл (500 мг) № 10 по основной схеме |
| Комбинированные методы | Сочетание различных методов лечения |
При остроконечных кондиломах проводится лечение обоих половых партнеров. Рекомендуется воздерживаться от половых контактов в период приема лекарств и барьерная контрацепция в течение 6 месяцев после завершения терапии. В целом тактику лечения определяет (Баткаев Э. А. и др., 2001):
- исходное состояние иммунитета,
- наличие сопутствующей соматической патологии,
- характер урогенитальной инфекции,
- локализация патологического процесса,
- характер патологического процесса шейки матки (наличие и степень тяжести дисплазии или ее отсутствие),
- предшествующая противовирусная терапия.
Как уже отмечалось выше, в основе местного лечения лежит удаление кондилом и измененных участков эпителия. Для решения указанной задачи разработано несколько подходов (табл. 7).
Из физических методов лечения аногенитальных бородавок наиболее часто применяется лазеротерапия, особенно в детской гинекологии и у беременных женщин. Используются углекислотные и неодимовые лазеры. Следует отметить, что углекислый лазер меньше повреждает окружающие ткани, а неодимовый обладает более выраженным гомеостатическим эффектом. При необходимости можно провести обезболивание нанесением крема EMLA (ASTRA) за 10-15 минут (слизистые оболочки) или 30-40 минут (кожа) до процедуры. Если после первого сеанса лазерной терапии отмечаются остаточные явления, то рекомендуется через три недели повторить курс, после которого наблюдается полная деструкция остроконечных кондилом. Лазеротерапию у беременных женщин следует проводить не позже 35 недель беременности, тогда роды у них проходят без осложнений, связанных с ВПЧ-инфекцией. Многие авторы считают, что лазерная терапия является основным методом лечения остроконечных кондилом у беременных женщин (Козлова В. И., Пухнер А. Ф., 2000).
Криотерапия с применением жидкого азота, оксида азота и диоксида углерода в большинстве случаев является безопасным и эффективным методом лечения бородавок. Криотерапия может применяться в виде одной процедуры длительностью от 10 до 120 секунд или двух отдельных циклов (от 10 до 90 секунд). Через 3 дня на участках, подвергающихся обработке могут наблюдаться пузырьки, покраснения и изъязвления, заживающие через 1-2 недели.
Хирургический метод наиболее приемлем при лечении больных с большой площадью и большим количеством папилломатозных элементов. Отрицательным моментом является необходимость обезболивания и возможность возникновения послеоперационного рубца, поэтому бородавки, располагающиеся вокруг ануса и уретры, необходимо удалять постепенно.
Из препаратов, которые можно отнести к группе химических средств, обладающих местным прижигающим действием, следует выделить солкодерм. По своей сути это кератолитическое средство, применяемое в виде раствора, активной составляющей которого являются продукты взаимодействия органических кислот и ионов металлов с азотной кислотой. Раствор содержит нитраты в количестве 0,02 мг/мл. Солкодерм оказывает ограниченное местное действие на патологически измененные ткани, на которые он наносится. Препарат проникает в обработанную ткань и вызывает изменение ее окраски, отражающее прижизненную фиксацию обработанной области. В последующем происходит мумификация патологической ткани, по мере усиления которой струп темнеет и через несколько дней самостоятельно отпадает. Заживление происходит быстро. В терапии используют также трихлоруксусную кислоту в концентрации 80-90%, которая является слабым деструктивным химическим препаратом, вызывающим локальный коагуляционный некроз. Препарат наиболее эффективен при небольших остроконечных или вульгарных папилломах, эффективность снижается при больших или ороговевших поражениях. Спустя 1-2 недели можно проводить повторные обработки. Трихлоруксусная кислота обладает сильным разъедающим действием, и избыточное ее нанесение может вызвать сильные болевые ощущения и образование изъязвлений, а впоследствии и рубцов, поэтому для нейтрализации избытка препарата или при случайном его попадании на здоровую кожу необходимо использование раствора бикарбоната натрия. При правильном применении трихлоруксусной кислоты образуются неглубокие эрозии, не оставляющие рубцов.
Из препаратов цитостатического действия для местного воздействия на папилломатозные элементы до настоящего времени широко используется подофиллин. Впервые для лечения бородавок аногенитальной области его применил Kaplan J. W. (1942). Лекарство ингибирует митозы, а в высоких концентрациях подавляет транспорт нуклеозидов, в результате чего происходит ингибирование синтеза ДНК и размножения клеток. Препарат применяется при лечении некератизированных бородавок препуциальной области головки полового члена, венечной борозды, вульвы. Используется в виде 10-25% раствора в сочетании с настойкой бензоина. Максимальная продолжительность лечения 5 недель. Возможно развитие побочных реакций, в частности контактного дерматита, отмечающегося в 10-15% случаев. Однако далеко не все авторы приветствуют использование подофиллина, особенно его самостоятельное применение. Так, Peterson С. и соавт. (1995) отмечают, что примерно 10% сухого вещества 20%-го раствора препарата составляют 2 мутагенных флавоноида: квартцетин и комферол, поэтому авторы рекомендуют использовать лишь высокоочищенный подофиллотоксин, причем самостоятельное его применение больными возможно лишь после тщательного инструктажа.
Подофиллотоксин (кондилин) — наиболее активная в клиническом аспекте фракция в составе подофиллина. Его несомненное достоинство — возможность самостоятельного применения больными. Препарат используется только для лечения остроконечных кондилом. Обычно его наносят хлопковым или пластиковым тампоном на папилломатозные элементы 2 раза в сутки в течение 3 дней с 4-дневным перерывом. Этот цикл терапии при необходимости можно повторять до 4 раз. Общая зона обработки не должна превышать 10 см2, а общий объем использованного лекарственного средства не должен превышать 0,5 мл в день. Однако, несмотря на более высокую очистку подофиллотоксина по сравнению с его предшественником подофиллином, как подчеркивает Bonner W. с соавт. (1994), у 57% пациентов возможно развитие местных воспалительных реакций, у 48% — эритема и чувство жжения, у 47% — болезненность, у 39% — мокнутия и эрозии. К недостаткам подофиллотоксина можно также отнести его высокую стоимость и умеренную эффективность.
В последние годы для лечения ВПЧ-инфекции предпринимались попытки использования различных лекарственных средств из онкологической практики. К этой группе препаратов относится 5-фтпорурацил, который является антагонистом пиримидина и обладает способностью нарушать синтез вирусной ДНК. В виде 5% крема препарат наиболее эффективен при лечении папилломатозных элементов на сводах влагалища и дистальной части уретры. При лечении интравагинальных бородавок лекарство назначается 1 раз на ночь в течение недели или 1 раз в неделю в течение 10 недель. Подобная схема терапии позволяет добиться регресса папилломатозных элементов в 85-90% случаев. Однако при этом могут возникать мокнущие эрозии на слизистой влагалища вплоть до развития контактного дерматита.
При лечении бородавок дистальной части уретры препарат используется сразу же после мочеиспускания, на ночь в течение 3-8 дней. Однако, несмотря на довольно высокую клиническую эффективность, в этом случае у мужчин отмечается множество побочных эффектов вплоть до развития стеноза и стриктуры уретры. Эффективность лечения кондилом составляет 50-94%, уровень рецидивирования в течение 3 месяцев после лечения не менее 25%.
Индинол (индол-3-карбинол) — противоопухолевое и противовирусное природное средство, эффективное в отношении гормонозависимых заболеваний и эпителиальных опухолей органов женской половой системы, а также ВПЧ-инфекции. Препарат препятствует образованию 16-а-гидроксистерона, блокирует синтез онкобелка Е7, подавляет рост эстрогензависимых опухолей. Выпускается в капсулах по 100 мг вещества. Назначается по 2 капсулы 2 раза в день натощак, за 10 минут до еды в течение 3 месяцев. Возможен сочетанный прием индинола с другими препаратами (Димтриев Г. А., Биткина О. А., 2006; Киселев В. И., 2004).

Едва ли можно найти человека без папиллом. Эти образования на коже могут доставлять серьезный дискомфорт и быть косметическим дефектом.
В этой статье мы подробно разберем что такое папилломы, и как дерматологи советуют с ними бороться. При этом важно помнить, что каждый случай уникален и требует предварительной консультации с врачом. Лечить или удалять папилломы самостоятельно мы категорически не рекомендуем.
Что такое папилломы?
Папилломы — вирусное заболевание, вызванное вирусом папилломы человека (ВПЧ). Заразиться им можно при простом бытовом контакте, использовании общих полотенец, мочалок.
Обязательным условием заражения является снижение иммунитета или наличие ран и язв на теле. И одно маленькое новообразование со временем распространяются по всему телу множеством кондилом — остроконечных бородавок. Они, в свою очередь, не только создают косметический дефект, но и еще сильнее снижают иммунитет.
Нужно ли лечить папилломы?
Если у вас есть папилломы (бородавки), то они требуют комбинированной, порой длительной и трудной терапии.
Обязательно перед началом терапии проконсультируйтесь с врачом,чтобы определить вид и подтвердить доброкачественный характер образования, провести ряд исследований, ведь для максимально быстрого и эффективного лечения необходимо установить тип возбудителя.
Также необходимо подобрать наиболее щадящий и эффективный способ удаления образований, предотвращающий рубцы, шрамы и дефекты кожи.
Где чаще всего бывают папилломы?
Вирус папилломы человека насчитывает более 170 штаммов. Некоторые из них вызывают вполне безобидные бородавки и кондиломы. А некоторые могут стать причиной рака. Так, в настоящий момент доказана инфекционная причина дисплазии и рака шейки матки, рассматривается вирусная природа рака прямой кишки и перианальный области.
Наиболее распространены бородавки на кистях и стопах, кондиломы — на половых органах, голове. Для мужчин самая частая локализация — подмышечные впадины, у женщин — шея, грудь, коже под молочными железами.
Как избавиться от папиллом?
Лечение любых форм новообразований, вызванных ВПЧ, предусматривает прямое воздействие на папилломы местными препаратами и прием противовирусных/иммуномодулирующих средств. Если же медикаментозная терапия не привела к выздоровлению, используют методы хирургического воздействия на образования. Возможно простое механическое удаление скальпелем, а также электроножом, лазером, жидким азотом.
- Местные средства: кремы, растворы, гели, мази для местного нанесения (кератолитики и некротизирующие);
- Иммуномодуляторы;
- Противовирусные местные и общие препараты.
Как убрать папилломы?
Гель и мазь от папиллом
Кератолитики — препараты, которые наносятся непосредственно на бородавку, размягчают ее и отшелушивают. В аптеках представлены салициловая кислота, Суперчистотело, Вартокс, Колломак, Антипапиллом, различные кислоты и ферменты, размягчающие кожу в области образования. Активные компоненты эффективно справляются с вирусными штаммами, однако чаще всего требуется несколько курсов лечения.
Некротизирующие препараты — средства, вызывающие гибель клеток, пораженных вирусом. Например, Солкодерм, Кондилин, Ляписный карандаш. Также наносятся на саму папиллому, но особенность этих средств в том, что они могу оставлять достаточно большие дефекты, рубцы и шрамы на теле после удаления бородавки.
Лучшее средство от папиллом - противовирусные препараты
Еще одна группа препаратов для лечения папиллом — противовирусные препараты. Их две разновидности: местные и общие. Местные препараты наносятся непосредственно на пораженное место и вокруг бородавок. Самый известный — оксолиновая мазь. Также Виферон и Ацикловир обладают местным противовирусным свойством. Все лекарства из этой группы наносятся на бородавку и убивают сам вирус внутри пораженных клеток.
Перед применением местных препаратов необходимо кожу обработать антисептическим раствором. Из антисептиков с противовирусной активностью в аптеках чаще всего встречаются Мирамистин и Хлоргексидин. Также на кожу вокруг папилломы нужно нанести жирный питательный крем или вазелиновую мазь, чтобы предотвратить ожог активными компонентами здоровых тканей.
Как вылечить папилломы - иммуномодуляторы
Для комбинированного лечения используется противовирусные таблетки и иммуномодуляторы (средства, повышающие иммунитет).
Гроприносин, Имунобекс, Генферон, Полиоксидоний — это препараты, которые стимулируют иммунную систему и повышают защитные силы организма, «заставляя» иммунные клетки вырабатывать иммуноглобулины, либо сами являются иммуноглобулина, идентичными человеческим. Все таблетки от папиллом проходят через печень и почки, людям с заболеваниями этих органов стоит быть максимально осторожными с приемом веществ данных групп.
ВПЧ требует обязательного квалифицированного лечения, ведь до конца его влияние на организм человека не установлено. Неправильное использование препаратов для домашнего применения может привести к образования глубоких язв, шрамов и риску заражения вирусом окружающих здоровых тканей. Чтобы минимизировать риски развития заболеваний, вызванных ВПЧ, обратитесь к врачу и следуйте назначенному плану лечения.

Данные ВОЗ свидетельствуют, что аллергией на нашей планете страдает более 40% людей. И каждый год это число увеличивается. Почему возникает патология, врачам и ученым выяснить точно пока не удалось. Отсутствие знаний в полном объеме, в свою очередь, не позволяет разработать средства, которые бы помогли избавиться от аллергии навсегда.
Но все же, благодаря развитию науки, сегодня создано немало средств, значительно уменьшающих ее проявления. Проверенные таблетки от аллергии помогают устранить большинство аллергических реакций и надолго забыть о неприятных симптомах.
Что это за болезнь
Аллергия – довольно загадочная болезнь. Она не провоцируется микроорганизмами и ею нельзя заразиться. В развитии аллергических реакций «виновата» собственная иммунная система, чересчур агрессивно реагирующая на вполне безвредные вещества. Наиболее распространенные аллергены: домашняя пыль, шерсть животных, растительная пыльца, компоненты продуктов. В результате патологических изменений иммунной системы, организм в ответ на эти вещества начинает образовывать антитела, вызывающие воспалительную реакцию.
- Чиханием
- Кашлем
- Затрудненным дыханием
- Зудом в носу и появлением выделений
- Слезотечением
- Высыпаниями на коже
Легкие формы заболевания имеют не сильно выраженную симптоматику. Но по разным причинам симптомы могут усиливаться.
При появлении аллергических признаков нужно обратиться к аллергологу. Врач назначит тесты, которые дают возможность «опознать» аллерген. Это поможет избегать с ним контактов и предотвращать обострения. Но избежать полного разобщения с аллергеном удается не всегда. В этом случае на помощь придут лекарства для устранения реакций или уменьшения их выраженности.
Нет времени читать длинные статьи? Подписывайтесь на нас в соцсетях: слушайте фоном видео и читайте короткие заметки о красоте и здоровье.
Мегаптека в соцсетях: ВКонтакте, Telegram, OK, Viber
Средство от аллергии
Эти средства относятся к группе антигистаминных препаратов. Они предотвращают выработку гистамина. В норме это вещество участвует во многих физиологических процессах. Но при сбоях в иммунной системе проникновение в организм аллергена начинает сопровождаться активным продуцированием гистамина. Слишком большие его количества вызывают воспалительную реакцию, проявляющуюся симптомами аллергии. Сегодня медицина располагает 3-мя поколениями антигистаминных средств.
Препараты 1-го поколения
Быстро устраняют неприятную симптоматику, но действуют недолго. А их длительный прием вызывает привыкание. Имеют побочные эффекты, которые проявляются:
- Сонливостью
- Слабостью
- Заторможенностью реакций
- Головной болью
Но при наличии недостатков, у препаратов есть и достоинства. Эти дешевые средства выпускаются не только в таблетках, но и в виде растворов, и используются для неотложной помощи.
Самые популярные из них: Диазолин, Супрастин. Не все из них подходят детям, поэтому при их применении нужно обязательно проконсультироваться с педиатром.
Лекарственные средства 2-го поколения
Лекарства 3-го поколения
Официально считается, что препараты еще до конца не разработаны. Но неофициально, к средствам нового поколения относят более усовершенствованные лекарства 2-го поколения. Отличаются высокой эффективностью, быстрым действием и минимальным количеством побочных явлений. Не вызывают привыкания, поэтому могут использоваться длительно.
Одно из самых популярных средств от аллергии на сегодняшний день – это Эриус. Выпускается в форме таблеток и сиропа. Другие современные средства: Цетрин, Ксизал.
Лучшее средство от аллергии на сегодняшний день
Кроме антигистаминных препаратов, при тяжелых аллергических проявлениях используются кортикостероиды и стабилизаторы мембраны тучных клеток. Также для борьбы с аллергией иногда используются БАДы. Но их применение нужно обязательно согласовать с врачом.
Как избавиться от аллергии навсегда
Антигистаминные препараты, даже самые современные, лишь купируют симптомы, но вылечить болезнь они не могут. Самым надежным способом избавления от аллергии сегодня считается иммунотерапия (АСИТ). Она заключается в введении веществ, вызывающих аллергические реакции. Постепенное увеличение дозы препарата приводит к формированию привыкания организма к аллергену.
АСИТ помогает значительно уменьшить проявления аллергии, сократить периоды обострения, а нередко излечить болезнь полностью. Недостаток иммунотерапии – ее длительность (занимает 3-5 лет).
- Мыть голову и принимать душ перед сном каждый день – так вы смоете пыльцу растений, которая осела на коже и в волосах.
- Ежедневно промывать нос – промывание даже простой водой избавит от вредных микрочастиц, оседающих на слизистых дыхательных путей.
- Стирать постельное белье в горячей воде – стирка при 30-40˚C не уничтожает постельных клещей-сапрофитов, которые относятся к самым распространенным аллергенам.
- Убирать в доме правильно – важна не только влажная уборка, для очистки ковров и мягкой мебели от пыли нужно обязательно использовать пылесос.

К сожалению, универсальных методов борьбы с аллергией не существует. И нередко поиск подходящих средств занимает немало времени. При появлении аллергических признаков нужно обратиться к врачу, который даст рекомендации и подберет препарат, исходя из особенностей вашего организма.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же Вы можете поделиться своим опытом с другими читателями Мегасоветов.
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисовой Элины Вячеславовны, гинеколога со стажем в 35 лет.
Над статьей доктора Борисовой Элины Вячеславовны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
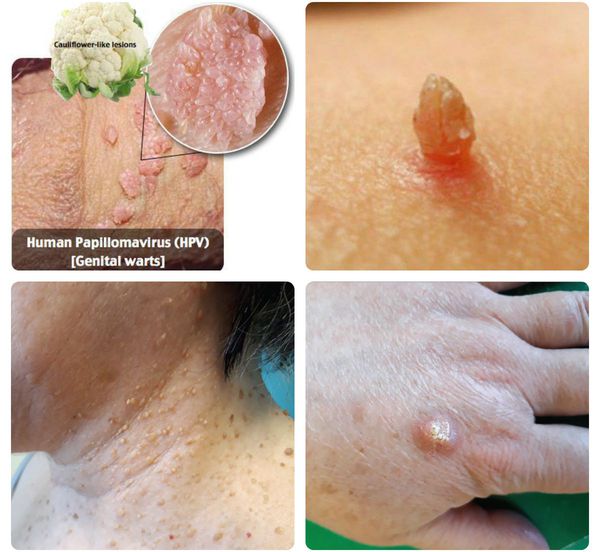
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
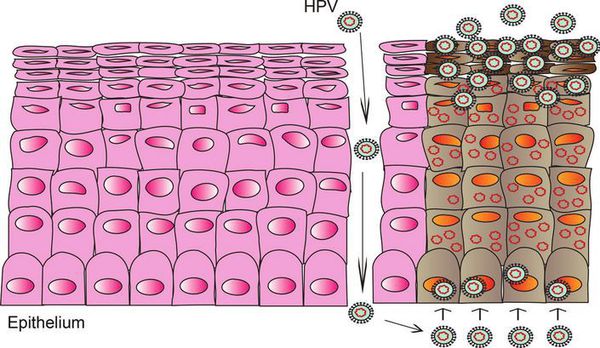
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
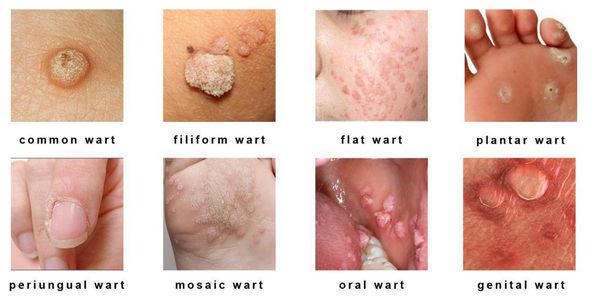
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
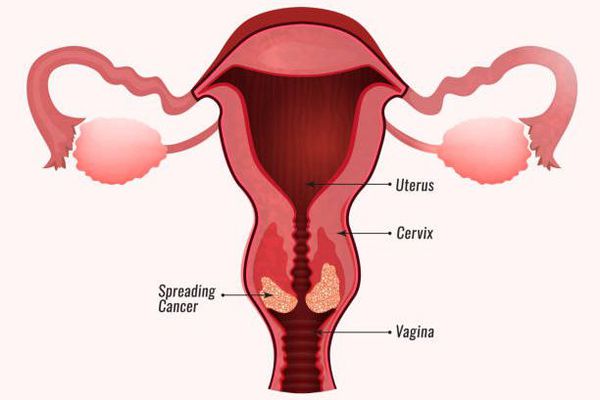
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
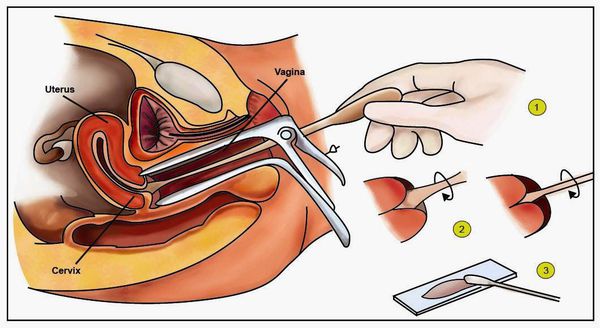
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
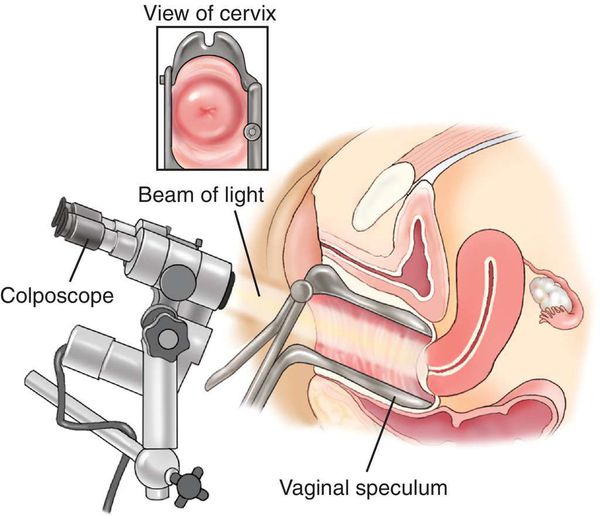
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
Читайте также:

