Последствия опоясывающего герпеса при вич
Обновлено: 25.04.2024
22264 04 Сентября
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
ВИЧ: причины появления, симптомы, диагностика и способы лечения.
Определение
ВИЧ (вирус иммунодефицита человека) – инфекционное хроническое заболевание, передающееся контактным путем, медленно прогрессирующее и характеризующееся поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИДа). СПИД – это финальная стадия ВИЧ-инфекции, когда из-за ослабленной иммунной системы человек становится беззащитным перед любыми инфекциями и некоторыми видами рака. Опасность представляют так называемые оппортунистические инфекции – заболевания, вызываемые условно-патогенной или непатогенной флорой: вирусами, бактериями, грибами, которые у здоровых людей не приводят к серьезным последствиям или протекают легко и излечиваются самостоятельно. При СПИДе они наслаиваются друг на друга, имеют затяжное течение, плохо поддаются терапии и могут стать причиной летального исхода.
Причины появления ВИЧ
Источником инфекции является человек, инфицированный ВИЧ, на любых стадиях заболевания. Вирус передается через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь (незащищенный секс с инфицированным партнером) – доминирующий фактор распространения ВИЧ-инфекции.
Передача ВИЧ от матери ребенку может произойти на любом сроке беременности (через плаценту), во время родов (при прохождении через родовые пути) и грудного вскармливания (при наличии язвочек, трещин на сосках матери и во рту ребенка).
Высокий риск инфицирования существует при внутривенном введении наркотических веществ нестерильными шприцами, при переливании ВИЧ-инфицированной крови и ее препаратов, использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, опасность могут представлять органы и ткани доноров, используемые для трансплантации.

Попадая в кровоток, вирус проникает в Т-лимфоциты хелперы, или CD-4 клетки (рановидность лейкоцитов), которые помогают организму бороться с инфекциями. Т-хелперы имеют на поверхности так называемые CD4-рецепторы. ВИЧ связывается с этими рецепторами, проникает в клетку, размножается в ней и в конечном счете уничтожает ее. Со временем вирусная нагрузка увеличивается, а количество Т-хелперов снижается.
При отсутствии лечения через несколько лет из-за значительного снижения числа Т-хелперов появляются связанные со СПИДом состояния и симптомы.
Классификация заболевания
- Стадия инкубации - от момента заражения до появления реакции организма в виде клинических проявлений острой инфекции и/или выработки антител (специфических белков, продуцируемых в ответ на проникновение антигена, в данном случае – вируса).
- Стадия первичных проявлений клинических симптомов:
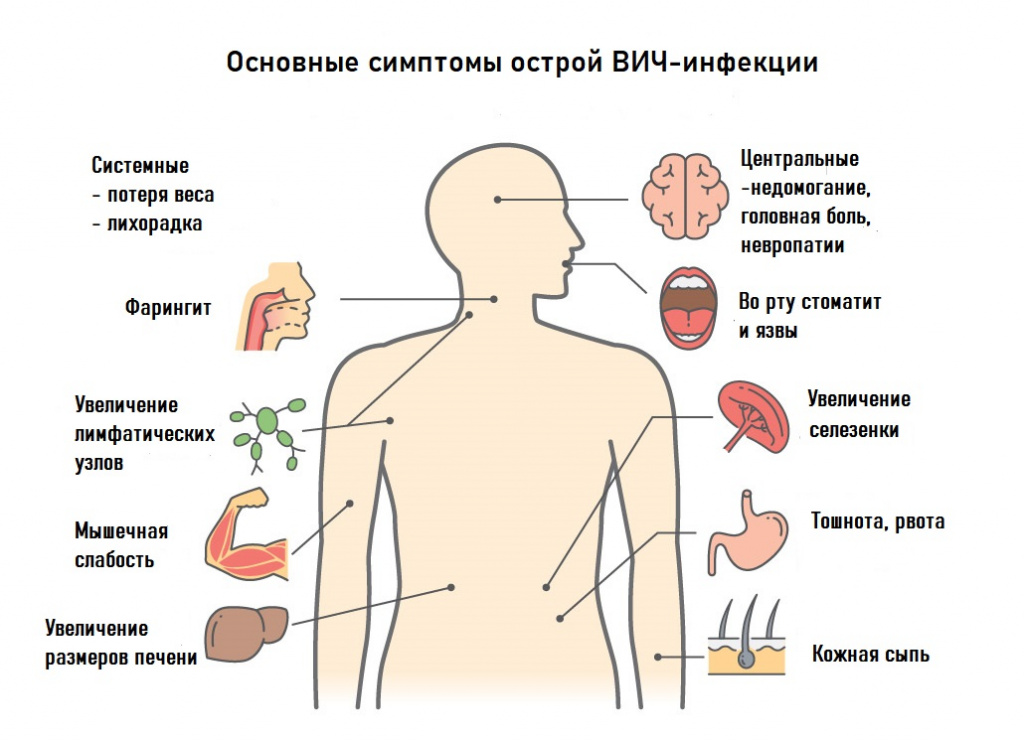
После инкубационного периода продолжительностью от нескольких дней до нескольких недель у большинства зараженных возникает острое заболевание с гриппоподобными симптомами (повышение температуры тела, ломота, общая слабость, отсутствие аппетита, головная боль, боль в горле, увеличение лимфатических узлов, кожные высыпания). Возможны похудание, образование язвочек на слизистой полости рта. Эта фаза продолжается, как правило, 7-10 дней. Из-за неспецифичности проявлений диагноз «ВИЧ» устанавливается редко. Редко на этой стадии заболевания фиксируются оппортунистические инфекции,. отмечается кашель с мокротой, боль в грудной клетке (при развитии пневмонии), болезненные пузырьковые высыпания на коже (при опоясывающем герпесе). Как правило, самочувствие быстро нормализуется без специфического лечения ВИЧ.
После этой стадии устанавливается временное равновесие между инфекционным процессом и сдерживающим его развитие противовирусным иммунитетом.
В дальнейшем продолжается активное размножение вируса и разрушение Т-лимфоцитов, развивается стадия вторичных изменений, для которой характерно прогрессирующее снижение веса, общая слабость, стойкое повышение температуры, озноб, выраженная потливость. Клинические проявления оппортунистических заболеваний обусловливают клиническую картину этой стадии: пациентов беспокоят кашель и одышка, тошнота, рвота, боли в животе, тяжелая диарея, кожные высыпания, сильные головные боли, снижение памяти и внимания и др.
Диагностика ВИЧ
Лабораторные методы исследования:
- Скрининг на ВИЧ.
- Обследование, подтверждающее факт инфицирования ВИЧ (при положительных или сомнительных результатах скрининга).
- Измерение и контроль количества вируса в крови человека - определение вирусной нагрузки у лиц с установленным диагнозом «ВИЧ».
- Определение иммунного статуса у пациентов с ВИЧ-инфекцией.
Скрининг (обследование здоровых людей) на ВИЧ должен быть проведен любому человеку, который считает, что может быть заражен, а также перед любой госпитализацией и операцией, всем беременным женщинам и их половым партнерам.
Обследование целесообразно проходить людям с высоким риском заражения ВИЧ, например, при наличии заболеваний, имеющих одинаковый с ВИЧ-инфекцией механизм передачи (вирусные гепатиты В и С, заболевания, передающиеся половым путем), лицам, имеющим регулярные незащищенные половые контакты, инъекционным наркоманам, детям, рожденным от матерей с ВИЧ-инфекцией, медицинским работникам, напрямую контактирующим с кровью на работе и др.
Существуют экспресс-тесты для скрининга ВИЧ, которые можно делать в домашних условиях. Для определения специфических антител/антигенов к ВИЧ (ВИЧ-1, 2, антиген p24) используют кровь, слюну или мочу. Точность любого экспресс-теста ниже, чем теста, проводимого в лаборатории.
Для стандартного скринингового обследования определяют антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) в крови с помощью иммуноферментного анализа (ИФА).
Внимание! При положительных и сомнительных реакциях срок выдачи результата может быть увеличен до 10 рабочих дней. Синонимы: Анализ крови на антитела к ВИЧ1 и 2 и антиген ВИЧ1 и 2; ВИЧ-1 p24; ВИЧ-1-антиген, p24-антиген; ВИЧ 1 и 2 антитела и антиген p24/25, ВИЧ тест-системы 4-го .
Впервые в России изучены и обобщены особенности клинического течения простого и опоясывающего герпеса у ВИЧ инфицированных больных.
Впервые проведен анализ комплексного обследования больных простым и опоясывающим герпесом на фоне на основании данных анамнеза, результатов объективных и дополнительных исследований, подтверждающих этиологическую роль ВПГ и ВЗВ.
Впервые в России выявлена ДНК ВИЧ в материале соскобов из очагов герпетических высыпаний методом ПЦР.
Впервые проведено комплексное изучение клинических проявлений и показателей иммунитета, а также их динамики до и после лечения Валацикловиром у больных простым и опоясывающим герпесом на фоне
Практическая значимость
Изученные особенности клинического течения простого и опоясывающего герпеса на фоне позволяют облегчить диагностику атипичных форм болезни.
Обнаруженная ДНК ВИЧ в материале из герпетических поражений кожи и слизистых оболочек методом ПЦР имеет важное эпидемическое значение, так как может служить дополнительным фактором распространения
Лечение Валацикловиром простого и опоясывающего герпеса у ВИЧ инфицированных лиц показывает клиническую эффективность препарата у данной группы пациентов.
Положения, выносимые на защиту
1. Изучены особенности проявлений и характер течения простого и опоясывающего герпеса на фоне и их связь с выраженностью изменений в системе иммунитета.
2. У значительного числа больных простым и опоясывающим герпесом (64,1%) выявлено пониженное количество (менее 0,500х109/л), а у 10,9% имеет место выраженное (менее 0,200х109/л) снижение
3. Показана значимость обнаружения ДНК ВПГ и ДНК ВЗВ в крови и в материале из очагов герпетических поражений кожи и слизистых оболочек методом ПЦР.
4. Впервые получены данные по обнаружению ДНК ВИЧ в материале соскобов из герпетических высыпаний, что может иметь эпидемиологическое значение.
Клинические проявления простого и опоясывающего герпеса у ВИЧ инфицированных лиц
Из числа обследованных больных простым герпесом наибольшее количество пациентов (35,6%) было с давностью заболевания от 6 мес. до 1 года. С давностью заболевания от 2 до 4 лет было 34,1% больных. Количество больных, страдающих простым гепатитом от 5 до 10 лет, составило 21,2%, а более 10 лет — 8,2% от общего числа обследованных. При этом 33 (38,8%) пациента из 85 больных простым герпесом в анамнезе уже имели рецидивирующий герпес, то есть они изначально были инфицированными вирусом простого герпеса, а затем ВИЧ.
Как известно, у "иммунокомпетентных лиц, страдающих простым герпесом, высыпания преимущественно локализируются на лице или половых органах. При этом, манифестации вирусного процесса возникают, как правило, на одних и тех же местах кожи и слизистой оболочки и крайне редко на различных участках кожи или на новом месте при каждом рецидиве.
Нами же выявлено, что герпетическая инфекция у больных имеет ряд особенностей, которые заключаются в следующем: в различной локализации патологических очагов, их распространенности, в частоте рецидивов, в клинических проявлениях заболевания. Так, помимо традиционных мест расположения простого герпеса — лабильного у 38 (44,7%) больных и генитального — у 35 (41,2%), герпетические высыпания имели иную локализацию. Из 12 (14,1%) пациентов с данной локализацией высыпания в области ягодиц наблюдались у 4 (4,7%) больных, в перианальной зоне у 3 (3,5%), в области бедра у 3 (3,5%), на пальце у 2 (2,4%) больных. Обращал на себя внимание тот факт, что у 17 (20%) больных имело место поражение сразу нескольких анатомических зон или высыпания локализовались в иных зонах при последующих рецидивах. Преимущественно наблюдалось сочетание генитального и лабиального герпеса, а также генитального и в области пальца, лабиального и в перианальной области, генитального и в области пальца, лабиального и в области крыльев носа, одновременное расположение высыпаний в периоральной области и тыльной поверхности кисти.
У "иммунокомпетентных« больных высыпания опоясывающего герпеса наиболее часто локализуются в области туловища, несколько реже в области головы и значительно реже — в области конечностей. В нашем исследовании у ВИЧ инфицированных больных высыпания в области туловища также встречались чаще (67,1%), чем в области конечностей (23,2%) и головы (9,7%). В то же время смежные локализации были у 29,3% больных.
Из черепно-мозговых нервов поражение 1 ветви тройничного нерва отмечалось у 2 больных. Поражение 3 ветви тройничного нерва выявлено у 3 больных в сочетании с поражениями шейных сегментов и у 2 больных в сочетании с поражениями шейных и грудных сегментов. Поражение лицевого, слухового и тройничного нерва (синдром Ханта) встретилось у 1 больного.
Поражение шейных сегментов отмечено у 3 (3,7%), грудных — у 27 (32,9%), поясничных — у 7 (8,5%) больных. С локализацией высыпаний в области верхних конечностей было 9 (11%) больных, а в области нижних конечностей — 10 (12,2%) больных.
У наблюдаемых больных по данным анамнеза отмечались частые рецидивы герпетической инфекции, что, безусловно, связано с прогрессированием иммунодефицита на фоне Из наблюдаемых нами больных 42,4% страдали легкой формой герпетической инфекции — с частотой рецидивов от 1 до 3 раз в год. У 37,6% больных с герпетической инфекцией со среднетяжелой формой частота рецидивов составила от 4 до 6 раз в год. Пациентов с тяжелой формой (частота реидивов от 7 до 12 раз в год) было 20% (таб. №2).
Таблица 2. Частота рецидивов у больных ПГ на фоне
| Частота рецидивов в год | 1-3 | 4-6 | 7-12 | Всего |
|---|---|---|---|---|
| Количество больных | 36 | 32 | 17 | 85 |
| % | 42,4 | 37,6 | 20,0 | 100 |
У 36 пациентов частота рецидивов составляла раза в год. Причем, 29 из них приходилось на IIБ и IIВ стадии В большинстве случаев мы не можем рассматривать частоту рецидивов от 1 до 3 раз в год на IIБ и IIВ стадии как свидетельство прогрессии основного заболевания, так как 17 из 29 больных изначально страдали простым герпесом, а затем были инфицированы ВИЧ. Увеличение количества частоты рецидивов простого герпеса на IIБ и IIВ стадии может свидетельствовать о нарастании иммунодефецита (у 14 больных количество лимфоцитов составляло менее 0,500х109/л, у половины из них — менее 0,300х109/л). Увеличение количества больных (29 чел.) с частотой рецидивов от 4 до 12 раз в год в более продвинутых стадиях (IIIA, IIIБ, IIIB) может быть связано как с нарастанием иммунодефецита, так и с неполным восстановлением показателей иммунитета при недавно назначенной высокоактивной антиретровирусной терапии (ВААРТ).
Как известно, у "иммунокомпетентных« лиц рецидив опоясывающего герпеса исключительно редкое явление и наблюдается оно, как правило, на фоне иммуносупрессивной терапии. Мы наблюдали 6 (7,3%) больных с рецидивирующим опоясывающим герпесом на IIIА и IIIБ стадиях Надо отметить, что у 3 больных при рецидивах высыпания располагались в иных зонах, чем при первой атаке. Следовательно, больные с подозрением или подтвержденным диагнозом рецидивирующего опоясывающего герпеса подлежат обследованию на
На момент исследования из симптомов интоксикации преобладали недомоганием (27,0%) и повышение температуры тела (23,5%) у больных простым герпесом. Наименьшее количество больных (8,2%) предъявили жалобы на головные боли. Из субъективных ощущений максимальное количество больных (88,2%) простым герпесом беспокоил зуд.
Важным клиническим симптомом, отличающим простой герпес на фоне явилось формирование эрозивно-язвенных дефектов, которые наблюдались у 14 (16,5%) больных. Данное обстоятельство указывает на прямую связь развития язвенных дефектов с иммунодефицитом, принимая во внимание тот факт, что язвенная форма простого герпеса у "иммунокомпетентных« лиц относится к атипичным клиническим вариантам болезни, развивающимся, как правило, фоне тяжелых общих заболеваний.
У больных опоясывающим герпесом симптомы интоксикации отмечали у всех пациентов, но из них преобладали недомогание (92,7%), головные и мышечные боли (84,1% и 76,8% соответственно). Наименьшее количество больных (14,6%) отмечали тошноту. В 100% случаев больные опоясывающим герпесом из субъективных ощущений предъявляли жалобы на боль в зоне высыпаний.
У 53 (64,6%) больных поражение кожи протекало с образованием пузырей. Значимость данного феномена подчеркивает тот факт, что у "иммунокомпетентных« больных опоясывающим герпесом везикулезные высыпания трансформируются в буллезные, примерно, в 100% случаев. Следовательно, пузырная форма опоясывающего герпеса в ряде случаев может служить своеобразным маркером
Следует отметить, что выраженность клинических проявлений и характер течения простого и опоясывающего герпеса у ВИЧ инфицированных больных зависела от величины снижения числа CD4 — лимфоцитов. То есть эрозивноязвенные дефекты, сопровождающиеся болезненностью, поражение сразу нескольких анатомических зон, частота рецидивов от 7 до 12 раз в год — при постом герпесе, множественные пузыри на фоне выраженной отечности, смежные локализации при опоясывающем герпесе наблюдались у больных с количеством CD4 — лимфоцитов менее 0,500х109/л.
Состояние иммунитета у больных простым и опоясывающим герпесом на фоне
Оценка глубины иммунодефецита при основывается на различных исследованиях иммунного статуса, в котором наибольшее значение имеет количество (CD4) и цитотоксических (CD8).
Иммунологическое исследование проводилось 52 больным простым и 40 — опоясывающим герпесом на фоне
Имел место дисбаланс абсолютного и относительного количенства иммунорегуляторных клеток. Так, наблюдалось уменьшение процентного содержания в 2,0 и в 2,7 раза при простом и опоясывающем герпесе соответственно по сравнению с показателями нормы. Так же отмечалось уменьшение и абсолютного количества у больных простым и опоясывающим герпесом (в 2,6 раза и в 3,0 раза соответственно). В свою очередь, процентное и абсолютное количество повышалось у больных обоими заболеваниями. Процентное содержание CD8 было в 2,3 раза выше средних показателей нормы при простом и в 2,5 раз при опоясывающем герпесе, CD8абс. — выше нормы в 1,8 раз и в 2,1 раза соответственно. CD4/CD8 составил 0,48 у больных простым и 0,36 у больных опоясывающим герпесом при средней норме 1,85, что ниже в 3,9 раз и в 5,1 раза соответственно и указывает на преобладание супрессорных влияний.
У значительного числа больных (6,1%) было обнаружено понижение количество (менее 0,500х109/10л) снижение То есть у большинства пациентов имело место наличие иммунодефицита, что способствовало развитию простого и опоясывающего герпеса. У остальных 33 (35,9%) пациентов с количеством более 0,500х109/10л, возможно, к возникновению простого и опоясывающего герпеса привел не количественный иммунодефицит, а функциональные изменения в системе иммунитета. Так, больные на IIБ, IIВ стадиях были лица, употребляющие наркотики. Использование наркотиков может приводить к изменениям в системе иммунитета, в частности, к функциональным нарушениям. Больные на более поздних стадиях получали ВААРТ, в связи с чем количество увеличилось, а функционально, скорее всего, они были неполноценны, так как возникновение простого и опоясывающего герпеса наступило в первые 3 месяца, когда происходило восстановление параметров системы иммунитета на фоне ВААРТ.
ПЦР и ИФА в диагностике простого и опоясывающего герпеса у ВИЧ инфицированных лиц
Оппортунистический характер заболеваний, вызываемых ВПГ и ВЗВ, а условиях широкого распространения иммунодефицитных состояний определяет актуальность проблемы своевременной и точной диагностики герпесвирусных инфекций.
В результате проведения исследований были получены следующие данные:
1. ДНК ВПГ и ВЗВ в материале из герепетических высыпаний обнаружили у подавляющего большинства больных — у 60 (88,2%), что подтверждает высокую диагностическую ценность этого метода.
2. В крови ДНК ВПГ и ВЗВ у 3 (4,4%) больных, из них у 1 простым и у 2 опоясывающим герпесом. Полученные данные дают основание предположить, что поиски вируса в крови имеют незначительную диагностическую ценность, поскольку продолжительность времени кратковременна.
3. Антитела ВПГ и типов класса Ig G в крови обнаружили у всех обследуемых больных простым герпесом (титры антител в среднем составили 8,9 ед/мл при положительном результате от 1 до 15 ед/мл).
4. У пациентов с инфекцией ВИЧ антитела класса Ig M не были обнаружены либо потому, что эти антитела не успели образоваться на момент обращения за помощью или, возможно, была слабая выработка антител за счет иммунодефицита.
Полученные результаты показали, что лабораторной диагностики ПЦР рекомендуется использовать как основной метод, ИФА — как вспомогательный метод.
Лечение простого и опоясывающего герпеса у ВИЧ инфицированных больных
Анализируя клиническое течение простого и опоясывающего герпеса у ВИЧ инфицированных больных, получавших противогерпетические препараты, были изучены такие показатели, как время образования корочек, скорость эпителизации эрозивно-язвенных дефектов кожи и слизистых оболочек и полный регресс высыпаний.
У больных с рецидивирующим простым герпесом на фоне эффективность лечения определяли, оценивая динамику клинических проявлений и частоту рецидивов.
Эффект, как "отличный« оценивался при отсутствии рецидивов у больных в течение 6 месяцев. Как »хороший« оценивался при удлинении времени ремиссии и уменьшения тяжести рецидивов без снижения количества рецидивов.
В процессе лечения больных простым герпесом (53 чел.) Валацикловиром обратное развитие сыпи (образование корочек и эпителизация) происходило на сутки, а полный регресс высыпаний наблюдали на сутки. У больных (22 чел.), которым назначали Ацикловир появление корочек и эпителизацию отмечали на сутки, а полный регресс очагов поражения наступал на сутки.
При лечении больных опоясывающим герпесом (45 чел.) Валацикловиром образование корочек и эпителизация происходила на сутки и полное заживление — на день с момента начала терапии.
У больных (28 чел.), которым лечение проводили Ацикловиром, обратное развитие сыпи отмечали на сутки, а полный регресс — на сутки.
Средняя продолжительность периода с момента появления высыпаний до постановки диагноза составила 4,2 дня.
У больных простым и опоясывающим герпесом, которым проводилась терапия Валацикловиром, сокращение сроков образования корок и полное заживление очагов поражения наступало на дня раньше, чем у больных, получавших Ацикловир.
Выводы
1. У больных помимо традиционных мест расположения простого герпеса — лабиального у 38 (44,7%) больных и генитального у 35 (41,2%), у 12 (14,1%) — герпетические высыпания имеют иную локализацию; у 17 (20%) больных отличаются мультифокальностью с вовлечением в патологический процесс сразу нескольких анатомических зон или с расположением в иных зонах при последующем рецидиве; эрозивноязвенные дефекты кожи и слизистых оболочек наблюдаются у 14 (16,55%) больных.
2. У 53 (64,6%) больных опоясывающим герпесом на фоне поражение кожи протекает с образованием пузырей; рецидивы опоясывающего герпеса наблюдаются у 6 (7,3%) больных, при этом, у половины из них высыпания располагаются в иных зонах, чем при первой атаке.
3. Выраженность клинических проявлений и характер течения простого и опоясывающего герпеса на фоне зависит от величины снижения числа У большинства больных (64,1%) количество составило менее 0,500х109/10л, что способствовало развитию простого и опоясывающего герпеса у ВИЧ инфицированных лиц.
4. ДНК ВПГ и ВЗВ в соскобах из пораженных участков кожи и слизистых оболочек обнаружена у 60 (88,2%) больных что указывает на высокую диагностическую ценность ПЦР при верификации простого и опоясывающего герпеса. При этом определение ДНК ВПГ и ВЗВ в крови обследованных больных не было информативным, поскольку дает положительный результат лишь у 3 (4,4%) пациентов. С помощью ПЦР метода выявления ДНК ВИЧ в материале соскобов из герпетических высыпаний у 9 (42,8%) пациентов, что может служить дополнительным фактором распространения
5. Через 1 месяц после лечения Валацикловиром отмечается статистически достоверное улучшение иммунологических показателей у ВИЧ инфицированных больных простым герпесом, тогда как у больных, страдающих опоясывающим герпесом, существенных сдвигов в системе иммунитета не наблюдается, что обусловлено прогрессированием
Практические рекомендации
1. При диагностике простого и опоясывающего герпеса у ВИЧ инфицированных больных наряду с данными анамнеза и объективными данными рекомендуется применять лабораторные методы исследования.
2. Для лабораторного исследования рекомендуется использовать как основной метод — полимеразную цепную реакцию (ПЦР). В качестве биологического материала использовать соскобы из очагов герпетических поражений кожи и слизистых оболочек.
3. Лечение простого и опоясывающего герпеса у ВИЧ инфицированных больных предпочтительно проводить Валацикловиром: а) при простомгерпесе — тпо 500 мг 2 раза в сутки в течение дней; б) при опоясывающем герпесе — по 1000 мг 3 раза в сутки в течение дней.
Категории МКБ: Герпетическая болезнь глаз (B00.5+), Герпетическая инфекция неуточненная (B00.9), Герпетическая экзема (B00.0), Герпетический везикулярный дерматит (B00.1), Герпетический гингивостоматит и фаринготонзиллит (B00.2), Герпетический менингит (B00.3+) (G02.0*), Герпетический энцефалит (B00.4+) (G05.1*), Диссеминированная герпетическая болезнь (B00.7), Другие формы герпетических инфекций (B00.8)
Общая информация
Краткое описание
Герпетическая инфекция (простой герпес, herpessimplex) – широко распространенная антропонозная вирусная болезнь, вызываемая вирусом простого герпеса 1 и 2 типов, преимущественно контактным механизмом передачи возбудителя, характеризуемая поражением кожи и слизистых оболочек, нервной системы, глаз, мочеполовой системы и других, внутренних органов, склонная к хроническому рецидивирующему течению.
Пользователи протокола: терапевты, врачи общей практики, инфекционисты, невропатологи, дерматовенерологи, акушер-гинекологи, стоматологи, офтальмологи, отоларингологи, урологи, анестезиологи-реаниматологи.
Класс I – польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III – имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию.
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Врожденная (внутриутробная инфекция).
- генерализованную (висцеральную, диссеминированную) ГИ.
- медленная форма герпетической инфекции.
- поражения слизистых оболочек желудочно-кишечного тракта (стоматит, гингивит, фарингит, эзофагит и др.);
- поражения глаз: офтальмогерпес (герпетический конъюктивит, кератит, иридоциклит, неврит зрительного нерва, оптикомиелит и др.);
- генитальный герпес (герпетическое поражение слизистых оболочек полового члена, вульвы, влагалища, цервикального канала и т.д.);
- поражения нервной системы (менингит, энцефалит, менингоэнцефалит, неврит, менингоэнцефалорадикулит, поражения бульбарных нервов и др.);
- Активная стадия инфекции: продуктивная вирусная инфекция, реализация генетической информации завершается образованием вирусного потомства, дочерних вирусных частиц.
- Неактивная стадия инфекции — абортивная вирусная инфекция, реализуется генетическая информация только неструктурных (альфа-) генов без образования новых дочерних частиц вируса.
- Первичная инфекция. Развивается после заражения вирусом неинфицированного ранее лица. В крови пациентов антитела к ВПГ до развития герпетической инфекции не выявляются. Инфекция сопровождается появлением противовирусных антител (сероконверсией), 4-кратным нарастанием концентрации иммуноглобулинов класса G.
- Первичная инфекция с одиночным местом внедрения вируса (например, через слизистую гениталий или ротовой полости).
- Первичная инфекция с множественными входными воротами инфекции (слизистая гениталий, ротовой полости, сосков молочных желез, кожные покровы промежности, ягодиц, внутренней поверхности бедер, перианальной области и т.д.).
- Аутоинокуляция— механический перенос вируса у инфицированного с одного участка на другие участки тела (например, из ротовой полости на гениталии).
- Латентная инфекция — неактивная стадия инфекции. Инфекционный вирус не обнаруживается в биологических материалах (слюне, моче, секретах гениталий). Вирус сохраняется в виде ДНК-белкового комплекса в нервных ганглиях.
- Первый эпизод герпеса: впервые выявленные клинические проявления герпеса у ранее инфицированных лиц.
- Суперинфекция (субклиническая и клиническая): наслоение одной инфекции на другую (например, заражение вирусом простого герпеса 2 типа половым путем лица, страдающим герпетическим стоматитом, вызванным ВПГ-1).
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий [1,2,3,4,5,6]
Основные диагностические исследования, проводимые на амбулаторном уровне:
- определение антител IgM и IgG к вирусу простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2) в сыворотке крови методом ИФА;
- определение ДНК ВПГ методом ПЦР (кровь, мазки со слизистых оболочек, содержимое герпетических пузырьков, СМЖ (в зависимости от локализации герпетических поражений));
- УЗИ плода (у беременных);
- определение антител к ВИЧ методом ИФА;
- офтальмоскопия (при поражении глаз);
- ЭКГ.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные диагностические исследования, проводимые на стационарном уровне:
- определение ДНК ВПГ методом ПЦР при поражении ЦНС, висцеральных и генерализованных формах ГИ (качественный);
- гистологическое исследование биопсийных материалов на ВПГ.
Дополнительные диагностические исследования, проводимые на стационарном уровне (в зависимости от клинической формы):
- биохимическое исследование крови (билирубин и фракции, АЛТ, АСТ, тимоловая проба);
- рентгенография органов грудной клетки;
- ЭГДС и колоноскопия;
- УЗИ органов брюшной полости;
- КТ, МРТ;
- спинномозговая пункция с исследованием СМЖ (маркеры ВПГ, антитела к ВПГ-1/-2, белок, лимфоциты и др.(при поражении ЦНС));
- офтальмоскопия;
- ЭКГ;
- определение антител к ВИЧ методом ИФА.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
Жалобы и анамнез:
Клинические проявления ПГ зависят от локализации патологического процесса и его распространенности, состояния иммунной системы больного и антигенного типа вируса.
- пузырьковые высыпания на коже в области красной каймы губ, вокруг рта, в области крыльев носа, на кистях, в области ягодиц;
Изучены особенности клинического течения локализированных и генерализированных форм герпетической инфекции, обусловленной вирусом простого герпеса І и ІІ типов у 100 больных на разных стадиях ВИЧ-инфекции. Установлено, что локализированные формы герпетической инфекции – лабиальный и генитальный герпес – преобладают у пациентов с І и ІІ стадиях ВИЧ-инфекции. Они отличаются от аналогичных форм у пациентов без ВИЧ-инфекции более тяжелым течением, рецидивирующим характером, склонностью элементов сыпи к распространению на соседние анатомические участки. Висцеральные и генерализированные формы герпетической инфекции, которые свидетельствуют о выраженной иммуносупрессии, характерны для стадии СПИДа. Они проявлялись эрозивно-язвенным эзофагитом, проктитом, интерстициальной пневмонией, энцефалитом, который был непосредственной причиной смерти таких больных. Как СПИД индикаторное заболевание следует рассматривать и локализированные формы герпетической инфекции – лабиальный и генитальный герпес – при эрозивно-язвенном, диссименированном характере поражений продолжительности более 1 месяца.

1. Бабий Н.А. Ко-инфекции вирусного генеза у больных ВИЧ-инфекцией / Н.А. Бабий, А.М. Щербинская // Инфекционные болезни. – 2007. – № 2. – С. 23–26.
2. Баринский И.Ф. Герпесвирусные инфекции – иммунодефицитные заболевания ХХ века / И.Ф. Баринский // Аллергология и иммунология. – 2004. – Т. 5, № 1. – С. 202–204.
3. Запорожан В.Н. ВИЧ-инфекция и СПИД / В.М. Запорожан, М.Л. Аряев. Изд. перераб. и доп. – Киев: Здоровье, 2004. – 636 с.
4. Казмирчук В.Е. Клиника, диагностика и лечение герпесвирусных инфекций человека / В.Е. Казмирчук, Д.В. Мальцев – М.: Феникс, 2009. – 247 с.
5. Казмирчук В.Е. Клиническая иммунология и аллергология / В.Е. Казмирчук, Л.В. Калюжная Л.Д. Ассоциации инфекций, передающихся половым путем у ВИЧ-инфицированных / Л.Д. Калюжная, Л.В. Гречанський // Украинский журнал дерматологии, венерологии, косметологии. – 2004. – № 1.– С. 78–80.
6. Лабораторная диагностика герпесвирусной инфекции человека / Л.А. Панченко, И.И. Торяник, Н.Г. Попова [и др.]. // Инфекционные болезни. – 2006. – № 3. – С. 62–66.
7. Малый В.П. СПИД-ассоциированные инфекции и инвазии: учебное пособие / В.П. Малый, И.С. Кратенко. – Харьков: Фолио, 2007. – 287 с.
8. Маричев И.Л. Герпесвирусы-СПИД маркерные заболевания / И.Л. Маричев // Современные инфекции. – 2005. – № 3–4. – С.55–59.
9. Маричев И.Л. Герпетическая инфекция у ВИЧ-инфицированных / И.Л. Маричев / Инфекционные болезни. – 2006. – № 2. – С.15–17.
10. Медико-профилактические аспекты ВИЧ-инфекции и СПИДа в врачебной практике / Б.М. Дикий, И.Г. Грижак, А.Д. Щербинская [и др.]. – Киев: Изд-во ИФДМУ, 2007. – 236 с.
Введение
Цель нашего исследования - провести ретроспективный анализ течения герпетической инфекции у больных с учетом стадии ВИЧ-инфекции на основании анализа данных медицинских карт стационарных и амбулаторных больных.
Материалы и методы исследования. Проведен ретроспективный анализ медицинской документации 100 больных ВИЧ-инфекцией. В исследуемую группу входили больные на разных стадиях заболевания в возрасте от 18 до 40 лет. I стадия - 24, II - 37, III - 22, IV - 17 больных. Установлено, что среди больных, которые находились на учете в областном Центре борьбы и профилактики ВИЧ/СПИДа, инфицированы ВИЧ парентеральным путем 42 человека, половым - 58. Диагноз ВИЧ-инфекции установлен на основании данных эпидемиологического, клинического и лабораторного обследования, подтверждено двукратным выявлением антител (АТ) к ВИЧ методом иммуноферментного анализа (ИФА). Диагноз ГИ устанавливали на основании выявленных изменений со стороны органов и систем, учитывая политропность возбудителя и генерализированный характер поражений в терминальной стадии заболевания. Этиологическая расшифровка ГИ базировалась на результатах полимеразной цепной реакции (ПЦР).
Ни одного случая острой ГИ у пациентов с ВИЧ-инфекцией не зарегистрировали. Во всех диагностировали различные формы хронической ГИ, реактивация которой имела место в 38 %, а рецидивирующее течение - в 62 % случаев. Так, ВПГ 1 вызывал рецидивы назального и лабиального герпеса (30 больных), его первые клинические проявления (10 больных), а также гингивостоматит (5 больных) и фаринготонзиллит (2 больных) только в I (21) и ІІ (26) стадиях ВИЧ-инфекции. Количество больных, у которых диагностировали ГИ в указанных стадиях, составляло соответственно 87,4 % и 70,2 %.
ВИЧ-ассоциированная ГИ с поражением кожи и слизистых характеризовалась не только более обильными и распространенными элементами везикулезной сыпи, но и замедленным ее регрессом, продолжительностью более 1 месяца (от 6 до 8 недель). Кроме этого, в 30,7 % больных во ІІ стадии ВИЧ-инфекции наблюдали эрозивно-язвенную форму ГИ - глубокие эрозии с трансформацией в язвы, которые медленно заживали. Следует отметить, что герпетические поражения кожи в виде сгруппированных пузырьков с серозным содержимым отмечали не только в местах их типичной локализации - на губах, крыльях носа. У больных во ІІ стадии ВИЧ-инфекции они распространялись на лоб, щеки, уши. Поражение слизистой ротоглотки всегда сопровождалось постоянной и выраженной болезненностью, гиперемией, гиперсаливацией, язвенным гингивитом.
Рецидивы лабиального герпеса у ВИЧ-инфицированных больных характеризовались большей частотой и выраженностью клинических проявлений в сравнении с больными, не инфицированными ВИЧ. У инфицированных ВИЧ ежемесячные рецидивы лабиального герпеса регистрировали у 26 больных, каждые 3 месяца они развивались у 20 больных и проявлялись групповыми (12 больных) и множественными (8 больных) везикулами, которые распространялись на щеки и околоушную область. У не инфицированных ВИЧ ежемесячных рецидивов не было, каждые 3 месяца они развивались у 4 больных, а каждые 6 месяцев - у 8. При этом элементы сыпи были единичными, не распространялись за пределы губ.
Рецидивы гингивостоматита сопровождались субфебрилитетом, умеренной интоксикацией, множественными глубокими эрозиями с отеком и гиперемией слизистой оболочки полости рта, тогда как у больных без ВИЧ-инфекции они протекали в более легкой форме, без нарушения общего состояния больного, с менее выраженними изменениями слизистой оболочки.
Данные анамнеза свидетельствуют, что до инфицирования ВИЧ рецидивы лабиального герпеса чаще всего имели место каждые 6 месяцев - у 13 больных, тогда как после инфицирования ВИЧ рецидивы у большинства больных (26) наблюдались ежемесячно.
Генитальный герпес (ГГ) чаще диагностировали у больных в ІІІ стадии ВИЧ-инфекции (49,9 %) в сравнении с больными во II стадии (24,3 %) и I (12,0 %). Заболевание имело рецидивирующее течение у 18,9 % больных во II стадии и 40,9 % больных в ІІІ стадии ВИЧ-инфекции. Если в I стадии поражались только наружные половые органы, то во II и III - еще и внутренние (вагинит, цервицит) в виде множественных глубоких эрозий и язв. В IV стадии ВИЧ-инфекции проявления ГГ наблюдали в 11,7 % больных в виде поражений только внутренних половых органов (язвенно-некротический вагинит, цервицит). Нередко ГГ проявлялся еще и экстрагенитальными поражениями, которые обнаруживали на ягодицах, задней и внутренней поверхности бедер у каждого второго больного с II и во всех с III и IV стадиями ВИЧ-инфекции. Явлениями тазового ганглионеврита сопровождался ГГ у 5,4 % лиц с II и 18,1 % с ІІІ стадией ВИЧ-инфекции. Кроме сыпи на больших и малых половых губах, слизистой влагалища, шейке матки, промежности, ГГ проявлялся язвенным поражением уретры и прямой кишки в III и IV стадиях ВИЧ-инфекции. Герпетический уретрит диагностировали у 13,6 % больных в ІІІ стадии, а герпетический проктит - соответственно в 18,1 % и 23,5 % больных в III и IV стадиях заболевания.
Для рецидивов ГГ у ВИЧ-инфицированных больных характерна большая частота и выраженность клинических проявлений, чем у больных не инфицированных ВИЧ. Среди инфицированных ВИЧ ежемесячные рецидивы ГГ наблюдались у 9 больных, каждые 3 месяца они развивались у 5 больных, проявлялись групповыми (2 больных) и множественными (3 больных) везикулами. Каждые 6 месяцев рецидивы ГГ с множественными элементами сыпи возникали у 2 больных. У не инфицированных ВИЧ ежемесячных рецидивов ГГ не было, регистрировались рецидивы каждые 3 месяца - в 3, каждые 6 месяцев - у 2 больных.
Анализируя данные анамнеза, мы установили, что до инфицирования ВИЧ рецидивы ГГ у больных чаще всего имели место каждые 6 месяцев (8 пациентов), тогда как после инфицирования ВИЧ максимальной была частота ежемесячных рецидивов (9 пациентов).
Диагностировали не только локализированные, но и висцеральные и генерализорованные формы ГИ. Гематогенная диссеминация ВПГ 1 в IV стадии ВИЧ-инфекции приводила к поражениям внутренних органов. Диагностировали эзофагит у 29,4 %, а интерстициальную пневмонию - 17,6 % больных. У всех больных пневмония сочеталась с эзофагитом. Генерализация ГИ на фоне выраженного ВИЧ-иммунодефицита сопровождалась поражением ЦНС. Оно проявилось в 17,6 % больных подострым энцефалитом, который был непосредственной причиной смерти. Тяжесть энцефалита обусловлена его некротическим характером.
Клинически у этих больных не наблюдали проявлений общей интоксикации и менингеальных симптомов. Очагово-неврологическая симптоматика развивалась постепенно, проявлялась различными расстройствами сознания с формированием симптомов поражения лобных, височных и теменных отделов мозга. О локальном и мозаичном поражение коры головного мозга свидетельствовали нарушение восприятия, мышления и памяти. Типичными клиническими проявлениями энцефалита были симптомы поражения передних отделов головного мозга - психические расстройства (афазия, дисфазия), агнозия, амнезия, центральные гемипарезы, а также невриты и плегия.
Ликвор при исследовании был прозрачным, бесцветным, ликворное давление нормальное или несколько повышено, плеоцитоз не превышал сотни клеток в 1 мкл, преобладали лимфоциты, белок в пределах нормы, белково-клеточной диссоциации не наблюдалось. По результатам МРТ выявляли гиподенсивные очаги размерами от 1,5 до 5 см в диаметре с локализацией в левой височно-теменной, правой лобной и затылочной долях. Очаги имели неправильную форму, с нечеткими контурами, незначительным перифокальным отеком и геморрагическим пропитыванием.
У больных, умерших от энцефалита, при гистиологическом исследовании тканей головного мозга обнаружили выраженные структурные изменения в сосудах и нервных клетках, которые возникли на фоне отека-набухания головного мозга. Энцефалит характеризовался преимущественно некротическими изменениями с образованием очагов деструкции в сером веществе передних отделов головного мозга (медио-базальных, лобных, височных и теменных) и воспалительной реакцией различной степени выраженности. В меньшей степени поражались оболочки мозга. Мягкие оболочки были утолщены, набухшие, умеренно инфильтрованны гистиоцитарными элементами, лимфоидными клетками, реже нейтрофильными лейкоцитами. Отмечались геморрагии и субарахноидальные кровоизлияния, глубокая дистрофия нейронов: гомогенизация и гиперхромия цитоплазмы, перераспределение хроматина в ядрах нейронов, их пикноз, лизис и гибель нервных клеток. Обнаруживали зоны выпадения нейронов и очаги некроза нервной ткани. В сосудах различного калибра, чаще в капиллярах, во всех случаях наблюдали проявления ДВС-агрегации эритроцитов, сладж и формирование тромбов, наличие геморрагий без периваскулярной инфильтрации.
У таких пациентов наблюдали очагово-некротические изменения в печени и надпочечниках, подобные очаги некрозов на слизистой оболочке ротовой полости, в легких - отек стенок альвеол, интерстициальную пневмонию.
Учитывая очень широкий спектр поражений - от кожи и слизистых оболочек до внутренних органов и ЦНС, диагностика ГИ на фоне ВИЧ-инфекции достаточно сложна. Поэтому без лабораторного подтверждения диагноза у таких больных она невозможна. При этом обнаружение вируса и его антигенов является основным, а антител к вирусу - вспомогательным методом диагностики ГИ.
Нами проанализированы серологические маркеры ВИЧ-ассоциированной ГИ в зависимости от числа СD4 + Т-лимфоцитов у больных без иммунодефицита (>500), с умеренным (500-350), выраженным (350-200) и глубоким (<200) иммунодефицитом.
Установлено, что титры IgG к ВПГ 1/2 у пациентов с ВИЧ-ассоциированной ГИ были разными. Их уровень в большинстве случаев был умеренным (50-100 МЕ/мл) - 51,0±5,0 %, значительно реже низким (100 МЕ/мл) - 22,0±4,1 %. Наблюдали зависимость диагностических уровней ІgG к ВПГ 1/2 от наличия иммунодефицита, обусловленного ВИЧ, и степени его тяжести. Высокий специфический гуморальный ответ на ГИ давали только больные без иммунодефицита (22,0±4,1 %), умеренный - больные с умеренным иммунодефицитом (40,0±4,9 %), незначительный процент с выраженным иммунодефицитом (3,0±1,7 из 13,0±3,4 %) и без иммунодефицита (8,0±2,7 из 0,0±4,6 %). Низкий гуморальний ответ на ГИ характерен для пациентов с глубоким иммунодефицитом (17,0±3,7 %) и большинства с выраженным иммунодефицитом (10,0±3,0 из 13,0±3,4 %).
Таким образом, диагностика ВИЧ-ассоциированной ГИ сопровождается значительными трудностями. Они связаны со сложностью верификации диагноза при помощи специфических серологических маркеров на фоне иммунодефицита. Угнетение синтеза противогерпетических антител класса IgG, низкие их титры у ВИЧ-положительных маскируют истинную частоту активных форм ГИ. Изучение специфических лабораторных маркеров ГИ у ВИЧ-инфицированных показало, что на основании только серологических обследований невозможно установить активность инфекционного процесса и определить тактику лечения больных.
Наиболее информативными являются результаты ПЦР, позволяющие своевременно выявлять активные формы инфекции, что имеет принципиальное значение для тактики лечения больных. Одновременно с серологическими обследованиями выявляли ДНК ВПГ 1/2 методом ПЦР. Герпес кожи и слизистых оболочек подтверждали методом ПЦР в 10,0 % пациентов с поражением слизистой ротоглотки и полости рта у 15,0 % пациентов с нетипичным поражением кожи (эрозивно-язвенным, геморрагически-некротическим, импетигоподобным). В 75,0 % случаев при типичном характера сыпи на коже в виде везикул диагноз не вызывал сомнения. У больных с ГГ чаще получали положительные результаты ПЦР при исследовании материала из влагалища и цервикального канала (соответственно 56,3 и 43,7 %), значительно реже - из прямой кишки и уретры (соответственно 12,5 и 9,38 %).
Положительные результаты ПЦР при исследовании крови, подтверждающие вирусемию и свидетельствующие о репликации ВПГ на системном уровне, получили в 62,5 % больных с генерализованной ГИ. Вирусемия сопровождалась герпетическим эзофагитом (62,5 %), пневмонией (37,5 %), проктитом (25,0 %). Поражались не только пищевод, легкие, прямая кишка, но и ЦНС. Герпетическая этиология энцефалита подтверждена у 100 % больных с генерализованной ГИ при исследовании ликвора методом ПЦР.
Ассоциированную с ВИЧ-инфекцией ГИ следует, по нашему мнению, называть не только СПИД-ассоциированным заболеванием, а суперинфекцией, патогенетически связанной с ВИЧ-инфекцией. На фоне вторичного иммунодефицита, обусловленного ВИЧ, ГИ приобретает генерализированный характер с множественными поражениями внутренних органов и ЦНС. Если в организме здорового иммунокомпетентного человека иммунные механизмы контролируют персистенцию ВПГ в паравертебральных нервных ганглиях, обеспечивая латентную форму ГИ, то на фоне ВИЧ-инфекции, сопровождающейся выраженным иммунодефицитом, ГИ приобретает рецидивное, манифестное течение с системными поражениями, генерализацией инфекционного процесса.
На основании анализа течения и диагностики ВИЧ-ассоциированной ГИ можно сделать следующие выводы:
1. Течение ГИ зависит от стадии ВИЧ-инфекции. У больных в I и II стадиях заболевания диагностировали только локализованные формы ГИ с поражением кожи, слизистой ротоглотки, гениталий, которые отличались рецидивирующим течением, склонностью элементов сыпи к распространению.
2. Клиника ГИ у больных в III и IV стадиях ВИЧ-инфекции полиморфная и проявляется поражениями внутренних органов, которые не наблюдаются у пациентов с ГИ без ВИЧ-инфекции. В условиях иммунодефицита ВИЧ-этиологии ГИ приобретает системный, нередко генерализированный характер с поражением внутренних органов (эзофагит, пневмония, проктит), ЦНС (энцефалит), характеризуется тяжелым и часто является непосредственной причиной смерти больных СПИДом.
3. Как СПИД индикаторное заболевание следует рассматривать и локализованные формы ГИ - лабиальный и генитальный герпес - при эрозивно-язвенном, диссиминированном характере поражений продолжительностью более 1 месяца.
4. Для своевременной диагностики генерализованных форм ГИ необходимо использовать метод ПЦР, диагностическая информативность которого при исследовании крови составляет 62,5 %, а ликвора у больных энцефалитом - 100 %. Диагностическая информативность ПЦР при исследовании материала из влагалища и цервикального канала составляет 100 % у больных с герпетическим цервицитом и вагинитом.
Рецензенты:
Дикий Б.Н., д.м.н., професор кафедры инфекционных болезней с курсом эпидемиологии Государственного высшего ученого заведения «Ивано-Франковский национальный медицинский университет» МОЗ Украины, г. Ивано-Франковск.
Пришляк А.Я., д.м.н., профессор, заведующий кафедрой инфекционных болезней с курсом эпидемиологии Государственного высшего ученого заведения «Ивано-Франковский национальный медицинский университет» г. Ивано-Франковск.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Герпес: причины появления, симптомы, диагностика и способы лечения.
Определение
Герпесом, или герпетической инфекцией, называют несколько заболеваний, вызываемых вирусами отряда Herpesvirales семейства Herpesviridae.
Все они характеризуются поражением кожи, слизистых оболочек с локализацией либо в области глаз, носа и губ, гениталий, а также нервных волокон.
У лиц с иммунодефицитом могут наблюдаться генерализованные формы инфекции с вовлечением в процесс других органов и тканей.

Среди известных науке восьми типов герпеса самым распространенным является вирус герпеса простого типа (Herpes simplex virus).
Простой вирус герпеса достаточно неустойчив во внешней среде. В условиях комнатной температуры сохраняется до 24 часов, на металле — до 2 часов. Под действием температуры выше 50°C погибает за 30 минут, под действием спирта и хлорсодержащих веществ - в течение нескольких минут, при замораживании сохраняется до пяти суток.
Причины герпетической инфекции
Источником инфицирования всегда служит человек. Он заразен в любую фазу болезни или носительства, но преимущественно при обострении.
Возбудитель может передаваться воздушно-капельным, контактно-бытовым или половым путем, а также от матери плоду через плаценту, во время родов или грудного вскармливания.
К вирусу восприимчивы все люди, хотя у многих отмечаются бессимптомные формы заболевания. Попадая через слизистую рта, половых органов или дыхательные пути в организм человека, герпесная инфекция остается в нем навсегда. Вирус, скрытый внутри клетки-хозяина, не доступен для иммунных клеток, уничтожающих возбудителей. Вирус активизируется при ослаблении иммунитета в результате переохлаждения, перегрева, простудного заболевания, недостатка витаминов, переутомления, стресса, нехватки сна. Рецидив инфекции могут вызвать травмы, оперативные вмешательства, а также половой контакт при условии повреждения слизистой оболочки. Использование лекарственных и косметических средств, содержащих стероидные гормоны, также способствует манифестации вируса герпеса.
Классификация герпеса
В МКБ-10 (Международной классификации болезней) выделяют две группы заболеваний, связанных с вирусом простого герпеса:
- Инфекционные герпетические заболевания:
- герпетическая экзема (экзема Капоши);
- герпетический везикулярный дерматит;
- герпетический гингивостоматит и фаринготонзиллит;
- герпетический менингит;
- герпетический энцефалит;
- офтальмогерпес;
- диссеминированная герпетическая болезнь (герпетический сепсис);
- другие формы герпетических инфекций;
- неуточненная герпетическая инфекция.
- Генитальные герпетические инфекции:
- герпетические инфекции перианальных кожных покровов и прямой кишки;
- неуточненная аногенитальная герпетическая инфекция.
По клинической картине и локализации высыпаний:
- Типичные формы:
- герпес кожи — с поражением губ, крыльев носа, лица, рук, ягодиц и других частей тела;
- герпес глаз — иридоциклит, кератит, конъюнктивит, неврит зрительного нерва;
- герпес слизистых оболочек желудочно-кишечного тракта — стоматит, гингивит, фарингит, эзофагит;
- герпес половых органов — поражение слизистой оболочки полового члена, влагалища, вульвы, цервикального канала;
- герпес внутренних органов — гепатит, пневмония, панкреатит, трахеобронхит;
- герпес нервной системы — неврит, менингит, менингоэнцефалит, поражения бульбарных нервов, энцефалит;
- генерализованный простой герпес — висцеральная форма (пневмония, гепатит, эзофагит) и диссеминированная форма (сепсис).
- Атипичные формы:
- герпетиформная экзема Капоши — обширные сливающиеся высыпания по всему телу;
- абортивный герпес — почти незаметные папулы на грубой коже или дискомфорт без высыпаний;
- язвенно-некротический герпес — с развитием некроза тканей;
- эрозивно-язвенный герпес — с образованием язв и эрозий;
- геморрагический герпес — с кровянистым пропитыванием высыпаний и тканей;
- отечный герпес — с отеком тканей и болью в области губ и век;
- зостериформный простой герпес — с локализацией по ходу нервного ствола;
- диссеминированный герпес — с тенденцией перехода в генерализованную форму при ВИЧ;
- рупиоидный герпес — возникает на лице с присоединением вторичной бактериальной флоры;
- мигрирующий герпес — с тенденцией к изменению локализации высыпаний.
- латентная стадия — носительство с отсутствием симптомов;
- локализованная стадия — наличие одного очага поражения;
- распространенная стадия — наличие не менее двух очагов поражения;
- генерализованная стадия — висцеральная, диссеминированная.
При заражении герпесом детей в возрасте от 6 месяцев до 3 лет чаще всего развивается герпетический стоматит, для которого характерно острое начало с симптомами интоксикации и подъемом температуры.
На слизистой оболочке полости рта появляются сгруппированные пузырьки с прозрачным содержимым, на месте которых после вскрытия образуются болезненные эрозии. У детей старшего возраста первичный герпес характеризуется появлением зудящих пузырьков на красной кайме губ и коже носогубного треугольника. После их вскрытия остаются неглубокие язвочки, которые покрываются корочками. Корочки, отпадая, не оставляют следов на коже.
При первичном заражении взрослых вирусом простого герпеса симптомы более выражены, чем при дальнейших рецидивах. Больной испытывает озноб, головные боли, повышенную утомляемость, у него отсутствует аппетит, может наблюдаться расстройство сна. Покраснение, а затем характерные пузырьки появляются на губах, возле крыльев носа. В некоторых случаях увеличиваются подчелюстные лимфоузлы.
Герпетические нейроинфекции сопровождаются наиболее тяжелым течением, особенно если вирус поражает оболочки или ткань головного мозга.
В этих случаях симптомы включают головные боли, подъем температуры тела, напряжение затылочных мышц, психомоторное возбуждение (болезненное состояние, при котором наблюдается беспокойство и двигательная активность различной степени выраженности, вплоть до судорог). При несвоевременной диагностике заболевания существует риск летального исхода.
Офтальмогерпес сопровождается покраснением глаза, развитием блефаро- или кератоконъюнктивита, эрозиями роговицы.
Диагностика герпеса
Типичные случаи герпетической инфекции выявляются на основании клинической картины и анамнеза заболевания. Характерно его волнообразное течение со сменой периодов обострения и ремиссии.
Косвенным признаком служит склонность к простудным заболеваниям, чувствительность к переохлаждению, периодически возникающие состояния, сопровождаемые подъемом температуры, усталостью, депрессией.

При атипичных формах герпетической инфекции необходимы дополнительные обследования: клинический анализ крови, биохимический анализ крови (общий белок, белковые фракции, С-реактивный белок, АЛТ, АСТ, ЛДГ, креатинин, электролиты: калий, натрий, хлор, кальций) и клинический анализ мочи - для выявления поражения внутренних органов и предупреждения осложнений.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

