Пласты цилиндрического эпителия в желудке что это
Обновлено: 26.04.2024
Опухоли пищевода. Доброкачественные и злокачественные опухоли пищевода.
В дистальном отделе пищевода изредка наблюдают аденому, имеющую такое же строение, что и аденомы желудка. Она может развиваться из слизистой оболочки при так называемом пищеводе Баррета, когда в результате хронического рефлюкс-эзофагита и гегеротопяи (что менее вероятно) многослойный плоский эпителий нижней части пищевода замещается цилиндрическим эпителием с формированием структур, соответствующих слизистой оболочке фундального или кардиального отделов желудка, нередко с явлениями кишечной метаплазии.
Рак — наиболее часто встречающаяся злокачественная опухоль пищевода. Чаще наблюдают у мужчин? возраст большинства которых 50—70 лет. К предрасполагающим факторам относятся особенности питания — употребление очень горячей и грубой пищи; недостаток витаминов, особенно В2, А; железа, меди, цинка; вредные привычки (курение, алкоголь и др.); некоторые географические особенности местности; аномалии и посттравматические рубцовые изменения пищевода, грыжа пищеводного отверстия диафрагмы, тилоз (гиперкератоз ладоней и подошв), синдром Пламмера—Винсона (железодефицитная анемия, гипохлоргидрия, дисфагия), наблюдающийся преимущественно у жительниц стран Скандинавского полуострова в возрасте 40 -45 лет и др.
Заболеваемость раком пищевода колеблется в очень широких пределах, достигая наиболее высоких показателей в некоторых районах Ирана, Китая, Туркменской, Казахской, Узбекской ССР и др. Эпидемиологические исследования показали, что в этих районах среди населения чрезвычайно широко распространен хронический эзофагит (60—80% населения и более), который, очевидно, имеет значение в развитии рака пищевода. При гистологическом исследовании на фоне хронического эзофагита обнаруживают очаговые и диффузные атрофические и гиперпластические изменения многослойного плоского эпителия, пролиферацию базальных клеток, очаги дисплазии, внутриэпителиальный и ранний инвазивный рак.
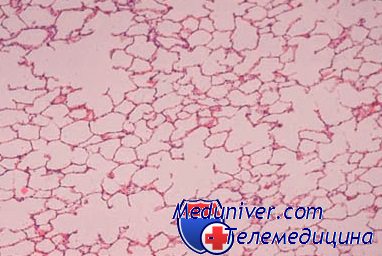
Такие же изменения часто можно обнаружить при раке пищевода, исследуя слизистую оболочку на различном расстоянии от опухоли. Эти изменения, по-видимому, являются основными этапами морфогенеза рака пищевода, что подтверждается динамическими наблюдениями, проведенными в районах Китая с повышенной заболеваемостью раком пищевода.
Предраковые изменения в многослойном плоском эпителии пищевода принципиально не отличаются от аналогичных изменений в шейке матки. Гистологическими критериями дисплазии являются усиление пролиферации и нарушение дифференцировки клеток. Количество базальных клеток, которые в норме занимают не более 15% толщины эпителиального пласта, при дисплазии увеличивается, клетки становятся более крупными, полиморфными, увеличивается число митозов. В зависимости от выраженности клеточных изменений и степени их распространения в эпителиальном пласте различают слабую» умеренную и тяжелую дисплазию. Выраженные полиморфизм и атипия клеток, большое количество митозов, утрата полярности расположения клеток и деления на слои при сохранении базальной мембраны характерны для внутриэпителиального рака.
В тех случаях, когда базальная мембрана не прослеживается, имеется тенденция к погружному росту и отшнуровка эпителиальных комплексов, изменения должны расцениваться как начало инвазивного рака.
При гистологическом исследовании, особенно по материалу эндоскопической биопсии, бывает трудно дифференцировать диспластические (предраковые) изменения и реактивную гиперплазию базальных клеток, которая может наблюдаться, например, при рефлюкс-эзофагите.
Трудности возникают также при дифференциальной диагностике тяжелой дисплазии, карциномы in situ и инвазивного рака. Для уточнения характера процесса необходимы динамическое наблюдение за такими больными и повторные биопсии.
Основная масса форм плоскоклеточного рака пищевода, видимо, развивается из покровного эпителия. Другим источником развития рака пищевода могут быть слизистые железы, в которых при хроническом гастрите также наблюдают атрофические и гиперпластические изменения, образование кист, пролиферацию резервных клеток, плоскоклеточную метаплазию и дисплазию эпителия. Из них могут возникать плоскоклеточный рак, аденокарцинома, железисто-плоскоклеточный рак, а также мукоэлидермоидная опухоль и аденокистозный рак (цилиндрома), аналогичные соответствующим опухолям слюнных желез. Аденокарциномы в пищеводе могут развиваться также от остатков цилиндрического эпителия, выстилающего пищевод на ранних стадиях эмбриогенеза, участков гетеротопии слизистой оболочки желудка.
Аденокарциномы дистальной части пищевода могут развиваться также на фоне так называемого пищевода Баррета. Во многих случаях труден или невозможен дифференциальный диагноз такой аденокарциномы и рака кардиального отдела желудка, прорастающего в пищевод.
Рак пищевода наиболее часто локализуется в средней его трети, затем следует нижняя треть пищевода; верхняя его треть поражается редко. Исключение составляет рак пищевода при синдроме Пламмера—Винсона, который наблюдается преимущественно у женщин 40—45 лет и поражает самый верхний отрезок пищевода.
Макроскопически большинство форм рака пищевода представляет собой изъязвленные блюдцеобразные или эндофитные опухоли, часто циркулярно охватывающие стенку, нередко на значительном протяжении. Экзофитные опухоли встречаются редко. Рак пищевода может распространяться по подслизистому слою далеко за пределы видимого очага опухоли, а также прорастать в прилежащие к пищеводу ткани и органы. Для суждения о степени распространенности процесса и радикальности оперативного вмешательства при исследовании удаленного отрезка пищевода необходимо изучение линий операционных разрезов и глубины прорастания стенки пищевода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эпителий желез желудка. Клетки желудка. Гормоны желудка.
Эпителий желез желудка представляет собой высокоспециализированную ткань, состоящую из нескольких клеточных дифферонов, камбием для которых служат малодифференцированные эпителиоциты в области шеек желез. Эти клетки интенсивно метятся при введении Н-тимидина, часто делятся митозом, составляя камбий как для поверхностного эпителия слизистой оболочки желудка, так и для эпителия желудочных желез. Соответственно этому дифференцировка и смещение вновь возникающих клеток идут в двух направлениях: в сторону поверхностного эпителия и в глубину желез. Обновление клеток в эпителии желудка происходит за 1-3 суток.
Значительно медленнее обновляются высокоспециализированные клетки эпителия желудочных желез.
Главные экзокриноциты вырабатывают профермент пепсиноген, который в кислой среде превращается в активную форму пепсин — главный компонент желудочного сока. Экзокриноциты имеют призматическую форму, хорошо развитую гранулярную эндоплазматическую сеть, базофильную цитоплазму с секреторными гранулами зимогена.
Париетальные экзокриноциты — крупные, округлой или неправильно угловатой формы клетки, расположенные в составе стенки железы кнаружи от главных экзокриноцитов и мукоцитов. Цитоплазма клеток резко оксифильна. В ней содержатся многочисленные митохондрии. Ядро лежит в центральной части клетки. В цитоплазме есть система внутриклеточных секреторных канальцев, переходящих в межклеточные канальцы. В просвет внутриклеточных канальцев выступают многочисленные микроворсинки. По секреторным канальцам из клетки на апикальную ее поверхность выводятся ионы Н и Сl, образующие соляную кислоту.
Париетальные клетки секретируют также внутренний фактор Кастла, необходимый для всасывания витамина Bi2 в тонкой кишке.
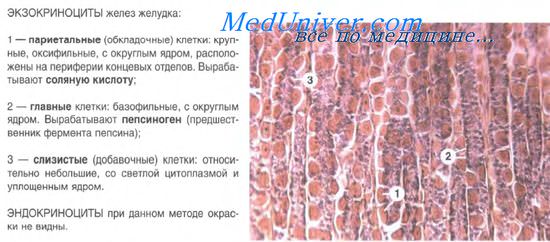
Мукоциты — слизистые клетки призматической формы со светлой цитоплазмой и уплотненным ядром, смещенным в базальную часть. При электронной микроскопии в апикальной части слизистых клеток выявляется большое количество секреторных гранул. Располагаются мукоциты в главной части желез, преимущественно в теле собственных желез. Функция клеток — выработка слизи.
Эндокриноциты желудка представлены несколькими клеточными дифферонами, для названия которых приняты буквенные сокращенные обозначения (ЕС, ECL, G, P, D, А и др.). Для всех этих клеток характерна более светлая цитоплазма, чем у других эпителиальных клеток. Отличительным признаком эндокринных клеток является наличие в цитоплазме секреторных гранул. Поскольку гранулы способны восстанавливать нитрат серебра, эти клетки называют аргирофильными. Они интенсивно окрашиваются также бихроматом калия, с чем связано другое название эндокриноцитов — энтерохромаффинные.
На основании строения секреторных гранул, а также с учетом их биохимических и функциональных свойств эндокриноциты классифицируются на несколько видов.
ЕС-клетки самые многочисленные, располагаются в теле и дне железы, между главными экзокриноцитами и секретируют серотонин и мелатонин. Серотонин стимулирует секреторную деятельность главных экзокриноцитов и мукоцитов. Мелатонин участвует в регуляции биологических ритмов функциональной активности секреторных клеток в зависимости от световых циклов.
ECL-клетки вырабатывают гистамин, который действует на париетальные экзокриноциты, регулируя продукцию соляной кислоты.
G-клетки называют гастринпродуцирующими. В большом количестве они встречаются в пилорических железах желудка. Гастрин стимулирует деятельность главных и париетальных экзокриноцитов, что сопровождается усиленной выработкой пепсиногена и соляной кислоты. У людей с повышенной кислотностью желудочного сока отмечается увеличение количества G-клеток и их гиперфункция. Имеются данные о том, что G-клетки вырабатывают энкефалин — морфиноподобное вещество, впервые обнаруженное в мозгу и участвующее в регуляции чувства боли.
Р-клетки секретируют бомбезин, который усиливает сокращения гладкой мышечной ткани желчного пузыря, стимулирует выделение соляной кислоты париетальными экзокриноцитами.
D-клетки вырабатывают соматостатин — ингибитор гормона роста. Он угнетает синтез белков.
ВИП-клетки продуцируют вазоинтестинальный пептид, расширяющий кровеносные сосуды и снижающий артериальное давление. Этот пептид стимулирует также выделение гормонов клетками островков поджелудочной железы.
А-клетки синтезируют энтероглюкагон, расщепляющий гликоген до глюкозы подобно глюкагону А-клеток островков поджелудочной железы.
В большинстве эндокриноцитов секреторные гранулы находятся в базальной части. Содержимое гранул выделяется в собственную пластинку слизистой оболочки и далее попадает в кровеносные капилляры.
Мышечная пластинка слизистой оболочки образована тремя слоями гладких миоцитов.
Подслизистая основа стенки желудка представлена рыхлой волокнистой соединительной тканью с сосудистыми и нервными сплетениями.
Мышечная оболочка желудка состоит из трех слоев гладкой мышечной ткани: наружного продольного, среднего циркулярного и внутреннего с косым направлением мышечных пучков. Средний слой в области привратника утолщен и образует пилорический сфинктер. Серозная оболочка желудка образована поверхностно лежащим мезотелием, а ее основу составляет рыхлая волокнистая соединительная ткань.
В стенке желудка расположены подслизистое, межмышечное и подсерозное нервные сплетения. В ганглиях межмышечного сплетения преобладают вегетативные нейроны 1-го типа, в пилорической области желудка больше нейронов П-го типа. К сплетениям идут проводники от блуждающего нерва и из пограничного симпатического ствола. Возбуждение блуждающего нерва стимулирует секрецию желудочного сока, тогда как возбуждение симпатических нервов, наоборот, угнетает желудочную секрецию.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Цитологическое исследование желудка. Гастрограммы.
При цитологическом изучении материала, полученного из желудка с помощью гастробиопсии, в препаратах отчетливо определяют клеточные элементы слизистой оболочки желудка: покровно-ямочный эпителий, главные и обкладочные клетки желез.
Соотношение в цитологических препаратах клеточных элементов слизистой оболочки желудка, различная степень их дифференцировки, появление признаков дегенерации и атипии, а также появление лейкоцитов, ретикулярных и гистиоидных элементов позволяют выявить типы гастроцитограмм. которые наиболее свойственны тому или другому заболеванию желудка.
Гастроцитограммы больных хроническим гастритом характеризуются наличием клеток покровно-ямочного эпителия, которые располагаются преимущественно небольшими пластами и скоплениями. Клетки имеют высоко- и низкоцилиндрическую форму, базально или центрально расположенное ядро. широкую,слабобазофильную цитоплазму. Ядра клеток отличаются некоторым полиморфизмом, имеются все переходы от незрелых относительно крупных, светлых с нежносетчатым рисунком хроматина до зрелых небольших размеров, интенсивно окрашенных ядер.
Главные и обкладочные клетки желез обнаруживают в различном количестве, расположены разрозненно, небольшими округлыми группами или ровными рядами, в которых отмечается правильное чередование главных и обкладочных клеток. В главных клетках отчетливо просматриваются окрашенные в сине-фиолетовый цвет грубые гранулы, заполняющие всю цитоплазму. Обкладочные клетки отличаются широкой светлой цитоплазмой, окрашенной в нежно-розовый цвет. В препаратах встречаются лимфоидные элементы и полиморфно-ядерные нейтрофильные лейкоциты.
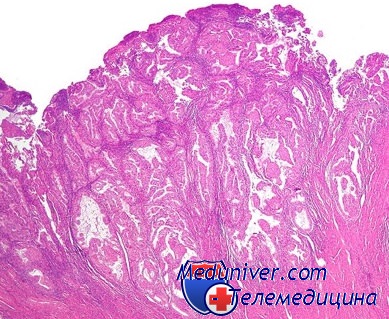
В цитограммах при полипах желудка большое количество пластов и больших скоплений покровно-ямочного эпителия, встречаются железисто-подобные структуры. По сравнению с цитограммами при гастрите можно отметить преобладание молодых, незрелых клеток с укрупненными ядрами и нежным рисунком хроматина в них.
При язвенной болезни желудка в гастроцитограммах преобладают сег менто-ядерные нейтрофилы, кроме того, обнаруживаются в значительном количестве лимфоциты, плазматические клетки, эозинофилы, клетки гистиоидного тина, скопления полиморфных эпителиальных клеток. В эпителии обычно отмечают признаки дегенерации в виде вакуолизации цитоплазмы и ядер, кариолизиса, кариорексиса и плазмолиза.
Однако необходимо отметить, что при цитологическом исследовании материала при неопухолевых и опухолеподобных поражениях желудка далеко не всегда возможно диагностировать эти заболевания. Последнее зависит от того, что изменения в клетках носят однотипный характер и часто можно обсуждать только степень клеточной пролиферации, атнпии и перестройки эпителия по кишечному типу.
Из злокачественных новообразований в желудке наиболее часто встречается аденокарцинома трех видов адеиокарцинома с высокой и низкой степенью дифференцировки, а также аденокарцинома с выраженным слизеобразованием. Реже встречаются перстневидноклеточный и недифференцированный рак, а также другие неэпителиальные опухоли.
Цитограммы больных раком желудка характеризуются наличием клеток с морфологическими признаками злокачественности. Клетки располагаются комплексами, в виде железисто-подобных или папиллярных структур, разрозненно. В комплексах и структурах отмечается беспорядочное нагромождение ядер. Клетки крупных размеров. Ядра занимают почтя всю клетку, преимущественно неправильной формы, гиперхромиые с грубым, неравномерно распределительным хроматином, гипертрофированными множественными нуклеоламн.
Гистологическую форму опухоли не всегда удается установить, чаше это возможно в случаях аденокарциномы, где, как правило, обнаруживаются железисто-подобные структуры. Коллоидный рак характеризуется наличием большого количества слизистых масс и перстневидных опухолевых клеток При малоднфференцированном раке резко анаплазированные клетки, с большим числом фигур деления, обычно располагающиеся разрозненно.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Рис. 1. Схематическое изображение эпителия в месте сочленения пищевода (Oesophagus) и желудка (Stomach), в котором встречаются эпителиальные клетки разных типов. Переходный эпителий (Transitional epithelium) образован базальными (Basal layer) и люминальными (Luminal layer) клетками, которые характеризуются различным уровнем экспрессии трех белков-маркеров (p63, KRT5 и KRT7). Рефлюкс, вызванный желчными кислотами, или нарушение экспрессии каких-то генов могут вызвать превращение эпителия пограничной области в аномальный — подобный эпителию кишечника — с включениями бокаловидных клеток (Goblet cell), и формируется разрастающаяся структура, называемая пищеводом Барретта (Barrett's oesophagus). Рисунок из популярного синопсиса к обсуждаемой статье
Ученым удалось разобраться в механизме возникновения предракового состояния в месте соединения пищевода и желудка — синдрома Барретта. Они смогли детально охарактеризовать эпителий в этой пограничной области и на лабораторных мышах показали, что базальные клетки с определенным набором маркеров могут стать предшественниками ткани, подобной ткани кишечника, которая замещает нормальный эпителий этой области. Клетки со сходными свойствами найдены на границе пищевода и желудка и у человека, поэтому данное исследование должно помочь улучшить методы ранней диагностики и лечения онкологических заболеваний.
Хорошо известно, что чем раньше диагностировать и начать лечить рак, тем легче может быть само лечение и тем выше шансы на выздоровление. Для некоторых типов рака выявлены так называемые предраковые состояния — изменения тканей, которые сами по себе не являются злокачественными, но повышают вероятность развития рака в этих тканях. Такие состояния известны пока для относительно небольшого числа раков. Поэтому, с одной стороны, нужно пытаться расширять список соответствий между злокачественными опухолями и предраковыми состояниями, а с другой стороны — выяснять механизмы возникновения этих состояний, чтобы повышать эффективность профилактики рака.
Один из типов предраковых состояний — метаплазии, при которых происходит замещение клеток одного типа клетками другого (как правило, обратимое). Метаплазии часто возникают на границах между разными типами эпителия и могут в таких случаях порождать карциномы — злокачественные опухоли эпителиальных клеток. Эпителий — это ткань, выстилающая поверхность тела (то есть, грубо говоря, кожа), внутренние полости и слизистые оболочки органов. В российской медицине различают два основных вида эпителия — многослойный плоский эпителий (кожа, слизистые оболочки, пищевод) и однослойный цилиндрический эпителий (желудок, кишечник). Особо выделяют эпителий, выстилающий органы, подвергающиеся сильному растяжению (например, в мочевыводящей системе), так называемый переходный. В западной медицине принята более детальная классификация эпителия (см. Epithelium).
Самая распространенная и активно исследуемая форма метаплазии — пищевод Барретта (синдром Барретта). Это — опасное осложнение рефлюксной болезни — заброса содержимого желудка в пищевод, при котором свойственный в норме пищеводу многослойный плоский эпителий в пограничной области соединения пищевода с желудком замещается цилиндрическим (свойственным желудку) с вкраплениями свойственных кишечнику бокаловидных клеток — «одноклеточных желез», выделяющих увлажняющую слизь (см. рис. 1). Частота встречаемости синдрома при рефлюксе составляет 10%, а в целом по популяции — 1%. За последние 40 лет частота встречаемости пищевода Барретта возросла почти в 8 раз. Он считается предраковым состоянием, так как высоколетальная аденокарцинома нижней части пищевода возникает при нем в 10 раз чаще, чем в нормальном пищеводе.
Хотя с момента описания синдрома Барретта в 1950 году он активно изучался, ключевые процессы его развития оставались неизвестными: как возникает замещение плоского эпителия на цилиндрический (метаплазия)? от каких клеток происходит вновь формирующийся цилиндрический эпителий пищевода? как идет последующая трансформация в злокачественные новообразования?
Для объяснения метаплазии было предложено пять основных теорий (они схематично показаны на рис. 2):
1) возможна прямая конверсия плоского эпителия в цилиндрический — повреждение может вызвать превращение одного типа ткани в другой (рис. 2, a);
2) предшественниками цилиндрического эпителия являются циркулирующие в кровотоке стволовые клетки, способные дифференцироваться в цилиндрический эпителий (рис. 2, b);
3) предшественниками цилиндрического эпителия являются клетки субмукозных (слизистых) желез, локализованных под плоским эпителием (рис. 2, c);
4) возможна экспансия в пограничную область клеток цилиндрического эпителия желудка (рис. 2, d);
5) предшественниками цилиндрического эпителия являются остаточные эмбриональные клетки, локализованные вблизи пограничной области (рис. 2, e).

Рис. 2. Гипотезы возникновения пищевода Барретта, предложенные ранее. a — передифференцировка плоского эпителия пищевода; b — дифференцировка циркулирующих в крови стволовых клеток костного мозга; c — экспансия клеток слизистых желез пищевода и их превращение в эпителий Барретта; d — превращение стволовых клеток слизистых желез; e — экспансия и дифференцировка спящих остаточных эмбриональных клеток пограничной области пищевода/желудка. Рисунок из обсуждаемой статьи в Nature
Но ни одна из этих теорий не получила строгого экспериментального подтверждения. И ни одна не объясняла появления вкраплений бокаловидных клеток, свойственных кишечнику (а не пищеводу или желудку).
Большой коллектив ученых из Медицинского центра Колумбийского университета и других научных учреждений США и Китая провел сравнительный анализ экспрессии генов, характерных для эпителия. Они показали, что у мышей пограничный эпителий, состоящий из базальных и люминальных (обращенных в просвет пищевода) клеток, характеризуется различной экспрессией в этих клетках трех маркеров. В базальных клетках экспрессируются два цитокератина — Krt5 и Krt7, а также фактор регуляции транскрипции р63. В клетках люминального слоя экспрессируется только Krt7. Это отличает пограничную область от выше расположенной области пищевода, в которой ни в базальных клетках, ни в плоском эпителии нет экспрессии Krt7 (рис. 1). В эпителии желудка ни один из этих маркеров не экспрессируется.

Рис. 3. Схема анастомоза между двенадцатиперстной кишкой и пищеводом мыши, в результате которого желчные кислоты (красные стрелки) поступают в пищевод. Рисунок из обсуждаемой статьи в Nature
В следующей серии экспериментов авторы провели тонкую хирургическую операцию на мышах и сделали анастомоз между пищеводом и двенадцатиперстной кишкой (рис. 3). В результате желчные кислоты поступали в пищевод, что позволило имитировать рефлюкс.
Через 18 недель после операции воздействие желчных кислот на пограничную область приводило к формированию клеток «пищевода Барретта», в которых экспрессировался характерный маркер CDX2, и в этой области появлялись бокаловидные клетки. Примечательно, что в расположенной выше части пищевода таких клеток не наблюдалось, несмотря на то что она также подвергалась воздействию желчных кислот.
Ученые решили исключить возможность замещения эпителия в пограничной области пищевода мигрирующими клетками соседних тканей. Для этого с помощью генно-инженерных методов они получили мышей, у которых экспрессия гена Krt7 в клетках эпителия пограничной области была сопряжена с экспрессией красного флюоресцирующего белка Tomato. Эксперименты показали, что в клетках цилиндрического эпителия «пищевода Барретта» экспрессируется Tomato, то есть Krt7. А как уже говорилось, ген Krt7 экспрессируется в эпителии пограничной области, но не экспрессируется в расположенной выше области пищевода и в желудке. Следовательно, клетки цилиндрического эпителия «пищевода Барретта» происходят исключительно от базальных клеток пограничной области (рис. 4).

Рис. 4. Предшественники базальных клеток (экспрессирующие гены p63 и KRT7) и люминальные клетки (KRT7 + ) эпителия пограничной области пищевод/желудок у мышей. Squamous epithelium — плоский эпителий пищевода. Transitional epithelium — эпителий пограничной области пищевода. Cardia — желудок. Рисунок из обсуждаемой статьи в Nature
В заключение авторы решили проверить, насколько похожа структура пограничной области между пищеводом желудком у человека и у мыши. Они провели анализ экспрессии эпителиальных маркеров человек и показали их сходство с мышиными. В этой области у человека были найдены базальные клетки с экспрессией генов p63, KRT5 и KRT7, а также люминальные клетки, в которых экспрессировался KRT7, но не было экспрессии гена p63. В базальных клетках, принадлежащих расположенной выше области пищевода, KRT7 не экспрессировался (рис. 5).


Рис. 5. В пограничной области пищевода и желудка человека локализован специфический переходный эпителий, который разрастается при пищеводе Барретта. a — микроскопическое изображение предшественников базальных клеток (отмечены стрелками) и люминальных клеток эпителия, окраска гематоксилином и эозином. Длина масштабного отрезка — 50 мкм. b — базальные клетки эпителия пограничной области экспрессируют гены p63, KRT5 и KRT7 (продукты экспрессии отмечены треугольниками). Базальные клетки плоского эпителия пищевода не экспрессируют KRT7 (отмечены стрелками). Иммуногистологическое окрашивание разными флюоресцирующими красителями. Длина масштабного отрезка — 50 мкм. c — схема строения эпителия пограничной области пищевод/желудок человека, обозначения как на рис. 4. Рисунок из обсуждаемой статьи в Nature
С помощью проточной цитометрии были разделены два типа базальных клеток пищевода человека (с маркерами p63 + KRT7 − и p63 + KRT7 + ). Из этих клеток in vitro были получены трехмерные культуры органоидов и оказалось, что органоиды, полученные из клеток типа p63 + KRT7 + и происходящие из пограничной области пищевода, способны формировать эпителиальные клетки, подобные эпителию кишечника. Органоиды, полученные из клеток типа p63 + KRT7 − , взятых из выше расположенной области, таким свойством не обладали.
Таким образом, ученым удалось на модели лабораторных мышей охарактеризовать эпителий пограничной области между пищеводом и желудком, который дает начало предраковому состоянию — пищеводу Барретта, а также проверить, что у людей все устроено аналогично. Оказалось, что этот эпителий более чувствителен к повреждающим факторам, чем эпителий расположенных выше областей пищевода или эпителий желудка. Полученные результаты лучше всего согласуются с выдвинутой ранее гипотезой происхождения пищевода Барретта о прямом превращении тканей эпителия пограничной области: показано, что базальные клетки пограничного эпителия могут быть предшественниками эпителия, подобного кишечному, который включает и бокаловидные клетки.
В то же время выявленные в ходе исследования генетические маркеры клеток эпителия пограничной зоны как таковые вряд ли могут быть причиной формирования пищевода Барретта и дальнейшего развития рака. В этом, скорее всего, задействованы какие-то иные факторы — кислотный рефлюкс, другие химические раздражители, гормональные нарушения или вирусные инфекции.
Несмотря на оставшиеся вопросы, обсуждаемая работа дает детальную картину формирования пищевода Барретта. Поскольку предраковые состояния и злокачественные опухоли особенно часто возникают именно в пограничных областях эпителия разных органов (матка, пищевод, прямая кишка), то можно надеяться, что там работают аналогичные механизмы. Впрочем, дальнейшие исследования должны будут прояснить этот вопрос, равно как и то, является ли пограничный эпителий единственным местом возникновения этой метаплазии и дальнейшей трансформации ее в рак. Ведь уже давно было показано, что структура, подобная пищеводу Барретта, может возникнуть и у больных, у которых пограничная область пищевода была удалена (S. R. Hamilton, J. H. Yardley, 1977. Regnerative of cardiac type mucosa and acquisition of Barrett mucosa after esophagogastrostomy). Так что полученные результаты могут способствовать разработке методов диагностики, профилактики и лечения этих состояний не только применительно к пищеводу, но и к другим органам.
Источники:
1) Ming Jiang, Haiyan Li, Yongchun Zhang, Ying Yang, Rong Lu, Kuancan Liu, Sijie Lin, Xiaopeng Lan, Haikun Wang, Han Wu, Jian Zhu, Zhongren Zhou, Jianming Xu, Dong-Kee Lee, Lanjing Zhang, Yuan-Cho Lee, Jingsong Yuan, Julian A. Abrams, Timothy C. Wang, Antonia R. Sepulveda, Qi Wu, Huaiyong Chen, Xin Sun, Junjun She, Xiaoxin Chen & Jianwen Que. Transitional basal cells at the squamous-columnar junction generate Barrett's oesophagus // Nature. 2017. V. 550. P. 529–533.
2) Lizhe Zhuang & Rebecca C. Fitzgerald. Cancer development: Origins in the oesophagus // Nature. 2017. V. 550. P. 463–464. Синопсис к обсуждаемой статье.
На сервисе СпросиВрача доступна консультация гастроэнтеролога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте!
Это значит, что в желудке много микробов хеликобактера, котопыеиполлерживают постоянное воспаление.
Его необходимо пролечить.

Здравствуйте.
Если обнаружен хеликобактер ,то нужно пройти лечение:
Амоксициллин 1000 мг 2 раза в день 10 дней, Азитромицин 500 мг в стуки 10 дней и Омепразол 20 мг 2 раза в день за 30 минут до еды

Здравствуйте пролиферация это деление клеток, вам нужно пролечить бактерию и сделать фгс с цитологие вновь, тревожные слова это дисплазия.


Здравствуйте это значит у вас гастрит вызванный хеликобактер пилори и его очень много и требуется лечение эрродикационная терапия: соблюдение диеты,омепразол 20мг по 1к*2раз 7дней,амоксициллин 500мг по 1т2раз7дней,клабел 500мг по 1т2раз 7дней,алмагельпо 1м.л2раз в день. Затем контроль через 7 дней после лечения и если ещё останутся то повторить курс но уже заменив клабел на метронидозол

Здравствуйте! Биопсия говорит о том, что атрофического гастрит нет, а есть хеликобактер-ассоциированный гастрит. Можно провести эрадикацию:пантораздол 20 мг 2 раза в день, де нол 2таб 2 раза в день и метронидазол по 21*3раза 10 дней. После принимать ребагит по 1*3раза 2 месяца.фгдс в плановом порядке через год желательно также с биопсией.


По лечению хеликобакторной инфекции мои коллеги Вам лечение написали.Я же немного хотела остановиться на лечении после курса с антибиотиками для снижения степени активности атрофии
ребамипид 100 мг 3 раза в день через 1 час после еды-2 мес

Здравствуйте, это-хеликобактер-ассоциированный гастрит с атрофией, в ст. обострения. Надо провести лечение: Де-нол 2т+ Омепразол или Рабепразол 20 мг + Амоксициллин 100мг + кларитромицин 500мг по такой дозе каждого декарства через каждые 12 часов в течение 12 дней, причем Де-нол принимать за 30 минут до еды, остальное- через 1, 5-2 часа после еды. с едой принимать ребагит 100мг 3 раза в день .Ближе к кончу курса свяжитесь снова, нужно будет продолжение лечения потом.

Здравствуйте! По тому, как вы написали, у вас обильное обсеменением слизистой желудка хеликобактером.Необходим осмотр гастроэнтеролога для назначения терапии, состоящей из двух антибиотиков и препарата, ингибирующего секрецию желудочных желез

Здравствйте! Что Вас беспокоит? По поводу чего начали обследование? Какие-то лекарственные препараты принимаете сейчас на постоянной основе?
Читайте также:

