Папилломатоз бдс что это
Обновлено: 26.04.2024
Оценка эффективности хирургического лечения пациентов с доброкачественными новообразованиями большого сосочка двенадцатиперстной кишки.
МАТЕРИАЛ И МЕТОДЫ
С января 2015 г. по январь 2020 г. в НИИ скорой помощи им. Н.В. Склифосовского пролечено 16 пациентов (7 (43,7%) мужчин и 9 (56,3%) женщин) с доброкачественными новообразованиями большого сосочка двенадцатиперстной кишки. Размер новообразований варьировал от 1 до 4 см (в среднем 2,5 см).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Удаление опухоли выполнено 4 (25%) больным из лапаротомного доступа, 6 (37,5%) пациентам выполнили эндоскопическую папиллэктомию в подлизистом слое. Остальные 6 (37,5%) пациентов на фоне улучшения общего состояния отказались от хирургического лечения. Одному (10%) больному из прооперированных пациентов в послеоперационном периоде выполнена релапаротомия, показанием к которой явилась острая перфоративная язва двенадцатиперстной кишки. Осложнений после выполнения эндоскопической папиллэктомии не выявлено. У всех пациентов при контрольном эндоскопическом исследовании через 3 и 6 мес данных, свидетельствующих о рецидиве опухолевого роста, не обнаружено. Малая травматичность эндоскопической папиллэктомии позволяет нам считать данный метод приоритетным при удалении аденомы большого сосочка двенадцатиперстной кишки. Мы предполагаем, что стентирование желчных протоков и главного панкреатического протока позволило избежать развитие острого панкреатита и механической желтухи.
ЗАКЛЮЧЕНИЕ
Эндоскопическая папиллэктомия — эффективный мини-инвазивный метод лечения новообразований большого сосочка двенадцатиперстной кишки. Несмотря на немалое число осложнений, большинство их устранимы консервативным лечением или эндоскопическими методами. Это позволяет рассматривать эндоскопическую папиллэктомию как метод выбора в лечении пациентов с доброкачественными новообразованиями большого сосочка двенадцатиперстной кишки.
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департаметнта здравоохранения Москвы»
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департамента здравоохранения Москвы»;
ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования»
- SPIN РИНЦ: 4044-9661
- Scopus AuthorID: 55970485700
- ResearcherID: P-9151-2017
- ORCID: 0000-0003-1270-5414
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департаметнта здравоохранения Москвы»
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департаметнта здравоохранения Москвы»
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департаметнта здравоохранения Москвы»
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департаметнта здравоохранения Москвы»
ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского Департаметнта здравоохранения Москвы»
Дата принятия в печать:
Введение
Аденома большого сосочка двенадцатиперстной кишки (БСДПК) составляет 1% всех новообразований желудочно-кишечного тракта [1]. По данным литературы, в мировой популяции на 100 000 человек приходится 0,5 случая аденомы БСДПК [2].
В 66—93% случаев аденома БСДПК не имеет клинической картины, что значительно затрудняет ее диагностику на ранних стадиях заболевания [3—5]. При увеличении размеров наиболее часто проявляется механической желтухой (7,1—26%), болевым синдромом (6,9—21,9%), острым панкреатитом (1,9—6,3%) и холангитом (0,3—1,6%), осложняется малигнизацией (15—30%) [1, 3].
В настоящее время для постановки окончательного диагноза необходимо гистологическое исследование биоптата, полученного при дуоденоскопии со взятием щипковой биопсии из опухоли [6].
Однако, по данным ряда авторов, и она не может считаться достоверным методом диагностики, поскольку в 16—30% наблюдений встречаются ложноотрицательные, а в 12—38% — ложноположительные результаты [7, 8]. В связи с этим эндоскопическая папиллэктомия (ЭП) может рассматриваться как вариант тотальной биопсии для постановки окончательного диагноза [9].
Сегодня единственным эффективным методом лечения аденомы БСДПК является хирургическое удаление [2, 10, 11].
Разработаны многообразные резекционные оперативные вмешательства из лапаротомного или лапароскопического доступов (панкреатодуоденальная резекция, дуоденотомия с последующей папиллэктомией). Однако послеоперационная летальность после этих операций достигает 10%, а частота рецидива опухоли — от 26 до 43% [3].
В последние годы активно внедряются мини-инвазивные методы удаления аденомы БСДПК с помощью гибкой эндоскопии, при их использовании послеоперационная летальность не достигает 1%, а частота рецидива не превышает 18% [3, 4, 10]. Однако среди авторов нет единого мнения в вопросах определения четких показаний к ЭП и выбора оптимальной методики данного оперативного вмешательства. Кроме того, актуальна задача профилактики послеоперационных осложнений.
Цель исследования — оценить эффективность ЭП при доброкачественных опухолях БСДПК.
Материал и методы
С января 2015 г. по январь 2020 г. в НИИ СП им. Н.В. Склифосовского пролечены 16 пациентов с доброкачественными новообразованиями БСДПК, в том числе 7 (43,7%) мужчин и 9 (56,3%) женщин.
Диагноз установлен на основании жалоб, инструментальных (дуоденоскопия, эндоскопическая ультрасонография (ЭУС), УЗИ органов брюшной полости), лабораторных (содержание общего, прямого билирубина, альфа-амилазы в биохимическом анализе крови) и гистологического методов исследования.
При проведении эндоскопического исследования определяли локализацию опухоли, ее размеры, наличие дефектов на ее поверхности, выполняли щипковую биопсию.
Применение ЭУС позволило уточнить размеры аденомы, определить степень инвазии опухоли в стенку ДПК, просвет общего желчного протока (ОЖП), окружающую клетчатку и сосуды, васкуляризацию опухоли в режиме цветного допплеровского картирования. При наличии патологического типа васкуляризации опухоли отмечали сформированный усиленный кровоток в новообразовании с наличием крупного «питающего» артериального сосуда.
При УЗИ органов брюшной полости определяли наличие или отсутствие конкрементов в желчных протоках и желчном пузыре, признаки билиарной или внутрипротоковой панкреатической гипертензии, уровень обструкции желчных путей и главного панкреатического протока (ГПП).
Для оценки интенсивности механической желтухи использовали классификацию по В.Д. Федорову и соавт. (2000), согласно которой легкой степени гипербилирубинемии соответствует концентрация общего билирубина до 100 мкмоль/л, средней — 101—200 мкмоль/л, тяжелой — более 201 мкмоль/л [12]. Содержание альфа-амилазы позволило определить степень тяжести острого панкреатита при наличии соответствующих жалоб.
С целью временной декомпрессии желчных протоков и ГПП выполняли чрескожную чреспеченочную микрохолецистостомию (ЧЧМХС) или транспапиллярные вмешательства (литоэкстрация, назобилиарное дренирование, билио- и панкреатодуоденальное стентирования).
После нормализации общего состояния и купирования симптомов механической желтухи всем пациентам предложено хирургическое удаление опухоли. Выбор в пользу открытой операции определялся инвазией опухоли в мышечный слой или дистальные отделы ОЖП, наличием патологического типа васкуляризации образования и тяжелой степени дисплазии эпителия. При лапаротомном доступе выполняли дуоденотомию с эксцизией аденомы БСДПК или пилоросохраняющую панкреатодуоденальную резекцию с формированием впередиободочного концепетлевого панкреатикогастроэнтероанастомоза и гепатикоэнтероанастомоза на одной петле тонкой кишки по Брауну. Показаниями к эндоскопическому удалению аденомы служило расположение опухоли в пределах слизистого и мышечного слоев без инвазии ее в дистальную треть ОЖП и отсутствие признаков патологического типа васкуляризации новообразования. Размеры опухоли не являлись определяющими при выборе хирургического доступа.
Для ЭП использовали стойку Exera III, дуоденоскоп TJF-Q180V фирмы «Olympus», рентгеновскую установку Ziehm Imaging, коагулятор ERBE VIO 300D, инъекционную иглу, полипэктомическую петлю, струну диаметром 0,035 дюймов и пластиковые билиарные и панкреатические стенты фирмы «Olympus».
Вмешательство осуществляли под эндотрахеальным наркозом в положении больного на спине. После позиционирования дуоденоскопа проводили контрольный осмотр для окончательной оценки размеров и подвижности новообразования с использованием режима узкоспектрального сканирования NBI (Narrow Band Imagine). При осмотре в режиме NBI определялись компактно расположенные маленькие округлые ямки либо большие, вытянутые ямки (тип III s, III L по Kudo — Fujii, 2010) [13].
Подслизистую инфильтрацию проводили 4% раствором гелофузина 10 мл с добавлением 0,1% раствора адреналина 1 мл, окрашенного индигокармином. Инъекции зоны резекции выполняли из нескольких точек для того, чтобы безопасно ее приподнять.
Эндоскопическое удаление опухоли выполняли методом петлевой резекции в смешанном режиме Endocut. Предпочтение отдавали методу удаления новообразования единым блоком. При отсутствии такой технической возможности опухоль удаляли несколькими фрагментами. Макропрепарат немедленно извлекали из просвета ДПК с целью профилактики его дистальной миграции и потери для последующего гистологического исследования. После чего осматривали края резекции с использованием режима NBI для выявления резидуальной ткани аденомы. При необходимости выполняли дополнительную резекцию в области измененной слизистой оболочки.
Далее при помощи катетера и струны выполняли селективную канюляцию ОЖП и ГПП с последующим их стентированием по стандартной методике. Для этого использовали пластиковые билиодуоденальные стенты диаметром 8,5 и 10 Fr длиной 5 и 9 см и панкреатические стенты диаметром 5 и 7 Fr длиной 4 и 6 см.
В послеоперационном периоде все пациенты получали анальгетическую (кетонал, анальгин), антацидную (алмагель, де-нол), спазмолитическую (платифиллин, дротаверин) и антисекреторную (омез, октреотид) терапию.
С целью оценки эффективности выполненных вмешательств и удаления билиарного и панкреатического стентов всем пациентам выполняли контрольное эндоскопическое исследование через 3 и 6 мес.
Результаты
У 11 (68,8%) из 16 больных отмечены симптомы механической желтухи (кожный зуд, желтушность кожных покровов и склер, потемнение мочи). При этом у 1 из них вышеописанные симптомы сочетались с клинической картиной гнойного холангита (гипертермия, озноб). У 5 (31,2%) пациентов наблюдали клинику острого панкреатита (опоясывающая боль в верхних отделах живота, гипертермия, тошнота, рвота).
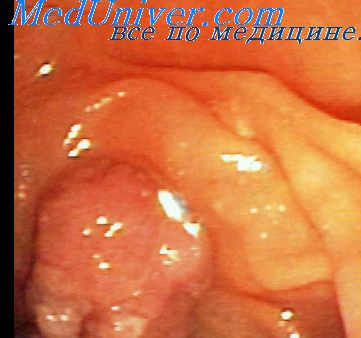
При эндоскопическом осмотре зоны БСДПК у 3 (18,8%) пациентов размер аденомы составил 2,5 см и более, у 13 (81,2%) — менее 2,5 см. Во всех случаях поверхность опухоли представлена аденоматозными разрастаниями с повышенной контактной кровоточивостью (рис. 1 и 2).

Рис. 1. Аденома большого сосочка двенадцатиперстной кишки (эндофотография).

Рис. 2. Эндофотография аденомы большого сосочка двенадцатиперстной кишки (режим NBI, виден мелкий округлый тип ямочного рисунка).
По результатам гистологического исследования у 7 (43,8%) пациентов выявлена аденома БСДПК слабой степени дисплазии эпителия, у 8 (50%) — умеренной, у 1 (6,2%) — тяжелой.
При ЭУС-сканировании у 4 (25%) пациентов опухолевые разрастания определены в пределах слизистой оболочки, у 6 (37,5%) — до мышечной оболочки ДПК, у 6 (37,5%) они распространялись на дистальную треть ОЖП (рис. 3 и 4).

Рис. 3. Эндоскопическая ультрасонограмма объемного образования большого сосочка двенадцатиперстной кишки (стрелкой указана инвазия опухоли в прилежащую клетчатку).

Рис. 4. Эндоскопическая ультрасонограмма объемного образования большого сосочка двенадцатиперстной кишки с прорастанием в дистальную треть общего желчного протока (стрелкой указаны внутрипротоковые разрастания опухолевой ткани).
ЭУС-признаки наличия патологического типа васкуляризации опухоли выявлены у 5 (31,2%) больных, у 11 (68,8%) они отсутствовали.
При УЗИ органов брюшной полости у 11 (68,8%) пациентов отмечены признаки билиарной гипертензии. Из них у 5 (45,4%) пациентов расширение желчных протоков сочеталось с наличием конкрементов в ОЖП, у 3 (27,2%) — с множественными конкрементами в желчном пузыре. Еще у 5 (31,2%) пациентов выявили признаки острого панкреатита и дилатации ГПП.
Гипербилирубинемия отмечена у 11 (68,8%) пациентов: у 6 (54,5%) — легкой степени, у 4 (36,5%) — средней, у 1 (9,0%) — тяжелой. В 5 (31,2%) наблюдениях уровень билирубина был в пределах нормы.
У 1 больного с клинико-инструментальной картиной острого панкреатита уровень альфа-амилазы достиг 567,0 Ед/л. В остальных наблюдениях этот показатель был в пределах нормы.
Папиллосфинктеротомия с последующей литоэкстракцией и билиодуоденальным стентированием выполнена у 5 (31,2%) пациентов, чрескожная чреспеченочнная микрохолецистостомия — у 7 (43,7%), билиодуоденальное стентирование — у 2 (12,5%), назобилиарное дренирование — у 1 (6,3%), панкреатодуоденальное стентирование — у 1 (6,3%). У всех больных лабораторные показатели снизились на 5—7-й день после дренирующих операций.
После первого этапа эндоскопического лечения 6 (37,5%) пациентов на фоне улучшения общего состояния отказались от хирургического лечения и в удовлетворительном состоянии были выписаны под наблюдение онкологом по месту жительства.
Из лапаротомного доступа удаление опухоли выполнено 4 больным: эксцизия аденомы — у 3 (75%), пилосохраняющая панкреатодуоденальная резекция — у 1 (25%).
Средняя длительность оперативных вмешательств открытым доступом составила 4,2 ч. Одному больному в послеоперационном периоде произведена релапаротомия, показанием к которой явилась острая перфоративная язва ДПК (осложнение IV степени по классификации Clavien — Dindo).
У 6 (50%) пациентов выполнили ЭП в подлизистом слое. В 3 (50%) наблюдениях новообразование удалено единым блоком (размер опухоли менее 2,5 см), у 3 (50%) — несколькими фрагментами (размер опухоли более 2,5 см).
Стентирование ОЖП и ГПП достигнуто во всех наблюдениях. При этом в 2 (33,3%) случаях наличие конкрементов в ОЖП потребовало предварительно выполнить литоэкстракцию корзиной Дормиа. Средняя длительность оперативных вмешательств составила 2,1 ч (рис. 5—7).

Рис. 5. Эндофотография этапа инфильтрации образования большого доуденального сосочка двенадцатиперстной кишки в подслизистом слое (стрелкой указана инъекционная игла).

Рис. 6. Эндофотография этапа удаления аденомы большого доуденального сосочка двенадцатиперстной кишки единым блоком (стрелкой указана полипэктомическая петля).

Рис. 7. Эндофотография окончательного вида операционного поля после удаления образования большого доуденального сосочка двенадцатиперстной кишки, билио- (1) и панкреатодуоденального (2) стентирования.
Послеоперационных осложнений не выявлено. На 5—7-е сутки пациенты в удовлетворительном состоянии выписаны из стационара.
У всех пациентов при контрольном эндоскопическом исследовании через 3 и 6 мес данных, свидетельствующих о рецидиве опухолевого роста не обнаружено. Пациентам после ЭП удалили ранее установленные стенты (рис. 8).

Рис. 8. Эндофотография результатов контрольного исследования через 3 мес после операции (стрелкой указан билиодуоденальный стент).
Наше исследование показало, что доброкачественные новообразования БСДПК могут проявляться такими неотложными состояниями, как механическая желтуха (91,6%) и даже острый панкреатит (8,4%), причина таких состояний была быстро и правильно установлена в скоропомощном стационаре.
Методика ЭУС позволяет определить размеры, степень инвазии опухоли, степень васкуляризации, что имеет решающее значение в выборе хирургического доступа и объема операции [2, 3]. По нашему мнению, инвазия аденомы в мышечный слой или дистальные отделы ОЖП, а также наличие патологического типа васкуляризации образования являются показанием к открытой операции, а ее расположение в пределах слизистого и мышечного слоев без прорастания в дистальную треть ОЖП и отсутствие усиленного кровотока в опухоли предполагает выполнение ЭП.
Мы солидарны с рядом зарубежных авторов, что малая травматичность ЭП позволяет считать данный метод приоритетным для удаления аденомы БСДПК [2, 4, 10, 11, 14]. Предполагаем, что стентирование желчных протоков и ГПП позволило избежать развития послеоперационных острого панкреатита и механической желтухи вследствие отека слизистой оболочки, а на этапе рубцевания и эпителизации пострезекционного дефекта слизистой оболочки стенты препятствуют формированию рубцового стеноза устья ОЖП и ГПП.
Полученные данные имеют ограниченную (С) степень статистической значимости и IV уровень доказательности публикации (по классификации степени достоверности публикаций Оксфордского центра доказательной медицины). Предложенная нами лечебная тактика показала 100% эффективность данного метода лечения, однако малое число наблюдений требует продолжения научного исследования для получения статистически значимого результата.
Аденомиоз дуоденального сосочка. Папиллярная аденома большого дуоденального сосочка.
Полипы заполняют просвет ампулы БСДК или просвет интрапаниллярного отдела главного протока поджелудочной железы. БСДК умеренно увеличен и уплотнен, сохраняет обычную форму и на его верхушке имеется одно отверстие. Морфологически эти полипы идентичны гиперпластическим полипам зоны устья БСДК, отличаясь от последних только своим расположением. Развитие таких полипов можно связать с хроническим продуктивным воспалением.
Самая частая разновидность гиперпластических изменений. Железы слизистой оболочки гипернлазированы, кисгозно расширены. Гроздевидные скопления таких желез могут образовывать полиповидные выпячивания, прикрывающие просвет устья БСДК. Некоторые исследователи считают это явление обычным у лиц старше 40 лет.
Единого мнения о природе аденомиоза не существует. Относят к группе гетеротопических процессов и считают, что он развивается вследствие перемещения гиперплазированных папиллярных желез в мышечный слой сосочка. Макроскопически сосочек приобретает шаровидную форму, увеличивается в диаметре до 1,0-1,5 см. Устье определяется с трудом. Консистенция сосочка плотная, что позволяет заподозрить злокачественную опухоль. На разрезе определяется волокнистая ткань серовато-желтого цвета.
В зависимости от особенностей строения различают три гистологические формы аденомиоза большого дуоденального сосочка: узловатую, узловато-диффузную и диффузную. Эти формы аденомиоза представляют собой морфологическое выражение последовательных фаз его развития. Узловатая форма аденомиоза соответствует ранней фазе развития, когда начинается внедрение гинерплазированных папиллярных желез в мышечный слой без заметного нарушения архитектоники последнего. Дальнейшее прогрессирование процесса приводит к развитию узловато-диффузной и далее диффузной формы,. морфологически характеризующейся полной перестройкой стенки БСДК.
Наблюдаемая при этом гипертрофия мышечных пучков является компенсаторной, возникающей в ответ на процессы перестройки стенки большого дуоденального сосочка.
У лиц, не страдающих желчнокаменной болезнью, аденомиоз выявляли не менее часто, чем у лиц с желчнокаменной болезнью и воспалительными изменениями желчных путей. Поэтому мы поддерживаем мнение Marzoli и Serio (1976) о том, что аденомиоз БСДК является процессом, не зависящим от патологии желчевыводящих путей. На основании большого сходства аденомиозных структур с гормонально обусловленными гиперилазиями молочной и предстательной желез можно считать обоснованным также предположение Lebert (1955) об эндокринной индукции аденомиоза БСДК.
В ряде случаев картины аденомиоза большого дуоденального сосочка могут представлять определенные трудности при дифференциальном диагнозе с опухолевым процессом, особенно, если исследованию подвергаются биоптаты небольших размеров. Однако, морфологические критерии свидетельствуют против опухолевого происхождения аденомиозных формаций, поскольку в них не наблюдается клеточной и ядерной атинии, отсутствуют митозы и признаки деструирующего роста.
Поэтому аденомиозные структуры следует отнести к числу опухолеподобных пролифератов гиперпластического происхождения.
Папиллярная аденома большого дуоденального сосочка.
Встречается редко. Внешний вид опухоли соответствует крупному полипу. Эпителиальный компонент аденомы предсгавлеп высоким призматическим эпителием со светлой эозинофильиой цитоплазмой и базально расположенным ядром, морфологические и функциональные свойства которого напоминают нормальный эпителий слизистой оболочки БСДК. Имеется некоторое сходство в гистологическом строении папиллярной аденомы и гиперпластических полипов БСДК. Существует даже мнение, что эти образования практически невозможно различить. Однако анализ морфофункциональных особенностей папиллярной аденомы и гиперпластических образований позволяет выделить признаки, являюпшеся основой для проведения дифференциального диагноза.
В гиперпластических полипах эпителиальные клетки сохраняют нормальное строение и ядра их располагаются строго однорядно вблизи базальной мембраны, митозы отсутствуют. Полипы имеют хорошо развитую строму из рыхлой соединительной ткани, богатую кровеносными сосудами и клеточными элементами, среди которых преобладают лимфоциты и плазматические клетки. В папиллярной аденоме эпителий приобретает черты атинии: клетки и ядра имеют большие, чем в норме, размеры; ядра становятся гиперхромными и сильно вытянутыми, они теряют строго полярное расположение, появляются митозы. Опухолевые клетки отличаются нарушением секреторной функции. В одних клетках аденомы выявляется резкая гиперсекреция слизи, в других секреция полностью отсутствует.
Строма в опухоли не столь развита, клеточный инфильтрат в ней более скудный и состоит преимущественно из лимфоцитов и фибробластов. Папиллярная аденома может малигнизироваться.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Папилломатоз — общее название для патологического процесса, характеризующегося образованием множественных папиллом на участке кожи или слизистых оболочек различных органов. Папиллома являет собой доброкачественное новообразование, развивающееся из плоского или переходного эпителия, возвышающееся над ним и имеющее форму сосочка.
Причины развития папилломатоза
В большинстве случаев папилломы имеют вирусную этиологию. Возбудитель заболевания — ДНК-содержащий вирус папилломы человека (ВПЧ) семейства паповавирусов. К настоящему времени определено около 100 типов этого вируса, многие из которых обладают различным по степени риска потенциалом к онкогенности.
Вирус может передаваться от человека к человеку контактным (в том числе половым) путём; установлено, что один из путей заражения вирусом — передача от матери плоду в течение беременности или во время родов, что обуславливает появление папилломатоза и у детей младшего возраста.
Чаще всего инфицирование ВПЧ приводит к бессимптомному носительству, но в ситуациях, когда иммунитет снижается (после длительной болезни, в стрессовых ситуациях, при авитаминозе, при беременности, в случае приёма определенных лекарств, например, глюкокортикостероидов), возникает непосредственное клиническое проявление в виде папиллом.
Помимо вирусной причины, папилломатоз может быть следствием хронических воспалительных процессов. Интересно отметить, что в отдельных ситуациях при выявлении папилломатоза не выявляется признаков вирусного инфицирования, что побуждает к поиску иных причин развития данного заболевания.
Отдельные виды папилломатоза
Папилломы могут поражать кожу и слизистую оболочку практически любого внутреннего органа. Ниже приведены описания отдельных видов папилломатоза в зависимости от того, какая часть тела поражена.
Папилломатоз гортани
Вызывается преимущественно ВПЧ 6 и 11 типов, менее распространены типы 16, 18. Частота встречаемости паппиломатоза гортани в популяции — 2 на 100 000 среди взрослых и 4 на 100 000 среди детей.
Характерными симптомами являются охриплость голоса и нарушения дыхания. Несмотря на то, что папилломатоз гортани является доброкачественным заболеванием, возможны такие серьезные осложнения, как стеноз гортани, распространение папиллом на трахею и бронхи с последующим развитием лёгочной недостаточности, а также перерождение в злокачественную опухоль, особенно если папилломатоз вызван вирусом ВПЧ 16 или 18 типа, у которых высокий уровень потенциальной онкогенности.
Кроме того, папилломатоз гортани может рецидивировать; выделяют «агрессивный» и «неагрессивный» типы рецидивирования. К агрессивному типу относится папилломатоз, по поводу которого проведено 10 и более операций, или более трех операций за год, или при распространении процесса на подголосовой отдел гортани.
Вестибулярный папилломатоз
Этот термин применяется для обозначения мелких паппиломовидных образований преддверия влагалища. Встречается довольно часто у женщин в возрасте до 30 лет и становится показанием к обследованию слизистых влагалища и шейки матки, в том числе и на предмет наличия вируса папилломы человека, так как может сочетаться с поражением шайки матки, хотя сам по себе вестибулярный папилломатоз может и не иметь вирусной природы.
Вестибулярный папилломатоз часто может развиваться без клинических симптомов и обнаруживается при осмотре у гинеколога с профилактической целью или по поводу иных жалоб, но может и проявляться белями, болями и жжением в области вульвы, явлениями диспареунии, сочетаться с локальным воспалительным процессом.
Вестибулярный папилломатоз, в отличие от поражений шейки матки, склонен к рецидивированию — по данным литературы, частота рецидивов составляет до 17%. Обычно рецидивы характерны при инфицировании папилломавирусном низкого онкогенного риска.
Папилломатоз кожи
Папилломатозом кожи называют разрастания многочисленных кожных новообразований на ограниченном участке. Папиллома образуется при разрастании верхнего слоя кожи — эпидермиса. Обычно кожные папилломы имеют размер 5–7 миллиметров, реже до 2 сантиметров. Форма варьирует от точечного или немного свисающего выроста кожи до горошины. Цвет папилломы чаще неотличим от цвета окружающего кожного покрова, но может быть и белого или коричневого цвета. Обыкновенные папилломы чаще всего локализуются на коже спины, ладоней и пальцев рук, подошв и стоп, нитевидные папилломы — в местах с тонкой кожей (веки, шея, подмышечные и паховые области).
Обычно имеет бессимптомное течение и являет собой преимущественно косметический дефект, однако папилломы кожи могут часто травмироваться, что может привести к развитию воспаления или быть фактором риска их озлокачествления.
Особого внимания заслуживает карциноидный папилломатоз кожи Готтрона — редкое предраковое заболевание, характеризующееся специфическими разрастаниями эпидермиса. Основным фактором его возникновения является предрасположенность к развитию множественного поражения кожи папилломами; среди прочих факторов риска следует упомянуть регулярную травматизацию кожных покровов, хронические заболевания кожи, нарушения кровообращения. При данном заболевании очаги расположены симметрично на голенях, чаще на передней поверхности, на фоне длительно существовавшего поражения кожи, имеют вид выступающих над поверхностью на 1–1,5 см папилломатозных бородавчатых разрастаний и вегетаций в виде бляшек значительного размера. Бороздки между очагами заполнены желтовато-белыми липкими массами с неприятным запахом, на некоторых участках они ссыхаются в желтовато-серые корки. Иногда возникают эрозии, поверхностные язвы, легко кровоточащие грануляции. В силу высокого риска озлокачествления (стоит отметить, что ряд авторов приравнивает карциноидный папилломатоз к высокодифференцированному плоскоклеточному раку кожи) данное заболевание требует консультации и лечения у онколога.
Папилломатоз пищевода
Является редкой патологией — согласно данным литературы, его частота составляет всего 4,5%. Папилломы имеют вид полиповидного или листовидного образования белесоватого цвета, размером обычно до 1 см. Характерна локализация поражений в дистальных отделах пищевода. Хотя основной причиной развития данной патологии считается наличие папилломовирусной инфекции, по данным ряда авторов, папилломатоз пищевода встречается и при отсутствии вирусной контаминации. Кроме того, отмечается связь между развитием папилломатоза и гастроэзофагеальным рефлюксом, который в силу длительного воздействия соляной кислоты, содержащейся в желудочном соке, приводит к повреждению и хроническому воспалению слизистой пищевода.
Папилломы пищевода могут долгое время не проявлять себя никакой симптоматикой, но по мере их роста могут появляться следующие жалобы: затрудненное глотание, легкая или умеренная боль за грудиной, отрыжка, тошнота.
В настоящее время считается, что папилломы пищевода являются предраковым заболеванием, и именно папилломатоз в силу распространённости поражения слизистой оболочки пищевода обладает наибольшим риском малигнизации, поэтому выявление папиллом пищевода — это показание к хирургическому лечению.
Внутрипротоковый папилломатоз
Под данным термином понимают папилломы, расположенные в млечных протоках молочной железы. Папилломы могут возникать как в периферических протоках любого квадранта молочной железы, так и в протоках, расположенных сразу за соском. Периферический папилломатоз представлен обычно мелкими, до 1 см, образованиями. В отдельных случаях внутрипротоковые папилломы могут иметь гигантский (более 5 см) размер, в этом случае они значительно деформируют молочную железу. По мере роста папилломы в просвете возникает механическое расширение протока, что может являться причиной развития болевого синдрома.
Внутрипротоковые папилломы могут развиваться в любом возрасте, но чаще возникают в возрасте 35–55 лет. Факторами риска их образования считаются приём оральных контрацептивов и препаратов заместительной гормональной терапии, семейный анамнез, эндокринологические нарушения, наличие хронических воспалительных процессов придатков. Наиболее частым симптомом является появление выделений из соска, не связанных с лактацией, янтарного цвета или с примесью крови. Кроме того, в связи с ростом папиллом может появиться болезненность, становится возможным пропальпировать уплотнения в молочной железе.
Внутрипротоковый папилломатоз требует хирургического лечения в объёме резекции поражённого квадранта или же, в случае значительной распространённости процесса, радикальной мастэктомии, так как обладает значительным потенциалом к перерождению в протоковый рак.
Диагностика папилломатоза
Установить диагноз «папилломатоз» возможно даже при первичном осмотре поражённой области из-за типичного вида новообразований. Папилломы представляют собой мягкую плотную опухоль на ножке (реже на широком основании) размером около одного-двух сантиметров с неровной внешней поверхностью, цвет варьируется от белого до коричневого. В некоторых случаях папиллома может разрастаться и приобретать вид, напоминающий цветную капусту.
Применяемые инструментальные методы диагностики зависят от локализации папилломатоза. Так, при папилломатозе гортани показано проведение ларингоскопии, при поражении пищевода — ЭГДС, при локализации папиллом в протоках молочной железы — дуктография.
Для подтверждения вирусной природы папиллом и определения конкретного типа вируса используются лабораторные методики, позволяющие идентифицировать ДНК вируса — полимеразная цепная реакция (ПЦР), гибридизационные методы.
Наконец, в рамках комплексного лечения целесообразно оценить иммунный статус пациента с целью назначения медикаментозной терапии для профилактики рецидивирования папилломатоза.
Лечение папилломатоза
Основной метод лечения – хирургический. При всей эффективности традиционного хирургического иссечения папиллом существует риск рубцевания слизистой оболочки, поэтому в настоящее время широкое распространение получили не менее эффективные, но более щадящие методы лечения папилломатоза:
- Лазерное удаление
- Ультразвуковая дезинтеграция
- Радиочастотная холодная аблация
- Фотодинамическая терапия
- Электродеструкция
- Криодеструкция
- Диатермокоагуляция
- Удаление химическими агентами (солкодерм, подофиллин)
К сожалению, ни одна из вышеуказанных методик даже при условии полного и тщательного удаления папилломатоза не гарантирует отсутствия рецидива.
Поэтому при наличии факторов риска развития рецидива в послеоперационном периоде может быть назначена адъювантная лекарственная терапия, в рамках которой могут быть назначены следующие препараты:
- Препараты α-интерферона,
- Противовирусные препараты (ацикловир, рибавирин, цидофовир)
- Иммуностимуляторы (ликопид, галавит, циклоферон)
Также в настоящее время проводятся клинические исследования вакцины против вирусов папилломы человека в качестве противорецидивного средства.
Несмотря на обнадеживающие результаты, на данный момент применение вакцины для профилактики рецидивов у больных с уже выявленным папилломатозом стандартом лечения не является.
Профилактика
До недавнего времени наиболее эффективной профилактикой папилломатоза считалось предотвращение заражения папилломавирусной инфекцией, а также лечение сопутствующих хронических инфекционных заболеваний и скрининг, направленный на раннее выявление болезни. Сейчас возможно выполнение профилактической вакцинации. Вакцина направлена против четырех типов папилломавируса, которые имеют наибольшее клиническое значение и наибольший онкогенный риск. Вакцинация возможна как у детей для профилактики заражения этими типами вируса, так и у взрослых. Перед вакцинацией обследование на наличие вирусов папилломы не требуется, так как даже если человек уже заражен один из тех типов, на которые направлена вакцина, иммунопрофилактика убережет его от заражения остальными тремя.
Если папилломатоз уже диагностирован и подвергнут лечению, пациенты подлежат динамическому контролю. Так, больные папилломатозом гортани подлежат обязательной диспансеризации в зависимости от частоты рецидивирования заболевания, но не менее чем раз в три месяца. В случае вестибулярного папилломатоза, даже если доказано отсутствие связи его возникновения с папилломавирусной инфекцией, также требуется активное динамическое наблюдение.
Существует мнение, что практически все живущие ныне люди заражены минимум одним из типов вируса папилломы человека. Большинство являются здоровыми носителями, но проявления инфекции в виде папилломатоза может развиться у любого человека, неся с собой проблемы — от безобидного косметического дефекта до грозного риска развития злокачественной опухоли. Своевременное обращение к врачам «Евроонко» гарантирует решение этих проблем и предотвращение их дальнейшего усугубления.
Рак большого дуоденального сосочка – злокачественная опухоль фатерова сосочка, расположенного в области двенадцатиперстной кишки. Характерен медленный рост и позднее метастазирование при раннем появлении механической желтухи. Наблюдаются боли, периодическое повышение температуры тела, увеличение печени и желчного пузыря. На поздних стадиях возможны кровотечения. Диагноз устанавливают с учетом симптоматики, данных рентгенографии, фиброгастродуоденоскопии и результатов биопсии. Лечение оперативное: гастропанкреатодуоденальная резекция, папиллэктомия, дуоденэктомия, паллиативные вмешательства.
Общие сведения
Рак большого дуоденального сосочка – злокачественная неоплазия большого дуоденального (фатерова) соска, локализующегося в нисходящей части двенадцатиперстной кишки и представляющего собой соустье главного панкреатического протока и общего желчного протока. Составляет 40% от общего количества онкологических поражений пилородуоденальной зоны, 5% от общего числа неоплазий ЖКТ и 1-2% от общего количества раков различных локализаций. Рак большого дуоденального сосочка является третьей по распространенности причиной возникновения механической желтухи. Обычно поражает пожилых пациентов, средний возраст больных составляет 54 года. Очень редко выявляется у детей. Женщины страдают реже мужчин. Лечение осуществляют специалисты в сфере онкологии, гастроэнтерологии и абдоминальной хирургии.

Причины рака фатерова сосочка
Причины возникновения опухоли точно не выяснены. Специалисты отмечают, что определенное значение имеет наследственная предрасположенность – заболевание нередко диагностируется в семьях, члены которой страдают семейным полипозом. Кроме того, у некоторых пациентов выявляется генетическая мутация K-ras. Установлено, что неоплазия может развиться в результате малигнизации аденомы фатерова соска. В список факторов риска также включают хронический панкреатит и заболевания гепатобилиарной системы.
Источником рака большого дуоденального сосочка являются трансформировавшиеся клетки эпителия слизистой двенадцатиперстной кишки, панкреатического протока либо общего желчного протока. Для новообразования характерен медленный экзофитный рост. По внешнему виду неоплазия напоминает папиллому, разрастание грибовидной формы или в виде соцветья цветной капусты. Реже выявляются эндофитные формы. При экзофитных формах рака большого дуоденального сосочка желтуха чаще ремиттирующая, при эндофитных – постоянная. Диаметр узла при его хирургическом удалении в среднем составляет 3 мм.
При микроскопическом исследовании выявляются клеточные скопления и отдельно лежащие эндокринные клетки веретенообразной, треугольной и цилиндрической формы. Число эндокринных клеток уменьшается по мере снижения уровня дифференцировки неоплазии. Обычно рак большого дуоденального сосочка прорастает общий желчный проток, возможно также поражение поджелудочной железы и стенки двенадцатиперстной кишки, лимфогенное и отдаленное метастазирование. Лимфогенные метастазы обнаруживаются у 21-51% больных. Отдаленные вторичные очаги выявляются достаточно редко. Обычно поражается печень, реже – кости, головной мозг, легкие и надпочечники.
Рак большого дуоденального сосочка может полностью обтурировать просвет желчного протока, реже выявляется стеноз. Даже при частичном сдавлении из-за отечности слизистой возникают грубые расстройства оттока желчи, становящиеся причиной развития механической желтухи. Появляется билиарная гипертензия, сопровождающаяся дилатацией желчевыводящих путей и протоков поджелудочной железы. Кишечная непроходимость развивается очень редко. При распространении процесса возможно прорастание стенки кишечника и распад неоплазии с развитием внутреннего кровотечения.
Симптомы рака фатерова сосочка
Первым проявлением болезни часто становится механическая желтуха, возникшая на фоне соматического благополучия. Вначале желтуха обычно перемежающаяся, нормализация биохимических показателей крови обусловлена уменьшением отека в области стенозированного желчного протока. При прогрессировании рака большого дуоденального сосочка желтуха становится более стойкой, изменение цвета кожи выявляется после интенсивных болей, сопровождающихся ознобами и проливными потами. Пациенты жалуются на выраженный зуд. Интермиттирующий характер желтухи на поздних стадиях (выявляется в 51% случаев) обусловлен распадом рака большого дуоденального сосочка, сопровождающегося временным восстановлением проходимости желчного протока.
При пальпации определяется гепатомегалия. У 60% пациентов под нижним краем печени прощупывается увеличенный желчный пузырь (симптом Курвуазье). При продолжительной обтурации желчевыводящих путей возникают цирроз печени и хронический панкреатит. При инвазии рака большого дуоденального сосочка в стенку кишечника и последующем распаде опухоли возможны кровотечения (острые массивные либо повторяющиеся незначительные) с развитием анемии. При региональном метастазировании отмечается изменение болевого синдрома.
Характерной особенностью рака большого дуоденального сосочка является ранняя потеря веса. Причиной похудания становятся стеноз либо обструкция панкреатических протоков, из-за которых в ЖКТ перестают поступать ферменты, необходимые для расщепления белков и жиров. Нарушение проходимости общего желчного протока еще больше усугубляет расстройства всасывания жиров и ухудшает всасываемость витаминов. Снижение веса и авитаминоз становятся причиной адинамии.
У больных раком большого дуоденального сосочка часто наблюдаются поносы, сопровождающиеся вздутием и болями в животе. Каловые массы зловонные, глинисто-серые. В запущенных случаях может выявляться жировой кал. При появлении регионарных метастазов отмечается изменение характера болевого синдрома. На поздних стадиях определяются истощение и расстройства функций органов, пораженных отдаленными метастазами.
Диагностика рака фатерова сосочка
Постановка диагноза сопряжена с существенными затруднениями из-за неспецифичности симптоматики. В процессе диагностики онколог ориентируется на жалобы, данные объективного осмотра, рентгенографии, чреспеченочной или внутривенной холангиографии, дуоденального зондирования, фиброгастродуоденоскопии и других исследований. При желтухе определяется высокий уровень билирубина с преобладанием прямой фракции, стеркобилин в кале отсутствует. На поздних стадиях рака большого дуоденального сосочка выявляется анемия.
Достаточно достоверным исследованием является дуоденальное зондирование, при проведении которого часто удается обнаружить кровь в дуоденальном содержимом. Иногда в ходе этого исследования выявляются клетки неоплазии и ферменты поджелудочной железы. Рентгенографическими признаками рака большого дуоденального сосочка являются неровность контуров либо дефект наполнения в зоне внутренней стенки двенадцатиперстной кишки, а также отсутствие проходимости либо деформация желчного протока в зоне, приближенной к фатеровому соску.
При проведении фиброгастродуоденоскопии обнаруживают опухолевидное образование и выполняют эндоскопическую биопсию подозрительного участка. В некоторых случаях диагноз рака большого дуоденального сосочка не удается установить при помощи стандартных методик, для уточнения характера патологии приходится проводить лапаротомию, рассекать фатеров сосок, осуществлять забор ткани, а затем принимать решение об объеме операции на основании данных срочного гистологического исследования. Дифференциальный диагноз осуществляют с гепатитом, раком головки поджелудочной железы и раком желчных путей.
Лечение рака фатерова сосочка
Основным способом лечения данной патологии является оперативное вмешательство, которое, в зависимости от распространенности процесса, может быть радикальным либо паллиативным. Группа паллиативных операций включает в себя около десяти различных вариантов анастомозов, позволяющих восстановить отток желчи в пищеварительный тракт либо (реже) предотвратить сдавление двенадцатиперстной кишки растущим раком большого дуоденального сосочка.
Радикальная операция является тяжелым и сложным вмешательством, поэтому проводится только после тщательного отбора пациентов в соответствии со стандартами, включающими в себя допустимую степень истощения, уровень белков в крови, определенные показатели пульса и жизненной емкости легких и т. д. Больным раком большого дуоденального сосочка проводят гастропанкреатодуоденальную резекцию. При наличии противопоказаний к радикальному вмешательству выполняют условно радикальные операции: папиллэктомию, дуоденэктомию либо экономную панкреатодуоденальную резекцию. Радиотерапия и химиопрепараты при раке большого дуоденального сосочка малоэффективны.

Под папилломатозом следует понимать патологический процесс, при котором образуются множественные папилломы на дерме либо слизистых оболочках органов. Папиллома – образование доброкачественное, по форме напоминающее сосочек, появляется который из эпителия.
Причины
Как правило, причиной папилломатоза является вирус. Возбудителем его является вирус папилломы человека (ВПЧ), имеющий почти сто различных типов, часть которых обладают потенциалом ракового заболевания.
Передается ВПЧ контактным путем, в том числе половым. ВПЧ может передаваться от матери к ребенку во время беременности либо родов.
Обычно никаких симптомов наличия вируса нет, но они проявляются в виде папиллом в случае снижения иммунитета человека.
Еще одна причина возникновения заболевания – хронические воспалительные процессы.
В ряде случаев появление заболевания вообще ничем не обусловлено.
Некоторые виды заболевания
Заболевание, как было сказано выше, может поразить кожу и слизистую любого органа. Вот некоторые виды его.
Заболевание в гортани
Статистика показывает, что данный вариант встречается у 2 человек из 100 000 взрослого населения и у 4 человек детей на 100 000 человек.
Симптомы, характеризующими этот вариант:
Развитие заболевания может привести к:
- Стенозу гортани;
- Проникновению папиллом в трахею и бронхи;
- Развитию легочной недостаточности;
- Перерождению в злокачественную опухоль.
Вестибулярное заболевание

Страдают им женщины в возрасте до 30 лет. При обнаружении заболевания данного типа необходимо провести обследование слизистых оболочек влагалища и шейки матки.
Данный тип, как правило, развивается без каких бы то ни было симптомов, обнаружить его можно лишь на приеме у гинеколога.
В ряде случаев симптомами заболевания является:
- Бели;
- Боли;
- Жжение в зоне вульвы;
- Диспареуния;
- Процесс воспаления.
Кожное заболевание
Это разрастание множества новообразований кожи на локальном ее участке. Обычный размер кожных папиллом 5–7 миллиметров, однако встречаются новообразования до 2 сантиметров.
По форме новообразования напоминают точечные или слегка свисающие кожные выросты либо горошины. Обычно цвет нароста точно такой же, как и кожный покров вокруг него, однако наблюдаются новообразования коричневого и белого цветов.
Характерная локализация новообразований – спина, ладони, пальцы, подошвы, стопы, веки, шея, зоны подмышечные и паховые.
Заболевание, как правило, не имеет симптомов, опасность его в том, что травмированные новообразования могут стать причиной воспаления либо превратиться в новообразования злокачественного характера.
Заболевание пищевода
Патология достаточно редкая. Образующиеся новообразования по своему виду напоминают полипы либо листовидные белесоватые образования. Обычный размер их не превышает сантиметра. Локализуются они в дистальных отделах пищевода.
Основная причина развития данной формы заболевания – папилломовирусная инфекция, однако папилломатоз может наблюдаться и при ее отсутствии.
Как правило, длительное время никакой симптоматики нет, но, развиваясь, заболевание напрямую связано с:
- Затрудненным глотанием;
- Болью за грудиной;
- Отрыжкой;
- Тошнотой.
Данный вид заболевания считается предраковым, поэтому при его выявлении необходимо хирургическое вмешательство.
Заболевание внутрипротоковое
В данном случае новообразования возникают в молочной железе, в ее молочных протоках. Как правило, образования не превышают сантиметра, но наблюдаются и гигантские - более пяти сантиметров. Последние деформируют молочную железу. Увеличиваясь в размерах, новообразования способствуют механическому расширению протока, что приводит к возникновению боли.
Обычно данным видом заболевания страдают женщины тридцати пяти – пятидесяти пяти лет. Заболевание может быть спровоцировано:
- Приемом оральных контрацептивов;
- Приемом гормональных средств;
- Семейным анамнезом;
- Нарушениями эндокринологического характера;
- Хроническими воспалительными процессами придатков.
Симптомическое проявление заболевания – янтарного цвета выделения из соска либо выделения с примесью крови.
Пациентка может жаловаться на дискомфорт и болезненность. При пальпировании в молочной железе обнаруживается уплотнение.
Высока вероятность перерождения новообразования в раковое, поэтому при его обнаружении необходимо хирургическое лечение.
Диагностические мероприятия
Часто заболевание обнаруживается при первичном осмотре, т.к. новообразования имеют характерные формы – мягкая плотная опухоль на ножке, размер которой обычно колеблется в диапазоне сантиметра – двух. Опухоль имеет неровную внешнюю поверхность, цвет ее белый либо коричневый. Иногда разросшееся новообразование внешне напоминает цветную капусту.
На выбор инструментальных диагностических методов влияет локализация заболевания:
- Гортань – ларингоскопия;
- Пищевод – ЭГДС;
- Молочная железа – дуктография.
Для того чтобы подтвердить вирусное происхождение новообразования и определить его конкретный тип, необходимо исследование посредством лабораторных методик – полимеразной цепной реакции, гибридизационных методов.
Важное значение в комплексном лечении имеет оценка иммунного статуса заболевшего, на ней основываются как при назначении терапии медикаментозной, так и для профилактических мер.
Лечение
Хирургическое вмешательство является основным методом лечения папилломатоза. При этом традиционное иссечение может стать причиной рубцевания слизистой. Чтобы избежать этого, сегодня применяют методы щадящих вмешательств:
- Удаление с помощью лазера;
- Дезинтеграция ультразвуком;
- Радиочастотную холодную аблацию;
- ФДТ;
- Электродеструкцию;
- Криодеструкцию;
- Диатермокоагуляцию и некоторые иные.
Гарантировать отсутствия рецидива при любом из перечисленных методов, нельзя. Для минимизации риска возникновения рецидива после операции в ряде случаев назначают адъювантную лекарственную терапию, включающую препараты противовирусного действия и иммуностимуляторы.
Профилактические мероприятия
В настоящее время разработана вакцина, направленная против нескольких типов заболевания, которые могут перерасти в рак. Она предназначена и для детей, и для взрослых.
При обнаружении заболевания для проведения лечения необходим динамический контроль пациентов. Страдающих от папилломатоза гортани обязательно нужно направлять на диспансеризацию. Периодичность ее - 1 раз в 3 месяца. При заболевании вестибулярного характера также необходим динамический контроль.
Клиника интегративной онкологии Onco.Rehab заботится о своих пациентах, стараясь предотвратить перерастание предраковой патологии в онкологию.
Читайте также:

