Образование кожи при заживлении
Обновлено: 26.04.2024
Общая картина и характеристики ран остаются неизменными на протяжении столетий. А вот подходы к их лечению по мере развития медицины претерпевали существенные изменения: чем больше медики разбирались в механизме заживления ран, тем более эффективными становились методики лечения и тем лучшие результаты достигались.
Детальное знание физиологии раневого процесса позволяет сегодняшним хирургам выбирать наиболее подходящие варианты местного лечения. Основной принцип выбора – удовлетворение специфических потребностей раны на каждой из трех его стадий, которые вне зависимости от типа и степени повреждения, характеризуются определенными морфологическими особенностями клеток и тканей. На современном этапе основное подспорье хирургов – широкое разнообразие готовых лечебных повязок.
Первая стадия - воспаление
С момента травмы начинается стадия воспаления, которая длится 3-4 дня. Первая задача организма на этом этапе – остановить кровотечение. Ее решение достигается кратковременным спазмом сосудов и замедлением кровотока: свежий сгусток крови останавливает кровотечение. Вторая задача – очистить рану от поврежденных и погибших тканевых клеток, которые могут стать источником инфекции. Для этого организм включает комплекс сложных клеточных реакций.
В рану мигрируют особые клетки, которые поглощают элементы погибших тканей и бактерии. Они же продуцируют биологически активные вещества. В микрососудах повышается давление крови за счет ее активного притока и затрудненного оттока. Вследствие этого проницаемость стенок сосудов увеличивается, в очаг воспаления выходит жидкая часть крови и образуется воспалительная жидкость - экссудат. Внешне стадия воспаления проявляется локальным отёком, болью, специфическим отделяемым и покраснением кожи вокруг раны.
Приоритетная задача местного лечения на первой стадии раневого процесса – способствовать очищению раны и удалению экссудата, который иногда бывает очень обильным. Наилучшим образом с этим справляются лечебные абсорбирующие повязки с особым липидоколлоидным комплексом. При наложении на рану они обеспечивают отток экссудата и создают наиболее благоприятные условия для ее заживления.
Вторая стадия - регенерация
Если ткани раны сохранили свою жизнеспособность, ее края плотно соприкасаются и не началось нагноение, с третьего дня раневой процесс вступает в стадию регенерации (пролиферации). На этом этапе важнейшая роль отводится особым клеткам - фибробластам. Их функция – синтезировать белок коллаген, из которого формируются волокна соединительной ткани. В процессе прорастания волокон капиллярами и восстановления проходимости лимфатических сосудов на месте раны образуется молодая рубцовая соединительная ткань.
С учетом особенностей второй стадии заживления ран, основная задача местного лечения на этом этапе - обеспечить оптимальное содержание жидкости в ране и защитить от повреждений легко травмируемую молодую соединительную ткань. Решение этих задач в полной мере обеспечивают готовые лечебные гидроколлоидные повязки, особенность которых состоит в образовании защитного геля при контакте с раной.
Третья стадия
Одновременно идет разрастание эпителия – клеток поверхностного слоя кожи. Тем самым процесс заживления раны вступает в третью стадию – эпителизации. Послеоперационные и небольшие резаные раны, края которых отстоят друг от друга не больше чем на 1 см, заживают так называемым первичным натяжением через 3-7 дней. Кожный рубец при этом ровный, гладкий и почти незаметный.
В случае нагноения раны, наличия в ней полостей или дренажных трубок, а также при невозможности сблизить края раны после иссечения тканей, заживление осуществляется вторичным натяжением. Его характерная черта - заполнение полости раны множеством тесно прижатых друг к другу гранул, состоящих из мелких разветвлений капилляров в окружении соединительнотканных клеток и лейкоцитов. Эта красная мелкозернистая масса, называемая грануляционной тканью, выстилает всю полость раны, образуя ее временный покров и защищая от внешних повреждений. В последующем на грануляционную ткань нарастают слои эпителия, постепенно покрывая всю раневую поверхность. Рубец при этом немного выдается над поверхностью кожи и имеет бледнеющий со временем красный цвет.
На стадии эпителизации заживлению ран способствуют готовые лечебные липидоколлоидные повязки с полимерной сетчатой основой. Их важнейшее свойство – атравматичность, которое достигается сочетанным действием мягкого парафина и образующегося геля. При использовании этих повязок эпителизация ускоряется, а молодая соединительная ткань не травмируется при перевязке.
Длительность заживления ран зависит от их природы, характера, размеров, общего состояния организма, и может достигать многих месяцев. При этом плавно сменяющие друг друга стадии раневого процесса не всегда удается обозначить четкими сроками, поскольку участки раны могут находиться на разных стадиях заживления.
Прочность раны увеличивается постепенно: при отсутствии осложнений уже ко второму месяцу рана достигает 50% своей конечной прочности, к третьему - восстанавливается 75% первоначальной прочности, к концу шестого месяца - 95%.
Каждая рана имеет естественный потенциал к восстановлению, который может быть стимулирован посредством избирательного применения современных технологий. Важность оптимизации процесса заживления ран не может быть преувеличена: в течение года в РФ выполнятся 17,4 млн операций и 6,8 млн хирургических манипуляций, 22,2 млн человек находятся на лечении с острыми ранами, 5,2 млн - с хроническими (2015г.).
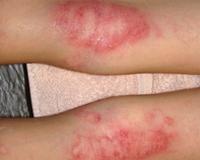
Мокнущая экзема — это острая форма экземы, которая протекает с выраженным экссудативным компонентом. Она проявляется отечностью, гиперемией кожи, образованием множественных везикулярных высыпаний и эрозий, сливающихся в очаги мокнутия. Для диагностики дерматоза проводится комплексное лабораторное обследование, гистологическое исследование биоптатов пораженных участков кожи, консультации смежных специалистов. Для купирования острой формы мокнущей экземы показано местное применение вяжущих препаратов, системное лечение антигистаминными, гипосенсибилизирующими, противовоспалительными средствами.
МКБ-10
Общие сведения
Экзема — самое распространенное кожное заболевание, на долю которого приходится 25-40% всех кожных патологий. Термин «мокнущая экзема» не используется в официальных классификациях, поскольку он отражает один из этапов островоспалительной кожной реакции, которая возникает при острой стадии различных клинических форм патологического процесса. Лечение дерматоза представляет сложную задачу ввиду хронического течения, частых рецидивов, сложного этиопатогенеза, поэтому болезнь не теряет своей актуальности в практической дерматологии.

Причины
Конкретные этиологические факторы болезни до сих по не установлены. Согласно современной общепринятой концепции, мокнущая экзема представляет собой мультифакториальное кожное поражение, протекающее с нарушениями функций эпидермиса. Она развивается при сочетании эндогенных и экзогенных провоцирующих факторов, основными из которых являются следующие:
- Генетическая предрасположенность. Если патология диагностирована у одного из родителей, риск заболеть составляет 40%, при наличии заболевания у обоих родителей — повышается до 50-60%. Отягощенная наследственность проявляется определенными генами HLA, которые контролируют иммунный ответ.
- Экзогенные факторы. Заболевание провоцируется негативным воздействием химических веществ (бытовая химия, профессиональные вредности), физических факторов (повышенная инсоляция, температурные перепады), аллергизацией при употреблении некоторых продуктов питания, лекарственных препаратов.
- Инфекционно-аллергические факторы. Дерматоз может возникать при попадании в организм бактериальных или грибковых агентов извне. Нередко он начинается на фоне хронических очагов инфекции, особенно при отсутствии адекватного лечения. Во втором случае появления экзематозных симптомов вызвано хронической сенсибилизацией организма к антигенным детерминантам микробов.
- Неврологические нарушения. Функциональные нервные расстройства с преобладанием парасимпатических влияний повышают вероятность появления мокнущих высыпаний. Патология периферических нервов, сопровождающаяся ухудшением микроциркуляции, провоцирует возникновение клинических симптомов в пораженной зоне.
- Соматические заболевания. Стимулируют развитие кожного поражения и отягощают его течение при несоблюдении схемы лечения многие патологии внутренних органов: желудочно-кишечного тракта, панкреатобилиарной системы, мочевыделительной системы. Важная роль отводится нейроэндокринным нарушениям, метаболическим расстройствам, возникающим вследствие поражения желез внутренней секреции.
Патогенез
Основной патогенетический компонент мокнущей экземы — иммунное воспаление в коже, протекающее по типу реакции замедленного типа. В его формировании выделяют 4 предрасполагающих фактора: нарушения клеточного и гуморального иммунитета, сенсибилизация к эндо- или экзоантигенам, изменение функции ЦНС, генетически обусловленные особенности иммунного ответа.
Образование типичных мокнущих поражений кожного покрова связывают с дисфункцией Т-лимфоцитов, которые выделяют в ткани провоспалительные вещества: интерлейкины, интерферон, фактор некроза опухолей. Одновременно усиливается выброс лейкотриенов, простагландинов, гистамина, что завершается острой воспалительной реакцией с преобладаем экссудативного компонента.
В патогенезе дерматоза немаловажную роль играют иммунологические расстройства, ассоциированные с конкретными антигенами главного комплекса гистосовместимости. У пациентов снижается активность Т-лимфоцитов хелперов и супрессоров, что проявляется угнетением иммунологической реактивности. Вследствие этого происходит активация хронической инфекции, замедляется выведение антигенов из организма.
Также в механизме развития мокнущей экземы выделяют снижение активности неспецифических защитных факторов — комплемента, лизоцима, фагоцитов. При этом повышается риск присоединения вторичной инфекции, осложненного течения болезни. Отягощает ситуацию аллергическая перестройка организма, из-за которой кожа приобретает повышенную поливалентную чувствительность к антигенам.
Классификация
На сегодня отсутствует общепринятая систематизация, что обусловлено разнообразием клинических вариантов патологии, разными точками зрения экспертов на причины и механизмы формирования дерматоза, подбор схем лечения. Практикующие дерматологи используют несколько вариантов классификации, при которых учитываются следующие признаки:
- По течению процесс бывает острым, подострым, хроническим.
- По клиническим проявлениям болезнь подразделяется на истинную, микробную, детскую, профессиональную, варикозную формы.
- По классификации Хорнштейна существует экзогенная, эндогенная, дисрегуляторная экзема.
- По классификации Американской академии дерматовенерологии выделяются конкретные нозологические единицы дерматоза (астеатотическая экзема, нумулярный дерматит, белый питириаз и т. д.).
Симптомы мокнущей экземы
Мокнущая экзема манифестирует покраснением и отечностью кожи с последующим появлением высыпаний в виде мелких пузырьков. При механическом воздействии или самопроизвольно везикулы лопаются, обнажая эрозии с интенсивным мокнутием. Характерным симптомом острой формы дерматоза являются «серозные колодцы» — эрозии, из глубины которых выделяется прозрачная или слегка желтоватая жидкость.
Постепенно мокнущие поверхности подсыхают с образованием тонких корок. Одновременно с этим на пораженных участках могут появляться папулы — мелкие розовые узелки, пустулы со стерильным содержимым. Присутствие на кожном покрове различных морфологических элементов называется истинным полиморфизмом сыпи, этот признак считается типичным для истинной (идиопатической) экземы, не встречается при других формах дерматоза.
Из субъективных ощущений без лечения на первое место выходит сильный кожный зуд, вследствие которого больные расчесывают кожу до крови, усугубляя течение процесса. Зачастую в результате интенсивного зуда возникают нарушения работоспособности, раздражительность, сон становится прерывистым и не снимает усталость. Обширные мокнущие эрозии сопровождаются болезненностью, которая усиливается при соприкосновении пораженной кожи с одеждой.
В клинической картине мокнущего дерматоза выделяют особенности, связанные с конкретной формой. Истинная экземы характеризуется симметричным расположением элементов с их локализацией на коже туловища, верхних и нижних конечностей. Для микробного поражения типичны асимметричные очаги мокнущих высыпаний на нижних конечностях. При детской форме очаги мокнутия имеют блестящую, гиперемированную поверхность.
Осложнения
В периоде мокнутия пораженная кожа представляет открытую раневую поверхность, которая становится хорошими входными воротами для патогенных микроорганизмов. Поэтому самым распространенным осложнением в остром периоде без лечения является присоединение вторичной бактериальной инфекции, наиболее часто вызванной стафилококками или стрептококками. В тяжелых случаях возникает флегмона, регионарный лимфаденит.
У больных с длительным стажем патологии мокнущие элементы и расчесы приводят к утолщению кожи, усилению кожного рисунка, гиперпигментации, повышенной сухости. Такие дерматологические изменения приносят дискомфорт, поскольку кожа теряет эластичность, формируется значимый косметический дефект, что особенно беспокоит женщин.
Диагностика
Данные анамнеза и кожные проявления дерматоза дают врачу-дерматологу ценную информацию для постановки диагноза и выбора лечения. Наличие множественных эрозий, серозного отделяемого, сероватых корок является подтверждением мокнущей стадии экземы. В сомнительных случаях, а также для выявления возможных первопричин болезни показаны:
- Гистологический анализ. На мокнущей стадии в биоптатах кожи определяется спонгиоз, мелкие везикулы, внутриклеточный отек эпидермиса. В структуре дермы наблюдается лимфоидно-клеточная инфильтрация вокруг сосудов, расширение поверхностной сети капилляров.
- Анализы крови. Для подтверждения инфекционно-аллергической этиологии измеряется уровень иммуноглобулина Е, производится аллергологическое исследование для обнаружения антител к специфическим антигенам. Чтобы оценить общее состояние здоровья, назначается клинический, биохимический анализ крови.
- Микробиологические исследования. При подозрении на микробную экзему, осложнении процесса вторичной инфекцией необходим бакпосев отделяемого кожных элементов. По его результатам устанавливают точный вид патогенного возбудителя, чувствительность к антибактериальным препаратам, подбирают подходящее для лечения средство.
- Консультации специалистов. Если при первичной диагностике у человека присутствуют признаки поражения внутренних органов, которые потенциально могли стать провоцирующим фактором мокнущего дерматоза, дальнейшее обследование и лечение проводится с участием профильных врачей. Чаще всего требуется помощь гастроэнтеролога, психоневролога, эндокринолога.
Лечение мокнущей экземы
Системная терапия
Терапия мокнущей экземы подбирается индивидуально с учетом предположительных причин развития заболевания, степени тяжести клинических проявлений, наличия у больного сопутствующих патологий или осложнений. Для уменьшения сенсибилизации организма больным рекомендуется соблюдать гипоаллергенную диету, из которой исключают жирные сорта рыбы и мяса, устрицы и другие морепродукты, кофе и какао-продукты, цитрусовые, томаты, бобовые.
Если обострение болезни связано с воздействием экзогенных факторов, их устранение является необходимым условием для успешности лечения. Учитывая конкретную ситуацию, пациентам может потребоваться сменить место работы, исключить бытовые аллергены, переехать в более подходящие климатические условия. Комплексное лечение мокнущего аллергодерматоза требует применения ряда препаратов:
- Антигистаминные средства. Для ликвидации кожного зуда в острой фазе применяются гистаминоблокаторы первого поколения, а после купирования симптоматики возможно продолжение лечения медикаментами второго и третьего поколения.
- Десенсибилизирующие препараты. Используются растворы кальция, натрия тиосульфат. Лечение уменьшает проницаемость сосудов, оказывает противовоспалительный эффект, нормализует метаболические реакции в дерме.
- Стабилизаторы клеточных мембран. Чтобы усилить эффективность антигистаминных препаратов, показано лечение стабилизаторами мембран тучных клеток. Некоторые авторы советуют применять полиненасыщенные жирные кислоты омена-3 для нормализации структуры мембран клеток.
- Глюкокортикостероиды. При генерализованных формах мокнущей экземы, отсутствии эффекта от других вариантов лечения применяются гормоны в режиме пульс-терапии или длительного приема.
- Иммунокорригирующие средства. Рациональная иммунокоррекция назначается для облегчения состояния при непрерывно рецидивирующей форме мокнущей экземы. Лечение включает препараты тимуса, стимуляторы лейкопоэза.
- Антибиотики. Лечение антибактериальными средствами требуется при микробной форме дерматоза и доказанной инфекционно-аллергической природе болезни.
Поскольку в патогенезе мокнущей экземы играют роль различные соматические нарушения, лечение включает коррекцию этих патологий. Чтобы нормализовать работу пищеварительного тракта, целесообразно использовать заместительную ферментную терапию, пробиотики и синбиотики, витаминно-минеральные комплексы. Чтобы сбалансировать состояние центральной нервной системы, в схему лечения включаются легкие седативные средства, по отдельным показаниям назначаются транквилизаторы, антидепрессанты.
Местная терапия
В фазе мокнутия используются примочки с вяжущими препаратами, которые уменьшают экссудацию, способствуют более быстрому появлению корочек и регрессу болезни. В острой стадии назначаются ежедневные процедуры длительностью 1-1,5 часа, которые предполагают постоянную смену повязок по мере их подсыхания. Затем переходят к нанесению мазей с топическими кортикостероидами, антисептиками, ингибиторами кальциневрина.
Из физиотерапевтических методов лечения наибольшую результативность показывает селективная ультрафиолетовая терапия, во время которой облучение проводится светом узкого диапазона (311 нм). Также выполняется низкоинтенсивное лазерное облучение красного или инфракрасного спектра, электропунктура биологически активных точек, локальная гипертермия. На этапе ремиссии хороший эффект дает озонотерапия, бальнеотерапия, пелоидотерапия.
Прогноз и профилактика
Правильное лечение мокнущей острой экземы дает возможность быстро купировать кожную симптоматику и улучшить состояние пациентов в целом, поэтому прогноз благоприятный. Спустя 5-6 дней интенсивной терапии уменьшается выраженность зуда, сокращается объем кожных поражений, а выздоровление в неосложненных случаях наступает спустя 3-4 недели. Менее оптимистичный прогноз при развитии экземы у страдающих иммуносупрессией, хроническими патологиями.
Профилактика болезни предполагает соблюдение личной гигиены, исключение типичных пищевых, бытовых и профессиональных аллергенов. Пациентам с экземой в ряде случаев помогает молочно-растительная диета. Обязательными превентивными мерами являются лечение сопутствующих расстройств и правильный уход за кожей тела: применение смягчающих кремов, мягких очищающих продуктов, избегание массажа сухой щеткой и других агрессивных воздействий.
2. Экзема в практике семейного врача: клинические формы, дифференциальный диагноз, лечение/ Е.А. Бардова// Клиническая иммунологии, аллергологии, инфектологии. — 2013. — №1.
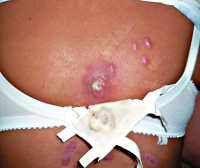
Глубокая пиодермия – группа гнойно-воспалительных поражений кожи (преимущественно ее глубоких слоев – дермы), обусловленных инфицированием тканей стафилококками, стрептококками или смешанной микрофлорой. Симптомы заболевания различаются в зависимости от выраженности воспаления и характера возбудителя, но обязательно включают в себя отек, болезненность, покраснение и образование гноя. Диагностика глубокой пиодермии основывается на внешних кожных проявлениях и микробиологических исследованиях для идентификации возбудителя. В лечении широко применяются хирургические приемы для обеспечения оттока гноя, местные и общие антибиотики, противомикробные и антисептические средства.
Общие сведения
Глубокая пиодермия – гнойное заболевание кожных покровов, особенностью которого является поражение дермы, подкожной клетчатки, глубоко расположенных волосяных фолликулов, потовых и сальных желез. Это состояние является одной из наиболее распространенных патологий в дерматологии – по разным данным, на нее приходится от 30 до 40% всех дерматологических заболеваний. Практически каждый человек минимум несколько раз в жизни страдал от проявлений различных форм глубокой пиодермии. Это объясняется высокой распространенностью возбудителей (стафилококков и стрептококков), их вирулентностью, огромным разнообразием штаммов. В большинстве случаев глубокая пиодермия не угрожает жизни человека и даже излечивается самостоятельно без специальной терапии, но иногда она может быть причиной интоксикации, источником метастатических гнойных очагов и даже причиной сепсиса.

Причины глубокой пиодермии
В широком плане, глубокая пиодермия – поражение кожи, обусловленное гноеродной микрофлорой, к которой относят стафилококков, стрептококков, синегнойную палочку и некоторые другие микроорганизмы. Однако более 95% случаев заболевания вызываются именно кокковой флорой, так как она широко распространена в окружающей среде и отчасти представлена даже на поверхности кожи здорового человека. При проникновении в ткани кожи через микротрещины, повреждения эпидермиса, вдоль волосяных стержней и по протокам кожных желез микроорганизмы начинают бурно размножаться. Выделяемые ими в процессе жизнедеятельности ферменты и различные токсины вызывают деструкцию клеток кожи. В результате этих процессов формируется первичный очаг, расположенный в дерме – симптомов глубокой пиодермии на этом этапе не наблюдается.
Сами микроорганизмы и выделяемые ими ферменты обладают сильными иммуногенными свойствами, поэтому практически сразу после формирования первичного очага происходит незамедлительная реакция иммунной системы. Традиционно первыми на инфицирование реагируют тканевые макрофаги, затем путем хемотаксиса в будущий очаг глубокой пиодермии попадают нейтрофилы, а затем и другие иммунокомпетентные клетки. Выделяемые ими биологически активные вещества приводят к местному отеку, покраснению, появлению болезненных ощущений. Клинически это соответствует первой стадии глубокой пиодермии – образованию воспалительного очага, который может иметь тенденцию к расширению.
На определенном этапе иммунитету удается локализовать воспаление, и его распространение в тканях останавливается. Нейтрофилы атакуют патогенные микроорганизмы и отчасти собственные ткани (вторичная альтерация) в очаге с формированием гноя – субстанции, состоящей из «осколков» возбудителей, разрушенных собственных клеток и погибших нейтрофилов. Развитие глубокой пиодермии облегчается при ряде обстоятельств – пониженном иммунитете, сахарном диабете, истощении, гиповитаминозах и других ослабляющих организм состояниях. Немаловажную роль играет пренебрежение правилами личной гигиены, избыточная продукция кожного сала, местное переохлаждение кожи. Для лиц с пониженным иммунитетом глубокая пиодермия опасна тем, что способна вызывать сильные поражения, стать причиной различных осложнений, некоторые из которых могут напрямую угрожать жизни человека.
Симптомы глубокой пиодермии
Существует несколько клинических разновидностей глубокой пиодермии, которые характеризуется разными возбудителями, выраженностью симптомов и типом поражаемых тканей. Все формы этого заболевания по характеру микрофлоры, вызвавшей воспаление, делят на стафилодермии, стрептодермии и смешанные разновидности, которые иногда называют стрептостафилодермиями. К глубоким пиодермиям, вызванным стафилококками, относят фурункулы, карбункулы, гидрадениты и глубокий фолликулит. Глубокие стрептодермии представлены вульгарной эктимой, а воспаления из-за смешанной микрофлоры – хронической язвенно-вегетирующей пиодермией.
Фурункул – разновидность глубокой пиодермии, особенностью которой является поражение волосяного фолликула гнойно-некротического характера с переходом на окружающие ткани. Его развитию может предшествовать поверхностное гнойное воспаление (фолликулит), однако возможно и первичное развитие глубокого процесса. На участке кожи, окружающей волос, формируется сначала очаг багрового цвета размером от нескольких миллиметров до 1-2 сантиметров, болезненный и плотный, его температура заметно выше окружающих кожных покровов. Затем глубокая пиодермия такого типа сопровождается появлением гноя, в центре которого будет стержень из некротизированной ткани. Гнойно-некротическое содержимое отторгается через 3-10 дней, на месте поражения кожи формируется небольшая язва, которая быстро рубцуется.
Карбункул – более тяжелая разновидность глубокой пиодермии, вызываемая стафилококковой флорой и характеризующаяся поражением глубоких слоев дермы и подкожной жировой клетчатки. В глубине кожи возникает плотный инфильтрат, кожные покровы над ним приобретают синюшно-багровый оттенок, становятся горячими и болезненными. Через несколько дней в очаге глубокой пиодермии начинают формироваться пустулы, происходит выделение гноя и некротических стержней, на месте поражения образуется язва. Все это сопровождается выраженными общими симптомами – интоксикацией, лихорадкой, болями стреляющего характера в месте карбункула. Отмечается регионарный лимфаденит и лимфангит. После разрешения этой формы глубокой пиодермии на месте поражения остается заметный рубец.
Гидраденит – форма глубокой пиодермии, при которой поражаются апокриновые потовые железы с развитием гнойного воспаления. Из-за этого характерная локализация патологических очагов – подмышечные впадины, околососковая и аногенитальная области. Гидраденит начинается с развития болезненного узла синюшного цвета, который за несколько дней значительно увеличивается в размерах и самопроизвольно вскрываются с выделением обильного количества гноя. Затем происходит постепенное заживление, рубцы образуются в крайне редких случаях. При этой форме глубокой пиодермии также отмечается регионарный лимфаденит и лимфангит, но общие симптомы выражены слабо. Гидрадениты, особенно в области подмышечных впадин, склонны к частым рецидивам.
Глубокий фолликулит – одна из наиболее легких форм глубокой пиодермии, которая отличается от обычного фолликулита более выраженным поражением волосяных луковиц. Симптоматика в целом сходна с фурункулом, однако проявления менее выраженные, общих симптомов практически никогда не наблюдается. Главный диагностический критерий, позволяющий дерматологу отличить фурункул от глубокого фолликулита – отсутствие гнойно-некротического воспаления, так как не образуется характерный некротический стержень.
Вульгарная эктима – форма глубокой пиодермии, вызываемая стрептококковой микрофлорой. Чаще всего поражает кожу голени у ослабленных больных, в крайне редких случаях возникает у здоровых людей. Эктима начинается с образования на поверхности кожных покровов пустулы с мутным содержимым серозного, иногда геморрагического характера. Затем пустула исчезает и на ее месте формируется типичный очаг глубокой пиодермии – болезненная язва с выраженным воспалительным ободком вокруг, дно образования покрыто слоем гноя. Через 2-3 недели после появления язвы начинается ее постепенное рубцевание с развитием заметного шрама.
Хроническая язвенно-вегетирующая пиодермия – кожное заболевание, возбудителями которого является смешанная микрофлора, наибольшую роль в развитии патологии играет золотистый стафилококк и стрептококки группы А. Глубокая пиодермия такого типа чаще всего развивается у ослабленных больных – истощенных лиц, страдающих алкоголизмом, пожилых людей. Характеризуется образованием на нижних конечностях эрозий неправильной формы с рваными краями, окруженных воспаленной кожей. Дно язвенных образований покрыто гноем, часто возникают выделения с неприятным зловонным запахом. Эрозии длительное время не заживают и склонны к частым рецидивам или поражению других участков кожных покровов.
Осложнениями любой разновидности глубокой пиодермии могут быть метастатические гнойные поражения регионарных лимфатических узлов и отдаленных органов. Особенно опасны в этом отношении глубокие фолликулиты и фурункулы, возникающие в пределах носогубного треугольника – имеющиеся там анастомозы кровеносных сосудов способствуют заносу инфекции в головной мозг и его оболочки. У ослабленных больных на фоне глубокой пиодермии могут возникать флегмоны и сепсис, являющиеся жизнеугрожающими состояниями. В редких случаях возможно развитие токсического шока.
Диагностика глубокой пиодермии
Диагностика различных форм глубокой пиодермии осуществляется посредством осмотра дерматолога (иногда может потребоваться консультация хирурга). Из дополнительных методов исследования наиболее часто применяют посев гноя для определения характера возбудителя и для выяснения его чувствительности к антибактериальным средствам. При развитии общих симптомов также в ряде случаев необходимо проведение общего анализа крови, в самых тяжелых случаях – бакпосев крови для диагностики сепсиса. Результаты осмотра зависят от формы глубокой пиодермии и стадии ее развития – это может быть просто воспалительный очаг, сформировавшийся гнойник, ранка или язва с гнойным отделяемым. При посеве определяются стафилококки или стрептококки, может обнаруживаться смешанная микрофлора. Микробиологические исследования посевов могут определить вид и штамм возбудителя, а также его чувствительность к антибиотикам.
Если имеется повышение температуры, головная боль, слабость то необходимо проведение общего анализа крови. Обычно при глубокой пиодермии определяются легкие неспецифические признаки воспаления – повышение скорости оседания эритроцитов, небольшой лейкоцитоз. В более тяжелых случаях наблюдаются уже выраженные изменения – значительный рост СОЭ, выраженный лейкоцитоз, выявляются изменения в распределении нейтрофилов. В крови появляется множество юных форм этой фракции лейкоцитов, что носит название нейтрофильного сдвига влево. Если есть подозрения, что глубокая пиодермия стала причиной сепсиса, производят посев крови на питательные среды – в норме кровь человека абсолютно стерильна, рост культур говорит о наличии возбудителя в крови. Для диагностики таких осложнений, как метастатические гнойные очаги могут применяться ультразвуковые, рентгенологические и другие методы клинических исследований.
Лечение глубокой пиодермии
При незначительных по выраженности гнойных поражениях без общих проявлений интоксикации рекомендуется ждать самопроизвольного разрешения глубокой пиодермии. Лечебные мероприятия сводятся к недопущению осложнений. При наличии волос вокруг гнойного очага их нужно аккуратно состричь – использование бритвы может привести к распространению инфекции. Мыть участок с очагом глубокой пиодермии не рекомендуется, допустимо только протирать кожу вокруг него дезинфицирующими растворами (хлоргексидином, раствором салициловой кислоты). Строго запрещается без участия дерматолога или хирурга самостоятельно вскрывать гнойник или каким-либо способом ускорять отделение гноя – это может привести к диссеминации возбудителя.
Если глубокая пиодермия характеризуется развитием крупных очагов с появлением общих симптомов (лихорадка, слабость, головные боли), то необходимо назначение антибактериальных средств, таких как эритромицин, тетрациклин, линкомицин – предварительно желательно сделать бактериальный посев и определить препарат, к которому наиболее чувствителен данный микроорганизм. Также при глубокой пиодермии применяют и противомикробные средства из группы сульфаниламидов – например, сульфаметоксазол+триметоприм. В последние годы в тяжелых случаях гнойных поражений кожи используют и иммунологические препараты – стафилококковый анатоксин, антистафилококковую гипериммунную плазму и ряд других.
При глубоком расположении значительного по размерам очага пиодермии прибегают к хирургическому вскрытию полости гнойника для формирования дренажа и оттока гноя. Кроме того, это позволяет доставлять антисептические и антибактериальные препараты непосредственно в область поражения, что ускоряет лечение. Вскрытие очага глубокой пиодермии должно происходить в стерильном помещении и осуществляться квалифицированным гнойным хирургом.
Прогноз и профилактика глубокой пиодермии
В большинстве случаев прогноз при развитии различных форм глубокой пиодермии благоприятный – после отделения гноя происходит заживление очага, довольно часто с образованием рубцов. Однако у ослабленных больных с низким уровнем иммунитета возможно развитие осложнений, некоторые из которых могут угрожать жизни и требуют лечения в условиях стационара. Для профилактики развития глубокой пиодермии необходимо придерживаться правил личной гигиены, своевременно обрабатывать кожные повреждения (ссадины, порезы) антисептиками. Кроме того, важно устранять возможные источники инфекции в организме – кариозные зубы, хронические инфекции ЛОР-органов.
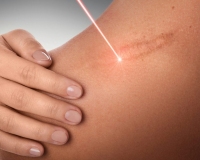
Гипертрофический рубец – это избыточное разрастание фиброзной соединительной ткани при патологическом заживлении кожной раны. Косметический дефект образуется при обширных поражениях кожи с неровными краями, врожденной предрасположенности, неадекватной хирургической помощи и чрезмерном натяжении тканей. Рубец выступает на несколько миллиметров над кожей, имеет багровый или розовый цвет, по форме и размерам соответствует ране. Диагностика проводится путем осмотра, в сомнительных ситуациях назначается патоморфологическое исследование. Коррекцию гипертрофических шрамов выполняют инъекциями, методами крио- и лазерной деструкции, пластической хирургии.
МКБ-10


Общие сведения
Физиологическая регенерация должна завершаться образованием нормотрофического рубца, который не выступает над уровнем кожи и со временем становится почти незаметным. Однако у многих пациентов наблюдаются нарушения регенераторных процессов, поэтому гипертрофические рубцы – серьезная проблема для всех направлений современной хирургии. Видимый эстетический недостаток и сложности в коррекции объясняют высокую актуальность гипертрофических шрамов, требуют от врачей разработки новых методов их эффективной маскировки и удаления.

Причины
Характер рубцевания и внешний вид зажившей раны во многом определяется этиологией кожного повреждения. По причинам появления рубцы бывают посттравматические, послеоперационные, образовавшиеся на месте патологических кожных элементов или вследствие лучевой терапии. Формированию патологического гипертрофического шрама на месте раны способствуют следующие факторы:
- Характер повреждения. Патологические рубцы чаще возникают при рваных, разможженных и укушенных ранах, когда травматизация кожи не соответствует линиям Лангера. Предрасполагающим фактором является заживление вторичным натяжением, нагноение и воспаление места травмы.
- Избыточное натяжение тканей. Такая ситуация встречается при ушивании и пластической коррекции рубца без пересадки кожи, когда собственные ткани пациента стягиваются для закрытия дефекта. В месте натяжения нарушается образование структурной соединительной ткани, возникают гипертрофические явления.
- Опасная локализация. Патологические рубцы в основном образуются по передней поверхности шеи, в области мочки уха. Это объясняется различными механическими свойствами кожи на разных участках тела, что оказывает значимую роль на процессы регенерации.
- Склонность к патологическому рубцеванию. Доказаны генетические и иммунные варианты предрасположенности к образованию гипертрофических и келоидных рубцов. У таких пациентов патологические шрамы образуются даже при отсутствии других провоцирующих факторов.
Патогенез
Классическое заживление раны длится до 1 года, завершается образованием рубца. В первые 10 суток наблюдается острое воспаление, которое в последующий месяц приводит к активному фибринолизу и образованию рыхлой соединительной ткани. На протяжении 2-3 месяцев после кожного повреждения ткани уплотняются, образуется прочный шрам. Окончательная перестройка рубца происходит 4-12 месяцев, именно в этот период появляются гипертрофические изменения.
При гипертрофическом процессе незрелая соединительная ткань располагается в субэпидермальном слое. Патоморфологически она представлена тонкими пучками коллагена, отдельными эластиновыми волокнами, избыточным количеством внеклеточного матрикса. Наблюдается большое число плазматических клеток, однако гигантские фибробласты отсутствуют. Сверху образование покрыто ровным слоем эпидермиса.

Классификация
Гипертрофический рубец – один из классических вариантов шрамов, согласно клинико-морфологической систематизации. В практической дерматологии используются и другие виды классификации, чтобы наиболее точно описать особенности кожной регенерации и подобрать методы коррекции патологических случаев. Существует несколько критериев систематизации рубцовых изменений:
- По возрасту: незрелые (до 3 месяцев), умеренно зрелые (3-12 месяцев), зрелые (старше 1 года).
- По конфигурации: линейные, дугообразные, зигзагообразные, звездчатые и другие варианты неправильной формы.
- По цвету: розовые, багрово-красные, цианотичные, белесоватые, пигментированные.
- По размеру: малые (до 1 см), средние (1-2 см), крупные (до 4,5 см), обширные (более 4,5 см).
Симптомы гипертрофического рубца
Такой тип шрама начинает расти спустя 3-4 недели после травмы, его увеличение в размерах продолжается в среднем 5-6 месяцев. Гипертрофический рубец имеет красноватый или синюшный оттенок, по размеру и форме соответствует границам раны, возвышается над поверхностью здоровой кожи не более чем на 4 мм. Со временем образование приобретает светло-розовый или телесный оттенок, спустя 12-18 месяцев возможна его частичная спонтанная регрессия.
Поверхность гипертрофического рубца неровная с выступающими участками, кожа над ним матовая. Его контуры четко очерчены, однако края плавно переходят на окружающие кожные покровы и постепенно сливаются с ними. В местах постоянного трения шрам покрывается ороговевшими наслоениями и небольшими язвами. При этом пациента беспокоит болезненность, сильный зуд, мокнутие или выделение сукровицы.
Осложнения
Гипертрофические рубцы не угрожают жизни и здоровью человека. Их основной проблемой является косметический дефект, особенно при локализации на лице и открытых участках тела. Крупные и заметные шрамы сказываются на психологическом состоянии пациентов, вызывают проблемы с социализацией, становятся препятствием для построения отношений с противоположным полом.
Неприятные последствия наблюдаются при расположении рубца в месте постоянной травматизации. Вследствие механического трения на его возвышающейся поверхности возникают раны и язвы, которые могут инфицироваться с развитием вторичных бактериальных осложнений. Также возникают явления гиперкератоза, которые усугубляют неэстетичный вид рубцовой ткани.
Диагностика
При образовании гипертрофических рубцов показано обследование у врача-дерматолога и хирурга. В большинстве ситуаций диагноз устанавливают на основании физикального осмотра: определяются внешние характеристики шрама, условия его появления, наличие субъективной симптоматики. При согласии пациента проводится фотографирование пораженной области тела для отслеживания динамики изменений. Дополнительные методы диагностики:
- УЗИ мягких тканей. Сонография назначается, чтобы оценить толщину и глубину залегания рубцовой ткани, исследовать характер и полноту заживления раны, исключить осложнения.
- Патоморфологическое исследование. Для изучения структуры гипертрофического рубца проводится световая и электронная микроскопия, микроскопическая морфометрия. Исследования необходимы при трудностях дифференцировки разных видов шрамов, необходимости исключить другие кожные патологии.
Дифференциальная диагностика
В клинической практике необходимо отличать гипертрофические и келоидные рубцы, которые имеют большое внешнее сходство и патоморфологические признаки. На келоидный тип шрама указывает распространение соединительной ткани за пределы повреждения, продолжающийся рост в течение многих месяцев и даже лет, интенсивные субъективные ощущения (зуд, жжение, болезненность). Патоморфологически келоид характеризуется атипичными гигантскими фибробластами.

Лечение гипертрофического рубца
Консервативная терапия
Не существует общепринятого протокола коррекции патологической рубцовой ткани. Программа лечения подбирается индивидуально для каждого пациента, основываясь на клинических особенностях, локализации, давности образования и других характеристиках гипертрофического рубца. Небольшие образования удается скорректировать нехирургическими методиками, самые эффективные из которых:
- Локальная компрессионная терапия. Давящие силиконовые пластины и эластичные бинты замедляют разрастание рубцовых тканей, способствуют образованию шрамов нормотрофического типа.
- Инъекции кортикостероидов. При маленьких свежих шрамах гормоны угнетают чрезмерное образование фибробластов и коллагена, замедляют темпы роста соединительной ткани. Уколы глюкокортикоидов проводятся, пока рубец не сравняется по высоте с поверхностью кожи.
- Физиотерапия. Для сокращения объема соединительнотканных волокон применяются фибринолитические ферменты (лидаза, коллагеназа), которые вводятся методами электрофореза и ультрафонофореза.
- Криодеструкция. Для неинвазивного удаления гипертрофического рубца применяется жидкий азот, который наносится на очаг поражения, замораживает патологические ткани и разрушает их. Для достижения хорошего косметического эффекта проводится несколько сеансов.
- Лазерная шлифовка. Коррекция гипертрофических разрастаний выполняется абляционными лазерами, которые удаляют неструктурную соединительную ткань и сглаживают контуры шрама. В основном применяется фракционный метод лазерной шлифовки, который отличается коротким периодом реабилитации.
Хирургическое лечение
Оперативная коррекция рубцовых тканей показана при неэффективности лекарственных и малоинвазивных методов лечения. Хирургическое вмешательство направлено на иссечение патологических разрастаний соединительной ткани, ликвидацию чрезмерного натяжения кожи. Вторичные раневые дефекты закрываются с помощью местных или перемещенных кожных лоскутов, дермотензии с применением тканевых эспандеров.
Прогноз и профилактика
Небольшие по размеру гипертрофические рубцы успешно корректируются инъекционными, аппаратными или хирургическими методиками. При крупных шрамах и генетической склонности к патологической регенерации прогноз менее благоприятный: комплексная терапия уменьшает размеры и бугристость рубца, однако достичь нормотрофии и полностью скрыть дефект зачастую не удается.
Профилактика патологического рубцевания заключается в своевременной и квалифицированной помощи хирургов при серьезных травмах, адекватной иммобилизации в раннем периоде заживления, соблюдении этапности хирургического лечения. При обширных повреждениях кожного покрова с самого начала лечения требуется консультация пластического хирурга для выбора оптимального метода закрытия дефектов, чтобы минимизировать формирование шрамов.
3. Лечение гипертрофических и келоидных рубцов/ Г.Э. Карапетян// Фундаментальные исследования. – 2013. – №3.
4. Применение ферментов при лечении больных с гипертрофическими рубцами/ Б.А. Парамонов, И.И. Турковский, С.В. Бондарев// Вестник хирургии. – 2007.
Лечение гнойных ран, в том числе трудно заживаемых трофических язв нижних конечностей, ран при сахарном диабете, пролежней, ран после травм, ожогов часто проводят в домашних условиях. Воспаленные гнойные раны всегда содержат большое количество разнообразных микроорганизмов – бактерий и грибов. Для такой раны характерны отечность, покраснение кожи вокруг раны, локальная боль и локальное повышение температуры в месте, где расположена рана.
Этапы заживления гнойной (инфицированной) раны
(концепция T.I.M.E.)
| Цель | Повязки |
| T. Очистить рану: |
Жидкость, выделяемая раной имеет неприятный запах и цвет. Это гнойный экссудат. Лечение гнойных ран включает в себя хирургическую обработку раны и применения перевязочных средств. Хирургическую обработку раны, вскрытие гнойных полостей всегда выполняют в медицинском учреждении - поликлинике, больнице. Лечение гнойных ран перевязочными средствами осуществляется как в медицинских учреждениях, так и в домашних условиях. Чтобы местное лечение было эффективным перевязочные средства должны бороться с инфекцией и обеспечивать отток гнойного экссудата из раны.
Антибактериальные повязки






Рана должна быть чистой
В гнойной ране могут присутствовать струпы, некрозы, корочки, фибрин (это желтая плотная ткань на ране), то такую рану необходимо очистить. Очищения можно добиться применением гидрогелей Neofix FibroGel AG, IntraSite Gel и IntraSite Conformable. Главное назначение этих гелей заключается в увлажнении некрозов и корочек, разрыхлении их, что способствует более легкому удалению некрозов при последующих перевязках. Гидрогели наносятся непосредственно на рану в достаточном количестве чтобы рана была полностью покрыта гидрогелем, слой гидрогеля при этом должен быть не менее 5 мм. Далее рану необходимо закрыть пленочной повязкой, например OpSite Flexigrid, или одной из послеоперационных повязок OpSite Post-Op, PRIMAPORE, NEOFIX Post. Поверх гелей можно использовать абсорбирующие повязки Allevyn Adhesive или Allevyn Sacrum, которые предпочтительнее и удобнее использовать при лечении пролежней, так как эти повязки имеют липкий край и мягкую губчатую подушечку. По истечении максимум трех дней необходимо провести перевязку, удалить гидрогель с поверхности раны, и вместе с ним размягченные некрозы и корочки. В случае если в ране остались участки некрозов, ступы, то необходимо гидрогель использовать не однократно до полного очищения раны. Преимуществом применения для этих целей антимикробного гидрогеля Neofix FibroGel AG заключается в том, что этот гидрогель содержит в своем составе серебро. Этот антимикробный компонент борется с любыми возбудителями инфекции в ране. В результате применения гидрогелей рана очищается. Перевязки необходимо проводить не реже одного раза в 1-3 суток, и лучше под наблюдением лечащего врача.
Необходимо подавить инфекцию
Для борьбы с инфекцией в ране лучше всего использовать повязки ACTICOAT и ACTICOAT7. Это сетчатые абсорбирующие повязки, которые осуществляют беспрепятственный отток экссудата из раны и борются с инфекцией. Данные повязки содержат серебро. Антибактериальная активность серебра известна уже в течение многих лет и его эффективность не вызывает сомнений. На активность серебра не влияет присутствие крови и гноя в ране. Все возбудители раневой инфекции, в том числе бактерии устойчивые к антибиотикам, не обладают устойчивостью к серебру. Серебро обладает универсальным широким спектром действия, в том числе против смешанной микрофлоры, содержащей различные бактерии, грибы, дрожжи. Применение повязок с серебром ведет к быстрому подавлению воспалительной реакции в ране, и вместе с этим уменьшается количество отделяемого экссудата.
Важно, что серебро в повязках ACTICOAT и ACTICOAT7 начинает высвобождаться сразу же как только повязку наложили на рану, и быстро, в течении первых 30 минут, в ране достигается необходимая концентрация серебра для борьбы с инфекцией, и эта концентрация серебра поддерживается на постоянном уровне в течении длительного времени - до 3 дней при применении повязок ACTICOAT и до 7 дней при применении повязок ACTICOAT7, обеспечивая тем самым длительную антибактериальную активность повязок, поэтому повязка ACTICOAT может быть на ране до 3 дней, а повязка ACTICOAT7 до 7 дней, при этом внешние абсорбирующие повязки (марлевые или губчатые Allevyn) необходимо менять ежедневно.
Используйте актикоатную повязку для эффективной борьбы с инфекцией.
Излишки экссудата
Если в ране нет корок, некрозов, то для активного оттока экссудата может быть применена методика локального отрицательного давления. Для этих целей применяют аппарат для лечения ран PICO, который создает постоянный отток гнойного экссудата из раны, что сопровождается уменьшением отека тканей, уменьшением количества бактерий в ране, в результате воспалительная реакция затухает, и начинается рост новых тканей, сосудов, которые заполняют рану, начинает расти эпителий, края раны постепенно сближаются и рана заживает. При применении данного аппарата нет необходимости проводить перевязки ежедневно. Смену повязок достаточно проводить в среднем 1 раз в три дня.
- Carbonet. Это многослойная повязка отлично впитывает вязкий гнойный экссудат, и, благодаря слою из активированного угля абсорбирует запах, который часто сопровождает гнойные раны. Так как Carbonet не содержит антимикробных компонентов, то на гнойных ранах необходимо менять повязки ежедневно.
- Губчатые повязки из полиуретана NEOFIX с серебром - NEOFIX FibroSorb AG и NEOFIX FibroSorb AG Sacrum. Серебро в повязках обеспечивает антимикробное действие.
При использовании для лечения ран повязок NEOFIX FibroSorb AG и NEOFIX FibroSorb AG Sacrum нет необходимости проводить перевязки ежедневно. Смена повязки рекомендуется проводить 1 раз в 2-3 дня в зависимости от степени наполнения повязки экссудатом.
Оптимальная среда для заживления
По мере очищения раны степень экссудации уменьшается, снижается отек тканей, уходит краснота и боль. В этот момент важно создать благоприятную среду, которая будет стимулировать рост грануляций и эпителия, и при этом важно обеспечить защиту раны от инфекции. Для этих целей необходимо применять гидроколлоидные повязки, например NEOFIX Fibrocold Ag, или сетчатые повязки NEOFIX Fibrotul Ag, Bactigras.
Гидроколлоидные повязки NEOFIX Fibrocold Ag имеют неоспоримое преимущество перед гидроколлоидными повязками других производителей - это наличие в повязке активного антимикробного компонента – серебра. Повязка NEOFIX Fibrocold Ag необходимо накладывать на рану со слабой экссудацией. Гидроколлоиды в повязке впитывают экссудат и образуют на поверхности раны гель, который создает оптимальную влажную среду на поверхности раны, при этом серебро оказывает профилактический и лечебный антимикробный эффект. Экссудат раны не изливается на окружающую кожу, а впитывается гидроколлоидами, тем самым обеспечивая защиту окружающей кожи. Внешняя сторона повязки представляет из себя пленочку, которая защищает рану от проникновения воды и бактерий извне. Повязка стимулирует рост грануляций и эпителия, способствует заживлению раны.
Ещё одно из преимуществ гидроколлоидной повязки NEOFIX Fibrocold Ag состоит в том что нет необходимости в ежедневных перевязках, такая повязка может находиться на ране до 7 дней в зависимости от клинической ситуации.
Основное свойство сетчатых повязок NEOFIX Fibrotul Ag и Bactigras это их атравматичность, т.е. эти повязки сменяются без последствий, в отличии от обычных марлевых повязок, которые прилипают к поверхности раны и при последующих перевязках их сложно снять не отрывая новообразованные грануляции и эпителий, поэтому марлевые повязки необходимо отмачивать перед заменой.
При применении сетчатых специализированных повязок NEOFIX Fibrotul Ag и Bactigras в этом нет нужды, т.к. повязки никогда не прилипают к ране, если следовать инструкции производителя и рекомендациям лечащего врача. Сетчатые повязки защищают рану от пересыхания, способствуют поддержанию оптимальной умеренной влажной среды для заживления раны. Кроме того, сетчатые повязки препятствуют скоплению экссудата на поверхности раны, они обеспечивают свободное прохождение выделения из раны в абсорбирующую повязку, что является очень важным, т.к. скопившейся экссудат служит питательной средой для микроорганизмов, и может привести к развитию инфекции в ране.
Повязка Bactigras содержит антисептик хлоргексидина ацетат, а сетчатая повязка NEOFIX Fibrotul Ag содержит серебро, антимикробное действие которого мы рассматривали выше. Хлоргексидина ацетат также обладает широким спектром антимикробного действия против возбудителей раневой инфекции.
Эти две повязки особенно актуально применять для профилактики появления инфекции в ране либо при начальных её проявлениях.
Поверх сетчатых повязок необходимо накладывать впитывающие повязки, например, несколько стерильных марлевых повязок, и фиксировать повязки бинтом. Марлевые повязки необходимо менять ежедневно. Сетчатые повязки можно использовать более долгий срок – до 7 дней.
Сетчатые повязки отлично себя зарекомендовали для лечения ран после проведения аутодермапластики (трансплантации кожи): донорских участков и для приживления пересаженного участка кожи. Повязки находятся на раневой поверхности и не прилипают к ней, а значит не травмируют рану при перевязках, перевязки не сопровождаются кровотечением и безболезненные.
Также преимуществом сетчатых повязок NEOFIX Fibrotul Ag и Bactigras является то, что волокна этих повязок не рвутся, волокна в ране не остаются. При применении обычных марлевых салфеток существует опасность оставления в ране волокон марли, что может привести к воспалительной реакции.
Сетчатые повязки очень гибкие, мягкие, их легко наложить на поверхность раны, в том числе на рану со сложным рельефом, на труднодоступные места, на сложные анатомические области, такие как пальцы, суставы, сгибы.
Повязки NEOFIX Fibrotul Ag и Bactigras имеют кроме стандартных размеров, ещё большие размеры 15 смх100 см, что особенно актуально для лечения больших ожоговых ран.
Таким образом, большое разнообразие перевязочных средств обеспечивает эффективность лечения гнойных ран как в домашних условиях, так и в условиях медицинских учреждений. Однако, лечение обширных гнойных ран должно происходить обязательно под наблюдением врача.
Читайте также:

