Может ли быть герпес в пищеводе
Обновлено: 29.04.2024
Эзофагит — это воспаление и раздражение пищевода. Причиной эзофагита, как правило, является кислотный рефлюкс, но он также может быть результатом герпесной инфекции. Пищевод — это трубка, которая начинается в задней части горла и является частью пищеварительной системы. Он несет пищу и жидкости от рта до желудка. Наиболее распространенной причиной эзофагита является изжога. Иногда бактериальные, вирусные и грибковые инфекции также могут вызывать эзофагит.
Когда это состояние возникает в результате заражения вирусом простого герпеса, или по другому ВПГ, его называют герпетический эзофагит (герпес-эзофагит). Этот тип эзофагита обычно встречается только у людей с ослабленной иммунной системой.
В этой статье мы рассмотрим симптомы, причины и факторы риска герпетического эзофагита.
Симптомы
Герпетический эзофагит может вызвать боль при глотании и возникновение ран в задней части горла.
Герпетический эзофагит вызывает воспаление и раздражение в пищеводе, что может вызвать такие симптомы, как:
- боль или затруднение при глотании;
- тошнота;
- изжога или боль в груди;
- лихорадочные симптомы;
- язвы в задней части горла или внутри или вокруг рта.
Язвы во рту называются герпес-лабиалис или оральный герпес.
Люди с оральным герпесом, как правило, испытывают вспышки герпеса, которые появляются и пропадают на протяжении всей их жизни.
Причины
ВПГ вызывает герпетический эзофагит. Существует два основных штамма ВПГ:
- ВПГ-1 является основной причиной орального герпеса, но он также может привести к генитальному герпесу. ВПГ-1 обычно передается через оральный путь, но человек может также передавать его через оральный секс.
- ВПГ-2 является основной причиной генитального герпеса, но также может вызывать оральный герпес. Люди обычно передают ВПГ-2 через вагинальный, анальный и оральный секс.
Оба типа ВПГ очень заразны, и заражение этим вирусом очень распространено.
Согласно Центрам по контролю и профилактике заболеваний (CDC) , в Соединенных Штатах в 2015-2016 годах:
- 47,8% людей в возрасте от 14 до 49 лет имели ВПГ-1;
- 11,9% людей в возрасте от 14 до 49 лет имели ВПГ-2.
Оба типа ВПГ могут вызывать герпетический эзофагит, но ВПГ-1 является наиболее распространенной причиной заболевания. Однако герпетический эзофагит редок и зачастую развивается у людей с ослабленной иммунной системой.
Герпетический эзофагит обычно возникает, когда ВПГ реактивируется и распространяется из других областей тела, например, через блуждающий нерв или рот в пищевод.
Факторы риска
Человек, подвергающийся химиотерапии, может иметь повышенный риск развития герпесного эзофагита. Человек может заразиться ВПГ через прямой контакт с ранами, пораженной кожей или физическими жидкостями через кого-то, у кого есть вирус. Инфекция является наиболее заразной во время или непосредственно перед вспышкой симптомов.
Однако заражение ВПГ обычно не приводит к герпесному эзофагиту. Основным фактором риска для этого состояния является ослабленная иммунная система в случае:
- ВИЧ, лейкемии и лимфомы;
- химиотерапии при лечении рака;
- приема иммунодепрессантов для, к примеру, трансплантации органов или костного мозга.
Диагностика
Чтобы диагностировать герпесный эзофагит, врач начинает изучать историю болезни человека и наблюдать симптомы. Врач также может осмотреть рот и горло. Несмотря на то, что состояние встречается редко, герпетический эзофагит обычно диагностируется, когда симптомы возникают у человека с ослабленной иммунной системой.
Дальнейшие тесты показаны для подтверждения диагноза врача и могут помочь различать типы эзофагита. Эти тесты могут включать:
- Анализы крови для проверки наличия вирусов и исключения других состояний;
- Эндоскопия для осмотра пищевода на предмет наличия воспаления и язв;
- Биопсия, которая включает взятие образца ткани из пищевода и анализ ее под микроскопом. Врачи могут взять образец во время эндоскопии.
У людей со здоровой иммунной системой герпетический эзофагит обычно излечивается сам по себе в течение 1-2 недель . Для людей с ослабленной иммунной системой врач может назначить пероральные противовирусные препараты, такие как:
- ацикловир;
- фамцикловир;
- валацикловир.
Если эти методы лечения не увенчались успехом, индивидуум может заразиться лекарственно-устойчивым штаммом ВПГ. В этом случае врачи могут назначить внутривенный противовирусный препарат, называемый фоскарнет . Врач может также рекомендовать болеутоляющие средства для тех, кто испытывает значительный дискомфорт. Изменения образа жизни могут быть необходимы, если глотание становится слишком болезненным и трудным. Они могут включать:
- прекращение курения;
- исключение продуктов питания, напитков или лекарств, вызывающих симптомы;
- исключение алкоголя и кофеина;
- дробное питание;
- удерживание головы выше уровня ног во время сна, например, подняв головную часть кровати.
Профилактика
Использование презерватива во время сексуальной активности может помочь предотвратить распространение ВПГ.
ВПГ — очень заразная и распространенная инфекция. Человек может снизить риск заражения или передачи вируса:
- использование презерватива или стоматологической плотины во время секса;
- избегая контакта рта-в рот или орального секса во время оральной вспышки герпеса;
- избегая полового контакта во время генитальной вспышки герпеса;
- не касаясь язв во время вспышки.
Выводы
Герпетический эзофагит — редкий вид эзофагита, который является результатом инфекции ВПГ. Это заболевание обычно развивается только у людей с ослабленной иммунной системой. Лечение герпесного эзофагита включает противовирусные препараты.
Авторы другого исследования утверждают, что вирус герпеса поможет в лечении рака кожи.
Перед применением советов и рекомендаций, изложенных на сайте «Medical Insider», обязательно проконсультируйтесь с врачом!


Учредитель сетевого издания (Medical Insider), главный редактор, автор статей.
Врач ультразвуковой диагностики в СЗЦДМ, травматолог-ортопед, г. Санкт-Петербург
Клиника и диагностика поражений вирусом простого герпеса при иммунодефиците
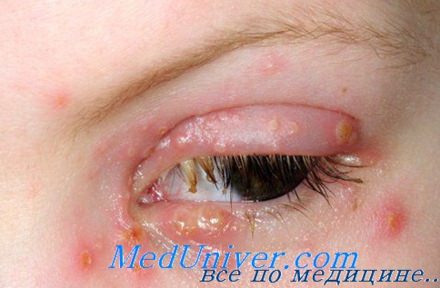
Поражение лица и ротоглотки наиболее типично для реактивации герпесвирусной инфекции. Морфология герпетических высыпаний зависит от типа пораженной эпителиальной ткани. На красной кайме губ и коже лица первичными элементами являются мелкие везикулы, которые возникают последовательно, имеют тенденцию к быстрому слиянию и формированию крупного вялого пузыря. Эти элементы умеренно болезненны, типично ощущение жжения.
После отторжения некротизированного эпителия обнажаются эрозированные кровоточащие поверхности, по краям которых появляются новые мелкие везикулы, и элемент начинает расти от центральной части к периферии.
Суперинфицирование элементов часто приводит к возникновению глубоких некрозов, заживающих с формированием рубца. Поражение лица вирусом герпеса следует дифференцировать от поражения зигомицетами (Absidia, Rhisopus, Mucor) и Aspergillus, которые вызывают тяжелые некрозы тканей лица, расплавление хрящей и костей лицевого скелета с быстрым обезображиванием внешнего облика пациента.
На слизистой оболочке рта наиболее типичным является возникновение нескольких одинаковых поверхностных некротических элементов диаметром 1—3 мм, которые затем углубляются и увеличиваются в размерах, часто сливаются. В самых тяжелых случаях значительная площадь полости рта поражена крайне болезненными глубокими некрозами серого цвета с кровоточащими участками эрозий.
В прошлом, до введения всеобщей профилактики ацикловиром, у больных после ТКМ герпетические поражения ротоглотки нередко становились причиной обструкции верхних дыхательных путей, в связи с чем возникала необходимость в протективной интубации трахеи.
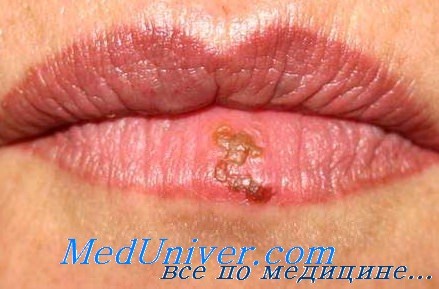
Герпетические элементы практически всегда суперинфицируются разнообразной оральной флорой: грибами рода Candida, стрептококками, фузобактериями и другими анаэробами, реже грамотрицательными бактериями, особенно стремительно в условиях нейтропении. Для практики полезно считать, что при нейтропении не бывает изолированных герпетических поражений полости рта, и стоматиты, объединяемые клиницистами под термином «герпетические», всегда являются результатом комбинированного вирусно-бактериально-грибкового поражения.
Стоматиты чаще всего возникают на фоне тяжелой нейтропении, обратное развитие претерпевают только по выходе из агранулоцитоза, полностью регрессируя через 5—12 дней после нормализации числа гранулоцитов. Заживление элементов всегда происходит от краев к центру — симптом «высыхающей лужи».
Процесс заживления глубоких некрозов часто проходит стадию отторжения фибриновых пленок с обнажением ригидных сосудов десен, что может быть чревато значительной кровопотерей, особенно у детей младшего возраста. Мы наблюдали кровотечения из язв на деснах в объеме до 400 мл в сутки. Кроме того, заживление язв нередко сопровождается обильной саливацией: потерей до 700—900 мл слюны в сутки, что может стать причиной обезвоживания у детей.
Знание закономерностей развития герпетического стоматита позволяет сделать вывод, что при нейтропении лечение его нельзя ограничивать ацикловиром: необходимо назначать препараты, активные в отношении стрептококков, анаэробов, грамотрицательной флоры и грибов. Монотерапии, отвечающей таким требованиям, не существует, поэтому при фебрильной нейтропении, сопровождающейся стоматитом, мы наряду с ацикловиром всегда используем бета-лактам с расширенным спектром антианаэробной активности (пиперациллин/тазобактам, имипенем, амоксициллин/клавуланат) либо к другим бета-лактамам добавляем метронидазол.
Часто драматического улучшения удается добиться при использовании клиндамицина или пенициллина. Кроме того, мы рекомендуем и сами всегда используем системную противогрибковую терапию.
Поражение вирусом простого герпеса пищевода
При распространении инфекции из полости ротоглотки поражается верхний сегмент пищевода. Другой путь — контаминация инфицированной герпес-вирусом слюной эрозированного (в результате желудочно-пищеводного рефлюкса или рвоты) пищевода. В этом случае поражается нижний сегмент пищевода. Клиническая картина среднего и дистального эзофагита очень типична: больные жалуются на ощущение кома за грудиной, сильное жжение и боли, которые значительно усиливаются после глотания и рвоты.
Следует отметить, что последняя локализация — одно из самых опасных проявлений герпесвирусной инфекции, поскольку именно дистальный эзофагит служит воротами для развития инвазивных бактериальных и грибковых инфекций. По морфологической картине (язвенно-некротические элементы, захватывающие все слои пищевода) отличить герпетическое поражение от цитомегаловирусного, бактериального или грибкового не представляется возможным. Без проведения биопсии установить точный микробиологический диагноз невозможно.
Если принято решение выполнить эзофагоскопию и биопсию, то для диагностики герпес-вирусного поражения необходимо получить биоптат эпителия края язвы, а для диагностики ЦМВ-поражения — ее дна. Это связано с тем, что герпес-вирус поражает эпителий, а цитомегаловирус — строму.
При герпетическом эзофагите, как и при герпетическом стоматите, особенно больным с фебрильной нейтропенией, наряду с ацикловиром всегда следует назначать антимикотик системного действия (амфотерицин В внутривенно в дозе 0,3—0,5 мг/кг в сутки, флюконазол внутривенно или внутрь, возможно вориконазол и итраконазол) и системные антибиотики, обладающие антианаэробной активностью.
Важную роль играют антацидная и антирефлюксная (ранитидин или омепразол, дофаминовые антагонисты) терапия и адекватное обезболивание наркотиками.
Поражение бронхиального дерева и легких вирусом простого герпеса
Чаще всего герпетический трахеобронхит развивается у иммунокомпрометированных больных с герпетическим эзофагитом, которые интубированы и находятся на искусственной вентиляции легких. Наблюдаются также фокальные герпетические пневмонии. Диффузные пневмонии с развитием дыхательной недостаточности, напротив, являются следствием диссеминированной герпетической инфекции у больных с глубоким дефицитом клеточного или гуморального иммунитета.
Поражение вирусом простого герпеса центральной нервной системы
Герпетический энцефалит — очень редкое проявление реактивации герпесвирусной инфекции у онкогематологических больных. Он не отличается от энцефалита у иммунокомпетентного хозяина, т. е. характеризуется энцефалитическим синдромом и признаками воспаления и некроза на компьютерных и ядерно-магнитных томограммах. Поражение спинного мозга вирусом герпеса является казуистикой. Описаны случаи восходящего поперечного миелита.
Диагностика поражений вируса простого герпеса
Известно несколько методов быстрой и специфической диагностики герпесвирусной инфекции. Классическим методом является выделение вируса, основанное на его цитопатическом действии на чувствительные культуры клеток млекопитающих. Этот метод достаточно быстрый (90 % позитивных результатов в первые 3 дня, 100% —в первые 7 дней культивирования) и весьма специфичный.
Существует более быстрый метод (комбинация иммуноферментного и культурального методов), которым выявляют наличие вирусных антигенов в чувствительной клеточной культуре, зараженной исследуемым материалом. Этот метод аналогичен описанному ранее методу shell vial для ЦМВ и позволяет получить результаты в течение суток.
Следует отметить, что, как и при ЦМВ-инфекции, серологические данные (наличие специфического IgM или повышение титра IgG) и выделение вируса простого герпеса со слюной не несут полезной оперативной информации. Особенно важно это при диагностике герпесвирусного энцефалита. Нам доводилось наблюдать неадекватную интерпретацию серологических тестов у больных с энцефалитическим синдромом и необоснованное назначение ацикловира в высоких дозах. Единственным надежным методом диагностики является проведение биопсии ткани головного мозга и вирусологического исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Герпетический эзофагит входит в группу инфекционных эзофагитов, к которым также относятся кандидозный эзофагит и цитомегаловирусный эзофагит.
Как правило, большинство случаев эзофагита связано с неинфекционными причинами, в основном с гастроэзофагеальной рефлюксной болезнью. Если выявляется инфекционный эзофагит, то следует прежде всего думать, что у данного пациента имеется то или иное нарушение иммунитета.

Полный текст статьи:
Как правило, этиологический фактор – ВПГ (вирус простого герпеса) типа 1, хотя сообщалось и о ВПГ типа 2.
- · Нарушения иммунитета,
- · Трансплантации органов,
- · Пересадка костного мозга [5, 10].
Герпетический эзофагит является в основном следствием реактивации ВПГ с распространением вируса в пищевод:
- · через блуждающий нерв или
- · путем прямого проникновения инфекции из полости рта в пищевод.
- · Одинофагия и/или дисфагия,
- · Лихорадка и загрудинная боль - в 50% случаев,
- · Возможны сопутствующие herpes labialis или язвы ротоглотки.
Диагноз герпетического эзофагита основывается, как правило, на заключении эндоскопического исследования, выводы которого подтверждаются гистологически.
- · Поражения, обычно в виде неглубоких изъязвлений менее 2 см в диаметре, вовлекают слизистую оболочку средне- и нижнегрудного отделов пищевода.
- · Эти язвы четко отграничены от окружающей слизистой оболочки и имеют вид «кратера», покрытого желтоватым налетом, могут располагаться цепочкой; кроме того, может выявляться циркулярный эрозивный эзофагит.
- · Биоптаты должны быть взяты из края изъязвления, где скорее всего будут наблюдаться признаки вирусного цитопатического действия.
- · При гистологическом исследовании отмечаются многоядерные гигантские клетки с ядрами в виде «матового стекла» и эозинофильными включениями.
- · Дополнительное обследование может предусматривать иммуногистохимический анализ на гликопротеины ВПГ [6].
Эндоскопическая классификация герпес-эзофагита:
Описание: мелкие штампованные дефекты с приподнятыми краями и желтоватым налетом

Описание: мелкие штампованные дефекты без приподнятых краев и без характерного желтоватого оттенка
Описание: множественные сливающиеся язвенные дефекты
Лечение при ВПГ-эзофагите зависит от патологии, лежащей в основе иммунного дефицита.
Пациенты без нарушения иммунитета:
Спонтанное выздоровление чаще всего наблюдается в течение 1–2 недель у больных без нарушения иммунитета, хотя некоторые из них могут реагировать более быстро, если приступить к терапии с короткого курса перорального применения ацикловира 200 мг 5 раз в сутки или по 400 мг 3 раза в день в течение 1–2 недель [6, 11].
Пациенты с нарушениями иммунитета:
- · Такие пациенты должны получать лечение, начиная с курса перорального приема ацикловира 400 мг 5 раз в день в течение 2–3 недель.
- · Может быть также назначен фамицикловир 500 мг 3 раза в день или
- · валацикловир по 1 г 3 раза в сутки.
- · Больным с тяжелой одинофагией может потребоваться госпитализация для парентерального введения ацикловира 5 мг/кг 3 раза в день в течение 1–2 недель. Тех, кто демонстрирует быстрое улучшение, можно перевести на пероральную терапию.
Отсутствие эффекта от вышеописанного лечение:
Пациенты, которые не реагируют на лечение, вероятно, заражены штаммом вируса, устойчивого к воздействию ацикловира в результате мутаций в генах тимидинкиназы или ДНК-полимеразы ВПГ. Вирусы с мутациями тимидинкиназы, как правило, обладают перекрестной устойчивостью к другим препаратам этого класса. В этом случае вариантом может быть терапия фоскарнетом [6].
Вам может быть интересно:
Список литературы:

Поражение толстой кишки, обусловленное вирусами семейства Herpesviridae.
Аникина М.С. врач-эндоскопист ГБУЗ НСО «ГНОКБ»
Распространенность герпесвирусных инфекций неуклонно возрастает во всем мире. Считается, что к 18 годам 60 - 90% жителей городов инфицируются одним или несколькими типами клинически значимых герпесвирусов. Рост заболеваемости в значительной мере связан с распространением бессимптомной и недиагностированной герпетической инфекции. Это вызвано легкостью распространения инфекции (возможны контактно-бытовой, половой, воздушно-капельный, вертикальный, трансфузионный и трансплантационный механизмы передачи). Универсальный тропизм герпесвирусов обусловил значительный полиморфизм клинических проявлений, которые попадают в поле зрения врачей различных специальностей. [5]
В настоящее время известно около 200 в разной степени изученных герпесвирусов. Это крупные оболочечные ДНК-содержащие вирусы. Из них патогенными для человека являются 8 типов:
1.Вирус простого герпеса – ВПГ тип 1 (Herpes simplex virus тип 1 – HSV-1), или герпесвирус человека ГВЧ-1.
2. Вирус простого герпеса – ВПГ тип 2 (HSV-2), или ГВЧ-2.
3. Вирус ветряной оспы – опоясывающего герпеса (Varicella-zoster virus – VZV), или ГВЧ-3.
4. Вирус Эпштейна-Барр – ВЭБ (Epstein-Barr virus – EBV), или ВГЧ-4.
5. Цитомегаловирус – ЦМВ (CMV), или ГВЧ-4.
6. Герпесвирус человека тип 6 – ГВЧ-6 (Human herpesvirus – HHV6).
7. Герпесвирус человека тип 7 – ГВЧ-7 (HHV7).
8. Герпесвирус человека тип 8 – ГВЧ-8 (HHV8).
Все они относятся к семейству Herpesviridae, которое делится на три подсемейства: α-herpesviruses, β-herpesviruses и γ-herpesviruses, в зависимости от характера поражения вирусом клетки, скорости репликации, места латенции и персистенции.
Альфа-вирусы (вирус простого герпеса 1 и 2 типа, вирус варицела Зостер). Характеризуются быстрой репликацией, 4—8 часов), способностью к цитолизу и бессимптомным персистированием в нейрональных клетках.
Бета-вирусы (цитомегаловирус, герпесвирус человека тип 6, герпесвирус человека тип 7) Медленно реплицируются, вызывают цитомегалическую трансформацию клеток, а основными очагами латенции являются моноциты и их предшественники, эндотелиальные клетки сосудов микроциркуляторного русла, альвеолярные макрофаги, Т-лимфоциты и стромальные клетки костного мозга.
Гамма-вирусы (вирус Эбштейн-Барр (синоним ВГЧ4), ВГЧ-8). Трансформирующие вирусы человека, способствующие развитию злокачественного перерождения клеток. Пожизненно персистируя в В-лимфоцитах или находясь в латентном состоянии, обладают способностью делать их злокачественными.
Персистенция бета- и гамма-вирусов в иммунокомпетентентных клетках может приводить к развитию вторичной иммунной недостаточности с выраженной депрессией клеточного иммунитета.
Формы взаимодействия герпесвирусов с организмом хозяина различны. Инфекционный процесс может протекать:
1 В острой форме.
2 В хронической форме (более 6 месяцев).
3 В инаппарантной (бессимптомной) форме.
4 В форме медленной вирусной инфекции — длительный инкубационный период (месяцы и годы) с последующим медленным прогрессирующим течением, с развитием тяжелых клинических симптомов и в итоге — смертью больного.
Уникальным биологическим свойством всех ГВ человека является их способность к персистенции и латенции в организме инфицированного человека. Персистенция представляет собой непрерывное и цикличное размножение (репликацию) вируса в инфицированных клетках тропных тканей, что является причиной развития инфекционного процесса. Латенция герпесвирусов клинически себя не проявляет, а диагностируется только при наличии специфических IgG против вируса (серопозитивность) в невысоких титрах, а сам вирус в этот период в периферической крови не определяется даже таким высокочувствительным методом, как ПЦР. В состоянии латенции нарушается полный цикл репродукции вируса, и он находится в клетках хозяина в виде субвирусных структур. [4; 5]
Таблица 1 Классификация клинических форм заболеваний, обусловленных герпесвирусами [4]
Первичная инфекция
Реактивация после латенции
Вирус простого герпеса I типа — ВПГ-1-ВГЧ-1 —
Герпес кожи. Лабиальный герпес. Гингивостоматит. Офтальмогерпес. Генитальный герпес. Неонатальный герпес. Энцефалит (редко). Невропатии
Рецидивирующий орально-лабиальный герпес. Рецидивирующий аногенитальный герпес.
Вирус простого герпеса II типа — ВПГ-2-ВГЧ-2 — HSV-2
Генитально-ректальный герпес. Неонатальный герпес. Менингоэнцефалит. Крестцовый
Генитальный герпес. Менингоэнцефалит. Хроническая кожно-слизистая форма
Вирус варицелла зостер-ВВЗ — вирус герпеса человека III типа — ВГЧ3-VZV
Опоясывающий герпес. Постгерпетическая невралгия
Вирус герпеса человека IV типа — ВГЧ-4 — Эпштейна-Барр вирус —
Инфекционный мононуклеоз. Саркома мышц. Энцефалит у новорожденных. Лимфоидная интерстициальная пневмония у детей
Лимфома Беркитта. Назофарингиальная карцинома.
Волосатая лейкоплакия языка.
EBV-ассоциированный лимфопролиферативный синдром.
Синдром хронической усталости и иммунной депрессии.
Вирус герпеса человека V типа — ВГЧ-5 — Цитомегаловирус — ЦМВ-СМV
CMV-колит/холангит. CMV-адреналовая недостаточность.
Реакция отторжения трансплантата. Атеросклероз
Летальный энцефаломиелит при инфицировании людей
Вирус герпеса человека VI типа —
Внезапная экзантема у детей. Гетерофильно-негативный мононуклеоз. Васкулит
Интерстициальная пневмония у лиц с иммунодефицитом.
Синдром хронической усталости и иммунной депрессии.
Аутоиммунная патология. Психозы
Вирус герпеса человека VII типа — ВГЧ-7-HHV-7
Возможна экзантема у детей
Синдром хронической усталости и иммунной депрессии.
Заболевания кожи и ЦНС аутоиммунной природы. Рак желудка
Саркома Капоши.
Лимфопролеферативное заболевание болезнь Кастлемана
Таким образом, поражение слизистых нижних отделов желудочно-кишечного тракта может быть обусловлено вирусами простого герпеса 1 и 2 типа, цитомегаловирусом (ВГЧ 5 типа) и вирусом герпеса человека 8 типа.
Герпесвирусы 1 и 2 типов
Герпетическая инфекция, вызванная вирусом простого герпеса (ВПГ, Herpes simplex virus — HSV), — это заболевания с пожизненной персистенцией вирусов в нервных клетках (особенно в нервных ганглиях), характеризующиеся периодическими обострениями с появлением клинических признаков, локализующихся на постоянных для каждого больного «Locus minoris» — глаза, кожа, слизистые. Более чем 90 % населения планеты являются носителями ВПГ. Первичная герпетическая инфекция (ГИ) возникает при первом контакте человека с ВПГ. После короткого инкубационного периода (от 2 до 14 дней) в крови начинают определяться антитела к ВПГ, и у 80—90 % лиц первичное инфицирование протекает в латентной форме. У 10—20 % лиц имеют место клинические проявления инфекции, для которых характерен общеинфекционный синдром с лихорадкой и другими признаками интоксикации, респираторные проявления или афтозный стоматит. Возможны поражения кожи и слизистых, в том числе конъюнктивы или роговицы. Первичная ГИ, независимо от клинической формы проявления и места поражения, сопровождается проникновением ВПГ в ганглии дорсальных корешков и реже — в вегетативные ганглии и завершается их острой инфекцией с последующим установлением латентности в нейронах.
Вторичная (рецидивирующая) ГИ встречается в любом возрасте после первичного герпеса. Поскольку рецидивы возникают на фоне наличия противовирусных антител, то они протекают со слабовыраженным общеинфекционным синдромом и, как правило, на фоне болезней и/или состояний, снижающих иммунитет.
В зависимости от распространенности процесса клинически выделяются следующие формы вирусной инфекции:
1. Локализованная форма, при которой отмечается так называемый "замкнутый круг хождения вируса: входные ворота - нервный ганглий - входные ворота". Как правило, при обострении заболевания патологические изменения всегда локализуются в одном месте.
2. Распространенная форма, при которой наблюдаются отсевы вируса из очага первичной инвазии в близлежащие зоны (например, лабиальный герпес – герпетический эзофагит)
3. Генерализованные формы (висцеральная и диссеминированная), которые наиболее часто встречаются у иммунокомпрометированных пациентов.
В течение заболевания выделяют две стадии: 1 стадия - везикулов и 2 стадия - образования дефектов слизистой оболочки.
Макроскопически при 1-й стадии обнаруживаются характерные изменения слизистой оболочки пораженного сегмента толстой кишки: множественные рассеянные или сгруппированные пузырьки диаметром 0,1-0,3 см с серозным или мутным содержимым. Пузырьки склонны к слиянию. Окружающая слизистая оболочка может быть не изменена или с явлениями очагового умеренно выраженного поверхностного воспаления.
При колоноскопии во 2-й стадии заболевания имеются множественные поверхностные дефекты слизистой оболочки округлой формы, размерами до 0,5 см с четко очерченными эритематозными приподнятыми краями и некротическим налетом в дне ("вулканические" изъязвления). При тяжелых генерализованных формах инфекции дефекты слизистой оболочки сливаются с образованием обширной изъязвленной поверхности (Морозова СВ., Пархоменко Ю.Г., 2002). Контактная кровоточивость выражена умеренно, на окружающей слизистой оболочке имеются множественные субэпителиальные кровоизлияния. При морфологическом исследовании тканей, взятых из краев изъязвления, на фоне воспалительной инфильтрации слизистой оболочки выявляются типичные для этой инфекции гигантские клетки с мультинуклеацией и феноменом "глаза совы" или (в более поздние сроки) внутриядерные включения, окруженные светлой зоной (Cirillo N.W. et al., 1993). Таким образом, для герпетических колитов характерны следующие эндоскопические признаки: поражение имеет сегментарный характер, сегменты короткие, могут локализоваться в любом анатомическом отделе, но чаще обнаруживаются в прямой кишке. Макроскопические изменения в пределах пораженного сегмента однородны. (Рис.1) При хроническом прогрессирующем течении заболевания отмечаются протяженные поражения толстой кишки с элементами герпетического процесса на разных стадиях его развития. [3: 9]
Рис.1 герпетический проктит [9]
Эндоскопическая картина слизистой оболочки прямой кишки. (а) эритема, рыхлость и множественные язвенные поражения слизистой оболочки прямой кишки. (B) кроме множественных язв на поверхности слизистой присутствует слизисто-гнойный экссудат.
Клинически распознавание герпетической инфекции в типичных случаях основывается на выявлении характерной сыпи в виде группы мелких пузырьков на фоне инфильтрирации. Для подтверждения диагноза используют методы выделения вируса и серологические реакции для выявления антител. Внутриядерные вирусные включения можно обнаружить при микроскопии окрашенных по Романовскому-Гимзе соскобов и биоптатов основания везикул. Однако такие включения обнаруживаются лишь у 60% больных герпетической инфекцией. Наиболее чувствительным и достоверным методом является выделение вируса на культуре тканей. Серологические реакции (РСК, реакция нейтрализации) имеют малую информативность. Нарастание титра антител в 4 раза и более можно выявить лишь при первичной инфекции, при рецидивах лишь у 5% больных отмечается нарастание титра. Наличие положительных реакций без динамики титров можно выявить у многих здоровых людей (за счет латентной герпетической инфекции). Важно одновременно использовать несколько методов диагностики. В качестве скринингового метода рекомендуется использовать метод ПЦР, иммуноферментный анализ (ИФА) и реакцию иммунофлюоресценции (РИФ), а в качестве подтверждающего — метод выделения ВГ на чувствительных клеточных культурах. Вирусологический метод является «золотым стандартом» в диагностике ГВИ. Отличительной особенностью данного метода является высокая степень достоверности полученных результатов, а также высокая чувствительность (85— 100 %) и специфичность (100 %), возможность получения чистой культуры возбудителя для его дальнейшего изучения, в частности испытания чувствительности к антивирусньм препаратам; недостатком — длительность проведения (от 2 до 5—14 дней). [2; 4]
ЦИТОМЕГАЛОВИРУСНАЯ ИНФЕКЦИЯ
Цитомегаловирусная инфекция (ЦМВИ) — общее инфекционное заболевание, вызываемое β -герпесвирусом человека, характеризующееся многообразием форм (от бессимптомных до генерализованных), морфологически проявляющееся образованием в слюнных железах, висцеральных органах и ЦНС цитомегалов — гигантских клеток с типичными внутриядерными и цитоплазматическими включениями. Инфекция относится к антропонозам. Отличается различными механизмами передачи: капельный, гемоконтактный, контактный. Пути передачи: воздушно-капельный; артифициальный (парентеральный); контактно-бытовой (в том числе при непосредственном контакте со слюной); половой; вертикальный, трансфузионный, трансплантационный. Иммунитет нестойкий, нестерильный. Механизм развития ЦМВИ зависит от дозы вируса, путей заражения, возраста пациента, генетических особенностей и состояния иммунитета в момент заражения.
При персистенции ЦМВ выделяют две стадии: стадию продуктивной репликации и стадию латенции. Обе стадии персистирующей инфекции не являются стабильными в течение жизни человека, сменяя одна другую. В популяции не менее 10 % населения являются вирусовыделителями. Реактивация ЦМВИ обычно не сопровождается какими-либо симптомами и для организма человека протекает незаметно.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Поражения пищевода вирусами простого герпеса или опоясывающего лишая встречаются нечасто и обычно протекают при одновременном поражении различных участков кожи и слизистых оболочек. В редких случаях герпетический эзофагит возникает в изолированном виде.

[1], [2], [3], [4]
Код по МКБ-10
Симптомы герпетического эзофагита
Симптомы герпетического эзофагита схожи с признаками банального катарального эзофагита и сопровождаются симптомами общей герпетической инфекции (внезапное начало, озноб, лихорадка, иногда судороги). Через 24-48 ч выраженность этих явлений значительно снижается или они полностью исчезают. Взамен появляются местные признаки герпетических поражений на коже, слизистой оболочке глотки и пищевода. Последние по клиническим проявлениям доминируют - боль при прохождении пищевого комка по пищеводу, дисфагия, иногда отрыжка слизью с примесью крови.
Где болит?
Диагностика герпетического эзофагита
Диагноз герпетического эзофагита устанавливают по наличию герпетических поражений кожи, слизистой оболочки глотки и при фиброэзофагоскопии. Герпетические поражения слизистой оболочки пищевода проявляются в виде везикул с фестончатыми краями, обладающих тенденцией к слиянию, наполненных серозной жидкостью желтоватого цвета. Везикулы замещаются язвами, дно которых покрыто желтоватым ложно-пленчатым налетом. Эти поражения слизистой оболочки пищевода сходны с теми, которые возникают на слизистой оболочке полости рта и глотки, что способствует диагностике гриппозного эзофагита. Герпетические высыпания на слизистой оболочке пищевода могут повторяться с небольшими интервалами, постепенно увеличивающимися, а число высыпаний при этом уменьшается.

[5], [6], [7], [8], [9], [10], [11], [12], [13]
Читайте также:

