Гематома после стентирования что делать
Обновлено: 27.04.2024
В работе проведен анализ методов лечения 87 больных с ложной аневризмой и пульсирующей гематомой периферических артерий после рентгенэндоваскулярных вмешательств. Всем пациентам с пульсирующей гематомой лечение начиналось с локальной компрессии давящей по
Methods of treatment of pulsating hematoma and false aneurysm peripheral arteries after endovascular interventions Yu. A. Vinogradova, L. S. Kokov, I. P. Mikhailov, V. P. Kiryuschenkov, E. V. Troshkina
87 cases of peripheral artery false aneurysm and pulsating hematoma after endovascular interventions were analyzed. For all patients with pulsating hematoma, the treatment began with local compression with a pressure bandage. The compression efficiency was 89.2%. Attempts of local compression in patients with false aneurysms were not successful and all the patients were operated. Surgical treatment was effective in 100% of false aneurysm cases. The effectiveness of treatment was influenced by: the patient’s intake of anticoagulant and disaggregant drugs, constitutional features of the patient, arterial hypertension, localization and diameter of the post-puncture artery defect. Definitions of pulsating hematoma and false aneurysm of peripheral arteries are formulated.
Эндоваскулярные вмешательства, несмотря на ряд преимуществ перед открытым хирургическим лечением, являются инвазивными методиками и предполагают такие осложнения, как пульсирующие гематомы и ложные аневризмы периферических сосудов, причем их количество увеличивается пропорционально распространению ангиографических методов диагностики и лечения [1, 3–7]. По данным литературы в структуре местных осложнений после пункции артерии ложные аневризмы занимают 60–80% [5]. Для снижения частоты осложнений в настоящее время чаще используют трансаксиллярный, трансбрахиальный и трансрадиальный доступы, ушивающие инструменты. Однако и при таких доступах и развитии эндоваскулярных технологий отмечены повреждения пунктируемой артерии [4–7]. На сегодняшний день актуальными видами лечения пульсирующих гематом и ложных аневризм являются хирургический и компрессионный методы с различными их модификациями [1, 3–5].
Цель работы: проанализировать результаты хирургического и компрессионного методов лечения ложных аневризм и пульсирующих гематом периферических артерий после эндоваскулярных вмешательств.
Материалы и методы исследования
Проанализированы результаты лечения 87 больных с пульсирующими гематомами и ложными аневризмами, находившихся в институте им. Н. В. Склифосовского с 2010 г. по январь 2018 г., в возрасте от 40 до 83 лет. У всех пациентов причиной патологии являлись эндоваскулярные вмешательства, 69 (79,3%) из которых выполнены в других лечебных учреждениях, с последующим поступлением по экстренным показаниям в сроки после манипуляций от 4 суток до 2 месяцев. Большая часть ложных аневризм (23 (88,5%) из 26 случаев) выявлена у пациентов с выполненными эндоваскулярными вмешательствами на коронарных артериях, причем у 14 (53,8%) больных с ложной аневризмой из 23 пациентов было выполнено стентирование коронарных артерий на фоне приема дезагрегантных препаратов (клопидогрел (Плавикс)).
Локализация повреждения: бедренная артерия в 75 случаях (86,2%), подмышечная артерия — 9 (10,3%), плечевая артерия — 2 (2,3%), в одном случае лучевая артерия. Из подтвержденной сопутствующей патологии артериальная гипертензия отмечена у 79 пациентов (90,8%); ожирение II–III степени у 21 (24,1%); сахарный диабет 2 типа средней тяжести у 25 (28,7%); атеросклеротический постинфарктный кардиосклероз у 44 пациентов (50,6%). Атеросклероз артерий нижних конечностей (гемодинамически значимые стенозы/окклюзия поверхностной бедренной артерии) выявлен у 38 больных (43,7%). Прием антикоагулянтных (варфарин, Ксарелто) и дезагрегантных препаратов (клопидогрел (Плавикс, Зилт)) до эндоваскулярных вмешательств отмечен у 61 (70,1%) пациента из 87.
Диагноз ложной аневризмы был установлен 26 (29,9%) больным, пульсирующей гематомы — 61 (70,1%).
При опросе пациентов при поступлении и первичном осмотре обращали внимание на наличие болезненности и припухлости в области выполненной пункции, пульсирующего образования и изменения кожных покровов над ним, систолического шума в области образования. При анализе анамнеза каждого пациента уделяли внимание таким моментам, как давность и объем эндоваскулярного вмешательства; сроки пребывания в стационаре. Ультразвуковое исследование было первым и основным этапом инструментального обследования пациентов. Исследование проведено на ультразвуковой системе Philips iU 22 мультичастотными линейными датчиками L9 — 3 МГц, L15 — 7 МГц.
Под пульсирующей гематомой понимали пульсирующее опухолевидное образование (до 3,0 см в диаметре) в области пункции с экхимозом и болью в области пункции в сроки от 2–5 суток после вмешательства или ограниченное/диффузное выпячивание сосудистой стенки либо полость, образовавшуюся около стенки сосуда, сообщающуюся с ее просветом в сроки от 2 до 5 суток после манипуляции. Постпункционной ложной аневризмой считали патологическую полость в окружающих тканях, образовавшуюся путем организации околососудистой гематомы вследствие дефекта артериальной стенки и сообщающейся с просветом артерии, в сроки после 17 дней с момента манипуляции.
Результаты исследования
Открытое хирургическое лечение выполнено 31 (35,6%) больному, из них 26 пациентов с ложной аневризмой (рис. 5–6) и 5 с пульсирующей гематомой. Сроки выполнения реконструктивной сосудистой операции варьировались от 1 часа до 7 суток. Структура оперативных вмешательств: сосудистый шов артериального дефекта — 28 (90,3%); реконструкция артерии — 3 (9,7%). У всех пациентов удалось добиться восстановления целостности сосуда.
На исход лечения влияли: прием дезагрегантных и антикоагулянтных препаратов и их дозировка до и после эндоваскулярных вмешательств; конституциональные особенности больного, артериальная гипертензия, атеросклеротическое поражение артерии. Положительный исход компрессионного лечения зависел также от величины дефекта артерии, который оценивали по данным ультразвукового метода. При размере дефекта 1–2 мм положительный результат у 46 (92%), при размере 2,1–3 мм — у 4 больных (8%). Эффективность оперативного лечения составила 100%. В послеоперационном периоде был один летальный исход вследствие декомпенсации основного заболевания на фоне до- и интраоперацонной кровопотери; у одного пациента развилась ишемическая гангрена нижней конечности (декомпенсированное кровообращение при поступлении (сахарный диабет)); у трех пациентов отмечалась кожная гиперестезия с последующим регрессом симптоматики через один месяц. Несостоятельности кожных швов, нагноений, лимфорреи, кровотечения из послеоперационной раны не было.
Выводы
- Основным и первым методом лечения пульсирующих гематом является локальная компрессия в течение суток с последующим ультразвуковым контролем.
- На эффективность локальной компрессии влияет прием пациентом антикоагулянтных и дезагрегантных препаратов, конституциональные особенности больного, артериальная гипертензия, локализация и диаметр постпункционного дефекта артерии, комплаентность больного.
- Компрессионное лечение эффективно у больных с пульсирующей гематомой при размере дефекта стенки артерии до 2 мм; при размере дефекта артерии более 2 мм результативно хирургическое лечение.
- Открытое хирургическое лечение эффективно в 100% случаев и является основным методом в лечении ложных аневризм периферических артерий.
Литература
- Гавриленко А. В., Синявин Г. В. Лечение ложных ятрогенных артериальных аневризм // Ангиология и сосудистая хирургия. 2005; 135–138.
- Бочаров С. М. Ангиографическая диагностика и эндоваскулярное лечение при травме артерий. Автореф. дис. … канд. мед. наук. М., 2009. 24 с.
- Seidel A. C., Miranda F. Jr., Fregadolli L. V. Atrogenic pseudoaneurysm of axillary artery // Arg. Bras. Cardiol. 2006; 86 (4): 303–305.
- Houlind K., Jepsen J M., Saicu C. et al. Current management of inguinal false aneurysms//J. Cardiovascular. Surg. 2017; 58 (2): 278–283.
- Панфилов Д. С., Козлов Б. Н., Панфилов С. Д. и др. Проблема лечения постпункционных ложных аневризм: компрессионный, хирургический, пункционный подходы // Сибирский мед. журнал. 2012; 27 (1): 39–44.
- Фокин А. А., Киреев К. А., Москвичева М. Г., Киреева Т. С. Профилактика постпункционных ятрогенных ложных аневризм бедренных артерий после коронарных вмешательств при инфаркте миокарда // Ангиология и сосудистая хирургия. 2016; 22 (2): 139–144.
- Михайлов И. П., Исаев Г. А., Коков Л. С. и др. Использование системного тромболизиса для лечения острой ишемии конечностей // Неотложная медицинская помощь. 2015; 2: 32–34.
Ю. А. Виноградова 1
Л. С. Коков, доктор медицинских наук, профессор, член-корреспондент РАН
И. П. Михайлов, доктор медицинских наук, профессор
В. П. Кирющенков
Е. В. Трошкина
ГБУЗ НИИ СП им. Н. В. Склифосовского ДЗМ, Москва
Методы лечения пульсирующих гематом и ложных аневризм периферических артерий после рентгенэндоваскулярных вмешательств/ Ю. А. Виноградова, Л. С. Коков, И. П. Михайлов, В. П. Кирющенков, Е. В. Трошкина
Для цитирования: Лечащий врач № 7/2018; Номера страниц в выпуске: 21-24
Теги: периферические артерии, осложнения, диагностика, стентирование

Операции с установкой стентов считаются наиболее предпочтительным способом интервенционного хирургического лечения патологического сужения сосудов во многих случаях. Этот метод позволяет эффективно бороться с ишемической болезнью сердца и её последствиями, не прибегая к аортокоронарному шунтированию. Но и при выборе стентирования осложнения всё же возможны.
Какие осложнения могут быть после стентирования коронарных артерий и сосудов сердца
Осложнения после стентирования могут возникать как сразу после операции, так и в отдалённом периоде. Непосредственно после имплантации эндопротеза возможно развитие аллергических реакций на лекарственные препараты, используемые во время вмешательства или в течение дальнейших нескольких дней. Некоторые стенты имеют специальные покрытия, включающие в свой состав вещества, действие которых направлено на предотвращение повторного сужения сосуда. У предрасположенных к аллергиям пациентов возможна реакция на их выделение в кровь.
При проведении стентирования сосудов сердца осложнениями могут являться и повторное сужение просвета сосудов, и образование тромбов. Это наиболее часто встречающиеся осложнения, на борьбу и предупреждение которых направлено в настоящее время внимание учёных-медиков. Не исключаются и такие осложнения после стентирования как возникновение перфорации стенок сосуда, развития кровотечения и образования гематом на месте введения катетера или других участках пути прохождения баллона со стентом.
Как избежать осложнений после стентирования сосудов сердца и коронарных артерий
Наиболее склонны к возникновению осложнений после стентирования коронарных артерий пациенты, имеющие различные серьёзные хронические заболевания – патологии почек, сахарный диабет, различные нарушения кроветворительной и свёртывающей функций. К факторам, повышающим риск, можно отнести и пожилой возраст, неудовлетворительное общее состояние организма пациента на момент операции.
Чтобы предупредить развитие при стентировании коронарных артерий осложнений, связанных с вышеперечисленными причинами, ещё на этапе подготовки к операции проводится тщательное обследование состояния здоровья кандидата на проведение ангиопластики. Сюда входит не только оценка состояния сосудов, но и комплексное обследование с внимательным отношением ко всем жалобам пациента, учёт всех принимаемых им лекарственных средств и их возможных реакций с медикаментами, вводимыми во время и после операции.
Как выявить осложнения после стентирования сосудов на ранней стадии и что делать в случае их появления
На возникновение осложнений после стентирования коронарных артерий может указывать ухудшение общего состояния больного или длительное отсутствие какого-либо эффекта после проведённого вмешательства. При плохой переносимости медикаментов появляются симптомы интоксикации – тошнота, рвота, слабость, повышение температуры – всё в зависимости от интенсивности реакции. Данное состояние может быть скорректировано изменением тактики ведения больного, назначением других доз или замены действующих препаратов.
При развитии тромбоза, рестенозе с повторным сужением сосуда в месте установки стента или на других участках артерий может потребоваться повторное хирургическое вмешательство. Срочность проведения операции будет зависеть от текущего состояния больного.
Каждый пациент, страдающий ишемической болезнью сердца, испытывающий приступы стенокардии, должен проходить регулярное медицинское обследование. После проведения операции ангиопластики со стентированием заболевание, приведшее к осложнениям, не исчезает, и нуждается в дальнейшем наблюдении и лечении.
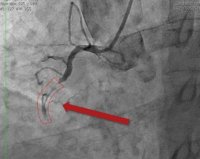
Тромбоз коронарного стента — это формирование тромба в пораженной венечной артерии после проведенного стентирования. Проявляется приступами загрудинной боли длительностью от нескольких минут до получаса и более, одышкой, слабостью вплоть до предобморочного состояния. Основными методами диагностики являются электрокардиография и анализ на кардиоспецифические ферменты. Для подтверждения тромбоза стента выполняется эхокардиография и коронарная ангиография. Лечение только хирургическое — в остром периоде рекомендована баллонная ангиопластика с последующей реимплантацией стента.
МКБ-10
Общие сведения
Тромбоз стента коронарной артерии — тяжелое осложнение кардиоваскулярного вмешательства, которое сопряжено с большим риском летального исхода. Встречается у 1,5-2,8% пациентов, частота зависит от использованных для реваскуляризации материалов. Вероятность повторного тромбоза коронарного стента намного выше — около 16%. Осложнение в основном развивается у мужчин старше 60 лет, которые имеют другие факторы риска сердечно-сосудистых заболеваний. У страдающих сахарным диабетом вероятность тромбоза после стентирования в 2-3 раза выше.

Причины
Развитие тромбоза во многом связано с типом имплантированного стента. Наиболее неблагоприятные результаты при использовании металлических конструкций, к которым очень быстро прикрепляются тромбоциты. При установке стентов с лекарственным покрытием вероятность осложнения намного ниже, но существует риск фатальных поздних тромбозов. Помимо материала стента, риск возникновения коронарного тромбоза зависит от:
- Иммунного ответа. Стент является инородным телом для организма, поэтому провоцирует ответную воспалительную реакцию. Процесс сопровождается пролиферацией гладкомышечных клеток артериальной стенки и усиленным выделением медиаторов, которые способствуют миграции тромбоцитов к месту имплантации коронарного стента.
- Состояния коронарного кровотока. Риск тромбоза возрастает на 20-30%, если у больного имеется многососудистое поражение коронарного бассейна или тяжелый кальциноз стенок артерий. Вероятность тромбообразования повышается, если окклюзия сосудов локализована в зоне их бифуркации, либо стенозированный участок имеет большую протяженность.
- Технических особенностей стентирования. Важная причина тромбоза — феномен замедленного или отсутствующего кровотока в области стентирования. Тромбообразование ускоряется при неполном (субоптимальном) раскрытии стента, когда диаметр просвета коронарного сосуда ниже нормы.
- Состояния пациента. Намного чаще тромбозы формируются, если в течение первых 30 суток послеоперационного периода развиваются кардиологические осложнения — острый коронарный синдром, низкая фракция выброса. Появление тромба наблюдается у 50-70% больных с наследственной резистентностью к антиагрегантам, применяемым в послеоперационном периоде.
Патогенез
Начало тромбообразования обусловлено сочетанием местных воспалительных реакций на участке стентирования и системных нарушений процессов свертывания крови. Под действием специфических факторов адгезии к поверхности коронарного стента «прилипают» тромбоциты, формирующие первичный нестабильный тромб. Тромбоциты начинают выделять собственные цитокины, запускающие каскад коагуляции с образованием прочного фибрина.
В результате образуется плотный тромб, нарушающий кровообращение в одной из коронарных артерий. Характер поражения сердечной мышцы определяется степенью окклюзии сосуда. При полном прекращении кровотока развивается крупноочаговый или мелкоочаговый некроз миокарда. Неполное перекрытие просвета сосуда обусловливает приступы обратимой ишемии миокарда, что клинически проявляется нестабильной стенокардией.
Классификация
По степени достоверности различают 3 типа тромбоза стента:
- Определенный тромбоз имеет ангиографическое или патологическое подтверждение.
- Вероятный тромбоз ставится при инфаркте миокарда в любой период после стентирования без ангиографического подтверждения.
- Возможный тромбоз — предварительный диагноз при любой внезапной сердечной смерти спустя месяц и больше после имплантации стента.
По времени начала выделяют 4 категории тромбоза:
- Острый (36%). Осложнение возникает в первые 24 часа после стентирования и обычно связано с нарушениями техники эндоваскулярного вмешательства.
- Подострый (42%). Тромб развивается на протяжении 30 дней после операции по установке коронарного стента. Подострые тромбозы, как правило, обусловлены некорректным ведением послеоперационного периода.
- Поздний (20%). Тромбообразование происходит в промежуток времени, больший 1 месяца, но меньший 1 года после реваскуляризации.
- Очень поздний (2%). К этой категории относят эпизоды повторного тромбообразования в коронарных артериях спустя 12 месяцев и дольше после вмешательства.
Симптомы
Клиника тромбоза коронарного стента представлена эпизодами загрудинной боли по типу ангинозного приступа. При физической нагрузке или эмоциональном стрессе человек ощущает внезапную давящую или сжимающую боль в груди. Для объяснения локализации болевых ощущений пациенты прикладывают кулак к области сердца. Болевые ощущения зачастую иррадиируют в левую руку, лопатку, шею и нижнюю челюсть.
Загрудинная боль может длиться около 10-15 минут и исчезать самостоятельно после отдыха. Чаще для купирования приступа требуется прием нитроглицерина. В случае полного прекращения тока крови в венечной артерии болевые ощущения длятся 20-30 минут и более, не устраняются медикаментами. Иногда боли настолько сильные, что человек принимает вынужденное неподвижное положение либо теряет сознание.
Ангинозные приступы сопровождаются выраженной одышкой, которая сохраняется даже в покое и усиливается при активных движениях. Кожа становится бледной и прохладной на ощупь, на лице выступает холодный пот. У человека учащается сердцебиение, бывают эпизоды «замирания» сердца. Характерна резкая слабость, головокружение и потемнение в глазах. Иногда на фоне боли начинается рефлекторная рвота.
Осложнения
Самое тяжелое последствие тромбоза коронарного стента — внезапная сердечная смерть, которая наблюдается в 10-16% случаев при несвоевременном получении медицинской помощи. Летальный исход вызван как тяжелыми аритмиями и асистолией, так и резким падением сердечного выброса из-за кардиогенного шока. При обширном некрозе ишемизированного миокарда есть вероятность разрыва сердечной стенки с формированием тампонады сердца.
При успешном лечении острой фазы патологии сохраняется риск отдаленных осложнений тромбоза. У 50-60% пациентов наблюдается хроническая сердечная недостаточность, обусловленная постинфарктным кардиосклерозом. У 20% людей возникают тромбоэмболические осложнения, вызванные попаданием фрагментов тромба в сосуды легких, почек и селезенки, головного мозга. Редко выявляется аутоиммунный постинфарктный синдром Дресслера.
Диагностика
Предположить тромбоз коронарного стента можно уже при первом осмотре при наличии информации о ранее проведенном стентировании. Патогномоничные физикальные данные отсутствуют, поэтому для постановки диагноза определенного тромбоза требуется лабораторно-инструментальное обследование. Диагностика назначается врачом-кардиологом, проводится в кратчайшие сроки и включает следующие методы:
- ЭКГ. На развитие некроза миокарда указывает регистрация на кардиограмме высокого зубца Т в сочетании с подъемом сегмента ST. Типичные изменения сочетаются с глубоким отрицательным зубцом Q, который обусловлен перенесенным ранее инфарктом. При нестабильной стенокардии наблюдаются различные проявления ишемии миокарда, экстрасистолы.
- Анализ на кардиомаркеры. Исследование позволяет установить окончательный диагноз в рамках острого коронарного синдрома. У больных с инфарктом миокарда выявляется повышение миоглобина, КФК МВ и тропонина в десятки раз. При стенокардии уровень ферментов нормальный или увеличивается не более чем на 50% от нормы.
- Эхокардиография. УЗИ сердца выполняется для оценки состояния миокарда и измерения фракции выброса. При ЭхоКГ визуализируется отсутствие сократительной активности участка сердечной стенки, наличие постинфарктного рубца. При снижении сердечного выброса менее 40% диагностируют сердечную недостаточность.
- Коронарная ангиография. Рентгеноконтрастное инвазивное исследование коронарных сосудов — основной метод для верификации тромбоза стента. При коронарографии обнаруживают дефект наполнения в одном из венечных сосудов и отсутствие кровотока дистальнее этого участка. Часто наблюдается многососудистая окклюзия коронарного бассейна.
Лечение тромбоза коронарного стента
Хирургическое лечение
Методом выбора при тромбозе коронарного стента является чрескожная первичная ангиопластика, цель которой — быстрая реваскуляризация миокарда. Введение медикаментозных тромболитиков у таких больных не эффективно. В острой фазе тромбоза проводится баллонная ангиопластика с применением устройств для аспирации тромба, которая в 90% обеспечивает полное восстановление кровообращения в венечных артериях.
Примерно у 45% пациентов после стабилизации состояния есть потребность в повторной установке стента. Необходимость операции кардиохирурги объясняют наличием выраженной остаточной диссекции. Для улучшения отдаленного прогноза выполняется имплантация типа «стент в стент». Вмешательство производится по рентгенэндоваскулярной методике, которая отличается минимальной травматичностью и коротким восстановительным периодом.
Экспериментальное лечение
В современной кардиологии есть успешный опыт применения ингибиторов гликопротеиновых рецепторов IIb/IIIa у больных, страдающих генетической нечувствительностью к антиагрегантным препаратам. Препараты действуют в течение 2-3 часов с момента введения, нарушают конечный этап агрегации тромбоцитов, благодаря чему риск тромбоза снижается в несколько раз. Ингибиторы IIb/IIIa используются во время операции и после восстановления коронарного кровотока.
Прогноз и профилактика
При проведении двойной антиагрегантной терапии и устранении поведенческих факторов риска тромбоза коронарного стента прогноз благоприятный. Назначение моноклональных антител улучшает прогноз у пациентов, которые нечувствительны к стандартным антиагрегантам. Первичная профилактика заключается в тщательном отборе больных перед стентированием и обеспечении полного открытия стента после установки.
1. Тромбоз стентов у пациентов с ишемической болезнью сердца: классификация, причины и методы лечения. Систематический обзор/ О. Тайманулы, И.Е. Сагатов, Е.С. Утеулиев, А.О. Мырзагулова, Т.В. Маслов// Вестник КазНМУ. — 2017.
2. Причины тромбозов стентов коронарных артерий/ В.И. Ганюков, А.А. Шилов, Н.С. Бохан, Г.В. Моисеенков, Л.С. Барбараш// Интервенционная кардиология. — 2012.
3. Реальная ли угроза позднего тромбозе стента с лекарственным покрытием? Сравнение стентов с лекарственным покрытием. Фокус на эверолимус/ Лупанов В.П., Самко А.Н., Бакашвили Г.Н.// Кардиоваскулярная терапия и профилактика. — 2009.
За последнее десятилетие во всем мире выросла доля эндоваскулярных методов лечения ишемической болезни сердца (ИБС). Выбор данной тактики лечения ИБС, в противовес хирургическому лечению, в сочетании с консервативной терапией обусловлен
За последнее десятилетие во всем мире выросла доля эндоваскулярных методов лечения ишемической болезни сердца (ИБС). Выбор данной тактики лечения ИБС, в противовес хирургическому лечению, в сочетании с консервативной терапией обусловлен непосредственной эффективностью и безопасностью эндоваскулярной процедуры, позволяющей добиться адекватного восстановления коронарного кровотока в большинстве случаев.
При атеросклеротическом поражении коронарного русла вид эндоваскулярного вмешательства выбирают на основании рентгенморфологических характеристик поражения венечных сосудов. У пациентов с поражением одного коронарного сосуда основным вмешательством является процедура транслюминальной баллонной ангиопластики (ТЛАП) или стентирования пораженного сегмента коронарной артерии. Операция аортокоронарного шунтирования (АКШ) рекомендуется преимущественно пациентам с поражением ствола ЛКА или пациентам с многососудистым поражением венечного русла. Однако в этом случае при наличии серьезных сопутствующих заболеваний, являющихся противопоказанием к проведению операции АКШ, бывает необходимо проведение эндоваскулярных вмешательств. При выявлении многососудистого поражения коронарных артерий возможно выполнение одномоментной эндоваскулярной процедуры реваскуляризации миокарда на нескольких коронарных сосудах или же выполнение поэтапной эндоваскулярной процедуры.
Увеличивающееся из года в год количество эндоваскулярных вмешательств на коронарных сосудах делает проблему лечения выявленных хронических окклюзий весьма актуальной. Хронически окклюзированные коронарные артерии составляют значительную часть коронарных поражений, выявляемых у пациентов при проведении диагностической коронароангиографии (КАГ) и, в определенной клинической ситуации, требуется проведение реваскуляризации миокарда.
Так, окклюзированные коронарные артерии выявляются примерно у 38% пациентов, а коронарная ангиопластика на хронически окклюзированных коронарных артериях составляет 10–20% всех интервенционных процедур [1, 2, 4].
Выявление полной окклюзии коронарной артерии при КАГ у больных с ИБС может серьезно влиять на выбор дальнейшей лечебной тактики. Хронически окклюзированная коронарная артерия часто является фактором, определяющим выбор специалистов в пользу проведения хирургического лечения, а не эндоваскулярной процедуры.
В Научно-практическом центре интервенционной кардиоангиологии (НПЦИК) Департамента здравоохранения г. Москвы при проведении плановой КАГ также довольно часто обнаруживаются полные хронические окклюзии одной, двух или более коронарных артерий.
Соотношение между общим количеством больных, которым в период с октября 1997 г. по декабрь 2002 г. выполнялась в НПЦИК диагностическая КАГ, и числом пациентов, у которых были выявлены одна или более хронически окклюзированные коронарные артерии, представлено на рисунке 1.
Большинство исследователей в своих работах показали, что одной из главных причин, определяющих различия в тактике лечения больных с наличием или отсутствием окклюзии коронарной артерии, является преобладание больных с трехсосудистым поражением коронарного русла. Считается, что наличие перенесенного инфаркта миокарда в области, кровоснабжаемой окклюзированной артерией, может препятствовать проведению более агрессивной процедуры реваскуляризации миокарда [3].
По данным большинства авторов, наличие окклюзии коронарной артерии у больных ИБС может изменить терапевтическую тактику по нескольким причинам.
- Катетерная реканализация требует более высокой квалификации врача.
- Доля первичного (непосредственного) успешного результата оказывается ниже, чем при стенотических поражениях венечного русла.
- Реканализация сосуда может быть чреспросветной, субинтимальной, пере- и трансатероматозной.
- Имеется риск развития диссекции или разрыва сосуда в месте воздействия инструмента. (У 42% больных непосредственно после ангиопластики окклюзий выявляются ангиографические признаки диссекции сосудов [3]. Известно, что диссекция значительно реже встречается при дилятации стенозов и относится к факторам, способствующим тромбообразованию.)
- При отсутствии удовлетворительного результата приходится увеличивать число и продолжительность раздуваний баллона, что впоследствии может приводить к развитию рестеноза.
- Кроме того, при наличии окклюзии имеется более высокий риск дилятации другого сосуда.
Как было сказано выше, коронарная ангиопластика хронических окклюзий составляет, по данным разных авторов, 10–20% всех интервенционных процедур [1, 2, 4]. Наряду с этим, эндоваскулярное восстановление просвета коронарной артерии при ее хронической окклюзии часто остается технически сложной задачей.
Реканализация становится более проблематичной при наличии негативных факторов, влияющих на успех процедуры, таких, как старые повреждения, протяженные, ангиографически неблагоприятные окклюзии, наличие мостовых коллатералей.
Проведению эндоваскулярной реваскуляризации при этом типе поражений препятствуют не только технические трудности, связанные с проведением проводников и других устройств, но и повышенный уровень рестеноза в отдаленном периоде [5, 6, 7].
Известно, что частота непосредственного успеха при ангиопластике на хронически окклюзированных артериях ниже, тогда как времени на облучение, использование аппаратуры затрачивается больше и стоимость процедуры выше, чем при ангиопластике у больных со стенотическими поражениями венечного русла [8].
В НПЦИК в период с октября 1997 г. по декабрь 2002 г. проведено 380 попыток механической реканализации хронически окклюзированных коронарных артерий у 375 больных. При этом успех процедуры был достигнут у 253 больных (67,5%), которым было реканализировано 258 сегментов. В 122 случаях (32,5%) процедура реканализации была безуспешной. Проводниковая реканализация и коронарная ангиопластика окклюзированной коронарной артерии выполнялись 107 больным на 107 сегментах; реканализация, ТЛАП и стентирование — 146 больным, которым был реканализирован 151 сегмент.
По результатам исследований, проведенных в НПЦИК, с технической стороны успех процедуры определялся как способность пройти окклюзированный сегмент и проводником, и баллонным катетером и успешно открыть окклюзированную артерию с величиной остаточного стеноза менее 40%.
При этом эффективной процедура считалась, если не было серьезных кардиальных осложнений на госпитальном этапе. Серьезные кардиальные осложнения определялись как случаи смерти, развития острого инфаркта миокарда или необходимость в проведении экстренной процедуры реваскуляризации миокарда.
По нашему мнению, важным в данной клинической ситуации, является проведение обязательного всестороннего контрольного обследования через 6 мес после эндоваскулярного вмешательства, включающего в себя проведение нагрузочных проб и контрольной КАГ для выявления возможного прогрессирования атеросклеротического процесса в коронарных артериях и развития in-stent стеноза.
Мы хотим продемонстрировать целесообразность проведения эндоваскулярных процедур у больной с двумя хронически окклюзированными коронарными артериями и несколькими гемодинамически значимыми стенозами, с высоким риском проведения операции аортокоронарного шунтирования, обусловленным тяжелой сопутствующей патологией.
Больная Ш., 59 лет поступила в мае 2001 г. в НПЦИК для планового обследования с диагнозом ИБС. Стенокардия напряжения III функционального класса (ФК), гипертоническая болезнь II степени, аутоиммунный тиреоидит Хашимото, гипотиреоз на стадии компенсации, ожирение III степени.
При поступлении в стационар пациентка предъявляла жалобы на давящие боли за грудиной при незначительной физической нагрузке и в покое, кратковременный эффект достигался при приеме нитроглицерина.
Из анамнеза было известно, что больная длительное время отмечает подъемы артериального давления до максимальных цифр 200/120 мм рт. ст. Около 6 лет беспокоят приступы стенокардии напряжения и покоя. Ухудшение самочувствия с 19.04.2001 г., когда при незначительной физической нагрузке стали возникать интенсивные загрудинные боли, с кратковременным эффектом от приема нитратов. Была госпитализирована в НПЦИК с подозрением на прогрессирующую стенокардию для обследования и лечения.
Состояние при поступлении: средней степени тяжести. Пациентка повышенного питания. В легких дыхание везикулярное, хрипов нет, ЧДД 16/мин. Тоны сердца приглушены, ритмичные, шумов нет. ЧСС 74/ мин. АД 140/90 мм рт. ст. Со стороны желудочно-кишечного тракта без патологии. Неврологический статус без особенностей.
В биохимических анализах крови у пациентки обращала на себя внимание гиперхолестеринемия — 6,7 ммоль/л.
На ЭКГ: ритм синусовый, нарушение кровоснабжения передне-перегородочно-верхушечно-боковой области левого желудочка, Т(-)III, aVF, V1 — V5.
По данным ЭхоКГ: полости сердца не расширены. ЛЖ сократимость: удовлетворительная, ФВ — 66%, КДР — 5,1 см, КСР — 3,2 см, КДО — 123 см 3 , КСО — 41 см 3 , толщина межжелудочковой перегородки в диастолу 13,3 мм, толщина задней стенки в диастолу 12,3 мм. Умеренная симметричная гипертрофия ЛЖ. Митральный клапан: движение створок разнонаправленное. Аорта уплотнена, не расширена, склероз створок аортального клапана. При Д-ЭхоКГ патологических потоков не выявлено.
При проведении суточного мониторирования ЭКГ было выявлено два эпизода депрессии сегмента S-T по 1 каналу до 2 мм, связанных с болевыми ощущениями.
По данным велоэргометрической пробы, на фоне отмены за 1 сут до исследования антиангинальной и гипотензивной терапии результат расценен как положительный: на нагрузке
75 Вт/мин появились типичные ангинозные боли без изменений на ЭКГ. Толерантность к нагрузке низкая.
Учитывая данные клинического течения основного заболевания, жалобы при поступлении в стационар, а также данные инструментальных методов обследования, пациентке было решено провести диагностическую вентрикулографию и коронароангиографию с целью выявления поражения коронарного русла и выработки дальнейшей тактики лечения основного заболевания. Вентрикулография: КДО — 91,3 мл, КСО — 21,2 мл,
ФВ — 77%. Митральная регургитация отсутствует. Сегментарная сократимость (правая косая проекция) удовлетворительная. Зон асинергии выявлено не было. Тип коронарного кровообращения правый. Ствол ЛКА обычно развит, не изменен. Передняя межжелудочковая ветвь (ПМЖВ) окклюзирована после отхождения первой диагональной ветви (1 ДВ). Коллатеральное заполнение дистального русла через межсистемные коллатерали отсутствует, через внутрисистемные — слабое (рис. 2). Огибающая ветвь (ОВ) стенозирована на двух уровнях: в проксимальном сегменте эксцентрический стеноз до 70% протяженностью до 10 мм с вовлечением устья, эксцентрический стеноз 60% маргинальной ветви (МВ) диаметром 2,5 мм в дистальном сегменте протяженностью до 10 мм. ПКА окклюзирована в проксимальном сегменте (рис. 3). Коллатеральное заполнение дистального русла через межсистемные коллатерали хорошее, через внутрисистемные — отсутствует.
Пациентке были выполнены механическая реканализация, баллонная ангиопластика и стентирование средней трети ПМЖВ (баллонная дилятация U-Pass 2 x 20, 17 атм 120 с — три дилятации давлением 14, 17, 12 атм по 120 с и установка стента Bx Velocity 2,5 х 23 мм, 13 атм, 45 с), прямое стентирование проксимальной трети ОВ (стентом Bx Velocity 3,5 х 8мм, 14 атм, 45 с) (рис. 4), проведена механическая реканализация, ТЛАП и стентирование проксимальной трети ПКА (баллон Raptor 2,5 х 15, 18 атм, 120 с, установка стента Multilink Tetra 3,5 х 13, 12 атм, 45 с, с последующей оптимизацией просвета сосуда в проксимальных и дистальных сегментах стента доставочным баллоном под давлением 12 атм по 120 с) и ТЛАП дистальной трети ПКА — баллонная дилятация (баллон Raptor 2,5 х 18, 15 атм, 150 с) (рис. 5).
После механической реканализации, ТЛАП и стентирования ПКА и ПМЖВ — определялся кровоток TIMI 3, диффузные изменения без резких стенозов.
Послеоперационный период протекал гладко, ангинозные боли не рецидивировали. Пациентка была выписана под наблюдение кардиолога по месту жительства, рекомендован прием следующих лекарственных средств: атенолол 25 мг 2 раза в день, норваск 2,5 мг 2 раза в день, эналаприл 2,5 мг 2 раза в день, аспирин 125 мг 1 раз в день после еды, моно мак 20 мг 1 табл. х 2 раза в день, L-тироксин — 1 табл. утром.
С целью оценки отдаленного результата процедуры стентирования при выявленных хронических окклюзиях коронарных артерий пациентка Ш. была вновь обследована. При поступлении в стационар — жалобы на редкие приступы болей за грудиной при физической нагрузке.
После выписки переносимость физических нагрузок значительно улучшилась, однако сохранялись боли при ходьбе быстрым шагом. Постоянно принимает атенолол, моно мак, эналаприл, аспирин.
В биохимических анализах крови выявлены гиперхолестеринемия, гипертриглицеридемия: холестерол 7,4 ммоль/л, триглицериды 2,8 ммоль/л.
При обследовании — на ЭКГ: ритм синусовый, правильный, ЧСС 68/мин, отрицательные зубцы Т в грудных отведениях.
На ЭхоКГ: полости сердца не расширены. Левый желудочек — сократимость удовлетворительная, ФВ — 69%, КДР — 5,0 см, КСР — 3,0 см, КДО —122 см 3 , КСО — 36 см 3 , толщина межжелудочковой перегородки в диастолу 13 мм, толщина задней стенки в диастолу 12,3 мм. Умеренная симметричная гипертрофия миокарда ЛЖ. Митральный клапан: движение створок разнонаправленное. Аорта не расширена, уплотнена, склероз створок аортального клапана. При Д-ЭхоКГ патологических потоков не выявлено.
При проведении контрольной диагностической вентрикулографии и КАГ было выявлено: КДО — 120 мл, КСО — 30 мл, ФВ — 75%. Сегментарная сократимость удовлетворительная. Зон асинергии не выявлено. Тип коронарного кровообращения правый. Ствол ЛКА обычно развит, не изменен. ПМЖВ диффузно изменена, отмечается рестеноз после стентирования — 75% (рис. 6). ОВ диффузно изменена, отмечается рестеноз после стентирования в проксимальном конце стента на 75% (рис. 6). ПКА: диффузно изменена, в проксимальной трети состояние после стентирования без рестенозирования, в дистальной трети стенозирована на 75% (протяженностью около 10 мм) с вовлечением бифуркации задней межжелудочковой ветви и пастеро-латеральной ветви (рис. 7). Выполнены процедуры ангиопластики in-stent стеноза среднего сегмента ПМЖВ на нескольких уровнях (в устье ПМЖВ и после отхождения ДВ) и ангиопластики in-stent стеноза ОВ с хорошим эффектом. Гладкий послеоперационный период. Пациентка была выписана из стационара под дальнейшее наблюдение у кардиолога и эндокринолога по месту жительства, рекомендован прием следующих лекарственных средств: кардикет 20 мг 2 раза в день, аспирин 125 мг 1 раз в день, тиклид 250 мг 2 раза в день в течение 2 нед с дальнейшей отменой препарата, атенолол 12,5 мг 2 раза в день. В связи с гиперхолестеринемией и гипертриглицеридемией назначен зокор 10 мг на ночь. С целью контроля уровня гормонов щитовидной железы и коррекции заместительной терапии пациентке было рекомендовано продолжать прием L-тироксина в дозе 100 мкг 1 раз в день.
С целью оценки результатов ТЛАП in-stent стенозов ПМЖВ и ОВ через 6 мес после проведения эндоваскулярного вмешательства пациентке была вновь проведена диагностическая коронароангиография. Эффективность ТЛАП in-stent стенозов была подтверждена (рис. 9).
Таким образом, на данном клиническом примере показано, что эндоваскулярные процедуры при многососудистом поражении венечного русла являются альтернативой аортокоронарного шунтирования у больных с тяжелыми сопутствующими заболеваниями. Кроме этого, применение интервенционных методов лечения ИБС эффективно и безопасно.
Литература
- Бабунашвили А. М., Иванов В. А., Бирюкова С. А. Эндопротезирование (стентирование) венечных артерий сердца. — М.: АСВ, 2001. — 704 с.
- Савченко А. П., Абдуллин Н. И., Матчин Ю. Г. и др. Особенности клинического течения и ангиографической картины при хронической окклюзии коронарной артерии//Вестник рентгенологии и радиологии/ — 2000; 4: 4–10.
- Бакланов Д. В., Огурцова О., Мэзден Р. Рестенозирование после успешной ангиопластики при окклюзиях коронарных артерий // Кардиология. — 1998; 1:10-126.
- Delacretaz E., Meier B. Therapeutic Strategy With Total Coronary Artery Occlusions // Am J Cardiol, 1997, 79: 185 — 187.
- Bauters C., Banos J. L., Van Belle E., Mc Fadden E. P., Lablanche J.M., Bertrand M.E. Six-month angiographic outcome after successful repeat percutaneous intervention for in-stent restenosis // Circulation 1998 Feb 3;97(4):318–21.
- Elchaninoff H., Koning R., Tron C., Gupta V., Cribier A. Balloon angioplasty for the treatment of coronari in-stent restenosis: immediate results and 6-month angiographic recurrent restenosis rate // J Am Coll Cardiol 1998 Oct;32(4):980–4
- Rubartelli P., Niccoli L., Verna E. et al. Stent Implantation Versus Balloon Angioplasty in Chronic Coronary Occlusions: Results From the GISSOC Trial. J Am Coil Cardiol 1998; 32: 90-6.Edelman ER., Rogers C. // Hoop Dreams. Stent without restenosis // Circulation, 1996, 94: p. 1199–1202.
Д. Г. Иоселиани, доктор медицинских наук, профессор
А. В. Кононов
М. В. Яницкая, кандидат медицинских наук
О. В. Захарова
Научно-практический центр интервенционной кардиоангиологии, Москва
Стентирование коронарных сосудов - хирургическое вмешательство, проводимое как в плановом, так и экстренном порядке. Операция может привести к осложнениям, часть из которых можно предотвратить, выполняя все рекомендации врача в реабилитационный период.

Что такое стентирование?
Доставка кислорода и питательных элементов к сердечной мышце происходит по двум коронарным артериям. Вследствие атеросклероза просвет этих сосудов постепенно сужается, что становится причиной ухудшения питания миокарда и соответственно ишемических процессов в нем.
Показания и противопоказания к стентированию коронарных сосудов определяет только врач после коронарографии, ЭКГ и других методик обследования сердца и сосудов.
Стентирование - это эндоскопическая операция, заключающаяся во введении в сосуд специального стента, который расширяет просвет артерии и поддерживает ее стенки.

В результате нормализуется кровоток, а также доставка кислорода и питательных элементов. Стентирование назначают при:


Перед операцией проводится обследование, позволяющее оценить степень закупорки сосудов, место расположения основных атеросклеротических бляшек.
Ход операции
Стентирование проводят в операционной в основном под местным обезболиванием. Для получения доступа к коронарным сосудам хирург проводит прокол бедренной артерии, после чего в нее вводит катетер-манипулятор со стентом на конце (в спавшемся виде). Процедура проводится под контролем рентгенографии. В суженном месте стент при помощи расположенного рядом с ним баллона расправляется. В результате имплантат вдавливает в стенки артерии бляшки и таким образом устраняется основная причина ишемии.

Хирургическое вмешательство занимает примерно около одного часа. При одновременном стентировании двух сосудов время процедуры увеличивается до 2,5-3 часов.
В ранний послеоперационный период пациент должен находиться под наблюдением медперсонала и строго соблюдать все указанные доктором рекомендации.
Стентирование проводят не только на коронарных артериях. Часто стенты устанавливаются в сонную артерию при ее закупорке более чем на 50%, в этом случае хирургическое вмешательство позволяет предотвратить ишемический инсульт. Стентирование подвздошных вен назначается в основном мужчинам при варикоцеле, эректильной дисфункции, варикозе вен малого таза. Возможно стентирование мочеточников при их сужении и нарушении оттока мочи.

Особенности периода восстановления
Реабилитация после стентирования сосудов сердца начинается сразу после хирургического вмешательства. В первые часы пациенту необходимо соблюдать полный покой, это ускорит образование сгустка крови в месте прокола бедренной артерии и снизит риск кровотечений. На второй день необходимо расширять двигательную активность за счет движений руками и ногами. Нагрузка должна увеличиваться постепенно. В стационаре после операции больные находятся в среднем от 3 до 7 дней.

Реабилитация после операции в санаториях - оптимальный вариант. В таких учреждениях пациент постоянно находится под присмотром медперсонала, проходит лечебные процедуры, занимается физкультурой, правильно питается. При развитии осложнений больному сразу же оказывается помощь, что существенно снижает риск дальнейшего прогрессирования нежелательных реакций.
Изменение образа жизни
В реабилитационный период необходимо соблюдать несколько основных правил:
- В первую неделю нагрузка должна быть минимальной. В этот период также запрещается принимать ванную, можно только душ.
- На протяжении двух месяцев нельзя самостоятельно управлять автомобилем. Не желательно также часто ездить, особенно по неровным трассам.


Необходимо также пересмотреть свой режим дня. Нужно вовремя ложиться спать, по возможности отдыхать днем, меньше находиться в одной позе. Желательно избегать психотравмирующих ситуаций, больше времени проводить на свежем воздухе.
Длительность периода восстановления
Организм каждого человека индивидуален и сроки полного восстановления здоровья после шунтирования сосудов зависят от множества факторов. К привычной жизни врачи рекомендуют начинать постепенно возвращаться через 2-2,5 недели. Однако стентирование - эта та операция, дальнейший исход которой во многом определяется тем, насколько прооперированный готов следовать рекомендациям врача.
В первую очередь необходимо полностью пересмотреть свой образ жизни. То есть подобрать правильное питание, отказаться от курения и злоупотребления алкоголем, избегать стрессов, выбрать дозированные физические нагрузки.

Это поможет снизить риск дальнейшего прогрессирования атеросклероза и значительно уменьшит вероятность развития ранних и поздних осложнений после установки стентов.
Продолжительность жизни пациентов со стентом
Многих больных перед хирургическим вмешательством интересует - сколько живут со стентом и дают ли инвалидность. Продолжительность жизни во многом зависит от возраста больного, сопутствующих заболеваний, осложнений после вмешательства.
Но большее значение для многих имеет существенная разница в самочувствии до и после операции - больного меньше беспокоят другие дискомфортные ощущения, у них расширяется двигательная активность и появляется возможность заниматься любимым делом.
Сколько будет длиться такая жизнь зависит от соблюдения диеты, выполнения лечебной физкультуры, своевременного лечения всех острых и хронических заболеваний.
Инвалидность после стентирования не дают, так как такая операция улучшает, а не ухудшает самочувствие больного и не требует значительных ограничений после ее проведения. Однако есть несколько исключений. Инвалидность после установки стента могут получить работники силовых структур, так как после подобного хирургического вмешательства чрезмерные физические нагрузки запрещены. Инвалидность нередко дают и лицам, имеющим сопутствующие тяжело протекающие заболевания. Решение о признании пациента инвалидом принимает экспертная комиссия, состоящая из нескольких врачей.

Осложнения после установки стентов
Согласно статистике, ранние и поздние осложнения после стентирования возникают не более чем в 5% случаев, что является достаточно низким показателем. Наиболее вероятные осложнения процедуры:
- образование обширной гематомы в области введения катетера;
- нарастание тромботических сгустков на стенках стента;
- нарушение мозгового и почечного кровообращения;
- инфаркт во время проведения операции;
- тромбоз сосуда вследствие его прокола;

На поздних сроках реабилитации возможен рестеноз. Это повторное сужение просвета коронарного сосуда, развивающееся чаще всего вследствие патологического нарастания тканей вокруг стента.
Признаки осложнений
Большинство послеоперационных осложнений на ранней стадии их развития успешно устраняются. Поэтому врачу обязательно нужно сообщить, если после операции:
-
на месте прокола бедренной артерии появился кровоподтек, сочится кровь или нарастает отек и гиперемия;


Многие осложнения легко устраняются при помощи лекарственной терапии, и их возникновение не отражается неблагоприятно на восстановлении и самочувствии пациента.
Диетотерапия после стентирования
Правильное питание не только ускоряет восстановление после стентирования, но и предупреждает дальнейшее прогрессирование атеросклероза и возвращение признаков стенокардии. Отмечается, что повторное проведение операции чаще всего требуется людям, которые не соблюдали диетотерапию.
Питание, прежде всего, должно быть гипохолестериновым, то есть необходимо свести к минимуму употребление пищи, богатой на животные жиры:
- мясо жирных сортов;
- субпродукты;
- колбасные изделия и копчености;

Меньше необходимо употреблять соли - в день ее нужно не более 4-х грамм. Нужно учитывать, что много соли содержат консервы, хлебобулочные изделия. Ограничить необходимо:
- яйца (до 4 штук в неделю);
- жирную сметану;
- сливочное масло, сыр, сливки;
- белый хлеб;
- кондитерские изделия;
- выпечку;
- газированные и кофеин содержащие напитки.

В питание следует преимущественно включать растительные плоды, молочнокислую продукцию, блюда из нежирного мяса и рыбы. Полезны каши, бобовые культуры, цельнозерновой хлеб, овощи, богатые на клетчатку. Нужно больше пить чистой фильтрованной воды, отваров шиповника. Сладости лучше заменить на сухофрукты и мед.
Примерное меню
Блюда необходимо преимущественно отваривать, запекать, тушить. Есть нужно небольшими порциями до 5-6 раз в день.
Таблица меню на день:
| Время приема пищи | Основные блюда | Напитки |
| Завтрак | Творожная запеканка либо белковый омлет, гречневая каша на воде. | Зеленый чай, компот из сухофруктов |
| Обед | Овощной суп, картофельное пюре с небольшим кусочком отварной курицы. Салат из овощей, приправленный оливковым маслом. | Отвар шиповника, компот |
| Ужин | Отварной рис, тушеная рыба, салат из свеклы. | Кефир обезжиренный, натуральный йогурт. |

Ужин должен быть не позднее 8 часов вечера, так как поздние перекусы повышают нагрузку на сердечно-сосудистую систему ночью. В рационе должны присутствовать орехи в небольших количествах, свежие фрукты, ягоды. Витаминизированное питание повышает общий тонус организма и дает сердечной мышце необходимое количество микроэлементов и витаминов.
Принципы лечебной физкультуры
Умеренные физические нагрузки после стенирования приводят к нескольким эффектам:
-
Улучшают циркулирование тока в сосудах. Это положительно отражается не только на работе сердца, но и на всем организме в целом.



После стентирования запрещены только интенсивные физические нагрузки и тренировки, при которых необходима хорошая выносливость сердечной мышцы. Поэтому больным можно заниматься:
- быстрой ходьбой - до 6-7 км в час;
- легким бегом;
- ездой на велосипеде;
- плаванием;
- аквааэробикой.

Интенсивность нагрузки следует увеличивать постепенно, внимательно отмечая все изменения в самочувствии. После установки стентов в сосуды многие врачи рекомендуют ежедневно уделять время терренкуру. Это занятие предполагает пешие прогулки с постепенным увеличением их времени и угла наклона. В первые дни нужно ходить только по ровной местности, затем маршрут нужно составлять так, чтобы на его протяжении были горки с углом наклона от 5 до 30 градусов. Постепенно продолжительность терренкура увеличивается.
Правила выполнения упражнений
Во время выполнения лечебной физкультуры нужно придерживаться следующих правил:
- по времени тренировка должна занимать от 30 до 45 минут;
- занятия проводят либо на голодный желудок, либо не ранее чем через полтора часа после еды;

Не следует выполнять те упражнения, которые приводят к болям и дискомфорту. Цель ЛФК - улучшение, а не ухудшение самочувствия.
Лечебная физкультура укрепляет иммунитет, помогает снизить вес, укрепляет нервную систему, стабилизирует давление. Занятия лучше подбирать с лечащим врачом, так как только специалист может знать предельный уровень допустимой нагрузки.

Жизнь после стентирования
Установка стента - одна из самых уникальных методик восстановления проходимости крупных сосудов, снижающая риск смертельного исхода тяжелых заболеваний и улучшающая качество жизни. При отсутствии противопоказаний операция проводится в считанные дни, основными ее преимуществами считаются:
- Отсутствие полостного вмешательства. Грудная клетка не вскрывается, так как стент вводится через бедренную артерию.
- Короткий реабилитационный период. Строгий постельный режим назначается не более чем на сутки, в дальнейшем двигательная активность постепенно расширяется.

Рекомендуемое изменение образа жизни и питания, отказ от вредных привычек после установки стента положительно отражается не только на работе сердца, но и на функционировании всех внутренних органов. Кроме того, техника эндоскопической операции и качество самих протезов год от года неуклонно повышаются, что снижает риск осложнений и позволяет проводить манипуляцию даже в самых запущенных и сложных случаях.
Читайте также:

