Что такое полиморфизм клеток эпителия
Обновлено: 26.04.2024
Основу цитологической диагностики составляет изучение клеток, изменений в их расположении и строении. Критерии цитологической диагностики включают анализ клеточного и неклеточного состава: количество клеток, наличие клеток разного типа, их расположение в структурах или разрозненно, вид структур, размер, форма, строение клеток и ядер, наличие или отсутствие клеточного и ядерного полиморфизма и другие параметры. По характеру и степени выраженности отклонения от нормального клеточного состава судят о природе патологического процесса. По признакам, характерным для определенных тканей, судят о тканевой принадлежности опухоли. При этом учитывают фон препарата — элементы крови, бесструктурное вещество, коллоид, жир и др.
Количество клеток в мазке определено прочностью межклеточных связей и обилием стромы. Богатый клеточный состав бывает в низкодифференцированных опухолях, гемато- и лимфосаркоме, нейроэндокринных опухолях. Скудный материал и даже единичные клетки встречают, в частности, при скиррозном и дольковом раке молочной железы.
Расположение клеток. Клетки в мазке могут располагаться разрозненно или в виде структур. Для доброкачественных поражений характерно правильное, упорядоченное расположение клеток, одинаковое расстояние между ними, сходные размеры клеток и ядер, образующих структуру. Для злокачественных новообразований характерны структуры (комплексы, пучки) с неупорядоченным расположением клеток.
Размеры клеток и ядер. Размеры клеток по возможности оценивают в сравнении с размерами нормальных клеток того же типа. Размеры ядер обычно сравнивают с размером эритроцита (в норме достаточно стабильным, примерно 7 мкм). Соотношение размера ядра и цитоплазмы (ядерно-цитоплазматическое соотношение) также весьма различно в разных клетках, и при его оценке учитывают степень отклонения этого параметра от нормальной клетки того же типа.
Фон препарата часто имеет большое диагностическое значение. Фоном могут быть элементы периферической крови или воспаления, связанного с инфекцией, сопровождающего опухолевый и другие процессы, клеточный детрит, межуточное вещество. Фон препарата может иметь диагностическое значение при определении тканевой принадлежности или гистологической формы опухоли.
При реактивных и фоновых поражениях чаще всего увеличено число клеток (гиперплазия, пролиферация), размер ядер и отмечается их более интенсивная окраска (гиперхромия). Хроматин распределен сравнительно равномерно. В некоторых ядрах (особенно характерно для железистого эпителия) увеличен размер ядрышек. При некоторых состояниях изменен размер клеток и наблюдаются особенности окрашивания цитоплазмы.
При пограничном процессе (поражении, близком к злокачественной опухоли) размер ядер увеличен значительно, ядро деформировано, контуры его неровные, ядерная мембрана неравномерно утолщена, встречаются многоядерные клетки. Хроматин распределен неравномерно, чередуются мелкие и крупные участки уплотнения. Образуются множественные мелкие ядрышки, возможно увеличение их размеров. Однако в отличие от злокачественной опухоли в разных клетках изменения оценивают как мономорфные (однотипные).
Изменения в клеточном составе мазка при злокачественной опухоли характеризуются клеточным и ядерным полиморфизмом (различием характеристик разных клеток), образованием структур, отличающихся от нормальных, изменением фона препарата; для многих злокачественных опухолей характерен так называемый опухолевый диатез — реакция соединительной ткани на инвазию (прорастание опухоли).
Если количество материала достаточное, клетки сохранены, хорошо приготовлен и окрашен препарат, то можно без характеристики микроскопической картины формулировать цитологический диагноз с указанием на гистологическую форму опухоли и степень дифференцировки (низкодифференцированная аденокарцинома, плоскоклеточный рак с ороговением, фиброаденома).
Морфология опухолевых клеток. Строение опухолевых клеток.
«Нет сомнения, что раковые клетки столь же разнообразны, как и сами опухоли. Ввиду чрезвычайной сложности каждой отдельной клетки можно даже полагать, что каждая раковая клетка, вероятно, отличается от любой другой»,— так писал В Бернар еще в 50-е годы. Действительно, полиморфизм опухолевых клеток — одна из их характерых черт, однако, степень полиморфизма в одной и той же и в разных опухолях колеблется в очень широких пределах и касается как формы, так и размеров клеток. Клеточный состав опухолей может быть представлен также и однообразными мономорфными клетками.
Принято считать, это следует подчеркнуть, что чем более резко выражен клеточный полиморфизм, тем злокачественнее опухоль и хуже прогноз. Однако полного соответствия между этими признаками нет, н нередко как раз наиболее злокачественные новообразования отличаются мономорфностью.
Для новообразований также характерно значительное варьирование формы, размеров и плотности ядер опухолевых клеток, высокое ядерно-цитоплазматическое отношение. Нередко ядра бывают крупные, резко полиморфные, гиперхромные. Они могут содержать несколько ядрышек, иногда гипертрофированных.
Изменения хроматина в опухолевых клетках могут характеризоваться нарастанием процесса его гетерохроматизации, при этом интенсивно окрашивающийся гетерохроматин имеет мелко- или круиноглыбчатое строение, занимает периферические или центральные участки ядра или распределяется диффузно по нему. Соответственно варьируют светлоокрашенные участки, содержащие эухроматин. Следует сказать, что соотношение в ядрах гетерохроматина, являющегося более инертной (конденсированной) частью хроматина, и эухроматяна, содержащего основную массу активно функционирующих генов, значительно варьирует от опухоли к опухоли н от одной клетки к другой в одном и том же новообразовании, отражая степень дифференцнровки ядра. На гистологических препаратах, окрашенных гематоксилином и эозином, степень гиперхромиости ядер обусловлена выраженностью в них гетерохроматизации.
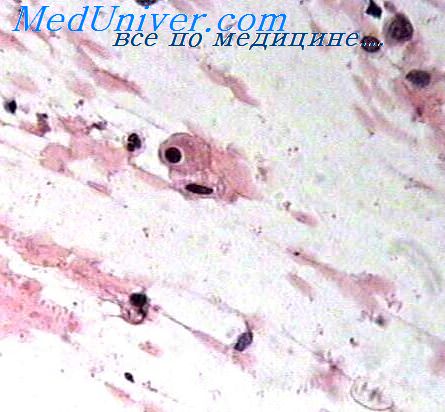
Специализированной разновидностью гетерохроматина является так называемый половой хроматин, иногда встречающийся в виде отдельной глыбки, часто расположенной под ядерной мембраной н образующейся за счет инактивации целой Х-хромосомы или ее части. Некоторые исследователи считают, что, во-первых, чем ниже содержание полового хроматина, в частности при раке молочной железы, тем выше степень злокачественности опухоли, и, во-вторых, они видят прямую связь между содержанием полового хроматина и гормональной чувствительностью опухоли. Обе эти точки зрения о значении полового хроматина не без основания оспариваются. При определении гормональной чувствительности опухоли предпочтение следует отдавать высокоспецифичным и высокочувствительным методам определения рецепторов гормонов, расположенных на поверхности опухолевых клеток и определяющих «поведение» последних.
Каждая конкретная опухоль обычно представляет собой популяцию клеток с изменчивым числом хромосом, т. е. неравномерным содержанием ДНК. Однако в опухоли при этом можно обычно выделить одну, две или несколько модальных линий со стабильно повышенным содержанием ДНК, соответствующим определенной плоидности числа хромосом. Гистограммы, построенные на основании цитоспектрометрни, цитоспектрофлуориметрии, импульсной цитофотометрии или иных способов, отражают модальную линию или линии и все варианты содержания ДНК в данной опухоли. Их анализ может иметь важное практическое значение для дифференциальной диагностики предопухолевых и опухолевых процессов, так как при последних количество ДНК увеличено.
Морфологическая катаплазия опухолевых клеток значительно варьирует от новообразования к новообразованию, в связи с чем делались многочисленные попытки найти корреляцию между ее выраженностью и степенью злокачественности опухоли.
Распространение получило исследование степени злокачественности плоскоклеточного рака гортани на основании определения различных сторон клеточной катаплазии (расположения клеток, степени их кератинизации, ядерного полиморфизма, митозов и др. ).
Разбирая значение клеточной катаплазии в определении степени злокачественности опухоли с точки зрения ее прогноза, следует подчеркнуть два обстоятельства. Во-первых, использование электронной микроскопии в диагностике опухолей человека позволяет, как никогда раньше, объективно оценивать степень дифференцировки опухолевых клеток и их гистогенетическую (точнее цитогенетическую) принадлежность, о чем подробнее будет изложено в следующем разделе. Во-вторых, важным является определение не одного, а суммы факторов (признаков), определяющих в своей совокупности степень злокачественности и прогноз для конкретного вида опухоли, в связи с чем наибольшие перспективы имеет многофакторный анализ с использованием электронно-вычислительной техники.
В определении степени злокачественности опухоли и ее прогноза важное значение имеют не только признаки клеточной катаплазни, но и другие факторы, как, например, состояние стромы, лимфоидная инфильтрация, глубина инвазии и многие иные клинико-анатомические проявления опухолевого роста, которых мы в рамках данной статьи не касаемся, но учитывать которые необходимо.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Доброкачественные опухоли щитовидной железы. Фолликулярный рак щитовидной железы.
Онкоцитарная аденома (аденома из В-клеток, клеток Ашкинази, клеток Гюртля) нередкая, преимущественно трабекулярного строения аденома, состоящая из тяжей крупных, светлых клеток с нежнозериистой цитоплазмой, напоминающих генатоциты. Оикоциты обладают высокой активностью сукцинатдегидрогеназы. Обычно фолликулообразование в них не выражено. В смешанных случаях онкоциты как бы наслаиваются на структуру юй или иной формы аденомы. Макроскопически онкоцитома имеет вид мятого узла желтого цвета.
Аденома из парафолликулярных С-клеток (апудома). В 50-е годы были выделены аденомы, источником развития которых оказались С-клетки, относящиеся к APUD-системе. Апудома имеет вид узла диаметром 3-5 см, серо-желтого цвета, разной плотности. Гистологически она opганондного строения и состоит из трабекуляриых и альвеолярных структур, из округлых, полигональных или веретенообразных клеток с бледной цитоплазмой и гиперхромным ядром. Moiyt наблюдаться некоторый клеточиый полиморфизм, образование ритмичных каршшоидных и перицитарных структур и псевдорозеток. Строма скудная, иногда содержит амилоид. Для верификации анудом необходимы электронная микроскопия, серебрение срезов и гистохимические методики (наличие щелочной эстераэы, сероюнина. везикул и гранул). Отсутствие чегких различий между локальными и метастазируюшими С-клеточными опухолями затрудняег дифференциацию аиудомы и медуллярного рака.
При всех формах аденом могут быть полиморфизм и атиния клеток при отсутствии основных признаков злокачественности способности к инвазии и метастазированию. Некоторые авторы предлагают называть такие опухоли а типичными адепомами. Однако большинство клиницистов негативно относится к этому термину, допуская лишь диагноз аденома или рак. В силу этого вместо понятия а типичная аденома целесообразно давать определение ее формы с характеристикой особенностей роста. Например, «трабекулярная аденома с пролиферацией и атинией, без признаков инвазии». Среди них могут встречаться карликовые экземпляры.
Рассмотренные разновидности аденом бывают в чистом виде, однако чаще наблюдают смешанные формы, что свидетельствует о едином гистогенезе их из трех клеточных зачатков (А. В и С-клеток).
С возрастом аденом нарастают вторичные изменения: фолликулы атрофируются и исчезают, секрет попадает в отечную строму, окружая группы уродливых эпителиальных клеток с причудливой формы ядрами. Происходит очаговое отложение извести, амилоида, костной и хрящевой ткани, кистообразование, что связано с расстройством васкуляризации. Возникающие очаги клеточной и стромальной атипии, имитирующие злокачественный рост, наблюдают главным образом в центре узла, в отличие от истинной малигнизации, которую следует искать прежде всего на периферии в зоне капсулы и субкансулярных сосудов, на границе с нормальной тиреоидной тканью.
При дифференциации аденомы от узловатою зоба принимают во внимание то, что аденома обычно одиночна, инкапсулирована, лишена дольчатого строения, резко отличается от сдавленной ею тиреоидной ткани.
Фолликулярный рак — самая сложная в диагностическом отношении форма рака» характеризующаяся дифференцировкой в направлении зрелой тиреоидной ткани. Это объясняет разнобой статистических данных (5—40%). Наблюдают преимущественно у женщин в возрасте 50—70 лет. Макроскопически имеет вид узла» похожего на фолликулярную аденому. Стереоморфологическое исследование иногда позволяет выявить инвазию паренхимы опухоли в капсулу и некоторую пестроту ее структуры.
При высокодифференцированной форме раковые элементы в большей или меньшей степени напоминают фолликулы зрелой щитовидной железы. Они различных размеров и формы; клетки, их выстилающие, могут быть с гиперхромными ядрами, наползающими одно на другое в виде притертых часовых стекол.
Пожалуй, только в щитовидной железе одно наличие атипии и полиморфизма клеток еще не решает вопроса о малигнизации. Не меньшее значение имеет характер роста, особенно склонность опухоли к инвазии и диссеминации. Непредсказуемая способность некоторых, казалось бы, зрелых опухолей щитовидной железы к метастазированию, по-видимому, связана с анатомотопографическими особенностями шейной области, в которой при огромной насыщенности сосудами возникает отрицательное давление, создающее биологические предпосылки к диссеминации и генерализации процесса.
Умеренно дифференцированный вариант фолликулярного рака состоит из солидных комплексов опухолевых клеток, иногда в виде выступов, расположенных внутри фолликулов. 6 отличие от сосочков папиллярного рака основа этих выступов целиком занята опухолевыми клетками. К этой разновидности рака относится пролиферирующая струма Лангханса, состоящая из ажурной сети фолликулярных клеток, окружающих мелкие полости и сосудистые щели.
Одной из разновидностей фолликулярного рака, которую не следует смешивать с раком из В-клеток и метастазом гипернефроидного рака, является светлоклеточный рак. Он состоит из клеток со светлой цитоплазмой и небольшим центрально расположенным ядром, формирующих микрофолликулы, солидные и иногда сосочковые структуры. Этот рак встречается крайне редко и отличается от метастаза светлоклеточного рака почки отсутствием липоидов.
Фолликулярный карликовый рак диаметром до 1 мм выявляется случайно в толще узлового или диффузного зоба или аденомы. Имеет вид желтовато-серого узелка. Стереоскопически и гистологически он в миниатюре воспроизводит структуру обычного фолликулярного рака. Отличием его от маленькой фолликулярной аденомы и склерозирующейся микрокарциномы является наличие капсулы с участком инвазии.
Фолликулярный рак развивается медленно, первым проявлением болезни обычно бывают отдаленные, реже регионарные метастазы. В отличие от других форм рака фолликулярная аденокарцинома иногда характеризуется гормональной активностью, причем чем выше степень катаплазии, тем слабее секреторная функция. В раке, имеющем солидное строение, коллоид обычно не содержится.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
- при профилактических осмотрах цитологические мазки следует брать у женщин независимо от жалоб, наличия или отсутствия изменений слизистой оболочки. Цитологическое исследование следует повторять не реже, чем раз в три года;
- желательно получать мазки не ранее, чем на 5-е сутки менструального цикла и не позднее, чем за 5 суток до предполагаемого начала менструации;
- нельзя брать материал в течение 48 ч после полового контакта, использования любрикантов, раствора уксуса или Люголя, тампонов или спермицидов, спринцевания, введения во влагалище медикаментов, свечей, кремов, в т. ч. кремов для выполнения ультразвукового исследования;
- беременность – не лучшее время для скрининга, так как возможны неправильные результаты, но, если нет уверенности, что женщина придет на обследование после родов, лучше мазки взять;
- при симптомах острой инфекции желательно получать мазки с целью обследования и выявления патологических изменений эпителия, этиологического агента; также необходим цитологический контроль после лечения, но не ранее, чем через 2 мес. после окончания курса.
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.

Нарушение строения эпителиальных клеток — это термин для обозначения клеток необычного размера или формы, обнаруженных на шейке матки. Этот результат теста, чаще всего полученный после мазка Папаниколау, не обязательно указывает на злокачественный рост опухоли, но уже говорит о том, что могут быть предраковые клетки или начальные раковые клетки.
Особенности анализа на атипичные клетки
- Существует несколько категорий аномальных клеток, которые можно обнаружить с помощью мазка Папаниколау. Поэтому анализ очень ценится в гинекологии.
- При обнаружении атипичных клеток может потребоваться повторное тестирование, иногда с интервалом в два-три месяца в зависимости от результатов. Это необходимо для подтверждения диагноза или для контроля лечения.
- Во многих случаях аномалия эпителия состоит из клеток, которые функционируют и растут нормально. Но такое состояние требует внимания — клетки способны быстро перерождаться.
Типы аномалий
Атипичные эпителиальные клетки делятся на две широкие категории: плоскоклеточные и железистые.
- Плоскоклеточные клетки — это просто гладкие клетки поверхностного слоя.
- Железистые клетки несут определенную функцию, например, выделяют вещества, такие как гормоны или пот.
Наиболее распространенными типами являются атипичные плоскоклеточные клетки (ASC), плоскоклеточные интраэпителиальные образования (SIL) или плоскоклеточный рак. Проблемы, возникающие обнаружением железистых клеток обычно классифицируются как атипичные железистые клетки (AGC) или аденокарцинома.
Из обнаруженных плоскоклеточных и железисто-клеточных аномалий только имеющие признаки плоскоклеточного рака и аденокарциномы почти наверняка указывают на развитие рака.
ASC-клетки
ASC-клетки явно не нормальны, но не совсем понятно, почему. Клетки в этой категории могут быть либо атипичными плоскоклеточными неопределенного значения (ASCUS), либо атипичными плоскоклеточными клетками с возможными изменениями высокого уровня риска рака (ASC-H).
- Первый тип, как правило, не вызывает особого беспокойства, хотя гинекологи обычно рекомендуют сдать повторный мазок Папаниколау, чтобы быть уверенным в диагнозе.
- Второй тип указывает на то, что на поверхности шейки матки могут быть SIL-клетки или другие предраковые клетки, но это не совсем точно, поэтому гинеколог дополнительно проводит кольпоскопию.
Кольпоскопия — диагностический тест, при котором гинеколог визуально исследует внутреннюю часть влагалища на наличие патологий или повреждений.
SIL-клетки
SIL — это клетки, образующие наросты на поверхности шейки матки, которые могут привести к раку. Они относятся к категории среднего или высокого риска в зависимости от вероятности возникновения рака.
После обнаружения SIL-клеток специалист обычно рекомендует кольпоскопию или биопсию, чтобы подтвердить уровень риска, связанного с обнаружением данной клетки.
Плоскоклеточный рак
Плоскоклеточный рак — наиболее распространенный тип рака шейки матки и может быть смертельным, если его не лечить.
Если на него указывает мазок Папаниколау, гинекологи срочно проводят кольпоскопию или биопсию, чтобы определить, на какой стадии находится рак, начиная с «in situ», что означает, что раковые клетки существуют, но еще не распространились в ткани, до стадии 4, на которой рак распространился за пределы шейки матки.
Как только это будет определено, женщина может начать лечение.
AGC-клетки
Их обнаружение может указывать на то, что у железистых клеток в шейке матки или слизистой оболочке матки, также называемой эндометрием, могут возникнуть проблемы. Около половины случаев обнаружения AGC-клеток не вызывают беспокойства, как ASCUS. Однако они могут быть предраковыми, поэтому также нужно пройти биопсию для уверенности.
Аденокарцинома
Это довольно редкий тип рака, который похож на плоскоклеточный рак, но поражает железистые клетки.
Как и в случае обнаружения плоскоклеточного рака, необходимо срочное дополнительное тестирование для определения стадии рака, а затем начинают лечение.
Причины
Одна из причин появления аномальных эпителиальных клеток — дисплазия шейки матки. В этом случае шеечные клетки растут ненормально, и они либо имеют странную форму, либо разрастаются в огромных количествах.
Рост клеток не является однозначно злокачественным симптомом, но со временем аномальная клетка может переродиться в рак в течение примерно 10 лет или немного дольше. Дисплазия шейки матки чаще встречается у женщин от 25 до 35 лет и обычно не имеет симптомов.
Иногда сообщается о необычных клетках, возникающих из-за инфекций, таких как герпес и вирус папилломы человека. ВПЧ — один из ведущих факторов риска развития рака шейки матки.
Наличие паразитов или грибковых инфекций также может дать положительный результат. Клеточная ткань может оказаться ненормальной из-за травмы. Если есть подозрение на инфекцию или травму, то, как правило, не возникает проблем с диагностикой рака в результате обнаружения такой аномалии эпителиальных клеток.
Лечение
Лечение аномалий эпителиальных клеток зависит от конкретной проблемы.
- Если клетки не злокачественные, обычно не проводится немедленное лечение, за исключением более худших повторных анализов.
- Лечение раковых поражений может варьироваться от случая к случаю. Если они обнаруживаются на ранней стадии, состояние часто поддается лечению с незначительным набором процедур — лазерное лечение и радиоволноваятерапия.
- Более сложные случаи могут потребовать хирургического вмешательства, химиотерапии и лучевой терапии.
Читайте также:

