Зуд кожи при альцгеймера
Обновлено: 28.04.2024
Зуд кожи является одним из наиболее распространенных своеобразных ощущений, возникающих под действием различных факторов. Зуд кожи сопровождается нанесением повреждений в виде расчесов различной степени выраженности. Единой точки зрения относительно спец
Зуд кожи является одним из наиболее распространенных своеобразных ощущений, возникающих под действием различных факторов. Зуд кожи сопровождается нанесением повреждений в виде расчесов различной степени выраженности. Единой точки зрения относительно специфичности рецепторов, объективирующих ощущение зуда, не существует. Большинство исследователей сходятся во мнении, что чувство зуда и боли воспринимается окончаниями безмиелиновых нервных волокон из дермо-эпидермальной зоны и передается в корковые центры головного мозга. При этом ученые не отрицают участие в этом процессе тактильных и осязательных рецепторов.
Зуд — это своеобразный сигнал об опасности, возникающий в результате воздействия на организм того или иного фактора, являющийся защитной реакцией и выступающий как механизм адаптации к среде. С физиологической точки зрения его можно определить, как восприятие сознанием кожного ощущения с последующим возникновением двигательной реакции, целью которой является устранение раздражителя с поверхности кожи. Зуд как симптом и как заболевание упоминается в трудах Гиппократа, Авиценны, Галена. В 1694 г. I. Lazonius описал тяжелую форму зуда, назвав это состояние pruritus (цит. А. М. Аминев). Из отечественных ученых проблемами зуда занимались И. Я. Раздольский (1922), П. В. Никольский (1922), А. М. Аминев, В. Л. Головачев, Ю. С. Скрипкин (1967), Ю. С. Бутов (1975), Е. В. Соколовский (1998), Г. И. Суколин и др. (2002).
Зуд может выступать как симптом при различных дерматозах и соматической патологии и как самостоятельное заболевание, входящее в группу нейродерматозов. Механизм зуда полностью не изучен. Известно, что у больных, страдающих кожным зудом, в коже в больших количествах накапливаются гистамин, брадикинин, энкефалин, опиатные белки и множество других различных пруритогенов, включая энзимы. Различают зуд физиологический и патологический.
Физиологический зуд, несильный и непродолжительный, возникает как ответ кожи на адекватные раздражения окружающей среды, в том числе длительное давление на ткани, трение, ползающих насекомых и другие факторы.
Возникновение патологического зуда связано с соматической патологией либо с дерматозами. При этом он становится более интенсивным, сопровождается глубокими повреждениями кожи, протекает в форме пароксизмов с выраженными невротическими нарушениями, неадекватными реакциями, нарушением сна.
Зуд по распространенности подразделяется на универсальный и локализованный. Развитие универсального зуда различной интенсивности связано с заболеваниями печени (гепатит, цирроз, рак), почек (пиелонефрит, амилоидоз), поджелудочной железы (диабет), эндокринной (гипотиреоз, гипертиреоз) и кроветворной (лейкемии) систем. Выяснить причину универсального зуда непросто. Необходимы тщательное изучение анамнеза и всестороннее исследование. Тем более что зуд как моносимптом на ранних стадиях может быть первым признаком онкологических заболеваний. Немало проблем связано и с локализованным зудом кожи. Областью наиболее частой локализации ограниченного зуда являются наружные половые органы, зоны ануса, шейно-воротниковая зона, голеностопные суставы. Реже патологический процесс локализуется в области внутренней поверхности бедер, голеней.
Согласно определению J. Jockart-Hummery (1931), pruritus ani представляет собой часто встречающееся, весьма неприятное и характеризующееся упорным течением заболевание (А. М. Аминев). Наблюдается почти исключительно у мужчин, особенно после 40 лет. У женщин встречается в сочетании с pruritus genitalium.
При длительно существующем зуде в коре головного мозга формируется доминанта — очаг патологического возбуждения, происходит стереотипизация нервных процессов, и зуд из защитной реакции превращается в стандартную реакцию на различные внешние раздражители. Формирующиеся на коже морфологические изменения в виде расчесов-экскориаций, трансформирующихся в последующем в лихенификацию, приводят к изменению чувствительности периферических рецепторов, снижению порога восприятия зуда и формированию ограниченного нейродермита.
Анальный зуд может быть первичным и вторичным, острым и хроническим. Этиология анального зуда зависит от многих факторов. Так, серьезную проблему представляют заболевания аноректальной области в виде анальных трещин, свищей, геморроя, проктитов, гипертрофии и воспаления анальных сосочков, хронических проктосигмоидитов, перианальных кондилом, лейкоплакий, дисфункций сфинктера, гнойного гидраденита, сопровождающиеся сильным зудом. Патологические процессы, протекающие в данной области, обусловлены изменениями рН в щелочную сторону, увеличением остаточного азота, раздражением нервных рецепторов перианальной области и возникновением зуда.
Заслуживают внимания исследования А. И. Рождественского, указывающие на серьезную роль, которую играет скрыто протекающий хронический проктосигмоидит или аногенитальный герпес. Формирование анального зуда автор связывает с резким сдвигом pH в щелочную сторону до 8,5–10,0 в сигмовидной и прямой кишках, усиливающим дисбактериоз и процессы гниения. Зуд никогда не развивается при повышенной кислотности в кишечных массах. Высокая концентрация протеолитических ферментов, воздействующих на нервные окончания, приводит к возникновению зуда. Вследствие усиленного протеолиза в пораженной коже в два-три раза (с 50—70 мг% в норме до 140—170 мг% при патологии) нарастает содержание остаточного азота, при этом, однако, в самих чувствительных окончаниях перианальной кожи каких-либо характерных изменений обнаружено не было. Вторичный зуд в качестве основного симптома возникает при соматических заболеваниях или дерматозах. Так, нарушение функциональной и перистальтической активности толстой кишки создает условия для задержки каловых масс и дополнительного инфицирования простаты. Это подтверждается частым обнаружением E. Coli в секрете простаты у пациентов с хроническим вялотекущим простатитом, что дает основание предположить наличие трансмиссии микроорганизмов из толстой кишки в простату и их участие в поддержании хронического процесса (А. М. Осадчук и др.). В литературе приводятся данные о том, что в ряде случаев хроническая дизентерия также может выступать в качестве фактора, обуславливающего развитие зуда (А. И. Фишбейн).
Зуд перианальной области может возникать при доброкачественной или злокачественной гиперплазии простаты. В 92% случаев в патологический процесс вовлекается толстая кишка. При этом в кишечнике отмечаются дисбиотические изменения различной степени выраженности, сопровождающиеся значительными морфологическими изменениями апудоцитов, как с увеличением их количества, так и повышением функциональной активности.
У пациентов с инфекционными заболеваниями урогенитального тракта (хламидиоз, уреаплазмоз, микоплазмоз, герпетическая инфекция, гонорея, трихомониаз, сифилис), особенно при рецидивирующем течении, отмечаются значительные изменения микробиоценоза кишечника (В. И. Кисина), которые сопровождаются выраженными ощущениями зуда, жжения и обусловлены воздействием токсинов бактерий, а также непосредственно кишечной слизи на нервные окончания перианальной области.
Гинекологическая патология (кольпиты различной этиологии, бактериальный вагиноз, крауроз вульвы, лейкоплакия), беременность, состояние менопаузы нередко сопровождаются зудом различной интенсивности. Возникновение зуда при беременности связывают с холестазом. Зуд, обусловленный холестазом, может также развиваться у женщин, принимающих пероральные контрацептивы. В отдельных случаях зуд наружных половых органов у женщин связывают с нейротрофическими и гормональными нарушениями (В. Л. Говорухина).
Особо следует обратить внимание на атопический дерматит, экзему, псориаз, красный плоский лишай, гельминтозы, чесотку, фтириаз, микозы, ксеродермии, характеризующиеся упорным течением и сопровождающиеся интенсивным зудом.
Патофизиология зуда при атопии до сих пор полностью не раскрыта. Его возникновение связывают с нарушениями в центральных и периферических отделах нервной системы, обусловленными феноменом β-адренергической блокады, активизацией биологически активных веществ, катехоламинов, ферментов (О. А. Синявская, Н. П. Торопова, 1993). Важную роль играют аутоиммунные нарушения, приводящие к накоплению IgE-комплексов, эозинофилов, цитокинов и медиаторов, определяющих формирование зуда и воспалительного процесса.
Ксеродермии чаще встречаются у пожилых и, более того, являются самой распространенной причиной зуда в этой возрастной группе. Ксероз в пожилом возрасте обусловлен пониженным содержанием воды и гиалуроновой кислоты в коже.
Определенное значение в формировании зуда играют аскаридоз, энтеробиоз, онхоцеркоз (И. Л. Микадзе, И. М. Ижевский), связанный с аллергизацией к чужеродному белку. Эндокринные и метаболические нарушения, такие, как сахарный диабет, гипертиреоз, тиреотоксикоз, карциноидный синдром, могут сопровождаться зудом, при этом важная роль отводится повышению активности кининов, активации бактериальной, кандидозной и дерматофитной инфекций.
Патология гепатобиллиарной системы, заболевания почек приводят к выраженным изменениям биохимии крови, накоплению токсических продуктов и развитию периферических нейропатий. В большинстве случаев гематологические и лимфопролиферативные заболевания сопровождаются выраженным зудом. В качестве медиаторов в настоящий момент рассматриваются гистамин и лейкопептидазы, выделяемые патологическими лимфоцитами и гранулоцитами.
Наибольший интерес и трудность в плане диагностики представляет паранеопластический зуд. На связь кожного зуда со злокачественными опухолями впервые указал еще в 1896 г. Дарье. Хотя и не часто, зуд может быть первым проявлением злокачественных опухолей внутренних органов, поэтому среди причин зуда неясного генеза опухоли занимают важное место. Паранеопластический кожный зуд отмечается у половины всех больных страдающих раком желудка, прямой кишки и у 1/4 больных с новообразованиями гениталий (Е. В. Соколовский, 1998). Нельзя отрицать важности воздействия факторов окружающей среды, так как они в значительной степени влияют на чувствительность кожи к пруритогенным стимулам. Хорошо известно, что существует связь между порогом восприятия зуда и температурой кожи, повышенной влажностью, ношением одежды из синтетических, шерстяных тканей, использованием разнообразных порошков, антистатических препаратов, дезодорантов, а также и ароматизированной туалетной воды.
Стресс, эмоциональные переживания отрицательно сказываются на течении любого заболевания, и зуд в этом смысле не является исключением.
При назначении лекарственных препаратов необходимо учитывать их побочное действие. Так, например, при лечении хронических запоров назначение касторового, вазелинового или миндального масла может непроизвольно приводить к загрязнению заднего прохода и вызывать зуд. Применение некоторых антибактериальных, сульфаниламидных, морфиноподобных препаратов, анальгетиков приводит к сенсибилизации, развитию аллергических реакций и формированию зуда. Прием определенных пищевых продуктов (томаты, пряности, вина, кофе, кока-кола и т. д.) может также провоцировать развитие кожного зуда.
Необходимо тщательно изучить жалобы, анамнез жизни, а также анамнез болезни пациентов, страдающих кожным зудом. С помощью скрининговых методов определяют уровень глюкозы в крови, проводят тест на толерантность к глюкозе, выявляющий уровни холестерина, билирубина, мочевины, мочевой кислоты, креатинина, железа; берут анализ кала на наличие гельминтов, диагностируют дисбактериоз и т. д. Затем больным проводят углубленное инструментальное обследование и направляют на консультации к специалистам.
Лечением зуда врачи занимались еще в древности, но и до настоящего времени проблема лечения этого заболевания не потеряла актуальности. «Не одна заработанная тяжелым трудом врачебная репутация разбилась вдребезги об этот подводный камень» (J. F. Montague). Упорное течение кожного зуда, неэффективность в ряде случаев общего и наружного лечения диктуют необходимость использовать индивидуальный подход к лечению этого заболевания, с учетом выявленных этиопатогенетических механизмов.
Диетотерапия
В связи с выраженной дисфункцией со стороны ЖКТ, своевременно и адекватно назначенная диетотерапия в большинстве случаев, способствует достижению ремиссии заболевания или полному выздоровлению. Гипоаллергенная диета предусматривает исключение продуктов, способных вызывать и спровоцировать развитие или обострение кожного зуда. Из пищевого рациона больных исключают продукты, содержащие красители, консерванты, эмульгаторы, а также яичный белок, крепкие мясные бульоны, жареное, пряности, рыбу, икру, сыры, кофе, мед, шоколад, цитрусовые фрукты, алкоголь, кока-колу, томаты и др.
В рацион включают легко усвояемые, калорийные каши (из овсяных, гречневых, перловых круп), кисло-молочные продукты, отварные овощи и мясо. Рекомендуемые диеты должны быть оптимальны по содержанию белков и витаминов и составляться в тесном сотрудничестве с диетологом.
Гигиенические мероприятия
Медикаментозная терапия
В связи с наличием выраженных невротических реакций назначают седативные препараты. Мягким седативным действием обладают препараты растительного происхождения — настойка пиона, пустырника, корня валерианы, ново-пассит. Используются антидепрессанты — амитриптилин внутрь 0,025—0,05 г; ниаламид внутрь 0,025—0,01. Из транквилизаторов назначают диазепам 0,005—0,015 в сутки, лоразепам 0,001—0,0025 г в сутки. Назначение антигистаминных препаратов обусловлено высоким уровнем гистамина в тканях и его важной ролью в механизме кожного зуда. Целесообразно назначение антигистаминных препаратов второго поколения — лоратидин, терфинадин, цитиризин, эбастин, семпрекс, телфаст, зиртек, тавегил и др., которые более эффективно снимают зуд, так как уменьшают беспокойство больных и вторичную адренергическую стимуляцию. Целесообразно назначение ферментных препаратов, таких, как вобэнзим, флогэнзим по 2-3 драже (таблетки) три раза в день за 30 мин до приема пищи. После проведенного лечения необходимо проводить комплекс профилактических мероприятий, которые включают в себя гигиенические мероприятия, рациональную гипоаллергенную диету, предупреждение заболеваний и действия эндо- и экзогенных факторов, способных вызывать зуд. По вопросам литературы обращайтесь в редакцию
Ю. С. Бутов, доктор медицинских наук, профессор
Е. П. Коновка
РГМУ, Москва
Старческий зуд – это разновидность идиопатического зуда, который развивается у людей пожилого возраста. Среди основных причин проблемы называют чрезмерную сухость кожи, хронические дерматозы, соматические заболевания. Патология проявляется постоянными субъективно неприятными ощущениями и потребностью механического раздражения кожи для их купирования. Комплексная диагностика старческого зуда требует дерматоскопии, стандартного набора анализов крови и мочи, методов инструментальной визуализации внутренних органов. Лечение состоит из интенсивного увлажнения кожи, применения местных и системных противозудных средств, методик физиотерапии и психотерапии.
МКБ-10



Общие сведения
Старческий (сенильный) зуд – распространенное состояние, которое беспокоит более 50% людей старше 70 лет. Мужчины болеют чаще женщин. Старческий зуд представляет серьезную физическую и психологическую проблему для пациентов, снижает качество жизни и становится причиной стойких эмоциональных расстройств. Перед специалистами в сфере практической дерматологии возникает сложная задача эффективного купирования симптомов и устранения их первопричины, что не всегда возможно, несмотря на усовершенствование клинических протоколов.

Причины
Кожный зуд у пожилых пациентов относятся к идиопатическим заболеваниям, его точные этиологические факторы пока не установлены. Большинство экспертов сходятся во мнении, что в развитии проблемы играют роль, как возрастные изменения структуры кожного покрова, так и системные нарушения работы организма, которые типичны для пациентов старческого возраста. К основным причинам сенильного зуда относятся:
- Сухость кожи. В пожилом возрасте происходят гистологические перестройки эпидермиса и дермы, снижается количество гиалуроновой кислоты, кожа теряет тургор и эластичность. Физиологические изменения вызывают сильную сухость, которая при отсутствии адекватного косметического ухода становится причиной зуда.
- Кожные заболевания. Неприятные ощущения развиваются на фоне экземы, грибковых инфекций, чесотки и других дерматозов, которые могут протекать со скудными объективными признаками. Зачастую заболевания не диагностируются вовремя из-за поздней обращаемости пожилых людей к врачу.
- Метаболические расстройства. К основным причинам формирования старческого зуда относят атеросклероз, железодефицитную анемию, снижение толерантности глюкозе и развитие сахарного диабета 2 типа. Изредка проблема связана с гипотиреозом, недостаточностью функции надпочечников.
- Заболевания внутренних органов. Типичными причинами зуда у людей старческого возраста выступают холестаз, хроническая почечная недостаточность, функциональные и органические заболевания ЖКТ. Неприятный симптом может быть одним из первых признаков онкопатологии органов брюшной полости, центральной нервной системы.
Патогенез
Зуд считается одним из вариантов восприятия раздражения кожным анализатором. Он возникает по тем же механизмам, что и чувства прикосновения, болевые реакции. Ощущения вызваны механическими, термическими, химическими и электрическими воздействиями на периферические нервные волокна типа С, которые составляют около 5% нервов и отличаются медленным проведением импульсов. Появлению симптома способствуют медиаторы: гистамин, вещество P, интерлейкины и простагландины.
В отличие от боли, которая провоцирует безусловный рефлекс «избегания», при зуде активизируются процессы обработки. Возникающие в коре головного мозга импульсы стимулируют человека почесывать, растирать, разминать зудящие участки, чтобы получить моментальное удовлетворение. Такие действия вызывают сильные тактильные и болевые импульсы, которые подавляют слабые сигналы зуда и на короткое время облегчают состояние.
Предполагается, что в развитии сенильного зуда играют роль возрастные трансформации структуры нервных волокон. В старческом периоде нарушается восприятие боли, изменяются центральные механизмы ингибирования зуда, поэтому такой симптом является более стойким и мучительным, чем у молодых людей. Уменьшение толщины кожи на 20% также участвует в патофизиологии зудящего дерматоза.

Симптомы старческого зуда
Первично возникает неприятное субъективное ощущение, которое сопровождается постоянным желанием расчесывать кожу, чтобы от него избавиться. Для старческого возраста типичен генерализованный зуд, который преимущественно начинается в области спины и туловища, постепенно распространяясь по всему телу с захватом волосистой части головы. Многие пациенты жалуются, что симптоматика усиливается при снятии одежды, в ночное время.
При идиопатической форме зуда на коже отсутствуют воспалительные элементы и высыпания. Постепенно на фоне расчесов формируются корочки и экскориации, кожные покровы утолщаются, покрываются трещинами и шелушением. При глубоком и многократном повреждении в отдельных зонах тела наблюдаются кровянистые корки. Вследствие привычки чесать зудящую кожу ногти на руках пациентов становятся гладкими и отполированными.
Осложнения
Старческий зуд существенно влияет на общее состояние и качество жизни пожилых людей. Длительно существующие симптомы вызывают бессонницу, дополняются ажитацией и раздражительностью пациентов. В тяжелых случаях неконтролируемого генерализованного зуда возникают депрессивные состояния, сопровождающиеся суицидальными мыслями и отдельными попытками их реализации.
Раны, которые образуются на месте глубоких расчесов кожи, становятся входными воротами для вторичной инфекции. На фоне физиологического снижения иммунитета в старческом возрасте существует высокий риск пиодермий, кожных микозов. В неблагоприятных случаях инфекционные агенты распространяются вглубь мягких тканей, вызывая флегмоны, длительно незаживающие язвы.
Диагностика
Старческий зуд рассматривается как диагноз-исключение, поэтому для его постановки требуется обследование у дерматолога и других профильных специалистов. Диагностика начинается с детального выяснения жалоб больного, давности появления симптомов и возможных провоцирующих факторов. Затем проводится внешний осмотр кожных покровов тела, чтобы выявить возможные первичные признаки дерматоза. В полную программу обследования входят следующие методы:
- Дерматологическая диагностика. Всем пациентам проводится обследование кожного покрова методом дерматоскопии, при подозрении на микоз показана люминесцентная диагностика лампой Вуда. При вторичном инфицировании расчесов требуется бактериологическое исследование мазка или соскоба поврежденных участков.
- Лабораторный комплекс. Для уточнения метаболического статуса и наличия соматических проблем проводится гемограмма, биохимическое исследование крови с печеночными пробами и липидограммой, анализы мочи и кала. Обязательно определяют уровень глюкозы натощак, по показаниям выполняется расширенный гормональный профиль.
- Инструментальные методы. Как скрининговые методы для исключения болезней внутренних органов назначают УЗИ брюшной полости и малого таза, сонографию щитовидной железы, контрастную рентгенографию желудочно-кишечного тракта.
- Консультация психиатра. Учитывая высокую частоту старческого слабоумия и сенильных психозов, при отсутствии других причин кожной симптоматики рекомендуется обследование у психиатра. При необходимости к диагностике подключают невролога, проводят КТ головного мозга и прочие методы нейровизуализации.

Лечение старческого зуда
Пациентам назначается комплексная симптоматическая терапия, которая определяется длительностью и тяжестью клинических проявлений. Значимую роль в коррекции субъективной симптоматики играют немедикаментозные меры, такие как водные процедуры с применением щадящей косметики, ношение легкой одежды из натуральных тканей, поддержание комфортной влажности и температуры в квартире.
Пусковым фактором старческого зуда является ксероз, поэтому на первый план выходят меры по глубокому увлажнению и питанию кожи. Для ежедневного ухода рекомендованы эмоленты, которые сочетают смягчающие, регенерирующие, антиоксидантные и увлажняющие компоненты. Рекомендованы линейки аптечной и профессиональной косметики, созданные для ухода за сухой и чувствительной кожей. В дополнение к ним назначается медикаментозная коррекция:
- Местная терапия. Для локального нанесения на зоны наибольшей интенсивности зуда применяются кремы и бальзамы с местными анестетиками, ингибиторами кальциневрина. Противозудные гормональные мази показывают хороший эффект при сухой коже в старческом возрасте.
- Антигистаминные препараты. Лекарства показаны для быстрого купирования зудящих ощущений. Они действуют на патогенетические механизмы появления старческого зуда, обеспечивают хороший симптоматический эффект. В дополнение назначаются гипосенсибилизирующие средства, стабилизаторы мембран тучных клеток.
- Седативные средства. Для нормализации психоэмоционального фона, ликвидации патологического цикла «зуд–расчесывание» применяются легкие анксиолитики, селективные ингибиторы обратного захвата серотонина.
Для усиления эффекта медикаментозного лечения применяются физиотерапевтические процедуры: акупунктура, рефлекторная лазеротерапия и магнитотерапия, чрескожная нервная стимуляция. По показаниям назначается индивидуальная психотерапия, направленная на коррекцию психоэмоциональных расстройств с учетом особенностей психологии старческого возраста. При неэффективности других видов терапии рассматривается возможность применения гипноза.
Прогноз и профилактика
Хотя старческий зуд не относится к угрожающим заболеваниям, мучительные симптомы существенно осложняют жизнь пациента. Комплексные программы терапии показывают хорошую эффективность для уменьшения или полного устранения субъективных признаков, однако нередко после лечения неприятные ощущения возвращаются. Профилактика проблемы включает правильный уход за старческой кожей, раннее выявление и коррекцию соматических нарушений без полипрагмазии.
1. Дерматовенерология/ под ред. проф. Ю.С. Бутова, акад. РАМН Ю.К. Скрипкина, проф. О.Л. Иванова. – 2013.
3. Синдром кожного зуда в практике врача первого контакта/ Д.И. Трухан// Справочник поликлинического врача. – 2015. – №3.
4. Коррекция кожного зуда у пациентов с зудящими дерматозами, сенильным и идиопатическим зудом/ С.С. Вялов, Г.А. Дроздова// Клиническая дерматология и венерология. – 2014. – №3.
Что такое болезнь Альцгеймера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Поляковой Татьяны Акимовны, невролога со стажем в 13 лет.
Над статьей доктора Поляковой Татьяны Акимовны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
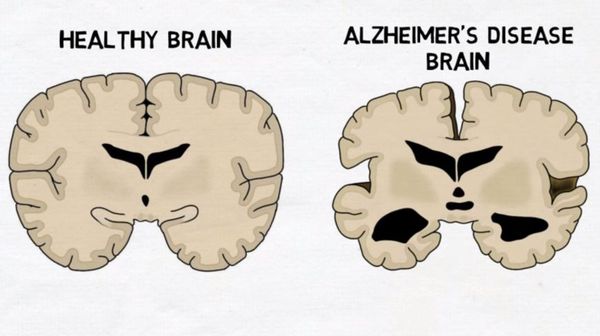
Болезнь Альцгеймера — это хроническое нейродегенеративное заболевание, с медленным началом и значительным ухудшением с течением времени. В 70 % случаев болезнь Альцгеймера приводит к деменции.
Этиология. Факторы риска
Заболевание на данный момент изучено плохо. Предполагается, что в 70% случаев болезнь Альцгеймера объясняется генетическими причинами, среди других факторов риска — черепно-мозговые травмы, депрессия, эндокринные заболевания в анамнезе (гипотиреоз), эстрогенная недостаточность у женщин.
Сопутствующие заболевания
Исследования последних лет показывают, что усиливают предрасположенность к болезни Альцгеймера гипертония, гиперлипидемия, гипергомоцистеинемия, сахарный диабет, метаболический синдром, инсулинорезистентность, заболевания сердца, а также наличие в истории болезни инсульта [1] .
Статистические данные
Болезнь Альцгеймера — наиболее распространённая форма деменции, она встречается в 60–70 % случаев. В мире деменцией страдают около 50 миллионов человек, каждый год выявляется 10 миллионов новых случаев [12] .
В развитых странах болезнь Альцгеймера является одним из наиболее дорогостоящих заболеваний. В России затраты на содержание больных деменцией составляют 74,8 млрд рублей в год [2] .
Распространённость и факторы риска
Заболевание более распространено среди женщин. Предположительно, это связано со следующими факторами:
- продолжительность жизни женщин больше, чем мужчин, а возраст — самый значимый фактор риска развития болезни Альцгеймера;
- риск развития болезни увеличивается на 70 % для людей с депрессией, у женщин она встречается чаще;
- более низкий уровень образования связан с повышенным риском деменции, в некоторых странах у женщин уровень образования ниже, чем у мужчин;
- при беременности часто возникают гипертонические расстройства, они связаны с повышенным риском ухудшения когнитивных функций даже спустя десятилетия после беременности [13] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы болезни Альцгеймера
Признаки болезни Альцгеймера на ранней стадии часто ошибочно принимаются за нормальные признаки старения.
Кратковременная потеря памяти — наиболее распространенный ранний симптом болезни Альцгеймера, который выражается в том, что больному трудно запоминать последние события. В трети случаев заболевание можно распознать по изменениям поведения.
По мере усугубления болезни возникают следующие симптомы:
- проблемы с речью;
- дезориентация;
- перепады настроения;
- потеря мотивации;
- снижение критики;
- больные не в состоянии вспомнить нужное слово, и им приходится заменять его другим (парафазии), однако они хорошо повторяют сказанное.
- со временем возникают затруднения при назывании предметов (аномии).
- уже на ранней стадии возникают трудности с пониманием сложных грамматических структур (семантическая афазия), к которому затем присоединяется отчуждение смысла слова. [3]
Важный признак болезни Альцгеймера — нарушение способности справляться с повседневностью. При заболевании возникают проблемы с самообслуживанием и поведенческие расстройства.
Признаки болезни Альцгеймера у мужчин и женщин
Признаки болезни Альцгеймера у женщин и мужчин схожи, однако у женщин она чаще сопровождается депрессией.
Патогенез болезни Альцгеймера
Существуют отличительные патоморфологические признаки болезни Альцгеймера: амилоидные (сенильные) бляшки — это внеклеточные отложения в виде скопления фрагмента белка, называемые бета-амилоидом; нейрофибриллярные клубочки — скрученные микроскопические нити тау-белка внутриклеточной локализации. Происходит потеря связи между клетками мозга, ответственными за память, обучение и общение. Эти соединения, или синапсы, передают информацию из клетки в клетку. Важная роль в патогенезе принадлежит воспалительному процессу, связанному с активацией микроглии, которая инициируется накоплением амилоида. [1]
Патофизиология болезни Альцгеймера:
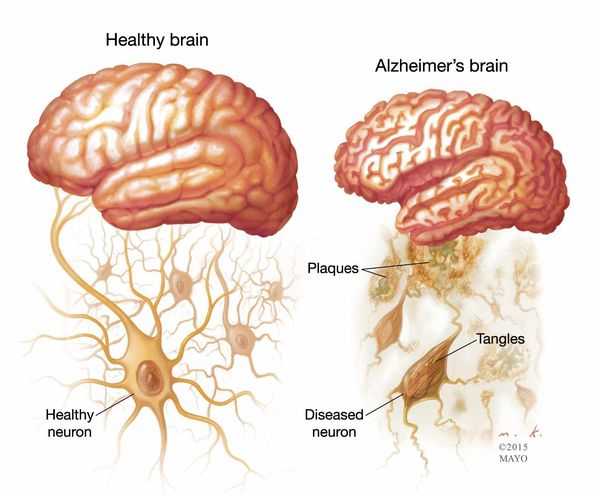
Макроскопически выявляется диффузная атрофия головного мозга с уменьшением объёма извилин и расширением боковых борозд, наиболее выраженная в височно-теменной области.
У значительной части больных цереброваскулярная патология может инициировать или усиливать дегенеративный процесс, связанный с отложением амилоида или другими характерными для заболевания изменениями.
Классификация и стадии развития болезни Альцгеймера
Типичный фенотип болезни Альцгеймера — сочетание выраженных мнестических нарушений гиппокампального типа с акустико-мнестической афазией, зрительно-пространственными нарушениями и апраксией. [3]
Три атипичных фенотипа болезни Альцгеймера (неамнестических):
- с ведущим афатическим дефектом (логопенический вариант первичной прогрессирующей афазии);
- с доминирующими зрительно-пространственными нарушениями (задняя корковая афазия);
- преимущественно с дизрегуляторными нарушениями (лобный вариант болезни Альцгеймера).
Заболевание также подразделяется на формы с ранним началом, зачастую с положительным семейным анамнезом (до 65 лет) и поздним началом (старше 65 лет). Они отличаются патогенезом, генетическими факторами и разной скоростью прогрессирования.
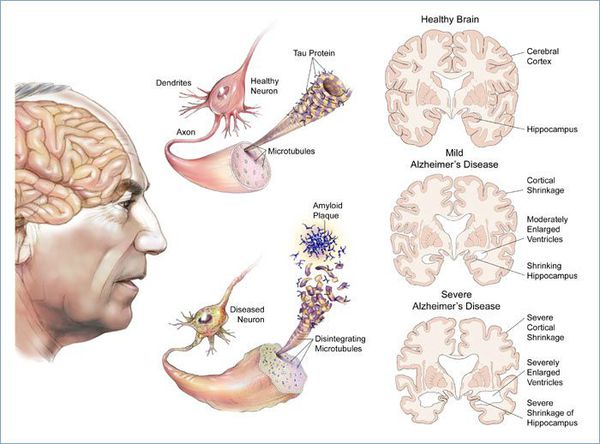
Три стадии болезни Альцгеймера:
Первая (предеменция, ранняя деменция): больные обслуживают себя сами, но им нужна помощь для решения финансовых вопросов, приготовления пищи и т. д.
Вторая (умеренная деменция): зависимость от посторонней помощи растет — больные не способны самостоятельно одеться, осуществить гигиенические процедуры, долго оставаться дома без присмотра.
Третья (тяжёлая деменция): больные не могут выполнить ни одно из привычных повседневных действий без помощи других людей.
Переход от одной стадии к другой коррелирует со снижением оценки по MMSE (Краткая шкала психического статуса), которая является надежным инструментом для отслеживания динамики заболевания.
Осложнения болезни Альцгеймера
Продолжительность жизни людей с болезнью Альцгеймера после установления диагноза обычно колеблется от трех до десяти лет. Более четырнадцати лет после установления диагноза живут менее 3% больных. Уменьшение выживаемости связано с тяжелыми когнитивными нарушениями, снижением уровня физической активности, частыми падениями и нарушениями в неврологическом статусе. Сопутствующие соматические заболевания также влияют на продолжительность и качество жизни при болезни Альцгеймера. Пневмония и обезвоживание — наиболее частые непосредственные причины смерти, вызванной болезнью Альцгеймера. Кроме того, чем старше возраст, тем выше общий возраст выживаемости. У мужчин прогноз менее благоприятен по сравнению с женщинами.
Диагностика болезни Альцгеймера
Трудности ранней диагностики болезни Альцгеймера во многом объясняются "маскированным" характером заболевания в этот период, когда отсутствуют явные внешние признаки деменции. Для постановки диагноза, определения тактики ведения пациента необходимо выявить характер и выраженность когнитивных нарушений.
Нейропсихологический тест
Основной метод оценки когнитивных функций — нейропсихологическое обследование, которое проводит врач, обученный данным методам исследования. В некоторых странах практикуется обследование больных их родственниками с помощью шкал для оценки когнитивных функций: монреальской когнитивной шкалы, Адденбрукской, шкала краткого исследования психических функций MMSE.
Биомаркеры болезни Альцгеймера
Молекулярная диагностика на ранней стадии заболевания также создаёт перспективы для раннего назначения лечения болезни Альцгеймера. Определение биомаркеров в плазме является менее инвазивной альтернативой для диагностики болезни Альцгеймера. Биомаркеры классифицируются на биомаркеры накопления амилоида и биомаркеры нейродегенерации. Основные биомаркеры отражают патологию амилоида (внеклеточное накопление Aβ1-40/1-42) или внутриклеточные включения нейрофибриллярных клубочков (гиперфосфорилированного тау). [4] [5]
Согласно рекомендациям 4-го Канадского консенсуса по диагностике и лечению деменции и рациональному использованию биомаркеров для диагностики болезни Альцгеймера и других деменций (CCCDTD4, 2011): [6]
1. Определение биомаркеров цереброспинальной жидкости не рекомендуются для диагностики болезни Альцгеймера с типичной клинической картиной (2А уровень).
2. Исследование биомаркеров не рекомендуется для скрининга здоровых людей с целью оценки риска развития болезни Альцгеймера в будущем (уровень 1В).
3.Биомаркеры цереброспинальной жидкости можно рассматривать в особых случаях, когда есть атипичные признаки или диагностические трудности при дифференциальной диагностике лобного варианта болезни Альцгеймера от лобно-височной деменции, а также случаи первично прогрессирующей афазии как следствие болезни Альцгеймера или лобно-височной дегенерации (уровень 2В).
МРТ и КТ головного мозга
Современные методы нейровизуализации — магнито-резонансная томография и компьютерная томография головного мозга — позволяют расширить диагностические возможности прижизненной диагностики болезни Альцгеймера.
МРТ и КТ проводят для выявления поддающихся лечению причин деменции и нарушений, которые могут усугубить симптомы. Структурные изменения по данным магнитно-резонансной томографии являются более прогностически значимыми для дальнейших изменений в когнитивной сфере, чем биомаркеры цереброспинальной жидкости. По данным магнитно-резонансной томографии, признаки цереброваскулярного заболевания, такие как лейкоареоз и множественные подкорковые лакунарные инфаркты, чаще наблюдаются у пациентов с болезнью Альцгеймера, чем в контрольной группе. [7] Асимметричная атрофия медиальных отделов височной доли также не исключает сосудистую деменцию.
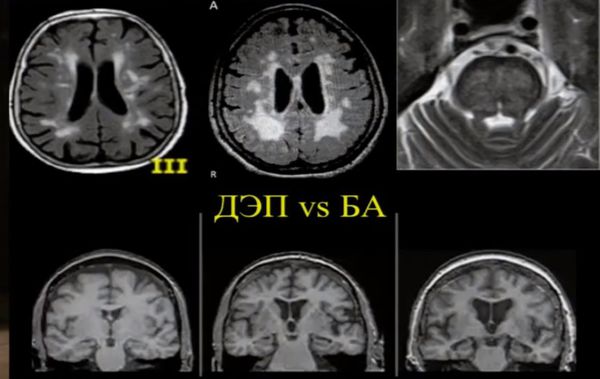
Описана смешанная модель патогенеза болезни Альцгеймера, которая предполагает взаимодействие церебральной амилоидной ангиопатии с сосудистыми факторами на ранних стадиях патологического процесса. Предполагается, что синергия между накоплением амилоида и цереброваскулярной патологией может инициировать дальнейшую дисфункцию нейронов и нейродегенерацию. [8] В этом отношении церебральные микрокровоизлияния, выявляемые в режиме Т2 градиентного эхо на магнитно-резонансной томографии, являются дополнительным и доступным диагностическим маркером, повышающим диагностическую значимость лейкоареоза и свидетельствующим в пользу церебральной амилоидной ангиопатии или гипертонической микроангиопатиии, особенно в случаях смешанной патологии и тяжелого когнитивного дефицита.
Локализация церебральных микрокровоизлияний является дифференциально-диагностическим признаком ведущего патологического процесса. В случае болезни Альцгеймера наблюдается корковая локализация микрокровоизлияний, в случае дисциркуляторной энцефалопатии или сосудистой деменции будут визуализироваться микрокровоизлияния в глубинных отделах мозга. [9] [10]
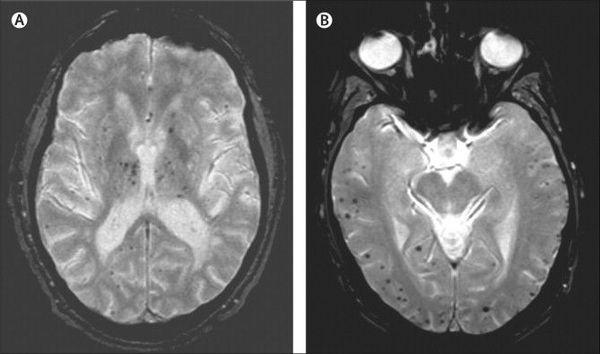
Одним из наиболее перспективных методов диагностики болезни Альцгеймера является позитронно-эмиссионная томография с лигандом, который связывается с амилоидом (PiB), однако накопление амилоида и захват соответствующего лиганда нарастают на стадии умеренных когнитивных нарушений, но после конверсии в деменцию дальнейшего накопления не происходит. [11]
Лечение болезни Альцгеймера
Болезнь Альцгеймера пока не поддается лечению. Но благодаря группе новых препаратов и симптоматическому лечению Альцгеймера можно сделать так, что снижение интеллекта больных будет более постепенным.
Лекарства
К таким средствам относятся:
- ингибиторы холинэстеразы (донепезил, ривастигмин, галантамин)
- блокаторы NMDA-глутаматных рецепторов (акатинол-мемантин).
Облегчение расстройств психики и поведения, сопровождающих болезнь Альцгеймера
С целью лечения сопутствующих расстройств психики и поведения используются также антидепрессанты и нейролептики.
Поддерживающие методы
Существуют и нелекарственные методы воздействия — тренировки интеллектуальных функций. Нейропсихологическая реабилитация позволяет стимулировать к развитию новых нейронный сетей, обучая рабочие нервные клетки.
Специальная диета при болезни Альцгеймера не требуется: питание не влияет на развитие заболевания.
Прекращение лечения
Причиной для прекращения приёма антидементных препаратов может стать выраженная брадикардия, но это осложнение возникает крайне редко.
Рекомендации для ухаживающих за близкими с болезнью Альцгеймера
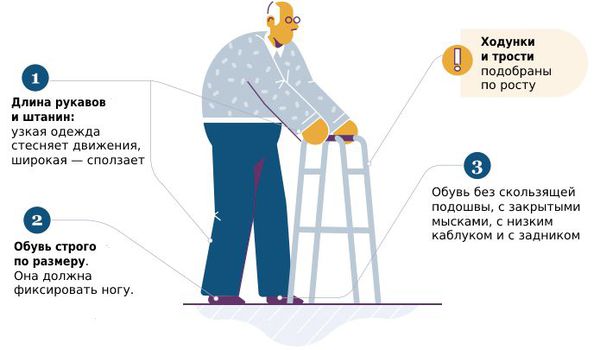
При уходе за больным человеком важно организовать для него безопасное и удобное пространство.
Также важно внимательно выбирать обувь и одежду.
Такими занятиями могут быть:
- прогулки;
- общение с домашними животными;
- уход за растениями;
- наблюдения за рыбками в аквариуме;
- прослушивание радиопередач и музыки;
- творчество, например лепка и живопись;
- чтение книг, при невозможности это могут делать близкие люди вслух.
Ухаживая за больным, не следует игнорировать своё здоровье. Пациенту нужно обеспечить нормальное питание, режим, активный образ жизни — это в полной мере относится и к близким больного человека.
Где обеспечивают уход при болезни Альцгеймера
Государственных специализированных пансионатов по уходу за людьми с болезнью Альцгеймера в нашей стране пока нет.
Прогноз. Профилактика
С увеличением осведомлённости общества о деменции будет расти и потребность в помощи по уходу, понадобятся значительные затраты для её организации. Пока же преобладает в основном неформальная помощь в семьях. Усилия по улучшению качества и доступности помощи потребуют вложений в меры первичной профилактики, и возможно, это позволит контролировать "эпидемии" деменций в разных регионах мира. В качестве основных мишеней первичной профилактики рассматриваются улучшение образования и устранение сосудистых факторов риска.
Профилактика
На сегодняшний день одной из основных целей профилактики является создание различных новых форм внебольничной помощи пациентам пожилого и старческого возраста с целью улучшения диагностики когнитивных нарушений разной степени тяжести, более раннее выявление заболеваний. С такой целью в развитых странах созданы клиники памяти, Альцгеймеровские центры. [2]
Человек с деменцией обращен в прошлое. Больных надо аккуратно «тормошить» и в интеллектуальном плане, и в двигательном. Неподвижность плохо влияет на мозг. Лучший способ сохранить разум, это, как ни странно, даже не интеллектуальная деятельность, а двигательная активность. Именно в этом случае в мозге создаются условия, которые способствуют образованию новых связей между нейронами и укреплению мозгового резерва, что впоследствии противодействует развитию деменции.
Продолжительность жизни
В среднем люди с болезнью Альцгеймера живут 3 – 11 лет после выявления заболевания, но некоторые — 20 лет и более. Продолжительность жизни зависит от степени нарушений при постановке диагноза [14] .
Юридические вопросы
Требования для признания гражданина недееспособным раскрываются в статье 29 Гражданского кодекса РФ. Потеря дееспособности компенсируется больному человеку установлением опёки. Опекун "восполняет" утраченные возможности гражданина, признанного недееспособным, и действует в его интересах.
Процедура признания гражданина недееспособным описана в 31 главе Гражданского процессуального кодекса РФ, в статьях 281–285.
Болезнь Альцгеймера — прогрессирующая форма сенильной деменции, приводящая к полной утрате когнитивных способностей, развивающаяся преимущественно после 60-65 лет. Клинически проявляется возникающим исподволь и постоянно прогрессирующим расстройством когнитивных способностей: внимания, памяти, речи, праксиса, гнозиса, психомоторной координации, ориентации и мышления. Диагностировать болезнь Альцгеймера позволяет тщательный сбор анамнеза, ПЭТ головного мозга, исключение других типов деменции при помощи ЭЭГ, КТ или МРТ. Лечение является паллиативным, включает медикаментозную (ингибиторы холинэстеразы, мемантин) и психосоциальную (арт-терапия, психотерапия, сенсорная интеграция, симуляция присутствия) терапию.
МКБ-10

Общие сведения
Болезнь Альцгеймера получила свое название по фамилии немецкого психиатра впервые описавшего ее в 1906 г. Заболеваемость в среднем колеблется от 5 до 8 чел. на 1000 населения, что составляет около половины всех случаев диагностики деменции. В мировом масштабе по данным 2006 г. количество пациентов, имеющих болезнь Альцгеймера, составила 26,5 млн. человек. Отмечается четкая тенденция роста заболеваемости, что делает проблему диагностики и лечения этой патологии одной из важных задач современной психиатрии и неврологии.
Характерна значительная корреляция между заболеваемостью деменцией альцгеймеровского типа и возрастом. Так, в возрастной группе 65 лет отмечается около 3 случаев болезни на 1000 человек, а среди людей в возрасте 95 лет уже 69 случаев на 1000. Показатель распространенности данной патологии в развитых странах значительно выше, поскольку их население имеет большую продолжительность жизни. Среди женщин болезнь Альцгеймера встречается чаще, чем среди мужчин, что частично связывают с более высокой, в сравнении с мужчинами, продолжительностью их жизни.

Причины
До сих пор этиопатогенез деменции альцгеймеровского типа остается загадкой для ученых и практиков в области медицины. Не установлена связь с какими-либо внешними факторами, запускающими болезнь Альцгеймера. Известно только, что морфологическим субстратом болезни является образование внутринейрональных нейрофибриллярных сплетений и церебральных скоплений бета-амилоида, так называемых «сенильных бляшек», что приводит к дегенерации и гибели нейронов. Отмечается также понижение уровня холинацетилтрансферазы. Эти особенности легли в основу 3 основных гипотез, пытающихся объяснить, как развивается болезнь Альцгеймера.
Более старой является холинергическая теория возникновения заболевания, связывающая его с дефицитом ацетилхолина. Однако результаты клинических исследований показали неспособность препаратов ацетилхолина хотя бы частично или временно купировать болезнь Альцгеймера. Амилоидная гипотеза развития болезни существует с 1991 г. Согласно ей основой патологии являются скопления бета-амилоида. Интересно, что ген, кодирующий белок-предшественник бета-амилоида, входит в состав 21-й хромосомы, трисомия которой лежит в основе синдрома Дауна. При этом у всех больных синдромом Дауна, достигших 40-летнего возраста, наблюдается альцгеймер-подобная патология.
Предрасполагающими факторами синтеза патологического бета-амилоида названы недостаточность процессов митохондриального окисления, более кислая реакция межклеточной среды, увеличенное количество свободных радикалов. Отложения патологического амилоида отмечаются как в мозговой паренхиме, так и в стенках церебральных сосудов. Следует отметить, что подобные отложения характеризуют не только болезнь Альцгеймера, они наблюдаются при церебральных гематомах врожденного генеза, синдроме Дауна и при нормально протекающих процессах старения.
По третьей гипотезе болезнь Альцгеймера связана с гибелью нейронов в результате накопления в них гиперфосфорилированного тау-протеина, нити которого склеиваются и образуют клубки. Согласно тау-гипотезе накопление белка связано с дефектом в его структуре; образование сплетений обуславливает дезинтеграцию внутринейронального транспорта, что в свою очередь приводит к нарушению передачи сигналов между нейронами, а затем и к их разрушению. С другой стороны, образование нейрофибриллярных клубков наблюдается и при других церебральных дегенерациях (например, при прогрессирующем надъядерном параличе и фронтотемпоральной атрофии). Поэтому многие исследователи отрицают самостоятельное патогенетическое значение тау-белка, считая его накопления следствием массового разрушения нейронов.
Среди возможных причин, запускающих болезнь Альцгеймера, называют синтез патологического аполипопротеина Е. Последний обладает сродством к амилоидному протеину и принимает участие в транспортировке тау-белка, что может лежать в основе типичных морфологических изменений заболевания, описанных выше.
По мнению многих исследователей болезнь Альцгеймера генетически детерминирована. Определены 5 основных генетических участков, с которыми связывают развитие заболевания. Они расположены на 1, 12, 14, 19 и 21 хромосомах. Мутации в этих локусах приводят к нарушениям протеинового обмена церебральных тканей, влекущим за собой накопление амилоида или тау-белка.
Симптомы болезни Альцгеймера
В типичных случаях болезнь Альцгеймера манифестирует у лиц старше 60-65 лет. Крайне редко встречаются случаи ранней формы заболевания, возникающие в период от 40 до 60 лет. Деменция альцгеймеровского типа характеризуется малозаметным и длительным началом, неуклонным прогрессированием без периодов улучшения состояния. Основным субстратом заболевания являются расстройства высших нервных функций. К последним относятся: кратковременная и долговременная память, внимательность, пространственно-временная ориентация, психомоторная координация (праксис), способность к восприятию различных аспектов внешнего мира (гнозис), речь, контроль и планирование высшей нервно-психической деятельности. Болезнь Альцгеймера подразделяют на 4 клинические стадии: предеменцию, раннюю, умеренную и тяжелую деменцию.
Предеменция
На стадии предеменции возникают малозаметные когнитивные затруднения, зачастую выявляемые лишь в ходе детального нейрокогнитивного тестирования. От момента их появления до верификации диагноза, как правило, проходит 7-8 лет. В подавляющем большинстве случаев на первый план выходят нарушения памяти на недавние события или полученную накануне информацию, значительные затруднения при необходимости запомнить что-то новое. Некоторые проблемы с исполнительными функциями: когнитивной гибкостью, способностью сосредоточиться, планированием, абстрактным мышлением и семантической памятью (затрудненное вспоминание значения некоторых слов) обычно остаются незамеченными или «списываются» на возраст пациента и физиологичные процессы старения, происходящие в его мозговых структурах. На стадии предеменции может наблюдаться апатия, являющаяся типичным нейропсихиатрическим симптомом, устойчиво присутствующим на всех стадиях заболевания.
Малая выраженность симптомов предеменции позволяет отнести ее к преклинической стадии заболевания, после которой развиваются более выраженные когнитивные изменения, характеризующие собственно болезнь Альцгеймера. Рядом авторов эта стадия именуется как мягкие когнитивные расстройства.
Ранняя деменция
Прогрессирующее ухудшение памяти приводит к настолько выраженным симптомам ее нарушения, что относить их к процессам обычного старения становиться невозможно. Как правило, это и является поводом для предположения диагноза «болезнь Альцгеймера». При этом различные виды памяти нарушаются в различной степени. Наиболее страдает краткосрочная память — способность запоминать новую информацию или недавние события. Мало страдают такие аспекты памяти, как неосознанная память заученных ранее действий (имплицитная память), воспоминания отдаленных событий жизни (эпизодическая память) и выученных когда-то давно фактов (семантическая память). Расстройства памяти зачастую сопровождаются симптомами агнозии — нарушениями слухового, зрительного и тактильного восприятия.
У отдельных пациентов на первый план в клинике ранней деменции выходят расстройства исполнительных функций, апраксия, агнозия либо нарушения речи. Последние характеризуются преимущественно снижением темпа речи, обеднением словарного запаса, ослаблением способности письменно и устно выражать свои мысли. Однако на этой стадии во время общения пациент вполне адекватно оперирует несложными понятиями.
Из-за расстройств праксиса и планирования движений при выполнении задач с применением тонкой моторики (рисование, шитье, письмо, одевание), пациент имеет неуклюжий вид. В стадии раней деменции больной еще способен независимо выполнять многие простые задачи. Но в ситуациях, требующих сложных когнитивных усилий, он нуждается в помощи.
Умеренная деменция
Прогрессирующее угнетение когнитивных функций приводит к значительному снижению способности совершать независимые действия. Очевидными становятся агнозия и расстройства речи. Отмечается парафазия — потеря грамматического строя речи и ее смысла, поскольку вместо забытых слов больные все чаще употребляют неверные слова. Это сопровождается утратой навыков письма (дисграфия) и чтения (дислексия). Нарастающее расстройство праксиса лишает пациента способности справляться даже с простыми повседневными задачами, такими как одевание-раздевание, самостоятельный прием пищи и пр.
В стадии умеренной деменции наблюдаются изменения в долговременной памяти, ранее незатронутой заболеванием. Нарушения памяти прогрессируют до такой степени, что пациенты не помнят даже своих ближайших родственников. Характерны нейропсихиатрические симптомы: эмоциональная лабильность, внезапная агрессивность, плаксивость, противление уходу; возможно бродяжничество. Примерно у 1/3 пациентов с болезнью Альцгеймера выявляется синдром ложной идентификации и др. проявления бреда. Может быть недержание мочи.
Тяжелая деменция
Речь больных сводится к употреблению отдельных фраз или единичных слов. В дальнейшем речевые навыки полностью утрачиваются. При этом длительное время сохраняется способность воспринимать и поддерживать эмоциональный контакт с окружающими. Болезнь Альцгеймера в стадии тяжелой деменции характеризуется полной апатией, хотя иногда могут наблюдаться агрессивные проявления. Пациенты истощены как психически, так и физически. Они неспособны самостоятельно совершать даже самые простые действия, с трудом передвигаются и в конечном итоге перестают подниматься с кровати. Происходит потеря мышечной массы. Из-за обездвиженности развиваются такие осложнения как застойная пневмония, пролежни и др. Именно осложнения обуславливают в конечном итоге летальный исход.
Диагностика
Одним из основных направлений диагностического поиска является сбор анамнеза и жалоб. Поскольку сам пациент на ранних стадиях заболевания зачастую не замечает происходящих с ним изменений, а при развитии деменции не может адекватно оценить свое состояние, опрос должен проводиться среди его близких. Важное значение имеют: невозможность точно определить начало когнитивных отклонений, указания на постепенный и неуклонно прогрессирующий характер усугубления симптомов, отсутствие в анамнезе церебральных заболеваний (энцефалита, внутримозговой опухоли, абсцесса головного мозга, эпилепсии, хронической ишемии, перенесенных ОНМК и др.) и черепно-мозговых травм.
Диагностировать болезнь Альцгеймера в стадии предеменции довольно затруднительно. В этот период только расширенное нейропсихологическое тестирование может выявить некоторые нарушения высших нервных функций. В ходе исследования пациентам предлагается запоминать слова, копировать фигуры, выполнять сложные арифметические действия, читать и пересказывать прочитанное.
С целью исключения других заболеваний, способных привести к развитию деменции, невролог проводит неврологический осмотр, назначает дополнительные обследования: ЭЭГ, РЭГ, Эхо-ЭГ, КТ или МРТ головного мозга. Определенное значение в подтверждении диагноза имеет выявление отложений бета-амилоида при проведении ПЭТ головного мозга с введением Питтсбургского состава B. Последнее время доказано, что еще одним маркером заболевания может служить обнаружение тау-протеина или бета-амилоида в цереброспинальной жидкости, взятой на анализ путем люмбальной пункции.
Дифференциальная диагностика деменции альцгеймеровского типа проводится с сосудистой деменцией, паркинсонизмом, деменцией с тельцами Леви, деменцией при эпилепсии и др. неврологической патологии.
Лечение болезни Альцгеймера
К сожалению, доступные на сегодняшний день методы лечения неспособны излечить болезнь Альцгеймера или замедлить ее течение. Все попытки терапии являются по сути паллиативными и могут лишь незначительно облегчить симптомы.
Наиболее признанные медикаментозные схемы включают мемантин и антихолинэстеразные препараты. Мемантин является ингибитором глутаматных рецепторов, чрезмерная активация которых характеризует болезнь Альцгеймера и может привести к гибели нейронов. Отмечается умеренный эффект мемантина при умеренной и тяжелой деменции. При его приеме возможны побочные эффекты: головокружение, замешательство, головные боли, галлюцинации.
Ингибиторы холинэстеразы (ривастигмин, донепезил, галантамин) показали умеренную эффективность при попытках лечить болезнь Альцгеймера в стадии ранней и умеренной деменции. Донепезил может применяться при тяжелой деменции. Использование ингибиторов холинэстеразы в стадии предеменции не смогло предупредить или замедлить развитие симптомов. К побочным эффектам этих медикаментов относятся: брадикардия, снижение веса, анорексия, мышечные спазмы, гастрит с повышенной кислотностью.
В случаях, когда болезнь Альцгеймера сопровождается антисоциальным поведением, для купирования агрессии возможно назначение антипсихотиков. Однако они могут вызывать цереброваскулярные осложнения, дополнительное снижение когнитивных функций, двигательные расстройства и при длительном использовании повышают смертность больных.
Наряду с фармакологическими применяются психосоциальные методы лечения пациентов, имеющих болезнь Альцгеймера. Так, поддерживающая психотерапия направлена помощь больным с ранней деменцией адаптироваться к своему заболеванию. В стадиях более выраженной деменции используется арт-терапия, сенсорная комната, терапия воспоминаниями, симуляция присутствия, сенсорная интеграция, валидационная терапия. Эти методики не приводят к клинически значимому улучшению, однако, по мнению многих авторов, они снижают тревожность и агрессивность пациентов, улучшают их настрой и мышление, смягчают отдельные проблемы (например, недержание мочи).
Прогноз и профилактика
К сожалению, болезнь Альцгеймера имеет неутешительный прогноз. Неуклонно прогрессирующая потеря важнейших функций организма приводит к летальному исходу в 100% случаев. После постановки диагноза продолжительность жизни в среднем составляет 7 лет. Более 14 лет проживают менее 3% больных.
Поскольку болезнь Альцгеймера является важной социальной проблемой в развитых странах, проведено немало исследований, призванных определить факторы снижающие вероятность ее развития. Однако подобные исследования предоставляют противоречивые данные и до сих пор нет твердых доказательств превентивного значения хотя бы одного из рассматриваемых факторов.
Многие исследователи склонны считать интеллектуальную активность (любовь к чтению, увлечение шахматами, разгадывание кроссвордов, владение несколькими языками и т. п.) фактором, отдаляющим начало болезни и замедляющим ее прогрессирование. Отмечается также, что причинные факторы развития сердечно-сосудистой патологии (курение, сахарный диабет, повышение уровня холестерина, артериальная гипертензия) вызывают более тяжелое течение деменции альцгеймеровского типа и могут повышать риск ее возникновения.
В связи с вышесказанным, чтобы избежать болезнь Альцгеймера и затормозить ее течение, рекомендуется вести здоровый образ жизни, в любом возрасте стимулировать мышление и выполнять физические упражнения.
Читайте также:

