Желтушность кожных покровов при печени
Обновлено: 27.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Цирроз печени: причины появления, симптомы, диагностика и способы лечения.
Определение
Причины возникновения цирроза печени
Основные причины возникновения цирроза печени – вирусные гепатиты B, C, D и алкогольные поражения печени (особенно тяжело протекают сочетанные алкогольно-вирусные циррозы). Кроме того, цирроз может развиваться в результате воздействия промышленных ядов и лекарственных средств, стать исходом неалкогольной жировой болезни печени, возникать при поражении желчных протоков (первичного билиарного цирроза, муковисцидоза), при иммунных нарушениях (аутоиммунном гепатите, первичном склерозирующем холангите), быть следствием наследственных заболеваний (гемохроматоза, болезни Вильсона–Коновалова, недостаточности альфа-1антитрипсина), болезни Банти, застойной сердечной недостаточности. К циррозу могут приводить инфекционные заболевания (например, шистосомоз, сифилис, эхинококкоз).
Их гибель запускает воспалительный процесс, в условиях которого на месте погибших клеток формируется соединительная ткань, что приводит к структурной деформации печени. Из-за разрастания соединительной ткани нарушается внутрипеченочный кровоток, а в ткани печени формируются узлы, что в конечном итоге обуславливает печеночную недостаточность.
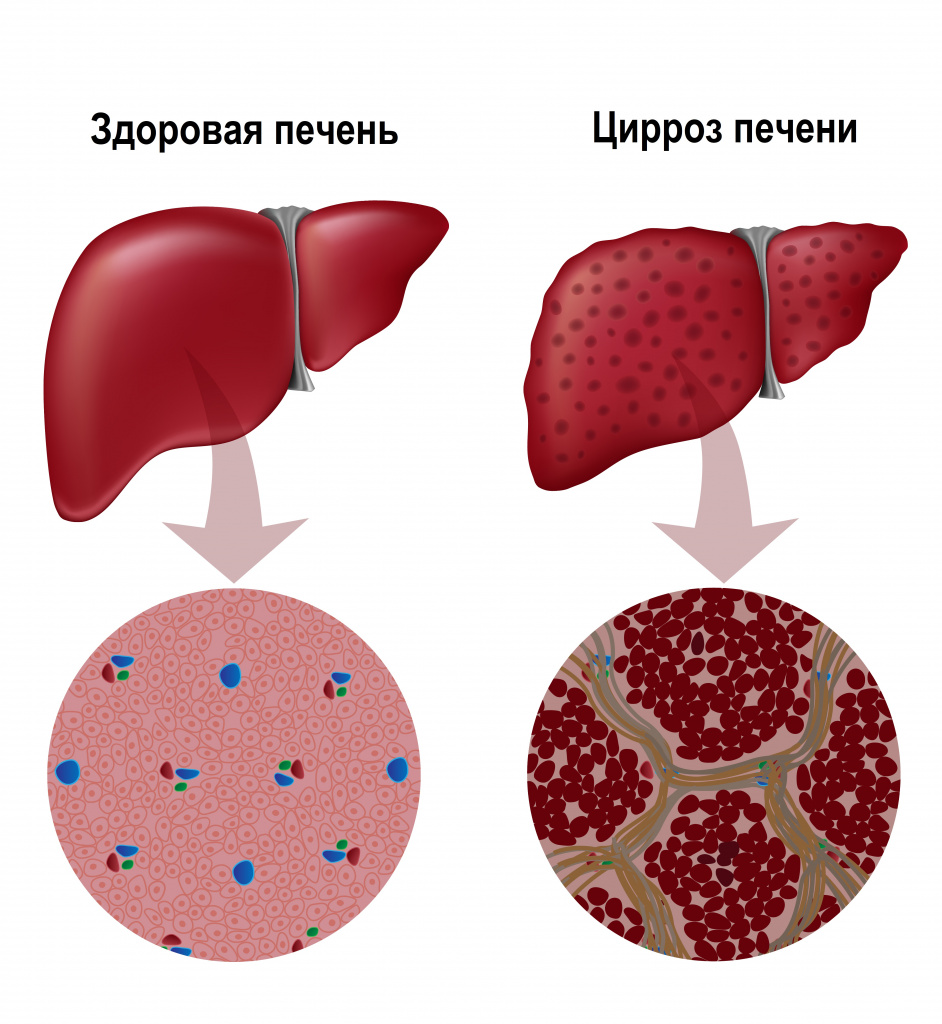
Классификация заболевания
- мелкоузловой цирроз (с узлами диаметром до 3-5 мм) - развивается, например, при алкогольном поражении печени;
- крупноузловой цирроз (с узлами до 2-3 см) – развивается при вирусных гепатитах В и С.;
- смешанный цирроз.
- активный, или прогрессирующий,
- неактивный.
- компенсированный цирроз,
- субкомпенсированный цирроз,
- декомпенсированный цирроз.
- класс А (Child A) — 5–6 баллов,
- класс B (Child B) — 7–9 баллов,
- класс C (Child C) — 10–15 баллов.
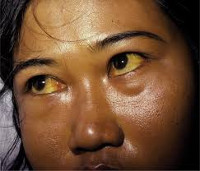
Самыми специфичными симптомами при поражениях печени являются: окрашивание кожи и слизистых в желтый цвет (желтуха), портальная гипертензия, асцит, печеночная энцефалопатия.
Желтый оттенок кожи и слизистых возникает, когда в крови накапливается слишком много билирубина – пигмента, входящего в состав желчи. При циррозе желтуха связана с повреждением гепатоцитов - так называемая паренхиматозная желтуха. При такой желтухе поврежденные клетки печени не могу захватывать из крови билирубин, связывать его с глюкуроновой кислотой и выделять в желчные пути, вследствие чего в крови повышается уровень непрямого билирубина. Возможно и обратное всасывание билирубина в кровеносные сосуды из желчных протоков с повышением в крови уровня прямого билирубина. При повышении содержания желчных кислот в крови нервные окончания раздражаются, и больных беспокоит сильный зуд.
Разрастающаяся соединительная ткань механически сдавливает венозные сосуды печени, в том числе крупную воротную (портальную) вену, которая собирает кровь от органов брюшной полости и несет в печень, где гепатоциты очищают кровь от токсичных веществ. Повышение давления в системе портальной вены называется портальной гипертензией. Это состояние является опасным осложнением многих заболеваний печени, в том числе цирроза. К признакам портальной гипертензии относят варикозное расширение вен пищевода и желудка с высоким риском кровотечений, появление извитых расширенных подкожных вен на передней брюшной стенке (так называемая «голова медузы»), расширенные геморроидальные узлы, увеличение живота из-за асцита.
Асцит (патологическое накопление жидкости в брюшной полости) - обязательный симптом декомпенсированного цирроза.
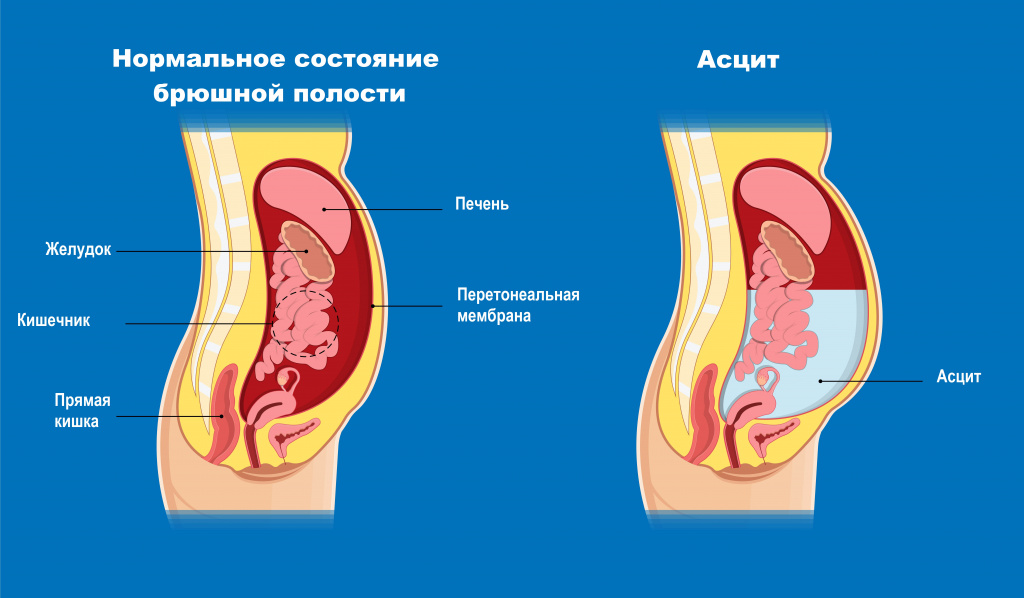
При печеночной недостаточности орган не может выполнять свою дезинтоксикационную функцию, и накапливающиеся токсины начинают оказывать неблагоприятное воздействие на мозг. Кроме того, могут формироваться функциональные или органические шунты между системами портального и общего кровообращения, что ведет к проникновению токсических продуктов кишечного происхождения в головной мозг. В результате возникают различные нервно-психические расстройства - печеночная энцефалопатия.
Развитие печеночной энцефалопатии при циррозе печени - наиболее тяжелое и прогностически неблагоприятное осложнение.
Врачи называют четыре стадии печеночной энцефалопатии:
- на 1-й стадии нарушается сон (появляется сонливость днем и бессонница ночью, кроме того, могут наблюдаться депрессия, раздражительность, эйфория, беспокойство, снижается способность к логическому мышлению, счету);
- на 2-й стадии сонливость нарастает и переходит в летаргию, наблюдается апатия, агрессия;
- на 3-й стадии присоединяется дезориентация во времени и пространстве, нарастает спутанность сознания;
- стадия 4 – кома: характеризуется отсутствием сознания и реакции на болевые раздражители.
Большинство клинических вариантов печеночной энцефалопатии потенциально обратимы – после трансплантации печени признаки энцефалопатии не рецидивируют.
Кроме того, при циррозе могут наблюдаться следующие симптомы:
- утолщение дистальных фаланг пальцев;
- изменение оттенка ногтевой пластины с ее помутнением;
- покраснение ладонной поверхности кистей, реже - стоп;
- расширение капилляров в области лица или тела;
- увеличение размеров молочных желез у лиц мужского пола с одновременным уменьшением яичек.
Лабораторная диагностика цирроза печени может включать:
-
общий анализ крови с определением уровня тромбоцитов;
Синонимы: Общий анализ крови (ОАК); Гемограмма; КАК; Развернутый анализ крови. Full blood count; FBC; Complete Blood Count (CBC); Hemogram; CBC with White Blood Cell Differential Count; Peripheral Blood Smear; Blood Film Examination; Complete blood count (CBC) with differential white blood cell coun.
Гемолитическая желтуха — это вариант надпеченочного желтушного синдрома, обусловленный гемолизом эритроцитов. Проявляется желтушностью и бледностью кожных покровов и слизистых, спленомегалией, потемнением мочи и кала, гемолитическими кризами. Диагностируется с помощью общего анализа крови, определения концентрации непрямого и общего билирубина, УЗИ органов брюшной полости. Для лечения используют кортикостероиды, цитостатики, антибиотики, активаторы печеночных ферментов, инфузионную и фототерапию, переливание компонентов крови. По показаниям проводят спленэктомию.
МКБ-10
Общие сведения
Гемолитическая (плейохолическая) желтуха развивается при превышении уровня свободного билирубина, который может беспрепятственно конъюгироваться в печени. В обычных условиях в человеческом организме разрушается до 100-200 млн. эритроцитов за час, при этом срок жизни красных клеточных элементов крови составляет в среднем 120 дней. Из 1 г гемоглобина, выделяющегося при гемолизе, образуется 35 мг неконъюгированного пигмента (около 250-350 г/сут).
Печень обладает 3-4-кратным функциональным резервом для связывания избытка билирубина. При укорочении срока жизни эритроцитов, их ускоренном разрушении концентрация пигмента превышает предельный печеночный порог конъюгации, непрямой билирубин накапливается в крови, откладывается в тканях, что сопровождается формированием характерной клинической картины.

Причины
Заболевание развивается на фоне гемолиза с образованием большого количества непрямого билирубина, который не успевает конъюгироваться гепатоцитами. Гемолитическая форма желтухи вызывается теми же этиологическими факторами, что и патологические состояния с усиленным внутрисосудистым или внесосудистым разрушением эритроцитов. Специалисты в сфере современной гастроэнтерологии и гематологии выделяют следующие причины расстройства:
- Наследственные дефекты эритроцитов и гемоглобина. Гемолиз может быть обусловлен генетически обусловленными энзимопатиями (недостаточностью пируваткиназы, глюкозо-6-фосфатдегидрогеназы), несостоятельностью эритроцитарных оболочек (наследственным микросфероцитозом, акантоцитозом, овалоцитозом, пароксизмальной ночной гемоглобинурией). Желтуха гемолитического типа также наблюдается при гемоглобинопатиях (талассемии, серповидно-клеточной анемии и др.).
- Воздействие гемолитических плазматических факторов. Реакцию гемолиза вызывают антитела при гемолитической болезни новорожденных и переливании изонесовместимой крови, гемолизины возбудителей кори, краснухи, сепсиса, эпидемического паротита, лептоспироза, малярийные плазмодии, змеиный и другие гемотоксичные яды (сероводород, мышьяк, свинец, фосфор, анилин, нитробензол), Эритроциты разрушаются под влиянием ряда фармпрепаратов (сульфаниламидов, антипиретиков, хининов).
- Обширные кровоизлияния, инфаркты. Повышенное образование свободного билирубина связано с массивным распадом элементов крови при рассасывании крупных гематом в мягких тканях, паренхиматозных органах, полостях тела. Гемолитической надпеченочной желтухой осложняются массивные желудочно-кишечные кровотечения, расслаивающая аневризма аорты, инфаркт миокарда, легкого, геморрагический инсульт, гемоторакс. Обычно такое состояние связано с существующим заболеванием, травмой.
- Механическое разрушение эритроцитов в сосудах. Красные кровяные тельца подвергаются внутрисосудистому гемолизу при их сдавлении в периферических кровеносных сосудах, прилегающих к костным выступам (маршевая гемоглобинурия), турбуленции потока крови при дисфункции протезов сердечных клапанов. Гемолиз также возникает при прохождении эритроцитов через фибриновые депозиты в артериолах при ДВС-синдроме, гемолитико-уремическом синдроме, тромботической тромбоцитопенической пурпуре.
У части пациентов разрушение красных кровяных клеток с развитием надпеченочной желтухи наблюдается в рамках клинической картины злокачественных опухолей разной локализации, лейкозов, лимфопролиферативных заболеваний, пернициозной анемии Аддисона-Бирмера, системных патологий соединительной ткани. Гемотоксическое действие оказывают мощные ионизирующие воздействия при лучевой болезни, радиотерапии. Физиологическая желтуха возникает у новорожденных при усиленном гемолизе фетального гемоглобина на фоне низкой активности печеночных ферментов.
Патогенез
В основе механизма развития гемолитической желтухи лежит относительная функциональная недостаточность печеночных клеток, неспособных связать большое количество свободного билирубина, образовавшегося при гемолизе эритроцитов. Дополнительным патогенетическим фактором является нарушение внутриклеточного транспорта пигмента в гепатоцитах при его высокой концентрации. В результате неконъюгированный билирубин связывается с альбуминами и циркулирует в крови в виде водонерастворимых билирубин-альбуминовых комплексов, которые не могут выводиться с мочой.
Жирорастворимый свободный пигмент легко проникает через клеточные и митохондриальные мембраны, окрашивает в желтый цвет кожу и слизистые оболочки, нарушает процессы окислительного фосфорилирования, синтез белков, трансмембранный потенциал клеток. Поражение ядер головного мозга, особо чувствительных к токсическому эффекту непрямого билирубина, приводит к развитию энцефалопатии (ядерной желтухи) с выраженной неврологической симптоматикой. Связывающая способность альбуминов оказывается недостаточной при непрямой гипербилирубинемии более 260-550 мкмоль/л.
Активная конъюгация пигмента в печени сопровождается его усиленной экскрецией в просвет кишечника с образованием уробилиногена в тонкой кишке и затем стеркобилиногена — в толстой. Избыточное количество всосавшегося в кровь уробилиногена, который не может полностью элиминироваться гепатоцитами, продолжает циркулировать в крови. Высокий уровень экскретируемого с мочой стеркобилиногена, всосавшегося в геморроидальных венах, и стеркобилина в кале придает экскрементам характерную коричневую окраску. После исчерпания способности гепатоцитов выделять прямой (конъюгированный) билирубин в желчь происходит обратная диффузия связанной формы пигмента в кровь.
Классификация
Систематизация форм гемолитической желтухи учитывает этиологические факторы, под влиянием которых произошел гемолиз. Такой подход позволяет выбрать оптимальную терапевтическую тактику, максимально компенсирующую действие первопричины заболевания. Гастроэнтерологи и гематологи различают следующие типы гемолитических надпеченочных желтух:
- Гемолитические корпускулярные желтухи. Связаны с различными видами несостоятельности эритроцитов — дефицитом или недостаточной активностью ферментных систем, дефектами гемоглобина, мембранных структур. Обычно корпускулярные плейохолические желтухи вызваны генетическими аномалиями, их лечение является преимущественно симптоматическим.
- Гемолитические экстракорпускулярные желтухи. К разрушению эритроцитов приводит действие различных внешних факторов — антител, микробных токсинов, гемолитических ядов, механических нагрузок. Наряду с устранением отдельных симптомов это позволяет использовать методы, направленные на элиминацию этиопатогена и отдельные звенья патогенеза гемолиза.
- Гемолитические постгеморрагические желтухи. Возникают на фоне массивного распада эритроцитов в участках кровоизлияний. Обычно осложняют течение тяжелых травм и других неотложных состояний. Прогнозирование развития надпеченочной желтухи дает возможность назначить превентивную терапию для предупреждения дальнейших осложнений.
Симптомы гемолитической желтухи
Характерный признак заболевания — сочетание бледности кожных покровов с лимонно-желтым окрашиванием кожи, конъюнктивы глаз при отсутствии кожного зуда. У большинства пациентов с надпеченочной желтухой наблюдается потемнение мочи. Могут возникать умеренные боли в животе, диспепсические расстройства – тошнота, отрыжка, диарея. Обострение заболевания (гемолитический криз) клинически проявляется фебрильной лихорадкой, головной болью, миалгиями, интенсивными болями в левом подреберье вследствие увеличения селезенки. Если заболевание вызвано острым отравлением химическими соединениями или лекарственными средствами, присоединяются интоксикационные симптомы в виде угнетения сознания вплоть до комы, выраженной тахикардии, падения АД, расстройств дыхания и мочевыделения.
Осложнения
Наличие у пациента надпеченочной желтухи повышает риск застойных явлений в желчном пузыре, что приводит к формированию пигментных камней и обструкции желчевыводящих протоков. Осложнением гемолитической желтухи может стать токсическая нефропатия с острой почечной недостаточностью, развивающаяся при выраженных нарушениях биохимического состава крови и накоплении токсических соединений. При длительном течении заболевания возможно возникновение печеночной недостаточности, при которой происходит резкое угнетение всех функций органа, что клинически проявляется кахексией, дистрофическими изменениями, стойкими нарушениями метаболических процессов. Плейохолическая желтуха иногда осложняется билирубиновой энцефалопатией вследствие интоксикации головного мозга.
Диагностика
Постановка диагноза не представляет затруднений при наличии типичной клинической картины заболевания. Отличительный признак гемолитической желтухи — желтушное окрашивание кожи без кожного зуда и увеличения печени. Диагностический поиск направлен на выявление первопричины болезни. План обследования включает следующие инструментальные и лабораторные методы:
- Общий анализ крови. При проведении исследования определяется резкое уменьшение количества гемоглобина и эритроцитов с одновременным повышением содержания ретикулоцитов свыше 1%. При морфологической оценке могут выявляться специфические клетки, указывающие на определенный вид гемолитической анемии: сфероциты, мишеневидные, серповидные эритроциты. В остром периоде и при аутоиммунных процессах наблюдается лейкоцитоз со сдвигом формулы влево.
- Биохимический анализ крови. Патогномоничный признак надпеченочной желтухи — повышение концентрации свободного билирубина. Исследование позволяет установить степень тяжести болезни по уровню общего билирубина: до 80 мкмоль/л — легкая, 80-150 мкмоль/л — средняя, свыше 150 мкмоль/л — тяжелая форма. О гемолитической природе заболевания свидетельствует повышение содержания ЛДГ-5, выделяющейся из разрушенных эритроцитов, и снижение гаптоглобина.
- УЗИ брюшной полости. При плейохолической желтухе во время ультразвукового исследования ОБП определяется значительное увеличение селезенки при обычно нормальных размерах печени и структуре печеночной паренхимы. Также сонографически удается выявить заболевания гепатобилиарной системы, которые могут сочетаться с гемолитической патологией: желчнокаменную болезнь, холецистит, фиброзные поражения печени, изменения печеночных сосудов.
Концентрация АЛТ, АСТ, щелочной фосфатазы обычно в пределах нормы. В общем анализе мочи обнаруживается высокое содержание стеркобилиногена и уробилина, билирубинурия отсутствует. В копрограмме отмечается повышенный уровень стеркобилина. Для комплексной оценки состояния печени при желтухе может выполняться КТ, МРТ, холангиопанкреатография. Дополнительно проводится исследование осмотической резистентности эритроцитов, которая повышается при талассемии и снижается при гемолитической сфероцитарной анемии. В тесте Кумбса могут выявляться антиэритроцитарные антитела.
Дифференциальную диагностику осуществляют с синдромом Жильбера, паренхиматозной и механической желтухой, а также с заболеваниями, которые могут служить причиной указанных видов гипербилирубинемий — гепатитами, лептоспирозом, желтушной формой инфекционного мононуклеоза, псевдотуберкулезом, иерсиниозом, амебиазом, желчнокаменной болезнью, опухолями печени и Фатерова соска. По направлению врача-гастроэнтеролога при наличии показаний пациента консультирует гематолог, абдоминальный хирург и другие специалисты.
Лечение гемолитической желтухи
Рекомендована комплексная терапия, позволяющая по возможности устранить причину гемолиза, воздействовать на патогенетические звенья, купировать угрожающие жизни симптомы. Лечение гемолитической формы надпеченочной желтухи обычно является консервативным и сочетается с диетотерапией, направленной на поддержание нормальной работы печени. Показано существенное ограничение или полное исключение жирных, жареных, острых блюд, продуктов, содержащих много каротина и грубой клетчатки. С учетом возможной причины гемолитической анемии и желтухи план лечения включает:
- Кортикостероиды. Назначение иммуносупрессорной гормональной терапии оправдано при диагностике аутоиммунных расстройств, провоцирующих развитие приобретенной гемолитической анемии. У некоторых пациентов с желтухой более эффективным оказывается прием цитостатических препаратов.
- Антибиотики. Используются при гемолизе, обусловленном действием бактериальных токсинов. Рекомендуются средства, не вступающие в конкурентное вытеснение билирубина из соединений с глюкуроновой кислотой. Препараты из групп амфениколов, цефалоспоринов, сульфаниламидов применяются с осторожностью.
- Инфузионная терапия. Проводится при гемолитических процессах токсического происхождения. Введение коллоидных и кристаллоидных растворов при необходимости дополняется форсированным диурезом, энтеросорбентами, антидотами для связывания отравляющих веществ, гемосорбцией, плазмаферезом, гемодиализом.
- Индукторы ферментов печени. Активируют микросомальную ферментную систему, которая связана с цитохромом P450. В результате повышения метаболизма гепатоцитов улучшается связывание билирубина, циркулирующего в крови. Стимуляция ферментов эффективна при наличии функционального резерва печени.
- Фототерапия. Направлена на снижение гипербилирубинемии. Используется при повышении уровня билирубина до субтоксических и токсических концентраций. Способствует переводу неконъюгированного пигмента в водорастворимую изомерную форму, которая экскретируется почками и печенью без образования альбуминовых комплексов.
- Обменное переливание крови. Обычно выполняется при иммунных гемолитических состояниях с критическим для нервной системы содержанием свободного билирубина. За одну процедуру может заменяться до 70% ОЦК, благодаря чему уменьшается билирубинемия, восполняется дефицит эритроцитов, купируется гипоксия.
- Удаление селезенки. Хирургическое лечение показано при тяжелом течении гемолитической корпускулярной желтухи у пациентов с наследственными эритроцитарными ферментопатиями и мембранопатиями. Спленэктомия позволяет исключить деструкцию эритроцитов в синусах органа и их утилизацию макрофагами.
Прогноз и профилактика
Поскольку гемолитический вариант надпеченочной желтухи зачастую проявляется на фоне наследственных анемий, которые трудно поддаются лечению, прогноз заболевания считается серьезным. Полное выздоровление наблюдается у пациентов без тяжелых интеркуррентных патологий при отсутствии необратимых нарушений функций печени. Специфическая профилактика гемолитической желтухи не разработана. Для предупреждения болезни необходимо проводить своевременную диагностику и комплексную терапию гемолитических анемий, тяжелых инфекционных заболеваний, соблюдать правила совместимости крови при гемотрансфузиях, избегать полипрагмазии и назначения потенциально гемотоксичных медикаментов.
2. Дифференциальная диагностика желтух/ Самсон А.А.// Медицина неотложных состояний. – 2013 - №5(52).
3. Дифференциальная диагностика синдрома желтухи у детей: учебно-методическое пособие/ Артемчик Т. А. – 2017.
Паренхиматозная желтуха — желтушный синдром, возникший в результате повреждения гепатоцитов и холангиол. Проявляется иктеричностью кожи, видимых слизистых, склер, потемнением мочи, обесцвечиванием кала, диспепсией, дискомфортом и болями в правой подреберной области, астеническим синдромом. Диагностируется с помощью биохимических анализов крови, мочи, кала, УЗИ, МРТ, ОФЭКТ, фиброэластометрии и пункционной биопсии печени, МСКТ брюшной полости. Для лечения применяют гепатопротекторы, противовоспалительные средства, периферические вазодилататоры, воздействие световыми лучами синего спектра, дополняющие этиопатогенетическую терапию основного заболевания.
МКБ-10
Общие сведения
Печеночная (гепатоцеллюлярная, паренхиматозная) желтуха является следствием заболеваний, при которых нарушается внутрипеченочный метаболизм и транспорт билирубина. В зависимости от уровня, возникновения дисфункции различают печеночно-клеточный, холестатический и энзимопатический варианты паренхиматозного желтушного синдрома. По наблюдениям специалистов в сфере гастроэнтерологии и гепатологии, у большинства пациентов расстройство проявляется в рамках острого или хронического инфекционного гепатита. Реже гипербилирубинемия обусловлена токсическим повреждением паренхиматозной ткани печени, ее склерозированием или малигнизацией. Ключевая особенность печеночной желтухи — одновременное повышение уровней как непрямого, так и прямого билирубина.

Причины паренхиматозной желтухи
Развитие гепатоцеллюлярного желтушного синдрома провоцируют различные патологические состояния, сопровождающиеся нарушением способности гепатоцитов к захвату, связыванию, экскреции в желчь билирубина. Расстройство может носить как врожденный, так и приобретенный характер. Основными причинами печеночно-клеточной желтухи являются:
- Инфекционные гепатиты. Наиболее часто некроз гепатоцитов вызван прямым и опосредованным цитотоксическим эффектом возбудителей вирусных гепатитов А, B, C, D, E. Реже к паренхиматозной дистрофии приводит инфекционный мононуклеоз, аденовирусная, энтеровирусная, герпетическая инфекции, лептоспироз, псевдотуберкулез, сепсис.
- Токсические воздействия. Разрушение печеночной паренхимы вызывают гепатотропные яды — гидразин, хлорэтан, этиленгликоль, окислители на основе окислов азота, алкоголь. Ятрогенные лекарственные гепатиты возникают при приеме сульфаниламидов, цитостатиков, антибиотиков, гормональных, сахароснижающих и ряда других фармпрепаратов.
- Перерождение печеночнойпаренхиматозной ткани. Функциональная несостоятельность гепатоцитов отмечается при их замещении соединительной тканью у пациентов с фиброзом и циррозом печени, склерозирующим холангитом. Печеночная недостаточность осложняет течение гепатоцеллюлярных карцином, холангиокарцином и других форм первичного рака печени.
- Аутоиммунное поражение гепатоцитов. Деструкция паренхиматозной печеночной ткани развивается вследствие повышения титра аутоантител. Гепатит может быть единственным проявлением аутоиммунного процесса или сочетаться с ревматоидным артритом, гломерулонефритом, витилиго, болезнью Шегрена, аутоиммунным тиреоидитом, язвенным колитом.
- Внутрипеченочный холестаз. Возможной причиной разрушения гепатоцитов и гипербилирубинемии является нарушение проницаемости базолатеральной и каналикулярной мембран. Цитолиз вследствие внутрипеченочного застоя желчи наблюдается при холестазе беременных, холестатическом гепатите, холангиолите, муковисцидозе, недостаточности α1-антитрипсина.
- Наследственные гепатозы. Конституциональные желтухи энзимопатического генеза возникают при врожденных дефектах фермента глюкуронилтрансферазы (синдромы Жильбера, Криглера-Найяра). У больных с синдромами Дабина-Джонсона, Ротора гипербилирубинемия обусловлена нарушением экскреции связанного билирубина и его обратным поступлением в кровь.
- Внепеченочные причины. Гепатоцеллюлярная желтуха у тяжелобольных пациентов формируется на фоне ишемических и эндотоксических изменений печени при сердечной недостаточности, шоке, ДВС-синдроме, трансфузиях, хирургических вмешательствах. Дистрофия гепатоцитов также наблюдается при длительном голодании, парентеральном питании.
Патогенез
Механизм развития паренхиматозной желтухи зависит от причин, вызвавших расстройство. При печеночно-клеточных вариантах желтушного синдрома, обусловленных инфекционным, токсическим повреждением печени, склеротическими процессами, злокачественным перерождением органа, уменьшается количество активных гепатоцитов, обратимо или необратимо снижается их функциональность. В результате нарушается захват свободного билирубина из крови, его глюкуронизация и экскреция с желчью. Одновременно за счет дистрофических и некробиотических процессов, происходящих в паренхиме, происходит обратная диффузия водорастворимого билирубин-глюкуронида из желчных капилляров в лимфатические и кровеносные сосуды. Пусковым моментом холестатического варианта гепатоцеллюлярной желтухи становится нарушение выделения желчи, приводящее к ее стазу и вторичному цитолизу печеночных клеток.
При наследственных формах паренхиматозной гипербилирубинемии ключевым звеном является нарушение конъюгации несвязанного пигмента, связанное с врожденной ферментной недостаточностью, или задержка в гепатоцитах связанного билирубина из-за генетического дефекта АТФ-зависимой транспортной системы. Независимо от особенностей пусковых моментов патогенеза в конечном результате в крови повышается содержание как свободного, так и связанного билирубина. За счет прямой билирубинемии возрастает фильтрация пигмента почками, что приводит к билирубинурии и потемнению мочи. Из-за недостаточной экскреции билирубина в желчь снижается количество стеркобилиногена и стеркобилина, вследствие чего кал становится светлым. При тяжелом повреждении печеночных тканей может нарушаться обмен уробилиногена, желчных кислот.
Симптомы паренхиматозной желтухи
Патогномоничный признак заболевания — появление интенсивного желтушного с красноватым оттенком окрашивания кожных покровов, слизистых оболочек и склер, которое сопровождается зудом. Для печеночной формы желтухи характерно потемнение мочи, возможно обесцвечивание кала вследствие уменьшения количества стеркобилина. У пациента наблюдаются тянущие боли в правом подреберье, диспепсические расстройства (тошнота и рвота, снижение аппетита, метеоризм, болезненность в эпигастрии). Может отмечаться ухудшение общего состояния — субфебрильная лихорадка, снижение массы тела, слабость. При паренхиматозной форме заболевания появляются внепеченочные знаки: покраснение ладонной поверхности рук (пальмарная эритема), телеангиоэктазии (сосудистые звездочки), увеличение грудных желез у мужчин.
Осложнения
Нарушение всасывания витамина D и кальция при желтухе приводит к деминерализации костей, что проявляется болями, патологическими переломами. При отсутствии лечения может формироваться печеночная недостаточность с интоксикацией организма азотистыми соединениями, энцефалопатией, нарушениями сознания, в тяжелых случаях возникает кома вследствие токсического поражения мозга. Частым осложнением заболеваний с хронической паренхиматозной желтухой является расширение околопупочных, пищеводных и геморроидальных вен, возникающее вследствие избыточного развития коллатерального кровообращения и в ряде случаев осложняющееся профузными кровотечениями.
Диагностика
Из-за наличия характерных клинических проявлений постановка диагноза паренхиматозной желтухи в типичных случаях не представляет затруднений. Диагностический поиск направлен на комплексное обследование пациента для выявления основной патологии, которая является первопричиной гипербилирубинемии. Больному рекомендованы следующие методы исследования:
- Биохимический анализ крови. Характерный признак паренхиматозного варианта желтухи — повышение количества общего билирубина, которое позволяет оценить тяжесть желтухи (до 80 ммоль/л — легкая, 80-150 ммоль/л — средняя, свыше 150 ммоль/л — тяжелая степень). Из-за деструкции гепатоцитов возрастают уровни АЛТ, АСТ, щелочной фосфатазы.
- УЗИ печени и желчного пузыря. При проведении сонографии обнаруживается увеличение размеров паренхиматозного органа, неоднородность структуры с чередованием участков гипо- и гиперэхогенности печеночной ткани, повышение объемного кровотока в воротной вене. При длительном течении желтухи выявляются очаги фиброзных изменений.
- Томография гепатобилиарной системы. МРТ печени и желчевыводящих путей, ОФЭКТ печени, МСКТ органов брюшной полости назначают при недостаточной чувствительности сонографии. Метод помогает обнаружить воспалительные инфильтраты, дистрофические изменения печеночной ткани, утолщение стенок желчного пузыря, патологию сосудистой сети.
- Фиброэластометрия. Неинвазивное сканирование органа при помощи аппарата Фиброскан дает возможность уточнить степень замещения паренхиматозной ткани фиброзными элементами по шкале Метавир и по эластичности печени (выраженной в кПа). Метод имеет высокую информативность, поскольку измерения проводятся одновременно в нескольких точках.
- Пункционная биопсия печени. Для оценки строения паренхимы выполняется чрескожная биопсия под контролем УЗИ с последующим гистологическим исследованием. При печеночной желтухе выявляются некротические изменения, воспалительные инфильтраты, признаки перипортального или перицеллюлярного фиброза, жировая дистрофия.
В клиническом анализе крови определяется увеличение СОЭ, нарушения в лейкоцитарной формуле (нейтрофилез или лимфоцитоз). В анализе мочи наблюдается повышение уровня уробилина, в анализе кала снижен или отсутствует стеркобилин. При подозрении на поражение билиарной системы производится ретроградная холангиопанкреатография. Для комплексной оценки состояния абдоминальных органов осуществляется МРТ. Дифференциальная диагностика проводится с гемолитической и механической желтухами, иктеричностью кожи вследствие употребления акрихина, а также между различными заболеваниями, способными вызвать печеночный желтушный синдром. Помимо гастроэнтеролога и гепатолога пациенту рекомендованы консультации инфекциониста, гематолога, онколога, генетика.
Лечение паренхиматозной желтухи
При печеночном желтушном синдроме по возможности проводится этиопатогенетическая терапия патологического состояния, которое осложнилось нарушением обмена билирубина. Основными целями лечения являются воздействие на этиологический фактор, восстановление метаболизма гепатоцитов, коррекция расстройств, вызванных гипербилирубинемией и печеночной дисфункцией. С учетом причины желтухи могут назначаться противовирусные, антибактериальные, иммуномодулирующие средства, глюкокортикостероиды, цитостатики, химиотерапевтические препараты для лечения опухолей печени.
Выраженная интоксикация считается показанием для проведения массивной инфузионной терапии с использованием коллоидных и кристаллоидных растворов, плазмозаменителей, препаратов крови, дезинтоксикационных средств, назначения специфических антидотов (ацетилцистеина при поражении печеночных клеток парацетамолом и др.). При тяжелом течении рекомендованы плазмаферез, гемосорбция, гемодиализ. Для непосредственного воздействия на печеночные паренхиматозные элементы применяют:
- Гепатопротекторы. Фосфолипидные, аминокислотные, антиоксидантные, витаминные препараты стабилизируют мембраны гепатоцитов и клеточных органелл, защищают печень от некроза, стимулируют регенераторные процессы. Некоторые средства обладают антитоксическим действием, нормализуют основные функции печени, предотвращают внутрипеченочный холестаз.
- Медикаменты, предотвращающие склероз паренхимы. Для профилактики избыточного образования соединительной ткани назначают противовоспалительные препараты, тормозящие процессы фиброза. Эффективны периферические вазодилататоры, которые усиливают кровоснабжение паренхиматозной ткани, уменьшают ишемию, улучшают доставку кислорода к гепатоцитам.
При значительном повышении уровня неконъюгированного билирубина показана фототерапия, позволяющая преобразовать несвязанный пигмент в водорастворимый изомер, который может экскретироваться почками. Для уменьшения зуда при холемическом синдроме применяют урсодезоксихолевую кислоту, которая также улучшает метаболизм гепатоцитов. Медикаментозную терапию дополняют коррекцией диеты с частым дробным питанием, ограничением жирной, жареной пищи, экстрактивных веществ. Хирургические методы лечения (различные виды резекции печени) используют в комплексной терапии объемных новообразований. При массивной необратимой деструкции паренхиматозной ткани рекомендована трансплантация органа.
Прогноз и профилактика
Исход зависит от тяжести основного заболевания, наличия осложнений, сохранности функций печени, общего состояния организма пациента. Прогноз паренхиматозной желтухи благоприятен при отсутствии необратимых патологических изменений органа и своевременном лечении первопричины болезни. Профилактика состояния заключается в предупреждении заболеваний, которые могут вызвать желтуху. Необходимо соблюдать меры личной гигиены, не употреблять воду из открытых водоемов, избегать случайных связей и незащищенных половых контактов, проводить прививки против гепатита В согласно схеме вакцинации. Для профилактики токсического повреждения паренхиматозной ткани важно ограничить употребление алкоголя, соблюдать осторожность при работе с производственными ядами, учитывать противопоказания при назначении гепатотоксичных лекарственных средств.
Механическая желтуха — желтушный синдром, связанный с нарушением выделения конъюгированного билирубина в просвет кишечника. Проявляется иктеричностью кожи, слизистых, склер, болезненностью в правой подреберной области и эпигастрии, диспепсическими явлениями, ахоличным калом и бурой мочой, холемическим кожным зудом. Диагностируется с помощью биохимического анализа крови, УЗИ гепатобилиарной системы, МСКТ брюшной полости, РХПГ. Для лечения применяется комплексная медикаментозная терапия, хирургические методы временного и постоянного восстановления тока желчи (литотрипсия, стентирование, дренирование, стомирование и др.).
МКБ-10
Общие сведения
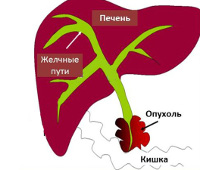
Синдром механической (подпеченочной, обтурационной, компрессионной, застойной) желтухи — вторичное патологическое состояние, осложняющее течение других заболеваний брюшной полости. У 20% пациентов расстройство связано с наличием желчнокаменной болезни, у 67% — с онкопатологией, у 3% — с другими причинами. До 30 лет желтушный синдром обычно вызывается холецистолитиазом, с 30 до 40 лет соотношение случаев неопухолевой и опухолевой механической желтухи составляет 1:1, после 40 лет преобладают онкологические этиологические факторы. До 82% составляют женщины, у которых холестаз возникает преимущественно на фоне ЖКБ. У мужчин чаще выявляется опухолевая обтурация (до 54% случаев).

Причины механической желтухи
Подпеченочный холестаз — полиэтиологическое синдромальное состояние, вызванное нарушением оттока желчи из печени. У большинства пациентов застой желчи обусловлен механической обтурацией, реже непроходимость желчевыводящих путей имеет динамическое (функциональное происхождение). Специалисты в сфере гастроэнтерологии, гепатологии, хирургии выделяют следующие группы причин подпеченочной желтухи:
- Аномалии развития. Нормальная экскреция желчи становится невозможной при врожденной атрезии желчевыводящих путей. Препятствиями для желчевыделения могут служить кисты общего желчного протока, дуоденальные дивертикулы, расположенные вблизи фатерова соска. Отток желчи существенно замедляется при гипоплазии желчных ходов.
- Невоспалительная патология желчных путей. Подпеченочный холестаз возникает при холангиолитиазе, осложнившем ЖКБ. Нарушение проходимости желчных путей наблюдается при обтурации большого дуоденального сосочка вколоченными камнями, его стенозе, рубцовых стриктурах желчных протоков, сдавливании холедоха кистой головки поджелудочной железы.
- Воспалительные процессы. К значительному сужению или перекрытию путей оттока желчи приводят холангит, острый холецистит, осложнившийся спаечным перипроцессом, панкреатит, острый папиллит. Во всех этих случаях физиологический отток желчи замедляется вследствие отека стенки протоков, паренхимы органов, механического сдавления спайками.
- Объемные образования. При раке головки панкреатической железы, фатерова сосочка, печеночных протоков и холедоха, папилломатозе желчных ходов создаются условия для стойкой механической обтурации желчных путей. Аналогичная ситуация возникает при расположении в воротах печени лимфом, метастатически пораженных лимфатических узлов.
У некоторых пациентов причиной подпеченочной желтухи становятся паразитарные заболевания – желчные ходы могут сдавливаться извне эхинококковыми и альвеококковыми кистами, а попадание гельминтов в просвет протоков приводит к механической обтурации. Крайне редко холестаз развивается из-за сдавления большого дуоденального соска при отеке поджелудочной железы или его закупорке слизистой пробкой, желчной «замазкой».
Патогенез
За счет выделения водорастворимого конъюгированного билирубина почками моча приобретает характерную темную окраску («цвет пива»), в ней появляются желчные кислоты. Застой усугубляется внутрипеченочной желчной гипертензией. При достижении уровня 270 мм вод. ст. желчные капилляры расширяются, их стенки повреждаются, что способствует попаданию компонентов желчи непосредственно в кровоток. Вторичное поражение гепатоцитов сопровождается нарушением захвата и конъюгации непрямого билирубина, что приводит к увеличению его уровня в плазме. Поскольку при полной механической обтурации желчь не поступает в кишечник и не подвергается дальнейшей трансформации, в кале и моче не определяется уробилин. Из-за отсутствия стеркобилина стул становится обесцвеченным.
Симптомы механической желтухи
Основными признаками заболевания являются интенсивное желтое окрашивание кожных покровов, слизистых и склер, тупые, постепенно усиливающиеся боли в правом подреберье и эпигастральной области, диспепсические расстройства (тошнота, рвота, снижение аппетита). Патогномоничный симптом механической обструкции желчевыводящих протоков — обесцвечивание кала, сочетающееся с темной окраской мочи. У большинства больных развивается сильный кожный зуд, который не поддается медикаментозной терапии. При желтухе, связанной с воспалительными процессами в желчных протоках, может выявляться гипертермия. При опухолевой природе заболевания у пациентов наблюдается резкая потеря массы тела вплоть до кахектического состояния.
Осложнения
Угнетение дезинтоксикационной функции печени при желтухе приводит к накоплению в крови аммиака, ацетальдегидов, что проявляется в виде синдрома эндотоксемии. В результате нарушается микроциркуляция, происходят дистрофические изменения в органах, в тяжелых случаях возникает ДВС-синдром. Самое опасное осложнение механической желтухи — формирование печеночно-почечной недостаточности, которая является частой причиной смерти пациентов. Вследствие проникновения токсинов в головной мозг через гематоэнцефалический барьер формируется печеночная энцефалопатия, которая проявляется ухудшением когнитивных функций, нарушениями сознания, дискоординацией движений. Избыточное накопление желчных кислот также может приводить к изменению свойств сурфактанта и нарушениям газообмена в легких.
Диагностика
Постановка диагноза механической желтухи не представляет затруднений при наличии характерной клинической картины. Диагностический поиск направлен на оценку тяжести состояния пациента и выявление основного заболевания, которое привело к блокировке выведения желчи. План обследования включает следующие лабораторные и инструментальные методы:
- Биохимический анализ крови. Основной признак – значительное (в несколько раз) повышения уровня прямого билирубина. Также при желтухе наблюдается возрастание показателей щелочной фосфатазы и холестерина, что указывает на синдром холестаза. Иногда отмечается увеличение печеночных трансаминаз, альдолазы, лецитина, липопротеинов.
- УЗИ печени и желчного пузыря. Ультразвуковое исследование позволяет обнаружить структурные изменения печеночной паренхимы (повышение или снижение эхогенности ткани), утолщение стенки желчного пузыря, дилатацию протоков. При сонографии определяют конкременты, которые вызывают механический блок выделения желчи в кишечник.
- МСКТ органов брюшной полости. При помощи послойного исследования тонкими срезами (0,625 мм) с последующим трехфазным контрастным усилением визуализируют взаимное расположение и размеры печени, поджелудочной железы, желчного пузыря. Компьютерная томография дает возможность выявить камни и новообразования, вызывающие развитие желтухи.
- Ретроградная холангиопанкреатография. Внутривенное контрастирование желчевыводящих протоков проводится для обнаружения конкрементов, которые на холангиограмме представлены в виде теней. При наличии противопоказаний возможно выполнение чрескожной холангиографии, особо ценной при подозрении на опухолевую природу желтухи.
В клиническом анализе крови зачастую обнаруживается повышение СОЭ до 20 мм/час и умеренный лейкоцитоз, может наблюдаться снижение эритроцитов и гемоглобина. Дополнительно проводят исследование крови на альфа-фетопротеин, концентрация которого повышается при наличии злокачественного новообразования. В лабораторном анализе мочи при механической закупорке желчевыводящих путей отсутствует уробилин. При затруднениях в постановке диагноза производят лапароскопию.
Дифференциальную диагностику осуществляют с печеночной и гемолитической желтухой, врожденными ферментопатиями, сопровождающимися повышением уровня билирубина в крови (синдромом Жильбера, Дабина-Джонсона), желтушностью кожи при длительном приеме акрихина. Помимо наблюдения гастроэнтеролога или гепатолога больному рекомендован осмотр абдоминального хирурга, инфекциониста, невропатолога, гематолога, онколога, анестезиолога-реаниматолога.
Лечение механической желтухи
На первом этапе при подпеченочном холестазе назначается комплексная терапия, позволяющая ликвидировать застой желчи, купировать эндотоксикацию и стабилизировать состояние пациента. Схема медикаментозного лечения включает гепатопротекторы, аминокислоты, репаранты, анаболические средства, витаминные препараты. В более тяжелых случаях обтурационной желтухи целесообразно применение кортикостероидов, инфузионной терапии с массивным вливанием коллоидных и кристаллоидных растворов, кровезаменителей. При выраженной интоксикации рекомендованы гемосорбция, плазмаферез, гемодиализ.
Для профилактики острых гастроинтестинальных язв назначают блокаторы протонной помпы, антацидные и обволакивающие средства. При риске развития острого холангита показано введение карбапенемов, цефалоспоринов 3-4 поколения и других антибактериальных средств широкого спектра действия, способных проникать в желчь. Для экстренной декомпрессии желчных путей используют хирургические подходы:
- Малоинвазивные инструментальные вмешательства. Эффективными способами устранения включений, блокирующих желчевыделение, являются литотрипсия конкрементов желчных протоков, эндоскопическое удаление камней в сочетании с ретроградной панкреатохолангиографией и рассечением устья фатерова соска, назобилиарное дренирование при РПХГ. При наличии стриктур и стенозе применяются эндоскопические техники — стентирование холедоха, бужирование желчных протоков, баллонная дилатация сфинктера Одди. Чрескожное транспеченочное дренирование желчевыводящих ходов позволяет выполнить декомпрессию при невозможности проведения манипуляции через эндоскоп.
- Операции на билиарной системе. Показаниями для прямых хирургических вмешательств на высоте желтухи являются сочетание желтушного синдрома с острым панкреатитом, случаи механической обтурации при поражении холедоха. При сохраненной проходимости пузырного протока для отведения желчи выполняется открытая, лапароскопическая, пункционная холецистостомия. Осуществление холедохотомии обеспечивает восстановление проходимости общего желчевыводящего протока. При сложной патологии с поражением нескольких органов более эффективным методом декомпрессии желчевыводящей системы может стать наружное дренирование желчных путей по Холстеду, Керру.
После стабилизации состояния пациента для окончательного устранения предпосылок механической обтурации путей желчевыделения на втором этапе лечения патологии, осложнившейся подпеченочной желтухой, применяют хирургические методы. При обструкции камнем общего протока производят холедохолитотомию — радикальное вмешательство, позволяющее восстановить желчевыделение. Извлечению камня может предшествовать холецистэктомия, проведенная наиболее подходящим для конкретного больного способом (лапароскопическая, открытая, SILS-операция, вмешательство из мини-доступа). При локальной злокачественной неоплазии показана холецистэктомия с резекцией ложа желчного пузыря и лимфодиссекцией.
Наложение билиодигестивных анастомозов (холедоходуоденостомия, холедохоэнтеростомия, холецистогастростомия, холецистодуоденостомия, холецистоэнтеростомия) используют при опухолевых процессах и грубой рубцовой деформации желчных протоков. Объем оперативного лечения при обструктивной гепатобилиарной, гастроинтестинальной и других видах хирургической патологии выбирают с учетом соответствующих медицинских протоколов.
Прогноз и профилактика
Вероятность полного выздоровления зависит от тяжести основного заболевания и наличия интеркуррентных патологий. При своевременном лечении смертность не превышает 5%, прогноз относительно благоприятный. При вынужденном проведении оперативного вмешательства на высоте механической желтухи уровень летальности достигает 10-30%. Меры специфической профилактики не разработаны. Для предупреждения развития желтухи необходимо осуществлять раннюю диагностику и адекватную терапию состояний, которые могут вызывать механическую закупорку холедоха, фатерова соска, выполнять плановую санацию при наличии в полости желчного пузыря мелких конкрементов.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирусный гепатит A: причины появления, симптомы, диагностика и способы лечения.
Определение
Гепатит А – это воспалительное заболевание печени, возбудителем которого является РНК-содержащий вирус гепатита А, относящийся к роду Hepatovirus (семейство Picornaviridae). Вирус представлен шестью генотипами (I–VI). Известен только один антиген вируса гепатита А – НААg, к которому вырабатываются антитела. По сравнению с другими представителями рода энтеровирусов, вирус гепатита А более устойчив к физико-химическим воздействиям факторов внешней среды. Он способен сохраняться в воде, пищевых продуктах, сточных водах, на различных объектах внешней среды в течение нескольких месяцев в температурном диапазоне от +4 до +20°С, устойчив к действию кислот и жирорастворителей. При кипячении вирус разрушается в течение 5 минут, при обработке хлорамином – через 15 минут.
Вирус гепатита А относится к числу распространенных инфекций пищевого происхождения. В мире ежегодно регистрируется около 1,5 млн случаев этого заболевания. Россию в целом относят к регионам со средней (промежуточной) эндемичностью.
Причины появления гепатита А
Человек – единственный источник вируса гепатита А. Риску заражения подвержен любой ранее невакцинированный и неинфицированный. Заболевание возникает как в виде единичных случаев, так и в виде эпидемий, которые имеют тенденцию к цикличности. Вспышки гепатита А тесно связаны с отсутствием безопасной воды или пищи, ненадлежащей санитарией и плохой личной гигиеной.
Вирус обладает высокой инфекциозностью: для заражения достаточно всего нескольких вирусных частиц. Передача вируса осуществляется посредством фекально-орального механизма, который реализуется всеми путями, характерными для кишечных инфекций:
- водным путем – вирус попадает в организм с недоброкачественной питьевой водой, во время купания в загрязненных водоемах и бассейнах. Крупные вспышки связаны с загрязнением фекалиями водоемов, являющихся источником водоснабжения, или с попаданием сточных вод в водопроводную сеть;
- пищевым путем – реализуется при употреблении продуктов, загрязненных вирусом во время производства на пищевых предприятиях, предприятиях общественного питания и торговли. Ягоды, овощи, зелень могут быть загрязнены при выращивании на полях орошения или на огородах, удобряемых фекалиями. Морепродукты могут быть инфицированы при отлове моллюсков в загрязненных сточными водами прибрежных водах;
- контактно-бытовым путем – в детских коллективах этот путь имеет наибольшее значение (через грязные руки и различные предметы обихода: игрушки, посуду, белье и т. д.). Реализуется при несоблюдении правил личной гигиены.
В подавляющем большинстве случаев (около 95%) вирус гепатита А внедряется в организм человека через ротовую полость и далее попадает в желудок. Будучи кислотоустойчивым, вирус легко преодолевает желудочный барьер, поступает в тонкую кишку, всасывается в кровь и по системе воротной вены достигает печени, в клетках которой осуществляется его репликация. На мембране гепатоцитов есть соответствующие вирусу рецепторы, к которым он прикрепляется и проникает внутрь печеночной клетки. Часть вновь образованных вирусных частиц поступает с желчью в фекалии и выделяется из организма, другая инфицирует соседние гепатоциты.
Активное выделение вируса из организма больного в инкубационном и преджелтушном (продромальном) периодах в сочетании с высокой устойчивостью вируса во внешней среде обусловливают широкое распространение гепатита А.
Актуальность заболевания обусловлена также частым сочетанием с вирусными гепатитами иной этиологии и хроническими заболеваниями печени, а также отсутствием в нашей стране широкой плановой вакцинации населения при наличии доступных высокоиммуногенных вакцин. Иммунитет после перенесенного гепатита А прочный и длительный, практически пожизненный.
Классификация заболевания
Клинические варианты:
- типичный (желтушный);
- атипичный:
- безжелтушный,
- стертый,
- субклинический (инаппарантный).
- преджелтушный,
- желтушный,
- реконвалесценции.
- легкая,
- среднетяжелая,
- тяжелая,
- фульминантная (злокачественная).
По исходам заболевания:
- выздоровление;
- остаточные явления:
- гепатофиброз,
- постгепатитный синдром (астенический),
- поражение билиарной системы,
- синдром Жильбера.
- гриппоподобный вариант – характеризуется резким повышением температуры до 38–39оC, которая держится 2-3 дня, головной болью, ломотой в мышцах и суставах, иногда небольшим насморком и болью в горле;
- для диспепсического варианта характерны боль и тяжесть в правом подреберье, снижение аппетита, тошнота и рвота, учащение стула до 2-5 раз/сутки;
- астеновегетативный вариант отличает слабость, раздражительность, сонливость, головная боль и головокружение;
- при смешанном варианте за два дня до появления желтушности склер и кожных покровов моча приобретает темный цвет, а стул светлеет;
- у детей возможны интенсивные боли в животе, имитирующие острый аппендицит, желчную колику. Для взрослых эти симптомы не характерны.
Примерно через месяц наступает выздоровление, исчезают клинические проявления и нормализуются показатели крови, улучшается общее самочувствие, светлеет моча, кал приобретает естественную окраску. Однако пациенты могут жаловаться на быструю утомляемость после физической нагрузки, тяжесть в животе после еды, иногда сохраняется незначительное увеличение печени. Продолжительность этого периода в большинстве случаев не превышает 3 месяцев.
У некоторых пациентов гепатит А рецидивирует. В этом случае за периодом выздоровления следует обострение. Тем не менее, после этого заболевание, как правило, заканчивается полным выздоровлением.
Как и при других острых вирусных гепатитах, основным критерием тяжести гепатита А является синдром интоксикации, который состоит из разных по степени выраженности признаков: общей слабости, адинамии, головокружения, диспепсических расстройств, вегетососудистых нарушений, в отдельных случаях наблюдается помрачнение сознания.
Диагностика гепатита А
По клинической картине гепатит А не отличается от других типов острого вирусного гепатита. Точный диагноз подтверждается путем анализа крови на наличие специфичных иммуноглобулинов:
-
класса IgM Аnti-HAV IgM, маркер острой фазы заболевания, начинает обнаруживаться в конце инкубационного периода, синтезируются у всех инфицированных независимо от течения заболевания, циркулируют в крови в среднем 3-4 месяца;
Иммуноглобулины класса М, характерны для острого периода гепатита А. Функции. Антитела класса IgМ практически всегда обнаруживаются уже в начале проявления клинических симптомов, достигают пика концентрации в течение месяца, персистируют в крови 3 - 6 месяцев и снижаются до неопределяемого.
Читайте также:

