Вич это все типы герпеса
Обновлено: 26.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Антитела к ВИЧ-1/2 и антиген ВИЧ-1/2 (HIV Ag/Ab Combo): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
ВИЧ-инфекция - инфекционная болезнь, развивающаяся в результате многолетнего персистирования (постоянного пребывания) в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (далее - ВИЧ), характеризующаяся медленно прогрессирующим дефектом иммунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (далее - СПИД).
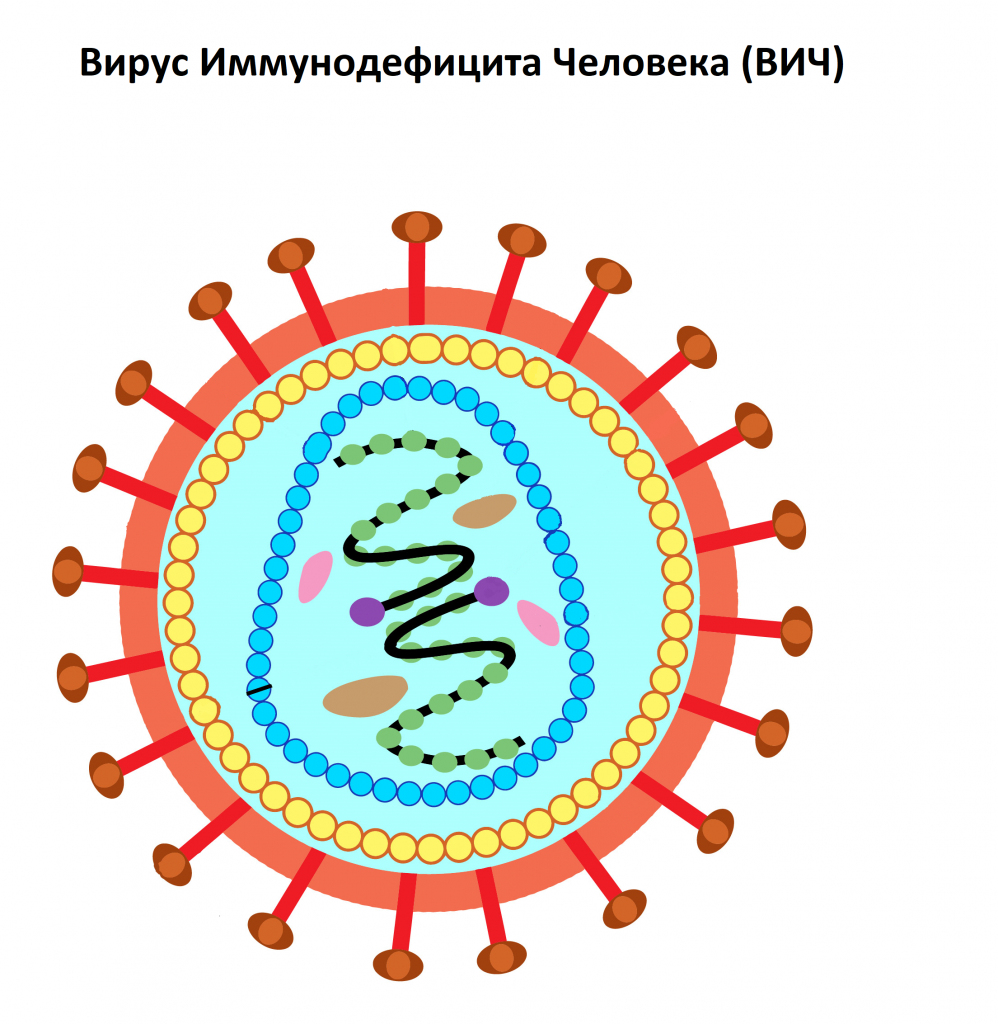
ВИЧ (Вирус Иммунодефицита Человека) – вирус, относящийся к семейству ретровирусов (семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных), который поражает клетки иммунной системы человека. Через несколько недель с момента заражения начинают вырабатываться антитела к ВИЧ.
Показания на проведение исследования
Показаниями для назначения анализа является подготовка к госпитализации и плановому оперативному вмешательству. В профилактических целях следует провести исследование при подозрении на заражение при половом контакте. В первую очередь это касается лиц групп риска: употребляющих наркотики, вводимые внутривенно, часто меняющих половых партнеров и не использующих средств защиты.
Вирус иммунодефицита человека размножается в организме человека достаточно медленно, и количественный результат в отношении антигенов и антител к вирусу можно получить, как правило, не ранее чем через 3-6 недель после инфицирования. При этом клинические симптомы заболевания еще отсутствуют.
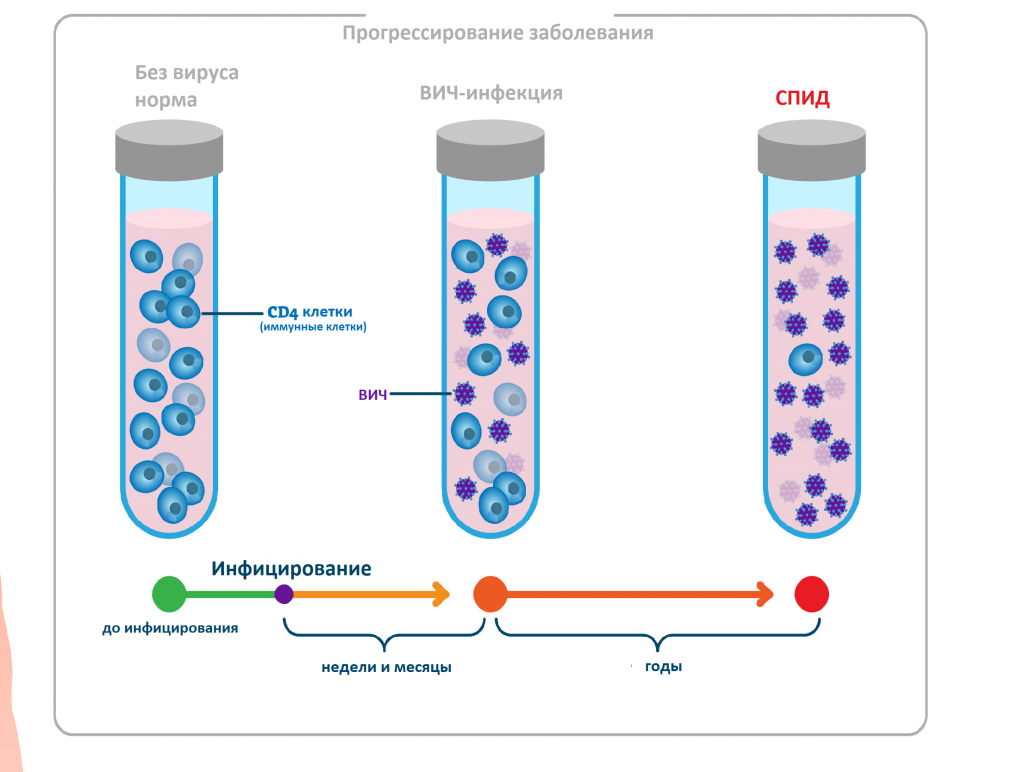
Через три месяца антигены ВИЧ и антитела к вирусу определяются практически у всех заболевших. Благодаря появлению новых комбинированных тест-систем четвертого поколения получение точного результата качественного анализа на ВИЧ-инфекцию возможно уже через две недели с момента попадания вируса в организм. При этом исследовании выявляют антиген р24 ВИЧ – белок вирусного капсида (внешней оболочки вируса).
Анализ на антитела к ВИЧ 1/2 и антиген ВИЧ 1/2 назначают на этапе планирования и при ведении беременности, когда возможна передача вируса плоду. Анализ проводят и после родов, поскольку ребенок ВИЧ-положительной матери может быть инфицирован во время прохождения через родовые пути и при кормлении грудью.

Лихорадка, потеря веса без объективных причин, повышенная утомляемость, увеличение регионарных лимфатических узлов, потливость, особенно в ночное время, длительный кашель, диарея – эти устойчивые клинические симптомы неясного происхождения, отмечаемые в течение 2-3 недель, также служат показанием к проведению исследования на антитела к ВИЧ 1/2 и антиген ВИЧ 1/2.
Кожные проявления также могут быть симптомом ВИЧ-инфекции, поскольку развиваются на фоне ослабления иммунитета. К их числу относится рецидивирующая герпетическая сыпь, поражающая обширные участки кожи, полость рта, половые органы. Герпес поражает и глубокие слои кожи с развитием язвенно-некротической формы. Образуются язвы и эрозии с последующим образованием рубцов, которых не бывает при обычном герпесе.
Еще один характерный симптом ВИЧ-инфекции – волосатая лейкоплакия, которая связана с активацией латентной инфекции, вызванной вирусом Эпштейна-Барр (что свидетельствует об иммуносупрессии). Заболевание проявляется нитевидными образованиями белого цвета с дальнейшим ороговением пораженных участков языка и слизистой оболочки рта.
Обширные грибковые поражения (в первую очередь дрожжевыми грибками рода Candida) также служат типичным признаком, сопровождающим ВИЧ-инфекцию. Сначала кандидоз поражает слизистую оболочку рта и пищевода, затем распространяется на слизистые желудочно-кишечного и мочеполового тракта. При этом формируются обширные очаги, характеризующиеся болезненностью и склонностью к изъязвлению.
ВИЧ-инфекция может сопровождаться развитием обширного папилломатоза. У ВИЧ-инфицированных женщин папилломы цервикального канала склонны быстро вызывать рак шейки матки.
СПИД-индикаторным заболеванием служит саркома Капоши – многоочаговая сосудистая опухоль, которая поражает кожные покровы и слизистые оболочки. Ее очаги в виде красноватых или буроватых узелков и бляшек сливаются, быстро распространяясь по всему телу. Со временем они образуют опухолевые поля, которые изъязвляются и нагнаиваются.
К числу патологических состояний, которые почти у всех пациентов сопровождают ВИЧ-инфекцию, относят полиаденопатию (увеличение лимфатических узлов). Как правило, в первую очередь увеличиваются под- и надключичные, подбородочные, околоушные и шейные лимфоузлы. В дальнейшем к ним может присоединяться увеличение паховых и бедренных лимфатических узлов. Они могут быть мягкими или плотными на ощупь, безболезненными и подвижными. Иногда несколько лимфоузлов сливаются, образуя своеобразный конгломерат. Воспаление двух и более групп лимфоузлов считают признаком генерализованной лимфаденопатии. Поражение лимфатических узлов может наблюдаться в течение нескольких лет, при этом периоды обострения сменяются ремиссией.
К легочным заболеваниям, сопровождающим ВИЧ-инфекцию, относят туберкулез и пневмонию.
Анализ на антигены и антитела к ВИЧ рекомендуют сделать, если у пациента выявлены заболевания, передаваемые половым путем (сифилис, хламидиоз, гонорея, генитальный герпес, бактериальный вагиноз).
Изучены особенности клинического течения локализированных и генерализированных форм герпетической инфекции, обусловленной вирусом простого герпеса І и ІІ типов у 100 больных на разных стадиях ВИЧ-инфекции. Установлено, что локализированные формы герпетической инфекции – лабиальный и генитальный герпес – преобладают у пациентов с І и ІІ стадиях ВИЧ-инфекции. Они отличаются от аналогичных форм у пациентов без ВИЧ-инфекции более тяжелым течением, рецидивирующим характером, склонностью элементов сыпи к распространению на соседние анатомические участки. Висцеральные и генерализированные формы герпетической инфекции, которые свидетельствуют о выраженной иммуносупрессии, характерны для стадии СПИДа. Они проявлялись эрозивно-язвенным эзофагитом, проктитом, интерстициальной пневмонией, энцефалитом, который был непосредственной причиной смерти таких больных. Как СПИД индикаторное заболевание следует рассматривать и локализированные формы герпетической инфекции – лабиальный и генитальный герпес – при эрозивно-язвенном, диссименированном характере поражений продолжительности более 1 месяца.

1. Бабий Н.А. Ко-инфекции вирусного генеза у больных ВИЧ-инфекцией / Н.А. Бабий, А.М. Щербинская // Инфекционные болезни. – 2007. – № 2. – С. 23–26.
2. Баринский И.Ф. Герпесвирусные инфекции – иммунодефицитные заболевания ХХ века / И.Ф. Баринский // Аллергология и иммунология. – 2004. – Т. 5, № 1. – С. 202–204.
3. Запорожан В.Н. ВИЧ-инфекция и СПИД / В.М. Запорожан, М.Л. Аряев. Изд. перераб. и доп. – Киев: Здоровье, 2004. – 636 с.
4. Казмирчук В.Е. Клиника, диагностика и лечение герпесвирусных инфекций человека / В.Е. Казмирчук, Д.В. Мальцев – М.: Феникс, 2009. – 247 с.
5. Казмирчук В.Е. Клиническая иммунология и аллергология / В.Е. Казмирчук, Л.В. Калюжная Л.Д. Ассоциации инфекций, передающихся половым путем у ВИЧ-инфицированных / Л.Д. Калюжная, Л.В. Гречанський // Украинский журнал дерматологии, венерологии, косметологии. – 2004. – № 1.– С. 78–80.
6. Лабораторная диагностика герпесвирусной инфекции человека / Л.А. Панченко, И.И. Торяник, Н.Г. Попова [и др.]. // Инфекционные болезни. – 2006. – № 3. – С. 62–66.
7. Малый В.П. СПИД-ассоциированные инфекции и инвазии: учебное пособие / В.П. Малый, И.С. Кратенко. – Харьков: Фолио, 2007. – 287 с.
8. Маричев И.Л. Герпесвирусы-СПИД маркерные заболевания / И.Л. Маричев // Современные инфекции. – 2005. – № 3–4. – С.55–59.
9. Маричев И.Л. Герпетическая инфекция у ВИЧ-инфицированных / И.Л. Маричев / Инфекционные болезни. – 2006. – № 2. – С.15–17.
10. Медико-профилактические аспекты ВИЧ-инфекции и СПИДа в врачебной практике / Б.М. Дикий, И.Г. Грижак, А.Д. Щербинская [и др.]. – Киев: Изд-во ИФДМУ, 2007. – 236 с.
Введение
Цель нашего исследования - провести ретроспективный анализ течения герпетической инфекции у больных с учетом стадии ВИЧ-инфекции на основании анализа данных медицинских карт стационарных и амбулаторных больных.
Материалы и методы исследования. Проведен ретроспективный анализ медицинской документации 100 больных ВИЧ-инфекцией. В исследуемую группу входили больные на разных стадиях заболевания в возрасте от 18 до 40 лет. I стадия - 24, II - 37, III - 22, IV - 17 больных. Установлено, что среди больных, которые находились на учете в областном Центре борьбы и профилактики ВИЧ/СПИДа, инфицированы ВИЧ парентеральным путем 42 человека, половым - 58. Диагноз ВИЧ-инфекции установлен на основании данных эпидемиологического, клинического и лабораторного обследования, подтверждено двукратным выявлением антител (АТ) к ВИЧ методом иммуноферментного анализа (ИФА). Диагноз ГИ устанавливали на основании выявленных изменений со стороны органов и систем, учитывая политропность возбудителя и генерализированный характер поражений в терминальной стадии заболевания. Этиологическая расшифровка ГИ базировалась на результатах полимеразной цепной реакции (ПЦР).
Ни одного случая острой ГИ у пациентов с ВИЧ-инфекцией не зарегистрировали. Во всех диагностировали различные формы хронической ГИ, реактивация которой имела место в 38 %, а рецидивирующее течение - в 62 % случаев. Так, ВПГ 1 вызывал рецидивы назального и лабиального герпеса (30 больных), его первые клинические проявления (10 больных), а также гингивостоматит (5 больных) и фаринготонзиллит (2 больных) только в I (21) и ІІ (26) стадиях ВИЧ-инфекции. Количество больных, у которых диагностировали ГИ в указанных стадиях, составляло соответственно 87,4 % и 70,2 %.
ВИЧ-ассоциированная ГИ с поражением кожи и слизистых характеризовалась не только более обильными и распространенными элементами везикулезной сыпи, но и замедленным ее регрессом, продолжительностью более 1 месяца (от 6 до 8 недель). Кроме этого, в 30,7 % больных во ІІ стадии ВИЧ-инфекции наблюдали эрозивно-язвенную форму ГИ - глубокие эрозии с трансформацией в язвы, которые медленно заживали. Следует отметить, что герпетические поражения кожи в виде сгруппированных пузырьков с серозным содержимым отмечали не только в местах их типичной локализации - на губах, крыльях носа. У больных во ІІ стадии ВИЧ-инфекции они распространялись на лоб, щеки, уши. Поражение слизистой ротоглотки всегда сопровождалось постоянной и выраженной болезненностью, гиперемией, гиперсаливацией, язвенным гингивитом.
Рецидивы лабиального герпеса у ВИЧ-инфицированных больных характеризовались большей частотой и выраженностью клинических проявлений в сравнении с больными, не инфицированными ВИЧ. У инфицированных ВИЧ ежемесячные рецидивы лабиального герпеса регистрировали у 26 больных, каждые 3 месяца они развивались у 20 больных и проявлялись групповыми (12 больных) и множественными (8 больных) везикулами, которые распространялись на щеки и околоушную область. У не инфицированных ВИЧ ежемесячных рецидивов не было, каждые 3 месяца они развивались у 4 больных, а каждые 6 месяцев - у 8. При этом элементы сыпи были единичными, не распространялись за пределы губ.
Рецидивы гингивостоматита сопровождались субфебрилитетом, умеренной интоксикацией, множественными глубокими эрозиями с отеком и гиперемией слизистой оболочки полости рта, тогда как у больных без ВИЧ-инфекции они протекали в более легкой форме, без нарушения общего состояния больного, с менее выраженними изменениями слизистой оболочки.
Данные анамнеза свидетельствуют, что до инфицирования ВИЧ рецидивы лабиального герпеса чаще всего имели место каждые 6 месяцев - у 13 больных, тогда как после инфицирования ВИЧ рецидивы у большинства больных (26) наблюдались ежемесячно.
Генитальный герпес (ГГ) чаще диагностировали у больных в ІІІ стадии ВИЧ-инфекции (49,9 %) в сравнении с больными во II стадии (24,3 %) и I (12,0 %). Заболевание имело рецидивирующее течение у 18,9 % больных во II стадии и 40,9 % больных в ІІІ стадии ВИЧ-инфекции. Если в I стадии поражались только наружные половые органы, то во II и III - еще и внутренние (вагинит, цервицит) в виде множественных глубоких эрозий и язв. В IV стадии ВИЧ-инфекции проявления ГГ наблюдали в 11,7 % больных в виде поражений только внутренних половых органов (язвенно-некротический вагинит, цервицит). Нередко ГГ проявлялся еще и экстрагенитальными поражениями, которые обнаруживали на ягодицах, задней и внутренней поверхности бедер у каждого второго больного с II и во всех с III и IV стадиями ВИЧ-инфекции. Явлениями тазового ганглионеврита сопровождался ГГ у 5,4 % лиц с II и 18,1 % с ІІІ стадией ВИЧ-инфекции. Кроме сыпи на больших и малых половых губах, слизистой влагалища, шейке матки, промежности, ГГ проявлялся язвенным поражением уретры и прямой кишки в III и IV стадиях ВИЧ-инфекции. Герпетический уретрит диагностировали у 13,6 % больных в ІІІ стадии, а герпетический проктит - соответственно в 18,1 % и 23,5 % больных в III и IV стадиях заболевания.
Для рецидивов ГГ у ВИЧ-инфицированных больных характерна большая частота и выраженность клинических проявлений, чем у больных не инфицированных ВИЧ. Среди инфицированных ВИЧ ежемесячные рецидивы ГГ наблюдались у 9 больных, каждые 3 месяца они развивались у 5 больных, проявлялись групповыми (2 больных) и множественными (3 больных) везикулами. Каждые 6 месяцев рецидивы ГГ с множественными элементами сыпи возникали у 2 больных. У не инфицированных ВИЧ ежемесячных рецидивов ГГ не было, регистрировались рецидивы каждые 3 месяца - в 3, каждые 6 месяцев - у 2 больных.
Анализируя данные анамнеза, мы установили, что до инфицирования ВИЧ рецидивы ГГ у больных чаще всего имели место каждые 6 месяцев (8 пациентов), тогда как после инфицирования ВИЧ максимальной была частота ежемесячных рецидивов (9 пациентов).
Диагностировали не только локализированные, но и висцеральные и генерализорованные формы ГИ. Гематогенная диссеминация ВПГ 1 в IV стадии ВИЧ-инфекции приводила к поражениям внутренних органов. Диагностировали эзофагит у 29,4 %, а интерстициальную пневмонию - 17,6 % больных. У всех больных пневмония сочеталась с эзофагитом. Генерализация ГИ на фоне выраженного ВИЧ-иммунодефицита сопровождалась поражением ЦНС. Оно проявилось в 17,6 % больных подострым энцефалитом, который был непосредственной причиной смерти. Тяжесть энцефалита обусловлена его некротическим характером.
Клинически у этих больных не наблюдали проявлений общей интоксикации и менингеальных симптомов. Очагово-неврологическая симптоматика развивалась постепенно, проявлялась различными расстройствами сознания с формированием симптомов поражения лобных, височных и теменных отделов мозга. О локальном и мозаичном поражение коры головного мозга свидетельствовали нарушение восприятия, мышления и памяти. Типичными клиническими проявлениями энцефалита были симптомы поражения передних отделов головного мозга - психические расстройства (афазия, дисфазия), агнозия, амнезия, центральные гемипарезы, а также невриты и плегия.
Ликвор при исследовании был прозрачным, бесцветным, ликворное давление нормальное или несколько повышено, плеоцитоз не превышал сотни клеток в 1 мкл, преобладали лимфоциты, белок в пределах нормы, белково-клеточной диссоциации не наблюдалось. По результатам МРТ выявляли гиподенсивные очаги размерами от 1,5 до 5 см в диаметре с локализацией в левой височно-теменной, правой лобной и затылочной долях. Очаги имели неправильную форму, с нечеткими контурами, незначительным перифокальным отеком и геморрагическим пропитыванием.
У больных, умерших от энцефалита, при гистиологическом исследовании тканей головного мозга обнаружили выраженные структурные изменения в сосудах и нервных клетках, которые возникли на фоне отека-набухания головного мозга. Энцефалит характеризовался преимущественно некротическими изменениями с образованием очагов деструкции в сером веществе передних отделов головного мозга (медио-базальных, лобных, височных и теменных) и воспалительной реакцией различной степени выраженности. В меньшей степени поражались оболочки мозга. Мягкие оболочки были утолщены, набухшие, умеренно инфильтрованны гистиоцитарными элементами, лимфоидными клетками, реже нейтрофильными лейкоцитами. Отмечались геморрагии и субарахноидальные кровоизлияния, глубокая дистрофия нейронов: гомогенизация и гиперхромия цитоплазмы, перераспределение хроматина в ядрах нейронов, их пикноз, лизис и гибель нервных клеток. Обнаруживали зоны выпадения нейронов и очаги некроза нервной ткани. В сосудах различного калибра, чаще в капиллярах, во всех случаях наблюдали проявления ДВС-агрегации эритроцитов, сладж и формирование тромбов, наличие геморрагий без периваскулярной инфильтрации.
У таких пациентов наблюдали очагово-некротические изменения в печени и надпочечниках, подобные очаги некрозов на слизистой оболочке ротовой полости, в легких - отек стенок альвеол, интерстициальную пневмонию.
Учитывая очень широкий спектр поражений - от кожи и слизистых оболочек до внутренних органов и ЦНС, диагностика ГИ на фоне ВИЧ-инфекции достаточно сложна. Поэтому без лабораторного подтверждения диагноза у таких больных она невозможна. При этом обнаружение вируса и его антигенов является основным, а антител к вирусу - вспомогательным методом диагностики ГИ.
Нами проанализированы серологические маркеры ВИЧ-ассоциированной ГИ в зависимости от числа СD4 + Т-лимфоцитов у больных без иммунодефицита (>500), с умеренным (500-350), выраженным (350-200) и глубоким (<200) иммунодефицитом.
Установлено, что титры IgG к ВПГ 1/2 у пациентов с ВИЧ-ассоциированной ГИ были разными. Их уровень в большинстве случаев был умеренным (50-100 МЕ/мл) - 51,0±5,0 %, значительно реже низким (100 МЕ/мл) - 22,0±4,1 %. Наблюдали зависимость диагностических уровней ІgG к ВПГ 1/2 от наличия иммунодефицита, обусловленного ВИЧ, и степени его тяжести. Высокий специфический гуморальный ответ на ГИ давали только больные без иммунодефицита (22,0±4,1 %), умеренный - больные с умеренным иммунодефицитом (40,0±4,9 %), незначительный процент с выраженным иммунодефицитом (3,0±1,7 из 13,0±3,4 %) и без иммунодефицита (8,0±2,7 из 0,0±4,6 %). Низкий гуморальний ответ на ГИ характерен для пациентов с глубоким иммунодефицитом (17,0±3,7 %) и большинства с выраженным иммунодефицитом (10,0±3,0 из 13,0±3,4 %).
Таким образом, диагностика ВИЧ-ассоциированной ГИ сопровождается значительными трудностями. Они связаны со сложностью верификации диагноза при помощи специфических серологических маркеров на фоне иммунодефицита. Угнетение синтеза противогерпетических антител класса IgG, низкие их титры у ВИЧ-положительных маскируют истинную частоту активных форм ГИ. Изучение специфических лабораторных маркеров ГИ у ВИЧ-инфицированных показало, что на основании только серологических обследований невозможно установить активность инфекционного процесса и определить тактику лечения больных.
Наиболее информативными являются результаты ПЦР, позволяющие своевременно выявлять активные формы инфекции, что имеет принципиальное значение для тактики лечения больных. Одновременно с серологическими обследованиями выявляли ДНК ВПГ 1/2 методом ПЦР. Герпес кожи и слизистых оболочек подтверждали методом ПЦР в 10,0 % пациентов с поражением слизистой ротоглотки и полости рта у 15,0 % пациентов с нетипичным поражением кожи (эрозивно-язвенным, геморрагически-некротическим, импетигоподобным). В 75,0 % случаев при типичном характера сыпи на коже в виде везикул диагноз не вызывал сомнения. У больных с ГГ чаще получали положительные результаты ПЦР при исследовании материала из влагалища и цервикального канала (соответственно 56,3 и 43,7 %), значительно реже - из прямой кишки и уретры (соответственно 12,5 и 9,38 %).
Положительные результаты ПЦР при исследовании крови, подтверждающие вирусемию и свидетельствующие о репликации ВПГ на системном уровне, получили в 62,5 % больных с генерализованной ГИ. Вирусемия сопровождалась герпетическим эзофагитом (62,5 %), пневмонией (37,5 %), проктитом (25,0 %). Поражались не только пищевод, легкие, прямая кишка, но и ЦНС. Герпетическая этиология энцефалита подтверждена у 100 % больных с генерализованной ГИ при исследовании ликвора методом ПЦР.
Ассоциированную с ВИЧ-инфекцией ГИ следует, по нашему мнению, называть не только СПИД-ассоциированным заболеванием, а суперинфекцией, патогенетически связанной с ВИЧ-инфекцией. На фоне вторичного иммунодефицита, обусловленного ВИЧ, ГИ приобретает генерализированный характер с множественными поражениями внутренних органов и ЦНС. Если в организме здорового иммунокомпетентного человека иммунные механизмы контролируют персистенцию ВПГ в паравертебральных нервных ганглиях, обеспечивая латентную форму ГИ, то на фоне ВИЧ-инфекции, сопровождающейся выраженным иммунодефицитом, ГИ приобретает рецидивное, манифестное течение с системными поражениями, генерализацией инфекционного процесса.
На основании анализа течения и диагностики ВИЧ-ассоциированной ГИ можно сделать следующие выводы:
1. Течение ГИ зависит от стадии ВИЧ-инфекции. У больных в I и II стадиях заболевания диагностировали только локализованные формы ГИ с поражением кожи, слизистой ротоглотки, гениталий, которые отличались рецидивирующим течением, склонностью элементов сыпи к распространению.
2. Клиника ГИ у больных в III и IV стадиях ВИЧ-инфекции полиморфная и проявляется поражениями внутренних органов, которые не наблюдаются у пациентов с ГИ без ВИЧ-инфекции. В условиях иммунодефицита ВИЧ-этиологии ГИ приобретает системный, нередко генерализированный характер с поражением внутренних органов (эзофагит, пневмония, проктит), ЦНС (энцефалит), характеризуется тяжелым и часто является непосредственной причиной смерти больных СПИДом.
3. Как СПИД индикаторное заболевание следует рассматривать и локализованные формы ГИ - лабиальный и генитальный герпес - при эрозивно-язвенном, диссиминированном характере поражений продолжительностью более 1 месяца.
4. Для своевременной диагностики генерализованных форм ГИ необходимо использовать метод ПЦР, диагностическая информативность которого при исследовании крови составляет 62,5 %, а ликвора у больных энцефалитом - 100 %. Диагностическая информативность ПЦР при исследовании материала из влагалища и цервикального канала составляет 100 % у больных с герпетическим цервицитом и вагинитом.
Рецензенты:
Дикий Б.Н., д.м.н., професор кафедры инфекционных болезней с курсом эпидемиологии Государственного высшего ученого заведения «Ивано-Франковский национальный медицинский университет» МОЗ Украины, г. Ивано-Франковск.
Пришляк А.Я., д.м.н., профессор, заведующий кафедрой инфекционных болезней с курсом эпидемиологии Государственного высшего ученого заведения «Ивано-Франковский национальный медицинский университет» г. Ивано-Франковск.
Герпетическая инфекция является одной из наиболее распространённых в мире. Безусловно, одной из главных особенностей вируса герпеса является то, что, попав в наш организм однажды, он сохраняется в течение всей жизни. Течение этого процесса напрямую зависит от функционального состояния иммунной системы и большую роль в этом играет вторичный иммунодефицит, к которому относится ВИЧ-инфекция. Стоит сказать, что клинические проявления герпетической инфекции многогранны: от мелких кожных высыпаний до тяжёлых генерализованных форм с поражением внутренних органов и требующие серьёзного лечения.
Важно отметить, что симптоматика герпетической инфекции, рассмотренная в данной статье, носит преимущественно атипичный характер и характерна для людей с выраженным иммунодефицитным состоянием/ВИЧ-инфекцией. Пациентам, принимающим АРВТ и следующим рекомендациям врачей, удаётся предотвратить развитие данных процессов. Выделяют 8 типов вируса герпеса, давайте рассмотрим их.
Герпетическая инфекция 1 и 2 типов или вирус простого герпеса (ВПГ) широко распространена: антитела обнаруживаются у 80-90% взрослого населения. У людей, с частыми рецидивами ВПГ, риск заражения при контакте с ВИЧ-инфекцией увеличивается в 3 раза. При наличии клинических проявлений герпетической инфекции у ВИЧ-положительных людей отмечается более выраженная симптоматика. Можно выделить ряд особенностей: отмечается нетипичная локализация высыпаний с большей площадью поражения, возможна диссеминация, т.е. распространение процесса, а также нередко отмечается везикуло-эрозивный или язвенно-некротический характер высыпаний.
Герпетическая инфекция 3 типа вызывает такие заболевания как ветряная оспа и опоясывающий лишай. При коинфекции с ВИЧ симптоматика может приобретать более тяжелое течение. Риск развития опоясывающего лишая при прогрессирующей ВИЧ-инфкции до 20 раз выше по сравнению с риском для населения в целом. В 10% отмечаются рецидивы в течение одного года. Выделяют следующие характеристики: интенсивные высыпания, обширные, более глубокие и длительные поражения кожи с образованием рубцов, чаще болевой синдром, частые рецидивы, часто возникает поражение внутренних органов и ЦНС.
Герпетическая инфекция 4 типа или вирус Эпштейна-Барр (ВЭБ) также многим известен. Распространен повсеместно, а у лиц старше 25 лет в 95% случаях уже определяются специфические антитела, указывающие на перенесённый инфекционный процесс. При ВИЧ-инфекции обострение проявлений вируса может наступить в любом возрасте и запустить ряд патологических процессов, связанных с формированием лимфом, поражением внутренних органов. Однако благодаря применению АРВТ удалось значительно снизить количество тяжёлых случаев данной инфекции.
Цитомегаловирусная инфекция, возбудителем которой является вирус герпеса 5 типа также крайне распространена и определяется у 50-80% взрослого населения. При выраженном иммуносупрессивном состоянии возможно поражение внутренних органов: дыхательной системы, желудочно-кишечного тракта, ЦНС, поражение органов зрения (ретинит).
Вирус герпеса 6 типа, как и другие представители семейства герпесов, чаще всего находится в нашем организме в латентном состоянии. Именно с ним связывают появление внезапной экзантемы у детей. И действительно, чаще всего заражение происходит именно в детском возрасте. Однако возможна реактивация, характерная для уже указанного нами иммуносупрессивного состояния, к которым относится и ВИЧ-инфекция.
Вирус герпеса 7 типа нередко связывают с синдромом хронической усталости.
Распространение вируса герпеса 8 типа значительно варьирует в зависимости от региона. В среднем, более 25% взрослого населения имеют антитела к ВГЧ-8. С данным вирусом связывают в первую очередь развитие такого заболевания, как Саркома Капоши.
Несмотря на все клинические проявления, указанные выше, хотелось бы отметить, что тяжесть течения герпетической инфекции напрямую зависит от прогрессирования и стадии ВИЧ-инфекции, поэтому приём АРВТ и систематическое наблюдение у специалиста предотвращает не только развитие тяжёлых форм заболевания, но и сокращает рецидивы герпеса.
Автор материала Дмитрий Вадимович Лавренчук - к.м.н., инфекционист, гепатолог ID-Clinic.
Леонид Борисович Марголис — докт. биол. наук, профессор МГУ. С 1993 г. работает в США, где заведует отделом в Национальном институте здоровья (National Institutes of Health — NIH) и является одним из признанных авторитетов в области фундаментальных исследований ВИЧ. Его работы напечатаны в ведущих мировых научных журналах и широко известны научному сообществу, но поводом к интервью послужила сенсационная статья о его исследованиях, опубликованная в популярнейшей американской газете The New York Times. Вопросы задавали Эмилия Ойгенблик и Алексей Левин.

— Леонид Борисович, Вы недавно завершили исследование, приближающее победу над самой страшной эпидемией нашего времени, вызванной вирусом иммунодефицита. Речь в нем идет не только об этом вирусе, но и о вирусе герпеса. Хотелось бы узнать подробности из первых рук. Расскажите, пожалуйста, о Вашей работе и о том, как вирус иммунодефицита человека связан с вирусом герпеса.
— Я начну издалека. В человеческом организме обитает множество микробов. В соответствии с русской и германской традициями, микроб — это бактерия, может быть клеточный паразит; короче говоря, что-то мелкое, но не вирус. А в английской традиции этот термин включает в себя и вирусы. Бактерии живут у нас на зубах, на слизистых оболочках ротовой и носовой полости, в кишечнике и много где еще. Бактериальных клеток в человеческом кишечнике очень много. Если их посчитать, то окажется, что собственных клеток, доставшихся нам от папы с мамой, всего 10%, а 90% — это бактерии (речь, естественно, идет о количестве, а не о массе). Современные методы генетического анализа показали, что бактерий этих не десяток видов, как полагали еще лет сто назад, а тысяча.
ДНК бактерий отличается от человеческой. Как говорят, она имеет собственный автограф, вследствие чего ее можно вычленить из анализируемых проб. У вирусов такого ДНКового автографа нет, поэтому выявить их генетическим анализом очень непросто. Микробы образуют экосистему, и каким образом ее члены, в особенности вирусы, взаимодействуют друг с другом — великая тайна. Мы даже не знаем, сколько вирусов обитает в организме, но, по аналогии с бактериями, можем предположить, что это огромный мир, дверь в который лишь чуть-чуть приоткрылась.
Вирусы в организме, как и во всякой экосистеме, взаимодействуют самым различным образом: помогают друг другу, противодействуют друг другу, игнорируют друг друга.
— А можно привести примеры?
— Ну, вот пара таких примеров для иллюстрации:
У больных, которых долгие годы лечили противоспидовыми препаратами и которые не прекращают их принимать, вирусных частиц в крови больше нет, но зато нередки атеросклероз и иные расстройства, связанные с повышенной активностью иммунной системы. С кем же иммунная система продолжает бороться, когда ВИЧ уже подавлен? Предполагают, что такая активация иммунной системы обусловлена еще каким-то вирусом. Не исключено, что это мегаловирус, «разбуженный» вирусом иммунодефицита.
И наоборот, у ВИЧ-инфицированных африканских детей на пике заболевания корью число вирусов иммунодефицита в крови значительно сокращается, а по завершении острого периода возвращается к прежнему уровню. То есть вирус кори подавляет ВИЧ. Несколько лет назад мы выяснили, что это работа хемокинов — разновидности белков-цитокинов, регулирующих иммунный ответ. Хемокины цепляются к тем же рецепторам на поверхности клетки, что и вирус иммунодефицита. Под влиянием вируса кори молекул хемокинов становится гораздо больше, и ВИЧ далеко не всегда удается найти место для «парковки».
— А теперь расскажите про вирус герпеса.
— В организме человека могут гнездиться восемь его разновидностей. Некоторые из них совершенно безвредны, другие же представляют серьезную опасность. Высыпания на губах весной, в просторечии называемые весенней лихорадкой (помните у Пастернака?), вызываются вирусом герпеса №1 и знакомы каждому. Кстати, этот вирус упоминает и Шекспир в «Ромео и Джульетте»:
И губы дев, которым снится страсть.
Шалунья Маб их сыпью покрывает
За то, что падки к сладким пирожкам.
Меркуцио прав! Этот вирус герпеса передается именно так. Другой знакомый всем вирус герпеса имеет №3. Он вызывает ветрянку, которой почти все мы болели. Но герпес — не только эти относительно легкие болезни, но и саркома Капоши, и генитальный герпес — заболевание, передающееся половым путем. Вирусы герпеса постоянно присутствуют в организме, но находятся под контролем иммунной системы, и только время от времени некоторые из них активируются. И, наверное, не зря! Есть теория, что на герпесе иммунитет отлаживает стратегию борьбы с прочими вирусами и потихоньку нарабатывает активные клетки, которые идут в ход при появлении настоящей опасности. Вообще, герпес — один из самых древних вирусов в организме человека. Именно поэтому мы научились с некоторыми его видами мирно уживаться. Герпесом-1 (лихорадка) заражено огромное число людей. Герпес шестой разновидности есть практически у всех. Герпес-2 (генитальный) и 8 (саркома Капоши), к счастью, встречаются гораздо реже.
Но это — лишь пока всё в порядке с иммунитетом. Даже десятилетия спустя после забытой детской ветрянки вызвавший ее герпес-3 организма не покидает, а проникает в нервные окончания и в случае ослабления иммунной системы выходит на тропу войны: активируется, начинает усиленно размножаться и вызывает сильнейшие боли в области шеи и головы.
Похожие вещи происходят и с ВИЧ-инфицированными. Особенно часто вирусу иммунодефицита сопутствует вирус герпеса под №2 (генитальный герпес). Что значит сопутствует? Если человек заражен герпесом, ему легче заразиться иммунодефицитом. Раньше считали, что это происходит потому, что герпетические язвочки — открытые ворота для ВИЧ-инфекции, однако и без язвочек герпес способствует заражению. Более того, при наличии герпеса синдром приобретенного иммунодефицита проявляется в гораздо более тяжелой форме.
— Можно немного о современных противоспидовых препаратах?
— Исследователи из Бельгии совместно с чешским ученым Хоули изобрели замечательное лекарство — тенофовир, и вот уже около 15 лет им пользуются во всем мире для лечения иммунодефицита. Химически он похож на аденозин — один из компонентов любой ДНК. Обратная транскриптаза ВИЧ, фермент, который строит цепочку вирусной ДНК, не отличается особой разборчивостью и посему встраивает на место аденозина тенофовир (точнее, его трифосфат, в который он превратился в клетке). Однако, в отличие от аденозина, тенофовир устроен таким образом, что к нему прицепить уже ничего нельзя, на этом месте цепочка ДНК обрывается, и синтез заканчивается.
Поэтому таблетки тенофовира применяются в качестве терапевтического средства против ВИЧ. Однако даже с помощью тенофовира и других лекарств полностью излечить зараженного ВИЧ не удается. Поэтому основная задача — предотвратить инфекцию, перекрыть пути ее проникновения.
— Вы ставите во главу угла профилактику ВИЧ-инфекции. Как ее можно осуществить?
— Во-первых, конечно, изменением модели социального поведения. Из медицинских средств — упование на вакцины. Но хороших вакцин пока просто нет. Недавно был некоторый успех: белок вируса иммунодефицита вставили в цитомегаловирус, на который есть хороший иммунный ответ, и на обезьянах эта вакцина вроде бы работала. Всё остальное либо никуда не годится, либо находится в стадии испытаний. Я считаю, что в ближайшее время вакцин не будет.
Другой способ — применение микробицидов, веществ, которые наносятся непосредственно на слизистую и локально предотвращают инфекцию. До последнего времени микробициды тоже не слишком радовали: положительных результатов не было, более того, дважды случалось так, что микробициды даже увеличивали риск заражения людей, на которых их испытывали. Вот такая скандальная ситуация.
Каждый исследователь пытался разработать собственный препарат, и в конце концов группа южно-африканских ученых при поддержке международных фондов взяла тенофовир, изготовила на его основе гель и испытала его в качестве микробицида. Положительные результаты этих испытаний оказались статистически достоверными — вероятность заражения СПИДом сократилась на 38%. Для науки это огромный прорыв, хотя для практики и не столь впечатляющий. Выяснилось также, что нанесенный на слизистую тенофовир уменьшает шансы заражения генитальным герпесом аж на 51%! Это было не слишком понятно, но стало приятным сюрпризом — оказалось возможным подавить два взаимодействующих вируса одним и тем же способом. Думали, что в основе этого лежит чрезвычайно сложный механизм — через активацию вирусов, через какие-то промежуточные вещества. Но дело неожиданно оказалось проще!
— И в чем же этот механизм заключается?
— Нам удалось показать, что в данном конкретном случае имеет место прямой эффект — тенофовир угнетает и вирус иммунодефицита, и вирус герпеса. Выяснилось, что то самое похожее на аденозин фосфорилированное производное тенофовира, которое останавливает синтез ВИЧ, включается с помощью фермента ДНК-полимеразы и в ДНК вируса герпеса и блокирует процесс ее репликации. Когда тенофовир был изобретен, его принялись испытывать на самых разных вирусах и выяснили, что он подавляет один лишь ВИЧ. Поэтому наша работа как бы противоречила предыдущим исследованиям. Но эти противоречия оказались мнимыми! Дело в том, что гель, с которым мы работали, содержит значительно больше тенофовира, нежели таблетки. Кроме того, гелеобразный тенофовир контактирует с гораздо большим числом клеток — потенциальных мишеней вируса, нежели пероральный препарат. Непосредственный контакт со слизистой оболочкой позволяет лекарству гораздо лучше проникать в ткань; его концентрация в клетке возрастает, и посему в данном случае гель работает намного эффективней, чем таблетки. Такой концентрации тенофовира никто никогда не испытывал. Она представлялась нефизиологической — чрезвычайно высокой. Да и все испытания тенофовира как противоспидового препарата показывали, что он работает при гораздо меньшей концентрации, превышение которой в тысячу раз выглядело бессмыслицей.
Следует отметить, что основная проблема фармакологии — направленная доставка лекарств к цели. Лекарства для растущих вне организма клеток есть от всего, но если человеку принимать их в действенных концентрациях, возникают такие побочные эффекты, что непонятно, что хуже — болезнь или ее лечение. Поэтому никто и не испытывает лекарства в концентрациях, значительно превышающих действующие. Так или иначе, при местном применении изобретенный для борьбы с ВИЧ тенофовир действует и против его спутника — вируса герпеса. Кстати, когда я говорю «наша работа», то имею в виду не только сотрудников моего отдела в Национальном институте здоровья США, но и моих коллег из Бельгии и Италии, вместе с которыми мы выполняли это исследование.
Интересно, что эта наша работа с тенофовиром является как бы зеркальным отражением нашего же предыдущего исследования с лекарством, созданным для борьбы с вирусом герпеса. Два года назад мы выяснили, что антигерпесный препарат ацикловир эффективно справляется с вирусом СПИДа. В чем сходство и различие действия этих препаратов, и почему эта история зеркальная? Тенофовир создали для борьбы с ВИЧ-инфекцией, ацикловир — для лечения некоторых разновидностей герпеса, в первую очередь генитального герпеса. Кстати, в любой аптеке можно купить зовиракс — мазь на основе ацикловира, помогающую избавиться от лихорадки на губах. Так же как тенофовир похож на аденозин, ацикловир похож на гуанозин. Он тоже встраивается в ДНК вируса иммунодефицита и останавливает удлинение ее цепи. Однако в этом случае фосфорилирование осуществляется не клеточными ферментами, а ферментами вируса герпеса, и поэтому происходить подобное может лишь в зараженной герпесом клетке. Тем не менее, фосфорилированный ацикловир как-то проникает в соседние клетки и угнетает там размножение вируса СПИДа.
— Возможна ли разработка комплексного лечения СПИДа и герпеса?
— Хотелось бы думать, что да, ведь этим мы и занимаемся! В настоящее время проводятся клинические испытания ацикловира как средства против ВИЧ. Нам бы хотелось испробовать его и как микробицид, но это дело будущего. К сожалению, степень подавления второго вируса не столь велика, как хотелось бы. Посему задача — химическая модификация этих препаратов.
Но даже в случае успеха одним веществом ВИЧ не победить! И основное достижение в этой области — комплекс веществ, каждое из которых угнетает один из ферментов в цикле размножения вируса. Таких соединений не очень много, но на каждый фермент есть свое вещество. Сейчас вот пробуют сделать ингибитор рецепторов, к которым цепляется вирус.
Почему вообще нужны еще и новые лекарства? Дело в том, что ВИЧ мутирует с бешеной скоростью. Мы привыкли верить в точность биологического копирования, ведь иначе дети не были бы похожи на родителей, кошка — на кошку, а мышка — на мышку. А вот вирус иммунодефицита избрал иную стратегию — частицы не должны быть похожи друг на друга. Это происходит потому, что обратная транскриптаза, которая считывает РНК для синтеза ДНК, «намеренно» делает ошибки. На десять вирусных частиц происходит три ошибки. Много это или мало? Для сравнения, в ясную ночь человеческий глаз различает в Млечном Пути 10 4 звезд, остальные воспринимаются как звездный туман. В хороший телескоп можно различить 10 11 звезд. И вот столько вирусных частиц образуется в организме за день! Посчитайте сами, у скольких из них ошибки — мутации. В результате 99% вирусов, образовавшихся в организме, уже ничего заразить не могут, поскольку их важнейшие белки испорчены мутациями. Зато некоторые вирусы благодаря мутациям приобрели независимость от лекарств (резистентность). Наш иммунитет тоже не поспевает за быстро изменяющимся вирусом потому, что для выработки полного иммунного ответа требуется время, за которое вирус успевает «убежать» далеко вперед. Мы надеемся, что окажемся расторопнее природы и создадим препараты, эффективные против ВИЧ и сопутствующих инфекций, к которым ВИЧ не сможет приобрести устойчивости. Но для этого нужно еще много узнать про биологию ВИЧ.
22212 04 Сентября
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
ВИЧ: причины появления, симптомы, диагностика и способы лечения.
Определение
ВИЧ (вирус иммунодефицита человека) – инфекционное хроническое заболевание, передающееся контактным путем, медленно прогрессирующее и характеризующееся поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИДа). СПИД – это финальная стадия ВИЧ-инфекции, когда из-за ослабленной иммунной системы человек становится беззащитным перед любыми инфекциями и некоторыми видами рака. Опасность представляют так называемые оппортунистические инфекции – заболевания, вызываемые условно-патогенной или непатогенной флорой: вирусами, бактериями, грибами, которые у здоровых людей не приводят к серьезным последствиям или протекают легко и излечиваются самостоятельно. При СПИДе они наслаиваются друг на друга, имеют затяжное течение, плохо поддаются терапии и могут стать причиной летального исхода.
Причины появления ВИЧ
Источником инфекции является человек, инфицированный ВИЧ, на любых стадиях заболевания. Вирус передается через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь (незащищенный секс с инфицированным партнером) – доминирующий фактор распространения ВИЧ-инфекции.
Передача ВИЧ от матери ребенку может произойти на любом сроке беременности (через плаценту), во время родов (при прохождении через родовые пути) и грудного вскармливания (при наличии язвочек, трещин на сосках матери и во рту ребенка).
Высокий риск инфицирования существует при внутривенном введении наркотических веществ нестерильными шприцами, при переливании ВИЧ-инфицированной крови и ее препаратов, использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, опасность могут представлять органы и ткани доноров, используемые для трансплантации.

Попадая в кровоток, вирус проникает в Т-лимфоциты хелперы, или CD-4 клетки (рановидность лейкоцитов), которые помогают организму бороться с инфекциями. Т-хелперы имеют на поверхности так называемые CD4-рецепторы. ВИЧ связывается с этими рецепторами, проникает в клетку, размножается в ней и в конечном счете уничтожает ее. Со временем вирусная нагрузка увеличивается, а количество Т-хелперов снижается.
При отсутствии лечения через несколько лет из-за значительного снижения числа Т-хелперов появляются связанные со СПИДом состояния и симптомы.
Классификация заболевания
- Стадия инкубации - от момента заражения до появления реакции организма в виде клинических проявлений острой инфекции и/или выработки антител (специфических белков, продуцируемых в ответ на проникновение антигена, в данном случае – вируса).
- Стадия первичных проявлений клинических симптомов:
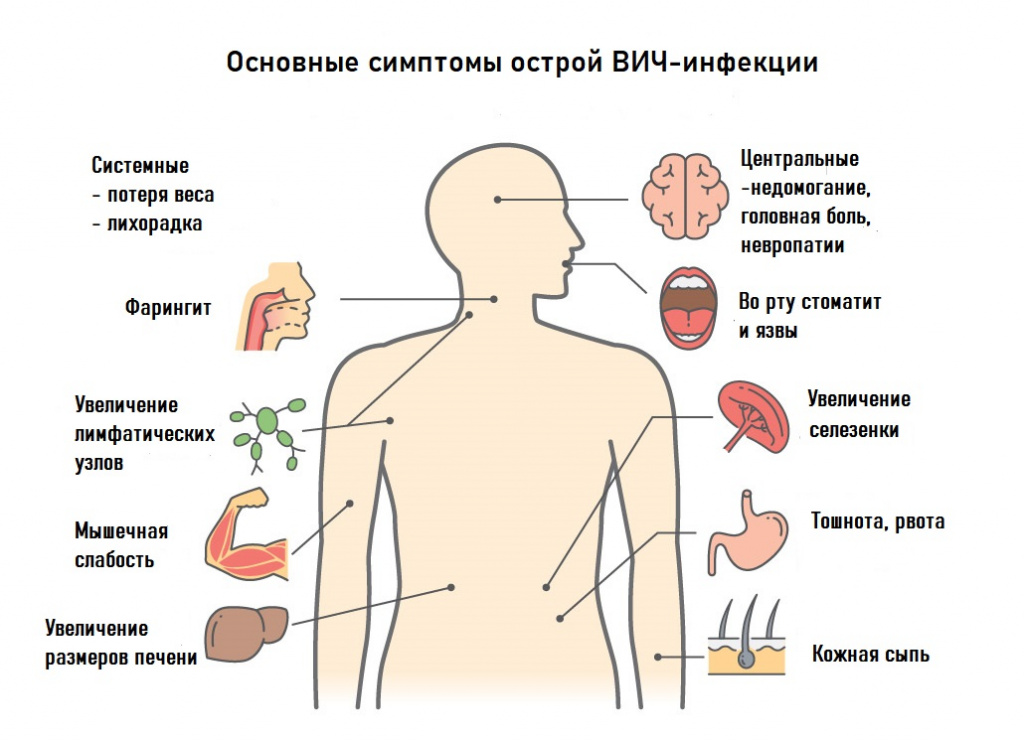
После инкубационного периода продолжительностью от нескольких дней до нескольких недель у большинства зараженных возникает острое заболевание с гриппоподобными симптомами (повышение температуры тела, ломота, общая слабость, отсутствие аппетита, головная боль, боль в горле, увеличение лимфатических узлов, кожные высыпания). Возможны похудание, образование язвочек на слизистой полости рта. Эта фаза продолжается, как правило, 7-10 дней. Из-за неспецифичности проявлений диагноз «ВИЧ» устанавливается редко. Редко на этой стадии заболевания фиксируются оппортунистические инфекции,. отмечается кашель с мокротой, боль в грудной клетке (при развитии пневмонии), болезненные пузырьковые высыпания на коже (при опоясывающем герпесе). Как правило, самочувствие быстро нормализуется без специфического лечения ВИЧ.
После этой стадии устанавливается временное равновесие между инфекционным процессом и сдерживающим его развитие противовирусным иммунитетом.
В дальнейшем продолжается активное размножение вируса и разрушение Т-лимфоцитов, развивается стадия вторичных изменений, для которой характерно прогрессирующее снижение веса, общая слабость, стойкое повышение температуры, озноб, выраженная потливость. Клинические проявления оппортунистических заболеваний обусловливают клиническую картину этой стадии: пациентов беспокоят кашель и одышка, тошнота, рвота, боли в животе, тяжелая диарея, кожные высыпания, сильные головные боли, снижение памяти и внимания и др.
Диагностика ВИЧ
Лабораторные методы исследования:
- Скрининг на ВИЧ.
- Обследование, подтверждающее факт инфицирования ВИЧ (при положительных или сомнительных результатах скрининга).
- Измерение и контроль количества вируса в крови человека - определение вирусной нагрузки у лиц с установленным диагнозом «ВИЧ».
- Определение иммунного статуса у пациентов с ВИЧ-инфекцией.
Скрининг (обследование здоровых людей) на ВИЧ должен быть проведен любому человеку, который считает, что может быть заражен, а также перед любой госпитализацией и операцией, всем беременным женщинам и их половым партнерам.
Обследование целесообразно проходить людям с высоким риском заражения ВИЧ, например, при наличии заболеваний, имеющих одинаковый с ВИЧ-инфекцией механизм передачи (вирусные гепатиты В и С, заболевания, передающиеся половым путем), лицам, имеющим регулярные незащищенные половые контакты, инъекционным наркоманам, детям, рожденным от матерей с ВИЧ-инфекцией, медицинским работникам, напрямую контактирующим с кровью на работе и др.
Существуют экспресс-тесты для скрининга ВИЧ, которые можно делать в домашних условиях. Для определения специфических антител/антигенов к ВИЧ (ВИЧ-1, 2, антиген p24) используют кровь, слюну или мочу. Точность любого экспресс-теста ниже, чем теста, проводимого в лаборатории.
Для стандартного скринингового обследования определяют антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) в крови с помощью иммуноферментного анализа (ИФА).
Внимание! При положительных и сомнительных реакциях срок выдачи результата может быть увеличен до 10 рабочих дней. Синонимы: Анализ крови на антитела к ВИЧ1 и 2 и антиген ВИЧ1 и 2; ВИЧ-1 p24; ВИЧ-1-антиген, p24-антиген; ВИЧ 1 и 2 антитела и антиген p24/25, ВИЧ тест-системы 4-го .
Читайте также:

