Сколько сеансов лучевой терапии при раке губы
Обновлено: 25.04.2024
Лучевая терапия — это один из ведущих методов противоопухолевого лечения, основанный на использовании ионизирующего излучения. Может применяться как самостоятельный вид терапии, так и в рамках комбинированного/комплексного лечения (совместно с другими методами), в качестве радикальной, нео- и адъювантной, консолидирующей, профилактической и паллиативной терапии.
Эффективность данного метода основана на повреждении ДНК. Существуют различные механизмы, позволяющие более эффективно разрушать опухолевые клетки в сравнении с нормальными. Во-первых, опухолевые клетки более активно делятся, соответственно, их ДНК чаще находится в «рабочем» режиме, когда она менее устойчива к воздействию ионизирующего излучения. По той же причине большая часть острых лучевых реакций представлена мукозитами, то есть воспалением слизистых, которым также свойственно активное деление. Во-вторых, окружающие здоровые клетки способствуют восстановлению поврежденных, подвергшихся лучевому воздействию. Поэтому важно сделать так, чтобы в объём облучения попало как можно меньше здоровой ткани. В-третьих, современное оборудование для лучевой терапии, управляемое командой грамотных специалистов, позволяет подвести максимально высокие дозы прямо в мишень, существенно снижая дозу ионизирующего излучения, приходящуюся к окружающим здоровым органам и тканям.

Виды лучевой терапии
Уже несколько десятилетий человечество изучает воздействие ионизирующего излучение на организм человека. При этом акцентируется внимание как на положительном, так и отрицательном эффекте, возникающем при его применении. Разрабатываются новые методы, которые позволяют добиваться максимального лечебного эффекта при снижении отрицательного действия на организм. Улучшается оборудование для проведения лучевой терапии, появляются новые технологии облучения.
Сейчас классификация методов лучевой терапии довольно обширна. Мы остановимся только на самых распространенных методиках.
Контактная лучевая терапия
При контактной лучевой терапии источник излучения вводится непосредственно в опухоль или прилегает к ее поверхности. Это позволяет прицельно облучать новообразование с минимумом воздействия на окружающие его ткани.
К контактным видам лучевой терапии относятся:
- Аппликационная лучевая терапия. Применяется при лечении поверхностно расположенных опухолей, например, новообразований кожи, слизистых оболочек гениталий. В этом случае используются индивидуально изготовленные аппликаторы, которые накладываются непосредственно на поверхность новообразования.
- Внутриполостная лучевая терапия. Источник ионизирующего излучения вводится в просвет полого органа, например, в пищевод, мочевой пузырь, прямую кишку, полость матки или влагалища. Для облучения используются специальные аппликаторы (их называют эндостатами), которые заполняются радионуклидами.
- Внутритканевое облучение. Источник ионизирующего излучения вводится непосредственно в ткань опухоли. Для этого используются интростаты, которые могут иметь вид игл, шариков, трубочек, заполненных источником излучения.
Кроме того, существует такой вид лечения, как радионуклидная терапия. В этом случае используются открытые источники излучения в виде растворов радионуклидов (радиофармацевтический препарат — РФП), которые при попадании в организм прицельно накапливаются в опухолевых очагах и уничтожают их. Чаще всего РФП вводится внутривенно. Наибольшее распространение получили следующие виды радионуклидной терапии:
- Терапия радиоактивным йодом. Используется для лечения ряда видов рака щитовидной железы, поскольку йод избирательно накапливается в тиреоидной ткани.
- Применение остеотропных РФП используется для лечения метастазов в костях или костных опухолей.
- Радиоиммунотерапия — радионуклиды присоединяют на моноклональные антитела, чтобы добиться прицельного воздействия на опухолевую ткань.
Дистанционная лучевая терапия
При дистанционной лучевой терапии источник излучения находится на расстоянии от тела пациента, при этом на пути его прохождения могут лежать здоровые ткани, которые в процессе проведения терапии также подвергаются облучению, что приводит к развитию осложнений разной степени выраженности. Чтобы их минимизировать, разрабатываются различные технологии, позволяющие сконцентрировать максимальную дозу ионизирующего излучения непосредственно на в мишени (опухоли). С данной целью используются:
- Короткофокусная рентгенотерапия. При облучении используется рентгеновское излучение малой и средней мощности, которое способно проникать в ткани на глубину до 12 мм. Метод назван так из-за того, что источник располагается на коротком расстоянии от облучаемой поверхности. Таким способом лечат неглубокие опухоли кожи, вульвы, конъюнктивы и век, ротовой полости.
- Гамма-терапия. Этот вид излучения имеет большую проникающую способность, поэтому может использоваться для лечения более глубоко расположенных опухолей, нежели рентген-терапия. Однако сохраняющаяся большая нагрузка на окружающие органы и ткани приводят к ограничению возможности использования данного метода в современной онкологии.
- Фотонная терапия. Именно этим видом излучения проводится лучевое лечение большинства онкологических пациентов в современном мире. Достаточно высокая проникающая способность в сочетании с высокотехнологичными способами подведения дозы (IMRT и VMAT), достаточно совершенные системы планирования позволяют очень эффективно использовать этот вид излучения для лечения пациентов с приемлемыми показателями токсичности.
- Применение корпускулярного излучения (электроны, протоны, нейтроны). Эти элементарные ядерные частицы получают на циклотронах или линейных ускорителях. Электронное излучение используют для лечения неглубоких опухолей. Большие надежды возлагаются на протонную терапию, с помощью которой можно максимально прицельно подводить высокие дозы излучения к глубоко расположенным опухолям при минимальном повреждении здоровых тканей за счет выделения радиационной дозы на определённом отрезке пробега частиц, однако пока эти виды излучения играют сравнительно небольшую роль в лечении онкологических заболевания из-за своей высокой стоимости и ряда не до конца решённых технологических аспектов реализации метода.
Этапы лучевой терапии
Весь процесс проведения лучевой терапии делят на три этапа:
- Предлучевая подготовка (КТ-симуляция), этап выбора объёмов облучения и критических структур, этап дозиметрического планирования, верификации плана лучевой терапии.
- Этап облучения.
- Постлучевой этап.
Этап планирования
Как правило, этап планирования занимает несколько дней. В это время проводятся дополнительные исследования, которые призваны дать возможность врачу более точно оценить границы опухоли, а также состояние окружающих ее тканей. Это может повлиять на выбор вида лучевой терапии, режима фракционирования, разовой и суммарной очаговых доз. Основой же данного этапа является выполнение так называемой КТ-симуляции, то есть компьютерной томографии необходимого объёма с определёнными параметрами и в определённом положении тела пациента. Во время КТ-симуляции на кожу пациента и/или его индивидуальные фиксирующие устройства наносятся специальные метки, призванные помочь правильно укладывать пациента в дальнейшем, а также облегчить задачу навигации по время проведения сеансов облучения.
Затем врач-радиотерапевт рисует объёмы облучения и критических структур (тех, на которые будет предписано ограничение дозы) на полученных срезах КТ с учётом данных других диагностических модальностей (МРТ, ПЭТ). Далее формируется задача для медицинского физика, включающая определение доз, которые должны быть подведены к мишени, мишеням или отдельным её частям, а также тех, которые не должны быть превышены в объёмах здоровых органов и тканей. Медицинский физик разрабатывает дозиметрический план в соответствии с заданными параметрами, при соблюдении которых и успешной верификации данного плана на фантоме, можно считать пациента готовым к лучевой терапии.
На этапе подготовки к лучевой терапии пациенту рекомендуется придерживаться нескольких правил:
- Отказаться от средств, раздражающих кожу.
- Если на коже в месте воздействия имеются повреждения или элементы сыпи, следует проконсультироваться с врачом.
- Если предполагается лучевая терапия в челюстно-лицевой области, требуется санация полости рта.
- Воздержаться от загара.
- Главное правило на любом этапе: обсудить все нюансы предстоящих подготовки и лечения с лечащим врачом-радиотерапевтом и строго придерживаться полученных рекомендаций!
Этап облучения
Проведение этапа облучения будет зависеть от выбранного метода лучевой терапии.
Проведение дистанционной лучевой терапии
Продолжительность курса дистанционной лучевой терапии зависит от выбранного режима фракционирования, а также цели лечения. Паллиативные курсы, как правило, короче неоадъювантных и адъювантных, а те, в свою очередь, менее продолжительны, чем радикальные. Однако подведение радикальной дозы возможно и за один-несколько сеансов в зависимости от клинической ситуации. В таком случае курс дистанционной лучевой терапии называется стереотаксической радиотерапией или радиохирургией. Варьирует и кратность сеансов в день и в неделю: чаще всего используются схемы с пятью сеансами в неделю, однако могут быть предложены и 2-3 сеанса в день (гиперфракционирование) и схемы с 1-4 и 6 сеансами в неделю.
Во время облучения пациент в подавляющем большинстве случаев располагается лежа на столе специальной установки. Крайне необходимо соблюдать полную неподвижность во время сеанса облучения. Для достижения этого могут использоваться специальные фиксирующие устройства и системы иммобилизации.
Перед тем как включить установку, медперсонал покидает помещение, и дальнейшее наблюдение осуществляется через мониторы или окно. Общение с пациентом осуществляется по громкой связи. Во время выполнения сеанса, части аппарата и стол с пациентом совершают движения по заданной траектории. Это может создавать шум и беспокойство у больного. Однако бояться этого не стоит, поскольку вся процедура контролируется.
Сам сеанс лучевой терапии может длиться как 5-10, так и 60-120 минут, чаще — 15-30 минут. Само воздействие ионизирующего излучения не вызывает никаких физических ощущений. Однако в случае ухудшения самочувствия пациента во время сеанса (выраженной боли, судороги, приступа тошноты, паники), следует позвать медицинский персонал заранее оговоренным способом; установку сразу отключат и окажут необходимую помощь.
Контактная лучевая терапия (брахитерапия)
Брахитерапия проводится в несколько этапов:
- Введение в облучаемую зону неактивных проводников — устройств, в которые затем имплантируют источник ионизирующего излучения. При внутриполостной лучевой терапии используются приспособления, называемые эндостатами. Их устанавливают непосредственно в полость облучаемого органа и рядом с ним. При внутритканевой лучевой терапии используются интростаты, которые устанавливаются непосредственно в ткань опухоли по заранее просчитанной схеме. Для контроля их установки, как правило, используются рентгенологические снимки.
- Перемещение источника излучения из хранилища в интро- и эндостаты, которые будут облучать опухолевую ткань. Время облучения и особенности поведения пациента будут зависеть от вида брахитерапии и используемого оборудования. Например, при внутритканевой терапии, после установки источника ионизирующего излучения пациент может покинуть клинику и прийти на повторную процедуру через рекомендуемый промежуток времени. Весь этот период в его организме будет находиться интростат с радионуклидами, которые будут облучать опухоль.
Проведение внутриполостной брахитерапии будет зависеть от используемых установок, которые бывают двух типов:
- Установки низкой мощности дозы. В этом случае один сеанс облучения длится около 2-х суток. Под наркозом имплантируются эндостаты. После контроля правильности их установки и введения радионуклидов, пациент переводится в специальное помещение, где должен будет находиться все время, пока длится процедура, соблюдая строгий постельный режим. Разрешается только немного поворачиваться на бок. Вставать категорически запрещено.
- Установки высокой мощности дозы. Время облучения составляет несколько минут. Для установки эндостатов наркоза не требуется. Но во время процедуры все равно необходимо лежать абсолютно неподвижно. Внутриполостная лучевая терапия установкой высокой мощности проводится несколькими сеансами с интервалами от одного дня до одной недели.
Радионуклидная терапия
При радионуклидной терапии пациент принимает радиофармпрепараты внутрь в виде жидкого раствора, капсул или инъекций. После этого он помещается в специальную палату, имеющую изолированную канализацию и вентиляцию. По истечении определенного срока, когда мощность дозы снизится до приемлемого уровня, проводится радиологический контроль, пациент принимает душ и переодевается в чистую одежду. Для контроля результатов лечения проводится сцинтиграфия, после чего можно покинуть клинику.
Как вести себя во время лучевой терапии
Лучевая терапия является серьезным стрессом для организма. У многих пациентов в этот период ухудшается самочувствие. Чтобы его минимизировать рекомендуется придерживаться следующих правил:
- Больше отдыхать. Минимизируйте физическую и интеллектуальную нагрузку. Ложитесь спать, когда почувствуете в этом необходимость, даже если она возникла в течение дня.
- Постарайтесь сбалансировано и полноценно питаться.
- Откажитесь на время проведения терапии от вредных привычек.
- Избегайте плотной обтягивающей одежды, которая бы могла травмировать кожу.
- Следите за состоянием кожи в месте облучения. Не трите и не расчесывайте ее, используйте средства гигиены, которые вам порекомендует врач.
- Защищайте кожу от воздействия солнечных лучей — используйте одежду и головные уборы с широкими полями.

Побочные эффекты лучевой терапии
Лучевая терапия, как и другие методы противоопухолевого лечения, вызывает ряд осложнений. Они могут быть общими или местными, острыми или хроническими.
Острые (ранние) побочные эффекты развиваются во время проведения радиотерапии и в ближайшие недели после неё, а поздние (хронические) лучевые повреждения — через несколько месяцев и даже лет после ее окончания.
Общие реакции
Угнетенное эмоциональное состояние
Подавляющее большинство пациентов, проходящих лечение по поводу злокачественного новообразования, испытывают тревожность, страх, эмоциональное напряжение, тоску и даже депрессию. По мере улучшения общего состояния, эти симптомы стихают. Чтобы облегчить их, рекомендуется чаще общаться с близкими людьми, принимать участие в жизни окружающих. При необходимости рекомендуется обратиться к психологу.
Чувство усталости
Чувство усталости начинает нарастать через 2-3 недели от начала терапии. На это время рекомендуется оптимизировать свой режим дня, чтобы не подвергаться ненужным нагрузкам. В то же время нельзя полностью отстраняться от дел, чтобы не впасть в депрессию.
Изменение крови
При необходимости облучения больших зон, под воздействие радиации попадает костный мозг. Это в свою очередь приводит к снижению уровня форменных элементов крови и развитию анемии, повышению риска кровотечения и развития инфекций. Если изменения выражены сильно, может потребоваться перерыв в облучении. В ряде случаев могут назначать препараты, стимулирующие гемопоэз (кроветворение).
Снижение аппетита
Обычно лучевая терапия не приводит к развитию тошноты или рвоты, но снижение аппетита наблюдается довольно часто. Вместе с тем, для скорейшего выздоровления требуется полноценное высококалорийное питание с высоким содержанием белка.
Локальные осложнения
Побочные реакции со стороны кожи
Вероятность развития кожных реакций и их интенсивность зависят от индивидуальных особенностей пациента. В большинстве случаев через 2-3 недели в области воздействия возникает покраснение. После окончания лечения оно сменяется пигментированием, напоминающим загар. Чтобы предотвратить чрезмерные реакции, могут назначаться специальные кремы и мази, которые наносятся после окончания сеанса. Перед началом следующего их необходимо смыть теплой водой. Если реакция выражена сильно, делают перерыв в лечении.
Реакции со стороны полости рта и горла
Если облучают область головы и шеи, могут развиться лучевой стоматит, который сопровождается болью, сухостью во рту, воспалением слизистых, а также ксеростомия вследствие нарушения функции слюнных желез. В норме эти реакции проходят самостоятельно в течение месяца после окончания лучевой терапии. Ксеростомия может беспокоить пациента в течение года и более.
Осложнения со стороны молочной железы
При прохождении лучевой терапии по поводу рака молочной железы могут возникать следующие реакции и осложнения:
- Покраснение кожи груди.
- Отек груди.
- Боль.
- Изменение размера и формы железы из-за фиброза (в некоторых случаях эти изменения остаются на всю жизнь).
- Уменьшение объема движения в плечевом суставе.
- Отек руки на стороне поражения (лимфедема).
Побочное действие на органы грудной клетки
- Воспаление слизистой пищевода, которое приводит к нарушению глотания.
- Кашель.
- Образование мокроты.
- Одышка.
Последние симптомы могут свидетельствовать о развитии лучевого пневмонита, поэтому при их возникновении следует немедленно обратиться к вашему врачу.
Побочные реакции со стороны прямой кишки/петель кишечника
- Расстройство стула — диарея или наоборот, запоры.
- Боли.
- Кровянистые выделения из заднего прохода.
Побочные действия со стороны мочевого пузыря
- Учащенное болезненное мочеиспускание.
- Наличие примеси крови в моче иногда может быть настолько выраженным, что моча приобретает кроваво-красный цвет.
- Наличие патологических примесей в моче — кристаллы, хлопья, гнойное отделяемое, слизь.
- Уменьшение емкости мочевого пузыря.
- Недержание мочи.
- Развитие везиковагинальных или везикоректальных свищей.
Побочные эффекты при облучении опухолей забрюшинного пространства, печени, поджелудочной железы
- Тошнота и рвота.
- Ознобы после сеансов.
- Боли в эпигастрии.
Химиолучевая терапия
Лучевая терапия довольно редко проводится в качестве самостоятельного лечения. Чаще всего она сочетается с каким-либо другим видом лечения: хирургическим, а чаще всего — с лекарственным. Это может быть как вариант одновременной химиолучевой терапии, так и последовательной, а также варианты сочетания лучевой терапии с иммунотерапией, таргетной и гормональной терапии. Такие виды лечения могут иметь ощутимо более высокую противоопухолевую эффективность, однако необходимо тщательно оценить риски совместных побочных эффектов, поэтому принятие решения о любом объёме лечения с онкологической патологией должен принимать мультидисциплинарный онкологический консилиум.
Карцинома (рак) губы - лечение, прогноз
Почти во всех случаях это карцинома сквамозного типа, часто хорошо дифференцирована и из-за своего расположения диагносцируется довольно рано. В последние 25 лет частота заболеваемости карциномой губы резко снизилась, и сейчас в Великобритании ежегодно регистрируется менее 300 новых случаев развития этой опухоли. Более часто рак развивается на нижней, а не на верхней губе (20:1), однако опухоль верхней губы более распространена у женщин.
Опухоль сравнительно редко метастазирует в регионарные лимфатические узлы. Так, лишь у 7% больных при обследовании обнаруживаются метастазы такой локализации. После первичного лечения метастазы обнаруживаются примерно у такой же части больных. Обычно опухоль метастазирует в поднижнечелюстные или подбородочные лимфатические узлы и редко в узлы другой локализации.
Лечение рака губы
Лечение проводят хирургическим или химиотерапевтическим методом. Во многих случаях больные также вылечиваются лучевой терапией, особенно при небольших размерах опухоли (Т1). Использовалось облучение внешним фотонным или электронным пучком, а также брахитерапия с применением радиевых шаблонов или иридиевых имплантантов. Во всех случаях был получен хороший лечебный результат.
Столь же эффективен хирургический метод, хотя этого нельзя сказать о косметических последствиях операции, особенно если при этом была затронута значительная часть губы. В случаях опухоли больших размеров (Т2) обычно наилучшим методом лечения признается лучевая терапия. Она дает хорошие косметические и функциональные результаты, поскольку после хирургической операции у больных часто плохо закрывается рот и возникают речевые затруднения.
В случаях более распространенного процесса (ТЗ, Т4 в настоящее время встречается редко) при любом методе лечения трудно получить приемлемый косметический и функциональный результат, и повышается вероятность локального рецидивирования. Лучевая терапия в высоких дозах может дать хороший результат, однако нередко больным необходима восстановительная хирургическая операция.

Хотя губа является одним из классических объектов для брахитерапии, чаще используется облучение внешним электронным пучком или фотонами невысокой энергии. Так же как при лечении кожных раков, в данном случае для формирования поля любого размера и формы можно использовать индивидуальные свинцовые шаблоны.
Используются различные режимы облучения, однако наилучшие косметические результаты получены при применении следующих схем: 40 Гр в режиме 10 фракций при ежедневном облучении в течение 2 недель; 50 Гр в режиме 10 фракций в течение 4 недель; 45 Гр в режиме 10 фракций (назначаемых через день в течение 3,5 недель). В некоторых клиниках предпочитают облучать радикальной дозой 60 Гр, которая назначается в протяженном режиме 30 ежедневными фракциями в течение 6 недель.
Вероятно, последний режим лучше всего подходит для облучения большого объема ткани.
Для немногих больных с метастазами в лимфатические узлы лучше всего подходит радикальная хирургическая операция, хотя лучевая терапия тоже может дать лечебный результат. Радикальная лучевая терапия, хирургический метод или их сочетание дают прекрасные результаты, и вылечиваются практически все больные с раком губы, без признаков поражения лимфатических узлов. Даже при наличии метастазов общая 5-летняя выживаемость больных составляет 60-70%.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Целесообразно проводить лечение в специализированных клиниках, персонал которых представлен хирургами, радиологами и онкологами. Основные принципы лечения больных с опухолями полости рта различной локализации, в общем, одинаковы и рассматриваются совместно. Исключение составляет карцинома губы.
Лечение небольших доступных опухолей (Т1) полости рта
Эти опухоли успешно вылечиваются методом радикальной лучевой терапии с сохранением функции ротовой полости. Часто эффективна имплантация источников излучения, поскольку при этом возможно облучить небольшой объем ткани в высокой дозе. Эта техника неприменима для лечения новообразований на губе. В качестве источников используют радиоактивные изотопы радия, цезия, золота, тантала и иридия, обладающие одинаковой эффективностью.
Обычно этим методом пользуются для лечения новообразований языка, букальной слизистой, дна ротовой полости, неба и нижней зубной альвеолы. Для небольших опухолей (менее 1 см) можно ограничиться имплантацией источника, не прибегая к дополнительному внешнему облучению. Тем не менее большинство радиологов в случаях несколько более крупных опухолей, однако по размерам не подходящих для введения имплантанта (Т1 и небольшие Т2), предпочитают использовать наряду с имплантацией источника также внешнее облучение.
При имплантированном источнике суммарная очаговая доза 60 Гр обычно достигается через 4-7 дней. При совместном применении импланта и внешнего облучения многие радиологи рекомендуют после облучения опухоли от имплантированного источника в суммарной очаговой дозе 50 Гр (за 5-7 дней) проводить фракционированное облучение внешним пучком в течение 3 недель до достижения суммарной дозы 30 Гр. В ряде клиник небольшие опухоли на кончике языка предпочитают удалять хирургическим путем. Иногда для этой цели используется лазерный метод.
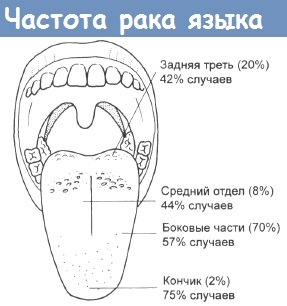
Относительная частота (в скобках) и эффективность контроля над ростом карцином языка различной локализации.
Лечение больших опухолей полости рта (Т2-Т4)
Традиционно эти опухоли лечили облучением внешним пучком, однако в последнее время все чаще используется комбинация лучевой и химиотерапии. При внешнем облучении обычно эффективной оказывается суммарная доза 60 Гр, назначаемая фракциями в течение 6 недель, причем переносимость дозы зависит от облучаемого объема ткани. Облучают с применением боковых полей без клиновидного фильтра или с применением фильтра. В поля включают место расположения первичной опухоли и ближайшую к ней группу лимфатических узлов. При раке языка, дна ротовой полости и нижней челюсти, можно избежать облучения неба с помощью роторасширителя, фиксирующего язык в нижнем положении.
Вопросы лечения метастазов в лимфатические узлы шеи остаются дискуссионными. Во многих клиниках больным с подвижными узлами рекомендуют их радикальное удаление. При профилактическом удалении лимфатических узлов без признаков патологии в значительном количестве случаев в них были обнаружены очаги микрометастазирования. Большинство радиологов предпочитают проводить профилактическое облучение шеи у больных без признаков поражения лимфатических узлов (N0).
При этом обычно используют дозу ниже радикальной (50 Гр за 5 недель или в эквиваленте), исходя из предположения о наличии скрытых поражений лимфатических узлов, и меньшей вероятности возникновения рецидивов. В большинстве клиник для контроля над состоянием шейных лимфатических узлов используют облучение внешним пучком, иногда в сочетании с хирургическим методом. Однако, независимо от метода лечения, выживаемость среди больных в стадии N2 или N3 крайне низкая,
Появление рецидива и общая выживаемость среди больных тесно связаны с размером опухоли и стадией ее развития. По данным одного из крупномасштабных исследований, кумулятивная выживаемость больных с опухолями подвижной части языка и дна ротовой полости, без признаков лимфоаденопатии, составляла 57%, в то время как у больных с пальпируемыми лимфатическими узлами она снижалась до 42% (24). Если при обследовании больного обнаружено поражение лимфатических узлов, то, несмотря на интенсивные методы, лечение первичной опухоли не приводит к благоприятному результату.
В отдельных случаях удается контролировать появление ограниченного рецидива опухоли (обычно на прежнем месте) с помощью имплантации радиоактивного источника, однако позже может потребоваться радикальное хирургическое вмешательство, поскольку эффект носит непродолжительный характер.

При появлении рецидива после первичной лучевой терапии, в клиниках Великобритании обычно используют хирургический метод. Однако все чаще в качестве первичной меры рекомендуется хирургическое вмешательство, а не лучевая терапия. Это связано с развитием в полости рта отдаленных побочных эффектов облучения. Как правило, проводится обширная резекция с последующей реконструктивной операцией.
Использование техники микрососудистой пересадки свободного кожного лоскута привело к существенному улучшению косметических результатов операции. Однако необходимость радикального удаления пораженной области часто приводит к значительному локальному повреждению ткани и к утрате ее функциональной активности. Типичная операция по поводу рецидива опухоли дна ротовой полости включает проведение гемиглоссэктомии, иссечение участка дна ротовой полости, гемимандибулоэктомию и иссечение шейных лимфатических узлов.
Затем проводится несвободная кожная пластика и/или микрососудистая пересадка свободного кожного лоскута. Такая операция проводится больным, которые часто настолько ослаблены, что перед ее выполнением им требуется гипералиментация. Чрезвычайно важную роль играет интенсивность реабилитации больных и выполнение ими упражнений, способствующих восстановлению речи. В отдельной статье на сайте подробно рассматриваются вопросы, связанные с реабилитацией таких больных. При сухости полости рта, которая развивается после лучевой терапии (ксеростомия), назначают перорально пилокарпин. При этом усиливается слюноотделение, что обычно сопровождается лишь незначительными побочными эффектами, такими как потливость и учащение мочеиспускания.
При первичном или вторичном лечении опухолей ротовой полости может оказаться эффективной химиотерапия. В отдельной статье на сайте обсуждаются вопросы лекарственного лечения.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Методы лечения рака полости рта и его осложнения
К трем основным методам лечения рака полости рта относятся хирургическое удаление, лучевая терапия и химиотерапия. На ранних стадиях (I—II) можно использовать лишь один метод лечения (хирургическая резекция или лучевая терапия).
При распространенных опухолях (III—IV) необходимо использовать как минимум два метода, в запущенных случаях требуются все три метода лечения. Если опухоль имеет признаки агрессивного роста (экстракапсулярное распространение, периневральная или сосудистая инвазия), то даже на ранних стадиях требуется комбинированное лечение.
Основные цели лечения: (1) излечить рак; (2) сохранить или восстановить форму и функцию пораженного органа; (3) свести к минимуму возможные побочные эффекты от лечения.
При планировании лечения также необходимо оценить положение опухоли в переднезаднем направлении, ее близость к костям, глубину инвазии, гистологический тип. Небольшие опухоли, располагающиеся в передних отделах полости рта, могут быть удалены внутриротовым доступом, какие-либо функциональные нарушения минимальны.
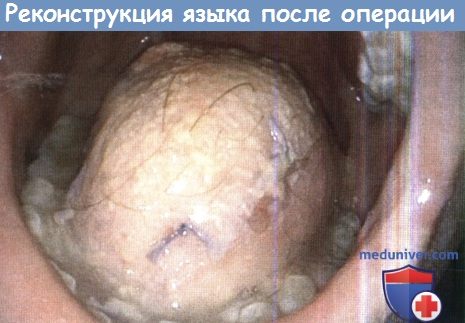
Реконструкция ротовой части языка при помощи свободного латерального лоскута бедра после практически тотальной глоссэктомии.
Пациент может есть и разборчиво говорить.
При опухолях ранних стадий предпочтительным методом лечения является хирургический, поскольку лучевая терапия сопровождается значительным риском развития ксеростомии, кариеса зубов, остеорадионекроза. Опухоли языка и дна полости рта со значительной инвазией в подлежащие ткани достаточно часто метастазируют в лимфатические узлы, поэтому если принято решение об их хирургическом удалении, даже при клинической N0 стадии поражения лимфоузлов необходимо выполнять селективную шейную лимфодиссекцию.
У пациентов с клиническими признаками поражения лимфоузлов при пальпации рекомендуется выполнять шейную лимфодиссекцию уровней I-V.
При больших опухолях рекомендуемым методом лечения является их хирургическое удаление с реконструкцией и последующей лучевой или химиолучевой терапией. Метод хирургического удаления зависит от локализации очага. К возможным доступам относятся мандибулотомия, верхний щечный лоскут, нижний щечный лоскут, visor flap.
В зависимости от степени поражения костной ткани или близости к ней может планироваться выполнение вертикальной, горизонтальной, либо сегментарной резекции нижней челюсти. Наиболее часто для восстановления формы и функции полости рта используют свободный малоберцовый лоскут, радиальный лоскут предплечья, антеро-латеральный лоскут бедра.
В некоторых случаях могут использоваться лоскуты на ножке, например, мышечно-кожный лоскут большой грудной мышцы или местные ротационные лоскуты, но их использование не является оптимальным.
Пациенты с тяжелыми сопутствующими заболеваниями могут не перенести длительных операций по пересадке свободных лоскутов с наложением микроваскулярных анастамозов, поэтому у них должны использоваться другие методы реконструкции, подразумевающие менее короткие сроки операции.
При дефектах, требующих реконструкции для предотвращения функциональных нарушений (например, при фиксации языка), но недостаточно больших для свободного лоскута с микрососудистым анастомозом приемлемы местные тканевые лоскуты и/или кожные трансплантаты.
К возможным осложнениям операции относятся кровотечение, аспирационная пневмония, формирование фистул. Возможные поздние осложнения: низкая разборчивость речи, нарушения жевания и глотания.
Ранними побочными эффектами лучевой терапии являются мукозит и нарушения вкуса, а поздними — перманентная ксеростомия, кариес зубов, остеорадионекроз. Химиотерапия может осложняться подавлением функции костного мозга, тошнотой и рвотой, аллопецией, мукозитом, нарушением функции легких, печени, почек, нейропатией, включая ото- и вестибулотоксичность вследствие поражения VIII пары черепных нервов.
Прогноз рака полости рта
Прогноз в первую очередь зависит от того, на какой стадии было выявлено заболевание. Общая пятилетняя выживаемость при заболевании I и II стадии составляет 80% и 70% соответственно; на III и IV стадиях выживаемость составляет 55% и 30%.
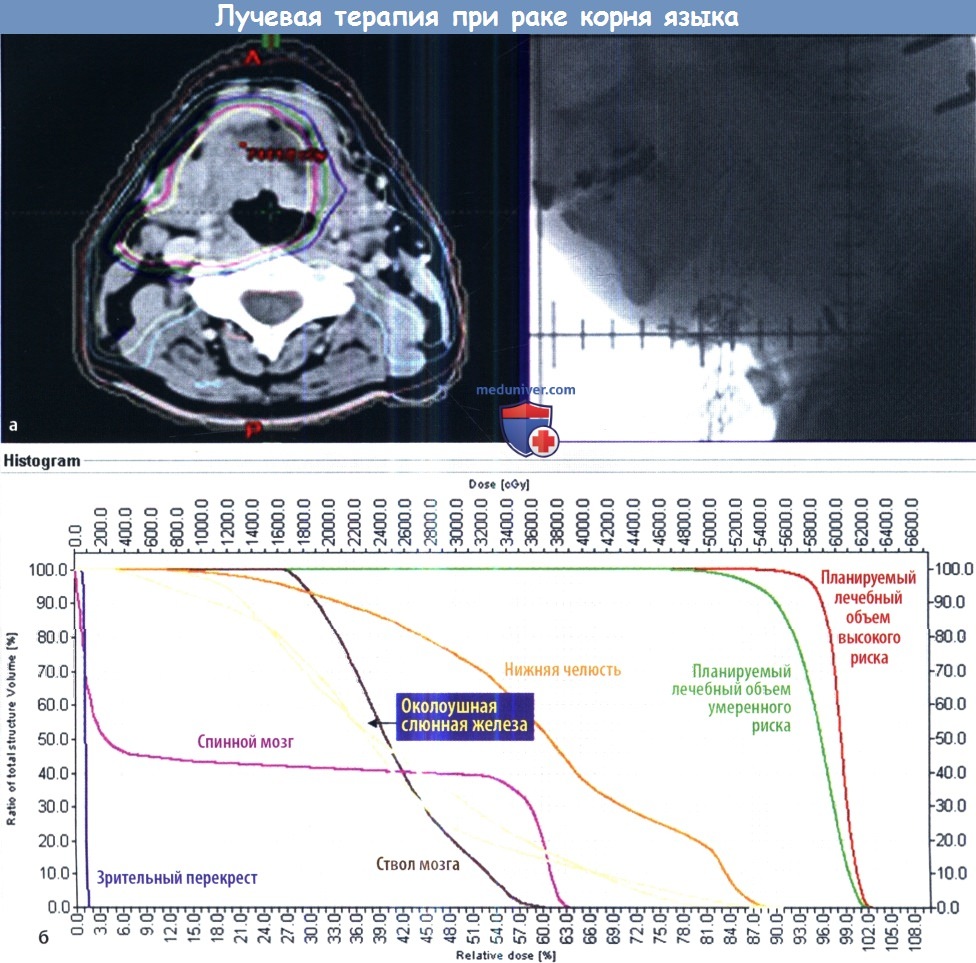
(а) Мужчина 62 лет болен раком корня языка стадии T2N2bM0. Проводилась наружная дистанционная лучевая терапия в сочетании с химиотерапией, брахитерапия и лимфодиссекция.
Облучение очага и первичных лимфоузлов проводилось в пониженной дозе в 5940 сГр, после чего проводился сеанс брахитерапии в дозе 20 Гр.
(б) Гистограмма доза-объем, демонстрирующая распределение дозы облучения в курсе лучевой терапии с модулированной интенсивностью.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Человека, у которого диагностировано онкологическое заболевание, всегда волнует, как теперь изменится его жизнь. Помимо предстоящего лечения, возникают некоторые ограничения, противопоказания.
Не стоит бояться, что теперь вся жизнь будет состоять из сплошных запретов. В целом во время лечения и после наступления ремиссии можно вести привычную жизнь, заниматься любимыми делами, принимать пищу, которая нравится. Но важно соблюдать некоторые рекомендации, потому что от этого может зависеть успех в борьбе с заболеванием.

Какие продукты питания противопоказаны при онкологических заболеваниях?
Принципы здорового питания едины для здоровых людей и онкологических больных. К продуктам, способствующим развитию рака и в целом ухудшающим состояние здоровья, относят красное (баранина, свинина, говядина) и обработанное (соленое, копченое, гриль, барбекю, бекон) мясо, колбасы и сосиски, фастфуд, продукты с добавленными сахарами, в первую очередь кондитерские изделия и сладкую газировку.
Это не означает, что одна плитка шоколада или один бургер сразу же ухудшат состояние онкологического больного. Речь о регулярном употреблении. Важно, какую часть рациона составляют те или иные продукты. Всё «вредное», конечно, надо ограничить. Но иногда можно себя побаловать.
Некоторые химиопрепараты вызывают тошноту, запоры, потерю аппетита, приводят к изменению чувства вкуса, поражению слизистых оболочек. В таких случаях нужна специальная диета. Соответствующие рекомендации вы найдете в нашей статье «Побочные эффекты химиотерапии».
Еще один возможный побочный эффект химиопрепаратов — лейкопения, снижение уровня лейкоцитов в крови. Из-за этого ослабляется иммунная защита и возрастает риск развития инфекций, в том числе пищевых. Для пациента с лейкопенией запрещены следующие продукты:
- Недоваренное мясо. Стоит приобрести специальный пищевой термометр, чтобы проверять готовность продуктов.
- Сыровяленые и сырокопченые колбасы, мясо.
- Непастеризованное молоко и любые приготовленные из него продукты (сыры, йогурты).
- Суши из сырой рыбы.
- Немытые свежие овощи и фрукты.
- Яйца, вареные всмятку, продукты, приготовленные из сырых яиц (например, домашний майонез).
Рекомендуемые продукты питания при раке
Организм онкологического больного борется с опасным заболеванием, испытывает дополнительную нагрузку из-за лечения. Чтобы вовремя восстанавливать ресурсы, ему нужно достаточное количество белков и других нутриентов, калорий. При этом пища должна быть здоровой.
К продуктам с наиболее высоким содержанием белка и калорий относятся: фасоль, курятина, мясо, йогурты, рыба, яйца. Они особенно важны для онкологических пациентов, которые сильно потеряли в весе, страдают анорексией.
Некоторые больные, напротив, страдают избыточным весом, ожирением. Им рекомендуется есть больше овощей и фруктов, выбирать нежирное мясо, максимально ограничить продукты с высоким содержанием жиров (масло, майонез, десерты, жареное), соль.
Для каждого пациента в онкологии диету подбирают индивидуально. Важно учитывать не только потребности организма, но и личные предпочтения человека — пища должна быть вкусной. В «Евроонко» есть собственный ресторан, в нем работают профессиональные повара.
Сколько воды можно пить онкологическому больному?
У многих онкобольных повышен риск обезвоживания из-за рвоты, диареи, лихорадки, некоторых лекарственных препаратов, которые используются при лечении рака. Для профилактики этого состояния рекомендуется ежедневно выпивать 2¬—2,5 литра воды (проконсультируйтесь с врачом — потребности в жидкости индивидуальны и зависят от ряда факторов).
Лучше пить обычную воду. Для придания вкуса в нее можно положить дольку лимона. Можно пить травяные чаи. Чая и кофе следует избегать: в них содержится кофеин, который действует как мочегонное. В газировках и магазинных соках содержатся добавленные сахара — они вредны для здоровья.
При некоторых состояниях в онкологии потребление жидкости, напротив, рекомендуется ограничить. Такие пациенты получают соответствующие рекомендации от лечащего врача.
Витамины и рак
Витамины важны для организма человека, но их не стоит переоценивать. Тут не работает правило «больше — лучше». Витамины не лечат от рака, некоторые из них, напротив, способствуют прогрессированию опухоли и ухудшают течение заболевания. Вы можете узнать об этом подробнее из нашей статьи «Витамины и рак».
Курение
О том, что курение вредит здоровью и приводит к онкологическим заболеваниям, наверное, знают все еще со школьной скамьи. Но курильщиков это не останавливает: среди тех, у кого уже диагностирован рак, более половины не расстаются с вредной привычкой. Обычно это аргументируют тем, что всё самое страшное уже произошло, и бросать курить нет смысла.
На самом деле, смысл есть. Позаботиться о своем здоровье никогда не поздно. Например, одно исследование показало, что больные раком легкого, которые бросили курить сразу после того, как им был установлен диагноз, или незадолго до этого, в среднем живут дольше. После отказа от сигарет противоопухолевые препараты начинают работать эффективнее, снижается риск побочных эффектов, рецидива, сокращается восстановительный период после лечения, в целом улучшается самочувствие и появляется больше энергии. Мы подробно рассказывали об этом в статье «Если уже рак: курить или не курить?».
Посещение бань и саун
В прошлом веке в онкологии существовал строгий запрет на посещение бань и саун для больных и людей, которые находятся в ремиссии. Считалось, что высокая температура провоцирует развитие рака и способствует распространению злокачественных клеток в организме. В настоящее время известно, что всё не так однозначно. Температура выше 40 градусов повышает чувствительность опухолей к препаратам и помогает их уничтожать. Этот принцип даже используют в современных клиниках онкологии — например, во время гипертермической интраперитонеальной химиотерапии (HIPEC).
Конечно же, тут нет никакого призыва лечить рак с помощью бани, как предлагают некоторые народные целители. Онкологические больные должны лечиться в специализированных клиниках онкологии, в соответствии с актуальными протоколами. А после завершения лечения никто не запрещает посещать бани, сауны и спа.
Некоторые люди боятся, что высокие температуры в бане и сауне могут вызвать рак кожи. Этому нет никаких доказательств. Для кожи опасны только солярии, в которых есть ультрафиолетовые лучи. Высокие температуры повышают риск развития злокачественных опухолей кожи, только если они вызывают сильные ожоги.
Солнечный загар
Ультрафиолетовое излучение повреждает ДНК и может привести к злокачественному перерождению клеток. Это один из самых значимых факторов риска развития рака кожи и меланомы. Чрезмерного воздействия ультрафиолетовых лучей нужно избегать даже здоровым людям, а для онкологических больных они особенно опасны, потому что многие химиопрепараты и лучевая терапия повышают чувствительность кожи.
Во время лечения важно соблюдать эти рекомендации:
- Старайтесь не бывать на улице в пик солнечной активности (между 10.00 и 16.00).
- Максимально закрывайте тело одеждой. Но помните, что перегревание и дегидратация опасны для онкологических больных. Выбирайте «дышащие» ткани: льняные, бамбуковые, хлопчатобумажные.
- Надевайте шляпу с широкими полями. Это особенно важно, если в результате химиотерапии выпали волосы.
- Старайтесь находиться в тени.
- Не сидите подолгу возле водоемов. Вода отражает солнечные лучи.
- Когда собираетесь на улицу в жаркую погоду, возьмите бутылку с водой.
- Используйте солнцезащитный крем.
Читайте подробнее о влиянии ультрафиолетового излучения на кожу в нашей статье «Загар — прямая причина рака кожи».
Употребление алкоголя при онкологических заболеваниях
Алкоголь — один из факторов риска развития многих онкологических заболеваний. Но строгого запрета на его употребление для больных в современной онкологии нет.
Важно помнить о двух моментах:
- Риски зависят от объема и регулярности употребления алкогольных напитков. Существуют максимальные безопасные дозы: для мужчин 28 граммов этилового спирта в день (700 мл пива, 300 мл вина или 90 мл водки), для женщин вдвое меньше. Конечно же, это не повод каждый день выпивать всю «норму», особенно если у человека онкологическое заболевание. Но от одного бокала вина не случится ничего страшного.
- Многие химиопрепараты выводятся из организма через печень. Она же утилизирует алкоголь. Таким образом, при употреблении спиртного орган испытывает двойную нагрузку. Некоторые противоопухолевые препараты поражают слизистые оболочки. Поэтому, если человек, страдающий раком, хочет принять алкоголь, предварительно нужно посоветоваться с лечащим врачом.
Читайте подробности в статье «Алкоголь при онкологических заболеваниях» на канале «Евроонко» в Яндекс Дзен.
Можно ли делать онкологическим больным массаж?
Онкологическое заболевание не является абсолютным противопоказанием к лечебному массажу. Он не способствует распространению раковых клеток в организме, этому нет никаких научных доказательств. В целом онкологические больные могут посещать массажистов, существуют лишь некоторые небольшие ограничения:
- Предварительно нужно проконсультироваться с лечащим врачом.
- При онкологических заболеваниях противопоказан глубокий массаж.
- Не стоит посещать сомнительные массажные салоны: пользуйтесь услугами сертифицированных массажистов.
- При проведении массажа нужно учитывать общее ослабленное состояние организма пациента, влияние химиотерапии и лучевой терапии, а также все осложнения и сопутствующие патологии.
- Массаж нельзя делать на частях тела, на которых проводится лучевая терапия, если на коже имеются раны и другие повреждения.
- На конечностях с лимфедемой (отеком в результате нарушения оттока лимфы после удаления лимфатических узлов) нельзя делать классический массаж, но можно специальный лимфодренажный для уменьшения отека.
Почему нельзя заниматься самолечением при раке?
Читайте также:

