Прыщи при синдроме жильбера
Обновлено: 26.04.2024
Институт дерматологии и косметологии, Москва
Институт повышения квалификации ФМБА России, Москва
ИПК ФМБА России;
КВД №9 Москвы
Системные ретиноиды в терапии тяжелых и резистентных форм акне
Журнал: Клиническая дерматология и венерология. 2013;11(3): 60‑62
Сафонова Т.Г., Владимиров В.В., Сирмайс Н.С. Системные ретиноиды в терапии тяжелых и резистентных форм акне. Клиническая дерматология и венерология. 2013;11(3):60‑62.
Safonova TG, Vladimirov VV, Sirmaĭs NS. Systemic retinoids in therapy for severe and resistant forms of acne. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):60‑62. (In Russ.).
Институт дерматологии и косметологии, Москва
Институт дерматологии и косметологии, Москва
Институт повышения квалификации ФМБА России, Москва
ИПК ФМБА России;
КВД №9 Москвы
В XXI веке угревая болезнь сохраняет свою актуальность, являясь одним из наиболее частых заболеваний, поражающих до 85% людей в возрасте 12—25 лет и 30—40% старше 25 лет. По данным многочисленных исследований [1—3], тяжелые формы заболевания встречаются в 5—14% случаев и требуют серьезного и длительного лечения.
Угревая болезнь — полиморфное мультифакторное заболевание волосяных фолликулов и сальных желез. Наиболее значимыми аспектами в патогенезе возникновения данной патологии являются:
— избыточное выделение кожного сала;
— нарушение процессов кератинизации;
— увеличение патогенности Propionibacterium acnes;
— нарушение циркуляции некоторых гормонов.
Существует корреляция между силой нарушения патологических факторов и тяжестью клинического процесса. Тактика лечения зависит от пола и возраста пациента, степени тяжести процесса, наличия сопутствующей патологии. Важный момент — психоэмоциональные расстройства разной степени выраженности. Высыпания на коже приводят к снижению самооценки и качества жизни, вызывают тревогу, депрессию, затрудняют общение с другими людьми [1, 4, 5].
Для лечения тяжелых форм акне и акне, торпидных к системным противомикробным средствам, широко применяются системные ретиноиды I поколения, такие как 13-цис-ретиноевая кислота (изотретиноин — ИТ), синтезированная в 1968 г.
Накоплен достаточно обширный опыт в применении ретиноидов в дерматологии. Так, ИТ применяют в Европе с 1971 г. В настоящее время показания к применению ИТ расширяются. Хороший клинический эффект достигнут при лечении тяжелых и атипичных форм акне, фолликулитов, вызванных грамотрицательными бактериями, псориаза, розацеа, Т-клеточных лимфом кожи, большой группы заболеваний, связанных с нарушением процессов ороговения. Кроме того, используются новые схемы лечения: низкие дозы ИТ — 0,2—0,3 мг/кг без набора стандартной кумулятивной дозы препарата [6—8].
В 2001 г. была создана новая форма ИТ — Акнекутан [*] , инновационная запатентованная технология LIDOSE — «твердый раствор», сочетающий свойства твердой оболочки препарата с характеристиками усвояемости жидкой формы.
При производстве новой формы препарата удалось добиться увеличения на 13,5% доли растворенной фракции ИТ в капсуле по сравнению с оригинальной формой препарата. В связи с этим на 20% повысилась биодоступность ИТ в Акнекутане, что привело к снижению разовой и суммарной дозы на курс терапии [2, 3].
С 2010 г. данный препарат поставляется на российский рынок компанией «Ядран» (Галенский Лабораторий, Хорватия) [3, 9].
Цель данного исследования — оценить эффективность и переносимость лекарственного препарата Акнекутан у больных, страдающих тяжелыми формами акне и акне, резистентными к другим видам терапии.
На всех пациентов, участвующих в исследовании, заводили амбулаторные карты, в которых фиксировали каждый прием, от всех больных было получено информированное согласие. Женщины прошли тест на беременность и были предупреждены о возможном тератогенном действии препарата.

Распределение пациентов по локализации высыпаний представлено в табл. 2.

У 17 пациентов наблюдалась сопутствующая патология: дискинезия желчевыводящих путей (ДЖВП), хронический тонзиллит, синдром Жильбера, поликистоз яичников, атопический дерматит, гайморит, гастрит (табл. 3).
Пациентам проведена монотерапия лекарственным Акнекутаном, который назначался, исходя из рекомендованных суточных доз, 0,4—0,8 мг/кг.
У женщин суточные дозировки Акнекутана в основном составили 0,4—0,6 мг/кг.
Результаты терапии оценивали во время каждого визита пациента по субъективным (жалобы) и объективным показателям (динамика изменения клинической картины заболевания: подсчет элементов — комедонов, папуло-пустулезных высыпаний, узлов, интенсивности гиперпигментации и рубцовых изменений). Оценку возможных побочных эффектов на функцию печени проводили по лабораторным показателям (биохимический анализ крови — холестерин, триглицириды, аланинаминотрансфераза, аспартатаминотрансфераза, глюкоза, щелочная фосфатаза, общий билирубин, γ-глутамилтранспептидаза). У женщин обязательным был тест на беременность.
Длительность лечения в среднем составила 38 нед. У всех пациентов наблюдалась положительная динамика кожного процесса: перестали появляться папулезные, папуло-инфильтративные и пустулезные элементы, а имевшиеся высыпания претерпевали обратное развитие.
В 2 случаях отмечены незначительные изменения биохимических показателей крови. У пациента с диагнозом синдром Жильбера выявлено увеличение прямого и общего билирубина. Пациент проконсультирован в Центре молекулярной генетики, после чего продолжил прием Акнекутана в более низкой суточной дозе. У одной пациентки незначительное повышение уровня холестерина было откорректировано диетой и снижением суточной дозы Акнекутана.
Переносимость Акнекутана у всех пациентов была хорошей. Побочные эффекты (хейлит, ретиноидный дерматит) наблюдались у всех пациентов, но быстро исчезали или уменьшались при присоединении дополнительного наружного лечения или снижения дозировки Акнекутана. При опросе в конце лечения пациенты отмечали хорошую переносимость препарата, видимое улучшение состояния кожи и повышение качества жизни. Кумулятивная доза Акнекутана была достигнута у 17 человек и в среднем составила 106 мг/кг. У 5 пациентов суммарная кумулятивная доза была менее 100—120 мг/кг: у 3 из-за хорошего клинического ответа на лечение и стойкой ремиссии, у 2 из-за сопутствующих заболеваний (синдром Жильбера и атопический дерматит).
Результаты проведенного клинического исследования свидетельствуют о высокой эффективности Акнекутана (клиническая ремиссия достигнута у всех 22 пациентов). Основными особенностями терапии данным препаратом являются снижение суточной и курсовой дозировки за счет повышения биодоступности (LIDOSE) ИТ в Акнекутане, более мягкое действие Акнекутана по сравнению с оригинальной формой препарата, и соответственно уменьшение побочных действий ИТ.
Московский клинический научно-практический центр, 111123 Москва, шоссе Энтузиастов, 86
Московский клинический научно-практический центр, 111123 Москва, шоссе Энтузиастов, 86
Клиническое значение функциональных проб в диагностике синдрома Жильбера
Журнал: Лабораторная служба. 2015;4(1): 20‑25
Московский клинический научно-практический центр, 111123 Москва, шоссе Энтузиастов, 86
Распространенность генетического дефекта UGT 1А1 в популяции значительна, гомозиготное носительство определяется от 5 до 10% в разных регионах, а гетерозиготное носительство достигает 40—45%. Диагностика синдрома Жильбера требует достаточно много времени и приводит зачастую к гипердиагностике хронических гепатитов, или нередко больные остаются недообследованными. Цель исследования — разработка алгоритма диагностики синдрома Жильбера. Материал и методы. В исследование были включены 88 человек. Из них 43 (49%) больных были с болезнью Жильбера, 25 (28%) больных с хроническим гепатитом и 20 (23%) пациентов контрольной группы. Всем пациентам были проведены пробы с гипокалорийной диетой и фенобарбиталом, генетическое обследование с помощью полимеразной цепной реакции промоторной области UGT1 Promotor (ta)n. Результаты. При проведении теста с гипокалорийной диетой чувствительность и специфичность при повышении уровня билирубина более чем на 21,4 мкмоль/л составляла 73,8 и 100% соответственно. При проведении пробы с фенобарбиталом нормализация уровня билирубина отмечена у 68 (77,2%) больных, чувствительность теста составила 82,9% и специфичность — 63,3%. Последовательное применение двух функциональных тестов увеличивает чувствительность и специфичность диагностики. Изменение функциональных проб отмечено у гомозиготных и гетерозиготных пациентов. Заключение. При проведении комбинаций пробы с низкокалорийной диетой и фенобарбиталом получены достаточные по диагностическому уровню результаты.
Московский клинический научно-практический центр, 111123 Москва, шоссе Энтузиастов, 86
Московский клинический научно-практический центр, 111123 Москва, шоссе Энтузиастов, 86
Функциональные гипербилирубинемии — группа наследственных (генетически обусловленных) не гемолитических гипербилирубинемий. Заболевания обусловлены нарушением процессов метаболизма билирубина и последующего его выделения с желчью. Одним из наиболее часто встречающихся вариантов функциональных гипербилирубинемий является синдром Жильбера (СЖ). СЖ известен уже более 100 лет и имеет следующие синонимичные названия: симптом Жильбера—Лербулета, врожденная семейная холемия, простая семейная холемия, врожденная гипербилирубинемия, конституциональная гипербилирубинемия, идиопатическая неконъюгированная гипербилирубинемия.
В 1980 г. определение СЖ претерпело изменения. В настоящее время СЖ называется гетерогенное, относительно часто встречающееся состояние, которое приводит к хронической, часто семейной [9] неконъюгированной гипербилирубинемии, характеризующееся превышением нормы билирубина на 30—40% [14] вследствие наследственного дефекта промоторной области гена UGT 1А1, находящегося на 2-й паре хромосом (2q37) [18], кодирующего фермент уридиндифосфат-глюкуронилтрансферазу, который играет главную роль в метаболизме билирубина.
Распространенность генетического дефекта UGT 1А1 в популяции значительна, гомозиготное носительство определяется от 5 до 10% в разных регионах, а гетерозиготное носительство достигает 40—45%. Эти цифры показывают, что диагноз СЖ является достаточно частым.
Диагностика СЖ до сих пор остается сложной, несмотря на развитие диагностических технологий. Диагноз, как правило, ставится методом исключения, с применением пункционной биопсии печени. Все это занимает достаточно много времени и приводит зачастую к гипердиагностике хронических гепатитов, или нередко больные остаются недообследованными.
Среди больных СЖ мужчины преобладают в отношении 10:1, возраст больных 15—25 лет. Значительно более высокая численность мужчин и возраст манифестации заболевания, вероятно, связаны с ингибированием процессов глюкуронизации собственными стероидными гормонами [12].
Основным клиническим симптомом СЖ является желтуха — желтая окраска кожных покровов, склер и слизистых в результате их окрашивания билирубином при повышении его уровня в крови. Визуально желтуха определяется при повышении билирубина выше 50 мкмоль/л. Средний уровень билирубина у мужчин достоверно выше, чем у женщин [17].
У таких пациентов при обследовании в поликлинике может быть обнаружено повышение билирубина за счет непрямой фракции. При ультразвуковом исследовании (УЗИ) в 11% случаев может выявляться незначительная гепатомегалия за счет правой доли [19]. Размеры селезенки, как правило, не изменены, редко выявляется небольшая спленомегалия. При исследовании моторной функции желчного пузыря часто определяется его дисфункция.
При проведении морфологического исследования с помощью световой микроскопии патологических изменений в печени не выявляется, за исключением липофусциноза [20].
Для диагностики СЖ существует большое количество функциональных тестов (гипокалорийный, рифампициновый, с никотиновой кислотой, фенобарбиталом) [4].
Ограничение пищевого рациона до 400 ккал на срок 72 ч вызывает увеличение уровня билирубина у всех людей [2], без дефекта гена уровень билирубина редко повышается более чем на 9,6 мкмоль/л у мужчин и на 4,1 мкмоль/л у женщин [10]. Однако у больных с СЖ он более выражен [7, 11]. Гипокалорийная диета может усиливать гипербилирубинемию из-за нескольких физиологических процессов. Во-первых, вследствие увеличения продукции билирубина [1], во-вторых, в результате уменьшения внутрипеченочного клиренса билирубина [3].
В ответ на прием 600 мг рифампицина у больных СЖ уже через 4 ч уровень билирубина в сыворотке крови повышается. Однако у больных с хроническим гепатитом в половине случаев может также отмечаться повышение билирубина [6]. Кроме того, повышение уровня билирубина при проведении теста с рифампицином имеет место и у здоровых добровольцев [13].
Внутривенное введение никотиновой кислоты (50 мг) приводит к повышению уровня неконъюгированного билирубина за счет разрушения эритроцитов и увеличения образования билирубина в селезенке. Этот тест наряду с гипокалорийной диетой является диагностическим [8, 16, 21], однако он плохо переносится больными и обладает довольно низкой чувствительностью (всего 70%), в сочетании с низкой специфичностью (60%). Он позволяет проводить дифференциальный диагноз между больным СЖ и здоровым индивидом, но не больными с хроническим гепатитом [5].
Клиническое течение СЖ
Нами проанализирована клиническая и клинико-лабораторная картина у 88 больных: 43 больных с СЖ, 25 больных с хроническим гепатитом и 20 пациентов контрольной группы.
Заболевание впервые выявлялось после перенесенных острых респираторных вирусных инфекций (ОРВИ) или кишечных инфекций, после нагрузок или стрессов (41,9%), у части больных (58,1%) причину манифестации установить не удалось (рис. 1).

Рис. 1. Причины, спровоцировавшие дебют СЖ.
При поступлении больные жаловались на слабость, утомляемость, нервозность, невозможность долго заниматься (эта группа преимущественно состояла из студентов профессионально-технических училищ и различных вузов). Характеристика жалоб больных с СЖ представлена на рис. 2.

Рис. 2. Распространенность симптомов у больных с СЖ.
Для подтверждения диагноза больным были проведены пробы с гипокалорийной диетой и фенобарбиталом.
Методика проводимых тестов
Тест с низкокалорийной диетой
1. Биохимический анализ крови.
2. В течение 3 дней низкокалорийная диета, не более 400 ккал/сут (4 йогурта 125 г с низкой жирностью, несладкая вода, несладкий чай, кофе без ограничения).
3. Контрольный биохимический анализ крови.
4. Тест считается положительным при повышении уровня билирубина на 21,5 мкмоль/л.
Тест с фенобарбиталом
1. После получения данных анализов уровня билирубина на фоне низкокалорийной диеты назначение фенобарбитала в дозе 0,1 г. На ночь в течение 7—10 дней.
2. Контрольный анализ крови.
3. Тест считается положительным, если уровень билирубина стал нормальным или значительно приблизился к норме.
Для оценки клинической эффективности данные тесты параллельно были проведены в контрольной группе и группе сравнения. Данные представлены на рис. 3.

Рис. 3. Показатели уровня билирубина в ответ на гипокалорийную диету и фенобарбитал.
При проведении теста с гипокалорийной диетой повышение уровня билирубина отмечено у всех пациентов. При проведении пробы с фенобарбиталом нормализация уровня билирубина отмечена у 68 (77,2%) больных, у 16 (18%) наблюдали значительное снижение билирубина, но не достигавшее нормальной величины, и у 4 билирубин оставался высоким (при условии значительного повышения на фоне гипокалорийной диеты). В группе больных с хроническим гепатитом на фоне гипокалорийной диеты отмечено незначительное падение билирубина (p>0,05) и практически отсутствие ответа на фенобарбитал. У здоровых добровольцев в ответ на голод отмечено увеличение билирубина, однако ни у кого этот показатель не превысил нормальных значений.
На основании полученных данных был проведен анализ чувствительности и специфичности пробы с гипокалорийной диетой и фенобарбиталом в зависимости от динамики биохимических показателей.
Чувствительность определяли как долю лиц с увеличением билирубина на 21,4 мкмоль/л в ответ на назначение гипокалорийной диеты. В качестве золотого стандарта принято гомозиготное носительство генетического дефекта УДФГТ. Данные представлены в табл. 1.

Таблица 1. Чувствительность теста с гипокалорийной диетой в зависимости от повышения уровня билирубина
Также рассчитывали чувствительность и специ-фичность теста с фенобарбиталом. Положительным результатом считали нормализацию показателя билирубина или снижение более чем в 3 раза от исходного при уровне билирубина выше 80 мкмоль/л при проведении предварительного гипокалорийного теста.
Как видно из данных табл. 2, у теста с фенобарбиталом достаточно высокая чувствительность (82,9%). Однако низкая специфичность теста не позволяет с высокой точностью диагностировать СЖ на основании лишь лекарственной пробы. Этот тест должен использоваться в сочетании с другими диагностическими методиками, а именно с тестом гипокалорийной диеты, генетическим типированием, морфологическим исследованием ткани печени.

Таблица 2. Чувствительность и специфичность теста с фенобарбиталом
На основании данных, полученных при расчетах чувствительности и специфичности описанных выше методик, проведена оценка чувствительности и специфичности сочетания этих двух тестов в зависимости от повышения уровня билирубина на фоне предварительно проведенной гипокалорийной диеты (табл. 3).

Таблица 3. Чувствительность и специфичность теста с фенобарбиталом в зависимости от повышения уровня билирубина на фоне гипокалорийной диеты
Из представленных данных видно, что сочетание тестов снижает чувствительность данных методик, но при повышении билирубина менее чем на 21,4 мкмоль/л значительно увеличивает специфичность. Следовательно, для постановки диагноза при первичном обследовании целесообразно проведение комбинации этих тестов последовательно, начиная с теста с гипокалорийной диетой и последующим назначением фенобарбитала с целью нормализации уровня билирубина.
Генетические исследования у пациентов с СЖ
В настоящее время во всем мире развивается ДНК-диагностика. В связи с этим диагноз наследственного заболевания без генетического обследования является неполным. При сборе анамнеза лишь у 5% пациентов отмечена у одного из родителей неконъюгированная гипербилирубинемия, около 40% родственников никогда не обследовались на предмет наличия повышения билирубина. До 12% родственников пациентов имели другие формы поражения печени (гепатиты алкогольной или вирусной этиологии, желчнокаменную болезнь и др.), оставшаяся часть пациентов затруднялась ответить на вопрос о наличии болезней у своих родителей.
Как видно из представленного выше анализа, диагностика наследственной предрасположенности к заболеванию доброкачественной гипербилирубинемией представляется затруднительной.
Генетические исследования широко используются в практической медицине, в том числе для установления множества гастроэнтерологических заболеваний, таких как гепатолентикулярная дегенерация, гемохроматоз, муковисцидоз. Появление возможности изучения генотипа значительно облегчило диагностику С.Ж. Однако данные о том, что не у всех больных с наличием мутации УДФГТ имеются клинические проявления доброкачественной гипербилирубинемии (при обследовании 300 человек в Германии выявлено 36 гомозигот, 159 гетерозигот, но только у 26 из них на момент обследования определено повышение билирубина [15]), не позволяют остановиться на этом анализе.
С целью подтверждения диагноза СЖ мы провели генетическое исследование у 43 из 88 обследованных пациентов. Получен положительный результат с помощью полимеразной цепной реакции (ПЦР) промоторной области UGT1 Promotor (ta)n. Все изменения обнаружены в промоторной области, что соответствует данным литературы о довольно редкой распространенности других видов мутаций. В связи с этим мы сочли возможным исследовать только промоторную область у оставшейся части пациентов. В результате этого у всех 43 обследованных выявлено увеличение количества повторов в области UGT1 Promotor (ta)n в гетерозиготном (n=8) или гомозиготном (n=35) состоянии.
СЖ всегда относится к аутосомно-рецессивному типу наследования. Однако в нашем исследовании доказано, что и гетерозиготные пациенты могут иметь клиническую картину этого заболевания. Хотя клинические проявления у них значительно менее выражены, чем у гомозиготных носителей, они также входят в группу риска по развитию этого заболевания.

Рис. 4. Уровень билирубина (в мкмоль/л) у больных с СЖ в зависимости от генетического статуса.
Как видно из представленного материала, в нашем распоряжении имеется огромное количество тестов и методик для диагностики С.Ж. Однако ни один из них не является универсальным. Даже генетическое исследование лишь подтверждает снижение активности фермента УДФГТ, но никак не исключает у больного наличие сопутствующих заболеваний (хронический гепатит, гемохроматоз, гепатолентикулярную дегенерацию). Вместе с тем, если при комбинации проб с низкокалорийной диетой и фенобарбиталом получено достаточное повышение уровня билирубина с последующей его нормализацией, то в генотипировании данный пациент не нуждается, что немаловажно для тех больниц и поликлиник, которые не имеют на сегодняшний день в своем распоряжении лабораторий ПЦР.
Исходя из этого, предлагаем алгоритм диагностики СЖ (рис. 5). Обследование по данному алгоритму позволяет до минимума снизить инвазивные (пункционная биопсия) исследования.

Рис. 5. Алгоритм диагностики СЖ.
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
ФГАОУ ВО «Российский университет дружбы народов»
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы, филиал «Коломенский»
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
ФГАОУ ВО «Российский университет дружбы народов»
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
Особенности применения изотретиноина в терапии акне у пациентов с синдромом Жильбера
Журнал: Клиническая дерматология и венерология. 2021;20(3): 53‑58
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
Эффективность и безопасность применения системных ретиноидов — одна из наиболее обсуждаемых проблем при выборе тактики лечения пациентов, страдающих тяжелыми формами акне. Наличие сопутствующей патологии нередко является причиной исключения изотретиноина из протоколов лечения таких пациентов.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Оценить эффективность и безопасность применения изотретиноина у пациентов, страдающих тяжелыми формами акне, с подтвержденным в раннем детском возрасте синдромом Жильбера.
МАТЕРИАЛ И МЕТОДЫ
Проведен ретроспективный анализ данных 20 пациентов с тяжелыми формами акне. Больных разделили на две группы: основную группу составили пациенты с подтвержденным синдромом Жильбера, группу сравнения — пациенты без этой патологии. Динамику кожного процесса и лабораторных показателей в сыворотке крови (общий и неконъюгированный билирубин, АЛТ, АСТ и триглицериды) оценивали до, а также после 3 мес и 6 мес терапии. Продолжительность курса лечения — 6 мес.
РЕЗУЛЬТАТЫ
Применение изотретиноина в течение 6 мес при лечении пациентов с акне и синдромом Жильбера сопровождалось двукратным снижением уровня общего билирубина в сыворотке крови и не приводило к значимому повышению уровня остальных лабораторных показателей.
ЗАКЛЮЧЕНИЕ
Полученные данные позволяют сделать вывод об относительной безопасности использования данного вида терапии у пациентов с подтвержденным синдромом Жильбера.
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
ФГАОУ ВО «Российский университет дружбы народов»
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы, филиал «Коломенский»
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
ФГАОУ ВО «Российский университет дружбы народов»
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы
ГБУЗ города Москвы «Московский научно-практический центр дерматовенерологии и косметологии ДЗМ»
Дата принятия в печать:
Акне — самое распространенное заболевание среди кожных заболеваний подросткового периода, у подростков оно встречаются в 80—90% случаев. С учетом того, что высыпания при акне локализуются преимущественно на открытых участках кожи и могут приводить к формированию стойких вторичных изменений (рубцов и гиперпигментированных пятен), у пациентов часто развиваются психоэмоциональные расстройства — смущение, стыд, депрессия, тревога, ипохондрический синдром [1, 2].
Как известно, ключевыми факторами в патогенезе акне являются: увеличение продукции кожного сала, дисбаланс липидов секрета сальных желез, фолликулярный гиперкератоз, обтурация протоков сальных желез, колонизация кожи бактериями Propionibacterium acnes и формирование воспалительных изменений в области сально-волосяных фолликулов. В последнее время появились сведения о том, что описанным событиям предшествует развитие субклинического воспаления в области сальных желез, триггерами которого могут быть микроорганизмы, липиды кожного сала, нейропептиды, высвобождаемые из нервных окончаний. Инициация воспалительного процесса с участием толл-подобных рецепторов (toll-like receptor — TLR), рецепторов, активируемых протеазами (protease-activated receptor-2 — PAR-2), а также рецепторов, активируемых пролифераторами пероксисом (peroxisome proliferator-activated receptor — PPAR), сопровождается миграцией и аккумуляцией лейкоцитов, продукцией провоспалительных цитокинов, антимикробных пептидов, нарушением кератинизации в устьях сальных желез и формированием микрокомедонов [3—5].
Наиболее эффективным методом лечения тяжелых форм акне является системное применение изотретиноина. Терапевтический эффект изотретиноина реализуется не только путем мощного угнетения функции себоцитов, уменьшения размеров сальных желез, нормализации ороговения кератиноцитов, но и благодаря выраженному противовоспалительному и иммуномодулирующему действию (уменьшению экспрессии TLR2 на макрофагах и продукции медиаторов воспаления) [6, 7].
Изотретиноин — препарат с доказанной эффективностью, применение его для лечения тяжелых форм акне утверждено Международной ассоциацией дерматологов. Для получения стойкого эффекта препарат назначают в дозе 0,5—1 мг/кг/сут длительными курсами (от 6 до 10 мес) или до достижения кумулятивной дозы 120—150 мг/кг [8].
При лечении изотретиноином примерно у 2% пациентов наблюдают ряд побочных эффектов, в том числе увеличение уровня печеночных ферментов и триглицеридов [9]. В большинстве случаев после отмены препарата уровень лабораторных показателей возвращается к исходному.
Особого внимания заслуживают вопросы, касающиеся безопасности назначения данного препарата пациентам с исходно повышенными показателями уровня билирубина, например при синдроме Жильбера.
Цель исследования — оценка влияния препарата изотретиноина (Акнекутана) на содержание биохимических показателей крови (общего и неконъюгированного билирубина, АЛТ, АСТ и триглицеридов) у пациентов, страдающих тяжелыми формами акне и синдромом Жильбера — с исходно повышенным уровнем общего билирубина.
Материал и методы
Проведен ретроспективный анализ данных 20 пациентов, страдающих тяжелыми формами акне и получавших терапию системным изотретиноином (Акнекутаном*). В исследование вошли пациенты обоих полов в возрасте от 15 до 17 лет включительно (средний возраст 16±0,63 года). Пациентов разделили на 2 группы, сопоставимые по возрасту. Основную группу составили 10 пациентов с подтвержденным в раннем детском возрасте синдромом Жильбера и повышенным уровнем общего билирубина в крови, группу сравнения — 10 пациентов без этой патологии и с нормальными исходными биохимическими показателями крови (общий и неконъюгированный билирубин, АЛТ, АСТ и триглицериды).
Пациенты обеих групп получали по поводу акне изотретиноин (Акнекутан) в стандартной дозе из расчета 0,5 мг/кг/сут в течение 6 мес. До лечения все пациенты подписали добровольное информированное согласие на проведение терапии данным препаратом. В рамках исследования предполагались ежемесячные визиты к врачу-дерматовенерологу с целью оценки клинической эффективности проводимой терапии и коррекции дозы изотретиноина. Оценку кожного процесса осуществляли путем подсчета количества элементов сыпи и определения дерматологического индекса акне (ДИА). До лечения, а также через 3 и 6 мес в сыворотке крови больных проводили исследование биохимических показателей (общий и неконъюгированный билирубин, АЛТ, АСТ и триглицериды).
Результаты
Продолжительность применения изотретиноина составила 25±1,24 нед. За время лечения достигнута курсовая доза препарата 100—120 мг/кг. В результате лечения изотретиноином (Акнекутаном) в течение 6 мес у всех пациентов, включенных в исследование, достигнута клиническая ремиссия (разрешение воспалительных элементов — узлов, папул, пустул, открытых и закрытых комедонов) (рис. 1, 2). Часть высыпаний трансформировалась в поствоспалительные пятна, атрофические и гипертрофические рубцы. У 18 пациентов во время терапии отмечалась сухость кожи, что купировалось применением эмолентов (крема Перфектоин).

Рис. 1. Пациент Е., 2004 года рождения.
а — до начала терапии; б — после окончания терапии изотретиноином Lidose в суточной дозировке 0,5 мг/кг достигнута курсовая доза препарата, равная 112 мг/кг.

Рис. 2. Пациент З., 2006 года рождения.
а — до начала терапии; б — после окончания терапии изотретиноином Lidose в суточной дозировке 0,5 мг/кг достигнута курсовая доза препарата, равная 120 мг/кг.
Динамика содержания биохимических показателей крови в процессе лечения представлена в таблице. Исходный уровень общего билирубина до лечения в основной группе составил 39,22±24,99 мкмоль/л, что превышает этот показатель (9,18±2,58 мкмоль/л) в группе сравнения более чем в 2 раза (p<0,05). То же самое наблюдали и в отношении уровня прямого билирубина — 9,78±2,78 и 4,1±0,61 мкмоль/л соответственно (p<0,05).
Таблица. Динамика биохимических показателей сыворотки крови больных в процессе лечения изотретиноином
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.
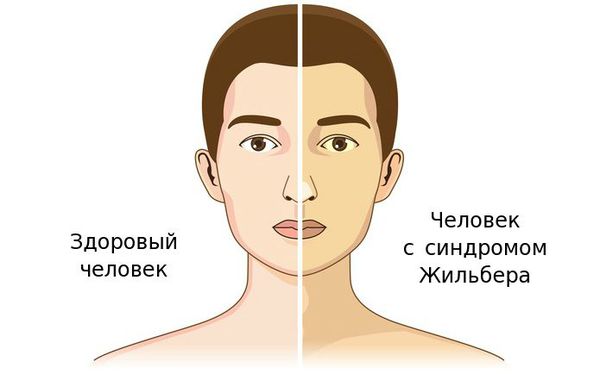
К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .
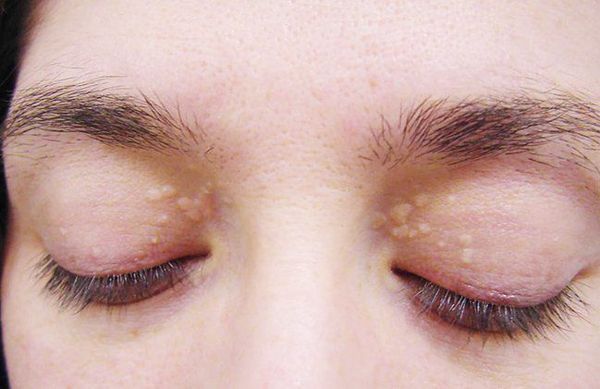
Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.
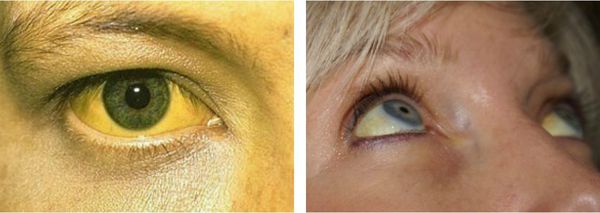
Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).
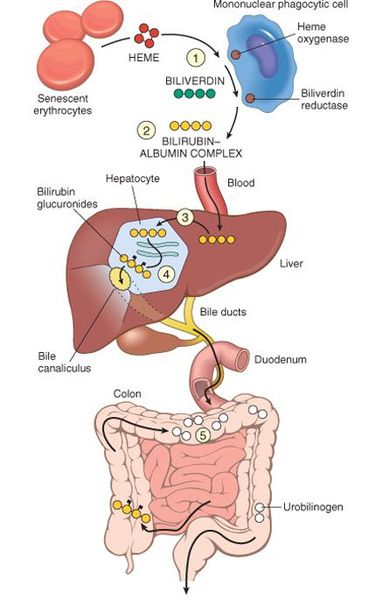
У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.
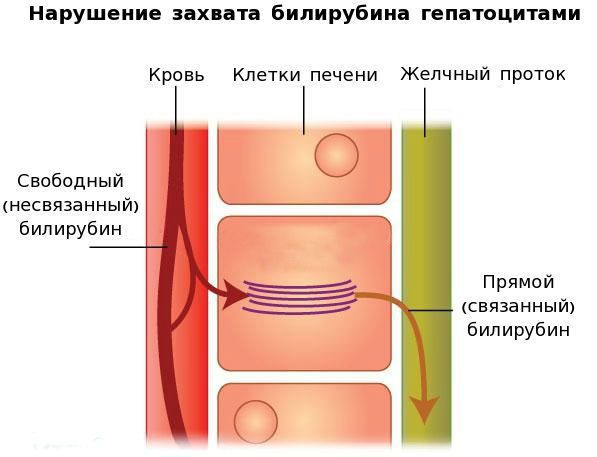
В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.

Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 28.08.2020
- Reading time: 4 минут чтения
Синдром Жильбера (семейная гипербилирубинемия) – распространенное, но легкое генетическое заболевание, при котором повышается уровень билирубина (желчного пигмента) в крови, что проявляется как желтуха. Узнайте, что вызывает синдром Жильбера и как его лечить.
Синдром Жильбера — что это и каковы причины этого состояния?
Синдром Жильбера — это легкое, безвредное генетически детерминированное заболевание, при котором наблюдается периодическое, обычно небольшое увеличение количества билирубина в крови (так называемая гипербилирубинемия). Повышение уровня билирубина может протекать бессимптомно и может быть случайно обнаружено с помощью анализов крови или может вызывать временное и легкое изменение цвета кожи и белков глаз на желтый, называемое желтухой.
Что такое билирубин
Билирубин представляет собой желчный пигмент, имеющий две формы — неконъюгированный и конъюгированный. Неконъюгированный билирубин вырабатывается в крови в основном из использованных красных кровяных телец. В печени здоровых людей неконъюгированный билирубин, образовавшийся при распаде эритроцитов, превращается ферментом UGT1A1 в конъюгированный билирубин.
Причина синдрома Жильбера — мутация в гене, отвечающем за UGT1A1, который определяет трансформацию билирубина (из неконъюгированной формы в конъюгированную).

Патогенез синдрома Жильбера
У здорового человека билирубин преобразуется и выводится из организма на постоянной основе с желчью. Напротив, у человека с синдромом Жильбера этот фермент работает менее эффективно и, следовательно, вывод отработанного вещества занимает немного больше времени. Это приводит к тому, что концентрация неконъюгированного билирубина в крови увеличивается, особенно при повышенной выработке билирубина (например, во время лихорадки), голоде, сильном стрессе, употреблении жирной пищи, некоторых лекарств и алкоголя.
Мутация гена UGT1A1, ответственного за синдром Жильбера, означает, что неконъюгированный билирубин остается в организме в большем количестве. Повышение уровня билирубина в крови может вызвать такие симптомы, как желтуха.
Тот же фермент, который метаболизирует билирубин (UGT1A1), также помогает выводить из организма некоторые лекарства, поэтому у людей с синдромом Жильбера эти препараты могут с большей вероятностью вызывать побочные эффекты. Поэтому, хотя это относится к редко используемым лекарствам, если у вас синдром Жильбера, важно сообщить об этом своему врачу.

Схема обмена билирубина
Синдром Жильбера — какова заболеваемость?
Синдром Жильбера — довольно распространенное генетическое заболевание, которым страдает 3-12% населения. В основном проблема наблюдается у мужчин. Первые симптомы заболевания чаще всего появляются у подростков.
В связи с тем, что мутация, вызывающая синдром Жильбера, передается по аутосомно-рецессивному типу, заболевание не возникает до тех пор, пока мутировавший ген не встретится у обоих родителей, и даже тогда шанс иметь больного ребенка составляет 25%. Только в случае более редкой доминантной наследственной мутации риск увеличивается до 50%.
Синдром Жильбера — как он проявляется? Симптомы гипербилирубинемии
Основной признак синдрома Жильбера — желтуха, которая характеризуется пожелтением кожи, слизистых оболочек и глаз. Это специфический симптом патологии. Легкая желтуха часто связана с накоплением билирубина в крови в определенной ситуации (например, голодание). У младенцев, находящихся на грудном вскармливании, синдром Жильбера может проявляться в виде длительной желтухи.
По крайней мере, 30% людей с синдромом Жильбера не имеют никаких специфических симптомов, но у них могут развиваться неспецифические симптомы:
Иногда накопление билирубина сопровождается симптомами, напоминающими грипп — головной болью, недомоганием, лихорадкой.
Симптомы и их тяжесть могут различаться у отдельных пациентов с этим синдромом, но чаще всего они легкие, временные и не оставляют постоянных последствий. Факторы, вызывающие желтуху, также могут быть разными, включая стресс, лихорадку, инфекцию, голодание, обезвоживание, недостаточный сон, хирургическое вмешательство, интенсивные упражнения, употребление алкоголя, половое созревание, а у женщин — перименструальный период.
Есть также пациенты, которые не испытывают никаких симптомов, связанных с синдромом Жильбера. К счастью, несмотря на временные недомогания, синдром Жильбера не вызывает серьезных проблем со здоровьем.
Синдром Жильбера – причины ухудшения симптомов
Желтуха и другие симптомы ухудшаются при повышении секреции билирубина. Основные причины:
- употребление жирных блюд;
- алкоголь;
- некоторые лекарства;
- голодная диета;
- беременность ;
- менструация;
- состояние после операции; ;
- чрезмерные нагрузки;
- повышенный стресс.


Что делать при появлении симптомов?
Симптомы синдрома Жильбера неспецифичны и могут возникать при многих других заболеваниях. Самый заметный симптом — желтуха. Если у вас развилась желтуха или какие-либо другие симптомы, предполагающие синдром Жильбера, вам следует обратиться к врачу.
Синдром Жильбера — это легкое заболевание, не имеющее каких-либо неблагоприятных последствий, но поскольку желтуха может иметь разные причины, первое, что нужно сделать, – это установить диагноз, поэтому визит к врачу необходим.
Синдром Жильбера — диагностика. Как врач ставит диагноз?
Врач сначала опрашивает пациента о времени и обстоятельствах появления симптомов, их течении во времени и возможных триггерных факторах. Затем он осматривает пациента. При необходимости он может заказать дополнительные анализы, например, лабораторные — тесты на билирубин в крови , ферменты печени, анализы крови, а также визуализационные исследования, например, УЗИ брюшной полости.

Тесты на билирубин в крови
Типичные исследования не показывают, что синдром Жильбера вызывает увеличение печени или селезенки – т.е.при осмотре эти органы будут в норме. Анализы крови на ферменты печени, такие как АЛТ и АСПАТ, также дают нормальные значения. Анализ крови может выявить только повышение билирубина.
Для синдрома Жильбера характерны колебания количества билирубина в крови, что означает, что количество билирубина иногда может быть нормальным, а иногда и повышенным. Обратите внимание, что это относится к неконъюгированному билирубину, поэтому общий билирубин также может быть повышен (общий билирубин = конъюгированный билирубин + неконъюгированный билирубин). Однако обычно концентрация неконъюгированного билирубина не превышает определенных значений — около 5 мг/дл (90 мкмоль/л).
Методы выявления аномалий билирубина — это тест на никотиновую кислоту или фенобарбитальный тест. Внутривенное введение никотиновой кислоты увеличивает уровень билирубина у пациентов, тогда как введение фенобарбитала в течение примерно недели снижает уровень свободного билирубина у людей с синдромом Жильбера.
На основе полученной информации он сможет не только распознать синдром Жильбера, но и исключить другие заболевания, например, патологии печени или тяжелые заболевания крови. Хотя описанной процедуры обычно достаточно для постановки диагноза, также возможно выполнить генетический тест, который обнаруживает мутацию в гене, кодирующем фермент UGT1A1. Это самый точный метод диагностики синдрома Жильбера. Генетический тест на синдром Жильбера проводится с использованием крови или слюны. Такой тест рекомендуется как людям с желтухой, так и тем, кто болеет в семье и хочет проверить, не является ли он носителем.
Синдром Жильбера — лечение
Синдром Жильбера — легкое, безвредное заболевание, не имеющее неблагоприятных последствий и поэтому не требующее лечения. Следовательно, нет необходимости использовать какие-либо препараты или добавки. Лишь в очень редких случаях у пациентов с крайне тяжелой желтухой применяют препараты для снижения билирубина .

Препараты для снижения билирубина
В первую очередь больным людям следует позаботиться о своем образе жизни так, чтобы не повышалось количество билирубина. Избегайте стресса и при необходимости используйте методы релаксации и легкие седативные препараты. Также важна диета: рекомендуется регулярно принимать пищу и избегать голодания. Диета должна соответствовать рекомендациям по здоровому питанию – в основном следует избегать низкокалорийных диет, а также тяжелых жирных блюд.
Возможно ли полное выздоровление?
Синдром Жильбера — наследственное генетическое заболевание, поэтому длится всю жизнь. Важно отметить, что это легкое заболевание — оно не ухудшается со временем и не несет значительного риска для пациента, не укорачивает жизнь и не повреждает печень. Прогноз для этого заболевания очень хороший, и пациенты могут вести нормальный образ жизни.
Что делать, чтобы не заболеть?
Так как это генетически детерминированное заболевание, возникновение синдрома Жильбера предотвратить невозможно.
Читайте также:

