Процесс свертывания крови при повреждении кожи
Обновлено: 01.05.2024
Гипокоагуляция – патологический процесс, характеризующийся нарушением работы свертывающей системы крови и приводящий к повышенной кровоточивости. Это одно из проявлений дисфункции гемостаза, сохраняющего жидкое состояние крови, поддерживающего структурную целостность сосудистой стенки и обеспечивающего ее быстрое тромбирование при повреждении. Гипокоагуляционный синдром встречается редко. Он бывает врожденным и приобретенным.
Кровь — биологическая среда организма, доставляющая кислород и питательные вещества к внутренним органам и тканям. У здоровых людей она находится постоянно в жидком состоянии. При повреждении кровеносных сосудов запускается процесс свертывания крови, образуется тромб, закрывающий дефект в сосудистой стенке. Пониженная способность крови к свертыванию называется гипокоагуляцией. Плохая свертываемость — причина длительных и повторных кровотечений, сильных кровоизлияний и большой кровопотери, которые могут образовываться самопроизвольно или из-за незначительной травмы. Эти явления чреваты проблемами со здоровьем. Поэтому важно своевременно выяснять их причины и принимать соответствующие меры. Даже самые простые хирургические манипуляции могут быть очень опасными для больного человека.
Гипокоагуляция не является самостоятельной нозологией. Это проявление целого ряда тяжелых заболеваний, а также одна из стадий жизненно опасного нарушения гемостаза — ДВС-синдрома. Развитию гипокоагуляции подвержены лица любого пола, возраста и происхождения. Нарушение свертываемости крови у женщин отмечается чаще, чем у мужчин. Это связано с особенностями физиологии женского организма и гормональными процессами, происходящими в нем. Причинами гипокоагуляции являются внутренние заболевания и внешние воздействия. У больных на коже появляются геморрагии, начинают кровоточить слизистые оболочки, возникают внутренние кровотечения. Симптоматика аномалии определяется местом локализации имеющегося сосудистого дефекта.

Этиология
Врожденный синдром гипокоагуляции — основа гемофилии, болезни Виллебранда и прочих патологий, передающихся по наследству и обусловленных отсутствием или дефицитом факторов свертывания крови.
Приобретенная гипокоагуляция может возникнуть в двух случаях:
- При повышении активности или концентрации антикоагулянтов,
- При недостаточной активности или дефиците прокоагулянтов.
Нехватка активных форм прокоагулянтов обусловлена снижением количества или изменением качества тромбоцитов. Тромбоцитопатии в отличии от тромбоцитопений характеризуются деструкцией и дисфункцией клеток, нарушением в них биохимических процессов. Пониженная свертываемость крови — результат недостаточного синтеза прокоагулянтов в печени или их слабой активации при сохранении количественных показателей. Также на процесс коагуляции оказывается влияние гиперактивация фибринолитической системы и противосвертывающих факторов.

Непосредственные причины приобретенной гипокоагуляции:
- гепатиты, цирроз и другие заболевания печени, в клетках которой вырабатываются факторы свертывания крови;
- гиповитаминоз К;
- недостаток фолиевой кислоты;
- дефицит кальция в организме;
- ДВС-синдром;
- апластическая анемия;
- гематологические заболевания;
- онкопатологии;
- массивные кровопотери;
- бесконтрольная антибиотикотерапия;
- длительный прием больших доз антикоагулянтов;
- лечение фибринолитиками;
- дисфункция иммунной системы;
- использование НПВС;
- аллергия с выбросом в кровь гистамина;
- плохая экология, занятость на вредном производстве.
Подобные факторы приводят к снижению концентрации в крови разных естественных факторов свертывания, форменных элементов, ферментов и прочих частиц.
Тенденция к гипокоагуляции отмечается у недоношенных детей, испытавших кислородное голодание в утробе матери, а также у младенцев, рожденных женщиной, которая употребляла во время беременности салицилаты, фенобарбитал, антибиотики.
Симптомы

Клинические признаки патологии объединяют в несколько синдромов — кожный, болевой, анемический, геморрагический с внутренними и наружными кровотечениями, кровоизлияниями в органы, полости и ткани.
Основными проявлениями гипокоагуляции являются кровотечения различной интенсивности и продолжительности. Они возникают беспричинно и отличаются большой тяжестью. Остальные клинические признаки патологии зависят от этиологического фактора и общего состояния организма больного. К ним относятся:
- необъяснимо возникшие синяки,
- обильные менструации,
- частые носовых кровотечений, которые трудно остановить,
- кровоточивость десен,
- геморрагическая сыпь на коже в виде мелких точечных петехий,
- кровоизлияния в суставы и мышцы, обездвиживающие больного,
- кровь в кале – признак внутреннего кровотечения,
- крупные кровоподтеки и экхимозы на коже,
- головокружения, слабость и прочие проявления анемического синдрома.
Больные отмечают, что кровотечения даже из небольших ран очень долго останавливаются.

синяки и гемартрозы (кровоизлияния в суставы) при гемофилии

петехии и пурпура при тромбоцитопении
Появление перечисленных признаков требует немедленного обращения к врачу, который обследует пациента, определить причину проблемы и назначит лечение.
Диагностика
Чтобы установить причину гипокоагуляции, необходимо тщательно собрать анамнез болезни, проанализировать клинику патологии и данные лабораторных исследований – гемограммы, коагулограммы и прочих вспомогательных методик. Специалистам следует оценить характер кровоточивости и уточнить стадию коагулопатии, отражающую глубину нарушений. Врачи интересуются характером кровотечений, осматривают сыпь на коже и гематомы около суставов, выясняют наличие сопутствующих патологий и время возникновения основных симптомов.
Коагулограмма — основной диагностический метод, позволяющий определить свертывающую способность крови. При выявлении гипокоагуляции следует искать причину, вызвавшую нарушение.

Лица, которым в обязательном порядке делают коагулограмму:
- перенесшим инсульт и инфаркт,
- страдающим заболеваниями печени и сосудов,
- беременным женщинам,
- готовящимся к операции,
- имеющим повышенную склонность к тромбозам.
показатели коагулограммы в норме
С помощью коагулограммы определяют время свертывания крови, протромбиновое время, протромбиновый индекс, фибриноген, тромбиновое время. Это основные показатели коагулограммы, которые определяются у всех обследуемых лиц.
Кровь берут из локтевой вены строго натощак. Больных предупреждают, чтоб накануне обследования они не ели острую, жирную и соленую пищу, не курили, не принимали антикоагулянтные препараты. Забор материала выполняют шприцем с широкой иглой без жгута. При этом медперсонал должен минимально воздействовать на вену, чтобы не сильно ее травмировать. Если в кровоток попадет много тромбопластина, результат исследования будет искажен. Пациенты получают результат анализа на следующий день.
В гемограмме определяют количество тромбоцитов, выявляют признаки воспаления и анемии, а в иммунограмме — уровень иммуноглобулинов каждого вида. По показаниям проводится УЗИ внутренних органов, стернальная пункция и гистологический анализ биоптата костного мозга.
Лечение
Лечение гипокоагуляции длительное и комплексное, зависящее от причинных факторов. Если нарушение свертываемости крови является проявлением врожденных патологий, проводится пожизненная терапия определенными лекарственными средствами. Тяжелое состояние пациента, сопровождающееся резким снижением свертываемости и обильными кровотечениями — повод для его госпитализации в стационар.
Препаратами выбора при данной патологии являются коагулянты — средства, способствующие коагуляционному гемостазу. Их назначают всем больным с признаками повышенной кровоточивости независимо от этиологических факторов и прочих особенностей процесса. Коагулянты бывают прямыми и непрямыми. Первые являются эндогенными факторами системы свертывания природного происхождения. Они принимают непосредственное участие в коагуляции. Непрямые коагулянты не сами повышают свертывание крови, а запускают синтез эндогенных факторов в гепатоцитах печени.
Группы лекарственных средств, используемых для лечения гипокоагуляции:

- коагулянты прямого действия, выделенные из донорской плазмы — «Тромбин», «Гемостатическая губка», «Фибриноген», «Кальция хлорид»;
- коагулянты непрямого действия, опосредованно повышающие свертываемость крови – витамин К1, К2, «Викасол»;
- ингибиторы фибринолиза, замедляющие растворение тромбов и оказывающие кровеостанавливающее действие – «Аминокапроновая кислота», «Транексамовая кислота», «Гордокс»;
- препараты, обладающие антигеморрагическим действием и стимулирующие адгезию и агрегацию тромбоцитов – «Дицинон», «Этамзилат», «Контривен»;
- железосодержащие средства – «Тардиферон», «Хеферол», «Ферронат»;
- заместительная терапия — переливания свежезамороженной плазмы, тромбоцитарной или эритроцитарной массы, криопреципитата, физраствора.
Конкретные препараты и их дозировки подбираются врачом индивидуально для каждого пациента. Необходимо строго соблюдать инструкцию по применению, так как передозировка таких средств может привести к негативным последствиям.
Неплохие результаты в лечении гипокоагуляции дают рецепты народной медицины и фитосборы. Средства, улучшающие состояние больных, которые имеют плохую свертываемость крови – отвары и настои лекарственных трав: тысячелистника, крапивы, скорлупы грецких орехов, арники, сушеницы топяной и кукурузы. В отдельных случаях использование народных средств может привести к появлению аллергических реакций. Перед их применением необходима консультация с врачом.

продукты содержащие витамин K
Специалисты рекомендуют обогатить рацион продуктами с высоким содержание кальция, калия, фолиевой кислоты и аминокислот. К ним относятся: свежие овощи, фрукты и ягоды, зелень, яйца, бобы, орехи, свежевыжатые соки, жирные сорта рыбы, печень трески, животные жиры, баранина, свинина, субпродукты. Больным необходимо полностью отказаться от алкоголя, крепкого чая и кофе, колбас, соусов, сдобы, конфет, полуфабрикатов, фаст-фуда. Питание должно быть сбалансированным, обогащенным витаминами и микроэлементами. Особенно необходим лицам с гипокоагуляцией белок и витамин К. Эти вещества участвуют в синтезе факторов свертывающей системы крови. Правильный рацион — немаловажный аспект лечения, помогающий быстрее восстановить здоровье.
Профилактика и прогноз
Мероприятия, позволяющие избежать развития гипокоагуляции:
- употребление продуктов с высоким содержание белка и витамина К,
- исключение травм,
- генетическое консультирование супружеских пар перед зачатием,
- регулярное обследование лиц из группы риска,
- диспансеризация здоровых людей.
Гипокоагуляция или пониженная свертываемость крови — опасное состояние, приводящее к серьезным и угрожающим жизни последствиям. При отсутствии лечения у больных на коже появляются большие гематомы самопроизвольно или при незначительном надавливании, регулярно возникают обильные кровотечения из носа, обнаруживается кровь в кале. Внутренние кровотечения и кровоизлияние в мозг — неотложные состояния, требующие оказания экстренной помощи и нередко приводящие к гибели больных.
Прогноз патологии неоднозначный. Он зависит от основного, причинного заболевания, тяжести нарушений гемостаза и своевременности начатого лечения. Гипокоагуляция легкой степени имеет благоприятный прогноз при условии, что будет вовремя проведена адекватная терапия. Если патологию обнаружили поздно и сразу не стали лечить, возникают тяжелые осложнения, приводящие к смерти. Чтобы этого избежать, следует при появлении первых симптомов расстройства обратиться к врачу.
Закрытие мелких повреждений в сосудах. Основная теория свертывания крови
а) Важность тромбоцитарного механизма для закрытия мелких повреждений в сосудах. Механизм формирования тромбоцитарной пробки очень важен для закрытия мельчайших разрывов в мелких кровеносных сосудах, которые появляются много тысяч раз ежедневно. Действительно, множество мелких дырочек в самих эндотелиальных клетках часто закрываются тромбоцитами, которые буквально сливаются с эндотелием, формируя дополнительную мембрану эндотелиальной клетки. У человека с низким содержанием тромбоцитов в крови ежедневно появляются буквально тысячи точечных кровоизлияний под кожей и во всех внутренних тканях, но этого не случается у людей с нормальным содержанием тромбоцитов в крови.
б) Свертывание крови в разорванном сосуде. Третьим механизмом гемостаза является формирование кровяного сгустка. Он начинает развиваться через 15-20 сек при серьезной травме сосудистой стенки, и через 1-2 мин — при незначительной. Запускают процесс свертывания покрывающие место повреждения вещества-активаторы, выделяющиеся из стенки травмированного сосуда, кровяных пластинок и белков крови. Физические явления этого процесса показаны на рисунке ниже, а в таблице перечислены наиболее важные факторы свертывания.
Процесс свертывания в травмированном сосуде
Если отверстие в сосудистой стенке не слишком велико, в течение 3-6 мин после повреждения сосуда все отверстие или разорванный конец сосуда заполняются сгустком крови. Через 20-60 мин происходит ретракция (сжатие) сгустка; это способствует дальнейшему закрытию сосуда. В ретракции сгустка важную роль играют также тромбоциты.
в) Фиброзная организация или растворение кровяного сгустка. После формирования кровяного сгустка возможны два пути его дальнейшего развития: (1) заполнение сгустка фибробластами, которые в дальнейшем формируют соединительную ткань на всем протяжении сгустка; (2) растворение сгустка. При небольшом отверстии в сосудистой стенке сгусток обычно заполняется фибробластами через нескольких часов после его формирования (этому способствует, по крайней мере, частично, фактор роста, секретируемый тромбоцитами). Процесс продолжается в течение примерно 1-2 нед вплоть до полной организации сгустка в фиброзную ткань.
Наоборот, если в ткань вытекло много крови и образовались сгустки там, где в них нет необходимости, внутри самого сгустка обычно активируются особые вещества, функционирующие как ферменты, растворяющие сгусток. Подробнее это изложено далее.
Механизм свертывания (коагуляции) крови
Основная теория. В крови и тканях обнаружены более 50 веществ, вызывающих свертывание крови или влияющих на него. Одни из них способствуют свертыванию и их называют прокоагулянтами, другие — тормозят этот процесс и их называют антикоагулянтами. Останется ли кровь жидкой или произойдет ее коагуляция, зависит от баланса между этими группами веществ. В нормальном кровотоке преобладают антикоагулянты, поэтому кровь, циркулирующая в кровеносных сосудах, не свертывается. Но при разрыве сосуда прокоагулянты из области повреждения ткани активируются и перекрывают действие антикоагулянтов, что способствует образованию сгустка.
Основные этапы коагуляции крови. Все исследователи, занимающиеся проблемой свертывания крови, согласны с тем, что в основе свертывания лежат три основных процесса: (1) в ответ на разрыв сосуда или повреждение самой ткани в крови происходит сложный каскад химических реакций с участием более дюжины факторов свертывания крови. Итогом этого каскада является образование комплекса активированных веществ, в совокупности называемых активатором протромбина; (2) активатор протромбина катализирует превращение протромбина в тромбин; (3) тромбин действует как фермент, превращающий фибриноген в нити фибрина, формируя сгусток, внутрь которого захватываются кровяные пластинки, клетки крови и плазма.
Начнем с обсуждения механизма формирования самого сгустка крови, а именно: с превращения протромбина в тромбин; затем вернемся к начальным стадиям процесса свертывания, в результате которых образуется активатор протромбина.
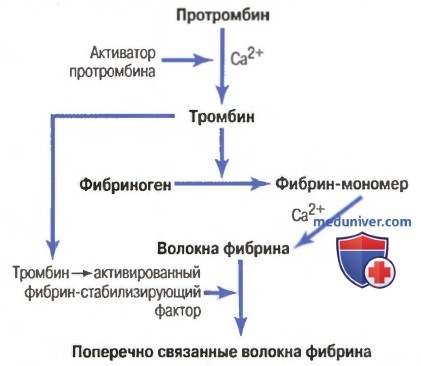
Схема превращения протромбина в тромбин и полимеризации фибрина с формированием волокон фибрина
Видео физиология остановки кровотечения (гемостаза) - профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гемостаз. Механизмы свертывания крови. Тромбоцитарный гемостаз. Тромбоцитарная реакция. Первичный гемостаз.
Тромбоцитарная реакция, т. е. реакция тромбоцитов на нарушение целостности сосудистой стенки, формируется параллельно реакции самих сосудов на повреждение — их сокращение в месте повреждения, вызывающее шунтирование крови выше поврежденного участка сосуда.
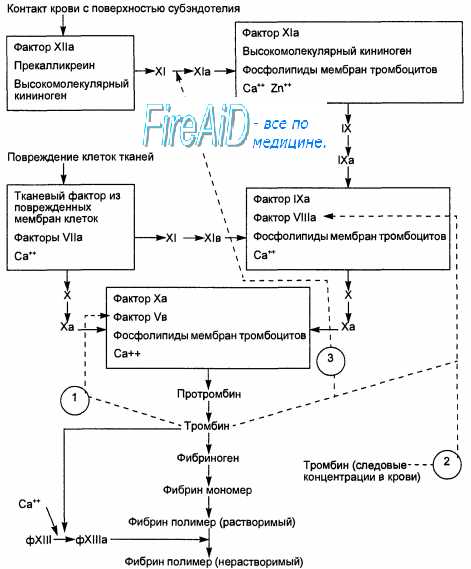
Рис. 7.8. Схема формирования коагуляционного гемостаза. 1 — активация тромбином ф.V; 2 — активация тромбином ф-VIII, высвобождаемого из связи с ф.Вилленбранта; 3 — активация тромбином ф.ХI. Контакт крови с поверхностью субэндотелия активирует «внутренний» путь свертывания крови; контакт крови с поврежденными клетками ткани активирует «внешний» путь активации свертывания крови.
Данная сосудисто-тромбоцитарная реакция на повреждение сосудистой стенки первой останавливает кровотечение из микрососуда и поэтому называется сосуди-сто-тромбоцитарным, или первичным, гемостазом. Формирование и закрепление тромбов с помощью плазменных факторов свертывания называют вторичным коагуляционным гемостазом. Первая волна агрегации тромбоцитов начинается с приклеивания тромбоцитов рецепторами гликопротеинов I и II к фактору Виллебранда, фибронектину и коллагену субэндотелия поврежденных тканей. Вторая волна агрегации тромбоцитов вызвана высвобождением АДФ из плотных гранул тромбоцитов, образованием тромбоксана А2 в их мембране, взаимодействием мембранных гликопротеинов IIb и IIIа с фибриногеном, а V — с тромбином. Но в основном вторую волну агрегации тромбоцитов обеспечивают тромбоксан А2 и тромбин.
Мощным стимулом для образования тромбоксана А2 в мембране тромбоцита являются коллаген и фактор Виллебранда, активирующий фосфолипазу А2. Сильный агрегационный эффект оказывает тромбин, который образуется на мембране тромбоцитов при участии фактора V и гликопротеина V. Ад-гезированные тромбоциты являются основой для агрегации, т. е. приклеивания к ним тромбоцитов, приносимых с кровью к участку поврежденного сосуда. В ходе агрегации тромбоцитарный тромб уплотняется и сокращается. Его формирование усиливается с образованием фибрина (фибринового тромба) вследствие активации плазменной системы свертывания крови (рис. 7.8).
Кровь является одной из важнейших частей человеческого организма. Эта жидкая субстанция питает все органы и ткани нашего тела. В норме у взрослого человека в теле от 3500 до 5000 мл крови. И чтобы это количество сохранялось, природой предусмотрен процесс остановки крови при ранениях. Рассмотрим факторы свертывания крови. Что такое гемостаз, и какое значение она имеет для жизни человека.
Что такое гемостаз
В нашем организме кровь должна поддерживаться в жидком состоянии, чтобы обеспечивать все органы и ткани необходимыми питательными элементами и кислородом. В то же время при необходимости жидкая субстанция должна превращаться в желеобразную, чтобы человек не умер от кровопотери. А после того, как желеобразный тромб выполнил свою миссию, он опять должен принять жидкое состояние. Этот процесс регулирования состояния крови называется гемостазом.

Гемостаз — это очень сложный механизм, в котором участвуют десятки веществ. Если в этом процессе происходит сбой, человек может столкнуться со многими заболеваниями, которые несут опасность для жизни. На гемостаз влияют факторы свертывания в крови.
Коагуляция
Коагуляция или свертываемость крови — это защитный механизм организма от большой кровопотери. Сегодня примерно половина человечества имеет проблемы с коагуляцией. Именно из-за них возникают такие страшные заболевания как тромбоз, инфаркт, инсульт, обширные кровотечения. Каждый десятый человек погибает в результате несвоевременного лечения данных патологий крови, а каждый второй вообще не подозревает у себя наличия нарушения коагуляции.
Коагуляция представляет собой последовательный ряд процессов, каждый из которых запускает следующий. При сбое на любом этапе свертывания возникает патология, которая препятствует нормальной свертываемости крови. Сегодня ученые выявили основные фазы свертывания крови, это:
- Возникновение протромбина.
- Возникновение тромбина.
- Активация фибрина.
Последней фазой остановки кровотечения является сужение и растворение тромба, который переходит в первоначально жидкое состояние.
Факторы влияющие на коагуляцию
За свертываемость крови в нашем организме отвечают две основные категории молекул – плазменные и тромбоцитарные. Плазменный гемостаз происходит при участии белков, которые участвуют в образовании тромба. Сколько факторов влияют на гемостаз? Таблица плазменных факторов состоит из 13 элементов, которые обозначаются в медицине римскими цифрами.
Каждый из этих компонентов выполняет свою роль в образовании фибрина.
Помимо пронумерованных факторов свертывания крови, существует еще несколько вспомогательных плазменных веществ, которые несут ответственность за реакцию всех компонентов.
Тромбоцитарные факторы свертывания крови — это составляющие тромбоцитов, относящиеся к компонентам, которые отвечают за свертываемость красных кровяных телец. Их в медицине насчитывается 10. При недостатке или избытке одного из компонентов происходит сбой в коагуляции и кровь свертывается медленнее нормы.
13 плазменных факторов
| № | Факторы | Подробное описание |
|---|---|---|
| 1 | Фибриноген | Производится в печеночной ткани, селезенке, костном мозге и лимфатических узлах человека. Отвечает за образование фибрина для создания сетчатой базы тромба. Плазма должна содержать от 2 до 4 г/л. |
| 2 | Протромбин | Производится в печеночной ткани при участии микроэлемента К. При недостатке этого витамина печенью производится неполноценный белок, который не может выполнять свои задачи в полной мере. |
| 3 | Тромбопластин (белок тканевый) | Содержится во внутренних органах человека. В крови находится в пассивном состоянии. Играет важную роль в активировании протромбина. |
| 4 | Ca | Обязательный фактор, свертывающий кровь. Играет роль во всех этапах коагуляции. Колличество в плазме в норме составляет от 0,09 до 0,1 г/л. Дефицит кальция выражается судорогами нижних конечностей. |
| 5 | Проакцелирин | Производится в печеночных тканях. Не зависим от уровня микроэлемента К в организме. Участвует в запуске метаморфозы протромбина и в синтезе протромбиназы (ф. десятый). Норма в плазме от 12 до 17 ед./мл. |
| 6 | Акцелирин | Имеет значение только пассивная форма — проакцелирин, которая активизируется при наличии тромбина. |
| 7 | Проконвертин (белок) | Относится к производным печеночной ткани. Активация наступает в начале цепи коагуляции при контакте с ранящей поверхностью. Участвует в синтезе тромбина и тканевой протромбиназы. Норма у взрослого человека в среднем 0,005 г/л. |
| 8 | А-глобулин (белок антигемофильный) | Норма у здорового человека от 0,01 до 0,02 г/л. Фактор свертывания крови VIII участвует в преобразовании протромбина. |
| 9 | В-глобулин (антигемофильный белок ф. Кристмаса) | Зависим от содержания микроэлемента К. Зарождается в печени. Один из самых значимых компонентов 10 фактора коагуляции. Отвечает за образование протромбиназы. Дефицит IX фактора ведет к кровоизлияниям. |
| 10 | Стюарта-Прауэра | Компонент напрямую зависит от третьего, седьмого и девятого факторов. Является основным фактором образования протромбиназы. |
| 11 | Компонент Розенталя | Предшественник тромбопластина. Активируется двенадцатым фактором. Не зависит от содержания витамина К. Синтезируется в печени. Содержание в крови около 0,005 г/л. |
| 12 | Хагемана | Контактное вещество активирует одиннадцатый фактор. Синтезируется в печени. |
| 13 | фибриназа | Тринадцатый фактор заставляет кровь свертываться. Его дефицит вызывает внутричерепные кровоизлияния. |
Также в коагуляции принимают участие дополнительные плазменные факторы свертывания крови.
К факторам свертывания в крови относятся компоненты: Виллебранда, Флетчера, Фитцджеральда. Эти составляющие участвуют в активации других факторов, и при их дефиците может нарушиться цепь коагуляции.
Дефицит одного или нескольких факторов свертывания крови ведет к развитию патологии под названием коагулопатия, которая представляет собой нарушение свертываемости крови. Коагулопатия может быть вызвана как наследственными, так и приобретенными причинами. К наследственным факторам развития заболевания относятся:
- Дефицит компонентов 8 и 9, 10 факторов.
- Дефицит компонентов 5, 7, 10 и 11 факторов.
- Дефицит компонентов других факторов.
- Синдром ДВС.
- Приобретенные ингибиторы.
- Дефицит факторов протромбина.
- Препараты гепарина и др.
Тромбоцитарные факторы
Тромбоцитарные факторы свертывания в крови содержатся непосредственно в тромбоцитах — красных кровяных тельцах. Сегодня ученые говорят, что их количество превышает 10, но точное число до сих пор остается под вопросом. В учебниках по медицине сегодня приводится 12 молекул свертываемости крови:
- Белок тромбина.
- Триггер фибрина акцелератор.
- Фосфолипопротеид.
- Ингибитор гепарина.
- Агглютинабелин.
- Ингибитор распада фибрина.
- Ингибитор распада протромбина.
- Ретрактозин.
- Серотонин.
- Котромбопластин.
- Активатор фибрина.
- АДФ отвечает за слипаемость тромбоцитов.
Факторы влияющие на свертываемость крови
Для того, чтобы поддерживать свое здоровье в порядке каждый человек должен знать факторы ускоряющие и замедляющие свертывание в крови. Эти знания помогут избежать развития опасных для жизни состояний и своевременно наладить систему коагуляции. Нарушение гемостаза на любой стадии может привести либо к обширным кровотечениям, либо к образованию тромбов. И то и другое опасно для жизни.
Низкая свертываемость крови. Это состояние опасно возникновением смертельных внутренних кровотечений. Причинами развития патологии могут стать:
- Генетические нарушения.
- Онкологические заболевания на поздней стадии.
- Препараты разжижающие кровь.
- Нехватка витамина К.
- Нехватка кальция.
- Заболевания печени.
Лечение данной патологии зависит от причин ее развития. Препараты назначает врач гематолог. Если причиной плохой свертываемости стало медикаментозное лечение, нужно ограничить прием лекарств или заменить их на более щадящие препараты.
Повышенная свертываемость крови. Данная патология опасна образованием тромбов сосудов, вен и артерий. При закупорке артерий происходит отмирание органов, которые она питает. Также опасность заключается в возможности отрыва тромба, который может закупорить жизненно важные артерии легких и сердца, это ведет к летальному исходу. Основными причинами развития этого нарушения являются:
- Инфекционные заболевания.
- Низкая физическая активность.
- Атеросклероз.
- Обезвоживание.
- Наследственные факторы.
- Сахарный диабет.
- Лишний вес.
- Беременность.
- Аутоиммунные заболевания.
- Стресс.
- Онкологические болезни.
- Артериальная гипертензия.
При лечении данной патологии главной целью врачей является снижение свертываемости крови до нормального уровня. Для этих целей используют специальные препараты — антикоагулянты. Их прием должен проходить под четким контролем лечащего врача. Сначала пациенту назначается курс гепарина, а затем проводят аспириновую терапию.
При наследственной тромбофелии аспирин назначается в малых дозах еще в младенчестве.
Анализ на функцию свертываемости крови необходимо проводить перед любым хирургическим вмешательством, чтобы исключить возможные осложнения. Также это исследование назначают беременным женщинам и при определенных жалобах пациентов. Обычно повышенная свертываемость наблюдается у пациентов пожилого возраста.
Если у вас обнаружили нарушение свертываемость крови, не нужно предаваться панике. Это значит, что вам необходимо более тщательно следить за своим здоровьем. Любое лекарственное средство нужно принимать только после консультации с врачом. Также необходимо сдавать все анализы, чтобы выяснить причину нарушения. Если не затягивать с лечением и выполнять все рекомендации доктора, болезнь быстро отступит и ваша жизнь вернется в здоровое русло.


Если посмотреть на каплю крови в микроскоп (пусть это будет световой микроскоп, но достаточно мощный), то можно увидеть клетки трёх типов: многочисленные эритроциты, или красные кровяные тельца, немногочисленные, но довольно крупные лейкоциты и мельчайшие тромбоциты, которые удаётся разглядеть с некоторым трудом. Эритроциты, плотно набитые белком гемоглобином, переносят кислород: гемоглобин связывает его в лёгких и отдаёт в тканях и органах, которые в нём нуждаются. Лейкоциты — клетки иммунной системы, и они вместе с иммунными белками защищают нас от инфекций и от некоторых неинфекционных заболеваний, например от рака. Лейкоцитов существует несколько типов, отличающихся в том числе и по численности; возможно, из лейкоцитов нам попадутся Т-лимфоциты, которые целенаправленно распознают и сами уничтожают как чужеродные, так и наши собственные клетки, которым не повезло заболеть. Наконец, тромбоциты. Про тромбоциты мы знаем, что они нужны для свёртывания крови.
Кто не представляет, как работает система свёртывания крови? Уколовши палец, мы наблюдаем, как он сначала кровоточит, а потом перестаёт — образовавшийся тромб остановил кровь. Если бы кровь не свёртывалась, то разбитый нос мог бы оказаться смертельным ранением. Но, наверно, едва ли не более важная функция механизма свёртывания — предотвращение внутренних кровотечений, которые часто случаются при различных заболеваниях (например, при тяжёлой инфекции или при злокачественной опухоли). При этом система свёртывания должна быть очень точно сбалансирована: если она будет работать плохо, то пойдут неостанавливаемые кровотечения, внутренние и наружные; если же механизм свёртывания будет слишком активным, начнут формироваться тромбы, грозящие закупоркой сосудов и остановкой кровоснабжения. В медицине есть масса примеров, когда процессы свёртывания крови и тромбообразования идут не так, как надо, и не там, где надо. Причиной тому могут быть либо другие болезни, и тогда нарушения системы свёртывания крови — это просто сопутствующий симптом, либо же сами эти нарушения представляют собой отдельные, самостоятельные заболевания (вроде небезызвестной гемофилии или болезни Виллебранда).
Бороться с аномалиями системы свёртывания можно по-разному, и сейчас есть медицинские средства, которые позволяют эффективно регулировать её работу. Но чтобы такие средства работали ещё лучше, чтобы сделать их ещё более совершенными, нужно как можно точнее знать, как на молекулярно-клеточном уровне устроен механизм свёртывания крови. Его изучают уже более ста лет, и сейчас его схему можно найти в любом школьном учебнике; правда, схему эту большинство из нас старается забыть, как страшный сон: ещё бы, около двух десятков белков, соединённых стрелками, — кто-то кого-то активирует, кто-то кого-то ингибирует. Однако если рассматривать свёртывание по этапам, то всё становится более или менее понятно.
Стоит сразу сказать, что собственно свёртывание — лишь часть более общего процесса гемостаза (от греч. haimatos — кровь, stasis — остановка). И этот процесс начинается как раз с тромбоцитов. Они происходят от мегакариоцитов — гигантских клеток костного мозга. От зрелых мегакариоцитов «отшнуровываются» куски цитоплазмы, которые и становятся безъядерными клетками тромбоцитами (хотя, учитывая их происхождение и отсутствие ядра, более корректно называть их просто тельцами крови или кровяными пластинками). Тромбоциты циркулируют по крови, пока не «заметят» брешь в сосуде. Сигналом для них служит соединительнотканный белок коллаген. Он обычно спрятан внутри стенки сосуда, но при её повреждении оказывается лицом к лицу с тромбоцитами и другими белками крови. На мембране тромбоцитов есть специальный рецептор, который хватает коллаген и заставляет кровяные пластинки прилипнуть к месту повреждения. Тут в дело вступает один из факторов свёртывания под названием «фактор фон Виллебранда». Это гликопротеин (его молекула состоит из белковой и углеводной частей), который помогает другим рецепторам тромбоцитов зацепиться за торчащий из стенки сосуда коллаген. Благодаря фактору фон Виллебранда тромбоциты не только прочнее взаимодействуют с местом повреждения, но и дополнительно активируются — подают молекулярные сигналы другим тромбоцитам и белкам свёртывания, меняют внешнюю форму и активно слипаются друг с другом. В результате на стенке кровеносного сосуда появляется затычка из тромбоцитов.
Одновременно с формированием тромбоцитарной пробки происходит процесс собственно свёртывания крови — свёртывания в строгом смысле слова. В нём участвует множество белков плазмы крови, большинство из них — ферменты-протеазы, то есть белки, отщепляющие куски от других белков. Если до расщепления «жертва» протеазы была неактивным белком-ферментом, то после расщепления фермент активируется и, если он сам протеаза, тоже может кого-то расщепить. Суть ферментативных реакций, которые идут во время свёртывания, в том, что белки активируют друг друга, и в итоге всё заканчивается появлением активного белка фибрина, который быстро полимеризуется, превращаясь в нити — фибриллы. Из нитей фибрина формируется фибриновый сгусток, дополнительно укрепляющий тромбоцитовую «затычку», — образуется тромбоцитарно-фибриновый тромб. Когда сосуд восстанавливается, тромб рассасывается.
Оба этапа — и формирование тромбоцитарной пробки, и свёртывание крови с участием плазматических факторов-ферментов — подчиняются множеству регуляторов. Для организма важно, чтобы система гемостаза работала как можно более точно, и многостадийность как раз помогает выполнять тонкую настройку: на каждом этапе, на каждой реакции ферменты и другие молекулы, задействованные в процессе, проверяют, не ложный ли сигнал к ним пришёл и действительно ли есть необходимость в тромбе. Естественно, тромбоциты и факторы свёртывания теснейшим образом связаны друг с другом и тромбоциты нужны не только для того, чтобы первыми заткнуть брешь в сосуде. Во-первых, они также выделяют белки, которые ускоряют восстановление стенки сосуда. Во-вторых, что особенно важно, кровяные пластинки нужны ещё для того, чтобы ферменты свёртывания продолжали работать.
После запуска процесса гемостаза мембрана некоторых тромбоцитов изменяется особым образом, так что теперь на неё могут садиться ферменты реакций свёртывания: после приземления на такие тромбоциты они начинают работать намного быстрее. Что при этом происходит, удалось выяснить лишь относительно недавно. Активированные тромбоциты, то есть те, которые почувствовали повреждение сосуда, бывают двух форм: простые (агрегирующие) и сверхактивированные (прокоагулянтные). Простые агрегирующие тромбоциты отчасти похожи на амёбы: они образуют выпячивания мембраны, похожие на ножки, которые помогают им лучше сцепляться друг с другом, и становятся более плоскими, как бы растекаясь по поверхности. Такие клетки формируют основное тело тромба. Сверхактивированные тромбоциты ведут себя иначе: они приобретают сферическую форму и увеличиваются в несколько раз, становясь похожими на воздушные шарики. Они не просто укрепляют тромб, но и стимулируют реакцию свёртывания, почему их и называют прокоагулянтными.


Почувствовав, что стенка кровеносного сосуда повреждена, тромбоциты активируются. Обычные активированные тромбоциты (слева; фото со сканирующего электронного микроскопа) делаются плоскими и образуют, подобно амёбам, многочисленные выросты мембраны; сверхактивированные, или прокоагулянтные, тромбоциты (справа; фото с просвечивающего электронного микроскопа) превращаются в шар и становятся площадкой для сборки и активации ферментативных комплексов аппарата свёртывания крови. Фото Михаила Пантелеева, МГУ
Как одни тромбоциты становятся простыми, а другие — сверхактивированными? Известно, что в прокоагулянтных тромбоцитах очень высок уровень кальция (ионы кальция вообще один из главных регуляторов гемостаза) и что у них выходят из строя митохондрии. Связаны ли эти изменения в клеточной физиологии со сверхактивацией тромбоцитов?
В прошлом году Фазли Атауллаханов * , директор Центра теоретических проблем физико-химической фармакологии РАН, вместе с Михаилом Пантелеевым, заведующим лабораторией молекулярных механизмов гемостаза центра и профессором кафедры медицинской физики физического факультета МГУ, опубликовали в журнале Molecular BioSystems статью с описанием модели митохондриального некроза как особой формы клеточной смерти. Мы знаем, что клетка может погибнуть в результате апоптоза, включив программу самоуничтожения (при апоптозе всё происходит по плану и с минимальным беспокойством для клеток-соседей), или в результате некроза, когда гибель случается быстро и незапланированно, например из-за разрыва наружной мембраны или из-за масштабных внутренних неприятностей, вроде вирусной или бактериальной инфекции.

Поперечный срез через митохондрии клетки лёгкого. Митохондрии выглядят как цистерны, окружённые двойной мембраной; поперечные полосы на снимке — впячивания их внутренней мембраны, на которой сидят ферменты энергетического обмена веществ. Фото: Louisa Howard/Wikimedia Commons
В чём особенность митохондриального некроза? Митохондрии, как известно, служат источниками энергии для любой нашей клетки: в митохондриях происходит кислородное окисление «питательных» молекул, а освобождённая при этом энергия запасается в удобной для клетки форме. Побочным продуктом при работе с кислородом оказываются агрессивные кислородные радикалы, которые могут испортить любую биомолекулу. Сами митохондрии стараются уменьшать концентрацию радикалов и не выпускать их из себя в клеточную цитоплазму.
При митохондриальном некрозе происходит следующее: митохондрии вбирают в себя кальций, и в какой-то момент, когда кальция становится слишком много, они разрушаются, выплёскивая в цитоплазму и кальций, и активные формы кислорода. В результате в клетке распадается внутриклеточный белковый скелет и клетка сильно увеличивается в объёме, превращаясь в шар. (Как мы помним, шарообразная форма характерна для сверхактивированных тромбоцитов.) Кроме того, и ионы кальция, и активные формы кислорода активируют фермент скрамблазу, который перебрасывает фосфатидилсерин — один из липидов цитоплазматической мембраны — из внутреннего слоя мембраны в наружный. И вот на такую модифицированную мембрану округлившихся тромбоцитов, обогащённую фосфатидилсерином, прилипают некоторые важные факторы свёртывания: здесь они собираются в комплексы, активируются, и в результате реакция свёртывания ускоряется в 1000–10 000 раз.
В новой статье, опубликованной в июне этого года в Journal of Thrombosis and Haemostasis, Михаил Пантелеев, Фазли Атауллаханов и их коллеги описывают эксперименты, которые полностью подтверждают такую модель активации тромбоцитов: кровяные пластинки стимулировали тромбином, одним из белков системы свёртывания, после чего митохондрии наполнялись ионами кальция, а в митохондриальных мембранах появлялись поры. Проницаемость митохондрий увеличивалась, и в какой-то момент, когда изменение проницаемости делалось необратимым, весь запасённый кальций оказывался в цитоплазме и запускал процесс «переформатирования» наружной мембраны.
Получается следующая картина: тромбоциты, подчиняясь внешним активаторам, впитывают кальций. Из их цитоплазмы кальций переходит в митохондрии. В самой цитоплазме уровень ионов кальция то повышается, то понижается (осциллирует), но в митохондриях он неуклонно растёт, и наступает момент, когда они уже не могут удерживать кальциевые ионы внутри себя. Весь кальций (с кислородными окислителями) выходит в цитоплазму и включает фермент, перебрасывающий липиды в цитоплазматической мембране тромбоцита. В результате на поверхности сверхактивированного и, очевидно, доживающего свои последние минуты тромбоцита собираются ферментативные комплексы, ускоряющие реакцию свёртывания.
Почему же не все тромбоциты становятся сверхактивированными — прокоагулянтными? Вероятно, потому, что для активации требуется сумма сигналов от разных регуляторов. Мы уже сказали, что тромбоциты чувствительны к тромбину, который плавает в плазме крови, а в начале статьи говорили, что одним из первых активирующих сигналов для кровяных пластинок служит коллаген из повреждённой стенки сосуда. Коллаген и тромбин действительно сильные активаторы, но кроме них тромбоциты «прислушиваются» и к некоторым другим молекулам. Степень активации зависит от количества разных входных сигналов, и превращение в прокоагулянтную форму, очевидно, происходит тогда, когда суммарный сигнал извне оказывается для конкретного тромбоцита особенно сильным.
Практические аспекты полученных результатов понятны каждому: чем больше подробностей узнаем про свёртывание крови, тем скорее научимся управлять этим процессом, ускоряя или замедляя его в соответствии с медицинскими показаниями.
Читайте также:

