При пониженном гемоглобине может быть крапивница
Обновлено: 27.04.2024
Анемия - клинико-гематологический синдром, характеризующийся снижением содержания гемоглобина в единице объема крови. В соответствии с рекомендациями всемирной организации здравоохранения (ВОЗ), анемия диагностируется при снижении гемоглобина ниже 110 г/л у детей в возрасте до 5 лет, ниже 115 г/л -в возрасте от 5 до 12 лет, ниже 120 г/л у детей старше 12 лет [1]. Анемия может быть проявлением многих патологических состояний, как связанных с первичным поражением системы крови,так и не зависящих от него.
Успех лечебных мероприятий и качество жизни ребенка с анемией во многом зависят от раннего установления ее причины. Сталкиваясь с проблемой анемии, каждый педиатр должен понимать, что проводимая терапия не сводится к восстановлению нормального уровня гемоглобина крови, она должна основываться на понимании патогенетических механизмов гематологических нарушений у пациента. В настоящее время существует несколько различных классификаций анемии, разработанных с целью выделения основных механизмов ее развития и систематизации проводимых диагностических мероприятий. В связи с тем, что причиной снижения гемоглобина крови может оказаться практически любое заболевание, строгая этиологическая классификация анемий невозможна. Однако общность патогенетических механизмов развития малокровия позволяет объединить ряд анемических состояний самой разнообразной этиологии в несколько групп.
Основные механизмы развития анемий были выделены еще в 1930-е годы профессором М.П. Конча-ловским: кровопотеря, усиленное кроверазрушение и нарушение кровообразования [2]. Данный патогенетический принцип лежит и в основе современной классификации анемических состояний, предложенной как отечественными, так и зарубежными авторами (табл. 1) 3.
Таблица 1. Этиопатогенетическая классификация анемий
Постгеморрагические анемии
Острая постгеморрагическая
Анемии вследствие нарушения образования эритроцитов
Анемии вследствие дефицита белка, микроэлементов (железа, меди), витаминов (С, В6, В12, фолиевой кислоты)
Дизэритропоэтические анемии вследствие подавления эритропоэза, снижения утилизации железа (на фоне инфекционных, онкологических заболеваний, патологии печени, почек, системных заболеваний соединительной ткани)
Анемии вследствие патологии костного мозга (гипо- и апластические анемии, анемии на фоне гематоонкологических заболеваний)
Внутриклеточный гемолиз (патология мембран эритроцитов, патология ферментов эритроцитов, дефекты гемоглобина)
Внеклеточный гемолиз (иммунная и неиммунная гемолитические анемии)
Данная классификация действительно важна для определения тактики ведения пациентов, однако в практической работе дифференциальный диагноз анемии обычно начинается с анализа гемограммы. Большинство современных анализаторов в настоящее время позволяют врачу получить данные не только об уровне гемоглобина и количестве эритроцитов, но и оценить дополнительные параметры, характеризующие состояние «красной крови» (табл. 2). В зависимости от цветового показателя, который обычно коррелирует с уровнем MCH, анемии могут быть разделены на гипо-, нормо- и гиперхромные (табл. 3). Средний объем эритроцитов свидетельствует о размерах красных клеток и позволяет разделить анемии на микро-, нормо- и макроци-тарные (табл. 4) [3]. Еще одним информативным показателем для дифференциальной диагностики анемических состояний является уровень ретикуло-цитов. В норме в периферической крови содержится 0,5-1% предшественников эритроцитов. Для аре-генераторных состояний (апла-стическая анемия) характерно полное отсутствие ретикулоцитов в мазке крови. При гипорегенера-торных анемиях (железодефицит-ная, В12-дефицитная, сидеробласт-ная анемии) доля ретикулоцитов обычно составляет менее 0,5%, хотя может оставаться и в пределах нормы. Норморегенератор-ный характер анемии (ретикуло-циты 0,5-2%) свидетельствует о нормальной способности костного мозга к усилению эритро-поэза, что характерно для острых постгеморрагических анемий. К гиперрегенераторным анемиям относятся практически все гемолитические анемии, при которых количество ретикулоцитов в периферической крови обычно превышает 2-5%. Еще более точным показателем эритропоэза является ретикулоцитарный индекс (РИ), который вычисляется по формуле: РИ = [число ретикулоцитов (%) х гематокрит больного (%) / гемато-крит в норме (%)]. В норме ретикулоцитарный индекс равен 1. При острой постгеморрагической анемии данный показатель повышается обычно в 2-3 раза, а при гемолизе - в 5-6 раз выше нормы.
Таблица 2. Параметры, характеризующие состояние эритроцитов
Показатель
Физиологическое значение
Нормальный уровень
Цветовой показатель (ЦП)*
Характеризует степень насыщения эритроцита гемоглобином
Среднее содержание гемоглобина в эритроците (MCH, Mean Corpuscular Hemoglobin)
Характеризует содержание гемоглобина в эритроците
27-31 пикограмм (pg)
Средняя концентрация гемоглобина в эритроците (МСНС, Mean Corpuscular Hemoglobin Concentration)
Характеризует степень насыщения эритроцита гемоглобином
Средний объем эритроцитов (MCV, Mean Corpuscular Volume)
Характеризует объем эритроцитов
72-79 мкм3 (фентолитров, fL)
Показатель анизоцитоза (RDW, Red cell Distribution Width)
Дает количественную оценку разброса эритроцитов по объему
Таблица 3. Классификация анемий в зависимости от уровня MCH и цветового показателя
Показатели
Анемии
Гипохромная анемия ЦП < 0,85; MCH < 27pg
Железодефицитная анемия Талассемии
Нормохромная анемия ЦП 0,85-1,05 MCH 27-31 pg
Острая постгеморрагическая анемия Гемолитические анемии Апластическая анемия
Анемия при неопластических заболеваниях костного мозга Анемия вследствие снижения выработки эритропоэтина
Гиперхромная анемия ЦП > 1,05 MCH > 31 pg
Витамин В12-дефицитная анемия Фолиеводефицитная анемия
Таблица 4. Классификация анемий в зависимости от объема эритроцитов
Показатели
Анемии
Микроцитарная (гипохромная) анемия
Железодефицитная анемия Талассемии
Сидеробластная анемия
Анемия при хронических инфекционных заболеваниях Анемия при выраженных нарушениях питания
Острая постгеморрагическая анемия Анемия при патологии печени и почек
Анемия при системных заболеваниях соединительной ткани Апластическая анемия
Анемия при диссеминированных злокачественных образованиях Дизэритропоэтическая анемия Ранние стадии дефицита железа
Витамин В12-дефицитная анемия Фолиеводефицитная анемия Апластическая анемия Гипотиреоз
Состояние после спленэктомии
Таким образом, определив характер анемии при первичном анализе гемограммы пациента, можно с довольно с высокой вероятностью определить возможную причину снижения гемоглобина и четко спланировать дальнейшие диагностические мероприятия с целью установления этиологии анемического состояния.
Приводим несколько собственных наблюдений.
Клинический пример № 1
Мальчик Ф., 2 года 9 месяцев, находился в грудном инфекционном отделении Тушинской ДГБ с диагнозом: Острая респираторная вирусная инфекция, острый левосторонний средний катаральный отит. Из анамнеза известно, что ребенок от первой беременности у женщины 27 лет, протекавшей с инфекцией мочевыводящих путей в третьем триместре, в связи с чем пациентка получала Канефрон. Роды срочные, физиологические. Вес ребенка при рождении 3890 г, длина тела - 56 см. Оценка по шкале Апгар 8/8 баллов. На грудном вскармливании до 1 года 9 месяцев. Прикорм введен с 4 месяцев (овощное пюре домашнего приготовления, каши инстантные). Острыми респираторными заболеваниями до 2 лет ребенок болел 3-4 раза в год в легкой форме. За 2 месяца до госпитализации пациент отдыхал с родителями в Турции. После возвращения в Москву у ребенка отмечалось 4 эпизода острой респираторной инфекции, рецидивирующее течение отита. Очер едной эпизод повышения температуры стал поводом для госпитализации в стационар. Данные осмотра ребенка при поступлении в отделение: состояние средней тяжести, температура тела 38 °С. Отмечаются симптомы интоксикации в виде вялости, быстрой утомляемости, снижения аппетита. Кожные покровы и видимые слизистые бледные, чистые от сыпи. Периферические лимфоузлы пальпируются в основных группах, мелкие, подвижные, безболезненные. Дыхание в легких везикулярное, проводится сим-ме трично во все отделы. Тоны сердца удовлетворительной звучности, ритмичные, нежный систолический шум на верхушке сердца. Печень пальпируется по краю реберной дуги. Физиологические отправления в норме. Показатели гемограммы: Hb 71г/л, эритроциты - 2,43 х 10 12, ЦП 0,88, МСУ 75 fL, MCH 30 pg, RDW 14%, ретикулоциты - 0,4%, тромбоциты 135 тыс, лейкоциты - 2,1 тыс, п/я -6%, с/я - 9%, лимфоциты - 81%, эозинофилы - 1%, моноциты - 3%, СОЭ - 35 мм/ч.
Результаты клинического анализа крови позволили диагностировать наличие у ребенка нормохромной нормоцитарной гипорегенера-торной анемии средней степени тяжести, сопровождающейся лейкопенией, нейтропенией, тромбоцитопенией, что указывает на вероятное вовлечение в патологический процесс костного мозга. Данная гемограмма с учетом возраста ребенка, указаний на предшествовавшую заболеванию повышенную инсоляцию, рецидивирующее течение инфекционных заболеваний требует обязательного исключения гемато-онкологического заболевания (дебюта острого лейкоза). В отделении ребенку были проведены дополнительные исследования:
■ в биохимическом анализе крови железо сыворотки, ферритин, общая железосвязывающая способность сыворотки крови и содержание фолиевой кислоты находились в пределах возрастной нормы;
■ при ультразвуковом исследовании брюшной полости выявлена умеренная гепатоспленомегалия, увеличение лимфоузлов в воротах печени до 6 мм в диаметре;
■ результаты обследования на ВИЧ, гепатиты В и С, цитомегаловирус,герпес 1, 2 типа, вирус Эпштейна-Барр - отрицательные.
■ Была проведена стернальная пункция, на основании анализа результатов которой у ребенка был диагностирован острый лимфобластный лейкоз, а выявленная анемия была проявлением основного заболевания.
Клинический пример № 2
Показатели гемограммы в первые сутки госпитализации: Hb 100 г/л, эритроциты - 3,0 х 10 12 , ЦП 1,0, МО/ 72 fL, MCH 29 pg, RDW 13,5%, ретикулоциты - 2%, тромбоциты 209 тыс, лейкоциты - 11,5 тыс, с/я - 65%, лимфоциты - 26%, моноциты 9%, СОЭ 51 мм/ч. На вторые сутки госпитализации у ребенка отмечалось ухудшение состояния в виде нарастания вялости, усиления бледности и появления желтушности кожных покровов. Моча приобрела темную окраску.
В контрольном анализе крови: Hb 65 г/л, эритроциты - 2,3 х 10 12 , ЦП 0,85, МС/ 75 fL, MCH 30 pg, ре-тикулоциты - 2,5%, тромбоциты -230 тыс, лейкоциты - 15,7 тыс, с/я - 65%, лимфоциты - 28%, моноциты - 7%.
На основании анализа клинического исследования крови у ребенка была диагностирована нормохромная нормоцитарная гиперрегенераторная анемия тяжелой степени, что, в сочетании с клиническими данными (появление иктеричности кожных покровов, потемнение мочи) позволило установить ее гемолитический характер.
По результатам дополнительно проведенных исследований было выявлено:
■ в биохимическом анализе крови: повышение уровня аспа-ратаминотрансферазы (АСТ) 114 ел/л, общего билирубина 80 мкмоль/л, прямого билирубина 16 мкмоль/л, лактатдегидрогена-зы (ЛДГ) 3049 ед/л;
■ на рентгенограмме органов грудной клетки выявлена легкая инфильтрация в нижних отделах справа без четких контуров, усиление легочного рисунка;
■ серологическое обследование на инфекции выявило наличие в диагностическом титре антител класса IgM к Mycoplasma pneumoniae.
Ребенку были назначены клари-тромицин из расчета 15 мг/кг/ сут, муколитики, гормональная терапия (преднизолон из расчета 1 мг/кг/сут). В связи с резким снижением уровня гемоглобина проведено переливание эритро-цитарной массы. На фоне проводимой терапии состояние ребенка стабилизировалось, пневмония разрешилась, бледность кожных покровов уменьшилась, иктерич-ность исчезла.
В контрольном клиническом анализе крови: Hb 103 г/л, эритроциты - 3,9 х 10 12 , ЦП 0,79, МС/ 72 fL, MCH 27 pg, ретикулоциты - 4%, тромбоциты 337 тыс, лейкоциты -22,9 тыс, с/я - 35%, лимфоциты -58%, моноциты 7%, СОЭ 3 мм/ч. В данном анализе, наряду с повышением уровня гемоглобина, отмечается рост количества ретикуло-цитов, лейкоцитов, тромбоцитов, что свидетельствует об активной гемопоэтической функции костного мозга и подтверждает гиперрегенераторный характер анемии. После купирования пневмонии ребенок был переведен в гематологическое отделение Измайловской ДГКБ для дообследования и уточнения характера гемолитической анемии.
Клинический пример № 3
Мальчик В., 1 год, госпитализирован в грудное инфекционное отделение Тушинской ДГБ с клиникой острой респираторной вирусной инфекции, жалобами на повышение температуры до 39 °С, насморк. Из анамнеза известно, что мальчик от женщины 30 лет, от первой беременности, протекавшей физиологически. У матери с 2004 года диагностирована желе-зодефицитная анемия (снижение гемоглобина до 90 г/л), в связи с которой она нерегулярно получала короткие курсы препаратов железа с нестойким положительным эффектом. Роды срочные, физиологические. Вес ребенка при рождении 3400 г, рост - 52 см, оценка по шкале Апгар 8/9 баллов. С рождения мальчик находился исключительно на грудном вскармливании, прикорм введен с 6 месяцев с использованием продуктов только домашнего приготовления. До 1 года ребенок не болел. Профилактические прививки не проведены в связи с отказом родителей. Аллергоанамнез не отягощен. Настоящее заболевание началось остро за 2 дня до поступления в стационар с повышения температуры до фебрильных значений, появления насморка. Стойкое повышение температуры, несмотря на проводимое симптоматическое лечение и прием жаропони-
жающих препаратов, послужило поводом для госпитализации в стационар. Данные осмотра при поступлении: состояние ребенка средней тяжести, симптомы интоксикации выражены умеренно. Кожные покровы бледные, чистые. Выражены катаральные явления. В легких хрипы не выслушиваются. Тоны сердца звучные, нежный систолический шум на верхушке. Печень и селезенка не увеличены. Физиологические отправления в норме. Показатели гемограммы: Hb 83 г/л, эритроциты - 3,4 х 10 12 , ЦП 0,73, МС/ 50 fL, MCH 24 pg, MCHC 30,25%, RDW 16,5%, ретикулоци-ты - 0,2%, тромбоциты 380 тыс, лейкоциты - 9,9 тыс, с/я - 46%, лимфоциты - 48%, моноциты 6%, СОЭ 11 мм/ч.
Результаты проведенного анализа свидетельствуют о наличии у ребенка гипохромной микроцитар-ной гипорегенераторной анемии, что в сочетании с данными анамнеза позволяет предполагать ее железодефицитный характер. В биохимическом анализе крови отмечается снижение уровня сывороточного железа 3,3 мкмоль/л, ферритина 40 нг/мл, повышение ОЖСС 65 мкмоль/л. Анализ мочи, исследование кала на скрытую кровь, ультразвуковое исследование брюшной полости патологии не выявили. Таким образом, у мальчика была диагностирована железодефицитная анемия средней степени тяжести. После купирования симптомов ОРВИ ребенок был выписан домой с рекомендацией приема препаратов железа.
Терапия анемических состояний не должна заключаться лишь в попытках нормализации уровня гемоглобина. Как видно из представленных клинических примеров, в первом и втором случаях дети нуждались в специализированном гематологическом обследовании и лечении. Несвоевременная постановка диагноза и назначение препаратов железа этим пациентам могли бы привести к прогресси-рованию основного заболевания и ухудшению прогноза для ребенка. Тем не менее, следует отметить, что гематоонкологические заболевания и гемолитические анемии в практике педиатра встречаются не очень часто, а в большинстве случаев врачу приходится сталкиваться именно с железодефицит-ными анемиями.
По данным ВОЗ, железодефицит-ные состояния занимают первое место среди 38 наиболее распространенных заболеваний человека и охватывают более 3 млрд людей на Земле. В России, по различным данным, железодефицитная анемия регистрируется у 6-40% детского населения [6, 7].
Таблица 5. Причины железодефицитной анемии у детей
Причины ЖДА
Нарушение маточно-плацентарного кровообращения, плацентарная недостаточность (токсикозы, угроза прерывания и перенашивание беременности, гипоксический синдром, острые или обострение соматических и инфекционных заболеваний)
Что такое крапивница? Причины возникновения, диагностику и методы лечения разберем в статье доктора Меркуловой Ирины Юрьевны, аллерголога со стажем в 12 лет.
Над статьей доктора Меркуловой Ирины Юрьевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Крапивница — одно из распространённых заболеваний в мире, характеризующееся кожными высыпаниями в виде волдырей. Иногда крапивница сопровождается ангионевротическим отёком (отёком Квинке — частным случаем крапивницы, т. н. гигантская крапивница). [1] Крапивница — самостоятельное заболевание, и её следует отличать от тех случаев, когда волдыри могут служить только симптомом других состояний, которые к ней не относятся: острой анафилактической реакции, при проведении кожных скарификационных проб и т. д . [2]
Причинами возникновения крапивницы могут служить:
- лекарственные препараты (антибиотики, витамины, НПВС, иАПФ, рентгеноконтрастные вещества);
- продукты питания (рыба, ракообразные, орехи, молоко, мёд, пищевые добавки, фрукты, специи при перекрёстной аллергии у пациентов с сезонными и круглогодичными аллергическими ринитами, аллергией на латекс);
- укусы насекомых;
- паразиты (простейшие, гельминты);
- аэроаллергены (пыльца деревьев и трав, шерсть и выделения животных, бытовая или книжная пыль, плесень),
- вирусные, бактериальные, грибковые инфекции (ЛОР-органов, мочеполовой системы, пищеварительной системы, в т.ч. хеликобактерная);
- химические вещества (соли, краски, строительные и ремонтные смеси, косметика);
- латекс (часто у медицинских работников, а также тех, кто вынужден часто пользоваться изделиями из латекса по роду своей деятельности);
- психогенные факторы;
- физическая нагрузка (в т.ч. профессиональный спорт);
- аутоиммунные заболевания (если есть системная красная волчанка, аутоиммунный тиреоидит, ревматоидный артрит и т. д.);
- новообразования;
- генетические факторы;
- УФ-излучение;
- температура (высокая и низкая);
- давление (при сдавлении кожи тугой одеждой, сумками/ранцами, ремнями, в т. ч. у профессиональных спортсменов);
- вибрация (часто у тех, кто по профессиональной необходимости вынужден иметь дело с вибрацией);
- обычная вода. [2]
Если причина не может быть идентифицирована даже после детального сбора анамнеза и проведения аллергологических тестов, то такую крапивницу называют идиопатической. Хроническая идиопатическая крапивница может быть связана с заболеваниями щитовидной железы, гормональным дисбалансом и в очень редких случаях с раковой опухолью. Даже если крапивница хроническая, она, скорее всего, пройдёт со временем.
Что такое нервная крапивница
Психогенные факторы, такие как стресс и яркие эмоции, могут провоцировать развитие острой крапивницы. Также они могут приводить к обострению хронической формы заболевания.
При таком многообразии провоцирующих факторов у трети пациентов причины крапивницы остаются неизвестными. Это связано с несовершенством диагностических возможностей и является предметом научного поиска для учёных по всему миру. [1]
Заразна ли крапивница
Крапивница не заразна и от человека к человеку не передаётся.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы крапивницы
Основные симптомы крапивницы:
- кожный зуд;
- высыпания на коже в виде волдырей.
Зуд кожи бывает разной интенсивности — от незначительного зуда до нестерпимого, особенно вечером и ночью. Волдыри могут быть различной формы, сливаться между собой, быть абсолютно любого диаметра (от нескольких миллиметров до нескольких десятков сантиметров), и появляться на любом участке кожи и иногда слизистых. Чаще бледные в центре с покраснением по периферии. В местах скопления большого количества рыхлой подкожно-жировой клетчатки (веки, уши, губы, пальцы, половые органы) крапивница может проявляться в своей гигантской форме — в виде отека Квинке. [2]
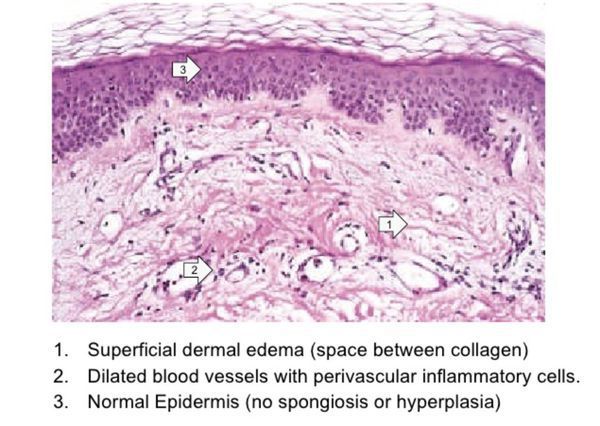
Главное отличие высыпаний — это их мономорфность, т. е. сыпь на коже при крапивнице всегда представлена только волдырём. Волдырь — это локальный отёк кожи (мини-отёк Квинке), который бледнеет при надавливании на него. Следующая отличительная черта высыпаний при крапивнице — это то, что волдыри бесследно исчезают в течение 1-2 суток. Это главные отличительные диагностические черты, которые не позволяют перепутать крапивницу с любыми другими заболеваниями, сопровождающимися высыпаниями на коже. Редко интенсивные высыпания могут сопровождаться незначительным повышением температуры тела, снижением давления, слабостью, болями в области эпигастрия или живота схваткообразного характера, жидким стулом. [1]
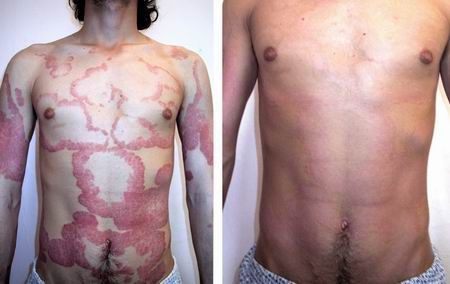
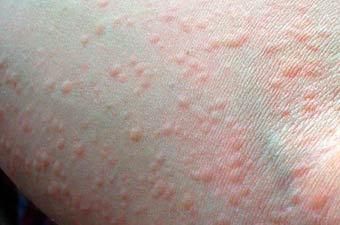
Крапивница у детей
По приблизительным данным, заболевание встречается у 0,3 − 7 % детей [11] . Симптомы крапивницы у них одинаковы со взрослыми.
Патогенез крапивницы
В основе любой крапивницы лежит активация тучных клеток с их дальнейшей дегрануляцией и высвобождением медиаторов.
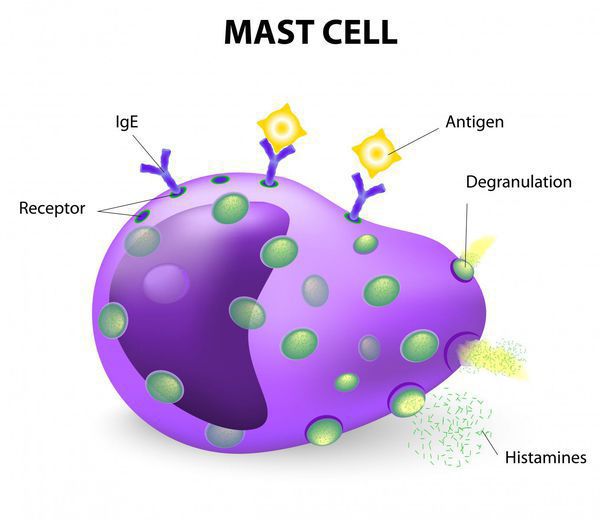
К активации тучных клеток приводят различные механизмы:
1. иммунные (с участием иммунной системы) с вовлечением медиаторов — гистамина, лейкотриенов, брадикинина, простогландинов, ФАТ и т. д. В зависимости от антигена (провоцирующего фактора) развивается крапивница:
- аллергическая (атопическая) при контакте с пищевыми и аэроаллергенами;
- инфекционно-аллергическая при наличии вирусной, грибковой или бактериальной инфекции;
- аутоиммунная при наличии аутоиммунного тиреоидита, системных заболеваний.
2. псевдоаллергические, неиммунные (реализуемые без участия иммунной системы) под влиянием лекарственных препаратов, продуктов-гистаминлибераторов (шоколад, кофе, клубника, копчёности), физического воздействия (высокие и низкие температуры, давление, инсоляция, вибрация и т. д.), ядов насекомых, химических веществ, воды и т. д. [2]
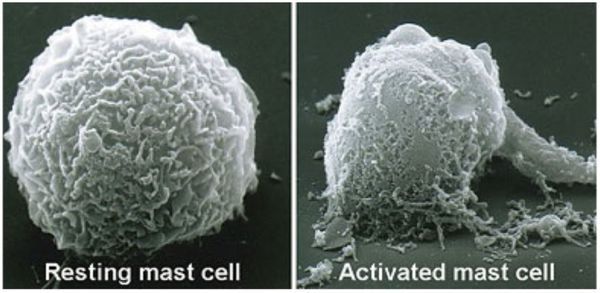
Тучных клеток, т. е. тех, которые реализуют клинические проявления болезни, при хронической крапивнице в организме больного человека в 10 раз больше по сравнению со здоровым. И они чересчур «отзывчивы» к провоцирующему фактору даже при его минимальной активности. Это состояние называется «феномен преходящей гиперреактивности» тучных клеток. [1]
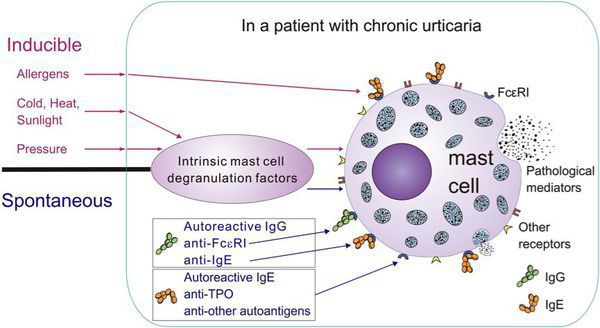
Классификация и стадии развития крапивницы
Выделяют иммунные (в т. ч. IgE-опосредованные), неиммунные, аутоиммунные и смешанные механизмы развития крапивницы.
IgE-опосредованная крапивница связана с выработкой иммуноглобулинов, специфических к аллергену. Такой механизм характерен для острой аллергической крапивницы и встречается чаще всего.
Не-IgE-опосредованная крапивница возникает без выработки специфических иммуноглобулинов. Предполагается, что при этом происходит стимуляция Т-лимфоцитов (клеток иммунной системы) и выработка цитокинов — сигнальных белков, усиливающих иммунный ответ и воспалительную реакцию.
Механизм развития крапивницы при воздействии физических факторов, например тепловых, связан с нарушением нейроиммунной регуляции.
Виды крапивницы по длительности течения:
- острая крапивница (менее 6 недель);
- острая рецидивирующая (длительность ремиссии больше длительности обострения, длительность обострения менее 6 недель);
- хроническая крапивница (более 6 недель). [2]
По степени активности крапивница бывает: [2]
Кроме того, крапивница может быть проявлением ряда заболеваний: наследственного ангионевротического отёка, уртикарного васкулита, пигментной крапивницы (мастоцитоз), семейной холодовой крапивницы (васкулита) и т. д. [2]
Осложнения крапивницы
- отёк Кивнке, или ангионевротический отёк в области гортани с риском развития асфиксии;
- анафилактический шок и другие варианты анафилактической реакции;
- тяжёлые формы крапивницы и ангионевротического отёка, устойчивые к лечению в амбулаторных условиях. [1]
Диагностика крапивницы
Чтобы диагностировать крапивницу, не требуется специфической лабораторной диагностики, в то время как выявление причин заболевания может этого потребовать. [3]
В первую очередь нужно как можно раньше обратиться к врачу аллергологу-иммунологу. Если на время визита высыпаний нет — постараться предоставить врачу фотографии высыпаний/отёков для наибольшей информативности (при условии, что клинические проявления не были тяжёлыми и не требовали экстренной помощи во время фотофиксации).
Врач аллерголог-иммунолог во время приёма соберет подробный анамнез заболевания, анамнез жизни, аллергоанамнез, проведёт физикальное обследование (осмотр, измерение АД, ЧСС, ЧДД, температуры тела, послушает сердце и лёгкие, пропальпирует периферические лимфоузлы, живот). В большинстве случаев этого комплекса диагностики будет достаточно для постановки диагноза и подбора терапии. [2]
Более чем в 90% случаев острая крапивница купируется в течение двух недель и не требует специального обследования, за исключением тех случаев, когда провоцирующий агент установлен. [1]
Какие анализы сдают при крапивнице
Если наблюдаются частые рецидивы острой крапивницы или есть хроническое заболевание, потребуются:
- общий анализ крови с лейкоцитарной формулой и подсчётом СОЭ;
- исследование некоторых биохимических показателей крови;
- обследование на наличие вирусных гепатитов В, С;
- проведение провокационных тестов (кубик льда при подозрении на холодовую крапивницу, горячая грелка при тепловой, водный компресс при аквагенной, тест с физической нагрузкой при подозрении на холинергическую крапивницу и т. д.);
- определение показателей антител к тиреоидной пероксидазе и тиреоглобулину с проведением внутрикожной пробы с аутологичной сывороткой;
- скарификационные пробы с неинфекционными аллергенами и/или наличие специфического иммуноглобулина Е в крови к какому-либо аллергену. [2]
При необходимости дальнейшего диагностического поиска будет целесообразным проведение:
- УЗИ внутренних органов (щитовидная железа, брюшная полость, малый таз);
- ФГДС или рентгеноскопии желудка;
- рентгенологического исследования органов грудной клетки и придаточных пазух носа;
- вирусологического или бактериологического обследования на наличие инфекционных агентов;
- анализа уровня антител к белку Cag A хеликобактера, лямблиям, гельминтам;
- ревмопробы (АНФ, АТ к ДНК, СРБ);
- исследования компонентов комплемента С3, С4 и т. д. [3]
Важным диагностическим тестом у пациентов с крапивницей являются кожные пробы. [9] Они информативны у пациентов с атопической крапивницей и отрицательны у пациентов с псевдоаллергической (при соблюдении сроков проведения тестов и сопутствующей подготовки к тестированию). [5] Также информативен билирубиновый тест на фоне элиминационной пробы (проводят в стационаре, назначается лечебный голод с приёмом только воды, душем и очистительными клизмами). При положительном результате элиминации, уменьшении или купировании симптомов подтверждают аллергический генез крапивницы. У пациентов с аллергической крапивницей уровень билирубина снижен или в пределах нормы, у пациентов с псевдоаллергической крапивницей — повышен. [4]
Лечение крапивницы
Лечение крапивницы состоит из нескольких этапов:
- Элиминация или устранение провоцирующих факторов, триггеров (отменить или заменить лекарственные препараты, избегать перегрева, переохлаждения, инсоляции, отказаться от тесной одежды и не носить тяжести, минимизировать физическую нагрузку и т. п.);
- Выявление и лечение очагов хронической инфекции у профильного специалиста;
- Соблюдение гипоаллергенной диеты (при устранении продукта-аллергена улучшение наступает через 1-2 суток при атопической крапивнице и через 2-3 недели при псевдоаллергической);
- Медикаментозное лечение крапивницы в соответствии с четырьмя линиями терапии в зависимости от эффекта (блокаторы Н1-гистаминовых рецепторов, антилейкотриеновые препараты, анти-IgE-препараты, и т. д.); [10] Лекарства назначает лечащий врач в зависимости от симптомов пациента. Антигистаминные средства бывают двух поколений:
- препараты первого поколения для лечения крапивницы не используются;
- препараты второго поколения — основный метод лечения крапивницы, к ним относятся, например, дезлоратадин и левоцетиризин;
- препараты третьего поколения не существуют, упоминание о них — это маркетинговый ход.
- Вспомогательная терапия, при неэффективности классической — блокаторы Н2-гистаминовых рецепторов, антидепрессанты, стабилизаторы мембран тучных клеток, системные ГКС, иммунодепрессанты, фотодесенсибилизаторы, гистаглобулин, плазмаферез и т. д.; [6]
- Глюкокортикоиды применяют при тяжёлом течении крапивницы. Например при развитии ангионевротического отёка может быть назначен преднизолон.
- Аллерген-специфическая иммунотерапия при подтверждённом аллергическом генезе крапивницы — наиболее эффективный метод лечения;
- Если развивается асфиксия на фоне ангионевротического отёка гортани, может потребоваться экстренная интубация или трахеостомия. [3]
- Энтеросорбенты — убедительных данных об их эффективности при крапивнице нет, в клинических рекомендациях и международных стандартах они не упоминаются.
Стоит помнить, что любая местная терапия в виде крема или мази при крапивнице неэффективна и применяться не должна.
Как снять зуд от крапивницы
Уменьшить зуд можно при помощи антигистаминных препаратов второго поколения, антилейкотриеновых и анксиолитических средств, например "Атаракса". Все препараты применяют только по назначению врача и по рекомендованным схемам. Лечение крапивницы народными средствами бесполезно и опасно.
Нужно ли при крапивнице вызывать скорую помощь
Немедленная медицинская помощь и госпитализация потребуются:
- При тяжёлых формах острой крапивницы и ангионевротического отёка в области гортани с риском удушья. В таких случаях пациент теряет голос, его дыхание становится свистящим и прерывистым.
- При развитии анафилаксии — острой, угрожающей жизни аллергической реакции. Её симптомы включают хрипы, одышку и снижение артериального давления.
Также госпитализация необходима при обострениях хронической крапивницы и ангионевротического отёка, устойчивых к амбулаторному лечению.
Неотложная помощь при отёке Квинке
При отёке Квинке следует:
- немедленно прекратить контакт с предполагаемым провоцирующим агентом;
- вызвать скорую;
- принять одну таблетку антигистаминного препарата второго поколения.
Особенности питания и образа жизни при хронической крапивнице
Рекомендуется не употреблять подтверждённые и предполагаемые аллергены, пищевые добавки и неизвестные ароматизаторы.
Больным с доказанной непереносимостью ацетилсалициловой кислоты следует исключить приём нестероидных противовоспалительных препаратов (НПВП). Остальным пациентам с крапивницей нельзя принимать ацетилсалициловую кислоту и НПВП при обострении заболевания.
Рекомендуется отказаться от тесной одежды и подъёма тяжестей, избегать длительных пеших походов.
Также важно исключить факторы, способствующие переохлаждению: одежду не по сезону, холодные пищу и напитки, длительное пребывание на морозе.
При солнечной крапивнице нужно избегать прямого воздействия солнца, ношения открытой одежды и отказаться от отдыха в южных регионах.
Можно ли принимать ванную или душ при крапивнице
Ограничений на водные гигиенические процедуры при крапивнице нет.
Прогноз. Профилактика
Прогноз при острой крапивнице, как правило, благоприятный. На исход заболевания влияют такие факторы как возраст, пол, длительность болезни, сочетание с ангионевротическими отёками, наличие провоцирующих факторов, ответ на медикаментозную терапию и элиминационные мероприятия. [8] При осложнении крапивницы асфиксией, вызванной отёком гортани, тяжёлыми анафилактическими реакциями, устойчивостью тяжёлых форм крапивницы и ангионевротического отёка к терапии прогноз может быть неблагоприятным (вплоть до смертельного исхода). Это особенно опасно, если медицинская помощь недоступна, невозможно быстро начать экстренные лечебные мероприятия и т. д. [4]
За какое время можно вылечить крапивницу
В течение 6 недель острая крапивница купируется более чем у 75 % пациентов. В хроническую форму болезнь переходит у четверти пациентов [7] . Такая форма крапивницы длится дольше 6 недель, иногда несколько лет, с периодами ремиссии или без них.
С целью профилактики неблагоприятных исходов крапивницы (при наличии соответствующих симптомов) необходимо:
- незамедлительно обратиться к врачу (первичного звена, врачу аллергологу-иммунологу, в экстренных ситуациях — вызвать скорую помощь);
- соблюдать рекомендации по диете, организации быта, образу жизни;
- неукоснительно соблюдать рекомендации врача по лечению, не бросать принимать препараты при первых признаках улучшения, не менять схему, кратность и дозу препаратов, рекомендованных врачом;
- иметь в домашней и автомобильной аптечке, в сумочке препараты для экстренного купирования симптомов, особенно если крапивница сопровождается ангионевротическим отёком, приобрела тяжёлую форму, не получается полностью исключить провоцирующий фактор;
- предупредить родственников/близких/друзей о вашем заболевании и принципах помощи, пока скорая будет спешить на помощь. [2]
Можно ли делать прививки, если у ребёнка крапивница
Хроническая крапивница — не причина отказываться от прививок. При её обострении и острой форме болезни следует дождаться ослабления симптомов и потом вакцинироваться.
«ФАРМАТЕКА»; Актуальные обзоры; № 13; 2012; стр. 9-14.
Д.Т. Абдурахманов
Кафедра терапии и профболезней ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздравсоцразвития РФ, Москва
Обсуждается проблема железодефицитной анемии (ЖДА), развивающейся в т. ч. при заболеваниях желудочно-кишечного тракта. Представлены сведения, касающиеся причин возникновения ЖДА, патогенеза, симптоматики, диагностики и лечения данной патологии. Особое внимание уделено препарату Феринжект (железа карбоксимальтозат), который применяется в комплексной терапии пациентов с ЖДА, обусловленной воспалительными заболеваниями кишечника.
Ключевые слова: железодефицитная анемия, дефицит железа, ферротерапия, железа карбоксимальтозат
The article discusses the problem of iron deficiency anemia (IDA), which develops against the background of many diseases, including gastrointestinal diseases. The data on the causes of IDA, pathogenesis, symptoms, diagnosis and treatment of this disease are presented. Particular attention is paid to the drug Ferinject (ferric carboxymaltosate) used for the treatment of IDA in patients with inflammatory bowel diseases.
Key words: iron deficiency anemia, iron deficiency, ferrotherapy, ferric carboxymaltosate
Наиболее частая в популяции причина анемии — дефицит железа в организме. По данным отчета Всемирной организации здравоохранения (ВОЗ) о состоянии здоровья за 2002 г., железодефицитная анемия (ЖДА) входит в десятку глобальных факторов риска развития нетрудоспособности. Так, показано, что ЖДА встречается среди 30 % населения планеты [1]. В США ЖДА наблюдается среди 5-12 % небеременных женщин и 1-5 % мужчин [2].
Метаболизм железа в организме
Общее количество железа в организме взрослого человека составляет около 3,5-4,0 г, в среднем 50 и 40 мг/кг у мужчин и женщин соответственно. Основная часть железа входит в состав гемоглобина эритроцитов (около 2,5 г), значительная часть железа (около 0,5—1,0 г) депонируется в составе ферритина или входит в состав гемсодержащих и других ферментов (миоглобина, каталазы, цитохромов) организма (около 0,4 г) и небольшая часть железа (0,003—0,007 г) находится в связанном с трансферрином состоянии в крови.
Баланс железа в организме поддерживается соответствием количества поступающего железа его потерям. В пище железо присутствует в составе гема или как негемовое железо. Ежедневно с пищей (стандартный пищевой рацион) в организм человека поступает 10—20 мг железа, из которого в норме в кишечнике всасывается около 10 % (от 3 до 15 %), что компенсирует суточные потери железа, главным образом при слущивании эпителиальных клеток. Организм обеспечивает баланс железа в организме, регулируя процесс его всасывания в кишечнике. В случае развития дефицита железа организм увеличивает процент всасываемого железа (может достигать 25 %), при избытке — уменьшает [3]. В этом процессе ключевое значение придают гепсидину — белку, который синтезируется в печени. Поступление с пищей или выведение железа, как правило, вне контроля организма.
Около 25—30 мг железа ежедневно реутилизируется после разрушения (вследствие старения) эритроцитов в селезенке и поступает снова в костный мозг для синтеза новых эритроцитов. Железо, которое всасывается в кишечнике, предварительно на поверхности энтероцита восстанавливается с участием ферроредуктаз из трехвалентного (Fe 3+ ) в двухвалентнтное (Fe 2+ ), затем с помощью специфического переносчика — транспортера двухвалентных металлов (DMT1) поступает в цитоплазму [4]. Железо в составе гема (содержится в мясе, рыбе) всасывается напрямую. В дальнейшем двухвалентное железо с помощью другого переносчика, ферропортина (также мобилизует железо из ферритина), секретируется в кровь, где снова окисляется до трехвалентного (при участии белка гефестина) и связывается с плазменным белком трансферрином [5]. Трансферрин осуществляет транспорт железа в костный мозг, где оно утилизируется для синтеза эритроцитов, или преимущественно в печень, где железо депонируется в составе ферритина (рис. 1) [6].
При снижении запасов железа, гипоксии, анемии, усиленном эритропоэзе в печени снижается синтез гепсидина, что усиливает всасывание железа в кишечнике, при хроническом воспалении синтез гепсидина в печени увеличивается и, соответственно, всасывание железа в кишечнике снижается.
Рис 1. Регуляция всасывания железа в кишечнике [Guidi G.C., Santonastaso C.L., 2010]
Ферритин — ключевой белок, отражающий запасы железа в организме. Он депонирует железо в нетоксической форме, которое при необходимости мобилизуется. В среднем одна молекула ферритина содержит до 4500 атомов железа. Главным образом железо депонируется в печени, костном мозге и селезенке. Снижение уровня ферритина в сыворотке крови является достаточно надежным показателем дефицита железа в организме, его увеличение, как правило, указывает на перегрузку организма железом. В то же время необходимо помнить, что ферритин относится к белкам острой фазы воспаления, поэтому увеличение его содержания в крови может быть следствием активного воспалительного процесса, а не телько избытка железа. В ряде случаев некоторые злокачественные опухоли обладают способностью синтезировать и секретировать в кровь большое количество ферритина (в рамках паранеопластического синдрома). В норме содержание ферритина в сыворотке крови составляет 30-300 нг/мл.
Причины железодефицитной анемии
Выделяют три глобальные причины развития дефицита железа в организме (рис. 2):
1. Недостаточное поступление с пищей или повышенная потребность.
2. Нарушение всасывания железа в кишечнике.
3. Хронические потери крови.
Рис 2. Основные причины железодефицитной анемии
В популяции наиболее частой причиной ЖДА является недостаточное поступление с пищей: по данным ВОЗ, от четверти до трети населения в мире хронически голодают из-за нехватки продуктов питания, особенно мясной пищи. Однако в клинической практике среди основных причин ЖДА выделяют хронические потери крови, прежде всего из желудочно-кишечного тракта.
Клиническая картина
При ЖДА наблюдаются общие для всех анемий проявления циркуляторно-гипоксического синдрома:
Кроме того могут встречаться специфические признаки тканевого дефицита железа:
Диагностика
Лабораторная диагностика ЖДА основана на изучении обмена железа и выявлении его дефицита. Выделяют ряд признаков, указывающих на железодефицитный характер анемии (табл. 1).
Таблица 1
Лабораторные признаки дефицита железа и ЖДА
| Параметры | Значения при ЖДА | Норма |
| Железо сыворотки, мкг/дл | < 50 | 50-180 |
| Насыщение трансферрина железом, % | < 20 | 20-50 |
| Ферритин сыворотки, нг/мл | 30-300 | |
| Средний объем эритроцита (MCV), мкм 3 | < 80 | 80-100 |
| Гипохромные эритроциты, % | > 5 | < 5 |
| Ретикулоциты, тыс/мкл | < 40 | 40-100 |
| Растворимые рецепторы к трансферрину (sTfR), мг/л | Повышены | 0,76-1,76 |
Как правило, клинико-лабораторные проявления анемии (главным образом снижение гемоглобина) развиваются при потере организмом не менее 20— 30 % запасов железа.
Дифференциальный диагноз
ЖДА наиболее часто необходимо дифференцировать с анемией хронических заболеваний и талассемией. Кроме того, могут наблюдаться смешанные формы анемии (сочетание дефицита железа с дефицитом фолиевой кислоты и/или витамина В12, сочетание ЖДА и анемии хронических заболеваний и др.).
Выявление анемии, а также установление ее железодефицитного характера, как правило, в большинстве случаев не представляет сложностей. Наиболее трудным может оказаться установление причины дефицита железа, которое часто требует длительного дифференциально-диагностического поиска, но является необходимым условием успешного лечения и улучшения прогноза заболевания. Сам по себе дефицит железа и вызванная им анемия, как правило, не угрожают жизни больного (за исключением анемической комы, которая, впрочем, в настоящее время встречается достаточно редко). Организм достаточно хорошо адаптируется к развитию дефицита железа, и клинические проявления анемии обычно развиваются только при повышенных функциональных потребностях организма (стрессе, повышенной физической нагрузке, беременности, у девушек в период становления менструального цикла и др.). Поэтому очень часто анемия протекает бессимптомно и в большинстве случаев выявляется при случайном или профилактическом обследовании. Однако заболевания, которые обусловливают развитие ЖДА, в частности злокачественные опухоли, могут быть опасными, угрожающими здоровью и жизни пациента. Поэтому независимо от выраженности клинических проявлений и тяжести ЖДА выявление причины дефицита железа является обязательным условием полноценного обследования пациента.
ЖДА при заболеваниях желудочно-кишечного тракта
Заболевания желудочно-кишечного тракта (ЖКТ) являются одной из основных причин развития ЖДА, что обусловлено нарушением всасывания железа в кишечнике или его потерями вследствие эрозивно-язвенных, опухолевых или аутоиммунных воспалительных поражений слизистой оболочки кишечника (табл. 2) [7].
Таблица 2
Заболевания ЖКТ, сопровождающиеся развитием ЖДА [Zhu A. и соавт., 2010]
| Верхние отделы ЖКТ | Нижние отделы ЖКТ | Весь ЖКТ |
| Язва желудка Язва 12-перстной кишки Рак желудка Грыжа пищеводного отверстия Эрозивный эзофагит Эрозивный гастрит Целиакия Атрофический гастрит Хронический гастрит, ассоциированный с Helicobacter pylori Операции на желудке | Аденома толстой кишки Рак толстой кишки Язвенный колит Идиопатическая язва слепой кишки | Болезнь Крона Телеангиэктазии сосудов ЖКТ Застойная гастро- и колонопатия при портальной гипертензии Паразитарные инфекции НПВС-ассоциированные гастропатия и энтеропатия |
Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия.
В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки.
При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС.
У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний).
При этом дефицит железа становится следствием нескольких причин:
Лечение
Лечение ЖДА включает прежде всего устранение причины дефицита железа (если это возможно) и прием препаратов железа (ферротерапия). Существует более 100 различных препаратов железа, в РФ наиболее часто используют около 10-15 лекарственных форм.
Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике.
При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа).
Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы.
Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]:
недостаточное поступление железа;
нерегулярный прием препаратов железа;
недостаточное содержание железа в принимаемом препарате.
Нарушение всасывания железа:
Продолжающиеся потери крови или повышенная потребность в железе:
Сопутствующие заболевания или состояния:
Неправильный диагноз или наличие других причин анемии:
Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа:
Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран.
Эффективность и безопасность Феринжекта при внутривенном введении были продемонстрированы при лечении ЖДА и в ряде других клинических ситуаций (у больных на гемодиализе, в послеродовом периоде, при тяжелом маточном кровотечении) 16.
Переливание компонентов крови (эритроцитарной массы) для лечения ЖДА применяется только при угрожающей жизни (анемической коме) или тяжелой анемии (Hb < 60 г/л), сопровождающейся признаками декомпенсации.
ЛИТЕРАТУРА
Гипотиреоз - симптомокомплекс изменений со стороны различных органов и систем, обусловленный снижением уровня тиреоидных гормонов.
Качество же жизни пациентов с гипотиреозом, постоянно получающих заместительную терапию левотироксином, незначительно отличается о такового для лиц без гипотиреоза. Сам гипотиреоз становится для пациента образом жизни, а не заболеванием.
Однако при отсутствии своевременного адекватного лечения гипотиреоза возрастает опасность развития осложнений. Гипотиреоидная кома (ГК) - это редкое, угрожающее жизни осложнение гипотиреоза. В первую очередь развивается у пожилых пациентов долгое время не- или плохо леченных. Пациенты с ГК умирают преимущественно от дыхательной и сердечной недостаточности, в некоторых случаях - от тампонады сердца. Даже при своевременно начатой энергичной терапии 40% больных погибают.
Клинические симптомы гипотиреоза
Клинические симптомы гипотиреоза развиваются у больного с постепенным нарастанием. Наиболее часто гипотиреоз характерен для пациентов, оперированных на щитовидной железе (первичный послеоперационный гипотиреоз).
Врач должен заподозрить наличие у пожилого больного синдром гипотиреоза и провести определение уровня тиреотропного гормона (ТТГ) в сыворотке крови в том случае, если пациент имел какое-либо заболевание щитовидной железы в анамнезе или получал лекарства, которые могут провоцировать развитие гипотиреоза. Кроме того, наличие запоров, резистентных к обычному лечению, кардиомиопатии, анемии неясного генеза, деменции, должно быть причиной исключения гипотиреоза у пожилого больного.
Лабораторная диагностика
Лабораторными параметрами для диагностики гипотиреоза являются определение базального (не стимулированного) ТТГ и показателей свободных Т4 и Т3. Нормальный базальный уровень ТТГ исключает гипотиреоз. При повышенном базальном ТТГ диагноз подтверждают обнаружением пониженных концентраций свободных Т4 и Т3.
Ошибки диагностики гипотиреоза
Диагноз гипотиреоза зачастую бывает несвоевременным, так как в начальной его стадии выявляемые симптомы крайне неспецифичны. Кроме того, синдром гипотиреоза может имитировать различные нетиреоидные заболевания, что связано с полиорганностью поражений, обнаруживаемых в условиях дефицита гормонов щитовидной железы. Очень часто проявления гипотиреоза у пожилых людей рассматриваются врачом и пациентом как признаки нормального старения. Действительно, такие симптомы, как сухость кожи, алопеция, снижение аппетита, слабость, деменция и др., аналогичны проявлениям процесса старения. Типичные симптомы гипотиреоза выявляются только у 25-50% пожилых людей, остальные же имеют либо крайне стертую симптоматику, либо гипотиреоз клинически реализован в виде какого-либо моносимптома.
Клиническая диагностика
| Клинические симптомы гипотиреоза | |
| Общие симптомы Усталость, утомляемость, слабость Увеличение массы тела, зябкость Сердечно-сосудистые симптомы Синусовая брадикардия Сердечная недостаточность Кардиомегалия Перикардит Артериальная гипотония или парадоксальная гипертония Органы дыхания Дыхательная недостаточность, гиперкапния Кожа и ее производные Сухость кожи, выпадение волос Утолщение ногтей Выпадение латеральных частей бровей Окраска кожи бледная с желтоватым оттенком Нервная система Апатия, сонливость, нарушение концентрации внимания Ухудшение памяти Депрессивные психозы Ступор и кома Гипорефлексия | Костно-мышечная система Мышечная слабость Мышечная атрофия Нарушение скелетообразования у детей Желудочно-кишечный тракт Отсутствие аппетита Запоры, мегаколон, илеус Половые органы У женщин: нарушение цикла по типу аменореи или меноррагии Бесплодие У мужчин: отсутствие либидо, снижение потенции, гинекомастия Обмен веществ Снижение основного обмена Увеличение массы тела, ожирение Высокий холестерин, гипогликемия Задержка жидкости с увеличением объема языка, отеки лица, особенно век Лабораторные данные Гипонатриемия Анемия Повышение уровня креатинкиназы Щитовидная железа Зоб или его отсутствие |
Гипотиреоидная кома
Разрешающими факторами являются тяжелые сопутствующие заболевания, операции, травмы, прием седативных препаратов и наркотиков, а также переохлаждение.
Основу патогенеза ГК составляет альвеолярная гиповентиляция с последующей гипоксией жизненно важных органов, следствием чего является снижение температуры тела, брадикардия и гипогликемия. При несвоевременном оказании помощи возможен летальный исход. Летальность при ГК составляет от 60 до 90%.
У пациента усиливаются все симптомы гипотиреоза. Выражены сонливость, дезориентация, коматозное состояние. Температура тела снижена до 34-35 ° С, возникает брадикардия. Кожные покровы холодные, пастозные.
Основным симптомом ГК является снижение температуры тела. Кома сопровождается прогрессирующими изменениями со стороны ЦНС, угнетением всех типов рефлексов. Изменения со стороны ЦНС ведут к нарастанию брадикардии, снижению артериального давления и гипогликемии.
Нарушения со стороны сердечно-сосудистой системы, развивающиеся у больного с ГК, нередко являются причиной летального исхода. Показатели периферической гемодинамики одними из первых реагируют на изменения концентрации гормонов щитовидной железы. Гипотиреоз сопровождается уменьшением частоты сердечных сокращений (ЧСС). Брадикардия, возникающая при гипотиреозе, обратима при достижении эутиреоза.
Другим эффектом при гипотиреозе является изменение общего периферического сопротивления сосудов (ОПСС). Гипотиреоз вызывает повышение ОПСС, с чем в определенной мере связано развитие диастолической артериальной гипертензии (АГ). Диастолическая гипертензия при гипотиреозе является распространенным явлением. У больных с гипотиреозом и наличием АГ содержание альдостерона и ренина в плазме крови снижено, т.е. диастолическая гипертензия при гипотиреозе носит гипорениновый характер.
Предполагаемыми причинами нарушения вазодилатирующей функции при гипотиреозе являются: снижение генерации вазодилатирующих субстанций и/или резистентность к ним сосудистых гладкомышечных клеток; снижение концентрации предсердного Na-уретического пептида.
Состояние гипотиреоза характеризуется уменьшением числа β-адренорецепторов, с чем связывают более низкую вероятность развития аритмий. Однако установлено, что у лиц с гипотиреозом секреция норадреналина и содержание его в плазме крови повышено. Норадреналин, являясь в основном стимулятором адренорецепторов, может способствовать спазму коронарных артерий.
Гипотиреоз характеризуется снижением сократительной способности миокарда, уменьшением фракции выброса, развитием сердечной недостаточности. Состояние гипотиреоза также сопровождается пролонгацией диастолы, увеличением времени изоволюметрической релаксации левого желудочка.
Лечение гипотиреоза
Поскольку ГК является результатом либо отсутствия лечения гипотиреоза, либо проведения неадекватной терапии данного синдрома и представляет собой крайне тяжелое состояние с высокой летальностью, врач любой специальности должен иметь представление об алгоритмах терапии гипотиреоза и используемых для этого препаратах.
Очень важно вовремя распознать гипотиреоз, который возможно диагностировать всего лишь по одному показателю гормонального анализа - ТТГ, и назначить заместительную терапию Эутироксом. Его отличием от других препаратов тиреоидных гормонов является возможность с легкостью подобрать нужную дозировку - 25,50,75,100, 125 или 150 мкг, что существенно облегчает проведение заместительной терапии гипотиреоза.
Режим дозирования лекарственного препарата
ЭУТИРОКС (левотироксин натрий)
Устанавливают индивидуально в зависимости от показаний, эффекта лечения и лабораторных данных. Всю суточную дозу принимают 1 раз/сут утром, не менее чем за 30 мин до завтрака и запивают жидкостью.
При гипотиреозе в начале лечения назначают в дозе 50 мкг/сут. Дозу увеличивают на 25-50 мкг каждые 2-4 недели до достижения признаков эутиреоидного состояния.
У больных с длительно существующим гипотиреозом, микседемой и, особенно, в случаях, когда имеются заболевания сердечно-сосудистой системы, начальная доза препарата должна составлять не более 25 мкг/сут. У большинства пациентов эффективная доза не превышает 200 мкг/сут. Отсутствие адекватного эффекта при назначении 300 мкг/сут свидетельствует о мальабсорбции либо о том, что пациент не принимает назначенную дозу Эутирокса. Адекватная терапия обычно приводит к нормализации уровня тиреотропного гормона и тироксина (Т4) в плазме через 2-3 недели лечения.
Представлена краткая информация производителя по дозированию лекарственных средств у взрослых. Перед назначением препарата внимательно читайте инструкцию.
Лечение ГК
Основная задача лечения ГК - восстановление нормальных физиологических функций всех органов и систем, нарушенных вследствие гипотиреоза. Критерием адекватности лечения служит исчезновение клинических и лабораторных проявлений гипотиреоза.
Тяжесть и длительность гипотиреоза являются основными критериями, определяющими тактику врача в момент начала лечения.
Чем тяжелее гипотиреоз и чем дольше он не был компенсирован, тем выше будет общая восприимчивость организма к тиреоидным гормонам, особенно это относится к кардиомиоцитам.
Основные лечебные мероприятия при ГК:
-
1. Заместительная терапия препаратами тиреоидных гормонов (левотироксин).
2. Применение глюкокортикоидов.
3. Борьба с гиповентиляцией и гиперкапнией, оксигенотерапия.
4. Устранение гипогликемии.
5. Нормализация деятельности сердечно-сосудистой системы.
6. Устранение выраженной анемии.
7. Устранение гипотермии.
8. Лечение сопутствующих инфекционно-воспалительных заболеваний и устранение других причин, которые привели к развитию комы.
Лечение ГК проводится в специализированном реанимационном отделении и направлено на повышение уровня тиреоидных гормонов, борьбу с гипотермией, устранение сердечно-сосудистых и нервно-вегетативных нарушений.
В основу лечения ГК положен принцип максимального введения тиреоидных гормонов, в первую очередь левотироксина, через зонд либо капельно, либо внутримышечными инъекциями.
Потребность в левотироксине увеличивается во время беременности. Оценка функции щитовидной железы у беременных женщин, подразумевающая исследование уровня ТТГ и свободного Т4, целесообразна в каждом триместре беременности. Доза препарата должна обеспечивать поддержание низконормального уровня ТТГ.
У женщин с гипотиреозом в постменопаузе, которым назначается заместительная терапия эстрогенами, для поддержания нормального уровня ТТГ может понадобиться увеличение дозы левотироксина.
Читайте также:

