Поражение миокарда при герпетической инфекции
Обновлено: 01.05.2024
Категории МКБ: Герпетическая болезнь глаз (B00.5+), Герпетическая инфекция неуточненная (B00.9), Герпетическая экзема (B00.0), Герпетический везикулярный дерматит (B00.1), Герпетический гингивостоматит и фаринготонзиллит (B00.2), Герпетический менингит (B00.3+) (G02.0*), Герпетический энцефалит (B00.4+) (G05.1*), Диссеминированная герпетическая болезнь (B00.7), Другие формы герпетических инфекций (B00.8)
Общая информация
Краткое описание
Герпетическая инфекция (простой герпес, herpessimplex) – широко распространенная антропонозная вирусная болезнь, вызываемая вирусом простого герпеса 1 и 2 типов, преимущественно контактным механизмом передачи возбудителя, характеризуемая поражением кожи и слизистых оболочек, нервной системы, глаз, мочеполовой системы и других, внутренних органов, склонная к хроническому рецидивирующему течению.
Пользователи протокола: терапевты, врачи общей практики, инфекционисты, невропатологи, дерматовенерологи, акушер-гинекологи, стоматологи, офтальмологи, отоларингологи, урологи, анестезиологи-реаниматологи.
Класс I – польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III – имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию.
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Врожденная (внутриутробная инфекция).
- генерализованную (висцеральную, диссеминированную) ГИ.
- медленная форма герпетической инфекции.
- поражения слизистых оболочек желудочно-кишечного тракта (стоматит, гингивит, фарингит, эзофагит и др.);
- поражения глаз: офтальмогерпес (герпетический конъюктивит, кератит, иридоциклит, неврит зрительного нерва, оптикомиелит и др.);
- генитальный герпес (герпетическое поражение слизистых оболочек полового члена, вульвы, влагалища, цервикального канала и т.д.);
- поражения нервной системы (менингит, энцефалит, менингоэнцефалит, неврит, менингоэнцефалорадикулит, поражения бульбарных нервов и др.);
- Активная стадия инфекции: продуктивная вирусная инфекция, реализация генетической информации завершается образованием вирусного потомства, дочерних вирусных частиц.
- Неактивная стадия инфекции — абортивная вирусная инфекция, реализуется генетическая информация только неструктурных (альфа-) генов без образования новых дочерних частиц вируса.
- Первичная инфекция. Развивается после заражения вирусом неинфицированного ранее лица. В крови пациентов антитела к ВПГ до развития герпетической инфекции не выявляются. Инфекция сопровождается появлением противовирусных антител (сероконверсией), 4-кратным нарастанием концентрации иммуноглобулинов класса G.
- Первичная инфекция с одиночным местом внедрения вируса (например, через слизистую гениталий или ротовой полости).
- Первичная инфекция с множественными входными воротами инфекции (слизистая гениталий, ротовой полости, сосков молочных желез, кожные покровы промежности, ягодиц, внутренней поверхности бедер, перианальной области и т.д.).
- Аутоинокуляция— механический перенос вируса у инфицированного с одного участка на другие участки тела (например, из ротовой полости на гениталии).
- Латентная инфекция — неактивная стадия инфекции. Инфекционный вирус не обнаруживается в биологических материалах (слюне, моче, секретах гениталий). Вирус сохраняется в виде ДНК-белкового комплекса в нервных ганглиях.
- Первый эпизод герпеса: впервые выявленные клинические проявления герпеса у ранее инфицированных лиц.
- Суперинфекция (субклиническая и клиническая): наслоение одной инфекции на другую (например, заражение вирусом простого герпеса 2 типа половым путем лица, страдающим герпетическим стоматитом, вызванным ВПГ-1).
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий [1,2,3,4,5,6]
Основные диагностические исследования, проводимые на амбулаторном уровне:
- определение антител IgM и IgG к вирусу простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2) в сыворотке крови методом ИФА;
- определение ДНК ВПГ методом ПЦР (кровь, мазки со слизистых оболочек, содержимое герпетических пузырьков, СМЖ (в зависимости от локализации герпетических поражений));
- УЗИ плода (у беременных);
- определение антител к ВИЧ методом ИФА;
- офтальмоскопия (при поражении глаз);
- ЭКГ.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные диагностические исследования, проводимые на стационарном уровне:
- определение ДНК ВПГ методом ПЦР при поражении ЦНС, висцеральных и генерализованных формах ГИ (качественный);
- гистологическое исследование биопсийных материалов на ВПГ.
Дополнительные диагностические исследования, проводимые на стационарном уровне (в зависимости от клинической формы):
- биохимическое исследование крови (билирубин и фракции, АЛТ, АСТ, тимоловая проба);
- рентгенография органов грудной клетки;
- ЭГДС и колоноскопия;
- УЗИ органов брюшной полости;
- КТ, МРТ;
- спинномозговая пункция с исследованием СМЖ (маркеры ВПГ, антитела к ВПГ-1/-2, белок, лимфоциты и др.(при поражении ЦНС));
- офтальмоскопия;
- ЭКГ;
- определение антител к ВИЧ методом ИФА.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
Жалобы и анамнез:
Клинические проявления ПГ зависят от локализации патологического процесса и его распространенности, состояния иммунной системы больного и антигенного типа вируса.
- пузырьковые высыпания на коже в области красной каймы губ, вокруг рта, в области крыльев носа, на кистях, в области ягодиц;
Миокардит представляет собой поражение сердечной мышцы преимущественно воспалительного характера, обусловленное опосредованным через иммунные механизмы воздействием инфекции, паразитарной или протозойной инвазии, химических и физических факторов, а также возникающее при аллергических и иммунных заболеваниях.
В данную подрубрику включены:
1. Гриппозный миокардит (острый):
- вирус идентифицирован (J10.8+);
- вирус не идентифицирован (J11.8+).
2. Паротитный миокардит (B26.8+).
Этиология и патогенез
Гриппозный миокардит - вызывается непосредственно вирусом гриппа (Myxovirus influenzae), относящимся к семейству ортомиксовирусов.
Паротитный миокардит - возбудителем инфекции является вирус, который относится к семейству парамиксовирусов. Является РНК-содержащим вирусом.
Эпидемиология
Гриппозный миокардит
В период эпидемии гриппа клинические и инструментальные признаки миокардита обнаруживаются у 1-5% больных. При гриппе типа А миокардит встречается у 9,7% пациентов, при гриппе типа В - у 6,6% (М. Kreunder).
Паротитный миокардит
Единственный источник инфекции - больной человек. Наиболее опасны в плане распространения вируса больные со стертыми или бессимптомными формами паротитной инфекции. Больной становится источником инфекции в последние 2 дня инкубационного периода (в это время вирус может быть найден у него в слюне и крови), а на 3-5 день от начала заболевания он наиболее заразен. После 9 дня заболевания вирусовыделение при паротитной инфекции прекращается.
Основной механизм передачи инфекции - воздушно-капельный. Восприимчивость к паротитной инфекции является высокой, индекс контагиозности Контагиозность - свойство инфекционной болезни передаваться от больных людей и животных здоровым
составляет 70%-85%.
Чаще всего паротитной инфекцией болеют дети в возрасте 7-15 лет. В последние годы увеличилась заболеваемость среди подростков. Мужчины заболевают в 1,5 раза чаще, чем женщины. Дети первых 6 месяцев жизни редко болеют паротитной инфекцией, так как имеют защитный титр антител, переданных от матери.
Клиническая картина
Cимптомы, течение
Выделяют следующие варианты течения вирусных миокардитов:
- острый;
- фатальный с летальным исходом через несколько дней от начала заболевания;
- острый с полным выздоровлением; подострый с обострениями и ремиссиями, с выздоровлением;
- хронический с летальным исходом.
Поражение сердечно-сосудистой системы при паротите проявляется в основном в виде миокардиодистрофии, более редко - в виде миокардита, который обнаруживается прежде всего транзиторными изменениями на электрокардиограмме.
Признаки миокардита выявляют к концу 1-й недели болезни, через 1,5-2 недели на электрокардиограмме отмечают улучшение показателей. Обычно паротитный миокардит не сопровождается клиническими проявлениями или нарушением функции сердца, однако в редких случаях он может закончиться смертью пациента.
Диагностика
1. Электрокардиография: практически всегда выявляются неспецифические изменения сегмента ST и зубца Т, реже – различные аритмии и нарушения АВ-проводимости.
Результаты эндомиокардиальной биопсии подтверждают клинический диагноз миокардита в 17-37% случаев. Сравнительно небольшая частота подтверждения диагноза обусловлена тем, что поражение миокарда, может носить очаговый характер.
Несмотря на высокую информативность биопсия миокарда осуществляется редко из-за высокой стоимости, инвазивности и в связи с низким процентом достоверных результатов.
3. Рентгенография органов грудной клетки не выявляет какие-либо специфические изменения, характерные для миокардитов. Однако метод дает ценную информацию о конфигурации сердца, кардиоторакальном индексе и выраженности легочной гипертензии.
При рентгенологическом исследовании больных миокардитом в 35-90% случаев обнаруживается дилатация сердца (в первую очередь - левого желудочка).
5. Магнитно-резонансная томография миокарда с контрастированием применяется для визуальной диагностики воспалительных процессов. Парамагнитные контрасты (омнискан, галодиамид) накапливаются во внеклеточной жидкости и вызывают изменение интенсивности МР-сигнала, выявляя воспалительный отек. Вывод о наличии или отсутствии миокардита можно сделать после обработки серии изображений миокарда до и после контрастирования. Чувствительность метода составляет 70-75%.
Лабораторная диагностика
В диагностике вирусного миокардита имеет значение выделение вируса из смывов носоглотки, кала и четырехкратное и более нарастание титра противовирусных антител в реакции связывания комплемента (РСК) и реакции торможения гемагглютинации (РТГА) в парных сыворотках (в повседневной практике вирусологические исследования не проводятся).
Следует иметь в виду, что выделение вируса из смывов информативно только в течение 1-ой недели заболевания, а титры противовирусных антител могут сохраняться повышенными в течение года.
Гриппозный миокардит
Специфические лабораторные диагностические методы предназначены для ранней (экстренной) или ретроспективной диагностики гриппа.
Первоочередные методы по скорости получения результатов (результат анализа может быть получен через 3-5 часов с момента доставки материала в лабораторию):
1. Иммунофлюоресцентный метод (РИФ) - выявляет вирусные антигены в клетках верхних дыхательных путей после взаимодействия антигенов со специфическими антителами, меченными флюорохромом. Формирование специфического комплекса антиген-антитело проявляется ярким красным свечением в поле зрения микроскопа.
2. Выявление адсорбции груженных антителами эритроцитов поверхности клеток, пораженных вирусом.
3. Выявление агглютинации обработанных противовирусными антителами эритроцитов под действием вируса гриппа, который содержится в опытном материале в лунках панели микротитратора Такачи.
4. Метод гемадсорбции (PIT), РСК.
Вирусологический метод относится к наиболее точным. Осуществляется выделение вируса гриппа из секретов верхних дыхательных путей или из крови. Материал от больного необходимо брать в ранние сроки болезни и доставлять в вирусологическую лабораторию в охлажденном состоянии.
Для выделения вируса гриппа обычно используют куриные эмбрионы, более редко - культуру клеток и лабораторных животных. Индикацию выделенного вируса проводят с помощью реакции гемагглютинации (РГА) и реакции торможения.
Применение вирусологического метода на практике ограничено, так как он является наиболее тяжелым и дорогостоящим.
Из методов ретроспективной диагностики серологические методы получили наибольшее распространение. Диагностическим является нарастание титра антител в 4 и больше раз при исследовании парных сывороток крови, взятых в разгар заболевания и еще через 7-14 дней.
На практике наиболее часто применяется РТГА, в некоторых случаях используется РСК, редко - реакции нейтрализации и радиального гемолиза.
Другие рекомендованные для ретроспективной диагностики методы: реакция непрямой гемагглютинации (РИГА); реакция определения антител к нейраминидазе, метод дифференцированного определения антител с помощью редуцирующих веществ и прочие.
Методы иммуноферментного анализа (ИФА) и молекулярной гибридизации (ММГ) пока еще не получили широкого распространения в практике.
С помощью серологической диагностики гриппа возможно точное определение этиологии вируса путем выявления в крови увеличения количества специфических антител в динамике заболевания. Наибольшее значение серологические методы имеют при атипичном или бессимптомном течении гриппозной инфекции.
Наиболее доказательный метод лабораторной диагностики - выделение вируса паротита из крови, смывов из глотки, секрета околоушной слюнной железы, цереброспинальной жидкости и мочи.
Иммунофлюоресцентные методы позволяют обнаружить вирусы на клеточной культуре уже через 2-3 дня (при стандартном методе исследования - лишь через 6 дней). Данные методы выявляют вирусный антиген непосредственно в клетках носоглотки, что дает возможность получить результат более быстро.
Серологические методы позволяют выявить нарастание титра антител только через 1-3 недели от начала заболевания. Наиболее информативным методом является твердофазный ИФА. Также применяются более простые реакции (РСК и РТГА), которые характеризуются более поздними результатами.
Исследуют парные сыворотки: первая берется в начале болезни, вторая - спустя 2-4 недели. Диагностическим считается нарастание титра в 4 раза и более.
Возможно использование внутрикожной пробы с антигеном (аллергеном). Диагностическим считается переход отрицательной пробы в положительную. Положительная кожная проба уже в первые дни болезни свидетельствует о том, что человек ранее перенес паротит.
Дифференциальный диагноз
Дифференциальная диагностика проводится с рядом заболеваний.
1. Нейроциркуляторная дистония (НЦД). В пользу НЦД свидетельствуют следующие факторы:
- возраст до 40 лет;
- респираторные жалобы (в особенности дыхание со вздохами);
- длительная тупая боль в области верхушки сердца, без иррадиации; боль появляется или усиливается при эмоциональном стрессе и исчезает или уменьшается при физической нагрузке, приеме транквилизаторов или β- блокаторов;
- склонность к тахикардии и повышению систолического артериального давления, редкость нарушений ритма;
- нормальные значения МВ-КФК, тропонина І и T;
- проявления симпатико-тонического ортостатизма, быстрая утомляемость и снижение трудоспособности, повышенная возбудимость, потливость, холодные конечности, повышение сухожильных рефлексов;
- отсутствие прогрессирования симптоматики.
3. Необходимо дифференцировать миокардиты средней степени тяжести с ишемической болезнью сердца (ИБС) в следующих случаях:
- при нетипичном для ИБС болевом синдроме;
- у лиц молодого возраста с патологическими изменениями ЭКГ;
- при наличии изменений ЭКГ в отсутствие болевого синдрома.
При проведении дифференциального диагноза следует учитывать:
- наличие факторов риска ИБС (артериальная гипертензия, сахарный диабет, нарушение липидного обмена, избыточный вес, курение, пол);
- результаты суточного мониторирования ЭКГ (эпизоды ишемии), нагрузочных проб (ВЭМ, тредмил-тест);
- данные коронарографии .
4. Тяжелый миокардит дифференцируют с дилатационной кардиомиопатией (ДКМП). В пользу ДКМП свидетельствует:
- отсутствие четкой связи с воздействием инфекционных и неинфекционных агентов (после тщательного анализа анамнеза);
- постепенное развитие признаков застойной сердечной недостаточности, устойчивой к проводимой противовоспалительной и симптоматической терапии;
- отсутствие лабораторных признаков воспаления, повышение биомаркеров повреждения кардиомиоцитов (МВ-КФК, тропонин I и T).
Решающее значение придается указывающим на ДКМП результатам эндомиокардиальной биопсии: отсутствие маркеров воспаления, большая мышечная масса, диффузный фиброз, минимальные атеросклеротические изменения.
5. Дифференциальная диагностика с перикардитом осуществляется при выраженной кардиомегалии (требуется исключение массивного перикардиального выпота) и при характерных для фибринозного перикардита постоянных болях в области сердца, которые иногда усиливаются в положении на животе и при глубоком дыхании. В последнем случае обычно выслушивается шум трения перикарда, подтверждающий наличие перикардита. Заключение об изолированном характере перикардита обосновывается дополнительным исключением поражения миокарда: отсутствие изменений ЭКГ, не характерных для перикардита (например, нарушений проводимости). В противном случае устанавливают диагноз миоперикардита.
Отсутствие характерной треугольной тени сердца при рентгенологическом исследовании позволяет исключать массивный выпот в перикардиальную область при кардиомегалии. Более достоверным методом является эхокардиография, с помощью которой можно не только выявить жидкость в полости перикарда, но и приблизительно оценить ее количество.
6. Исключение митрального порока сердца необходимо в случаях, когда возникновение систолического шума сочетается с преимущественным увеличением левых отделов сердца, имитирующих картину органической митральной недостаточности. В отличие от последней, при миокардите систолический шум обычно не примыкает к I тону сердца, изменяется по интенсивности в разные дни и может исчезать после улучшения сократительной функции.
На фонокардиограмме систолический шум определяется как мезосистолический и зачастую сочетается с наличием III тона, удлинением интервала Q - I тон. Рентгенологически при миокардите выявляется снижение, а не повышение, пульсации контуров сердца, почти не встречаются коромыслоподобные движения между III и IV дугами по левому контуру сердца.
Эхокардиография позволяет исключить органическое поражение створок митрального клапана и иногда обнаружить причину систолического шума (например, функциональный пролапс створки).
Известно, что инфаркт миокарда с подъемом сегмента ST (ИМПST) сопровождается активацией иммунной системы с повышенной выработкой всех факторов гуморальной и клеточной защиты. Недостаточная их выработка способствует прогрессированию субэпикардиальной и субэндокардиальной ишемии при ИМПST. У пациентов с ИМПST, осложненным нарушениями ритма, на фоне хронической персистирующей герпесвирусной инфекции (низким уровнем концентрации α-ИФН (от 0,072 до 0,084 пг/мл) и АИФН (от 0,025 до 0,031 нг/мл) наряду с диагностированными высокими титрами специфических IgM (от 0,86 до 1,67 ЕД) и IgG (от 2,42 до 3,01 ЕД) к ВПГ1+2 и ЦМВ), добавление к лечению с иммунокоррегирующей целью препарата Кипферон позволяет улучшить результаты лечения ИМПST, его осложнений в виде аритмий сердца и исход заболевания.

1. Аникин В.В. Показатели иммунной системы у больных с нарушениями сердечного ритма / В. В. Аникин, М.Н. Калинкин, Ю.Л. Вороная // Российский кардиологический журнал. – 2001.– № 6. – С.4-6.
2. Бокерия Л.А. Интервенционные методы лечения ишемической болезни сердца /Л.А. Бокерия, Б.Г. Алекян, Ю.И. Бузиашвили. – М.: Изд-во НЦССХ им. А.Н.Бакулева РАМН, 2002. – № 4. – С.22-39.
3. Караулов А.В. Клиническая иммунология / А.В. Караулов. – М.: Медицинское информационное агенство,1999. – 315 c.
5. Малиновская, В.В. Виферон – новый противовирусный и иммуномодулирующий препарат / В.В. Малиновская // Лечащий врач. – 2008. – № 5. – С. 3-6.
6. Оранский П.П., Ханферян Р.А. Уровни цитокинов у больных Q-позитивным инфарктом миокарда в сыворотке крови и культурах мононуклеаров крови // Цитокины и воспаление. – 2009. – № 2. – С.112-114.
7. Чичкова М.А. Острофазовые маркеры воспаления в дифференциальной диагностике экссудата и транссудата при ИБС / М.А. Чичкова // По материалам международной научно-практической конференции). – Москва: Изд-во РУДН, 2002. – № 4. – С.425-426.
10. Li, Н. The detection of the antibodies of human cytomegalovirus in sera of patients with coronary heart disease. / Н. Li, C. Xu, Q. Wang // Chung. Hua. Nei. KoTsa. Chih. – 1996. – Vol.35. – № 11. – P.741-743.
В клинической медицине проблема изменения некоторых иммунологических факторов, их влияние на течение ИМПST и методы коррекции изучены недостаточно. В литературе имеются данные о реактивации хронической герпесвирусной инфекции при различной соматической патологии [1,3]. Известно, что герпесвирусы способны к длительной персистенции в организме и обладают наиболее высокой степенью вирулентности, токсичности и длительностью воспалительной реакции, а также склонностью к вторичной иммуносупрессии [3,4,9].
В последние годы были получены данные о высокой инфицированности населения вирусом простого герпеса – 60–80 % населения [5,7,8].
Стандартная терапия острого инфаркта миокарда включает в себя купирование болевого синдрома, применение β-блокаторов, ингибиторов АПФ, дезагрегантов, антикоагулянтов и статинов.
Известно, что при инфаркте миокарда повышается концентрация циркулирующих иммунных комплексов, уровень иммуноглобулинов IgG, повышается уровень В-клеток, снижается уровень IgM и снижается уровень Т-клеток [2,6,10].
Так, в настоящее время имеются сведения оприменении в лечении различной соматической патологии с иммунокорегирующей целью препарата Виферон, который включает в себя α-интерферон [5]. Данных о применении препарата Кипферон у пациентов синфарктом миокарда с подъемом сегмента ST на фоне хронической герпесвирусной инфекции ранее не было.
В клинической медицине до настоящего времени патогенетическое значение сдвигов иммунологических показателей у больных с ИМПST и пути их коррекции оставалось недостаточно изученным.
Цель исследования: оптимизировать лечение пациентов с инфарктом миокарда с подъемом сегмента ST на фоне хронической герпесвирусной инфекции.
Материалы и методы исследования. Материалом исследования послужили 40 пациентов группы исследования – (мужчин – 25, женщин – 15) с инфаркта миокарда с подъемом сегмента ST на фоне хронической герпесвирусной инфекции, с нарушением ритма сердца, с применением иммунотерапии препаратом Кипферон в дозе 500000 единиц/ в сутки;
38 пациентов группы сравнения – (мужчин – 26, женщин – 12) с инфарктом миокарда с подъемом сегмента ST с нарушениями ритма сердца на фоне стандартной терапии без иммунокоррекции.
Материал исследования был отобран после клинической и электрокардиографической диагностики инфаркта миокарда с подъемом сегмента ST.
Методы исследования: физикальные, общеклинические лабораторные (общий анализ крови, мочи) и биохимические (анализ крови на содержание тропонина T, креатинфосфокиназу МВ, лактатдегидрогеназу, электролиты крови, аспарататаминотрансферазу, алатаминотрансферазу, креатинин, мочевину, фибриногена «А» и «В», АЧТВ, протромбинового индекса, общего холестерина, триглицеридов, b-липопротеидов, липопротеидов высокой и низкой плотности, атерогенный индекс), инструментальные (ЭКГ, холтеровское мониторирование ЭКГ, ЭХО-КГ в режимах 2-D, 3-D, селективная коронароангиография), проведенные по общепринятым методикам. Общепринятая стандартная схема лечения инфаркта миокарда с подъемом сегмента ST не позволяет повлиять на измененные показатели иммунитета пациента и тем самым предупредить возникновение аритмий сердца.
В связи с этим нами были дополнительно проведены специальные исследования на базе иммунологической лаборатории ФБУН «Московский научно-исследовательский институт эпидемиологии и микробиологии имени Г.Н. Габричевского».
Был сделан двухсайтовый иммуноферментный анализ (ИФА) сыворотки крови больных инфарктом миокарда на 1-е и 10-е сутки заболевания, осложненными аритмиями сердца и без осложнений, на определение уровней иммуноглобулинов IgM и IgG к вирусу простого герпеса (ВПГ1+2), стрипированных на лунках планшета и набора реагентов фирмы «DSL» (США). Учет полученных данных произведен на спектрофотометре «ELx800 Universal Microplate Reader» фирмы «Bio - Tekinstruments INC» (США).
Результаты реакции трактованы как положительные при достижении диагностически значимого результата (ДЗР), полученного при расчете соотношения средней оптической плотности образца (ОП сред) к Сutt-Off (оптической плотности контрольной сыворотки) при коэффициенте, равном для IgM 1,0 – 1,1 раз; IgG – 1,1 раз и выше.
Уровни концентрации α-интерферона и антител к α-интерферону в сыворотке крови определялись методом твердофазного иммуноферментного анализа с помощью набора реагентов для иммуноферментного определения фирмы «ВЕКТОР-БЕСТ» (Россия, Новосибирск).
Оптическая плотность образцов определялась с помощью спектрофотометра в двухволновом режиме: основной фильтр – 450 нм, референс-фильтр – в диапазоне 620–655нм. Концентрация α-интерферона измерялась в пг/мл, антител к α-интерферону – в нг/мл. Учитывалось, что уровень антител к α-интерферону в сыворотке здоровых доноров не превышает 15нг/мл, а уровень концентрации α-интерферона – 0-5пг/мл.
В результате полученных данных уровня α-интерферона и антител к α-интерферону к стандартному медикаментозному лечению инфаркта миокарда с подъемом сегмента ST была добавлена интерферонозаместительная терапия с первых суток поступления пациента в стационар и далее в течение последующих 10 суток.
Гендерные и возрастные показатели обследованных пациентов представлены в таблице.
Распределение обследованных пациентов по полу и возрасту
40
25
15
60,57±1,4
Пациенты с осложненным течением ИМПST с иммунокоррекцией препаратом кипферон
38
26
12
58,5±2,9
с осложненным течением ИМПST без иммунокоррекции
Примечание: n – число больных в группе; М – средний показатель, m – ошибка среднего показателя.
Препаратом для коррекции ранних нарушений иммунологических показателей был выбран Кипферон — рекомбинантный интерферон α-2, обладающий системным иммуномодулирующим действием, мембраностабилизирующим, противовоспалительным, антибактериальным, противовирусным. В одном суппозитории кипферона содержится 500000 МЕ интерферона альфа –2 и 60 мг КИП. Препарат Кипферон в форме выпуска ректальных суппозиториев пулевидной формы, желтовато-белого цвета однородной консистенции с диаметром не более 10 мм (500000 МЕ в 1 свече). Выбор лекарственной формы в виде суппозиториев не случаен, так как это позволяет успешно применять Кипферон по месту развития инфекционного начала при терапии пациентов разного возраста и функционального состояния. Высокое содержание белка в препарате Кипферон способствует повышению стабильности и активности интерферона в присутствии агрессивных факторов секретов слизистых и отделяемого из инфекционных очагов. При применении препарата Кипферон повышается местный и системный неспецифический иммунный ответ, снижается выраженность бактериальной и вирусной интоксикации, а также стимулируются процессы регенерации тканей. Показания к применению: в составе комплексной терапии у взрослых с первичной или рецидивирующей герпетической и цитомегаловирусной инфекцией. Препарат кипферон совместим и хорошо сочетается со всеми лекарственными препаратами.
Результаты. В результате проведенного исследования у больных, имеющих в анамнезе проявления герпесвирусной инфекции, высокий риск возникновения нарушений ритма при наличии в крови положительных титров специфических иммуноглобулинов к кардиотропному ВПГ1+2, были получены данные о необходимости иммунокоррегирующей терапии препаратом Кипферон. Приведение соотношения показателей исследуемых параметров к модели поверхности позволило построить график в поле трех показателей: уровень иммуноглобулинов IgА, уровень иммуноглобулинов IgМ и уровень иммуноглобулинов IgG отдельно для пациентов с ИМПST с нарушениями сердечного ритма на фоне стандартной медикаментозной терапии без иммуномодуляции Кипфероном и для пациентов с ИМПST, с нарушениями сердечного ритма на фоне комбинирования стандартной медикаментозной и иммуномодулирующей терапии Кипфероном (Рис.1,2).

Рис.1. График поверхности для пациентов с ИМПST с нарушениями сердечного ритма группы на фоне стандартной медикаментозной терапии без иммунотерапии Кипфероном
Примечание: по оси Х – уровень иммуноглобулинов IgА, МЕ/мл; по оси Y – уровень иммуноглобулинов IgМ, МЕ/мл; по оси Z – уровень иммуноглобулинов IgG, МЕ/мл.

Рис.2. График поверхности для пациентов с ИМПSTс нарушениями сердечного ритма на фоне комбинирования стандартной медикаментозной и иммунотерапии Кипфероном
Примечание:по оси Х – уровень иммуноглобулинов IgА, МЕ/мл; по оси Y – уровень иммуноглобулинов IgМ, МЕ/мл; по оси Z – уровень иммуноглобулинов IgG, МЕ/мл.
На графике поверхности показано, что уровни IgА, IgМ,IgG, на фоне проведенной иммунокоррекции Кипфероном значительно отличались от пациентов на фоне стандартной терапии, а именно – отмечалось повышение уровня иммуноглобулинов IgМ, сопровождалось повышением иммуноглобулинов IgА и иммуноглобулинов IgG.
Выводы
Применение препарата Кипферон в комбинировании со стандартной терапией инфаркта миокарда позволило снизить уровни содержания IgM и IgG к герпесвирусам и повысить уровень α-интерферона до физиологических показателей, что приводит к стабилизации клинического течения инфаркта миокарда, достоверному регрессу массы миокарда левого желудочка на 2,4 %, улучшению диастолической функции на 27 %, нормализации продолжительности интервалов PQ и QT на ЭКГ (р<0,05) с профилактикой аритмий сердца.
В результате проведенного исследования было установлено, что у больных инфарктом миокарда при определении низкого уровня концентрации α-интерферона 0,077±0,012 пг/мл и α-интерфероновых антител 0,028±0,002нг/мл наряду с диагностированными высокими титрами специфических IgM 1,03±0,11 ДЗР и IgG 2,08±0,31 ДЗР к ВПГ1+2, целесообразно назначение Кипферона в дозе 500000Ед/сут в течении 10 дней с последующей коррекцией дозы в соответствие с нормализацией α-интерферонового ответа и отсутствия IgM к герпесвирусам в сыворотке крови. У пациентов с ИМПST, осложненным нарушениями ритма, на фоне хронической персистирующей герпесвирусной инфекции (низким уровнем концентрации α-ИФН (от 0,072 до 0,084 пг/мл) и АИФН (от 0,025 до 0,031 нг/мл) наряду с диагностированными высокими титрами специфических IgM (от 0,86 до 1,67 ЕД) и IgG (от 2,42 до 3,01 ЕД) к ВПГ1+2 и ЦМВ), добавление к лечению с иммунокоррегирующей целью препарата Кипферон позволяет улучшить результаты лечения ИМПST, его осложнений в виде аритмий сердца и исход заболевания.
Подводя итог вышеизложенному, проводя комбинированное лечение инфаркта миокарда с иммунокоррекцией Кипфероном, мы смогли восполнить дефицит α-интерфероновых антител, подавить и заблокировать активность герпесвирусной инфекции, восстановить процесс релаксации левого желудочка сердца после его сокращения, снизить постнагрузку в связи с уменьшением полости левого желудочка сердца, соответственно, и системного артериального давления с последующим снижением работы левого желудочка сердца и быстрому восстановления внутрисердечной гемодинамики, улучшению перфузии миокарда и снижению риска возникновения и быстрому купированию аритмий сердца.
Предложенное лечение пациентов с инфарктом миокарда с подъемом сегмента ST на фоне хронической герпесвирусной инфекции позволяет ускорить купирование нарушений ритма, снизить частоту их возникновения, улучшить прогноз течения инфаркта миокарда.
Данный подход к лечению инфаркта миокарда с подъемом сегмента ST позволяет учитывать изменение таких иммунологических показателей, как уровни α-интерферона и антител к α-интерферону, особенности патогенетического участия герпесвирусов в развитии осложнений острого периода ИМПST, а также влияние иммунокоррекции препаратом Кипферон на прогноз и течение заболевания.
Миокардит – воспаление мышечной оболочки сердца (миокарда), чаще ревматического, инфекционного или инфекционно-аллергического характера. Течение миокардита может быть острым или хроническим. Острый миокардит проявляется одышкой, цианозом, отеками на ногах, набуханием вен на шее, болями в сердце, сердцебиением, аритмиями. Часто развитию миокардита предшествует перенесенная инфекция (дифтерия, ангина, скарлатина, грипп и др.). В дальнейшем возможны рецидивы заболевания (при ревматическом миокардите), развитие сердечной недостаточности и тромбоэмболий сосудов различных органов.
Общие сведения
Миокардит – воспаление мышечной оболочки сердца (миокарда), чаще ревматического, инфекционного или инфекционно-аллергического характера. Течение миокардита может быть острым или хроническим. Острый миокардит проявляется одышкой, цианозом, отеками на ногах, набуханием вен на шее, болями в сердце, сердцебиением, аритмиями. Часто развитию миокардита предшествует перенесенная инфекция (дифтерия, ангина, скарлатина, грипп и др.). В дальнейшем возможны рецидивы заболевания (при ревматическом миокардите), развитие сердечной недостаточности и тромбоэмболий сосудов различных органов.
Частота заболеваемости миокардитом намного выше статистической из-за поздней диагностики и латентных форм, когда заболевание протекает стерто или в легкой форме. Признаки воспалительного процесса в миокарде в 4–9% случаев обнаруживаются только на аутопсии (по результатам патологоанатомических исследований). От острого миокардита умирает от 1 до 7% больных, у людей молодого возраста в 17-21% случаев он становится причиной внезапной смерти.
Миокардит приводит к развитию сердечной недостаточности и нарушению ритма сердца, что является ведущими причинами летального исхода. Миокардиты встречаются чаще у молодых людей (средний возраст пациентов 30 – 40 лет), хотя заболевание может возникнуть в любом возрасте. Мужчины заболевают миокардитом несколько реже женщин, но у них чаще развиваются тяжелые формы заболевания.

Причины миокардита
Миокардиты включают большую группу заболеваний сердечной мышцы воспалительного генеза, проявляющихся поражением и нарушением функции миокарда. Частой причиной миокардита являются различные инфекционные заболевания:
- вирусные (вирусы Коксаки, гриппа, аденовирусы, герпеса, гепатита В и С);
- бактериальные (коринеобактерии дифтерии, стафилококки, стрептококки, сальмонеллы, хламидии, риккетсии);
- грибковые (аспергиллы, кандиды),;
- паразитарные (трихинеллы, эхинококки) и др.
Тяжелая форма миокардита может возникать при дифтерии, скарлатине, сепсисе. Высокой кардиотропностью обладают вирусы, вызывающие миокардит в 50% случаев. Иногда миокардит развивается при системных заболеваниях соединительной ткани: системной красной волчанке, ревматизме, васкулитах, ревматоидном артрите, при аллергических заболеваниях. Также причиной миокардита может служить токсическое воздействие некоторых лекарственных препаратов, алкоголя, ионизирующее излучение. Тяжелое прогрессирующее течение отличает идиопатический миокардит невыясненной этиологии.
Провоцирующими моментами возникновения миокардита являются острые инфекции (чаще вирусные), очаги хронической инфекции; аллергозы, нарушенные иммунологические реакции; токсическое воздействие на организм (лекарств, алкоголя, наркотиков, ионизирующего излучения, при тиреотоксикозе, уремии и др.).
Патогенез
Миокардит в большинстве случаев сопровождается эндокардитом и перикардитом, реже воспалительный процесс затрагивает только миокард. Повреждение миокарда может возникать при прямом миокардиоцитолитическом действии инфекционного агента; под влиянием токсинов, циркулирующих в крови (в случае системной инфекции); и как результат аллергической или аутоиммунной реакции. Нередко встречаются инфекционно-аллергические миокардиты.
Иммунные нарушения, наблюдаемые при миокардите, проявляются расстройством всех звеньев иммунитета (клеточного, гуморального, фагоцитоза). Инфекционный антиген запускает механизм аутоиммунного повреждения кардиомиоцитов, приводящий к значительным изменениям миокарда: дистрофическим изменениям мышечных волокон, развитию экссудативных или пролиферативных реакций в интерстициальной ткани. Следствием воспалительных процессов при миокардите является разрастание соединительной ткани и развитие кардиосклероза. При миокардите заметно снижается насосная функция сердечной мышцы, что часто носит необратимый характер и приводит к тяжелому состоянию недостаточности кровообращения, нарушениям сердечного ритма и проводимости, служит причиной инвалидности и летального исхода в молодом возрасте.
Классификация
В зависимости от механизма возникновения и развития миокардита выделяют следующие формы:
- инфекционные и инфекционно-токсические (при гриппе, вирусах группы Коксаки, дифтерии, скарлатине и др.);
- аллергические (иммунные) (сывороточный, инфекционно-аллергический, трансплантационный, лекарственный, миокардиты при системных заболеваниях);
- токсико-аллергические (при тиреотоксикозе, уремии и алкогольном поражении сердца);
- идиопатические (невыясненной природы).
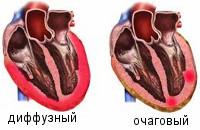
По распространенности воспалительного поражения миокардиты делятся на диффузные и очаговые. По течению различают острые, подострые, хронические (прогрессирующие, рецидивирующие) миокардиты. По степени тяжести - легкий, миокардит средней тяжести, тяжелый.
По характеру воспаления выделяют экссудативно-пролиферативный (воспалительно-инфильтративный, васкулярный, дистрофический, смешанный) и альтернативный (дистрофически-некробиотический) миокардиты. В развитии инфекционного миокардита (как наиболее часто встречающегося) выделяют 4 патогенетические стадии:
- Инфекционно-токсическая
- Иммунологическая
- Дистрофическая
- Миокардиосклеротическая
По клиническим вариантам (по преобладающим клиническим симптомам) различают миокардиты:
- малосимптомный
- болевой или псевдокоронарный
- декомпенсационный (с нарушением кровообращения)
- аритмический
- тромбоэмболический
- псевдоклапанный
- смешанный
Симптомы миокардита
Клиническая симптоматика миокардита зависит от степени поражения миокарда, локализации, остроты и прогрессирования воспалительного процесса в сердечной мышце. Она включает проявления недостаточности сократительной функции миокарда и нарушения ритма сердца. Инфекционно-аллергический миокардит в отличие от ревматического начинается обычно на фоне инфекции или сразу после нее. Начало заболевания может протекать малосимптомно или латентно.
Основные жалобы пациентов - на сильную слабость и утомляемость, одышку при физической нагрузке, боли в области сердца (ноющие или приступообразные), нарушения ритма (сердцебиение, перебои), повышенную потливость, иногда боль в суставах. Температура тела обычно субфебрильная или нормальная. Характерными проявлениями миокардита являются увеличение размеров сердца, понижение артериального давления, недостаточность кровообращения.
Кожные покровы у больных миокардитом бледные, иногда с синюшным оттенком. Пульс учащенный (иногда уреженный), может быть аритмичным. При выраженной сердечной недостаточности наблюдается набухание шейных вен. Возникает нарушение внутрисердечной проводимости, которое даже при небольших очагах поражения может стать причиной аритмии и привести к летальному исходу. Нарушение сердечного ритма проявляется суправентрикулярной (наджелудочковой) экстрасистолией, реже приступами мерцательной аритмии, что заметно ухудшает гемодинамику, усиливает симптомы сердечной недостаточности.
В большинстве случаев в клинической картине миокардита преобладают лишь отдельные из перечисленных выше симптомов. Примерно у трети пациентов миокардит может протекать малосимптомно. При миокардитах, возникающих на фоне коллагеновых заболеваний, а также вирусной инфекции часто возникает сопутствующий перикардит. Идиопатический миокардит имеет тяжелое, иногда злокачественное течение, приводящее к кардиомегалии, тяжелым нарушениям ритма и проводимости сердца и сердечной недостаточности.
Осложнения
При длительно текущем миокардите развиваются склеротические поражения сердечной мышцы, возникает миокардитический кардиосклероз. В случае острого миокардита при тяжелых нарушениях работы сердца быстро прогрессирует сердечная недостаточность, аритмия, становящиеся причиной внезапной смерти.
Диагностика
Существенные трудности в диагностике миокардитов вызывает отсутствие специфических диагностических критериев. Мероприятия по выявлению воспалительного процесса в миокарде включают:
- Сбор анамнеза
- Физикальное обследование пациента - симптомы варьируют от умеренной тахикардии до декомпенсированной желудочковой недостаточности: отеки, набухание шейных вен, нарушение ритма сердца, застойный процесс в легких.
- ЭКГ - нарушение сердечного ритма, возбудимости и проводимости. ЭКГ-изменения при миокардите не являются специфичными, так как сходны с изменениями при различных заболеваниях сердца.
- ЭхоКГ - выявляется патология миокарда (расширение полостей сердца, снижение сократительной способности, нарушение диастолической функции) в разной степени в зависимости от тяжести заболевания.
- Общий, биохимический, иммунологический анализы крови не являются столь специфичными при миокардите и показывают увеличение содержания α2 и γ - глобулинов, повышение титра антител к сердечной мышце, положительную РТМЛ (реакцию торможения миграции лимфоцитов), положительную пробу на С-реактивный белок, повышение сиаловых кислот, активности кардиоспецифичных ферментов. Исследование иммунологических показателей должно проводиться в динамике.
- Рентгенография легких помогает обнаружить увеличение размеров сердца (кардиомегалию) и застойные процессы в легких.
- Бакпосев крови для выявления возбудителя, или ПЦР диагностика.
- Эндомиокардиальная биопсия при помощи зондирования полостей сердца, включающая гистологическое исследование биоптатов миокарда, подтверждает диагноз миокардита не более чем в 37% случаев в связи с тем, что может иметь место очаговое поражение миокарда. Результаты повторной биопсии миокарда дают возможность оценить динамику и исход воспалительного процесса.
- Сцинтиграфия (радиоизотопное исследование) миокарда является физиологичным исследованием (прослеживается естественная миграция лейкоцитов в очаг воспаления и нагноения).
- Магнитно-резонансная томография (МРТ сердца) с контрастированием дает визуализацию воспалительного процесса, отека в миокарде. Чувствительность данного метода составляет 70-75%.
Лечение миокардита
Острая стадия миокардита требует госпитализации в отделение кардиологии, ограничения физической активности, строгого постельного режима на 4 - 8 недель до достижения компенсации кровообращения и восстановления нормальных размеров сердца. Диета при миокардите предполагает ограниченное употребление поваренной соли и жидкости, обогащенное белковое и витаминизированное питание для нормализации метаболических процессов в миокарде.
Терапию миокардита проводят одновременно по четырем направлениям, осуществляя этиологическое, патогенетическое, метаболическое симптоматическое лечение. Этиологическое лечение направлено на подавление инфекционного процесса в организме. Терапию бактериальных инфекций проводят антибиотиками после выделения и определения чувствительности патогенного микроорганизма. При миокардитах вирусного генеза показано назначение противовирусных препаратов.
Необходимым условием успешного лечения миокардитов служит выявление и санация инфекционных очагов, поддерживающих патологический процесс: тонзиллита, отита, гайморита, периодонтита, аднексита, простатита и др. После осуществления санации очагов (хирургической или терапевтической), курса противовирусной или антибактериальной терапии необходимо проведение микробиологического контроля излеченности.
В патогенетическую терапию миокардитов включают противовоспалительные, антигистаминные и иммуносупрессивные препараты. Назначение нестероидных противовоспалительных средств осуществляется индивидуально, с подбором дозировок и длительности курса лечения; критерием отмены служит исчезновение лабораторных и клинических признаков воспаления в миокарде. При тяжелом, прогрессирующем течении миокардита назначаются глюкокортикоидные гормоны. Антигистаминные средства способствуют блокированию медиаторов воспаления.
Для улучшения метаболизма сердечной мышцы при миокардитах применяют препараты калия, инозин, витамины, АТФ, кокарбоксилазу. Симптоматическое лечение миокардитов направлено на устранение аритмий, артериальной гипертензии, симптомов сердечной недостаточности, профилактику тромбоэмболий. Длительность лечения миокардита определяется тяжестью заболевания и эффективностью комплексной терапии и составляет в среднем около полугода, а иногда и дольше.
Прогноз
При латентном малосимптомном течение миокардита возможно самопроизвольное клиническое излечение без отдаленных последствий. В более тяжелых случаях прогноз миокардитов определяется распространенностью поражения миокарда, особенностями воспалительного процесса и тяжестью фонового заболевания.
При развитии сердечной недостаточности у 50% пациентов отмечается улучшение по результатам лечения, у четверти наблюдается стабилизация сердечной деятельности, у оставшихся 25% состояние прогрессирующе ухудшается. Прогноз при миокардитах, осложненных сердечной недостаточностью, зависит от выраженности дисфункции левого желудочка.
Неудовлетворительный прогноз отмечается при некоторых формах миокардитов: гигантоклеточном (100%-ая смертность при консервативной терапии), дифтерийном (смертность составляет до 50–60%), миокардите, вызванном болезнью Шагаса (американским трипаносомозом) и др. У этих пациентов решается вопрос о трансплантации сердца, хотя и не исключается риск развития повторного миокардита и отторжения трансплантата.
Профилактика
Для снижения риска заболеваемости миокардитом рекомендуется соблюдать меры предосторожности при контакте с инфекционными больными, санировать очаги инфекции в организме, избегать укусов клещей, осуществлять вакцинацию против кори, краснухи, гриппа, свинки, полиомиелита.
Пациенты, перенесшие миокардит, проходят диспансерное наблюдение у кардиолога 1 раз в 3 месяца с постепенным восстановлением режима и активности.
Herpes simplex - герпес простой или пузырьковый лишай известен человечеству с античных времен, а название «герпес» имеет греческое происхождение – «ползти», «подкрадываться», что полностью соответствует клиническим проявлениям заболеваний, вызванных вирусом простого герпеса (ВПГ). Благодаря типичной клинической картине, диагностика простого герпеса является достаточно простой задачей. В сомнительных случаях проводят исследование отделяемого герпетических везикул. Лечение простого герпеса сводится к местному или системному назначению антигерпетических препаратов на основе ацикловира, при необходимости проводится иммуномодулирующая терапия.


Общие сведения
Herpes simplex - герпес простой или пузырьковый лишай известен человечеству с античных времен, а название «герпес» имеет греческое происхождение – «ползти», «подкрадываться», что полностью соответствует клиническим проявлениям заболеваний, вызванных вирусом простого герпеса (ВПГ). Заболевания, причиной которых является вирус простого герпеса, довольно распространенны, некоторые осложнения инфекции заканчиваются летальным исходом. Данные центра по контролю заболеваемости в США регистрируют около полумиллиона случаев герпетической инфекции в год, отсюда можно предположить, что носителями герпетической инфекции являются от 2 до 20 млн. американцев. В Англии рост заболеваемости герпетической инфекции гениталий превышает другие инфекции, передающиеся половым путем. В Скандинавских странах, простой герпес обнаруживают примерно у 8% женщин, обратившихся к венерологу. В нашей стране нет статистических данных о заболеваемости герпеса, но герпетическая инфекция распространена повсеместно, на это указывают данные частных обследований на носительство вируса простого герпеса.
Рецидив герпетической инфекции происходит в случае реактивации вируса, это возможно после переохлаждений, перегревания, при пониженном иммунитете, в частности герпетическая инфекция является специфическим осложнением при ВИЧ-инфекции. Высыпания, вызванные серотипом 1 вируса герпеса, обычно локализуются в носогубной области, так же вирус проявляется в виде кератоконъюктивита, а высыпания, вызванные ВПГ-2, локализуются в области гениталий. Но, учитывая особенности полового поведения, локализация высыпаний может быть прямо противоположной. Поэтому герпес требует проведения серологических исследований для установления серотипа.

Этиология и патогенез
Группа вирусов герпеса включает в себя 4 сходных по морфологии вируса: ВПГ (герпес простой), varicella-zoster – вирус-возбудитель опоясывающего лишая и ветряной оспы, вирус Эпштейна-Барра и цитомегаловирус; в 1962 году выявлено, что вирус простого герпеса имеет два серотипа – серотип 1 и серотип 2. Серологические исследования подтверждают, что к концу 18 месяца жизни, практически каждый человек контактировал с ВГП-1, входными воротами же как правило, являются дыхательные пути. После чего вирус проникает в клетки ганглия тройничного нерва, но в течение жизни может ни разу не вызвать клинических проявлений инфекции.
С ВПГ-2 первый контакт обычно наступает в пубертатном периоде при начале сексуальных отношений. При этом после внешних проявлений, которых может и не быть, вирус так же переходит в неактивную форму и в клетках сакрального ганглия способен сохраняться длительное время.
Простой герпес, особенно второго типа обладает онкогенными свойствами, что имеет большое значение, учитывая распространенность инфекции. Уровень заболеваемости герпетической инфекции примерно одинаков во всех возрастных группах и одинаково распространен вне зависимости от пола. Клинические проявления же зависят от локализации и размера очага поражения, а так же от общего состояния иммунной системы.
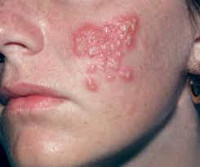
Проявления герпеса

Простой герпес чаще всего локализуется вокруг крыльев носа, уголков рта, красной каймы губ и в области гениталий, то есть вокруг естественных отверстий. В одном, реже в двух-трех местах на фоне ограниченной гиперемии появляются мелкие пузырьки; каждый очаг содержит от двух до десяти и более. Пузырьки расположены группой и наполнены прозрачным экссудатом, который через несколько дней мутнеет. В некоторых случаях единичные пузырьки сливаясь, образуют несколько многокамерных пузырей, которые имеют неровный фестончатый край и в диаметре достигают до 1,5 см.
При локализации процесса пузыри на участках кожи, не подверженных мацерации и трению, ссыхаются в желтовато-серую корку, которая самостоятельно отпадает через 5-7 дней. А на месте пузырька остается пигментированный участок, по истечению некоторого времени приобретающий нормальную окраску.
На слизистых, а так же на тех участках, которые подвержены мацерации или трению пузырьки вскрываются, вследствие чего образуются эрозии полициклического очертания с ярко-красным дном. Высыпания сопровождаются жжением, болью и чувством покалывания, в случае если высыпаний достаточно много – происходит отек близлежащих тканей. Общее состояние пациента при инфекции, вызванной вирусом простого герпеса не страдает, но в отдельных случаях может отмечаться озноб, мышечные боли и субфебрильная температура. В целом, процесс протекает 10-14 дней, при присоединении вторичной инфекции длительность заболевания увеличивается.
Вирус простого герпеса может вызывать герпетический стоматит, клиническими проявлениями которого являются поражения слизистой оболочки рта, губ, щек, десен и неба. Небольшие группы мелких пузырьков возникают на отекшей и гиперемированной слизистой оболочке. Пузырьки вскрываются в первые несколько часов, оставляя эрозии, которые из-за слияния имеют мелкофестончатые очертания. Через 2-4 дня эрозии покрываются нежной фиброзной пленкой, а затем эпителизируются. Герпетический стоматит, не осложненный другими инфекциями, протекает 6-14 дней, общее состояние пациента при этом удовлетворительное, но отмечается болезненность в полости рта и гиперсаливация.

У детей младшего и дошкольного возраста вирус герпеса чаще всего вызывает острый афтозный стоматит. Во время непродолжительного продромального периода отмечается общее недомогание, слабость, потеря аппетита и незначительное повышение температуры тела. Слизистая полости рта резко отечна и гиперемирована, а афтоидоподобные высыпания локализуются повсеместно. В отличие от простого стоматита высыпания имеют форму афт с участком некроза в центре и резко выраженным воспалительным ободком по периферии, диаметр единичных высыпаний до 1 см. По мере прогрессирования процесса афты сливаются и образуют обширные эрозивно-язвенные участки с неровными краями. Отмечается гиперсаливация, потеря аппетита, повышение температуры и резкая болезненность.
У некоторых пациентов возможны рецидивы герпетической инфекции в зависимости от сезонности или же без связи со временем года; при пониженном иммунитете рецидивы могут возникать несколько раз в месяц. Клинические проявления рецидивирующего герпеса зависят от локализации, общего состояния пациента, но не отличаются от проявлений герпеса простого.
Основой патогенеза рецидивирующего герпеса являются предрасполагающие факторы: переохлаждение или же перегрев организма, общие и простудные заболевания, ранее перенесенные инфекционные заболевания, а так же все заболевания, которые ослабляют клеточный иммунитет. У женщин наблюдается связь между периодами менструального цикла и обострениями рецидивирующей герпетической инфекцией.
Диагностика герпеса
Диагностика заболеваний, вызванная вирусом простого герпеса, не составляет труда и в типичных случаях клинические проявления позволяют поставить точный диагноз. Но при локализации в области гениталий, герпетические язвы могут иметь сходство с твердым шанкром. Эрозия, вызванная вирусом герпеса, имеет полицикличные очертания и наблюдается тенденция к слиянию мелкопузырьковых элементов, отсутствует специфичная для шанкра инфильтрация, на основе этого и происходит их дифференциация. Простой герпес, в отличие от сифилиса, протекает остро и в большинстве случаев носит рецидивирующий характер. В сомнительных случаях прибегают к лабораторной диагностике и тестируют отделяемое эрозии на наличие бледной трепонемы.
Герпес, локализирующийся на слизистой рта и протекающий по типу стоматита, следует дифференцировать от вульгарной пузырчатки и от многоформной экссудативной эритемы, которая имеет сезонное течение и рецидивирует весной и осенью. Диагностика герпетического стоматита основывается на клинических проявлениях. Для стоматита, вызванного вирусом простого герпеса, характерен отек и гиперемия слизистой рта, возникновение крупных пузырей, склонных к слиянию. Пузыри в течение нескольких часов вскрываются, а на их месте остаются эрозии с фестончатым краем, сверху прикрытые фиброзной пленкой. Если поражается красная кайма губ, то экссудат из серозного быстро переходит в кровянистый, высыпания же ссыхаются в единые кровянистые корочки. Отмечается потеря аппетита, гиперсаливация и болезненность при приеме пищи. Высыпания при пузырчатке обыкновенно располагаются единично на не склонной к отечности слизистой, эпителизации и образования фиброзной пленки так же не происходит, в мазках с эрозированной поверхности обнаруживают акантолитические клетки, а симптом Никольского положительный, чего при инфицировании вирусом герпеса не наблюдается.
Если требуется подтверждение диагноза на присутствие вируса герпеса, то в первые несколько дней от начала заболевания цитологические исследования наиболее информативны. Материал берется методом соскоба и окрашивается по Романовскому-Гимзе, после окрашивания четко видны гигантские многоядерные клетки с базофильной цитоплазмой. Ядра внутри клеток расположены скученно, образуя наслоения, и внешне напоминают единый конгломерат. Если произошло нечеткое окрашивание, то ядра могут не иметь четких очертаний, что не затрудняет подтверждение диагноза простой герпес. Дополнительно проводится ПЦР-исследование на вирус простого герпеса, реакция иммунофлуоресценции (РИФ) и исследование на противогерпетические антитела путем иммунно-ферментного анализа (ИФА).
Лечение герпеса
Лечение рецидивирующего герпеса заключается в иммунореабилитации пациентов, это помогает добиться снижения рецидивов или стойкой ремиссии. Герпес простой не терпит монотерапии, так как она является нецелесообразной, к ней прибегают только для лечения острой фазы заболевания. Если же использовать подобную терапию в качестве единственного метода лечения, то постоянный прием препаратов типа ацикловира и валацикловира, использование мазей напоминают замкнутый круг, из которого невозможно вырваться, а стрессовые ситуации лишь усугубляют состояние пациента.
Комплексное лечение инфекции, вызванной вирусом простого герпеса, в короткие сроки позволяет купировать процесс и привести к стойкой ремиссии. В начальной фазе рецидива назначается курс препаратов супрессоров, например ацикловир, валацикловир. Принятие этих препаратов в течение 5-7 дней резко снижает количество вирусов герпеса в организме. После этого назначаются имуннотерапевтические препараты, в виде курсов рекомбинантных альфаинтерферонов или/и иммуномодуляторов. Длительность курса зависит от тяжести инфекции и от состояния иммунной системы пациента. В тяжелых случаях альфа-интерферон принимают 10 дней и более. По истечению 1-2 месяца после купирования процесса целесообразным является применение герпетической вакцины, что позволяет добиться стойкой ремиссии.
Эффективность вакцинации зависит от состояния иммунитета, от назначенной схемы и от кратности введения препарата. Вакцину вводят внутрикожно с образованием специфической «апельсиновой корочки» на месте введения. Но отсутствие своевременной ревакцинации существенно снижает эффективность всего многомесячного курса лечения, поэтому следует проводить ревакцинацию против вируса простого герпеса, не нарушая сроков.
Самостоятельное применение герпетической инактивированной вакцины должно быть исключено, так как, несмотря на всю простоту, процедура требует определенных условий и знаний медицинского персонала, а инструкция по применению не содержит всей необходимой информации. Отрицательное мнение о вакцине основывается на том, что она несколько повышает возможность возникновения опухоли, но персистирующая инфекция, вызванная вирусом герпес простой, способна причинить более серьезный вред иммунной системе.
В состав вакцины входят инактивированные вирусы ВПГ-1 и ВПГ-2, которые, как и обычные серотипы простого герпеса могут трансформироваться, что по заключениям некоторых исследований способно индуцировать рак шейки матки в единичных случаях. Но вакцина и присутствующий в организме вирус имеют одинаковую способность индуцировать развитие онкологических процессов, а потому, пациентам, у которых обнаружен герпес, вакцинация не несет дополнительной опасности развития индуцированного рака. Для предотвращения образования опухолей надежным способом является применение профилактических специфических противораковых вакцин. Из физиотерапевтических методов в лечении простого герпеса применяют УФО-облучение, лазеротерапию, ОКУФ, инфракрасное облучение и др.
Читайте также:

