Образование рубцов в результате хронических воспалений это мти
Обновлено: 28.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
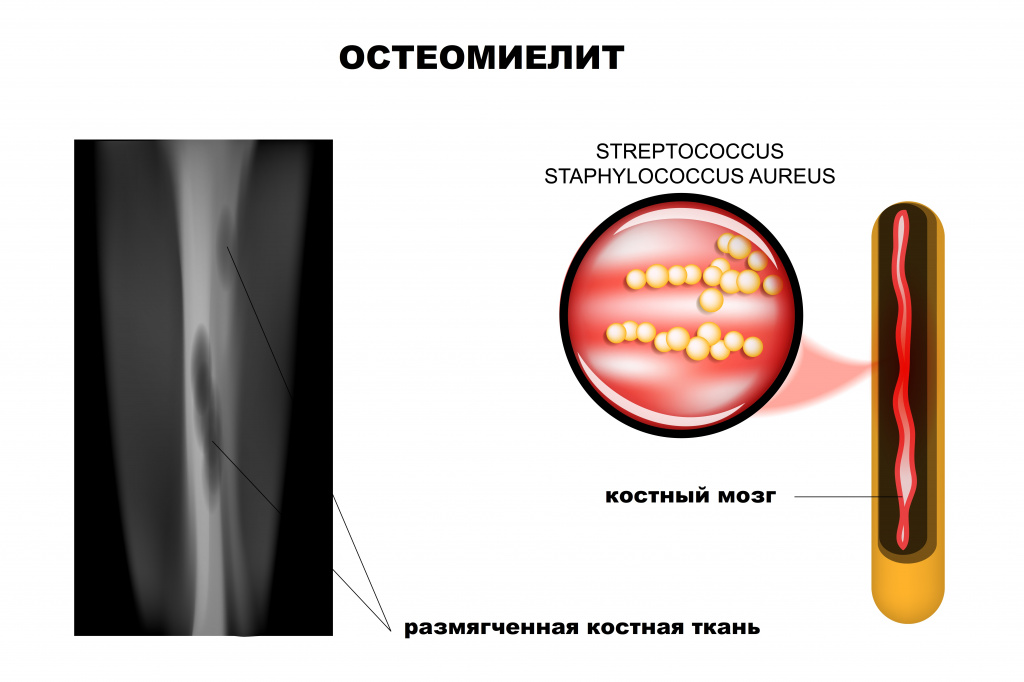
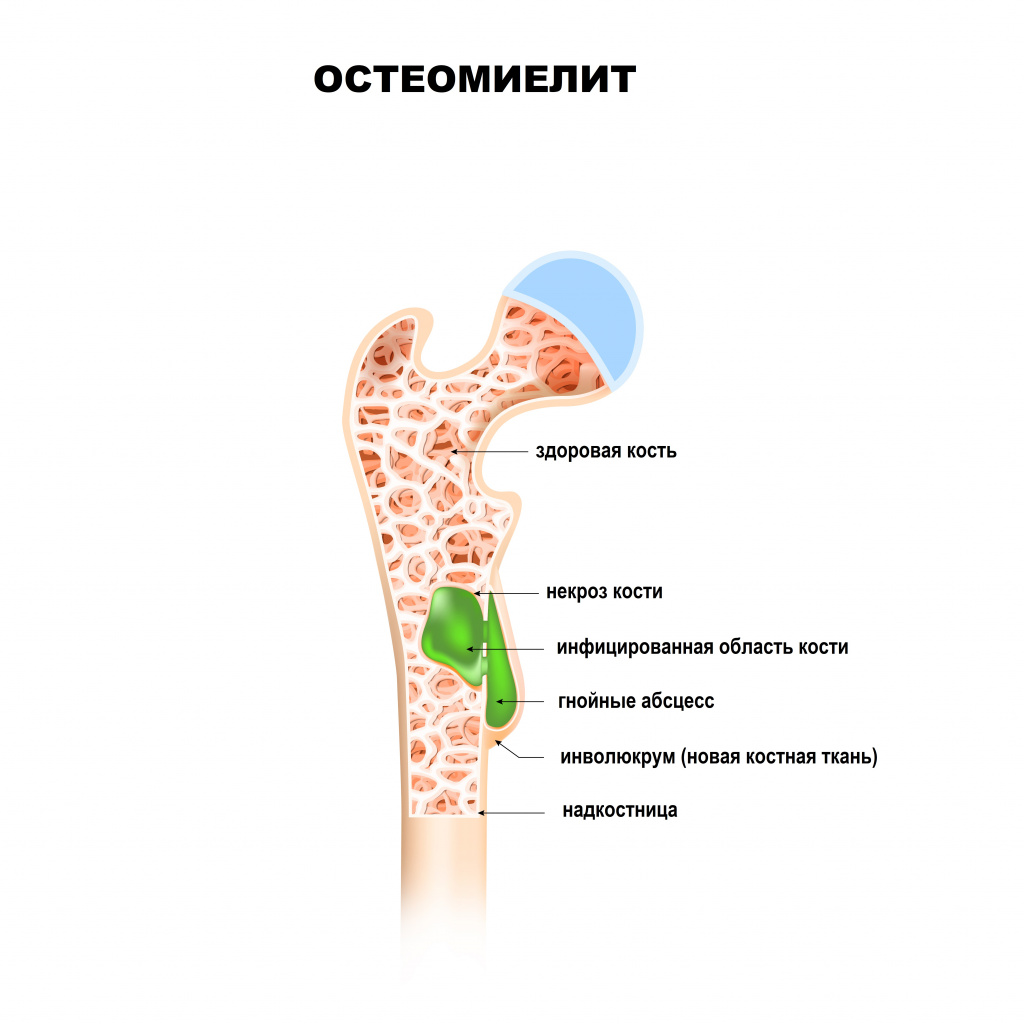
Остеомиелит: причины появления, симптомы, диагностика и способы лечения.
Определение
Остеомиелит – это тяжелый инфекционно-воспалительный процесс, поражающий все элементы кости. Под термином «остеомиелит» в настоящее время понимают неспецифическое гнойное или гнойно-некротическое поражение костной ткани (остит), костного мозга (миелит), надкостницы (периостит) и окружающих мягких тканей.
Причины появления остеомиелита
Ведущая роль в развитии заболевания принадлежит патогенным стафилококкам (золотистый стафилококк обнаруживается почти у 90% больных остеомиелитом), гемолитическим стрептококкам, грамотрицательной кишечной и анаэробной микрофлоре, грибковым инфекциям.
Специалисты считают, что в развитии остеомиелита имеют значение снижение реактивности организма больного (в результате травмы, переохлаждения, сенсибилизации) и нарушение кровоснабжения поражаемого отдела кости.
Основными путями проникновения инфекции в костную ткань являются:
- Гематогенный – патогенные микроорганизмы из какого-либо источника инфекции (например, фурункулов, кариозных зубов, воспалительных очагов в деснах, миндалинах или придаточных пазухах, легких, мочеполового тракта и др.) с током крови проникают в костную ткань, приводя к развитию остеомиелита. Воспалительный процесс начинается с внутренних слоев кости – в первую очередь поражается костный мозг, губчатое вещество кости. В последующем процесс переходит на компактное вещество (наружный плотный слой кости) и надкостницу. Данный вид остеомиелита часто встречается в детском возрасте. Особенностью костной ткани у детей является ее обильное кровоснабжение. В большинстве случаев остеомиелит развивается в зонах роста костей (метафизах). При этом чаще поражаются длинные (большеберцовая, бедренная или плечевая) кости конечностей ребенка. У взрослых гематогенный остеомиелит, как правило, поражает тело позвонков.
- Прямое инфицирование костной ткани может наблюдаться при открытых переломах, обширных, глубоких ранах. Посттравматический остеомиелит развивается вторично после открытых переломов. Особую группу составляет остеомиелитическое повреждение костей после ДТП, спортивных травм, огнестрельных и минно-взрывных ранений, поскольку в характере перелома играет роль обширное поражение окружающих тканей. При этом возникает не только дефицит костной, но и мягких тканей с образованием больших дефектов. В некоторых случаях данным путем может происходить проникновение патогенных бактерий при различных хирургических ортопедических вмешательствах.
- Инфицирование из близлежащих гнойных очагов (контактный путь) – патогенные бактерии проникают в костную ткань из длительно существующих гнойно-воспалительных очагов в окружающих мягких тканях. Данная форма в основном встречается у взрослых. В процесс обычно вовлечена одна кость, но иногда наблюдается поражение нескольких участков. Экзогенное распространение инфекции от сопредельных зараженных тканей или открытых ран вызывает около 80% случаев остеомиелита и часто имеет полимикробный характер. Факторами риска у взрослых являются мужской пол, пожилой возраст, истощение, ослабленный иммунитет, длительный прием глюкокортикоидов, гемодиализ, серповидноклеточная анемия (наследственное заболевание, которое характеризуется образованием патологического белка гемоглобина в эритроцитах) и употребление инъекционных наркотиков. Травмы, ишемия, инородные тела, пролежни, повреждение тканей лучевой терапией также предрасполагают к остеомиелиту.
Остеомиелит, обусловленный инфицированием окружающих тканей, часто локализуется в области стоп (у больных с сахарным диабетом или заболеваниями периферических сосудов).
Любой остеомиелит может перейти в хроническую форму, имея, в конечном счете, общую патофизиологию с нарушением целостности оболочки мягких тканей, наличием окружающей омертвевшей, инфицированной и реактивной новой костной ткани.
Классификация заболевания
Остеомиелит различают:
- по пути инфицирования: экзогенный и эндогенный;
- по этиологии:
- острый гематогенный остеомиелит, вызванный золотистым стафилококком, стрептококками, коагулаза-отрицательными стафилококками, Haemophilus influenzae, грамотрицательными микроорганизмами;
- остеомиелит позвоночника, вызванный золотистым стафилококком, грамотрицательными кишечными палочками, микобактериями туберкулеза, грибами;
- остеомиелит при наличии местного очага или сосудистой недостаточности, вызванный комбинацией аэробных и анаэробных микроорганизмов;
- остеомиелит, развившийся на фоне инфекции протезных аппаратов, вызванной коагулаза-отрицательными стафилококками, золотистым стафилококком, коринеформными бактериями, грамотрицательными микроорганизмами.
- острый гематогенный остеомиелит:
- генерализованный (септикотоксемия, септикопиемия),
- очаговая форма;
- после перелома,
- огнестрельный,
- послеоперационный;
- абсцесс Броди,
- альбуминозный (Оллье),
- склерозирующий (Гарре).
- острая (2-4 недели);
- подострая (от 2 недель и более):
- выздоровление,
- продолжение процесса;
- обострение,
- ремиссия,
- выздоровление.
- остеомиелит трубчатых костей (эпифизарный, метафизарный, диафизарный, тотальный);
- остеомиелит плоских костей.
К симптомам заболевания относят боль в области пораженной кости, сопровождающуюся общей реакцией организма (при остром остеомиелите) или без нее (при хроническом остеомиелите).
Первые признаки остеомиелита в острой форме:
- сильная распирающая боль в пораженной кости;
- выраженный локальный отек, который приводит к натяжению кожного покрова;
- температура тела поднимается до 38оС;
- при постукивании можно определить очаг воспаления – в этом месте пациент чувствует наибольшую болезненность.
![Кость.jpg]()
Признаки остеомиелита кости часто дополняются симптомами общей интоксикации, если инфекция распространяется на соседние ткани или проникает в кровь. У пациента в таком случае наблюдаются:
- высокая температура (около 39оС);
- сильная головная боль;
- лихорадка, озноб;
- бледные кожные покровы;
- учащенное сердцебиение;
- тошнота и рвота.
Если у пациента наблюдается хронический остеомиелит, симптомы кардинально меняются. Клиническая картина становится стертой. Основные признаки остеомиелита хронической формы:
- боль уменьшается, приобретает ноющий характер;
- появляются свищи (каналы, соединяющие гнойный очаг с внешней средой) с гнойным отделяемым, которые часто имеют выход далеко от локализации воспаления.
Развитие остеомиелита у детей сопровождается теми же симптомами что и у взрослых, хотя патология чаще протекает в легкой форме без общей интоксикации и осложнений.
Остеомиелит позвоночника обычно вызывает локальную боль в спине с паравертебральным (по сторонам позвоночного столба) мышечным спазмом, которые не поддаются консервативному лечению. На поздних стадиях заболевание может привести к компрессии спинного мозга или нервных корешков с радикулопатией и слабостью или онемением конечностей. Повышения температуры тела, как правило, не наблюдается.
Диагностика остеомиелита
При подозрении на остеомиелит необходимо выполнить следующие лабораторные исследования:
-
общий анализ крови и определение скорости оседания эритроцитов;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
С-реактивный белок – белок острой фазы, чувствительный индикатор повреждения тканей при воспалении, некрозе, травме. Синонимы: Анализ крови на СРБ; С-реактивный белок сыворотки крови. C-reactive Protein (CRP), quantitative; C-reactive protein test; CRP test. Краткое описание опред.
Рентгенологическое исследование считается одним из наиболее эффективных методов диагностики остеомиелита. Признаки патологии у детей видны на снимке уже на 5-й день, а у взрослых — только через 2 недели от начала воспалительного процесса.
Самым точным и эффективным видом диагностики является радионуклидная сцинтиграфия костей. С помощью специальных препаратов, накапливающихся в зоне очага болезни, можно точно выявить начало поражения кости. Однако этот метод не позволяет провести дифференциальную диагностику между инфекцией, переломами и опухолями.
Скопление гноя в мягких тканях выявляют с помощью ультразвукового исследования.
Исследование мягких тканей для выявления патологических изменений и диагностики новообразований.
Для лечения большое значение имеет биопсия очага воспаления костной ткани (аспирационная или открытая) и посев гнойного отделяемого на флору с определением чувствительности к антибиотикам и бактериофагам.
Синонимы: Wound/tissue Culture. Aerobic Bacteria Identification and Antibiotic Susceptibility extended testing. Краткое описание исследования «Посев раневого отделяемого и тканей на микрофлору и определение чувствительности к расширенному спектру антимикробных препаратов» Микробиолог.
Синонимы: Wound/tissue Culture. Aerobic Bacteria Identification. Antibiotic Susceptibility and Bacteriophage Efficiency testing. Краткое описание исследования «Посев раневого отделяемого и тканей на микрофлору, определение чувствительности к антимикробным препаратам и бактериофагам» .
К каким врачам обращаться
Лечение остеомиелита
Консервативные методы лечения в большинстве случаев стандартизированы и включают антибиотикотерапию с определением микробного возбудителя и чувствительности микроорганизмов к антибактериальным препаратам, противовоспалительную терапию. Большое значение имеет проведение иммуномодулирующей терапии, в том числе с использованием методов квантовой гемотерапии (реинфузия обработанной ауто- и донорской крови и др.), а в отдельных случаях гормонотерапии.
В большинстве случаев хирургическое лечение остеомиелита направлено, прежде всего, на ликвидацию очага гнойно-некротического поражения, замещение остаточных полостей или образовавшихся дефектов.
При остром гематогенном остеомиелите начальная антибиотикотерапия должна включать полусинтетические пенициллины или ванкомицин и цефалоспорины 3-го или 4-го поколения. При хроническом остеомиелите, возникающем в результате распространения инфекции с окружающих мягких тканей, особенно у больных диабетом, лечение проводят с использованием препаратов, эффективных как против грамположительных и грамотрицательных аэробов, так и против анаэробной флоры.
Осложняет лечение хронической формы заболевания нарушение кровоснабжения кости, которое затрудняет проникновение антибактериальных препаратов, снижает эффективность местного иммунного ответа в костной ткани.
Некоторые симптомы остеомиелита свидетельствуют о том, что болезнь перешла в крайне тяжелую форму. Нередко единственным выходом в этой ситуации становится хирургическое вмешательство. Главная его цель — удаление гнойного очага воспаления. Это в разы ускоряет процесс выздоровления и улучшает общее самочувствие больного.
Показания к операции:
- гнойная форма заболевания;
- флегмона надкостницы;
- наличие свищей и секвестров;
- обширное гнойное течение заболевания.
В последние годы широко разрабатываются методы закрытия костной полости, такие как мышечная или кожно-мышечная пластика.
Существуют современные методы, которые позволяют сохранить имплантаты при остеосинтезе (хирургической репозиции костных отломков при помощи различных фиксирующих металлических конструкций) в случае ранних нагноений. Это вакуумная терапия, применение гидрохирургической системы, ультразвуковой кавитации и других методов обработки ран, которые дают возможность предотвратить развитие так называемой бактериальной биопленки на поверхности имплантата, что, в свою очередь, позволяет сохранить имплантат и конечность.
Остеомиелит – тяжелое заболевание, поэтому даже при своевременном и компетентном лечении есть риск возникновения нежелательных последствий. Остеомиелит кости может вызвать как самостоятельные осложнения, так и такие, которые возникают как следствие хирургического вмешательства. Некоторые из них требуют отельного лечения. Прогрессирование гнойно-воспалительного процесса приводит к разрушению костной ткани, нарушается ее кровоснабжение, что еще больше усиливает некротические процессы в кости. Заболевание может вызвать такие нарушения:
- развитие абсцессов и свищей, нарывов в мягких тканях и на коже;
- возникновение флегмоны — пропитывания мышечных волокон гноем;
- развитие артрита с образованием гнойных масс в полостях;
- самопроизвольные переломы;
- анкилозные сращивания суставных частей;
- контрактурная неподвижность мышечных соединений.
Гнойно-воспалительные поражения костей приводят к инвалидизации около 55% пациентов. Остеомиелит может закончиться потерей конечности, если речь идет о поражении руки или ноги.
В связи с особенностью локализации остеомиелитического процесса у детей в последующем может наблюдаться замедление развития костей за счет повреждения воспалительным процессом зон роста.
Разрушение позвонков, сдавливание спинного мозга может приводить к двигательным и чувствительным нарушениям.
Профилактика остеомиелита
Для снижения риска развития остеомиелита рекомендуется:
- своевременно реагировать на возникновение инфекционных процессов в организме;
- проводить лечение гайморита, кариеса, воспаления носоглотки и верхних дыхательных путей;
- осуществлять тщательную обработку ран, обморожений и ожогов, чтобы исключить возможность их инфицирования;
- вести здоровый образ жизни, избегать чрезмерных физических нагрузок, недоедания, следить за сбалансированностью питания;
- не допускать переохлаждения организма.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хроническое воспаление – один из главных биологических маркеров старения и элементов патогенеза возрастных заболеваний. В обзоре рассмотрены молекулярно-генетические механизмы персистирующего системного воспаления, сопровождающего физиологическое старение
Хроническое воспаление при старении
Fumihiro Sanada1, Yoshiaki Taniyama1,2*, Jun Muratsu1,2, Rei Otsu1, Hideo Shimizu1, Hiromi Rakugi2 and Ryuichi Morishita1*
1Department of Clinical Gene Therapy, Graduate School of Medicine, Osaka University, Suita, Japan
2Department of Geriatric and General Medicine, Graduate School of Medicine, Osaka University, Suita, JapanОригинал статьи: © 2018 Sanada, Taniyama, Muratsu, Otsu, Shimizu, Rakugi and Morishita, распространяется по лицензии CC BY 4.0.
Перевод статьи: © 2021 ООО «Издательство «Открытые системы», распространяется по лицензии CC BY-NC-ND 4.0.
Аннотация
Хроническое воспаление – один из главных биологических маркеров старения и элементов патогенеза возрастных заболеваний. В обзоре рассмотрены молекулярно-генетические механизмы персистирующего системного воспаления, сопровождающего физиологическое старение
Ключевые слова: Хроническое Воспаление, Старение, Клеточное Старение, Старение Иммунитета, Провоспалительные Цитокины, Система Свертывания Крови, Дисбактериоз Кишечника, Chronic Inflammation, Aging, Cell Senescence, Immunosenescence, Proinflammatory Cytokines, Coagulation System, Gut Dysbiosis
В процессе биологического старения системное воспаление прогрессирует в отсутствие патогенных факторов («воспалительное старение», «inflammaging») и характеризуется резистентностью к гиполипидемической (снижение уровня липопротеинов низкой плотности, ЛПНП) и гипотензивной (контроль активности ренин-ангиотензиновой системы, РАС) терапии.
При клеточном старении центральными звеньями патогенеза хронического воспаления являются иммунная дисрегуляция и нарушение активности системы свертывания крови. Обзор посвящен рассмотрению молекулярно-генетических механизмов персистирующего системного воспаления, сопровождающего физиологическое старение, и его роли в патогенезе возрастных заболеваний.
Введение
Системное воспаление при старении – один из главных элементов патогенеза сердечно-сосудистых, эндокринных и онкологических заболеваний (1), распространенность которых неуклонно растет с каждым годом. Несмотря на центральную роль немедикаментозной терапии (изменение образа жизни и рациона питания, снижение влияния сопутствующих факторов риска) в профилактике возрастных заболеваний, требуется разработка фармакологических подходов, основанных на регуляции ключевых клеточных и молекулярных механизмов, участвующих в прогрессировании хронического воспаления.
Важную роль в прогрессировании хронического воспаления играют диетические факторы, старение клеток, снижение уровня половых гормонов и курение. Кроме того, в процессе старения наблюдается повышение уровня циркулирующих провоспалительных факторов, включая интерлейкин-6 (ИЛ-6) и фактор некроза опухоли-α (ФНО-α) (2), способствующих повреждению ДНК, развитию мышечной атрофии, метаболических нарушений и онкологических заболеваний. Повышение образования и секреции ИЛ-6 и ФНО-α при старении также наблюдается в адипоцитах висцеральной жировой ткани (3, 4), увеличение количества макрофагов в которых пропорционально значениям индекса массы тела (ИМТ) и является важным биомаркером хронического воспаления и предиктором инсулинорезистентности у людей с ожирением (5, 6). Среди факторов внешней среды повышению уровня провоспалительных цитокинов – ИЛ-6, ФНО-α и интерлейкина-1-β (ИЛ-1-β) – в крови способствуют хроническое воздействие сигаретного дыма, психоэмоциональный стресс и воспалительные заболевания полости рта (7). Однако системное воспаление низкой интенсивности персистирует даже после коррекции провоспалительного статуса – уровня ЛПНП и активности РАС – и отказа курения, что указывает на существование секреторного фенотипа клеток, ассоциированного со старением (senescent associated secretory phenotype, SASP) и иммунологического импринтинга. В обзоре рассмотрены данные о ключевых биомаркерах, молекулярных механизмах и сигнальных каскадах, участвующих в развитии системного воспаления низкой интенсивности в процессе биологического старения (Рис. 1).
![Хроническое воспаление при старении]()
Рисунок 1. Молекулярные элементы системного воспаления, ассоциированного со старением: старение клеток, нарушение гемостаза, накопление клеточного детрита (в т.ч. циркулирующей митохондриальной ДНК, цмДНК), дисбактериоз и иммунная дисфункция. Дополнительные факторы: возраст, окислительный стресс, циркулирующие микроРНК и агалактозилированные N-гликаны.
Источники медиаторов хронического воспаления при старении
Острое воспаление – ключевой компонент в механизме формирования иммунного ответа на воздействие патогена или повреждение тканей и активации регенерации тканей. Системное воспаление низкой интенсивности, наоборот, вызывает хроническое повреждение клеток, способствуя развитию дегенеративных изменений в тканях (8). Воздействие провоспалительных цитокинов – ИЛ-6, ИЛ-1-β и ФНО-α – на структуры нервной и костно-мышечной систем (9) приводит к снижению активности анаболических процессов, опосредованных действием инсулина и эритропоэтина, вызывая развитие саркопении (10).
Клеточный детрит и накопление иммуноглобулинов
Накопление клеточного детрита и иммуноглобулинов в результате нарушения метаболических процессов в клетках стимулируют активацию иммунной системы и развитие системного воспаления. Важную роль в регуляции межклеточных и межмолекулярных взаимодействий и активности иммуноглобулинов играет гликозилирование – один из наиболее распространенных типов посттрансляционной модификации, основанный на присоединении углеводных остатков к аминокислотам (напр., к азоту аспарагиновых остатков в N-гликанах) (11, 12). Данные клинических (13–15) и экспериментальных исследований на животных (16–18) демонстрируют повышение уровня агалактозилированных N-гликанов, не имеющих в составе остатка галактозы в позиции Asn297 Fc-фрагмента IgG (IgG-G0), у пациентов с синдромом Гетчинсона-Гилфорда (прогерия) и некоторыми аутоиммунными заболеваниями.
Провоспалительный эффект IgG-G0 реализуется посредством усиления лектинового пути активации комплемента, связывания с Fcγ-рецепторами и образования агрегатов аутоантител. Кроме того, накопление IgG-G0 с возрастом служит независимым предиктором гиперактивации иммунной системы и развития системного воспаления.
Дополнительным биомаркером старения является митохондриальная дисфункция и высвобождение молекулярных паттернов, ассоциированных с повреждением (МПАП; damage-associated molecular patterns). Рядом исследований показана роль циркулирующих митохондриальных МПАП в патогенезе хронического воспаления и дегенеративных заболеваний (19, 20).
Старение сопровождается снижением барьерной функции эпителиальной выстилки кишечника и ротовой полости (21, 22), что способствует развитию дисбактериоза. Качественные и количественные изменения нормального состава кишечной микробиоты в процессе старения – снижения числа представителей «противовоспалительной» микрофлоры (напр., Clostridium XIVa, Bifidobacterium spp., F. prausnitzii) и увеличением количества условно-патогенных микроорганизмов (напр., Streptococcus spp., Staphylococcus spp., Enterococcus spp., Enterobacter spp.; 23) – может повышать уязвимость пожилых людей к инфекциям. Например, количество бактерий рода Bifidobacterium отрицательно коррелирует с уровнем провоспалительных цитокинов – ФНО-α и ИЛ-1β – в плазме крови.
Нарушение баланса микрофлоры кишечника в большинстве случаев вызвано особенностями рациона питания и наиболее выражено у пожилых лиц, длительно находящихся в учреждениях стационарного социального обслуживания по сравнению с пациентами в частных домах престарелых (24).
Старение клеток
Клеточное старение – необратимая остановка клеточного цикла и потеря способности клетки к делению. Остановка клеточной пролиферации происходит в результате ряда молекулярно-генетических изменений, включая укорочение теломер, генотоксический стресс, действие митогенных стимулов и провоспалительных цитокинов, активацию белка-супрессора опухоли p53 и/или ингибитора циклин-зависимой киназы p16 (25). С возрастом в различных тканях и органах увеличивается количество клеток, утративших способность к пролиферации и приобретающих секреторный фенотип, ассоциированный со старением. Это сопровождается высвобождением провоспалительных цитокинов и инициацией системного воспаления и лежит в основе патогенеза атеросклероза, онкологических заболеваний и сахарного диабета (26–28).
В исследованиях на животных неоднократно показана центральная роль процесса клеточного старения в прогрессировании дегенеративных заболеваний, включая атеросклероз и остеоартрит (29–31). Удаление стареющих клеток и контроль провоспалительных каскадов, участвующих в приобретении клетками секреторного фенотипа, ассоциированного со старением, может служить потенциальной терапевтической мишенью при разработке подходов к профилактике и терапии возрастных заболеваний.
Старение иммунной системы
Дисрегуляция системы врожденного иммунитета и активация воспалительного ответа является ключевым механизмом старения иммунной системы («иммуно-старение»; 32), который приводит к повышению уязвимости пациентов пожилого возраста к аутоиммунным, инфекционным и онкологическим заболеваниям, снижению иммунного ответа на вакцинацию и ухудшению регенерации тканей (33, 34). Хронические воспалительные заболевания, в свою очередь, также способствуют снижению количества клеток и нарушению функций иммунной системы. В частности, в процессе старения наблюдаются изменения характера экспрессии паттерн-распознающих рецепторов (pattern recognition receptors), активация которых при связывании с эндогенными лигандами – маркерами повреждения клеток – стимулирует секрецию провоспалительных цитокинов и прогрессирование хронического воспаления.
Таким образом, наряду с клеточным старением, возрастное снижение функции врожденной иммунной системы является важным элементом патогенеза системного воспаления низкой интенсивности при старении.
Система гемостаза: факторы свертывания крови и фибринолиза
Развитию возрастных заболеваний – атеросклероза и фиброза легких – у пациентов пожилого возраста способствует повышенная активация системы свертывания крови и стимуляция процесса фибринолиза, которые вызывают развитие хронического воспаления через активацию рецепторов, активируемых протеазами (protease-activated receptors, PAR; 35–38).
Увеличение сердечно-сосудистого риска, в частности риска развития тромботических заболеваний, с возрастом связано с повышением уровня факторов свертывающей системы плазмы крови I, V, VII, VIII и IX (39, 40) и концентрации фактора X в атеросклеротических бляшках эндотелиальных, гладкомышечных и иммунных клеток (41). Результаты клинического исследования ATLAS ACS 2–TIMI 51 Investigators показали, что высокоселективный прямой ингибитор фактора Xa ривароксабан снижает риск инфаркта миокарда, инсульта и сердечно-сосудистую смертность у пациентов с ишемической болезнью сердца (42). Увеличение активации системы свертывания крови и содержания фибриногена в плазме крови, наоборот, способствует развитию тромбоза, а повышение уровня фактора коагуляции Xa и тромбина усиливает провоспалительный каскад и вызываемую тромбином PAR-1/2-опосредуемую активацию тромбоцитов (43). Патогенетическая роль PAR-1/2-опосредованной сигнализации FXa и фибринолитического фактора плазмина в процессах клеточного старения и системного воспаления реализуется посредством повышения экспрессии протеина, связывающего инсулиноподобный фактор роста 5 (IGFBP-5; 37, 41, 44, 45). Как показали результаты работы Kojima et al., IGFBP-5, белок семейства сигнальных трансдукторов и активаторов транскрипции (STAT3), участвует в активации ИЛ-6-индуцированного образования активных форм кислорода (АФК), повреждению ДНК и гибели фибробластов (46).
IGFBP-5-опосредованная активация сигнального пути MAPK и транслокация EGR-1 в ядро приводит к активации транскрипции генов медиаторов воспаления и развитию фиброза, способствуя прогрессированию фибротического фенотипа (47). Важным звеном механизма старения гладкомышечных и эндотелиальных клеток является активация пути EGR-1-IGFBP-5-p53 с участием белков раннего ответа при повышении каталитической активности FXa (37). Все эти данные демонстрируют центральную роль IGFBP-5 в регуляции процессов «воспалительного старения», гиперкоагуляции и старения клеток (Рис. 2).
Учитывая равное распределение FXa- и IGFBP-5-положительных областей в атеросклеротических бляшках (41), можно утверждать, что, как и тромбин, местный синтез фактора коагуляции Xa является ключевым индуктором экспрессии IGFBP-5 и патогенетическим фактором SASP-опосредованного клеточного старения (41, 48).
![Хроническое воспаление при старении]()
Рисунок 2. Активация каскада свертывания крови в патогенезе клеточного старения и хронического воспаления.
Заключение
В норме элиминация патогенного фактора позволяет устранить воспаление и активировать регенерацию поврежденных тканей. Однако с возрастом хроническое воспаление низкой интенсивности прогрессирует в отсутствие инфекционного агента, способствуя развитию деструктивных изменений в тканях и органах. Хроническое повышение уровня провоспалительных медиаторов при системном воспалении является ведущим фактором риска развития онкологических, сердечно-сосудистых и нейродегенеративных заболеваний, сахарного диабета II типа, саркопении и остеопороза у пожилых пациентов. Учитывая многофакторную природу процесса старения, существующие методы симптоматической и противовоспалительной терапии возрастных заболеваний в большинстве случаев не позволяют достигнуть устойчивого снижения прогрессирования дегенеративных процессов, что делает актуальным разработку методов «сенолитической» терапии, направленной на селективное устранение стареющих клеток (49–52).
Список литературы
Дисклеймер: все утверждения, высказанные в статье, относятся к суждениям авторов и необязательно согласуются с точкой зрения аффилированных организаций, издателя, редакторов и рецензентов. Любой продукт или утверждение производителя не гарантируются и не поддерживаются издателем.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Фиброз: причины появления, симптомы, диагностика и способы лечения.
Определение
Фиброз — особое патологическое состояние, при котором происходит аномальное избыточное разрастание соединительной ткани с появлением рубцовых изменений в различных органах. В результате активного роста клеток, которому предшествует воспалительный процесс, при нарушении механизмов заживления в пораженных тканях образуются рубцы. Фиброз рассматривается как реакция организма, направленная на изоляцию очага воспаления от окружающих тканей и системного кровотока и препятствующая его дальнейшему распространению по организму.
Рубцовая ткань состоит преимущественно из коллагена и отличается от тканей, которые она замещает, сниженными функциональными свойствами. Например, рубцы на коже более чувствительны к ультрафиолетовому излучению, в них отсутствуют потовые железы и волосяные фолликулы, а рубец в сердечной мышце после инфаркта миокарда не участвует в сокращении сердца и может приводить к сердечной недостаточности.
Фиброз способен поражать любые ткани и органы, но чаще всего встречается фиброз легких, печени, почек и сердца.Причины появления фиброза
Причинами фиброза могут стать инфекционные и вирусные заболевания, нарушения обменных процессов, аллергические реакции, облучение, травмы, хирургическое вмешательство, воспалительные процессы, воздействие некоторых лекарственных препаратов, токсических веществ, а также определенные генетические и неинфекционные заболевания (например, жировая болезнь печени может привести к ее фиброзным изменениям).
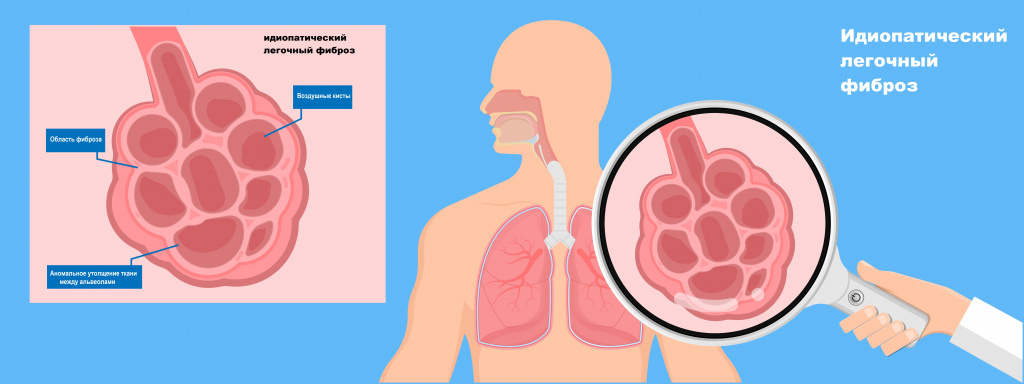
Легочный фиброз (пневмосклероз) относится к состояниям, при которых снижается эластичность и растяжимость легочной ткани, затрудняется прохождение кислорода и углекислого газа через стенку альвеол (легочных пузырьков, в которых происходит контакт вдыхаемого воздуха с кровью). Может возникать как вторичное состояние при других заболеваниях, но в большинстве случаев его основная причина не ясна, поэтому используется термин идиопатический легочный фиброз.
![Идиопатический фиброз.jpg]()
Фиброз печени
Фиброз печени - это рубцовая ткань и узелки, которые замещают ткань печени и нарушают ее функцию. Состояние обычно сопровождает алкоголизм, жировую болезнь печени, гепатит B или C. Каждый раз, когда печень подвергается стрессу или травме, запускается процесс регенерации и при этом образуется рубцовая ткань.По мере нарастания рубцовой ткани функция печени ухудшается, а при прогрессировании фиброза развивается цирроз печени.
Сердечный фиброз
Фиброз формируется в тех областях сердца, которые были повреждены в результате инфаркта миокарда. Сердечный фиброз увеличивает риск сердечной недостаточности.Фиброз средостения
Эта форма фиброза характеризуется кальцинированным фиброзом лимфатических узлов, который может блокировать дыхательные каналы и кровеносные сосуды.Фиброз забрюшинной полости
Относится к фиброзу мягких тканей забрюшинного пространства - аорты, почек и других структур.
Фиброз костного мозга
Миелофиброз - это рубцы в костном мозге, которые препятствуют нормальному образованию клеток крови.
Рубцовая ткань, которая образуется на коже в ответ на травму, называется келоидом.
Склеродермия, или системный склероз
Склеродермия - это аутоиммунное заболевание соединительной ткани, которое, в первую очередь, поражает кожу, но также может наблюдаться и в других органах - почках, сердце и легких.
Фиброзная дисплазия кости
Существует мнение, что фиброзная дисплазия кости развивается из-за мутации в генах. В основном болезнь показывает себя при рождении, хотя описаны редкие случаи, когда ее первые проявления диагностировались у взрослых пациентов.
Фиброзные изменения при новой коронавирусной инфекции COVID 19
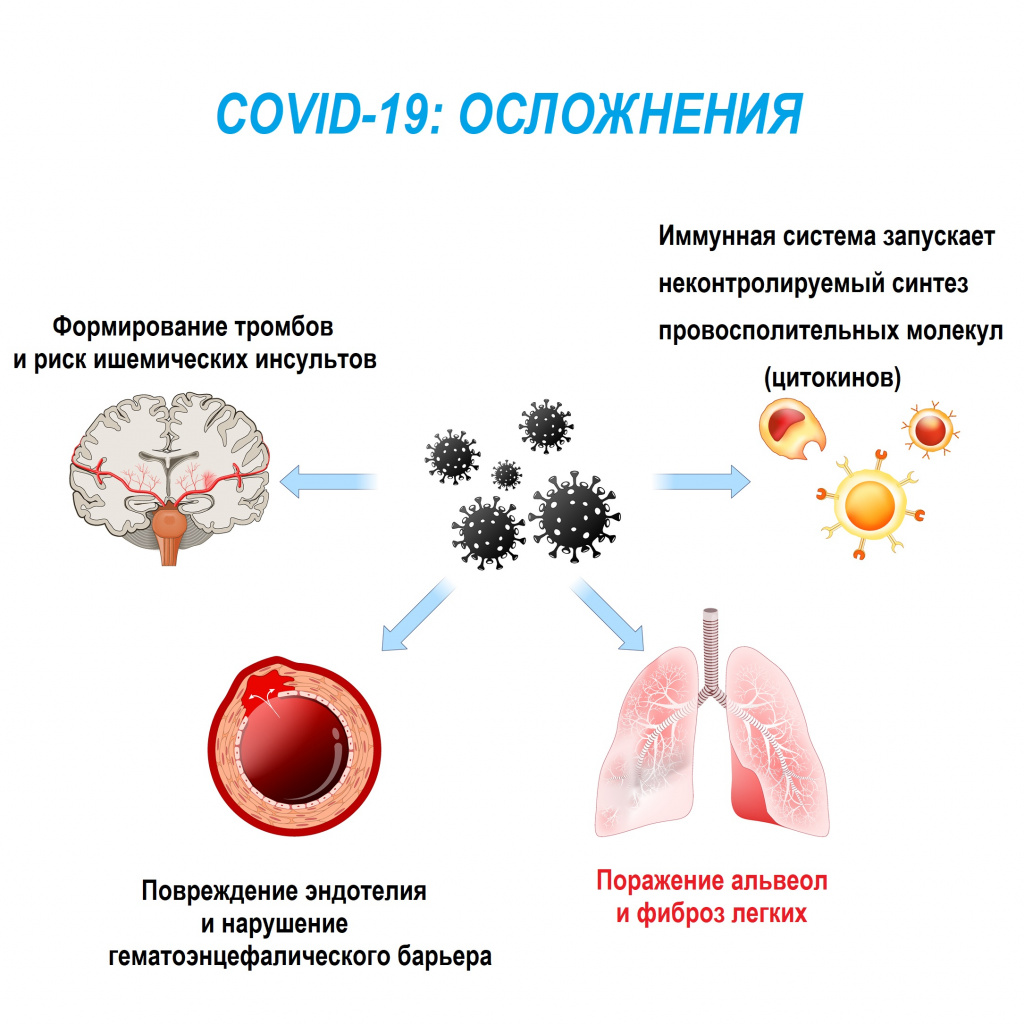
Особую актуальность проблема фиброза приобрела в свете последствий распространения новой коронавирусной инфекции. У 27-45% пациентов, перенесших инфекцию, развиваются явления фиброза со стороны дыхательной и сердечно-сосудистой систем, с которыми могут быть связаны большинство неблагоприятных исходов заболевания.
![ковид 19.jpg]()
Особенностью данной инфекции является гипоксия, кислородное голодание. Системный воспалительный ответ, индуцируемый вирусной инфекцией и реализуемый, в том числе, посредством цитокинового шторма, также может затронуть мозг, носоглотку, глаза, сердце, кровеносные сосуды, печень, почки и кишечник, то есть буквально все жизненно важные органы.
Классификация заболевания
Фиброз классифицируют в зависимости от органа, который он захватывает.
- фиброторакс;
- легочный фиброз:
- муковисцидоз,
- идиопатический фиброз легких;
- переходный фиброз – продвинутая стадия фиброза печени, проявляющаяся во время прогрессирующих форм хронических заболеваний печени,
- цирроз.
- глиальный шрам.
- фиброз миокарда:
- интерстициальный фиброз, описанный при застойной сердечной недостаточности, гипертонии и старении организма,
- замещающий фиброз, который указывает на перенесенный инфаркт миокарда.
- артериальная жесткость,
- фиброзная дисплазия кости,
- артрофиброз (коленного, плечевого, других суставов),
- хроническая болезнь почек,
- болезнь Крона,
- контрактура Дюпюитрена,
- келоидные рубцы кожи,
- фиброз средостения,
- миелофиброз костного мозга,
- фиброзные изменения молочной железы,
- болезнь Пейрони,
- нефрогенный системный фиброз кожи,
- прогрессирующий массивный фиброз легких - осложнение пневмокониоза угольщиков,
- забрюшинный фиброз,
- склеродермия / системный склероз,
- некоторые формы адгезивного капсулита.
- Локальное разрастание соединительной ткани – очаговый фиброз. Патология имеет четкие границы, возможно появление нескольких очагов фиброза на одном типе ткани. Очаговый фиброз также может рассматриваться как начальная стадия диффузного фиброза.
- Тотальный, или диффузный фиброз – характеризуется обширным поражением ткани различных органов. Диагностируется на поздних стадиях развития процесса.
- Кистозный фиброз. Рассматривается специалистами как отдельная патология, которая развивается в результате обменных нарушений.
Пневмофиброз чаще всего проявляется одышкой, которая сначала возникает только во время активных физических нагрузок, а по мере прогрессирования процесса даже в покое. Состояние пациента характеризуется как средней тяжести: поступают жалобы на слабость и быструю утомляемость. При выраженном патологическом процессе развивается сопутствующее заболевание - легочное сердце. Наиболее часто фиброз формируется в корнях легких и крупных бронхах.
Фиброз печени проявляется развитием гипертензии печеночного генеза (портальной гипертензии). Этот вид гипертензии плохо купируется, у больного появляются отеки, асцит (скопление жидкости в брюшной полости), увеличиваются печень и селезенка. Пациенты жалуются на чувство тяжести в правом боку, выраженный кожный зуд. В дальнейшем манифестируют различные кожные высыпания.
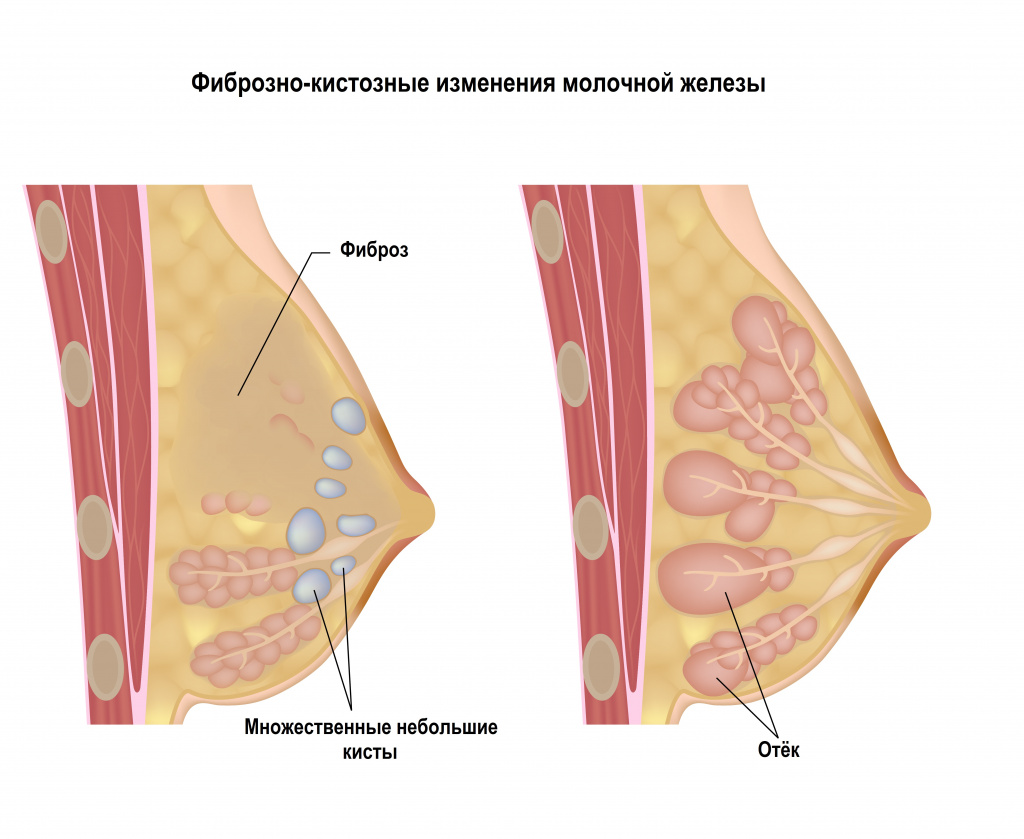
Фиброз молочной железы (развивается только у женщин) характеризуется хорошо пальпируемыми уплотнениями в молочной железе. Внешне такой фиброз может проявляться гиперемией кожного покрова над местом поражения.
![Молочные железы.jpg]()
При фиброзе матки (фиброматозе матки) ее структурные слои заменяются соединительной тканью. Женщину могут беспокоить кровянистые выделения в середине цикла, более сильные болезненные ощущения во время менструации, дискомфорт при половом акте.
Фиброз сухожилий может привести к таким состояниям, как контрактура Дюпюитрена (ладонный фиброматоз), которая вызывает деформацию пальцев рук.
Диагностика фиброза
В зависимости от локализации и причины фиброзных образований могут потребоваться различные диагностические процедуры:
Исследование молочных желез, позволяющее оценить структуру органа, для диагностики и выявления заболеваний молочных желез у женщин на ранних стадиях.
![Язва желудка]()
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Язва желудка – одно из самых распространенных заболеваний желудочно-кишечного тракта. Это хроническая патология, при которой возникают дефекты в слизистой оболочке желудка. При несвоевременном лечении или полном его отсутствии может стать причиной инвалидности человека или даже гибели.
Язвой желудка и двенадцатиперстной кишки страдают люди в возрасте от 20 до 65 лет. Мужчины от 25 до 40 лет болеют в 5-6 раз чаще женщин по той причине, что мужские половые гормоны косвенно повышают кислотность и агрессивность желудочного сока, а женские — понижают.
Строение человеческого желудка
Желудок – это орган пищеварительной системы, в котором скапливается пища, и под действием желудочного сока, подвергается первичному перевариванию с образованием кашицеобразной смеси.
Желудок по большей части располагается в верхней левой области брюшной полости. Определённой формой и размером желудок не обладает, так как они зависят от степени его наполнения, состояния его мышечной стенки (сокращённая или расслабленная) и возраста. Вместительность органа около 3 литров, длиной 21-25 см.
Желудок обладает двумя основными функциями:
- Секреторной. Выведение желудочного сока, который содержит необходимые компоненты для начальных этапов пищеварения и образования химуса (пищевого комка). За сутки примерно выделяется около 2 литров желудочного сока. При расстройстве секреторной функции желудка, у человека повышается кислотность, т.е. усиливается выделение соляной кислоты, либо снижается кислотность, сопровождаясь уменьшением выделение соляной кислоты.
- Моторной. Мышечный слой желудка сокращается, в результате чего происходит перемешивание пищи с желудочным соком, первичное переваривание и продвижение по двенадцатиперстной кишке.
Нарушения моторики желудка из-за нарушения тонуса его мышечной стенки приводит к нарушению пищеварения и эвакуации желудочного содержимого в кишечник. Это проявляется различными диспепсическими нарушениями (тошнота, рвота, вздутие, изжога и другие).
Механизм образования язвы желудка
Язва желудка, представляет собой дефект слизистой оболочки желудка, редко меньше 1см (иногда подслизистой), окружённый воспалительной зоной.
Наиболее частой причиной образования язв желудка и двенадцатиперстной кишки является инфекция Helicobacter Pylori. Различные факторы приводят к дисбалансу между защитными факторами (желудочная слизь, гастрит, секретин, гидрокарбонаты, слизисто-эпителиальный барьер желудка и другие) слизистой желудка и факторами агрессии (Helicobacter Pylori, соляная кислота и пепсин).
Под действием лечения, дефект зарастает соединительной тканью (образуется рубец). Участок, на котором образовался рубец, не обладает функциональной способностью (секреторной функцией).
Причины развития патологии
Бактерия Helicobacter Pylori (возбудитель язвы) – оказывает разрушающее действие на клетки слизистой желудка, разрушает местные факторы защиты. В результате чего образуется такой дефект, как язва. Заражение бактерией через слюну инфицированного человека (несоблюдение правил личной гигиены, использование немытой посуды после инфицированного человека).
Повышенная кислотность – развивается в результате усиленного выделения соляной кислоты, которая оказывает разъедающее действие на слизистую оболочку желудка, с последующим образованием дефекта.
Что влияет на образование язвы желудка?
- Нервно-эмоциональное перенапряжение приводит к повышению выделения желудочного сока (соляной кислоты).
- Генетическая предрасположенность к образованию язвы желудка.
- Курение, употребление алкогольных напитков, потребление кофе в больших количествах, никотин и этиловый спирт стимулируют образование желудочного сока, тем самым повышая кислотность.
- Наличие предъязвенного состояния: хронический гастрит, хроническое воспаление слизистой желудка.
- Нарушенный режим питания: еда в сухомятку, длительные перерывы между приёмами пищи приводят к нарушению выделения желудочного сока.
- Злоупотребление кислой, острой и грубой пищи.
- Длительный приём медикаментов, которые оказывают разрушительное действие на слизистую желудка.
Симптомы язвы желудка
- Болезненные ощущения. Боль при язве может беспокоить днём и ночью. Чаще всего боль при патологии проявляется во время голода. Она локализуется в верхних отделах живота, может уменьшаться или усиливаться сразу, или через время после приёма пищи в зависимости от места расположения язвенного дефекта.
Неприятные признаки язвы желудка могут быть настолько ярко выраженными, что появляется тошнотой или даже рвотой, которая усиливается с утра и проходит после приема пищи. Язва проявляет себя чаще в осенне-весенние периоды.
- Чувство тяжести в желудке. Человек часто начинает уменьшать порции еды, так как поглощение даже небольшого количества пищи, которая попадает на воспалённые участки слизистой желудка и язвы, может вызывать эти неприятные ощущения.
- Запах изо рта, налет на языке. Частые спутники любых воспалительных заболеваний верхних отделов желудочно-кишечного тракта, в том числе и гастрита (воспаления желудка), на фоне которого язвы чаще всего и появляются.
Диагностика язвы желудка
Диагностика типичной язвы желудка достаточно проста, проводится терапевтом или гастроэнтерологом. При осмотре врач определяет общее состояние пациента, выясняет жалобы, характер и особенности течения болезни, при пальпации уточняет границы болезненных зон и их характер.
Чтобы сформировать точное представление о состоянии здоровья пациента, врач может назначить общий анализ крови и инструментальное обследование. Чаще всего это эндоскопическое исследование (ЭГДС).
Процедура безопасна, длится несколько минут, сопровождается неприятными, но вполне переносимыми ощущениями. Позволяет обследовать верхние отделы желудочно-кишечного тракта, установить наличие и характер воспалительных и эрозивно-язвенных процессов, а также появление новообразований.
Лечение язвы желудка
Лечением язвенной болезни занимается терапевт или гастроэнтеролог. Оно направлено на устранение симптомов, заживление язв и ликвидацию причины этого заболевания с помощью диеты, изменения образа жизни и назначения медикаментов.
Медикаментозная терапия
Для избавления от инфекции Хеликобактер Пилори врач назначает антибиотики, а для снижения кислотности желудочного сока — кислотоснижающие препараты и др. Если язва желудка вызвана приёмом обезболивающих препаратов (НПВС) или иных медикаментов, которые могут спровоцировать развитие язвы, то врач подбирает пациенту другие препараты, у которых нет язвообразующего действия.
Сначала снимается боль с помощью обезболивающих. Принимаются препараты только при ощущении дискомфорта в желудке. Также прописываются энтеросорбенты, которые нейтрализуют негативное действие токсинов. Кроме того, больному необходимо пропить курс витаминов.
Питание
Важно при язве желудка не обострять симптомы при помощи вредных привычек. Нужно перестать курить и употреблять спиртные напитки. А также следить за своим питанием. При язве желудка должна быть назначена специальная диета.
Она предполагает полноценное питание, разделённое на 5-6 приёмов пищи в день. Ограничивается употребление сильных раздражителей желудочной секреции (кетчупов, острых специй), грубых продуктов и блюд. Пища готовится в основном протёртой, варится на пару или в воде, рыба и негрубые сорта мяса подаются кусками. Из рациона исключаются очень холодные и горячие блюда. Ограничивается приём поваренной соли.
Появление избыточного количества соляной кислоты в желудке ведет к тому, что возникают боли, пациента мучает изжога. Необходима вода, которая обладает ощелачивающим эффектом – при ее применении вредное воздействие соляной кислоты нейтрализуется.
Противоположная проблема – пониженная кислотность. В этом случае желудочного сока вырабатывается мало. Итог: пища плохо переваривается, возникает ощущение переполнения желудка.
Щелочные минеральные воды ускоряют обработку пищи и способствуют быстрому продвижению ее по желудочно-кишечному тракту.
Профилактика язвы желудка
При здоровом образе жизни, правильном питании, бережном отношении к своему здоровью вероятность появления язвы желудка крайне низкая. Как мы уже выяснили, к развитию язвы желудка приводят нарушения сна и питания, чрезмерно активный образ жизни, а также несоблюдение правил личной гигиены.
Если у родственников была язвенная болезнь, то независимо от жалоб рекомендована ЭГДС с определением кислотности желудочного сока, уточняющими биопсиями для определения инфекции H. Pylori и гистологическим изучением подозрительных участков хотя бы раз в 2 года.
Также нужно придерживаться здорового образа жизни: отказаться от вредных привычек, быть физически активным, спать ночью не менее 7 часов. Избегать стрессовых ситуаций, учиться правильно их воспринимать.
Регулярно посещать врача в рамках диспансеризации и устранять очаги хронической инфекции. Начиная с 25 лет раз в два года проходить плановое комплексное эндоскопическое обследование — ЭГДС с определением H. Pylori.
Где пройти диагностику и лечение язвенной болезни желудка в Красноярске?
Для вас работает частная медицинская клиника «Медюнион» на Никитина. Мы занимаемся профилактикой, диагностикой и лечением язвы желудка. Наши специалисты проведут комплексное обследование на новейших аппаратах, в стерильно чистых кабинетах.
Для записи заполните онлайн-форму обратной связи, указанную на сайте, или позвоните и уточните информацию по номеру телефона клиники 201-03-03.
![You are currently viewing Воспаление. Распространение. Последствия. Принципы лечения. Часть 8]()
Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 26.11.2020
- Reading time: 4 минут чтения
Воспаление всегда начинается с изменения. Через некоторое время процессы инфильтрации, протеолиза, некроза и синяков уменьшаются или прекращаются, и на первый план выходит регенерация тканей.
Наибольшее повреждение тканей вызывает гнойное воспаление. После эвакуации гноя в тканях остается полость (тканевой дефект), которая постепенно заполняется соединительнотканными элементами – происходит разрастание соединительной ткани.
Разрастанию соединительной ткани в месте воспаления способствует особый материал, присутствующий в повышенных количествах в воспаленных тканях и экссудате, активаторы роста, возникающие в результате процессов изменения, снижение хилона (ингибиторы пролиферации), пролиферация cAMF и слабый ацидоз.
В условиях слабого ацидоза для диссоциации оксигемоглобина на ткани требуется более высокое парциальное давление кислорода, чем обычно – кривая диссоциации Hb02 смещается вправо. Это уже начало следующей фазы – регенерации. Все интенсивно пролиферирующие ткани нуждаются в большом количестве воды, и регенерация соединительной ткани также начинается в гипергидратационных условиях (фаза гипергидратации).
Микрофаги в очаге воспаления постепенно погибают, и начинают преобладать макрофаги. Повышается фагоцитарная активность этих клеток, они фагоцитируют мертвые клетки и другие продукты изменения. В очаге воспаления один тип клеток заменяет другой (микрофаги – макрофаги – фибробласты), каждый из которых выполняет свою функцию, а затем отдает свое место другому типу клеток.
Таким образом, основные изменения соединительной ткани в очаге воспаления – это разрастание макрофагов, фибробластов и гистиоцитов, образование капилляров (2-3 дня) и развитие волокон соединительной ткани (3-6 дней). Дефект ткани постепенно заполняется грануляционной тканью – новой, энергично растущей и богатой сосудами тканью, которая окружает очаг воспаления.
В условиях повышенной активности фагоцитоза, ацидоза, протеолитических и липолитических ферментов уничтожаются микроорганизмы и элементы омертвевшей ткани, ограничивается воспаление, уменьшается экссудация и площадь гиперемии.
После заполнения дефекта ткани кровеносные сосуды и лимфатические сосуды начинают опорожняться (лимфатические сосуды выполняют дренажную функцию для устранения воспалительного отека). Воспалительный отек исчезает, наступает фаза гипогидратации. Происходит регенерация не только соединительной ткани, но и клеток органов и тканей. Однако по мере увеличения числа дифференцированных клеток, интенсивность регенерации снижается.
Если повреждение ткани невелико, регенерация часто бывает полной, тогда как при большом повреждении возникает рубцевание. Клетки высокодифференцированной паренхимы органов (головной мозг, миокард) неспособны к регенерации после травмы. Соединительная ткань часто перерастает в некротическую массу, например, после инфаркта миокарда, плеврита, операций на брюшной полости. Особенно интенсивно разрастается соединительная ткань вокруг инородного тела – вокруг него образуется плотная капсула.
Асептическая рана, края которой соприкасаются, заживает в первую очередь. В этом случае происходит выраженное разрастание макрофагов и интенсивное образование соединительнотканных волокон, которые вместе с эпителиальными клетками замещают фибрин тромба в ране.
Иногда поврежденные клеточные элементы, такие как слизистые оболочки, кожа, способны регенерировать и заполнить дефект определенными тканями, и тогда рана заживает без рубца. Напротив, инфицированные раны, а также асептические раны, если их края не совпадают, заживают вторично, и образуется рубец.
Последствия воспаления
Если регенерация ткани, поврежденной при воспалении, завершена, то функции также полностью восстанавливаются (restitutio ad integrum). Когда определенные ткани заменяются соединительной тканью, функции восстанавливаются только частично (restitutio incpleta). В результате такого воспаления образуется рубе ц, а функции тканей остаются ограниченными (замещение).
![Рубец]()
Рубец
Большой рубец часто негативно влияет на организм. По мере сокращения рубцовой ткани развивается значительная дисфункция органа или конечности. Спайки и рубцы, например, в брюшной полости после перитонита или хирургического вмешательства, стеноз пищевода и желудка после ожога кислотой или щелочью, деформируют органы и нарушают их функцию. Распространены нарушения движений конечностей из-за воспаления нервов, сухожилий и суставов. Также в паренхиматозных органах (легких, печени, поджелудочной железе, почках) часто возникают тяжелые функциональные нарушения после воспаления.
Процессы изменения, которые убивают высокодифференцированные клетки жизненно важных органов, могут угрожать существованию организма. Очень опасны рубцы, например, после воспаления сердечных клапанов или мозговых оболочек.
Биологическое значение воспаления в организме
Уже И. Мечников доказал, что воспаление, усложняющееся в ходе эволюции, является одним из неспецифических механизмов защиты всех организмов от действия патогенного агента. Даже сегодня воспаление считается типичным патологическим процессом, при котором компоненты повреждения и защиты связаны в неразрывное целое, а также во взаимной борьбе.
Вредные для организма процессы – это ухудшение функции и интоксикация, когда нарушаются функции воспаленного органа (ткани). Например, при воспалении сустава движения в нем болезненны и ограничены или даже невозможны.
Воспаление как защитная реакция организма проявляется по-разному. Уже во время смены высвобождаются биологически активные вещества, которые участвуют в сосудистых реакциях и процессах пролиферации. Спазм сосудов предотвращает дальнейшее распространение инфекционного агента в организме. В условиях венозной гиперемии уменьшается кровоток и лимфоток, поэтому токсические и пирогенные вещества дольше задерживаются в очаге воспаления.
Также важен для защиты воспалительный экссудат.
- Из-за кислой среды экссудат является бактерицидным. Его белки связывают бактериальные токсины.
- Экссудат разжижает и ферментативно расщепляет, препятствуя абсорбции и дальнейшему распространению токсинов в организме.
- Экссудат используется для доставки антител к специфическим антигенам в месте воспаления.
Особое значение имеет фагоцитарная и пролиферативная функция клеток соединительной ткани. Грануляционная ткань , образующаяся в процессе пролиферации, и соединительнотканный барьер изолируют воспаление от окружающих тканей. Благодаря этим защитным механизмам подопытному животному можно вводить токсины в очаге воспаления, но заметной реакции организма не происходит. С другой стороны, в здоровых тканях токсины вызывают у животного значительную реакцию или даже гибель.
![Грануляционная ткань]()
Грануляционная ткань
Как и другие типичные патологические процессы в организме, защитная функция воспаления не безгранична. Если действие вредного агента сильное, защитные реакции могут стать ненормальными, вредными для организма. Например, тяжелый фурункулез, разлитой гнойный перитонит, септическое состояние и т. д. нельзя считать положительной защитной реакцией.
Способность реагировать на действие болезнетворных агентов воспалением – очень важный типичный патологический процесс в организме, нарушение которого может иметь опасные последствия. Эти нарушения могут быть связаны с уменьшением количества нейтрофилов (нейтропения) и проблемами с их функцией.
В свою очередь, наиболее частыми причинами тяжелой нейтропении являются лекарственный агранулоцитоз и лейкоз. В редких случаях возникает так называемая циклическая (периодическая) нейтропения, когда каждые 21 день наблюдается значительное снижение количества нейтрофилов. Эта нейтропения чаще встречается у пациентов с инфекционными кожными заболеваниями, отитом и артритом.
Дисфункция лейкоцитов может включать хемотаксис, эмиграцию и фагоцитоз. Например, нарушения хемотаксиса и эмиграции лейкоцитов возникают при диабете, пародонтите, терапии кортикостероидами и других.
Также описаны многие наследственные дефекты фагоцитарной системы. Некоторые дефекты – это нарушения бактерицидной активности фагоцитов, другие – нарушения подвижности фагоцитов.
- К первой группе относится хронический гранулематоз у детей, в основе которого лежит снижение активности НАДН2-зависимой оксидазы. В результате в клетке не образуется H 2 O 2 и не повреждается мембрана фагоцитирующего объекта. Процесс фагоцитоза не завершается, и из гистиоцитов развиваются гранулемы (чаще всего в легких). Гранулемы разрушаются, лейкоциты и микроорганизмы оставляют очаги воспаления, развивается сепсис.
- Вторая группа наследственных дефектов включает синдром Чедиака-Хигаси. Признаки включают лейкоцитарные аномалии и нарушения пигментации кожи, склонность к рецидивам, гнойные инфекции, анемию, лейкоцитопению, тромбоцитопению и т. д.
Воспаление развивается плохо из-за нарушения фагоцитоза. Снижается сопротивляемость организма инфекции, и ухудшается состояние больного. Например, в случае пониженной реактивности смертность больных пневмонией намного выше.
Принципы противовоспалительной терапии
Поскольку воспаление и часто связанная с ним лихорадка являются защитными, с ними не всегда нужно бороться. Иногда эти типичные патологические процессы изолируют возбудителя болезни, иногда – благотворно влияют на течение некоторых хронических заболеваний. Однако при многих острых воспалительных заболеваниях (фурункулез, тромбофлебит, острый аппендицит, острый панкреатит и т. д.) Необходимо бороться с воспалением, чтобы избежать опасных для организма осложнений.
Воспалительная терапия бывает этиологической и патогенетической.
- Цель этиологической терапии – устранить биологический агент воспаления (антибиотики, противотуберкулезные препараты, терапевтические сыворотки и т. д.) Или подавить действие аллергена.
- Задача патогенетического лечения – предотвратить или полностью заблокировать один из этапов воспалительного патогенеза.
- Противовоспалительные препараты (салицилаты, глюкокортикоиды) стабилизируют лизосомальную мембрану, снижают активность ферментов (трансаминаз, дегидрогеназ, эстераз, протеаз) и тем самым уменьшают образование биологически активных веществ.
- Индометацин подавляет синтез простагландинов. Гиперосмолярные растворы (как местные, так и внутривенные) используются для уменьшения воспалительного отека.
- Глюкокортикоиды подавляют фагоцитоз, пролиферацию клеток и иммунологические процессы. В результате течение воспаления ослабевает и замедляется. Эти препараты широко используются при лечении аллергических воспалений.
Чтобы создать наиболее благоприятные условия для развития воспаления как защитного процесса организма, воспаленным тканям нужен покой. В случае острого воспаления механические движения могут помешать локализации воспаления и способствовать распространению инфекции.
В лечении воспалений играют роль различные тепловые процедуры: они улучшают кровообращение и циркуляцию лимфы в воспаленных тканях и стимулируют экссудацию, тем самым усиливая и ускоряя воспалительные процессы. Холод снижает интенсивность этих процессов.
Основная задача хирургических методов лечения – удаление внутренних ограниченных инфекционных очагов воспаления (флегмонозный отросток, желчный пузырь), а также вскрытие и дренирование гнойной полости (абсцесс, флегмона).
В современной медицине, в том числе при лечении воспалений, успешно применяются каликреин и препараты ингибиторов каликреина.
Ингибиторы протеаз, обладающие широким спектром действия, участвуют в регуляции хининов и фибринолитической системы. Эти ингибиторы играют защитную роль при различных заболеваниях, включая панкреатит. Они препятствуют образованию калькреина и прогрессированию воспаления. Многие ингибиторы каликреина содержатся в бычьей печени, слюнных железах, поджелудочной железе. Препараты-ингибиторы (трасилол, калол, контральтик) используются при лечении острого панкреатита.
Препараты каликреина (падутин, депокаликреин, дилминал D, ангиотропин) расширяют кровеносные сосуды и играют важную роль в лечении облитерирующего эндартериита.
В период разрастания соединительной ткани для борьбы с негативными последствиями рубцевания, особенно контрактур, движения следует выполнять постепенно, увеличивая их амплитуду до максимума.
Читайте также:


.jpg)
.jpg)