Меланоз кожи при аддисоновой
Обновлено: 26.04.2024
Краткое описание 100 микропрепаратов типовых патологических процессов заболеваний человека. Пособие для подготовки к практическим занятиям и экзаменам.
Задача пособия - предоставить в сжатой форме описание типовых патологических процессов на примере 100 микропрепаратов кафедры патологической анатомии, используемых на практических занятиях и экзаменах 3 курса медицинского университета. Материал подобран применительно все существующей программой по патологической анатомии для медицинских ВУЗов Российской Федерации. Предлагаемые описания изложены таким образом, чтобы облегчить студентам самостоятельное изучение препаратов на занятии. С этой целью отмечаются наиболее существенные морфологические признаки, которые имеются во всех вариантах данной патологии. Следует подчеркнуть, что пособие не заменяет учебника и атласа патологической морфологии.
Введение
(рекомендации для самостоятельного изучения микропрепаратов)
1. Все препараты рассматривают с начала при малом увеличении (м.ув.), а если нужно - при большом увеличении (б.ув.) микроскопа.
2. Под м.ув. следует ориентироваться в общей гистологической картине: найти участки ткани, сохранившие нормальную характерную для данного органа структуру (например, почечные клубочки, альвеолы легких и т.д.), а также видоизмененную ткань характерными признаками исследуемого патологического процесса (кровоизлияния, опухоль, воспаление и т.д.).
3. Под б.ув. рассматриваются наиболее важные для изучаемой патологии детали препарата, например, клетки-сидерофаги в легком, полиморфные опухолевые клетки и др.
4. Рисунок препарата в рабочей тетради - это не буквальный перенос на бумагу конкретного поля зрения микроскопа, а схематическое изображение характерных микроскопических признаков, свойственных данному патологическому процессу.
5. Все микропрепараты, которые изучают на кафедре патологической анатомии - это парафиновые срезы патологически измененных органов и тканей человека, полученных при биопсии у больных людей или при вскрытии трупов умерших.
Подавляющее большинство срезов окрашено гематоксилином-эозином; если используются другие методы изготовления окраски срезов, то это специально оговаривается после названия препарата.
Часть 1. Общие патологические процессы.
А) Паренхиматозные дистрофии
Зернистая дистрофия почки.
Окраска гематоксилин-эозин. Клубочки почек не изменены. Цитоплазма эпителиальных клеток извитых канальцев набухшая, просвет канальцев сужен, границы между клетками нечеткие, ядра окрашены в бледно-синий цвет. Под большим увеличением в цитоплазме клеток обнаруживаются мелкие белковые включения розового цвета.
2*Роговая дистрофия эпидермиса (гиперкератоз.) № 42
Окраска гематоксилин-эозин. Избыточное (гиперкератоз) образование рогового вещества. Гиперкератоз проявляется в резком (в 2-3 раза) утолщении рогового слоя эпидермиса, который в остальном сохраняет свое обычное строение. Кератин окрашивается эозином в розовый цвет, а пикрофуксином по Ван Гизону — в желтый. Он обладает осмиофильностью и высокой электронной плотностью. Помимо эпидермиса, этот процесс может наблюдаться в условиях патологии в слизистых оболочках (лейкоплакия), в некоторых раковых опухолях.
3*Жировая дистрофия печени № 11
Окраска гематоксилин-эозин. В цитоплазме гепатоцитов (преимущественно на периферии долек) содержатся крупные бесцветные вакуоли, жировые ткани растворились при обработке ткани в спиртах (см. приготовление гистологических препаратов) различных размеров. Вакуоли оттесняют ядро к периферии и гепатоцит становится похожим на жировую клетку (крупнокапельное ожирение). Частой причиной этого вида обратимого ожирение печени является алкогольная интоксикация.
Б) Мезенхимальные (стромально - сосудистые) дистрофии
Мукоидное набухание стенки вены
Окраска толуидиновым синим. Выявляется феномен метахромазии, особенно с толуидиновым синим: в фокусах мукоидного набухания происходит накопление гликозоаминогликанов, дающих метахроматичное (сиреневое) окрашивание. Стенка вены (главным образом – интима) утолщена вследствие отека и набухания и окрашивается не в синий, а в сиреневый цвет (явление метахромазии), что указывает на избыточное накопление в межуточной ткани свободных гликозаминогликанов (гиалуроновой и хондроитинсерной кислот). Мукоидное (слизеподобное) набухание оболочек и стромы органов характерно для ревматических и аллергических заболеваний, состояния гипоксии тканей.
5*Амилоидоз селезенки («Саговая селезенка»). №107
Окраска Конго красный. Массы амилоида, избирательно окрашиваются в кирпично-красный цвет и располагаются преимущественно в фолликулах, занимая с начала их периферии, а по мере прогрессирования дистрофии распространяются на весь фолликул, который сохраняет свои очертания. Лимфоциты фолликулов, а также прилежащие к ним клетки пульпы селезенки сдавливаются амилоидными массами атрофируются. Такой вид селезенка может иметь у больных общим амилоидозом на фоне туберкулеза костей, хронических нагноительных процессов, третичного сифилиса и других болезней.
Гиалиноз артерии селезенки
Окраска гематоксилин – эозин. Гиалин откладывается в интиму центральных артерий фолликулов и артериол красной пульпы и имеет вид гомогенных эозинофильных (т. е. розовых) масс, суживающих просвет сосуда. При этом мышечная оболочка сдавливается, однако эндотелий, выстилающий просвет сосуда сохраняется.
7*Ожирение сердца №52
Окраска гематоксилин - эозин. Мышечные волокна миокарда раздвинутые тяжами жировых клеток, цитоплазма которых выглядит «пустой» вследствие растворения жировой вакуоли спиртом (см. приготовление гистологических препаратов). Кардиомиоциты находятся в состоянии атрофии – ядро и цитоплазма уменьшены, некоторые кардиомиоциты сохранили поперечную исчерченность. Таким образом, жировая ткань при этом виде ожирения (так называемое простое ожирение) находится в строме сердца между мышечными волокнами.
В) Смешанные дистрофии
8*Желтое размягчение головного мозга (очаг хронического кровоизлияния) №146
Окраска гематоксилин - эозин. Излившаяся кровь представлена массой гемолизированных эритроцитов, среди которых видны волокна фибрина, а так же мелкоочаговые отложения глыбок внеклеточно расположенного буро-коричневого гемосидерина . В прилежащей мозговой ткани происходит реактивная пролиферация мелких сосудов и глиальных клеток, в цитоплазме последних хорошо видны золотисто-желтые и бурые зерна пигментов (главным образом – гемосидерина, гематоидина). С течением времени остатки крови рассасываются, и весь очаг приобретает желто-бурую окраску, а затем может превратиться в кисту.

9*Меланоз кожи при аддисоновой болезни №402
Окраска гематоксилин - эозин. Меланоз (приобретенная гиперпигментация кожи) при аддисоновой болезни: цитоплазма меланоцитов (их число увеличено) базального слоя эпидермиса и некоторых кератиноцитов заполнена большим количеством зерен меланина (пигмент бурого цвета). В дерме меланин можно видеть в меланоцитах и макрофагах (меланофагах), фагоцитирующих пигмент при гибели меланоцитов. Эпидермис атрофичен, отмечается избыточное образование кератина (гиперкератоз).
Болезнь Аддисона (гипокортицизм, хроническая надпочечниковая недостаточность) — это редкое заболевание, характеризующееся недостаточной выработкой надпочечниками глюкокортикоидного гормона кортизола и минералокортикоидного гормона альдостерона.
Чаще всего гипокортизицм, которому подвержены как мужчины, так и женщины, возникает в 30-50 лет, однако дебют (первое клиническое проявление) заболевания может наблюдаться в любом возрасте.
Распространенность болезни Аддисона во всем мире составляет 40-60 пациентов с установленным диагнозом БА на 1 миллион человек.
Причины возникновения
Как правило, болезнь Аддисона возникает из-за повреждения или разрушения коры надпочечников в результате развития аутоиммунного процесса (иммунная система воспринимает кору надпочечников как чужеродную, атакует и разрушает ее) или другого аутоиммунного заболевания, имеющегося у пациента.
К другим причинам возникновения заболевания относятся:
-
(в основном в развивающихся странах);
- другие (вторичные, например — грибковые) инфекции;
- злокачественные опухоли (с распространением опухолевых клеток из первичного очага, лимфомы);
- кровотечение в надпочечниках (надпочечниковый инфаркт);
- генетическая предрасположенность (в редких случаях).
Дефицит глюкокортикоидных и минералокортикоидных гормонов, вызванный снижением функции коры надпочечников, называют первичной надпочечниковой недостаточностью. Если надпочечники не способны продуцировать эти гормоны по другим причинам (например, из-за аномалий гипофиза или его дисфункции), речь идет о вторичной надпочечниковой недостаточности.
Симптомы
Болезнь Аддисона прогрессирует медленно, в течение нескольких месяцев. Симптомы могут варьироваться от человека к человеку. Первые клинические проявления часто неспецифичны, то есть сходны с симптомами других — распространенных — заболеваний.
Обычно на начальных стадиях заболевания пациент не ощущает никаких симптомов. К сожалению, дебют БА ассоциирован с 90% повреждения коры надпочечников.
К симптомам болезни Аддисона относятся:
- повышенная утомляемость;
- снижение энергии;
- общее недомогание;
- гиперпигментация кожи, затрагивающая ладонные сладки, фаланги пальцев, шрамы, слизистые оболочки полости рта, места трения;
- нарушение пигментации кожи (витилиго);
- снижение аппетита и потеря веса;
- обезвоживание;
- низкий вес и отставание в физическом развитии (у детей);
- тяга к соли или соленой пище; , рвота; , диарея;
- обмороки;
- мышечная и суставная боль;
- раздражительность, снижение концентрации, депрессия;
- гнездная алопеция; на некоторых участках тела, сухость кожи, снижение либидо, нарушения менструального цикла (у женщин);
- гипогликемия (снижение концентрации глюкозы в крови);
- постуральная гипотензия (резкое снижение АД при изменении положения тела).
Иногда болезнь Аддисона, не проявлявшая себя ранее, может возникнуть внезапно и остро — например, при отсутствии необходимого лечения или в результате воздействия стрессовых факторов (несчастный случай, травма, хирургическое вмешательство), инфекции, другого заболевания. В этом случае речь идет о жизнеугрожающем состоянии — т. н. аддисоническом кризе или острой надпочечниковой недостаточности. Характерные признаки: сильная слабость, спутанность сознания, боли в спине, ногах и животе, рвота и диарея, низкое артериальное давление, гиперкалиемия, гипонатриемия.
Диагностика
Диагноз устанавливается на основании анамнеза, жалоб и симптомов пациента, результатов лабораторной и инструментальной диагностики (КТ, МРТ).
Анализы крови направлены на определение уровня натрия, калия, кортизола и адренокортикотропного гормона (АКТГ), который стимулирует выработку гормонов корой надпочечников, а также на выявление специфических антител, ассоциированных с болезнью Аддисона.
Пациенту может быть назначена стимуляционная проба АКТГ, во время которой (для стимуляции выработки кортизола) вводится адренокортикотропный гормон. Если стимуляция не приводит к выработке нормального уровня кортизола, это указывает на повреждение надпочечников или нарушение их функции.
Также проводится инсулин-индуцированная гипогликемическая проба, которая помогает установить взаимосвязь характерных симптомов болезни Аддисона с аномалиями гипофиза или нарушениями его функции. Во время этого теста пациенту вводится быстродействующий инсулин, уровень сахара в крови замеряется до и после инъекции.
Для оценки функции надпочечников и их структурных особенностей дополнительно проводится визуализация с помощью КТ и МРТ. Эти исследования помогают уточнить характерные изменения, наблюдаемые при развитии болезни Аддисона.
Дифференциальный диагноз
Чаще всего болезнь Аддисона дифференцируют (различают) со следующими заболеваниями:
- вторичной надпочечниковой недостаточностью, вызванной снижением выработки гипофизом адренокортикотропного гормона;
- врожденной гиперплазией надпочечников (группа наследственных патологий, возникающих из-за нарушения биосинтеза кортизола);
- адренолейкодистрофией (наследственное дегенеративное заболевание ЦНС, которое передается по X-сцепленному рецессивному типу и ассоциируется с надпочечниковой недостаточностью);
- аутоиммунным полиэндокринным синдромом 2 типа (синдром Шмидта, редкое аутоиммунное заболевание, при котором происходит резкое снижение функции нескольких эндокринных органов: надпочечников, щитовидной железы, паращитовидных желез, гонад, поджелудочной железы);
- аутоиммунным полиэндокринным синдромом 1 типа (редкий генетический синдром APECED, который характеризуется поражениями кожи и слизистых оболочек грибами рода Candida, снижением функции паращитовидных желез и аутоиммунной недостаточностью функции надпочечников).
Лечение болезни Аддисона
Лечение болезни Аддисона основано на применении медикаментозной терапии, направленной на замещение глюкокортикоидного и минералокортикоидного гормонов. Рекомендуется пероральный прием гидрокортизона и флудрокортизона, дозировка препаратов подбирается индивидуально. Терапия проводится на протяжении всей жизни.
Некоторым пациентам может быть предложена андроген-заместительная терапия (тестостерон или андростендион). Больные, получающие такое лечение, сообщают о снижении проявлений усталости, улучшении настроения и психоэмоционального состояния в целом, повышении либидо (у женщин), однако эти подходы к лечению пока исследуются.
Лечение аддисонического криза включает внутривенное введение гидрокортизона, жидкостей, электролитов и препаратов, нормализующих артериальное давление.
Особенности и преимущества лечения болезни Аддисона в клинике Рассвет
Своевременная диагностика и эффективное лечение редких синдромов и болезней входят в область интересов всех врачей клиники Рассвет.
Наши эндокринологи — врачи высокой квалификации, прекрасно подготовлены и имеют большой практический опыт.
Пациентам с подозрением на болезнь Аддисона проводятся все необходимые диагностические исследования для подтверждения или исключения диагноза. При необходимости индивидуально подбирается адекватная схема терапии.
Рекомендации врача-эндокринолога клиники Рассвет пациентам с болезнью Аддисона
Помимо приема препаратов заместительной терапии, пациенту необходимо следить за тем, чтобы получать достаточное количество соли (натрия) из рациона, особенно во время физических нагрузок, при жаре или желудочно-кишечных расстройствах.
Дозировка принимаемых лекарств может быть временно увеличена, если пациент испытывает стресс, связанный с проведением операции, инфекционными и другими заболеваниями. Если из-за тошноты и рвоты пациент не может принимать необходимые препараты перорально, ему назначаются инъекции.
Пациентам с болезнью Аддисона важно знать, что прием стероидов в их случае не связан с серьезными побочными эффектами, поскольку осуществляется восполнение недостатка выработки гормонов. При правильном подборе дозировки лекарств побочные эффекты практически не наблюдаются.
Пациентам с болезнью Аддисона необходимо постоянно иметь при себе медицинский документ, свидетельствующий о наличии заболевания, для случаев оказания экстренной медицинской помощи.
Болезнь Аддисона нельзя предотвратить, но для нее существует эффективное лечение. При своевременной диагностике, правильном подборе терапии, соблюдении мер профилактики острой надпочечниковой недостаточности, ожидаемая продолжительность жизни у пациентов с этим заболеванием не снижается.
Наблюдением невусов занимается дерматолог или дерматоонколог. Удалить невус может дерматолог, дерматоонколог, хирург. Если невус расположен на конъюнктиве глаза, необходимо наблюдение офтальмолога.
Что такое невусы
Невусы — это доброкачественные новообразования кожи.
Формы и осложнения невусов
Различают меланоцитарные (содержащие пигментные клетки-меланоциты) и немеланоцитарные невусы (образованы другими клетками, кроме меланоцитов), которые включают эпидермальный невус, невус сальных желез, невус Беккера и некоторые другие доброкачественные образования, сосудистые невусы кожи.
Меланоцитарные невусы
Выделяют приобретенные и врожденные меланоцитарные невусы.
Приобретенные меланоцитарные невусы (ПМН) являются доброкачественными опухолями кожи. Как правило, они не имеют склонности к злокачественной трансформации. К особым формам приобретенных меланоцитарных невусов относят невус Шпица, невус Рида, пятнистый невус (спилус), галоневус (Сеттона), залегающий в глубоких слоях кожи синий невус (Ядассона-Тиче).
В отдельную группу выделяют атипичные (диспластические) невусы (АН). В отличие от обыкновенных приобретенных меланоцитарных невусов, атипичные меланоцитарные невусы могут иметь некоторые клинические характеристики меланомы, такие как асимметрия, нечеткие границы, несколько цветов или размер более 6 мм. Основное их отличие от злокачественной опухоли — стабильность, отсутствие изменений на протяжении долгого времени и сходные характеристики у одного человека. Атипичные меланоцитарные невусы имеют относительно повышенный риск злокачественной трансформации и требуют тщательного наблюдения.
Врожденные меланоцитарные невусы возникают как порок развития (гемартома) и обычно имеются уже при рождении ребенка. Врожденные меланоцитарные невусы больших размеров также ассоциируются с повышенным (но все же невысоким) риском злокачественной трансформации. Крайне редко они могут быть ассоциированы с патологическим накоплением меланоцитов в центральной нервной системе (нейрокожный меланоз). Врожденные меланоцитарные невусы с ожидаемым размером у взрослого (в течение жизни они будут увеличиваться пропорционально росту ребенка) также требуют повышенного внимания и наблюдения врача.
Меланоцитарную структуру имеют также невусы Ота и Ито, но в их основе не избыточное деление клеток, а их накопление в глубоких слоях кожи.
Причины появления невусов
Основной причиной их появления считаются ультрафиолетовые лучи (лучи солнца), может играть роль наследственная предрасположенность, особенности пигментации кожи и волос.
Симптомы невусов
Невусы выглядят как пятна или узелки на коже. Одни из них едва заметны, другие имеют насыщенный коричневый (меланоцитарные или пигментные) или красный (сосудистые невусы) цвет.
Невусы могут менять свой вид, увеличиваться на протяжении жизни. Важно правильно оценивать эти изменения, такие проявления могут быть не только вариантом нормы, но и служить одним из признаков злокачественных образований кожи.
Стадии изменений невусов
Для меланоцитарных невусов — как приобретенных, так и врожденных — характерны стадийные изменения на протяжении жизни. Классический путь развития включает 3 стадии, которые отличаются глубиной расположения образования:
- простой невус или пограничный представляет собой поверхностное плоское коричневое пятно;
- сложный или комбинированный невус располагается глубже и выглядит как коричневое пятно или возвышающееся образование на коже;
- внутридермальный невус представляет собой светлое, возвышающееся и расположенное глубоко в коже образование.
Лечение невусов
В большинстве случаев лечение не проводится, требуется только наблюдение, поскольку невусы являются доброкачественными образованиями. При подозрении на злокачественный характер и выявлении образований с высоким риском злокачественной трансформации проводится хирургическое иссечение. Возможно проведение удаления невуса по желанию пациента из эстетических соображений или из-за дискомфорта (например, при локализации в зонах частой травматизации одеждой).
Особенности методики лечения
Оптимально проведение хирургического иссечения невуса. Этот метод позволяет осуществить радикальное удаление скальпелем с последующим ушиванием раневой поверхности. В некоторых случаях, когда невусы выступают над поверхностью кожи, может применяться радионож, электро- или лазерный нож. Во всех случаях хирургического лечения меланоцитарных невусов необходимо проведение гистологического исследования удаленных тканей.
Как происходит лечение невусов в клинке Рассвет
Врач проведет осмотр кожного покрова пациента полностью, для исключения риска пропустить меланому или другой рак кожи. Подозрительные образования дополнительно изучаются с помощью прибора, позволяющего осмотреть кожу с увеличение в 10 раз – дерматоскопа. В карте пациента описываются невусы, требующие наблюдения. Подозрительные невусы врач предложит удалить хирургическим способом с последующим гистологическим исследованием удаленного материала (направляется в экспертную лабораторию). Удаление невусов по эстетическим показаниям может выполняться по желанию пациента.
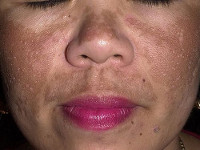
Токсическая меланодермия (меланоз Риля) – меланотический профессиональный дерматоз, вызываемый токсическим действием продуктов нефти, каменного угля и фотосенсибилизацией. Особенностью заболевания является возможность возникновения, как на производстве, так и в быту, при использовании печного отопления, обогрева керосином, газом. Дерматоз протекает стадийно, первым проявлением меланодермии становится сетчатая пигментация кожи синевато-коричневого оттенка с последующим развитием кератоза и атрофии. Патология диагностируется клинически с установлением профвредности. Лечение заключается в устранении провоцирующего фактора с подключением витаминотерапии, гепатопротекторов, энтеросорбентов, фотозащиты.
Общие сведения
Токсическая меланодермия – одна из редких разновидностей профессионального меланоза, возникающая на фоне интоксикации углеводородами и фотосенсибилизации. В отличие от других профессиональных дерматозов заболевание не обладает возрастными рамками из-за возможности возникновения в быту. Патологический процесс неэндемичен, не имеет возрастных и расовых различий, при этом причиной возникновения всегда является контакт пациента с вредным веществом. Профдерматоз развивается преимущественно в нефтедобывающих и нефтеперерабатывающих странах у рабочих НПЗ, нефтегазовой отрасли. Впервые описание заболевания появилось в дерматологии в 1917 году, когда венгерский врач Г. Риль выявил 17 случаев дерматоза, связав их с лишениями военного времени. Через два года Э. Хоффман предположил, что причина патологических проявлений связана с контактом пациентов с вредными веществами, ещё через год Р. Габерманн доказал, что токсическая меланодермия является результатом воздействия паров пыли, насыщенных акридином.
Французский дерматолог А. Сиватт в 1923 году описал идентичные клинические проявления, связав их с фотосенсибилизацией. С тех пор дерматологи не могут прийти к консенсусу по вопросу, чем являются заболевания с похожей симптоматикой – разновидностями токсической меланодермии или самостоятельными нозологиями. Актуальность темы связана с ростом заболеваемости в результате развития нефтеперерабатывающего комплекса, с экономическими потерями государств в случаях утраты работоспособности пациентами, страдающими данной патологией, нарушением их качества жизни.

Причины токсической меланодермии
Профессиональные триггеры заболевания известны, ими являются вещества, вызывающие фототоксические реакции: продукты нефтеперегонки, недоброкачественная парфюмерия, гиперинсоляция. Имеет значение и внутреннее состояние организма пациента: недостаток витаминов, патология пищеварительного тракта, вредные привычки. Механизм развития до конца не изучен. Считается, что меланогенез в норме является адаптацией организма к изменениям в окружающей среде. При развитии патологических процессов образования меланина в 60% случаев имеет значение чрезмерное ультрафиолетовое излучение, в 20% – беременность и в 20% – эндокринологические нарушения, не связанные с беременностью.
В первом случае кератиноциты, получившие меланин от меланоцитов, выносят его на поверхность в составе роговых клеток, что визуально проявляется пигментацией кожи. Во втором случае гипоталамо-гипофизарная система стимулирует дисперсию и перемещение меланина из меланоцитов в кератиноциты, которые сами по себе деструктированы. Поэтому одновременно с гиперпигментацией кожи наблюдаются гиперкератоз и явления воспаления.
Поскольку кожа гормонозависима, нарушения в гормональной системе вызывают гипермитотическую активность меланоцитов и кератиноцитов эпидермиса, которые, обмениваясь меланином, инициируют воспаление кожи и её гиперпигментацию. Т-лимфоциты при этом дополнительно сенсибилизируют дерму, разрушая её клетки, провоцируя выброс в дерму цитокинов, интерлейкинов, стимулируя процессы воспаления и пролиферации. Так «каскадно» развивается токсическая меланодермия.
Классификация и симптомы токсической меланодермии
Единого мнения о классификации патологического процесса в современной дерматологии не существует. По первичным элементам выделяют узелковую, буллёзную и смешанную меланодермию. Что касается клинических проявлений, то некоторые дерматологи считают вариантами, точнее – разными стадиями развития токсической меланодермии пойкилодермию Сиватта и меланоз Габерманна-Гоффманна, однако большинство авторов придерживаются мнения о самостоятельности этих нозологий. Специалисты полагают, что с учетом механизма развития токсическая меланодермия вместе с пойкилодермией Сиватта и меланозом Габерманна-Гоффманна входит в большую группу меланоза (его токсическую ретикулярную разновидность), и все перечисленные патологии должны рассматриваться как самостоятельные заболевания.
Болезнь развивается медленно. Дерматологи выделяют три стадии клинического течения токсической меланодермии: эритематозную, пигментную, атрофическую. Первичным элементом клинических проявлений патологического процесса является эритема, которая трансформируется в сетчатую буро-синюшную гиперпигментацию в виде небольших пятен, имеющих тенденцию к росту и слиянию, на открытых участках кожного покрова, особенно в области висков. На поверхности пятен появляются кистозно расширенные капилляры в виде мелких шелушащихся узелков. Гиперпигментированная кожа утолщается, кожный рисунок усиливается, образуются пустулы с исходом в атрофию кожи. Иногда в процесс вовлекаются слизистые. Высыпания сопровождаются продромальными явлениями, из-за нарушения обменных процессов пациент теряет вес. Иногда присутствует неинтенсивный зуд.
Диагностика и лечение токсической меланодермии
Диагноз заболевания ставит дерматолог на основании анамнеза (установление причины дерматоза, выявлении профвредности), клинических и гистологических данных: гиперкератоза, акантоза, скопления меланина в эпидермисе, периваскулярного инфильтрата в дерме. Дифференциальный диагноз проводят с другими меланодермиями, гемохроматозом, пеллагрой, пигментными фотодерматитами, болезнью Аддисона, мышьяковой дисхромией. Лечение состоит в устранении причины, вызвавшей патологический процесс, курсовой витаминотерапии с использованием гепатопротекторов и энтеросорбентов, корректировке обменных процессов. Наружно применяют средства фотозащиты, кератолитические, противовоспалительные и отшелушивающие мази, отбеливающие кожу препараты. Показано соблюдение специальной диеты, насыщенной витаминами и минералами. В качестве профилактики проводят регулярные профосмотры на производстве, улучшают условия труда, пациентов с выявленной токсической меланодермией переводят на другую работу вне контакта с профвредностями. Большое значение в профилактике заболевания принадлежит экспертизе трудоспособности.
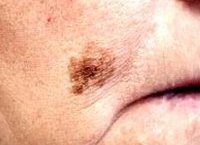
Меланоз Дюбрейля — предмеланомное заболевание кожи, представляющее собой единичное пигментное пятно с неровными очертаниями, располагающееся на открытом участке кожного покрова. Цвет пятна варьирует от светло-коричневого до черного и может быть различным в разных участках пятна. С целью дифференциации меланоза Дюбрейля от других невоидных заболеваний кожи проводится дерматоскопия, цитологическое исследование мазка-отпечатка кожного новообразования. Поскольку меланоз Дюбрейля часто малигнизируется и переходит в меланому, в лечении предпочтительно его полное хирургическое иссечение до здоровых тканей; возможно проведение рентгенотерапии.
Общие сведения
Меланоз Дюбрейля – пигментное образование, являющееся пограничным предмеланомным поражением кожи. Относится к числу меланомоопасных невусов. Меланоз Дюбрейля развивается, как правило, у лиц пожилого возраста. По некоторым данным это заболевание встречается у 3-х человек из 1000 лиц старше 50 лет. Различные авторы приводят цифры, согласно которым меланомы, развившиеся из меланоза Дюбрейля, составляют от 10% до 33% от всех меланом кожи. Частота трансформации заболевания в меланому составляет 35-40%, у некоторых авторов указана цифра 75%. Причинами злокачественного перерождения меланоза Дюбрейля считаются инсоляция, механические, химические и иные травмы новообразования.

Симптомы меланоза Дюбрейля
Заболевание представляет собой плоское единичное пигментное пятно, неровные края которого напоминают географическую карту. В начале заболевания пятно обычно имеет светло-коричневую окраску и диаметр 2-3 см. Постепенно отмечается рост пятна и потемнение его окраски. В результате размеры очага поражения кожи могут достигать 20 см в диаметре. Пятно приобретает неравномерную окраску от коричневого до черного цвета с серыми или синюшными участками. На поверхности пятна могут наблюдаться участки с отсутствием окрашивания, соответствующие зонам спонтанной регрессии заболевания.
Характерна локализация меланоза Дюбрейля — это открытые участки кожи, в основном лицо (нос, щеки, лоб) и шея. В связи с этим некоторые авторы указывают на связь возникновения заболевания с имеющимся у пациента хроническим солнечным дерматитом.
При переходе меланоза Дюбрейля в меланому на участке пигментного пятна обнаруживается уплотнение с папилломатозной поверхностью, происходит изменение цвета пятна (потемнение или осветление), усиливается процесс шелушения, вокруг пятна возникает покраснение, а на его поверхности может появиться эрозирование. Точные причины малигнизации меланоза не установлены. Определенную роль в этом процессе отводят инсоляции и травматизации пораженного участка кожи.
Диагностика меланоза Дюбрейля
Современная дерматология не может применять биопсию кожного образования для диагностики трансформации меланоза Дюбрейля в меланому, поскольку такой метод исследования может стимулировать рост опухоли и ее диссеминацию. Поэтому применяется цитологическое исследование мазка-отпечатка с поверхности образования. Простое снятие отпечатка с поверхности бывает малоинформативно. По этой причине дерматолог перед взятием мазка немного скребет поверхность образования. Диагностическим критерием возникновения меланомного рака кожи является обнаружение в отпечатке атипичных меланоцитов.
В ходе диагностики меланоз Дюбрейля дифференцируют от невуса Ота, участка гиперпигментации, себорейной кератомы, пигментированой базалиомы, пигментного невуса и меланомы.
Лечение меланоза Дюбрейля
В виду большого процента малигнизации заболевания в случае диагностики меланоза Дюбрейля должно проводиться радикальное иссечение всего участка поражения кожи вплоть до здоровых тканей. При этом захватывают 1-2 см неизмененной кожи по всему периметру пятна. Учитывая локализацию процесса на лице, его удаление иногда представляет для хирурга нелегкую задачу и требует применения методов пластической хирургии. При больших размерах пятна и связанных с эти затруднений для его хирургического иссечения может применяться локальное воздействие на образование рентгеновскими лучами, которое часто дает хорошие результаты.
Читайте также:

