Лактобактерин при атопическом дерматите у детей
Обновлено: 28.04.2024
Для цитирования: Хамаганова И.В., Никифорова Г.Д., Шекрота А.Г., Колибрина А.М. Применение гастроинтестинальных препаратов в комплексной терапии атопического дерматита. РМЖ. 2004;14:828.
Терапия атопического дерматита остается одной из актуальных задач дерматологии. Отсутствие эффективных десенсибилизирующих, противозудных средств предопределило интерес к необходимости воздействия на другие патогенетические механизмы. В настоящее время хорошо известно, что патологический процесс развивается на фоне функциональных нарушений центральной нервной системы, психических расстройств, изменений реактивности вегетативной нервной системы. Клинические поражения кожи варьируют в зависимости от возраста, нередко сочетаясь с поражением органов дыхания, почек, глаз, желудочно–кишечного тракта. Последнее обусловило необходимость включения в комплексную терапию препаратов, нормализующих моторику желудка и кишечника, состояние микрофлоры, желчеотделение, ферментативную активность [1]. В настоящей работе представлены результаты применения Дюфалака и Креона 10 000 в комплексном лечении атопического дерматита у взрослых и детей.
Дюфалак представляет собой раствор лактулозы (6–га – лактозид–фруктоза).100 мл сиропа содержит лактулозы 67 г; выпускается в полиэтиленовых флаконах по 200 и 500 мл, в комплекте с мерным стаканчиком. Препарат в неизмененном виде достигает уровня толстой кишки, оказывает осмотический «подсасывающий» эффект по типу «внутренней клизмы».Та часть лактулозы, которая успевает разложиться под влиянием кишечной флоры (в особенности при дисбактериозе) преобразуется в молочную и уксусную кислоту, частично – углекислоту. Указанные продукты закисляют содержимое толстой кишки, подавляя гнилостное брожение и всасывание аммиака (переводя его в аммоний). Последнее свойство препарата позволяет нормализовать кишечную флору при дисбактериозе, распространенном среди больных атопическим дерматитом, и уменьшить сопровождающую поражение кожи интоксикацию. Применение лактулозы приводит к изменению состояния кишечной микрофлоры, выражающемуся в повышении содержания бифидобактерий, лактобацилл и в снижении количества условно–патогенных микроорганизмов [3]. Обосновано применение лактулозы у больных язвенной болезнью, ассоциированной с Helicobacter pylori. Показана целесообразность назначения препарата больным, принимающим блокаторы Н 2 –рецепторов гистамина, так как последние активизируют антрагастральную бактериальную пролиферацию [4]. Препарат показан при хронических заболеваниях печени, желчно–каменной болезни [3,5]. Лактулоза является высокоэффективным средством для лечения печеночной энцефалопатии [5]. Ранее было показано, что гепато–билиарная патология распространена среди больных атопическим дерматитом [1,6–9].
Креон 10 000 (панкреатин) является препаратом, восполняющим дефицит ферментов поджелудочной железы.1 капсула с минимикросферами, покрытая кишечнорастворимой оболочкой, содержит 150 мг панкреатина, что соответствует 8000 МЕ амилазы, 10 000 МЕ липазы и 600 МЕ общих протеаз. Препарат применяется при нарушениях процессов пищеварения в качестве заместительной или симптоматической терапии. Многочисленные свидетельства дефицита ферментов поджелудочной железы при атопическом дерматите широко представлены в литературе [6–9], что является основанием к изучению применения Креона 10 000 в дерматологической практике. Под нашим наблюдением находилось 118 больных атопическим дерматитом в возрасте от 6 до 32 лет, в том числе 96 женщин, 22 мужчины (основная группа). Давность заболевания составляла от 2 до 29 лет (у всех пациентов заболевание началось до трехлетнего возраста). Все больные отмечали значительное улучшение состояния в летнее время года. Обострения были связаны с психоэмоциональными стрессами, погрешностями в диете, контактом с бытовыми аллергенами. Все пациенты ранее получали терапию, включающую десенсибилизирующие, седативные, антигистаминные средства, наружные противовоспалительные препараты (содержащие глюкокортикоиды, АСД, нафталан) с временным эффектом. К началу нашего обследования у всех пациентов процесс на коже носил распространенный характер и был представлен характерными для каждой возрастной группы очагами поражения на лице, шее, сгибательных поверхностях конечностей. Пациентов беспокоил зуд (разной степени выраженности, от умеренного до нестерпимого). Критериями исключения из данной (основной) группы были: повышеннаячувствительность к лактулозе, панкреатину, галактоземия, непроходимость кишечника, панкреатит. Ранее была показана целесообразность применения эбастина в сочетании с наружными нестероидными противовоспалительными средствами при атопическом дерматите [10]. Эти препараты использовались как в лечении больных основной, так и контрольной группы. Всем больным был назначен Дюфалак: детям в возрасте 6 лет по 5 мл, от 7 до 14 лет по 10 мл, взрослым по 15 мл утром натощак. Креон 10000 назначали: детям от 6 до 14 лет по 1 капсуле во время обеда, взрослым в течение первой недели лечения по 1 капсуле во время обеда, затем по 1 капсуле во время завтрака и обеда. Кроме того, все пациенты получали эбастин: дети в возрасте от 6 до 12 лет по 5 мг, от 12 лет по 10 мг 1 раз в сутки. Наружно применяли – противовоспалительные нестероидные средства. Контрольную группу составили 32 пациента с атопическим дерматитом в возрасте от 6 до 32 лет (28 женщин, 4 мужчин). Давность заболевания составляла от 2 до 29 лет. Клиническая картина была сопоставима по степени тяжести процесса и распространенности процесса у больных основной группы. Пациентам назначали эбастин в тех же дозировках, что и пациентам основной группы, аналогичные наружные нестероидные противовоспалительные средства. Продолжительность курса лечения в обеих группах составляла 20 дней. В основной группе некоторое уменьшение зуда, эритемы было отмечено на 2–3–й день лечения. В дальнейшем регресс высыпаний продолжался, и к окончанию курса лечения у 96 из 118 больных (81,36 %) сохранялась легкая гиперпигментация, частично – лихенизация, явления экссудации, инфильтрации, разрешились полностью, что было расценено нами, как значительное улучшение. У 22 отмечено улучшение состояния. В контрольной группе некоторое уменьшение зуда, эритемы отмечено на 2–3–й день. Значительное улучшение состояния достигнуто к окончанию терапии у 6 пациентов (27,27%), у 16 – улучшение состояния (72,73%). Как в основной, так и в контрольной группе пациентов нами не было отмечено отрицательной динамики лабораторных показателей периферической крови, мочи. Все больные в двух группах лечение переносили хорошо, побочных реакций и нежелательных явлений отмечено не было. Таким образом, результаты наших наблюдений свидетельствуют об обоснованности и целесообразности включения в комплексную терапию атопического дерматита средств, нормализующих кишечную флору, моторику желудка и кишечника, дезинтоксикационных, восполняющих дефицит ферментов поджелудочной железы.
Представленные данные свидетельствуют о высокой эффективности комплексной терапии атопического дерматита с применением таких препаратов, как Дюфалак, Креон 10 000, эбастин. Высокая эффективность, хорошая переносимость, отсутствие побочных эффектов позволяют рекомендовать их для использования в дерматологической практике.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Лиофилизат д/приг. суспензии д/приема внутрь и местн. применения 2 млрд.КОЕ: 3 дозы или 5 доз фл. 10 шт.
Лиофилизат д/приг. суспензии д/приема внутрь и местн. применения 4 млрд.КОЕ: 3 дозы или 5 доз фл. 10 шт.
Форма выпуска, упаковка и состав препарата Лактобактерин сухой
| Таблетки | 1 таб. |
| Lactobacillus acidophilus | 2 млрд. КОЕ |
20 шт. - флаконы (5) - пачки картонные.
20 шт. - флаконы (10) - пачки картонные.
| Таблетки | 1 таб. |
| Lactobacillus acidophilus | 4000000000 КОЕ |
3 дозы - флаконы (10) - пачки картонные.
5 доз - флаконы (10) - пачки картонные.
Фармакологическое действие
Лечебный эффект препарата обусловлен антагонистическим действием лактобактерий по отношению к патогенным и условно-патогенным микроорганизмам, включая стафилококки, энтеропатогенные кишечные палочки, протеи, шигеллы, что определяет коррегирующее действие препарата при нарушениях бактериоценоза. Препарат улучшает обменные процессы, препятствует формированию затяжных форм кишечных заболеваний, повышает неспецифическую резистентность организма.
Показания препарата Лактобактерин сухой
При заболеваниях желудочно-кишечного тракта:
- реконвалесценты, перенесшие острые кишечные инфекции, при наличии дисфункций кишечника или выделении патогенных и условно-патогенных бактерий;
- соматические заболевания, осложненные дисбактериозами, возникшими в результате применения антибиотиков, химиотерапии и других причин;
- комплексное лечение ослабленных детей с заболеваниями инфекционной и неинфекционной этиологии, сопровождающимися дисбактериозами и атопическим дерматитом;
- хронические колиты различной этиологии, в том числе неспецифические язвенные колиты.
При заболеваниях женской половой сферы:
- для санации половых путей при неспецифических воспалительных заболеваниях гениталий и предродовой подготовке беременных группы "риска" с нарушениями чистоты вагинального секрета до III-IV степени.
| Код МКБ-10 | Показание |
| A03 | Шигеллез |
| A04.0 | Энтеропатогенная инфекция, вызванная Escherichia coli |
| A09 | Другой гастроэнтерит и колит инфекционного и неуточненного происхождения |
| K51 | Язвенный колит |
| K52 | Другие неинфекционные гастроэнтериты и колиты |
| K63 | Другие болезни кишечника |
| L20.8 | Другие атопические дерматиты (нейродермит, экзема) |
| N76 | Другие воспалительные болезни влагалища и вульвы |
Режим дозирования
Лактобактерин при кишечных заболеваниях применяют внутрь, а в акушерско-гинекологической практике - интравагинально.
Содержимое флакона растворить кипяченой водой комнатной температуры из расчета 5 мл (чайная ложка) воды на 1 дозу препарата.
Растворение осуществить следующим образом: в стакан налить необходимое количество воды (в соответствии с количеством доз, указанных на флаконе); вскрыть флакон, удалив колпачок и пробку; из стакана перенести во флакон небольшое количество воды; после растворения (препарат растворяется не более 5 мин с образованием гомогенной взвеси беловато-серого или желтовато-бежевого цвета) содержимое флакона перенести в тот же стакан и перемешать. Одна чайная ложка растворенного таким образом препарата составляет 1 дозу.
При кишечных заболеваниях препарат следует принимать за 40-60 мин до еды и желательно запивать молоком. Лечение рекомендуется сопровождать применением витаминов.
При кишечных заболеваниях лактобактерин применяют в следующих суточных дозах:
| Возраст | Доза |
| До 6 мес | 3 дозы 2 раза в день |
| От 6 мес до 1 года | 3 дозы 3 раза в день |
| От 1 до 3 лет | 5 доз 2 раза в день |
| Старше 3 лет и взрослые | 5 доз 2-3 раза в день |
Курс лечения лактобактерином при различных заболеваниях составляет:
а) при затяжном и хроническом течении дизентерии, постдизентерийном колите, долечивании реконвалесцентов после ОКИ, а также при длительной кишечной дисфункции неустановленной этиологии лечение - не менее 4-6 недель;
б) при неспецифическом язвенном колите, а также хронических колитах и энтероколитах - до 2 мес;
в) при дисбактериозах различной этиологии - 3-4 недели.
При отсутствии эффекта от применения препарата на протяжении 2 недель необходимо повторное исследование микрофлоры желудочно-кишечного тракта и коррекция ее другими препаратами в зависимости от полученного результата.
Для закрепления полученного клинического эффекта или при отсутствии полной нормализации микрофлоры после окончания курса лечения, при заболеваниях, протекающих с рецидивами, целесообразны повторные курсы лечения. В этих случаях перед назначением препарата необходимо повторное исследование микрофлоры. Поддерживающие дозы препарата (половину суточной дозы) назначают через 2-3 недели в течение 1-1,5 мес.
При воспалительных заболеваниях гениталий лактобактерин назначают по 5 доз 2 раза в день интравагинально в течение 10-12 дней, начиная с 10-12 дня менструального цикла. Для предродовой подготовки беременных группы "риска" лактобактерин назначают по 5 доз 1 раз в день в течение 5-8 дней.
При интравагиналыюм применении содержимое флакона растворить в 5-10 мл кипяченой воды комнатной температуры, стерильный тампон пропитать растворенным препаратом, ввести тампон во влагалище и оставить на 2-3 часа.
Лечение проводить под контролем восстановления чистоты вагинального секрета до I-II степени, появления лактофлоры и исчезновения клинических симптомов заболевания.
вспомогательные вещества: компоненты защитной среды высушивания (желатин; сахароза (сахар); молоко).
Состав защитной среды высушивания (на 1 л среды): желатин пищевой - от 3 до 8,5%; сахар белый кусковой или сахароза - от 8 до 28%; молоко сухое обезжиренное или молоко питьевое пастеризованное обезжиренное, или молоко обезжиренное, или молоко натуральное коровье - сырье (в пересчете на сухое вещество) - от 6 до 14%.
Содержание компонентов защитной среды высушивания в готовом препарате не определяют.
Описание
Кристаллическая или пористая масса желтовато-бежевого или беловато-серого цвета, со специфическим запахом.
Фармакотерапевтическая группа
Код АТХ
Фармакодинамика:
Препарат представляет собой микробную массу живого антагонистически активного штамма лактобактерий (Lactobacillus plantarum 8Р-А3 или Lactobacillus fermentum 90Т-С4) лиофилизированную в среде культивирования с добавлением защитной сахарозо-желатино-молочной среды высушивания.
Лактобактерин обладает высокой антагонистической активностью в отношении патогенных и условно-патогенных микробов включая стафилококки энтеропатогенные кишечные палочки протеи шигеллы что определяет коррегирующее действие препарата при нарушениях бактериоценоза. Препарат улучшает обменные процессы препятствует формированию затяжных форм кишечных заболеваний повышает неспецифическую резистентность организма.
Показания:
Лечение заболеваний желудочно-кишечного тракта и женских гениталий сопровождающихся нарушениями нормальной микрофлоры.
Препарат применяют взрослым и детям независимо от возраста.
При заболеваниях желудочно-кишечного тракта :
- реконвалесценты перенесшие острые кишечные инфекции при наличии дисфункций кишечника или выделении патогенных и условно-патогенных бактерий;
- соматические заболевания сопровождающиеся дисбактериозами возникшими в результате применения антибиотиков химиотерапии и других причин;
- комплексное лечение ослабленных детей с заболеваниями инфекционной и неинфекционной этиологии сопровождающимися дисбактериозами атопическим дерматитом;
- хронические колиты различной этиологии в том числе неспецифические язвенные колиты.
При заболеваниях женской половой сферы :
- для санации половых путей при неспецифических воспалительных заболеваниях гениталий и предродовой подготовке беременных "группы риска" с нарушениями чистоты вагинального секрета до III-IV степени.
В связи с отсутствием возрастных ограничений для назначения препарата возможность применения у подростков и детей младшего возраста оценивает врач с учетом возможной пользы риска и возрастных особенностей пациента.
Противопоказания:
Повышенная чувствительность к компонентам препарата.
Дефицит сахаразы/изомальтазы непереносимость фруктозы глюкозо-галактозная мальабсорбция.
Противопоказано местное применение при вульвовагинальных кандидозах.
Безопасность и терапевтическая эффективность перорального применения препарата при вульвовагинальных кандидозах клинически не исследовалась.
Беременность и лактация:
Способ применения и дозы:
Лактобактерин при кишечных заболеваниях применяют внутрь а в акушерско-гинекологической практике - интравагинально.
Содержимое флакона растворить кипяченой водой комнатной температуры из расчета 5 мл (чайная ложка) воды на 1 дозу препарата.
Растворение осуществить следующим образом: в стакан налить необходимое количество воды (в соответствии с количеством доз указанных на флаконе); вскрыть флакон удалив колпачок и пробку; из стакана перенести во флакон небольшое количество воды; после растворения (препарат растворяется не более 5 мин с образованием гомогенной суспензии желтовато-бежевого или беловато-серого цвета) содержимое флакона перенести в тот же стакан и перемешать. Одна чайная ложка растворенного таким образом препарата составляет 1 дозу. Детям содержимое флакона растворяют из расчета 1 мл на 1 дозу препарата.
При кишечных заболеваниях препарат следует принимать за 40-60 мин до еды и желательно запивать молоком. Лечение рекомендуется сопровождать применением витаминов.
Суточную дозу и продолжительность курса лечения определяет врач в зависимости от клинической формы заболевания и выраженности дисбактериоза.
При кишечных заболеваниях Лактобактерин применяют в следующих суточных дозах:
Возраст
Доза
3 дозы 2 раза в день
От 6 мес до 1 года
3 дозы 3 раза в день
5 доз 2 раза в день
Старше 3 лет и взрослые
5 доз 2-3 раза в день
Курс лечения Лактобактерином при различных заболеваниях составляет:
а) при затяжном и хроническом течении дизентерии постдизентерийном колите долечивании реконвалесцентов после ОКИ а также при длительной кишечной дисфункции неустановленной этиологии - не менее 4 недель;
б) при неспецифическом язвенном колите а также хронических колитах и энтероколитах - до 2 мес;
в) при дисбактериозах различной этиологии - 3-4 недели.
При отсутствии эффекта от применения препарата на протяжении 2 недель необходимо повторное исследование микрофлоры желудочно-кишечного тракта и коррекция ее другими препаратами в зависимости от полученного результата.
Для закрепления полученного клинического эффекта или при отсутствии полной нормализации микрофлоры после окончания курса лечения при заболеваниях протекающих с рецидивами целесообразны повторные курсы лечения. В этих случаях перед назначением препарата необходимо повторное исследование микрофлоры.
При воспалительных заболеваниях гениталий Лактобактерин назначают по 5 доз 2 раза в день интравагинально в течение 10-12 дней начиная с 10-12 дня менструального цикла.
Для предродовой подготовки беременных "групп риска" Лактобактерин назначают по 5 доз 1 раз в день в течение 5-8 дней.
При интравагинальном применении содержимое флакона растворить в 5 -10 мл кипяченой воды комнатной температуры стерильный тампон пропитать растворенным препаратом ввести тампон во влагалище и оставить на 2-3 часа. У подростков и детей младшего возраста можно использовать спринцевания (орошения).
Лечение проводить под контролем восстановления чистоты вагинального секрета до I-II степени появления лактофлоры и исчезновения клинических симптомов заболевания.
Побочные эффекты:
Побочное действие препарата не установлено.
У отдельных людей с измененной реактивностью могут развиваться аллергические реакции на компоненты препарата.
При появлении побочных действий не упомянутых в инструкции необходимо обратиться к лечащему врачу.
Передозировка:
Взаимодействие:
Ввиду высокой антибиотикоустойчивости лактобактерий допускается применение Лактобактерина при антибиотикотерапии.
Особые указания:
Перед применением препарата необходимо проконсультироваться с врачом.
Непригоден для применения препарат целостность упаковки которого нарушена (треснувшие флаконы) препарат с измененным внешним видом биомассы при наличии посторонних включений препарат без маркировки.
Не рекомендуется растворение препарата в горячей воде (выше 40 °С). Растворенный препарат хранению не подлежит.
Влияние на способность управлять трансп. ср. и мех.:
Форма выпуска/дозировка:
Упаковка:
По 3 или 5 доз во флаконе.
По 10 флаконов в пачке (коробке) с инструкцией по применению.
Условия хранения:
При температуре от 2 до 8 °С. Хранить в недоступном для детей месте.
Условия транспортирования. При температуре от 2 до 8 °С.
Срок годности:
Препарат с истекшим сроком годности использованию не подлежит.
Условия отпуска
Производитель
Федеральное государственное унитарное предприятие "Научно-производственное объединение по медицинским иммунобиологическим препаратам "Микроген" Министерства здравоохранения и социального развития Российской Федерации (ФГУП "НПО "Микроген" Минздравсоцразвития России), 634040, Томская область, г. Томск, ул. Ивановского, д. 8, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ФГУП "НПО "Микроген" Минздравсоцразвития России
Лактобактерин - цена, наличие в аптеках
Указана цена, по которой можно купить Лактобактерин в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
Н.А. Иванова, ФГБВОУ ВПО «Военно-медицинская академия имени С.М. Кирова» Министерства обороны РФ, г. Санкт-Петербург, к. м. н.
Ключевые слова: пробиотики, лечение атопического дерматита, адаптация желудочно-кишечного тракта, Линекс для детей ®
Keywords: probiotics, treatment of atopic dermatitis, adaptation of gastrointestinal tract, Lineks for children ®
В основе развития АтД лежит «вторая ошибка» иммунитета, а именно генетически детерминированная потеря толерантности к экзогенным неинфекционным аллергенам («первая ошибка» иммунитета – врожденные иммунодефициты). С рождения до конца первого месяца жизни ребенок находится в первом критическом периоде становления иммунной системы [1].
В это время начинается постнатальная антигенная селекция и «обучение» иммунной системы для достижения зрелости и формирования толерантности. Манифестация аллергических заболеваний у предрасположенных к атопии детей наступает тогда, когда сумма наследственных факторов (нерегулируемых) и неблагоприятных факторов внешней среды (регулируемых) превышает пороговое значение.
Каждый ребенок после рождения имеет постоянный контакт с пищевыми белками, которые абсорбируются из желудочно-кишечного тракта (ЖКТ) без каких-либо патологических иммунологических и клинических реакций. В норме поступление пищевых белков формирует пищевую толерантность – специфическое подавление иммунного ответа при пероральном поступлении аллергена.
Толерантность поддерживает баланс между нормальным ответом на внешний агент и ги-перергическим ответом, который характерен для детей, предрасположенных к развитию аллергических заболеваний.
Формирование толерантности зависит от:
- возраста ребенка;
- дозы и свойств аллергенов;
- состояния барьерной функции ЖКТ;
- адекватности распознавания аллергена иммунной системой.
Профилактические меры следует начинать в пренатальном периоде, ограничивая (но не исключая) наиболее значимые пищевые аллергены в последнем триместре беременности. Большое значение имеет раннее прикладывание к груди и исключение докорма молочной смесью в родильном доме. При наличии абсолютных показаний к докорму и искусственном вскармливании с рождения следует использовать смеси на основе частичного гидролиза белков коровьего молока.
Большое значение в формировании толерантности имеет анатомическая и функциональная состоятельность эпителиального барьера слизистой оболочки кишечника, что напрямую связано с адекватной работой иммунной системы, ассоциированной со слизистой оболочкой желудочно-кишечного тракта (GALT – gut-associated lymphoid tissue), которая обеспечивает адекватную работу врожденного и приобретенного иммунного ответа.
Поддержание целостности барьера ЖКТ и адекватный иммунный ответ на пищевые аллергены во многом обеспечиваются нормальной микрофлорой кишечника. Значимость микрофлоры кишечника в формировании иммунной системы доказана экспериментально на животных. Врожденное и созданное искусственно отсутствие микробиоты у животных приводит дефектам строения и функции GALT – основным лимфоидным органом, ответственным за формирование оральной толерантности. У стерильных животных отмечено уменьшение количества лимфоидных образований GALT, в которых происходит распознавание аллергенов. Основная мембрана слизистой оболочки ЖКТ более тонкая, чем у животных с нормальной микрофлорой. Лимфатические узлы меньших размеров и с меньшим количеством клеток. Помимо структурных нарушений у стерильных животных отмечено снижение Toll-like-рецепторов, которые ответственны за распознавание и презентацию антигенов и за направление иммунного ответа в сторону развития толерантности. Стерильные животные не способны к развитию оральной толерантности [2].
До рождения кишечник плода стерилен, но начиная с интранатального периода быстро заселяется микроорганизмами. В течение нескольких часов после рождения микроорганизмы появляются в кале. При грудном вскармливании преобладают Bifidobacterium, поскольку комплекс олигосахаридов, которые содержатся в грудном молоке, обеспечивает колонизацию этими микроорганизмами кишечник новорожденного ребенка. При искусственном вскармливании микробиоту новорожденных детей составляет микст микроорганизмов, но коррекция состава адаптированных молочных смесей может эти различия уменьшить. К 2 годам микрофлора ребенка мало отличается от микрофлоры взрослых [3], что указывает на огромную значимость поддержания и, при наличии показаний, коррекцию состава кишечной микрофлоры в раннем детском возрасте. При исследовании микрофлоры кишечника детей из группы риска до манифестации АтД были выявлены количественные, качественные и функциональные различия микрофлоры кишечника по сравнению с детьми без предрасположенности к атопии [4]. Количественные изменения характеризуются снижением числа Bifidobacterium species и количественным преобладанием B. Adolescentis, присутствие которых характерно для взрослых людей. Функциональные нарушения характеризуются снижением адгезии Bifidobacterium species, снижением продукции IL10 и увеличением секреции провоспалительных цитокинов [5]. Данные наблюдения позволяют предположить, что пищевые добавки, которые содержат живые микроорганизмы, могут изменить имеющийся дисбаланс и метаболическую активность микрофлоры кишечника и таким образом повлиять на становление иммунологической реактивности ребенка, угрожаемого по атопии, то есть предотвратить развитие заболевания.
Пробиотики представляют собой препараты, содержащие культуры или смеси культур живых микроорганизмов, которые применяются для достижения сбалансированного равновесного состава микрофлоры, заселяющей, в частности, ЖКТ.
Обнаружение бактерий в грудном молоке существенно повысило интерес к пробиотикам, поскольку и молоко здоровой матери рассматривается как источник пробиотических бактерий, которые способствуют защите ребенка от инфекционных и аллергических заболеваний. Пробиотические бактерии, которые первоначально выделены из человеческого молока, находятся в симбиозе с ребенком с рождения, и они изначально адаптированы для проживания в желудочно-кишечном тракте новорожденного. Их использование физиологично у особо чувствительных категорий – новорожденных детей и у детей первого года жизни. Bifidobacterium animalis subsp. lactis BB-12 является повсеместно признанным пробиотическим штаммом, который широко применяется в клинической практике для симптоматического лечения инфекционных диарей (например, при ротавирусной инфекции), антибиотик-ассоциированной диареи, метеоризма и других пищеварительных расстройств. Кроме того, в последнее десятилетие проведены многочисленные исследования эффективности пробиотиков, в которых содержатся Bifidobacterium и Lactobacillus, в профилактике аллергических заболеваний у детей.
В 2014 году опубликованы результаты мета-анализа исследований, посвященных эффективности первичной профилактике атопиче-ского дерматита у детей с наследственной отя-гощенностью по аллергическим заболеваниям [6]. В метаанализ было включено 16 исследований, соответствующих критериям доказательной медицины.
В 11 исследованиях пробиотики назначались беременным женщинам в последнем триместре беременности и во время вскармливания грудью, в 4 – только в постнатальный период (матери или новорожденному ребенку), в 1 исследовании – только пренатально. В 7 исследованиях использовали монопрепарат, в 9 – комбинации бактерий. Эффективность лечения оценивали по частоте манифестации АтД на первом году жизни у детей основной группы и группы сравнения – дети с отягощенной наследственностью, но не получавшие про-биотики. Более эффективным оказалось назначение пробиотиков в пре- и постнаталь-ном периоде (последние месяцы беременности и ребенку с момента рождения до 1 месяца жизни) по сравнению с назначением только в пренатальном и только в постнатальном периоде.
Профилактическое влияние пробиотиков на иммунную систему детей, предрасположенных к аллергическим заболеваниям, реализуется через их влияние на эпителиальные и дендритные клетки субэпителиального слоя слизистой оболочки ЖКТ, где они активируют образраспознающие Tool-lake-рецепторы, что приводит к формированию пищевой толерантности. Помимо новорожденных детей с отягощенным семейным анамнезом, воздействие многих постнатальных факторов может вызывать нарушение формирования нормальной микрофлоры. К ним можно отнести детей, рожденных путем кесарева сечения, с недоношенностью, поздним прикладыванием к груди, длительным пребыванием в родильном доме, раннем искусственном вскармливании.
АтД является, как правило, самым ранним клиническим проявлением атопии и наиболее часто встречающимся атопическим заболеванием у детей первых лет жизни. Кожные покровы ребенка раннего возраста не случайно становятся «органом-мишенью» аллергической реакции. Это связано с анатомо-гистологическими особенностями, а также с характером иммунного ответа кожи на воздействие антигенов внешней среды у новорожденного и грудного ребенка. Собственно кожа (дерма) и подкожная жировая клетчатка детей первых месяцев жизни представляют собой «средоточие» клеток, участвующих в распознавании, представлении антигенов и в ответе на них. Особенно большое значение имеет наличие в коже и подкожной клетчатке множества тучных клеток. Исследователи отмечают, что с конца ХХ века появилась тенденция к более ранней манифестации заболевания (с первого-второго месяца жизни), частая манифестация заболевания у детей, находящихся на грудном вскармливании, более тяжелое течение с увеличением площади поражения кожи, более частое, чем в предшествующие десятилетия, формирование респираторной аллергии у детей с АтД [7]. Аллергические болезни кожи у детей первых лет жизни составляют 80–85% случаев всей аллергической патологии [8]; у 50% пациентов манифестация АтД происходит на первом году жизни (9); у 60– 65% детей с АтД выявлены дисбиотические нарушения кишечника [10].
АтД гетерогенен по клинико-иммунологическим формам и ответу на терапию. В настоящее время рассматривают иммунную и неиммунную формы заболевания. При IgE-зависимой форме АтД положительный эффект влияния пробиотиков на течение заболевания может быть связан с иммунотропным действием пробиотиков, которое описано ранее, хотя не следует переоценивать влияние пробиотиков на сформировавшийся атопический фенотип ребенка. Тем не менее такие механизмы пробиотиков, как активация синтеза sIgA, стимуляция образования биопленки и др., способствуют повышению барьерной функции ЖКТ, что снижает триггерную роль пищевых аллергенов у детей как с IgE, так и не с IgE-зависимой формой заболевания. Секреция противомикробных пептидов (бактериоци-нов), конкурентное блокирование адгезии патогенных бактерий повышает резистентность ребенка с АтД инфекциям ЖКТ и тем самым также способствует сохранности барьерной функции слизистой оболочки кишечника. Пробиотики не могут быть монотерапией АтД, но вносят существенный вклад в эффективную комплексную терапию этого распространенного заболевания. Кроме того, применение пробиотиков актуально при совместном течении двух столь часто встречающихся патологических состояний, как острые кишечные инфекции (ОКИ) и АтД. Иммунный дисбаланс и нарушения микробиоценоза ЖКТ, возникающие в результате подобного сочетания, могут приводить как к усилению клинических проявлений, так и к низкой эффективности традиционного лечения этих двух патологических состояний. Назначение симбиотического препарата Линекс детям с АтД с первых дней острой кишечной инфекции (курсом не менее 2 недель) заметно ускоряло сроки выздоровления, улучшало прогноз и исход заболевания, а также способствовало снижению риска и длительности обострения фоновой аллергической патологии, доказанно влияя на выраженность микроэкологических нарушений кишечника [11].
В метаанализе, проведенном в 2014 году [12], подтверждена клиническая эффективность пробиотиков и симбиотиков в комплексной терапии АтД у детей и взрослых.
Данные литературы свидетельствуют о высокой эффективности Lactobacilli LGG и Bifidobacteria ВВ-12 [13], при этом подчеркивается, что нет преимуществ в использовании микста бактерий перед монопрепаратами [14]. Линекс для детей отвечает всем требованиям, предъявляемым к пробиотику, который можно с успехом использовать у детей с целью профилактики и комплексного лечения АтД. Это пищевая добавка, которая содержит только Bifidobacterium animalis subsp. lactis ВВ-12 не менее 1,0×10*8 КОЕ/г (что соответствует 1,5×10*8 КОЕ/саше). Линекс для детей не содержит лактозы. Вспомогательный компонент мальтодекстрин нейтрален для пищеварения младенца. Пробиотик Линекс для детей хорошо переносится и может быть рекомендован при любых неблагоприятных состояниях, которые сопряжены с риском нарушения микробиоценоза и иммунологической толерантности кишечника [15].
Д.м.н. Л.С. Круглова
Московский Научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения г. Москвы
Современная медицинская наука дает возможность практикующему врачу рассматривать заболевания не только в узких рамках симптомокомплекса, но и с точки зрения изменения функциональных резервов организма человека в результате нарушения его адаптационных возможностей. Неуклонный рост заболеваемости атопическим дерматитом (АтД), наличие рецидивирующих, хронических форм создают потребность в интеграции лечебно-реабилитационных технологий, направленных на восстановление и сохранение здоровья, нарушенного данной патологией.
По современным представлениям человеческий организм является определенной экологической нишей для множества разнообразных микроорганизмов, которые в норме формируют своего рода различные биотопы, являющиеся достаточно сложными системами, сформировавшимися в процессе эволюции и со временем приобретшие определенную устойчивость применительно к особенностям макроорганизма. Биотопы отличаются не только многокомпонентностью, но и количественным разнообразием входящих в них представителей микрофлоры [1].
Постоянство бактериальной аутомикрофлоры организма человека позволяет рассматривать бактерий, существующих преимущественно в четырех локализациях - на коже и слизистой полости рта, кишечника, половых органов - как своеобразный прокариотический орган. Причем изменения в одном из биотопов могут приводить к нарушениям в других. Формирование микрофлоры биотопов организма, и в первую очередь кожи и кишечника, происходит уже с самого рождения ребенка при прохождении по родовым путям. В дальнейшем на формирование влияет много факторов: состав микрофлоры биотопов матери, вид вскармливания, а затем и характер питания, состояние соматического здоровья ребенка и состояние окружающей среды [2,3].
Из всех биотопов организма наибольшая численность и видовое разнообразие бактерий отмечается в биотопе кишечника: так, на площади в 200 м 2 обитает 10 12 -10 14 бактерий, может встречаться до 450 видов различных микроорганизмов, общая масса которых доходит до 5% массы самого кишечника [4,5]. При этом в разных отделах кишечника количество и состав микроорганизмов биоценоза различен. В тонком кишечнике микробов меньше - это преимущественно лактобациллы, стрептококки и веилонеллы, в толстом кишечнике их больше, причем преобладают кишечные палочки и анаэробные бактерии.
Многочисленные микроорганизмы обеспечивают такие важные функции, как выработка ферментов, участвующих в метаболизме белков, липидов, жиров, нуклеиновых и желчных кислот, формирование механизмов иммунной защиты, поддержание гомеостаза организма, продукция биологически активных веществ и витаминов, детоксикация эндогенных и экзогенных субстратов и многие другие.
Микрофлора кишечника условно подразделяется на защитную, сапрофитную и оппортунистическую (условно-патогенную). Защитная микрофлора наиболее многочисленная (до 95%) и в основном представлена лактобактериями, бифидобактериями и кишечной палочкой с нормальными ферментативными свойствами. Именно они обеспечивают постоянство микрофлоры за счет колониальной резистентности. Так, бифидобактерии, лактобактерии выделяют молочную, уксусную кислоты, другие вещества, обладающие избирательным антимикробным действием. Кислая среда, обусловленная жизнедеятельностью этих микроорганизмов, препятствует проникновению и закреплению на слизистой патологических микробов, не свойственных данному биотопу. Помимо этого, бифидобактерии стимулируют клеточное звено иммунитета и участвуют в синтезе иммуноглобулинов. Данные бактерии являются естественными биосорбентами и способны накапливать значительное количество соединений тяжелых металлов, фенолов, формальдегидов и других токсичных веществ [6,7]. Однако в соответствии с современными воззрениями, скорее всего, недостаточное количество лактобактерии является основным отягчающим фактором при атопическом дерматите.
Именно лактобактерии в значительной степени снижают всасывание аллергенов в кишечнике и стимулируют синтез иммуноглобулинов класса А, которые, особенно в раннем детском возрасте, являются основными антителами против пищевых аллергенов [8,9].
Сапрофитная микрофлора кишечника представлена эпидермальным и сапрофитным стафилококками, энтерококками и другими микроорганизмами, основной функцией которых является утилизация конечных продуктов метаболизма макроорганизма [5].
Оппортунистическая микрофлора может быть представлена различными микроорганизмами (3-гемолитический стрептококк, золотистый стафилококк, спороносные анаэробы, грамотрицательные энтерококки, грибы рода Candida ), которые при определенных условиях вызывают патологический процесс [5].
Таким образом, в кишечном микробиоценозе, как в единой системе, существуют корреляционные связи между различными видами бактерий. Нарушение колонизационной резистентности кишечника, связанное с изменением состава постоянной микрофлоры, способствует колонизации патогенными и условно-патогенными бактериями, нарушению основных функций, что и приводит к формированию дисбиоза [Мельникова, 1997; Билимова, 2000; Белова с соавт., 2004; Cammaro-ta, Ogava, 1998].
Согласно существующему в России медицинскому стандарту оказания специализированной помощи при патологии желудочно-кишечного тракта (ЖКТ) дисбиоз кишечника рассматривается, как своеобразный клинико-лабораторный синдром, который характеризуется изменением качественного и/или количественного состава аутомикрофлоры, с возможной транслокацией микроорганизмов в несвойственные для них биотопы; при этом данные изменения могут сопровождаться клиническими симптомами поражения кишечника. В широком понимании дисбиоз является проявлением общего нарушения в различных микробиотах организма, которое приводит к нарушению функционирования микробиот и сопровождается определенными симптомами, ассоциированными с различными патологическими состояниями [5,10,11].
При развитии дисбиоза защитная микрофлора кишечника перестает выполнять свои функции в достаточной степени, что приводит к формированию патологических состояний либо усугублению течения имеющейся соматической патологии [12,13]. Ассоциированные с дисбиозом заболевания в зависимости от преобладания механизмов, отягчающих течение болезни, условно подразделяются на 4 группы:
- заболевания органов пищеварения,
- гнойно-воспалительные заболевания,
- аллергические заболевания,
- заболевания, связанные с нарушением обмена веществ (метаболизма).
Безусловно, рациональные схемы лечения атопического дерматита должны включать методы детоксикации (в частности, энтеросорбции) и использование препаратов, восстанавливающих и поддерживающих нормальную микрофлору кишечника. Энтеросорбция является неинвазивным методом детоксикации и направлена на выведение из организма различных эндогенных и экзогенных аллергенов, токсинов, патогенных микроорганизмов и продуктов их жизнедеятельности. Известно, что на фоне проведения энтеросорбционных мероприятий происходит повышение функциональной активности клеточного и гуморального иммунитета, ускоряется регресс объективных и субъективных симптомов АтД [17,18].
Существенным является и то, что сорбенты позволяют снизить медикаментозную нагрузку, а в ряде случаев и обходиться без них. Требования к современным энтеросорбентам следующие: высокие сорбционные свойства (емкость); отсутствие токсических свойств и системной фармакокинетики; атравматичность для слизистых оболочек ЖКТ; хорошая эвакуаторная способность; высокая комплаентность [19].
Механизм процесса энтеросорбции зависит от двух факторов - характеристик сорбента и структуры подлежащих сорбции веществ. Сорбенты могут отличаться по ряду признаков: лекарственная форма, физические свойства и химическая структура. Одними из самых эффективных сорбентов являются природные органические на основе пищевых волокон, такие как лигнин, который не усваивается в пищеварительной системе человека и полностью ферментируется кишечными бактериями. Важнейшее свойство лигнина - высокая сорбционная активность.
Вместе с тем большой интерес представляет развитие относительно нового направления в лечении атопического дерматита - включение в комплекс терапевтических мероприятий пребиотиков , выделенных из естественных источников и обладающих определенными регулирующими свойствами в отношении функционирования биотопа кишечника. В отличие от пробиотиков, которые поставляют необходимые бактерии извне, пребиотики выступают в качестве питательной среды для развития собственной нормальной микрофлоры организма, что способствует более быстрому и устойчивому восстановлению нормальной аутомикрофлоры кишечника [20,21]. Как правило, в качестве пребиотиков используют вещества, содержащие бифидогенные факторы, стимулирующие рост и развитие полезных бактерий. Таким веществом, в частности, является лактулоза - синтетический стереоизомер молочного сахара - лактозы.
Таким образом, на сегодняшний день идеальным сочетанием можно считать комбинированные лекарст венные средства, содержащие пребиотик и адсорбент. Таким средством является препарат Лактофильтрум ® , включаюший сорбент и пребиотик. В качестве сорбента препарат содержит растительный компонент - лигнин, который обладает неспецифическим дезинтоксикационным действием. За счет большой площади поверх ности и развитой системы пор обладает высокой сорбционной емкостью и таким образом способен выводить из организма токсины, аллергены и патогенные микро организмы. В качестве пребиотика выступает лактулоза, положительное влияние которой на микрофлору кишечника обусловлено целым рядом фармакологических свойств. Так, продукты бактериального метаболизма лактулозы сдвигают рН среды в толстой кишке в кислую сторону, что при водит к подавлению размножения патогенных микроорганизмов и угнетению процессов гниения. Помимо этого, являясь пищевым субстратом для бактерий, лактулоза стимулирует рост собственных бифидобактерий и лактобактерий в толстом кишечнике, а это, в свою очередь, восстанавливает, нарушенные функции биотопа кишечника.
Активные составляющие препарата не инактивируются в агрессивных средах желудка и двенадцатиперстной кишки, что обеспечивает 100%-ю доставку непосредственно к месту действия.
Лактофильтрум ® производится из компонентов природного происхождения в таблетированной форме и удобен в применении. Препарат зарекомендовал себя как высоко безопасный, который практически не имеет противопоказаний к применению и побочных эффектов [22,23].
В клинических условиях под нашим наблюдением находилось 40 пациентов (средний возраст 18,9±2,3 года, продолжительность заболевания 11,4±2,7лет) с диагностированным по основным критериям атопическим дерматитом в стадии обострения. У большинства пациентов АтД носил распространенный характер - ДИШС (Дерматологический индекс шкалы симптомов) составил 18,2±2,3 балла, что соответствует среднетяжелому течению АтД. В зависимости от проводимого лечения пациенты были разделены на 2 сопоставимые по всем параметрам группы. В основную группу вошли 20 больных, которые получали препарат
Лактофильтрум ® по 2 таблетки 3 раза в сутки на протяжении 21 дня и фармакотерапию, соответствующую стандартам при данной патологии. Пациенты 2 группы (20 человек) получали традиционную медикаментозную терапию.
До лечения у 97,5% пациентов был диагностирован дисбиоз кишечника, причем у 52,5% пациентов он протекал с клиническими симптомами (метеоризм, усиление перистальтики, нарушение стула, дискомфортные субъективные ощущения). После комплексного лечения в основной группе у 95% пациентов отмечалась нормализация содержания лактобактерий, бифидобактрий и Е. coli. Такая же тенденция наблюдалась и в отношении клинических симптомов дисбиоза. В группе сравнения достоверно значимых изменений количественного содержания лактобактерий, бифидобактрий и Е. coli не отмечалось (рис.1).
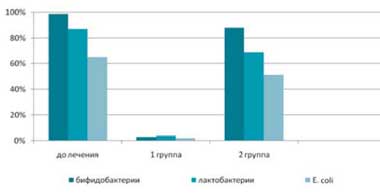
Рис. 1. Число пациентов с нарушением колониальной резистентности
до и после комплексного лечения, включающего применение Лактофильтрума ®
и традиционного медикаментозного лечения
Под влиянием комплексного лечения (1 группа) через 3 недели общие проявления всех объективных симптомов заболевания сохранялись в среднем лишь у 10% больных, в то время как в группе сравнения они были выражены в 54% случаев (рис. 2).
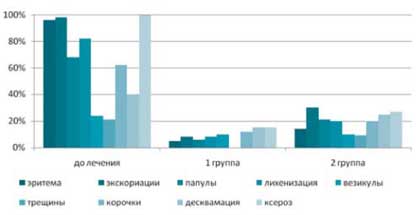
Рис. 2. Динамика регресса клинических симптомов у больных атопическим дерматитом под влиянием различных методов лечения
К концу лечения индекс ДИШС, отражающий тяжесть течения АтД, в основной группе снизился на 84%, в группе сравнения лишь на 53%. Анализ выраженности зуда с использованием опросника Behavioral rating scores (BRS) показал выраженное отрицательное влияние зуда на повседневную деятельность пациентов с АтД. Так, до лечения в 1-й группе значение BRS составило 7,1 ±0,4 баллов, во 2-й группе - 6,8±0,5 баллов. Уже через 1 неделю от начала лечения в 1-й группе отмечался более выраженный регресс субъективной симптоматики: снижение BRS на 55%, во 2-й группе - на 26%. К концу лечения в 1-й группе значение BRS составило 0,4±0,1 балла. В контрольной группе к концу лечения индекс снизился лишь на 58% (рис. 3). Эти данные находились в соответствии с показателями биохимических маркеров зуда (табл. 1).
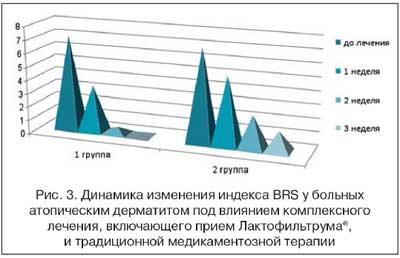
Таблица 1.
Динамика показателей гистамина и серотонина в сыворотке крови у больных АтД под влиянием комплексного лечения, включающего прием Лактофильтрума ® и традиционной медикаментозной терапии
| Изучаемый показатель | Контроль(n=20) | До лечения (n=40) | После лечения | |
|---|---|---|---|---|
| 1 группа (n=20) | 2 группа (n=20) | |||
| Серотонин (мкмоль/л) | 0,6±0,03 | 2,35±0,24Р1** | 0,81±0,32Р2*** | 1,46±0,22РГ**,РЗ* |
| Гистамин (мкмоль/л) | 0,8±0,06 | 2,14±0,62Р1** | 0,87±0,13Р2*** | 1,35±0,25Р1***,Р2** |
| Примечание: Р1 - сравнение с нормой; Р2 - сравнение с показателями до лечения; РЗ - сравнение с основной группой; *- р | ||||
Как видно из приведенных в таблице данных, после комплексной терапии, включающей применение Лактофильтрума ® отмечалось восстановление повышенных в исходном состоянии показателей серотонина и гистамина до нормальных значений - 0,81 ±0,32 и 0,87±0,13 (рВ процессе лечения с улучшением клинической картины заболевания пропорционально улучшались и показатели качества жизни (рис. 4). В результате анализа полученных данных, более выраженная положительная динамика дерматологического индекса качества жизни (ДИКЖ), особенно в первые дни терапии, была отмечена у пациентов 1 группы. Так, в первую неделю параметры ДИКЖ улучшились на 30% в 1 группе и лишь на 8% во 2 группе (рис. 5). К концу курса лечения ДИКЖ улучшился на 87 и 54% соответственно.
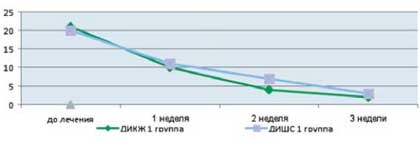
Рис. 4. Динамика изменения показателей, отражающих субъективные и объективные симптомы заболевания
у пациентов с АтД под влиянием комплексного лечения, включающего прием Лактофильтрума ®
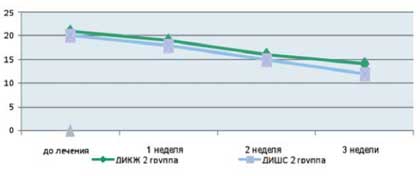
Рис. 5. Динамика изменения показателей, отражающих субъективные и объективные симптомы заболевания
у пациентов с АтД под влиянием традиционной медикаментозной терапии
Таким образом, по оценке самими пациентами эффективности и комфортности проводимого лечения, метод, включающий применение Лактофильтрума ® , является наиболее эффективным.
Выводы
Нарушение колониальной резистентости кишечника, приводящее к повышенной эндотоксинемии, аллергизации и нарушению гомеостаза, может отразиться на состоянии кожи и течении атопического дерматита.
Представители нормальной микрофлоры биоты кишечника выполняют физиологически важную функцию поддержания постоянства внутренней среды организма, принимают участие в формировании иммунобиологической реактивности макроорганизма. Нарушение нормоценозаспособствуетхронизации патологических процессов (в частности, атопического дерматита).
Включение препарата Лактофильтрум ® в комплекс терапии больных АтД приводит к более быстрому и выраженному регрессу кожных высыпаний и субъективных ощущений, нормализации функции биотопа кишечника, что в конечном итоге способствует значитель-номуулучшению качества жизни. Препарат не токсичен, не вызывает побочных эффектов, обладает высокой комплаентностью.
Литература
Читайте также:

