Какой слой кожи содержит фибробласты
Обновлено: 29.04.2024
Настоящая кладовая жировых запасов человека, состоящей из жировых клеток (адипоцитов) и соединительной ткани, богатой коллагеном. Здесь также располагаются кровеносные сосуды, нервы и волосяные фолликулы.
Толщина гиподермы варьируется в зависимости от участка тела: наиболее толстый - в зоне ягодичных мышц, наиболее тонкий - в области ладоней. Полностью отсутствует жировая прослойка в зоне век, губ и шеи. Размеры жировых клеток же обусловлены привычками и образом жизни человека.
Основные функции гиподермы:
- крупный источник энергии для организма человека
- присоединение верхних слоев кожи к нижележащим
- защита внутренних органов человека
- терморегуляция
- является главным депо для жирорастворимых витаминов и их производных
- участник синтеза гормонов
- гиподерма заполняет пространство между тканями и внутренними органами
Кроме этого, в гиподерме находятся стволовые клетки, которые могут превращаться в клетки другой этиологии: фибробласты, адипоциты, васкулаторные клетки.
За молодость кожи отвечают не только коллагеновые и эластиновые волокна, но и состояние гиподермы. С течением времени количество жировой ткани в области лица значительно уменьшается, что напрямую влияет на тургор и эластичность кожи, обуславливая признаки птоза кожи. К этому добавляется деградация костной и мышечной ткани лица, также негативно влияющие на общий вид лица.
Возможны состояния, когда в связи с истончением эпидермиса с дермой, начинает просвечивать гиподерма. Для данной патологии характерен желтоватый оттенок лица и встречается у пациентов после длительных болезней.
Адипоциты
Жировые клетки, находящиеся в гиподерме. Количество адипоцитов у каждого человека заложено генетически и без инвазивного вмешательства повлиять на их количества невозможно (в меньшую сторону).
Особенностью жировых клеток является их способность увеличиваться в размерах в 27 раз! От профицита калорий адипоциты увеличиваются до определенного момента, а далее под влиянием преадипоцитов жировые клетки начинают размножаться, увеличивая общее количество адипоцитов. Повернуть вспять данный процесс невозможно.
Более подробно об особенностях ПЖК и работы с жировой тканью вы можете узнать на нашем курсе: "Коррекция тела. Комплексный подход к работе с подкожно-жировой клетчаткой. Теория, постановка руки":
Цель курса: получить устойчивую теоретическую базу и практические навыки для проведения процедур по коррекции тела при помощи комплексных инструментов косметологии и диетологии.
Курс для специалистов со средним и высшим медицинским профессиональным образованием, прошедших практические курсы по мезотерапии.
Группа до 8 человек.
Преподаватели:

Иванов Александр Игоревич - врач-дерматовенеролог, косметолог высшей категории; главный врач ВШМК «MEDERi»; тренер-эксперт по работе МЕSOPHARM; разработчик ряда новых методик в практической мезотерапии; сертифицированный тренер школы Ли Хин Чоля, одного из основоположников применения мезонитей в косметологии.

Сергеев Сергей Сергеевич - врач-диетолог, член национальной ассоциации диетологов и нутрициологов, член Российского общества медицинской элементологии, эксперт на радио и ТВ.
ОТЗЫВЫ ОБ ОБУЧЕНИИ В ВШМК "MEDERi"
Нашем YouTube-канале Вы можете найти для себя бесплатные видеоуроки от наших преподавателей и партнеров!
Обучение проходит по адресу:
СПб, станция метро "Петроградская", Каменноостровский пр. 61/2, вход в арку со стороны улицы Чапыгина.
Анатомия и физиология кожи
Кожа – наш самый большой орган, составляющий 15% от общей массы тела. Она выполняет множество функций, прежде всего защищает организм от воздействия внешних факторов физической, химической и биологической природы, от потери воды, участвует в терморегуляции. Последние научные данные подтверждают, что кожа не только обладает собственной иммунной системой, но и сама является периферическим иммунном органом.
Структура кожи
Кожа состоит из 3 слоев: эпидермиса, дермы и подкожной жировой клетчатки (ПЖК) (рис. 1). Эпидермис – самый тонкий из них, представляет собой многослойный ороговевающий эпителий. Дерма – средний слой кожи. Главным образом состоит из фибрилл структурного белка коллагена. ПЖК содержит жировые клетки – адипоциты. Толщина этих слоев может значительно варьировать в зависимости от анатомического места расположения.
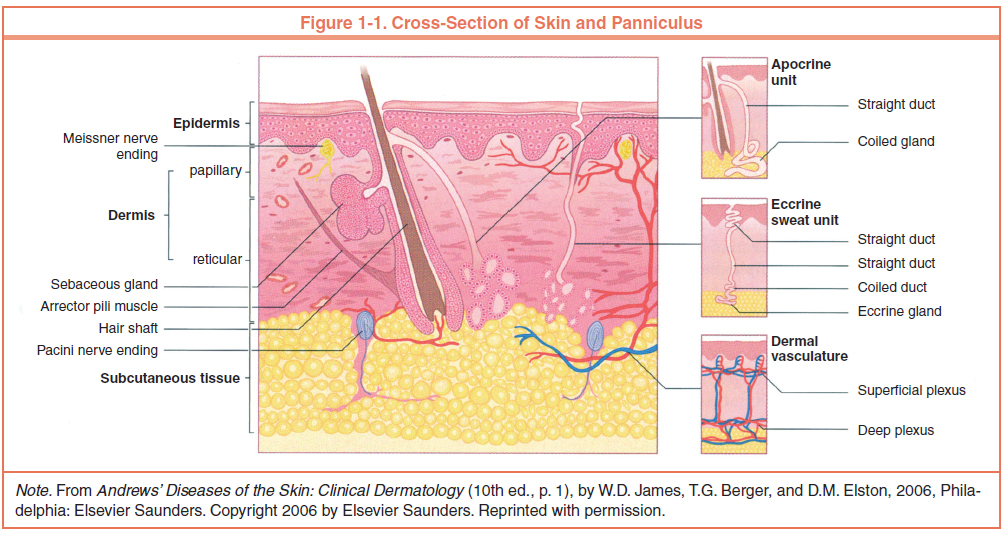
Рис.1. Структура кожи
Эпидермис
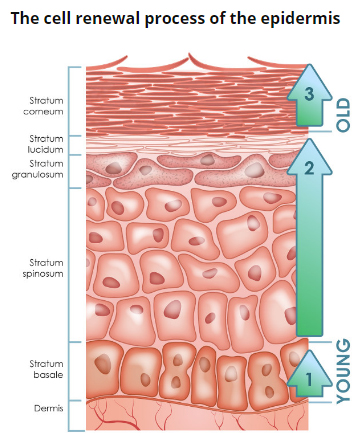
Рис. 2. Эпидермис
Эпидермис – постоянно слущивающийся эпителиальный слой кожи, в котором представлены в основном из 2 типа клеток – кератиноциты и дендритные клетки. В небольшом количестве в эпидермисе присутствуют меланоциты, клетки Лангерганса, клетки Меркеля, внутриэпидермальные Т-лимфоциты. Структурно эпидермис разделяется на 5 слоев: базальный, шиповатый, зернистый, блестящий и роговой , различающиеся положением и степенью дифференцировки кератиноцитов, основной клеточной популяции эпидермиса (рис. 2).
Кератинизация. По мере дифференцировки кератиноцитов и продвижения от базального слоя до рогового происходит их кератинизация (ороговевание) – процесс, начинающийся с фазы синтеза кератина кератиноцитами и заканчивающийся их клеточной деградацией. Кератин служит строительным блоком для промежуточных филаментов. Пучки из этих филаментов, достигая цитоплазматический мембраны, формируют десмосомы, необходимые для образования прочных контактов между соседними клетками. Далее, по мере процесса эпителиальной дифференцировки, клетки эпидермиса вступают в фазу деградации. Ядра и цитоплазматические органеллы разрушаются и исчезают, обмен веществ прекращается, и наступаетапоптозклетки, когда она полностью кератинизируется (превращается в роговую чешуйку).
Базальный слой эпидермиса состоит из одного ряда митотически активных кератиноцитов, которые делятся в среднем каждые 24 часа и дают начало новым клеткам новым клеткам вышележащих эпидермальных слоев. Они активируются только в особых случаях, например при возникновении раны. Далее новая клетка, кератиноцит, выталкивается в шиповатый слой, в котором она проводит до 2 недель, постепенно приближаясь к гранулярному слою. Движение клетки до рогового слоя занимает еще 14 дней. Таким образом, время жизни кератиноцита составляет около 28 дней.
Надо заметить, что не все клетки базального слоя делятся с такой скоростью, как кератиноциты. Эпидермальные стволовые клетки в нормальных условиях образуют долгоживущую популяцию с медленным циклом пролиферации.
Шиповатый слой эпидермиса состоит из 5-10 слоев кератиноцитов, различающихся формой, структурой и внутриклеточным содержимым, что определяется положением клетки. Так, ближе к базальному слою, клетки имеют полиэдрическую форму и круглое ядро, но по мере приближения клеток к гранулярному слою они становятся крупнее, приобретают более плоскую форму, в них появляются ламеллярные гранулы, в избытке содержащие различные гидролитические ферменты. Клетки интенсивно синтезируют кератиновые нити, которые, собираясь в промежуточные филаменты, остаются не связанными со стороны ядра, но участвуют в образовании множественных десмосом со стороны мембраны, формируя связи с соседними клетками. Присутствие большого количества десмосом придает этому слою колючий вид, за что он и получил название «шиповатый».
Зернистый слой эпидермиса составляют еще живые кератиноциты, отличающиеся своей уплощенной формой и большим количеством кератогиалиновых гранул. Последние отвечают за синтез и модификацию белков, участвующих в кератинизации. Гранулярный слой является самым кератогенным слоем эпидермиса. Кроме кератогиалиновых гранул кератиноциты этого слоя содержат в большом количестве лизосомальные гранулы. Их ферменты расщепляют клеточные органеллы в процессе перехода кератиноцита в фазу терминальной дифференцировки и последующего апоптоза. Толщина гранулярного слоя может варьировать, ее величина, пропорциональная толщине вышележащего рогового слоя, максимальна в коже ладоней и подошв стоп.
Блестящий слой эпидермиса (назван так за особый блеск при просмотре препаратов кожи на световом микроскопе) тонкий, состоит из плоских кератиноцитов, в которых полностью разрушены ядра и органеллы. Клетки наполнены элейдином – промежуточной формой кератина. Хорошо развит лишь на некоторых участках тела – на ладонях и подошвах.
Роговой слой эпидермиса представлен корнеоцитами (мертвыми, терминально-дифференцированными кератиноцитами) с высоким содержанием белка. Клетки окружены водонепроницаемым липидным матриксом, компоненты которого содержат соединения, необходимые для отшелушивания рогового слоя (рис. 3). Физические и биохимические свойства клеток в роговом слое различаются в зависимости от положения клетки внутри слоя, направляя процесс отшелушивания наружу. Например, клетки в средних слоях рогового слоя обладают более сильными водосвязывающими свойствами за счет высокой концентрации свободных аминокислот в их цитоплазме.
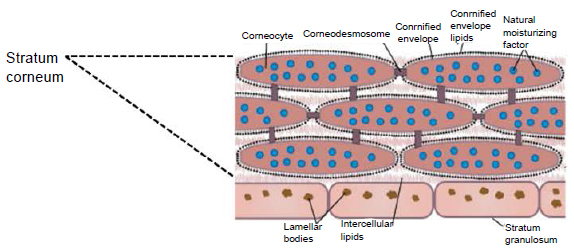
Рис. 3. Схематичное изображение рогового слоя с нижележащим зернистым слоем эпидермиса.
Регуляция пролиферации и дифференцировки кератиноцитов эпидермиса . Являясь непрерывно обновляющейся тканью, эпидермис содержит относительно постоянное число клеток и регулирует все взаимодействия и контакты между ними: адгезию между кератиноцитами, взаимодействие между кератиноцитами и мигрирующими клетками, адгезию с базальной мембраной и подлежащей дермой, процесс терминальной дифференцировки в корнеоциты. Основной механизм регуляции гомеостаза в эпидермисе поддерживается рядом сигнальных молекул – гормонами, факторами роста и цитокинами. Кроме этого, эпидермальный морфогенез и дифференцировка частично регулируются подлежащей дермой, которая играет критическую роль в поддержании постнатальной структуры и функции кожи.
Дерма
Дерма представляет собой сложноорганизованную рыхлую соединительную ткань, состоящую из отдельных волокон, клеток, сети сосудов и нервных окончаний, а также эпидермальных выростов, окружающих волосяные фолликулы и сальные железы. Клеточные элементы дермы представлены фибробластами, макрофагами и тучными клетками. Лимфоциты, лейкоциты и другие клетки способны мигрировать в дерму в ответ на различные стимулы.
Дерма, составляя основной объем кожи, выполняет преимущественно трофическую и опорную функции, обеспечивая коже такие механические свойства, как пластичность, эластичность и прочность, необходимые ей для защиты внутренних органов тела от механических повреждений. Также дерма удерживает воду, участвует в терморегуляции и содержит механорецепторы. И, наконец, ее взаимодействие с эпидермисом поддерживает нормальное функционирование этих слоев кожи.
В дерме нет такого направленного и структурированного процесса клеточной дифференцировки, как в эпидермисе, тем не менее в ней также прослеживается четкая структурная организация элементов в зависимости от глубины их залегания. И клетки, и внеклеточный матрикс дермы также подвергаются постоянному обновлению и ремоделированию.
Внеклеточный матрикс (ВКМ) дермы , или межклеточное вещество, в состав которого входят различные белки (главным образом коллаген, эластин), гликозаминогликаны, самым известным из которых является гиалуроновая кислота, и протеогликаны (фибронектин, ламинин, декорин, версикан, фибриллин). Все эти вещества секретируются фибробластами дермы. ВКМ представляет собой не беспорядочное скопление всех компонентов, а сложноорганизованную сеть, состав и архитектоника которой определяют такие биомеханические свойства кожи, как жесткость, растяжимость и упругость. К белкам ВКМ прикрепляются кератиноциты эпидермиса, которые тесно состыкованы друг с другом. Именно они и формируют плотный защитный слой кожи. Структура ВКМ также способна оказывать регулирующее влияние на погруженные в него клетки. Регуляция может быть как прямой, так и косвенной. В первом случае белки и гликозаминогликаны ВКМ непосредственно взаимодействуют с рецепторами клеток и инициируют в них специфические пути передачи сигнала. Косвенная регуляция осуществляется посредством действия цитокинов и ростовых факторов, удерживаемых в ячейках сети ВКМ и высвобождаемых в определенный момент для взаимодействия с рецепторами клеток. Структурная сеть ВКМ подвергается ремоделированию ферментами из семейства матриксных металлопротеиназ (ММР). В частности, ММР-1 и ММР-13 инициируют деградацию коллагенов I и III типов. Плотность сети ВКМ дермы неравномерна – в папиллярном слое она более рыхлая, в ретикулярном - значительно плотнее как за счет более близкого расположения волокон структурных белков, так и за счет увеличения диаметра этих волокон.
Коллаген – один из главных компонентов ВКМ дермы. Синтезируется фибробластами. Процесс его биосинтеза сложный и многоступенчатый, в результате которого фибробласт секретирует в экстрацеллюлярное пространство проколлаген, состоящий из трех полипептидных α-цепей, свернутых в одну тройную спираль. Затем мономеры проколлагена ферментивным путем собираются в протяженные фибриллярные структуры различного типа. Всего в коже не менее 15 типов коллагена, в дерме больше всего I, III и V типов этого белка: 88, 10 и 2% соответственно. Коллаген IV типа локализуется в зоне базальной мембраны, а коллаген VII типа, секретируемый кератиноцитами, играет роль адаптерного белка для закрепления фибрилл ВКМ на базальной мембране (рис. 4). Волокна структурных коллагенов I, III и V типов служат каркасом, к которому присоединяются другие белки ВКМ, в частности коллагены XII и XIV типов. Считается, что эти минорные коллагены, а также небольшие протеогликаны (декорин, фибромодулин и люмикан) регулируют формирование структурных коллагеновых волокон, их диаметр и плотность образуемой сети. Взаимодействие олигомерных и полимерных комплексов коллагена с другими белками, полисахаридами ВКМ, разнообразными факторами роста и цитокинами приводит к образованию особой сети, обладающей определенной биологической активностью, стабильностью и биофизическими характеристиками, важными для нормального функционирования кожи. В папиллярном слое дермы волокна коллагена располагаются рыхло и более свободно, тогда как ее ретикулярный слой содержит более крупные тяжи коллагеновых волокон.
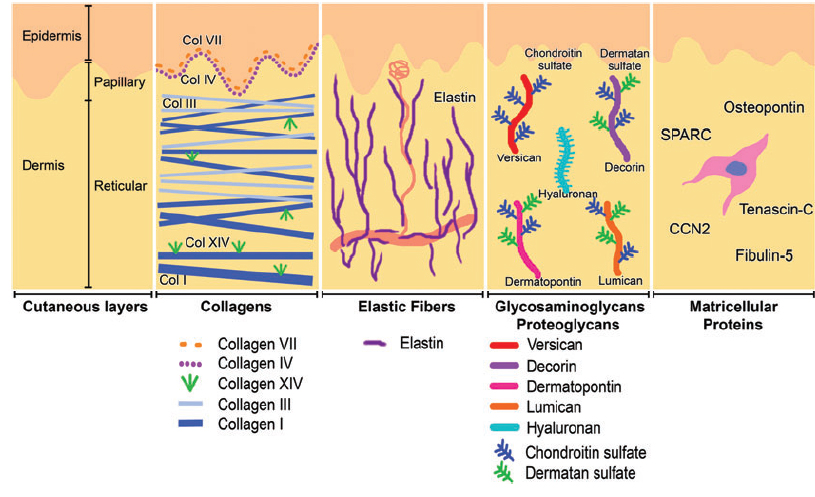
Рис. 4. Схематичное представление слоев кожи и распределения коллагенов разных типов.
Коллаген постоянно обновляется, деградируя под действием протеолитических ферментов коллагеназ и замещаясь вновь синтезированными волокнами. Этот белок составляет 70% сухого веса кожи. Именно коллагеновые волокна «держат удар» при механическом воздействии на нее.
Эластин формирует еще одну сеть волокон в дерме, наделяя кожу такими качествами, как упругость и эластичность. По сравнению с коллагеном эластиновые волокна менее жесткие, они скручиваются вокруг коллагеновых волокон. Именно с эластиновыми волокнами связываются такие белки, как фибулины и фибриллины, с которыми, в свою очередь, связывается латентный TGF-β-связывающий белок (LTBP). Диссоциация этого комплекса приводит к высвобождению и к активации TGF-β, самого мощного из всех факторов роста. Он контролирует экспрессию, отложение и распределение коллагенов и других матриксных белков кожи. Таким образом, интактная сеть из волокон эластина служит депо для TGF-β.
Гиалуроновая кислота (ГК) представляет собой линейный полисахарид, состоящий из повторяющихся димеров D-глюкуроновой кислоты и N-ацетилглюкозамина. Количество димеров в полимере варьирует, что приводит к образованию молекул ГК разного молекулярного веса и длины - 1х10 5 -10 7 Да (2-25 мкм), оказывающих, соответственно, различный биологический эффект.
ГК - высокогидрофильное вещество, влияющее на движение и распределение воды в матриксе дермы. Благодаря этому ее свойству наша кожа в норме и в молодости обладает высоким тургором и сопротивляемостью механическому давлению.
ГК с легкостью образует вторичные водородные связи и внутри одной молекулы, и между соседними молекулами. В первом случае они обеспечивают формирование относительно жестких спиральных структур. Во втором – происходит ассоциация с другими молекулами ГК и неспецифическое взаимодействие с клеточными мембранами, что приводит к образованию сети из полимеров полисахаридов с включенными в нее фибробластами. На длинную молекулу ГК, как на нить, «усаживаются» более короткие молекулы протеогликанов (версикана, люмикана, декорина и др.), формируя агрегаты огромных размеров. Протяженные во всех направлениях, они создают каркас, внося вклад в стабилизацию белковой сети ВКМ и фиксируя фибробласты в определенном окружении матрикса. В совокупности все эти свойства ГК наделяют матрикс определенными химическими характеристиками – вязкостью, плотностью «ячеек» и стабильностью. Однако сеть ВКМ является динамической структурой, зависящей от состояния организма. Например, в условиях воспаления агрегаты ГК с протеогликанами диссоциируют, а образование новых агрегатов между вновь синтезированными молекулами ГК (обновляющимися каждые 3 дня) и протеогликанами блокируется. Это приводит к изменению пространственной структуры матрикса: увеличивается размер его ячеек, меняется распределение всех волокон, структура становится более рыхлой, клетки меняют свою форму и функциональную активность. Все это сказывается на состоянии кожи, приводя к снижению ее тонуса.
Помимо регуляции водного баланса и стабилизации ВКМ, ГК выполняет важную регуляторную роль в поддержании эпидермального и дермального гомеостаза. ГК активно регулирует динамические процессы в эпидермисе, включая пролиферацию и дифференцировку кератиноцитов, окислительный стресс и воспалительный ответ, поддержание эпидермального барьера и заживление раны. В дерме ГК также регулирует активность фибробластов и синтез коллагена. Ремоделируя матрикс, ГК управляет функционированием клеток в матриксе, влияя на их доступность для различных факторов роста и изменяя их функциональную активности. От действия ГК зависит миграция клеток и иммунный ответ в ткани. Таким образом, изменения в распределении, организации, молекулярном весе и метаболизме ГК имеют значимые физиологические последствия.
Фибробласты представляют собой основной тип клеточных элементов дермы. Именно эти клетки отвечают за продукцию ГК, коллагена, эластина, фибронектина и многих других белков межклеточного матрикса, необходимых для формирования соединительной ткани. Фибробласты в различных слоях дермы различаются и морфологически, и функционально. От глубины их залегания в дерме зависит не только количество синтезируемого ими коллагена, но и соотношение типов этого коллагена, например I и III типов, а также синтез коллагеназы: фибробласты более глубоких слоев дермы производят меньшее ее количество. Вообще, фибробласты – очень пластичные клетки, способные менять свои функции и физиологический ответ и даже дифференцироваться в другой тип клеток в зависимости от полученного стимула. В роли последнего могут выступать и сигнальные молекулы, синтезированные соседними клетками, и перестройка окружающего ВКМ.
Подкожно-жировая клетчатка
Подкожно-жировая клетчатка , или гиподерма, - самый нижний слой кожи, располагается под дермой. Состоит из жировых долек, разделенных между собой соединительнотканными септами, содержащими коллаген и пронизанными крупными сосудами. Главными клетками жировых долек являются адипоциты, количество которых варьирует в различных областях тела. В настоящее время ПЖК рассматривают не только как энергетическое депо, но и как эндокринный орган, адипоциты которого участвуют в выработке ряда гормонов (лептина, адипонектина, резистина), цитокинов и медиаторов, оказывающих влияние на метаболизм, чувствительность к инсулину, функциональную активность репродуктивной и иммунной систем.
В этой статье поговорим о функции дермальных фибробластов в коже, процессе их старения, а также о методе обновления и стимуляции регенерации кожи путём введения аутологичных фибробластов.
Введение
Роль дермальных фибробластов (ДФ) в обновлении кожи трудно переоценить, поскольку они являются основным клеточным компонентом соединительнотканной основы кожи, обеспечивающим её гомеостаз и морфофункциональную организацию. Очевидна актуальность этой темы для регенеративной (репаративной) косметологии, задача которой — омоложение кожи путём активации естественных процессов её восстановления.
Функции дермальных фибробластов
Из всех функций ДФ наибольшее внимание специалистов в области эстетической медицины и дерматологии сосредоточено на продуцировании этими клетками компонентов внеклеточного матрикса (ВКМ) дермы: коллагена, эластина, протеогликанов, особенно гиалуроновой кислоты (ГК), и структурных гликопротеинов.
Повышенный интерес именно к этой функции ДФ понятен: названные компоненты ВКМ формируют и поддерживают структуру кожи, обеспечивая её упругость и прочность. Причём ДФ не только синтезируют эти вещества, но и обеспечивают их катаболизм путём прямого фагоцитоза «отработанных» фрагментов фибрилл коллагена и эластина, секреции коллагеназы, гиалуронидазы и прочих ферментов.
Резидентные клетки ткани — образующиеся и постоянно пребывающие в этой ткани.
Другая, и не менее значимая для кожи, активность ДФ оставалась до недавнего времени несколько на обочине поля зрения врачей-практиков, однако сегодня она тоже становится объектом пристального внимания клиницистов. Речь идёт о целом ряде важнейших функций фибробластов. Так, продуцируя коллаген IV типа и ламинин, они влияют на формирование базальной мембраны. Фибробласты формируют строму, которая не только служит каркасом (опорой) для эпителия, но и регулирует структурную организацию и функционирование эпителиальных клеток. Они вырабатывают и выделяют факторы клеточного роста (KGF-1 — фактор роста кератиноцитов, GM–CSF — гранулоцитарно-макрафагальный колониестимулирующий фактор роста), иммунорегуляторные интерлейкины IL-6, IL-8. За счёт секреции факторов роста и интерлейкинов и непосредственного взаимодействия с эпителиальными клетками ДФ играют ключевую роль в регуляции эпидермального морфогенеза. Их паракринная активность служит основой для поддержания гомеостаза стволовых кератиноцитов.
Дермальные фибробласты секретируют факторы, влияющие на дифференцировку лимфоцитов, и факторы, регулирующие численность, миграцию и функции гранулоцитов и макрофагов, обеспечивая тем самым поддержание иммунитета кожи. Вырабатывая множество проангиогенных факторов, которые индуцируют дифференцировку и миграцию эндотелиальных клеток, ДФ способствуют образованию и стабилизации сосудов.
Они принимают участие в процессах нейроэндокринной регуляции кожи. Синтезируют биологически активные пептиды: гормоны, биогенные амины, нейропептиды и нейротрансмиттеры, идентичные таковым в центральной нервной и эндокринной системах, экспрессируют рецепторы андрогенов и эстрогенов, посредством которых осуществляется влияние этих гормонов на кожу человека.
Фибробласты, взаимодействуя с различными резидентными клетками: эпидермальными, эндотелиальными, нервными, жировыми, гемопоэтическими, участвуют практически во всех кожных процессах, в том числе — физиопатологических. Таким образом, ДФ представляют собой центральное звено в биологии кожи: они поддерживают не только гомеостаз ВКМ дермы, обеспечивая её ремоделирование и обновление, но и физиологическое состояние других слоёв и структур кожи.
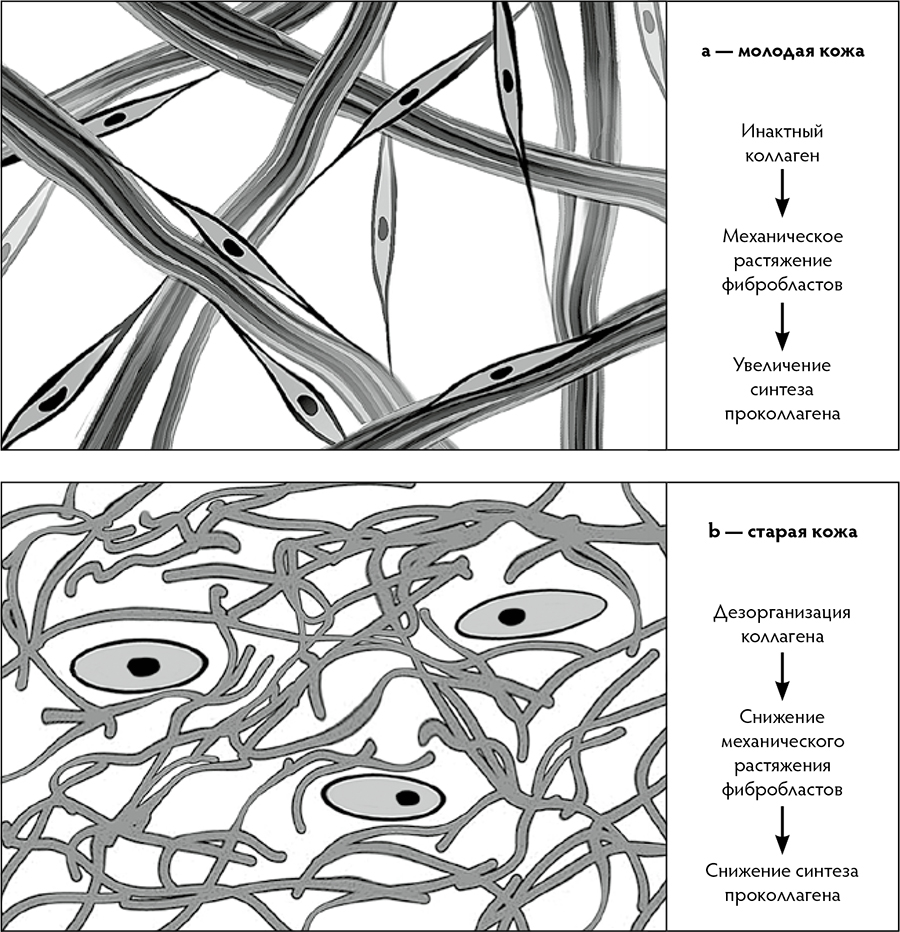
Рис. 1. Взаиморасположение фибробластов и коллагеновых волокон: a — в коже молодых людей (18–29 лет); b — в коже людей старшего возраста (старше 80 лет) (Varani J., et al. 2006, с изм.)
Инволюция дермальных фибробластов
По мере старения организма растёт число ДФ, в которых происходят возрастзависимые изменения, связанные преимущественно с непрерывным накоплением повреждений. Такие ДФ обозначают как «стареющие», или сенесцентные фибробласты (ДФст). Снижается их способность к ремоделированию и организации ВКМ, так как уменьшается синтез и секреция ими основных компонентов ВКМ. Нарушается эпидермальный гомеостаз из‑за негативных изменений в паракринных механизмах, связывающих эпидермис и папиллярный слой дермы. В популяции ДФст происходит увеличение секреции богатого цистеином ангиогенного индуктора — белка 61 (CYR61, или CCN1), стимулирующего продукцию провоспалительных цитокинов и матриксных металлопротеиназ (MMPs). CCN1 и MMPs поддерживают старение клетки путём негативной регуляции гомеостаза коллагена и увеличения его деградации.
Постепенно баланс между синтезом и деградацией коллагена нарушается в пользу последней. Повреждённый коллагеновый каркас ВКМ уже не может удерживать фибробласты в растянутом состоянии, свойственном молодым клеткам. Происходит своего рода коллапс фибробластов, что приводит к нарушению их функций. В процессе инволюции уменьшается численность фибробластов. Снижается и биосинтетическая активность этих клеток, нарушается баланс между синтезом и деградацией ВКМ дермы. В среднем, у пожилых / старых людей, по сравнению с молодыми, общее количество ДФ меньше на 35 %, продукция коллагена в коже снижена на 75 %, причём содержание коллагена уменьшается приблизительно на 1 % в год.
Все сенесцентные изменения в популяции ДФ приводят к постепенному и значительному снижению способности кожи к регенерации и обновлению. Как при этом меняется статус кожи? Уменьшается её толщина, снижается упругость и эластичность, появляются морщины, заломы, птоз тканей — кожа стареет.
Очевидно, что именно ДФ должны быть основной «мишенью» омолаживающих кожу косметологических методов. Так оно и есть: все современные терапевтические воздействия в целях коррекции возрастных изменений кожи — инъекционные, включая PRP-терапию, аппаратные (лазерные, радиочастотные, ультразвуковые) — направлены прежде всего на стимуляцию функциональной активности ДФ, как пролиферативной, так и биосинтетической. Особое место в этом ряду занимает применение аутологичных (собственных) дермальных фибробластов, или SPRS-терапия.
SPRS-терапия как метод оздоровления и обновления кожи
SPRS-терапия (SPRS — от англ. Service for Personal Regeneration of Skin — персонифицированный комплекс лечебно-диагностических процедур для восстановления кожи) — метод регенеративной медицины (РУ ФС №2009 / 308 от 21.07.2010). Его применение позволяет восполнить уменьшившуюся с возрастом популяцию ДФ за счёт введенных в кожу специализированных молодых и функционально активных клеток. Трансплантируются собственные фибробласты кожи пациента, поэтому они полноценно приживаются, интегрируют с резидентной клеточной популяцией и живут «по законам» дермы.
После трансплантации их биосинтетическая активность сохраняется не менее года, причём без какой‑либо дополнительной стимуляции. Как результат, увеличивается синтез коллагена и других компонентов ВКМ, благодаря чему происходит ремоделирование микроструктуры дермы, увеличение её толщины, уменьшение количества и глубины морщин.
Сенесценция — это состояние, при котором клетки с накопленными повреждениями ДНК и истощением механизмов её восстановления перестают делиться, теряют способность к ремоделированию и организации ВКМ.
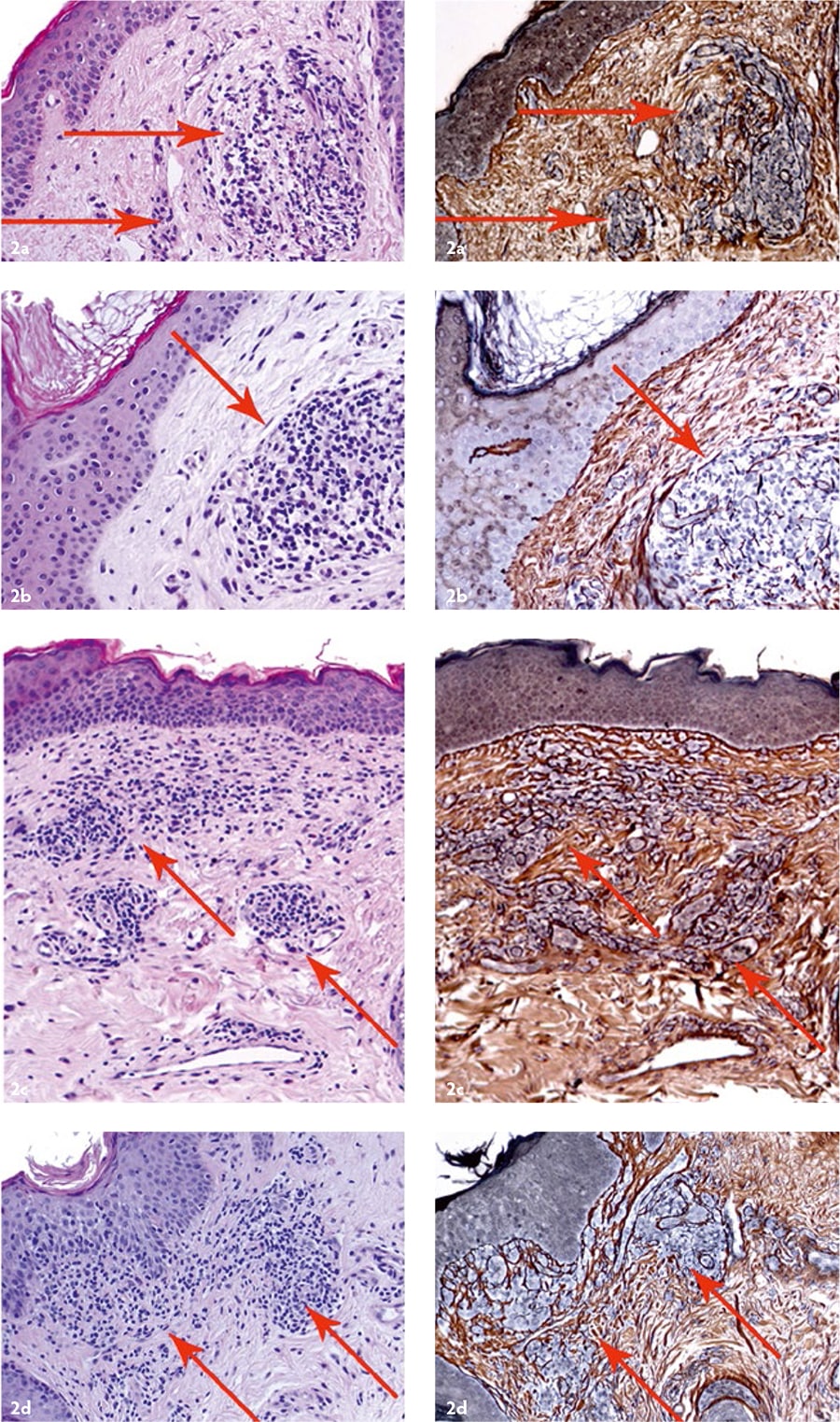
Рис. 2. Кожа после применения аутоДФ: a — через 1 месяц, b — через 3 месяца, c — через 6 месяцев, d — через 12 месяцев. Стрелками указаны группы введённых культивированных аутоДФ. Левая колонка — окраска гематоксилином и эозином, правая колонка — импрегнация нитратом серебра. Ув. ×200. Препараты и микрофотографии Р. В. Деева.
Описание технологии
В специализированной лаборатории Института стволовых клеток человека, соответствующей международным стандартам GMP*, из 4 мм биоптата кожи пациента получают клеточный препарат, содержащий культивированные аутологичные ДФ (аутоДФ). На этапах клеточного процессинга происходит отбор и стимуляция только функционально активных ДФ, которые, несмотря на старение организма, сохраняют высокую способность к делению и синтезу важных для кожи компонентов. Дело в том, что пролиферативный потенциал всей популяции дермальных фибробластов взрослого человека в течение всей его жизни остаётся на довольно высоком уровне — благодаря наличию в фибробластическом диффероне стволовых / прогениторных клеток. Это клетки-предшественницы, которые отвечают за обновление клеточной популяции дермы. Как показали исследования in vitro, первичные культуры, полученные даже от очень пожилых людей (95 лет), содержат до 14 % митотически активных фибробластов.
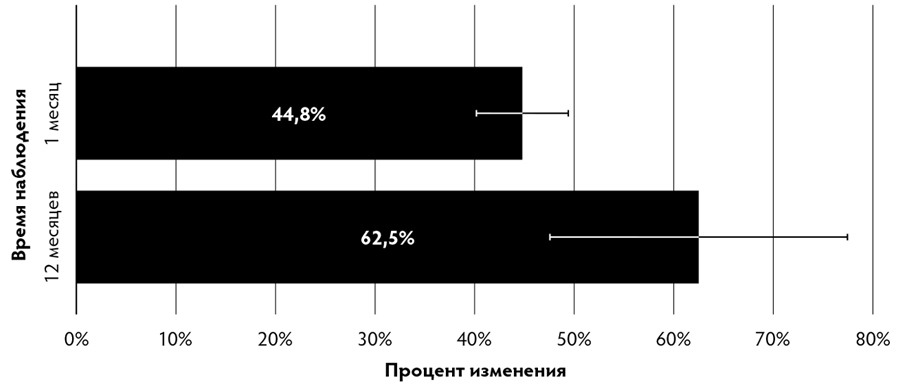
Рис. 3. Относительное изменение толщины кожи после применения аутоДФ (по результатам гистологических исследований).
Данный факт подтверждается и нашими экспериментами: культуры фибробластов дермы, полученные от пациентов 18–82 лет, характеризуются довольно высокой эффективностью колониеобразования (45.0±9.5 %), независимо от возраста донора. Это даёт возможность из небольшого биоптата кожи любого взрослого человека получить необходимое для проведения терапии количество функционально активных клеток.
После трансплантации культивированных ауто ДФ в дерму их биосинтетическая активность сохраняется. В своей работе мы вводили полученный клеточный материал одновременно и в кожу лица, и в кожу за ушной раковиной, откуда затем проводили забор биоптата для гистологического изучения. Наши исследования показали:
- трансплантированные аутоДФ синтезировали компоненты ВКМ дермы на протяжении как минимум 12 месяцев [Рис. 2];
- трансплантированные аутоДФ присутствовали в дерме небольшими группами, без признаков митотической активности, то есть без признаков деления клеток (следовательно, риск развития каких‑либо гиперпластических процессов при их использовании отсутствует);
- образовались новые коллагеновые волокна;
- толщина дермы увеличилась в среднем на 62,5±13,6 % (р=0,028) в течение первых 12 месяцев после применения аутоДФ [Рис. 3].
Через 24 месяца после применения аутоДФ в дерме также регистрировали отдельные группы фибробластоподобных клеток [Рис. 4], продуцирующих коллагеновые волокна. Однако признаков созревания (утолщения) коллагена не наблюдали, из чего следует, что через два года после трансплантации аутоДФ интенсивность их синтетической активности (по сравнению с таковой в течение первого года после трансплантации) была снижена.
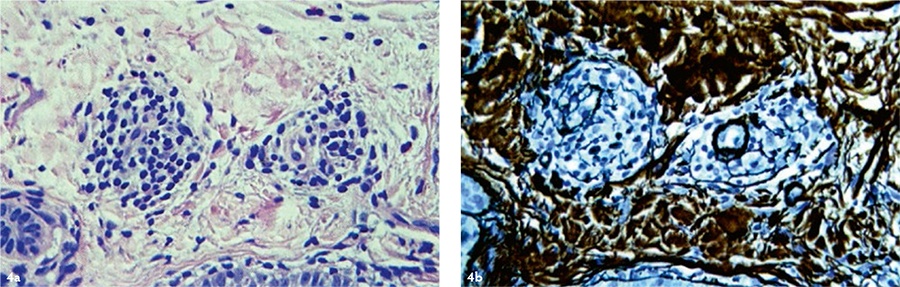
Рис. 4. Кожа пациента М. (54 г.) после применения аутоДФ через 24 месяца. Левая колонка — окраска гематоксилином и эозином, правая колонка — импрегнация нитратом серебра. Ув. ×200. Препараты и микрофотографии Р. В. Деева.
Скорее всего, это связано с уровнем физиологических потребностей дермы (известно, что для обеспечения её физиологического состояния достаточно незначительной функциональной активности фибробластов). По всей видимости, трансплантированные аутоДФ полноценно интегрировались с дермой, стали естественной составляющей её основной клеточной популяции — фибробластического дифферона — и находятся под контролем микроокружения.
Выводы гистологического исследования:
- введенные аутоДФ сохраняют свою жизнеспособность в дерме;
- они располагаются в дерме преимущественно группами;
- их функционирование не приводит к неблагоприятным последствиям, клетки пролиферативно не активны;
- на всех сроках наблюдения в дерме регистрируются признаки увеличения её объёма и процесс синтеза молодых коллагеновых волокон.
Выявленная на гистологическом уровне положительная динамика изменений кожи после применения аутоДФ полностью соответствует клинической картине. Уже через 10–14 дней после окончания курса SPRS-терапии отмечается повышение упругости кожи, уменьшение её рельефности (уменьшение выраженности морщин), улучшение цвета и контуров лица. Эффект имеет нарастающий характер. Так, если через месяц после инъекции на «хорошо» и «отлично» клинический результат оценили 88 % пациентов, то уже через три месяца и позже — 100 %. Врачи-исследователи через месяц определили результат как «хороший» и «отличный» у 86 % пациентов, через три месяца и позже — у 100 % пациентов. Положительные, прогрессирующие со временем (на протяжении как минимум 12 месяцев) изменения состояния кожи подтверждены нами и с помощью инструментальных методов исследования.
Заключение
Инновационная технология — SPRS-терапия, основанная на принципах регенеративной медицины, — позволяет восстанавливать утраченные с возрастом структуру и функции дермы за счёт уникального биологического механизма собственных коллагенобразующих клеток кожи пациента.
SPRS-терапия используется в отечественной эстетической медицине более восьми лет, зафиксировано более 1000 клинических наблюдений пациентов, из которых более 80 % повторно (два и более раз), пролечив одну область кожи, обращались в клиники для лечения этим методом кожи других областей.
Для врачебной практики важно, что SPRS-терапия является не только самостоятельным эффективным методом ремоделирования дермы, но и хорошей базовой основой для применения других косметологических вмешательств, направленных на стимуляцию синтетической активности фибробластов, что позволяет в течение длительного времени поддерживать кожу пациента в хорошем состоянии.
Авторы:
Алла Зорина, к. м. н., врач-биохимик, Москва.
Вадим Зорин, к. б. н., врач-биофизик, Москва.

Тело человека состоит из триллионов разнообразных клеток. Наиболее важными клетками самого большого органа в теле человека – кожи, являются фибробласты. Их называют клетками молодости, так как именно активная работа фибробластов способствует поддержанию молодости и красоты кожи.
Фибробласты
Зародышевые клетки соединительной ткани организма. Они участвуют в процессах регенерации и синтеза белков, наиболее важных для омоложения клеток дермы.
В организме человека фибробласты могут находиться в двух формах: активные и неактивные. Активный фибробласт имеет большой размер, отростки, овальное ядро и много рибосом. Такая клетка может делиться и интенсивно вырабатывать коллаген. Неактивные фибробласты называются также фиброцитами. Они являются высокодифференцированными клетками, которые образовываются их фибробластов, не имеют способности к делению, но принимают активное участие в синтезе волокнистых структур и заживлении ран. Неактивные фибробласты имеют несколько меньший размер, чем активные, и отличаются веретенообразной формой.
Все активные фибробласты разделяются на несколько структурно-функциональных типов, каждый из которых выполняет определенные функции:
- малодифференцированные фибробласты обладают выраженными пролиферативными свойствами, то есть, они активно размножаются и растут;
- юные фибробласты – более дифференцированные клетки, которые также способны к пролиферации, но в отличие от малодифференцированных, могут синтезировать коллаген и кислые гликозаминогликаны;
- зрелые фибробласты образуются из юных форм, практически не могут размножаться, и разделяются на три подтипа:
- фиброкласты разрушают коллаген путем фагоцитоза и внутриклеточного лизиса;
- коллагенобласты синтезируют коллаген;
- монофибробласты играют роль в сокращении фиброзной ткани при заживлении ран.
Фибробласты располагаются в среднем слое кожи человека – в дерме. Там они вырабатывают внеклеточный матрикс, компоненты которого и формируют своеобразный каркас кожи. Основными компонентами внеклеточного матрикса являются гликопротеины, протеогликаны и гиалуроновая кислота. Широко известный коллаген является превалирующим гликопротеином внеклеточного матрикса. Кроме того, фибробласты продуцируют также белки фибрин, эластин, тинасцин, нидоген и ламинин, которые используются в качестве «строительного материала» для кожи.
Еще один продукт синтеза фибробластов – это факторы клеточного роста, к которым относятся:
- основной фактор, усиливающий рост всех клеток кожи;
- трансформирующий фактор, способствующий стимулированию выработки эластина и коллагена;
- эпидермальный фактор, ускоряющий деление клеток и перемещение кератиноцитов;
- фактор роста кератиноцитов.
Основные функции фибробластов:
- синтез коллагена, эластина, гиалуроновой кислоты и других компонентов внеклеточного матрикса;
- формирование сосудов;
- усиление процессов клеточного роста;
- ускорение разрастания тканей;
- заживление поврежденной кожи;
- направление клеток иммунной системы к бактериям и другим чужеродным агентам.
С возрастом в организме человека способности фибробластов в плане активного синтеза и пролиферации в тканях кожи снижаются, в результате чего происходит уменьшение содержания их главных компонентов — гиалуроновой кислоты, коллагена, эластина, сосудистой сети. Это отражается на внешнем виде кожного покрова.
Сегодня, благодаря успехам биотехнологии, появилась возможность естественным путем повлиять непосредственно на причину возрастного увядания кожных тканей. Этого удалось достигнуть способом обогащения ее собственными молодыми фибробластами, которые являются строителями внеклеточного матрикса.
Трансплантация в кожу лица собственных молодых клеток фибробластов способна эффективно и достаточно быстро активизировать процессы обновления и восстановления ее структуры. Аутологичные (свои) клетки не воспринимаются собственной иммунной системой как антиген (чужеродные) и, следовательно, организмом не отторгаются, а полноценно функционируют. Преимуществом клеточного омоложения является и то, что трансплантированные фибробласты долгое время (от полугода до полутора лет) сохраняют функциональную активность в части усиленного синтеза гиалуроновой кислоты, коллагена, эластина и других компонентов матриксной системы кожи. В течение этого срока постоянно продолжается улучшение ее состояния.
Такая методика аутотрансплантации фибробластов в косметологии получила официальное разрешение Росздравнадзора.

Основа всех основ для любого косметолога. Знание строения, функций и клеток кожи необходимо для эффективной работы с пациентами.
Кожа является самым большим органом нашего тела, которая выполняет множество важнейших функций:
- регуляция температуры;
- защита внутренних органов от повреждений;
- предохранение организма от обезвоживания;
- барьерные функции;
- произведение гормональных соединений;
- передача различных ощущений в мозг с помощью рецепторов;
- выделение продуктов обмена веществ: мочевая кислота, соль, холестерин и др.;
- отражение состояния внутренних органов.
Сама кожа делится на три слоя: эпидермис, дерму и гиподерму. Каждый слой отличается по строению и функциям. Рассмотрим каждый из них.
Эпидермис
Самый верхний слой кожи, представляющий собой типичную пролиферативную ткань, которая способна к постоянному самообновлению. Эпидермис в свою очередь делится еще на 5 уровней: роговой, блестящий, зернистый, шиповатый, базальный.
Роговой слой
Является внешним слоем эпидермиса. В нем содержится от 15 до 30 слоев клеток, выполняющих защитные функции. Роговой слой – это конечный продукт процесса дифференцировки клеток. Прочность рогового слоя обусловлена качеством кератина и наличием межклеточного диффузионного барьера. Целостность и качество рогового слоя сильно зависит от pH. Воздействие на pH-градиент рогового слоя может привести к изменению активности ферментов, что влечет за собой нарушения во всем эпидермисе.
Блестящий слой
Идет сразу после рогового. Это очень тонкий слой безядерных клеток, которые пропитаны особым веществом – элеидином.
Зернистый слой
Состоит 3-4 слоев клеток, в которых скапливаются нити кератина (строительный материал рогового слоя). Здесь кератиноциты производят липиды и компоненты, составляющие NMF (естественный увлажняющий фактор).
Шиповидный слой
Состоит из 4-8 рядов полигональных клеток, которые соединены прочной связью протоплазматических отростков. Слой получил свое название благодаря шиповатым клеткам, которые имеют в своем составе артефакт, возникающий при гистологической обработке образцов ткани. В клетках шиповидного слоя откладываются продукты синтеза, такие как кератин и липиды. Здесь же располагаются иммунологически активные клетки Лангерганса.
Базальный слой
Состоит из коллагеновых и эластиновых волокон, а также из протоплазматических отростков эпителиальных клеток. В базальном слое расположены меланоциты, несущие в меланосомах запасы пигмента. Каждый меланоцит контактирует приблизительно с 30 кератиноцитами через разветвлённые дендриты и поставляет им пигмент. Таким способом меланоциты защищают кожу от негативного воздействия УФ-излучения. Базальной слой контактирует с дермой и, следовательно, с зоной дермо-эпидермального соединения.
Дерма и гиподерма
Глубже эпидермиса находится дерма, имеющая толщину от 1.5 до 5 мм. Она состоит из двух слоев: сосочкового и сетчатого. Дерма пронизана кровеносными и лимфатическими сосудами, железами.
Сосочковый слой
Представляет собой рыхлую волокнистую соединительную ткань, которая состоит из коллагеновых, эластических и ретикулярных волокон, а также из клеток: фибробластов, тучных клеток, макрофагов и других. Сосочковый слой получил свое название благодаря большому количеству сосочков, вдающихся в эпителий. Размер и количество сосочков по всему тело неодинаково. В дерме лица сосочки совсем плохо развиты и с возрастом имеют тенденцию исчезать.
Также в этом слое находятся гладкие мышечные клетки, которые собираются в пучки, связанные с корнем волоса. Здесь же происходит процесс появления «гусиной кожи», когда сокращаются мышечные клетки. При этом снижается теплоотдача организма, так как мелкие кровеносные сосуды сжимаются, тем самым уменьшая приток крови к коже.
Сетчатый слой
Состоит из плотной соединительной ткани с пучками коллагеновых волокон и сетью эластических волокон. Коллагеновые волокна проходят в двух направлениях: параллельно и косо к поверхности кожи. В сетчатом слое дермы на участках кожи, подверженных сильному растяжению, располагается узкопетлистая коллагеновая сеть. В зонах, где кожа испытывает особое давление, коллагеновая сеть является широкопетлистой. Сеть эластических волокон повторяет расположение коллагеновых пучков. В сетчатом слое фибробласты являются основными клеточными элементами. Кроме этого, в сетчатом слое располагаются кожные железы: потовые и сальные, а также корни волос.
Гиподерма или подкожная жировая клетчатка образуется из соединительнотканных фиброзных тяжей, которые образуют ячейки, наполняющиеся жировой тканью. Жировая ткань состоит из адипоцитов (жировых клеток). В фиброзных тяжах располагаются лимфатические сосуды, нервы, малые артерии, венулы и артериолы. Гиподерма в некоторых областях тела человека отсутствует, например, ее нет в области век, в мошонке и на половом члене. Слой подкожной жировой клетчатки обуславливает подвижность и тургор кожи, принимает участие в жировом обмене организма, является жировым депо и амортизатором внешних механических воздействий. Важно понимать, что ПЖК является сложным органом с важными метаболическими и эндокринными функциями в организме человека.
Читайте также:


