Какие витамины пить при опоясывающем герпесе
Обновлено: 04.05.2024
Для цитирования: Масюкова С.А., Владимирова Е.В. Фамцикловир в лечении герпетических инфекций. РМЖ. 2001;11:444.
Центральный научно-исследовательский кожно-венерологический институт МЗ РФ, Москва
Учитывая, что у 20–30% больных герпесом в течение первых двух–трех лет развивается рецидив заболевания, общее число таких больных постоянно увеличивается. Причиной возникновения генитального герпеса является так называемый вирус простого герпеса (ВПГ). Различают два основных антигенных типа вируса – ВПГ–1 и ВПГ–2, которые отличаются по иммуногенности, вирулентости, устойчивости к воздействию различных факторов, что в конечном итоге определяет особенности клинических проявлений заболевания. Ранее считалось, что ВПГ–1 вызывает только поражение кожи лица, верхних конечностей и туловища, а также слизистых оболочек полости рта. За последние годы установлена его этиологическая роль при генитальном герпесе, что может отражать распространеннность орогенитального секса. Согласно данным сероэпидемиологических исследований, инфицирование ВПГ–1 обнаруживается у 20–40% , а ВПГ–2 – у 50–70% больных генитальным герпесом. Рост заболеваемости также в значительной мере связан с распространением бессимптомной и недиагностированной форм болезни: только 20% инфицированных ВПГ имеют диагностированный симптоматический генитальный герпес, 60% – нераспознанный симптоматический герпес (атипичную форму) и 20% бессимптомный герпес. В настоящее время только 27% пациентов с установленным диагнозом генитального герпеса получают противовирусное лечение. Кроме риска передачи вируса сексуальному половому партнеру, бессимптомное выделение вируса у женщин является причиной неонатальной инфекции и 50% всей инфекции новорожденных Герпетическая инфекция также может быть причиной нарушения репродуктивной функции, невынашивания беременности, преждевременных родов и патологии плода. Возможно участие ВПГ в развитии, онкологических заболеваний гениталий, иммунодефицитных состояний, что позволяет считать герпесвирусные инфекции важной медико–социальной проблемой практического здравоохранения.
Вторым по значению из семейства герпесвирусов является варицелла–зостер вирус (ВЗВ). Он вызывает 2 различных по клинической картине заболевания – ветряную оспу и опоясывающий лишай (Herpes zoster). Развитие опоясывающего лишая является результатом реактивации латентного вируса, находящегося в организме после перенесенной в детстве ветряной оспы. По данным зарубежной литературы [3] , каждый второй человек, который достиг возраста 85 лет, однажды заболевает Herpes zoster, а в 4% случаев заболевание встречается более одного раза. Важной проблемой при опоясывающем лишае является болевой синдром, примерно у половины пациентов старше 60 лет развивается постгерпетическая невралгия. При этом частота ее развития увеличивается с возрастом. 67% врачей в Великобритании считают ее наиболее трудным аспектом лечения герпеса. Даже после разрешения высыпаний боль может оставаться от нескольких месяцев до года. Кроме того, Herpes zoster у иммунно ослабленных больных может осложниться гематогенной диссеминацией, возникновением поражений со стороны ЦНС, а также висцеропатий.
За последние годы были достигнуты значительные успехи в лечении герпеса благодаря внедрению в клиническую практику синтетических нуклеозидов, среди которых перспективным является фамцикловир (Фамвир).
Фамцикловир является предшественником пенцикловира и обладает рядом существенных преимуществ по сравнению с ацикловиром:
• высокое сродство к тимидинкиназе вируса (в 100 раз выше) и более выраженное блокирование репликации вируса между приемами препарата;
• фамцикловир обладает самой высокой биодоступностью (77% против 10–20% у ацикловира) и самым длительным периодом нахождения в инфицированной вирусом клетке (до 20 часов);
• постоянная концентрация препарата в инфицированных клетках обеспечивает длительный противовирусный эффект и дает возможность реже принимать препарат;
• фамцикловир обладает свойством проникать в шванновские клетки, окружающие нервные волокна. В клетках, инфицированных ВЗВ, периоды полувыведения составляют 9 часов для фосфорилированного пенцикловира и 0,8 часа для фосфорилированного ацикловира [6,7,8]. Поэтому фамцикловир является единственным противовирусным препаратом, уменьшающий длительность постгерпетической невралгии при опоясывающем лишае (на 100 дней по сравнению с плацебо) (рис. 1).
Рис. 1. Длительность постгерпетической невралгии при опоясывающем лишае.
Для врачей–клиницистов важное практическое значение имеет высокая клиническая эффективность Фамвира при генитальном герпесе:
• фамвир уменьшает количество рецидивов на 80% (рис. 2) [11];
• обусловливает отсутствие рецидивов почти у одной трети пациентов;
• предупреждает распространение вируса (у 73% пациентов, получавших фамвир, культуральный анализ на вирус оказался отрицательным по сравнению с 46% пациентов, получавших плацебо) (рис. 3) [12];
• уменьшает сроки распространения вируса до 1,8 дня по сравнению с 3,4 днями в группе плацебо (Р<0,001);
• 30% штаммов вирусов, резистентных к ацикловиру, чувствительны к терапии фамвиром.
Рис. 2. Фамвир уменьшает количество рецидивов на 80%.
Рис. 3. Фамвир способен останавливать распространение вируса.
Стратегия лечения больных генитальным герпесом определяется рядом факторов: частотой рецидивов и тяжестью клинических проявлений заболевания, а также наличием психосоциальных проблем и риска передачи инфекции половому партнеру или новорожденному.
В настоящее время существует два подхода к лечению: эпизодическая или профилактическая (супрессивная) терапия. Целями лечения являются купирование острых симптомов заболевания, уменьшение частоты и тяжести рецидива, предупреждение реактивации вируса и улучшение качества жизни пациента. Эпизодическая терапия проводится только в период обострения заболевания и значительно уменьшает боль, дискомфорт в зоне поражения, сокращает время заживления герпетических высыпаний, а также сокращает период вирусовыделения до 1,8 дня по сравнению с 3,4 днями в группе плацебо.
В США Центром по контролю и профилактике заболеваний (CDC) Фамцикловир одобрен как средство эпизодического лечения рецидивов генитального герпеса в дозе 125 мг два раза в день в течение 5 дней, при первом эпизоде генитального герпеса фамвир рекомендован по 250 мг 3 раза в день в течение 5–10 дней [5,9,10].
По результатам многоцентрового исследования, проведенном Merz с сотр. (1997), включавшем 375 женщин, имевших в анамнезе не менее 6 рецидивов генитального герпеса, прием фамцикловира в дозе 250 мг два раза в день в течение 4 месяцев оказался наиболее эффективным: предотвращение рецидивов наблюдалось у 90 % пациенток данной группы в сравнении с другими режимами дозирования и приема препарата, а также с группой плацебо [9,10].
В другом исследовании, проведенном Diaz–Mitoma с сотр. (1998), подавляющую (супрессивную) терапию фамцикловиром осуществляли в течение 1 года введением 125 мг препарата 3 раза в день, 250 мг 2 раза в день, 250 мг 3 раза в день или плацебо. Все три дозы фамцикловира значительно отдаляли появление клинически подтверждаемого рецидива. В группе, получавшей 250 мг 2 раза в день, медиана интервала времени до появления первого рецидива составила 336 дней в сравнении с группой плацебо, в которой аналогичный показатель был равен 47 дням. У 72% больных, получавших терапию фамцикловиром, рецидивы генитального герпеса в течение 1 года после начала лечения не наблюдались. В группе без лечения (плацебо) таких больных было всего 22%. Таким образом было показано, что фамцикловир эффективен в качестве средства профилактической терапии рецидивов генитального герпеса в дозе 250 мг 2 раза в день [9,10].
Клинические испытания по изучению эффективности фамцикловира при опоясывающем лишае показали , что фамцикловир по 250 мг 3 раза в сутки в течение 7 дней обладает такой же эффективностью при заживлении кожных высыпаний, как и ацикловир по 800 мг 5 раз в сутки в течение того же промежутка времени, однако. у больных с наиболее высоким риском длительного сохранения боли – это пациенты старше 50 лет – боль острой фазы исчезала в 1,5 раза быстрее , чем при применении ацикловира.
Назначение фамцикловира дает возможность уменьшения суточной и курсовой доз препарата в 5 раз, по сравнению с ацикловиром: курсовая доза у фамцикловира – 5,25 г, у ацикловира – 28,0 г. Данное обстоятельство особенно актуально при лечении пожилых пациентов. Необходимо отметить, что лечение наиболее эффективно при назначении фамвира в первые 48 ч с момента появления высыпаний [3,8].
В ГУ ЦНИКВИ МЗ РФ также было проведено клинико–лабораторное изучение эффективности фамцикловира при генитальном герпесе [2]. Монотерапия рецидивов была проведена у 110 больных (62 мужчин и 48 женщин) в возрасте от 18 до 50 лет. Давность заболевания варьировала от нескольких месяцев до 10 лет, длительность рецидивов составила от 5 до 21дней. 79 больных (71,8%) имели тяжелое течение генитального герпеса (рецидивы 1–2 раза в месяц и ремиссии менее 6 недель), 28 пациентов (25,5%) – заболевание средней тяжести (обострения 1 раз в 2–3 месяца и ремиссии 2–3 месяца), легкое течение заболевания (1–3 рецидива в год, ремиссии не менее 4 месяцев) наблюдалось только у 3 пациентов (2,7%).
Результаты исследования подтвердили высокую эффективность фамвира в лечении генитального герпеса. Монотерапия рецидивов ГГ фамцикловиром в курсовой дозе 2,5 г сокращала длительность рецидивов герпеса более, чем в 2 раза – с 8,7 до 3,8 дней (Р<0,05), при приеме фамцикловира в курсовой дозе 1,25 г длительности рецидива также уменьшалась, но в меьшей степени – с 8,6 до 5,0 дней.
Переносимость фамцикловира была хорошей, побочные реакции в виде головной боли отмечали 5 из 110 пациентов (4,5%), у 2 больных развилась диарея (1,8%). Других реакций, в том числе аллергических, отмечено не было. Данные явления не были поводом для прекращения приема препарата или коррекции дозы.
Сравнительная оценка клинической эффективности фамцикловира показала достоверное (Р<0,05) снижение продолжительности обострения при курсовой дозе 2,5 г, по сравнению с 1,25 г.
1.Фамцикловир является высокоэффективным препаратом для лечения и профилактики рецидивов генитального герпеса и опоясывающего лишая.
2. Фамцикловир обладает анальгезирующим действием, особенно выраженном при опоясывающем лишае.
3. Фамцикловир является единственным противовирусным препаратом, уменьшающим длительность постгерпетической невралгии при опоясывающем лишае.
4. Супрессивная терапия фамвиром в течение 1 года уменьшает количество рецидивов генитального герпеса на 80% и отсутствие рецидивов почти у трети пациентов.
5. При генитальном герпесе фамвир предупреждает распространение вируса и уменьшает сроки распространения вируса.
6. 30% штаммов вирусов, резистентных к ацикловиру, чувствительны к терапии фамвиром.
1. Яцуха М.В., Губанова Е.И., Масюкова С.А. Динамика заболеваемости генитальным герпесом и деятельность ЛПУ в Москве и Московской области. Актуальные проблемы дерматологии и венерологии.Сб.научных работ.Москва, 2000, с.94–95
2. Владимирова Е.В. Эффективность фамцикловира в лечении рецидивирующего генитального герпеса (клинико–лабораторное исследование).Дисс. канд.мед.наук., Москва, 1998, 110 с.
3. Gross G. Herpes – simplex – Virus und Varicella – Zoster – Virus – Infektionen // “Dermatologie, heutiger Stand”, Stuttgart – New – York, Georg Thieme Verlag, – 1995, s.43 – 50.
4. Elion G.B. Acyclovir discovery, mechanism of action and selectivity // J. Med.Virol. – 1993 – , – Suppl.1, – p.2 – 6.
5. Centers for Disease Control and Prevention. 1998.CDC 1998. Guidelines for treatment of Sexually Transmitted Diseases. Morb.Mortal.Wkly.Rep.47,1–118.
6. Earnshaw D.L., Bacon T.H., Darlison S.J. et al. Penciclovir mode of action studies in HSV – I. HSV – 2 and VZV infected MRC – 5 cells, providing a rationale for its persistent antiviral activity.// Antimicrob Agents Chemother, 1992, 36: p.2747 – 57.
7. Pue M.A., Benet L2.Pharmacokinetiks of famciclovir in man // Antiviral Chem Chemother, – 1993, – (Suppl. 1) – p.47 – 55.
8. Degreef H, Famciclovir Herpes Zoster Clinical Study Group. Famciclovir, a new oral antiherpes drug: results of the first controlled clinical study demonstrating its efficacy and safety in the treatment of uncomplicated herpes zoster in immunocompetent patients // Int.J. Antimicrob Agents, – 1994, – 4: p.241 – 6.
9. Stanberry L. et al. Antiviral Research 42(1999), 1–14
10. Leung D.T, Sacks S.L. Current Recomendations for the treatment of genital herpes//Drags, 2000, Dec;60 (6): 1329–1352
11. Diaz–Mitoma F et al. Oral famciclovir for the supression of recurrent genital herpes: a randomized controlled trial. JAMA. 1998; 280: 887–892
12. Saks SL et al. Patient–initiated, twice–daily oral famciclovir for early recurrent genital herpes: a randomized double–blind multicenter trial. JAMA. 1996; 276: 44–49.
Фамвир (торговое название)
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Опоясывающий герпес или, как его еще называют, опоясывающий лишай, – одно из самых непонятных для обычного человека заболеваний вирусной природы. Его часто путают с другими видами лишая (розовый, стригущий, чешуйчатый), к которым приводят грибковые инфекции кожи, а также различные аутоиммунные процессы.
В случае опоясывающего лишая к появлению клинических симптомов и высыпаниям на коже приводит вирус герпеса 3 типа, Varicella zoster. Этот вирус также вызывает хорошо известную ветряную оспу. Выходит, что один и тот же вирус вызывает сразу два заболевания? Но как такое может быть? Давайте разбираться!
Когда организм человека встречается с вирусом Varicella zoster впервые, чаще всего развивается ветряная оспа. И обычно это происходит в детском возрасте, хотя в редких случаях заболевание может развиться и у взрослого человека. О том, что происходит, когда вирус дает о себе знать во второй раз, читайте далее. Также узнаете о том, как подобрать лекарство от опоясывающего герпеса.
Всем известно, что вирусы герпеса никогда не покидают организм, и Varicella zoster здесь не исключение. Проникая в скопления нервных клеток, он «впадает в спячку» и часто остается с нами навсегда, никак себя не проявляя. Однако, под воздействием внешних факторов вирус все-таки может «проснуться», вызывая при этом опоясывающий лишай. Также к развитию опоясывающего герпеса может привести контакт с больным ветряной оспой. Это происходит, когда человек, чаще пожилой, у которого снижены показатели иммунитета, контактирует с больным ребенком. Даже самое название вируса представляет интерес: «варицеллой» чаще называют именно ветряную оспу, а «зостер», что в переводе означает «ремень», ассоциируется с лишаем, так как характерная для этого заболевания сыпь появляется именно в области нижней части спины и живота.
Итак, мы выяснили, что опоясывающий герпес (опоясывающий лишай, герпес зостер, herpes zoster, ОГ) является вирусным заболеванием кожи и нервных тканей, которое возникает как результат реактивации вируса герпеса III типа (Human herpesvirus) подсемейства Alphaherpesviridae, семейства Herpesviridae. Встречается он примерно у 15 человек из 100 и проявляется у каждого четвертого взрослого из тех, кто ранее переболел ветряной оспой.
Важно помнить, что опоясывающий герпес у взрослых требует иного подхода к терапии: лекарства, которые педиатр рекомендует детям от ветряной оспы, не помогут. Терапию для лечения опоясывающего герпеса должен назначать врач-терапевт или врач-дерматолог после осмотра пациента и с учетом его анамнеза.
Как вирус герпеса зостер проникает в организм и как проявляется
Чаще всего первичное инфицирование вирусом, вызывающим ОГ, происходит в детском возрасте, когда ребенок заражается ветрянкой воздушно-капельным путем. После выздоровления вирус длительное время продолжает персистировать в области периферических нервных сплетений, спинальных ганглий (ограниченных скоплений нейронов) и ганглий мозга. К реактивации вируса могут привести иммунодефицитные состояния, когда естественная защита ослабевает и заболевание получает возможность «развернуться» в полную мощь.
Главные факторы, которые могут спровоцировать появление ОГ:
- возрастные изменения в организме – согласно данным статистики, это заболевание чаще всего встречается среди людей старше 50 лет;
- аутоиммунные и онкологические заболевания, в том числе сахарный диабет, лучевая и химиотерапия, состояние после тяжелых травм;
- беременность и вследствие этого повышенная нагрузка на организм;
- ВИЧ-инфекция – с ОГ сталкиваются почти 25% ВИЧ-инфицированных лиц, что в восемь раз превышает средний показатель заболеваемости пациентов среднего и старшего возраста;
- трансплантация органов, когда необходим прием иммуносупрессивных препаратов, предназначенных для искусственного угнетения иммунитета в целях предупреждения отторжения органа; i
- рецидив хронических заболеваний, затрагивающих сердечно-сосудистую систему, почки, печень и легкие;
- длительное лечение антибиотиками, цитостатиками, глюкокортикостероидами;
- частые стрессы, отсутствие достаточного отдыха, переутомление, переохлаждение или перегрев.
Опоясывающий герпес: симптомы и лечение
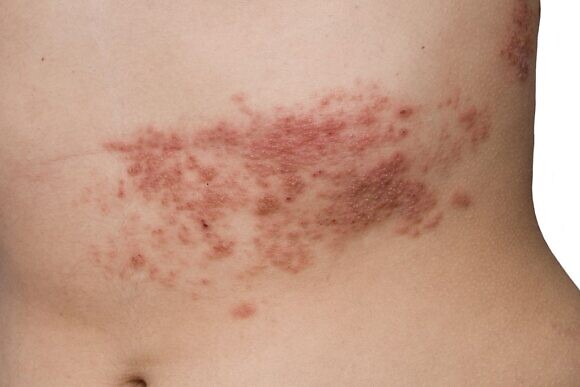
В отличие от ветряной оспы, при опоясывающем лишае не наблюдается резких вспышек заболеваемости, как в детских коллективах, также отсутствует и сезонная зависимость. Хотя некоторые ученые отмечают, что ОГ чаще встречается в теплое время года и поздней осенью. Тяжесть течения заболевания зависит от возраста. Дети, которые тоже болеют опоясывающим лишаем после перенесенной ветрянки, а также лица молодого возраста обычно переносят болезнь более благоприятно, чем пожилые люди.
Среди основных симптомов опоясывающего герпеса – кожные проявления и неврологические расстройства. Большинство инфицированных сталкивается с общеинфекционными клиническими признаками, которые проявляются в виде повышения температуры тела, головной и мышечной боли, тошноты, слабости, увеличения регионарных лимфатических узлов. Интенсивность проявления этих симптомов варьируется у каждого пациента. Продолжительность начального периода составляет примерно четыре-пять дней.
Клинические признаки ОГ могут быть похожими на плеврит, невралгию тройничного нерва и даже синдром острого живота, например, аппендицит, который требует немедленной помощи специалиста. Поэтому при общем плохом самочувствии и появлении на коже высыпаний любой природы необходимо сразу же обратиться к врачу.
В месте высыпаний перед появлением сыпи могут ощущаться легкие зуд и жжение. Потом на коже появляются розовые пятна круглой или неправильной формы, которые не склонны к слиянию, они отечные и немного приподнятые над поверхностью кожи. Затем на коже появляются везикулы с жидким серозным содержимым. Через несколько дней пузырьки подсыхают, на их месте появляются серозные корки, которые со временем отпадают и на их месте появляются пигментированные участки кожи. При правильном лечении снижается температура тела и исчезают симптомы общей интоксикации организма.
Как лечить опоясывающий герпес геморрагической, гангренозной абортивной и других форм
Кроме наиболее часто встречаемой формы опоясывающего лишая, о которой идет речь выше, также встречаются другие, которые могут выглядеть не совсем обычно и даже пугающе для неподготовленного человека. Например, при геморрагической форме везикулы заполняются кровянистым содержимым, поэтому на теле сыпь выглядит как пятна темно-коричневого цвета. Иногда везикулы не заживают бесследно, по разным причинам их дно некротизируется, после чего на коже остаются рубцы. Абортивная форма ОГ характеризуется появлением практически незаметных визуально папул (пузырьки не образуются), поэтому пациент не обращается к врачу.
При буллезной форме пузырьки на коже достаточно крупные, они могут сливаться в единый конгломерат с неровными краями. Их повреждение может приводить к инфицированию ранки, после чего может начаться гнойный процесс. В самых тяжелых случаях везикулы сливаются в обширные области, которые со временем некротизируются. В этом случае речь идет уже о гангренозной форме. Чаще эта форма развивается у пожилых людей, у лиц с язвенной болезнью и сахарным диабетом. В данном случае пациенту может быть необходима госпитализация и комплексное лечение.
Одна из главных целей лечения опоясывающего герпеса у взрослых, которые не требуют лечения в стационаре, – максимально быстрое купирование клинических симптомов заболевания (высыпаний и субъективных ощущений). Это обусловлено тем, что в зависимости от длительности цитопатического (приводящего к дегенеративным изменениям в клеточных структурах) действия вируса варицелла-зостер на клетки пораженных нервов значительно возрастает риск развития постгерпетической невралгии и других осложнений.
Возможные последствия отказа от лечения опоясывающего герпеса
ОГ приводит к многочисленным поражениям периферического и центрального отделов нервной системы. Чаще всего встречается такое осложнение, как постгерпетическая невралгия. Она проявляется в виде сильных болей, которые сохраняются или появляются через несколько недель и даже месяцев после появления первых высыпаний. Человек ощущает жгучие, резкие и приступообразные боли в области расположения сыпи. Этот симптом особенно усиливается по ночам. Особенно часто с таким осложнением болезни сталкиваются пожилые люди. Также встречаются случаи, когда вирус опоясывающего герпеса поражает брюшные мышцы и мочевой пузырь.
Кроме того, ОГ может поразить нервы, которые находятся в черепе. Подобное поражение может затронуть мозговые оболочки, что приводит к массе проблем со здоровьем. Одна из них – это поражение офтальмической ветви тройничного нерва, что неблагоприятно влияет на зрение.
Исследователи утверждают, что персистирующая, т.е. упорно протекающая и периодически вспыхивающая герпетическая инфекция может привести иммунную защиту организма к так называемой клеточной депрессии. Без поддержки в виде правильного лечения и возможности полноценно защитить себя организм может столкнуться с самыми разными осложнениями со стороны функционирования различных органов и систем.
Диагностика и правильное лечение опоясывающего герпеса у взрослых
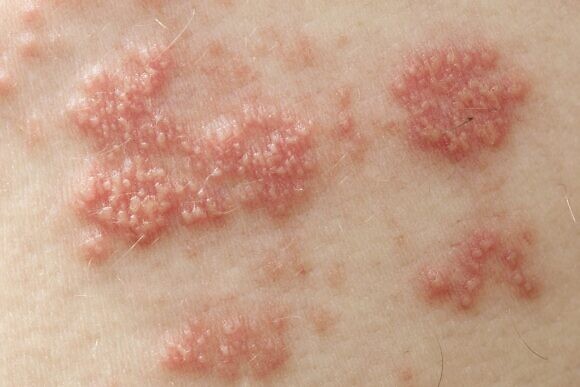
При подозрении на опоясывающий герпес необходимо обращаться к врачу-терапевту для осмотра и начала курса лечения. Также может понадобиться помочь врача-дерматолога и врача-иммунолога, а при выраженном болевом синдроме – врача-невролога.
Диагностика ОГ является преимущественно клинической, для подтверждения диагноза может потребоваться проведение лабораторных исследований. Также необходимо дифференцировать это заболевание от других похожих. Для этой цели широко применяется метод полимеразной цепной реакции (ПЦР), иммуноферментный анализ (ИФА) и иммунофлуоресцентный анализ, которые обычно не оставляют сомнений в диагнозе. Кроме того, могут потребоваться результаты общего и биохимического анализа крови, общего анализа мочи. При развитии генерализованной формы врач может дополнительно назначить анализ на ВИЧ.
Лечение ОГ чаще всего проводят амбулаторно, оно должно быть комплексным и включать как этиологические, так и патогенетические средства. Эффективность терапии во многом зависит от сроков начала лечения: чем раньше вы обратитесь к врачу и начнете лечение, тем быстрее наступит выздоровление и тем ниже будут риски развития осложнений.
Опоясывающий герпес: лечение народными средствами
Не стоит слепо доверять советам родственников и знакомых, не имеющих медицинского образования. Любые настойки, ванночки, растирания и аппликации на кожу могут принести вред, усилить зуд и расширить область появления высыпаний. Ведь во многих случаях народная медицина может не только не помочь избавиться от заболевания, но и быть небезопасной.
Опасность кроется и в том, что во время экспериментов с самолечением заболевание прогрессирует, у человека ухудшается самочувствие и могут развиться осложнения, что усложняет процесс лечения тогда, когда все же появляется решимость обратиться к врачу. Помните, что аргумент «даже если не поможет, то не навредит» в этом случае не работает. При подозрениях на опоясывающий лишай необходимо сразу же обратиться к врачу и начать лечение проверенными лекарственными препаратами.
Опоясывающий герпес: лечение, препараты и методы терапии
В настоящее время все методы лекарственного лечения и профилактики ОГ можно объединить в три основные группы, куда входят химиотерапия (прием ациклических нуклеозидов), иммунотерапия и комбинация этих двух групп, где пациент одновременно принимает химио- и иммуномодулирующие препараты.
Также применяют витамины B1, В6 и В12, аскорбиновую кислоту, рутин и при необходимости – антигистаминные препараты. При сильном болевом симптоме пациенту показан прием НПВП и анальгетиков.
Многие врачи придерживаются мнения, что приема только ациклических нуклеозидов в качестве основного лечения недостаточно, подобная монотерапия себя не оправдала. i Эти препараты наиболее эффективны только в первые 72 часа от начала развития болезни, они способны подавлять только вирусы герпеса в стадии активной репликации – процессе создания двух дочерних молекул ДНК на основе родительской молекулы ДНК. Они не оказывают влияния на те вирусы, которые уже существуют и находятся в латентном, т.е. «спящем» состоянии. Кроме того, ациклические нуклеозиды не помогают восстанавливать иммунитет.
Для лечения опоясывающего герпеса на теле пациентам необходима иммунокоррекция. Поэтому в этом случае будет уместной стратегия сочетания ациклических нуклеозидов и препаратов интерферона альфа-2b, которая признана врачами обоснованной и наиболее эффективной, что отражено в клинических и методических рекомендациях.
Интерфероны – «универсальные» бойцы, которые в отличие от антител не ориентированы на определенные патогены, а представляют неспецифический (врожденный) иммунитет и
способны бороться с любыми вирусными частицами. Интерфероны способны останавливать размножение и распространение вирусных частиц или бактерий.
Противовирусный препарат ВИФЕРОН в лечении опоясывающего герпеса
Одним из препаратов, применяемых для лечения герпеса, является ВИФЕРОН – противовирусный и иммуномодулирующий препарат, который обладает рядом уникальных фармакологических свойств.
ВИФЕРОН в своем составе сочетает рекомбинантный интерферон а-2b и комплекс антиоксидантов (витамины Е и С), в присутствии которых возрастает специфическая противовирусная активность главного действующего вещества, а также усиливается его иммуномодулирующее действие, что позволяет повысить эффективность собственного иммунного ответа организма на патогенные микроорганизмы. ii
Препарат представлен в виде ректальных суппозиториев (свечи), которые обеспечивают системное действие, то есть на весь организм в целом, а также в виде мази и геля, которые способны бороться с вирусами в «воротах» инфекции: в данном случае на поверхности кожи. Наличие как местных, так и системных форм позволяет применять препараты линейки ВИФЕРОН одновременно, усиливая тем самым эффекты проводимой терапии.
Препарат в форме свечей удобен в применении и для взрослых: он не перегружает желудочно-кишечный тракт (ЖКТ), что особенно актуально для людей, страдающих гастритом и другими заболеваниями ЖКТ, а также для тех, кто принимает большое количество таблетированных препаратов (пожилые пациенты и лица с сопутствующими заболеваниями).
Для лечения герпесвирусных инфекций у взрослых применяются свечи в дозировке 1 000 000 МЕ, у беременных женщин – 500 000 МЕ с последующими поддерживающими курсами с использованием дозировки 150 000 МЕ.

ВИФЕРОН Гель в виде полоски не более 0,5 см наносят на предварительно подсушенную пораженную поверхность 3-5 раз в день в течение 5-6 дней.
Сочетание ациклических нуклеозидов с препаратом ВИФЕРОН гарантированно сокращает сроки купирования ОГ и позволяет значительно снизить риск развития осложнений за счет комбинированного противовирусного действия (нарушение размножения вируса варицелла-зостер и препятствие прямому токсическому воздействию). iii
Как применять мазь при опоясывающем герпесе
Любая противогерпетическая мазь при опоясывающем герпесе может применяться в качестве дополнения к системной терапии, но не вместо нее.
Национальное научное общество инфекционистов и Московский научно-практический центр дерматовенерологии и косметологии рекомендуют включать препарат ВИФЕРОН в комплексную терапию опоясывающего герпеса у детей и взрослых, включая беременных женщин. iv
Справочно-информационный материал
Автор статьи
Врач общей практики
iii Халдин А.А., Васильев А.Н., Д.В. Баскаков Д.В. Виферон: опыт применения в дерматологической практике // Ремедиум Приволжье. – январь-февраль 2009. – С.20-22.
iv Потекаев Н.Н., Халдин А.А., Жукова О.В., Дмитриев Г.А. Методические рекомендации. Простой герпес. Опоясывающий герпес. Цитомегаловирусная инфекция. Московский научно-практический центр дерматовенерологии и косметологии ДЗМ. – 2019. – 32 с.
По данным ВОЗ около 90% населения земного шара инфицированы одним или несколькими видами герпеса. В большинстве случаев первичное инфицирование происходит еще в детстве, после чего вирус переходит в латентное состояние. Он не размножается, его белки не синтезируются в клетках. Чаще всего реактивация вируса происходит на фоне других инфекций, неблагоприятных факторов внешней среды, психоэмоциональных перегрузок, эндокринных нарушений или изменений, а также иммунодефицитных состояний. Одна из самых распространенных детских инфекций – ветряная оспа – вызывается вирусом Varicella zoster (VZV), который относится к 3-му типу вирусов герпесгруппы и вызывает два заболевания: ветряную оспу и опоясывающий герпес (лишай). Причем как правило, при первичном заражении – развивается ветрянка, а впоследствии, – лишай.
Что такое опоясывающий лишай, чем он вызван и при чем здесь детская ветрянка
Это разновидность герпетической инфекции, поражающей нервную систему и имеющей кожные проявления. Вызвано заболевание тем же типом вируса, что и ветряная оспа. Принято считать ветрянку не слишком серьезным детским заболеванием, однако она не проходит бесследно. После перенесенной инфекции в ганглиях задних корешков спинного мозга формируется пожизненное носительство вируса в «дремлющем» состоянии, которое не требует лечения. В момент ослабления иммунитета, вызванного различными факторами, о которых говорилось выше, происходит реактивация вируса. Интересно, что опоясывающий герпес назван именно «опоясывающим», потому что клинически проявляется в виде сыпи, которая располагается вдоль нервных стволов и визуально, особенно при запущенных случаях, напоминает «пояс». Также важно понимать, что только опоясывающий лишай вызывается вирусом VZV. Другие лишаи могут иметь совершенно иное происхождение, от того и подход к их лечению может сильно отличаться.
Симптомы опоясывающего лишая
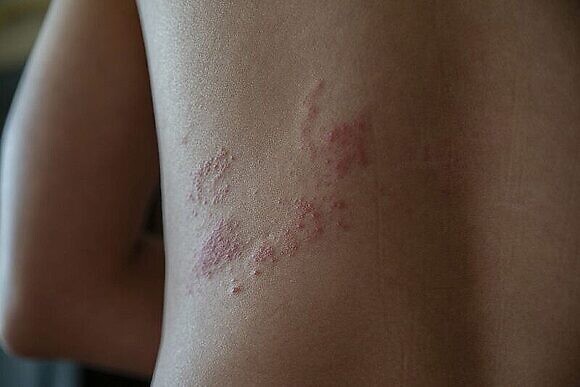
Помимо таких симптомов как увеличение лимфатических узлов, слабость, головная боль, тошнота, озноб и повышенная температура во время опоясывающего лишая на коже появляются участки, покрытые сыпью. Высыпания представлены мелкими сгруппированными пузырьками с прозрачной жидкостью внутри. Чаще они располагаются вдоль ребер, по ходу нервных стволов, как бы опоясывая тело. Однако высыпания при опоясывающем лишае могут появляться и на голове, животе, конечностях, ягодицах. Кожа на поражённых участках отекает, краснеет и нестерпимо зудит. Характерны интенсивные кожно-мышечные боли, обусловленные повреждением нервных волокон.
Кто может заболеть
Случаи заражения взрослых от больных опоясывающим лишаем чрезвычайно редки. При этом у детей, контактирующих с больными опоясывающим герпесом, может развиться ветряная оспа. Взрослые, общающиеся с ребенком, страдающим ветряной оспой, заболевают опоясывающим лишаем крайне редко. Заболевание чаще всего появляется один раз в жизни, эпидемий не наблюдается. Важным фактором риска развития опоясывающего герпеса является возраст. Заболеваемость ОГ в различных странах мира составляет от 0,4 до 1,6 случая заболевания на 1000 человек в год у лиц в возрасте до 20 лет, и от 4,5 до 11,8 случая на 1000 человек в год в старших возрастных группах. Риск развития опоясывающего герпеса у пациентов со сниженной способностью противостоять вирусам в 20-100 раз выше, чем у людей того же возраста с нормальным иммунитетом. К иммунодепрессивным состояниям, ассоциированным с высоким риском развития опоясывающего лишая, относятся: инфекция ВИЧ, пересадка костного мозга, лейкемия и лимфомы, химиотерапия и лечение системными кортикостероидами. Опоясывающий герпес может быть ранним маркером инфицирования ВИЧ, указывающим на первые признаки развития иммунодефицита. К другим факторам, увеличивающим риск развития опоясывающего герпеса, относят: женский пол, специфические поражения участков кожи, генетические нарушения i . Число больных увеличивается зимой и осенью.
Патогенез опоясывающего лишая не вполне ясен, однако, по современным данным, опоясывающий лишай можно расценивать как вторичную инфекцию на фоне частичного снижения иммунитета, развившуюся в результате контакта организма с вирусом в прошлом. Вирус в латентном состоянии находится в нервных ганглиях и при реактивации инфекции продвигается по ходу нерва к коже, где вызывает характерные высыпания. В большинстве случаев болезнь развивается у практически здоровых людей без видимых предрасполагающих факторов. Вместе с тем инфекция может быть спровоцирована травмой, рентгеновским облучением, переохлаждением, рядом других факторов, а также иммунодефицитом. Болезнь не рецидивирует, что отличает ее от ВПГ ii .
Сведения о вирусах герпесгруппы
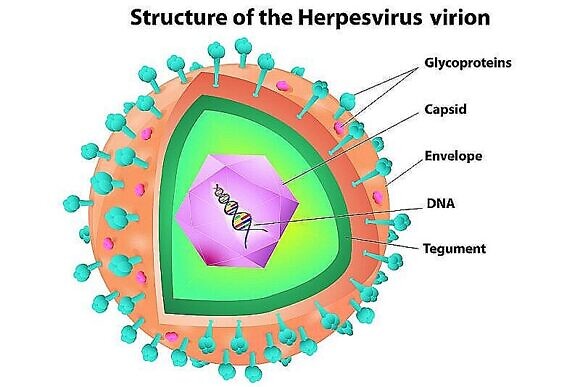
На практике врачи многих специальностей довольно часто сталкиваются с лечением заболеваний, вызванными ВПГ 1 и 2 типа (лабиальный и генитальный герпес), ВВО (ветряная оспа, опоясывающий герпес), для которых разработаны и стандартизированы методы диагностики и терапии. Однако, несмотря на наличие большого арсенала противовирусных препаратов, эффективность системной терапии рецидивирующей герпетической инфекции зачастую, увы, невысока. Для достижения длительной ремиссии в лечении важен комплексный подход: препараты, которые оказывают воздействие непосредственно на вирус плюс стимуляция антивирусного иммунитета.
Герпес 3-го типа (VZV) особенно опасен для беременных женщин, так как негативно влияет на плод. Уровня антител в крови матери бывает недостаточно для защиты плода, это связано со снижением иммунитета во время беременности, могут потребоваться препараты, обладающие иммуномодулирующим действием. Опоясывающий герпес во время беременности является маркером иммунного ответа: если случился рецидив ветрянки, необходимо срочно принимать меры по недопущению заражения плода. Степень опасности для плода зависит от срока беременности и титра защитных антител у матери. Препараты, которые можно использовать при опоясывающем герпесе во время беременности – ВИФЕРОН Гель, ВИФЕРОН Мазь.
Лекарства от опоясывающего герпеса
Лечение тем эффективнее, чем раньше оно начато. Домашнее лечение допустимо в легких случаях. Основной целью лечебных мероприятий является: подавление репродукции вируса в период обострения; формирование адекватного иммунного ответа и его длительное сохранение; предотвращение развития или восстановление тех нарушений, которые вызывает активация инфекции в организме. Разумеется, золотым стандартом лечения герпетических инфекций являются препараты на основе ацикловира или его дериватов. Это препараты прямого противовирусного действия, которые способны достаточно быстро купировать симптомы острой фазы заболевания. Однако у этих препаратов часто имеются противопоказания по возрасту, а также ограничения по использованию во время беременности. Также нужно помнить, что в последние годы растет уровень резистентности вируса опоясывающего герпеса к препаратам на основе ацикловира, что может сказаться на эффективности лечения iv . Являясь препаратами прямого противовирусного действия, ацикловиры не оказывают никакого воздействия на показатели иммунитета, а значит не предотвращают развитие рецидивов. Именно поэтому все чаще и чаще специалисты отдают предпочтение комплексной терапии, которая помимо вышеуказанных методов лечения, включает в себя препараты для поддержания иммунитета, а также витамины группы В.
Клинические рекомендации по лечению герпеса у взрослых v среди прочих содержат препараты интерферона, которые помимо противовирусного действия обладают также выраженным иммуномодулирующими свойствами. К таким препаратам относится ВИФЕРОН Суппозитории/Мазь/Гель. Местная терапия при опоясывающем лишае заключается в соблюдении рационального режима (запрещается мытье, кожу вокруг очагов протирают 2% салициловым спиртом) и применении противовирусных препаратов локального действия и симптоматических средств. Для устранения болевого синдрома используют акупунктуру, физиотерапию, УФ облучение, лазер. К рекомендуемым иногда при опоясывающем лишае кортикостероидным средствам нужно относиться с осторожностью, так как их применение может вызвать распространение процесса. При присоединении вторичной инфекции проводится лечение антибиотиками. Лечение постгерпетических невралгий проводится неврологом. Опоясывающий лишай может приводить к развитию серьёзных осложнений, поэтому даже домашнее лечение опоясывающего лишая должно проводиться согласно врачебным рекомендациям.
Направленное действие интерферона
Целесообразно проводить лечение опоясывающего лишая иммуностимуляторами, так как оно обеспечивает направленное воздействие непосредственно в очаге воспаления. Для лечения герпетической инфекции используют противовирусные средства на основе интерферонов, например, ВИФЕРОН. Терапевтическое действие препарата во многом обусловлено его комплексным составом. Противовирусное и иммуномодулирующее действия интерферона усиливаются благодаря наличию высокоактивных антиоксидантов, витаминов Е и С. Для системной терапии применяются ректальные суппозитории ВИФЕРОН в дозировке 1 000 000 ME 2 раза в сутки, 10 дней. У беременных с 14-й недели используется дозировка 500 000 ME два раза в день, курс лечения – смотрите в инструкции по медицинскому применению.

Для наружной терапии опоясывающего лишая могут быть использованы препараты ВИФЕРОН Мази или ВИФЕРОН Гель. Их наносят 3–5 раз в день 5-7 дней чистым шпателем или ватным тампоном/палочкой на предварительно подсушенную пораженную поверхность до исчезновения клинических проявлений. Врач как правило назначает комплексную схему лечения. Рекомендуется применять ВИФЕРОН при появлении первых признаков: зуд, жжение, покраснение слизистых или кожи.
О безопасности данных средств свидетельствует то, что суппозитории и гель можно использовать у детей с первых дней жизни, а мазь — с одного года. Если высыпания покрыты корками, то для их размягчения следует использовать мазь. Если их нет, то лучше использовать гель, особенно на слизистых оболочках.
Одной из нозологических форм, которую вирусы простого герпеса (ВПГ) вызывают у человека, является генитальный герпес. В настоящее время эта форма ВПГ-инфекции считается наиболее распространенной среди всех инфекций, передающихся половым путем.
Одной из нозологических форм, которую вирусы простого герпеса (ВПГ) вызывают у человека, является генитальный герпес. В настоящее время эта форма ВПГ-инфекции считается наиболее распространенной среди всех инфекций, передающихся половым путем. Генитальный герпес вызывают два серотипа вируса простого герпеса: ВПГ-1 и ВПГ-2; причем наиболее часто — ВПГ-2. Согласно данным сероэпидемиологических исследований, инфицирование ВПГ-1 выявляется у 20—40%, а ВПГ-2 — у 50—70% больных генитальным герпесом [2]. Заболевание передается преимущественно при сексуальных контактах от больного генитальным герпесом. Нередко генитальным герпесом заражаются от лиц, не имеющих симптомов заболевания на момент полового контакта или не знающих о том, что они инфицированы [5]. Эта особенность ВПГ, связанная с бессимптомным вирусоносительством, является сложной задачей, от решения которой зависит не только трудоспособность и здоровье, но и личная судьба миллионов потенциальных больных. Имеются сведения о том, что от 60 до 80% новорожденных, у которых развивается неонатальный герпес, рождаются от матерей с бессимптомным носительством [6].
ВПГ-инфекция также может быть причиной нарушения репродуктивной функции, невынашивания беременности, преждевременных родов и патологии плода. Возможно участие ВПГ в развитии онкологических заболеваний гениталий, иммунодефицитных состояний, что позволяет считать герпесвирусные инфекции важной медико-социальной проблемой практического здравоохранения [2].
Лечение хронических, часто рецидивирующих форм ВПГ-инфекции, до настоящего времени представляет определенные трудности, которые объясняются особенностями взаимодействия вируса с макроорганизмом. Жизнедеятельность вирусов герпеса основывается на следующих биологических особенностях:
- все вирусы герпеса являются внутриклеточными паразитами;
- герпесвирусы пожизненно персистируют в аксоноганглиальных структурах центральной и периферической нервной системы;
- в течение жизни человек многократно реинфицируется новыми штаммами вирусов герпеса, при этом возможно одновременное сосуществование нескольких видов и штаммов вирусов [12];
- при нарушении динамического равновесия между иммунным гомеостазом и вирусами последние переходят в активную форму [9].
Согласно данным проведенных исследований только 20% инфицированных ВПГ имеют диагностированный генитальный герпес, 60% — нераспознанный симптоматический генитальный герпес (атипичную форму) и 20% — бессимптомный герпес. В настоящее время только 27% пациентов с диагнозом генитальный герпес получают противовирусную терапию, из них треть — местное лечение [2]. По данным некоторых авторов, около 95% пациентов с клиническими проявлениями генитального герпеса вообще никак не лечатся [11].
Все разнообразие методов терапии и профилактики герпесвирусных инфекций в конечном счете сводится к трем главным подходам:
- химиотерапия;
- иммунотерапия;
- комбинация этих двух методов.
Каждый врач в своей практической работе так или иначе сталкивается с необходимостью решения этой сложной задачи, требующей тонкого индивидуального подхода к каждому пациенту, страдающему ВПГ.
Теоретически идеальным вариантом химиотерапии был и остается механизм прямой инактивации вирусной ДНК, но из-за неизбежного общего токсического, цитопатического и канцерогенного эффекта этот способ для клинического использования оказался неприемлемым [8]. Поэтому был разработан менее опасный способ инактивации вирусной ДНК — подавление активности вирусных ферментов, обеспечивающих жизнедеятельность ДНК. Наиболее безопасным вариантом оказалось создание синтетических аналогов нуклеозидов герпесвирусной ДНК, которые избирательно фосфорилируются не клеткой, а вирусспецифическим ферментом — тимидинкиназой. В процессе копирования вирусной ДНК эти псевдонуклеазиды встраиваются в дочерние вирусные ДНК, что приводит к генетическому дефекту или нежизнеспособности вирусной ДНК [1]. Первый лечебный синтетический нуклеозид — ацикловир (ациклический аналог гуанозина) — стал «золотым стандартом» противогерпетической химиотерапии. Ацикловир, будучи включен в какой-либо участок новой ДНК, никогда не заменяется естественным гуанином [13]. В последнее время синтезированы и широко используются новые противовирусные препараты этой группы — валтрекс и фамвир.
Различают два способа применения противовирусных химиопрепаратов: эпизодическое назначение (при обострениях герпесвирусной инфекции по мере необходимости) и супрессивная или превентивная терапия. В первом случае препарат назначается коротким курсом (5—10 дней), во втором — ежедневный прием препарата в течение нескольких месяцев, а то и лет призван помочь не столько купировать рецидив, сколько предотвратить развитие рецидивов как таковых.
Однако за последние 10 лет увеличилось число исследований, в ходе которых было показано, что изоляты вируса простого герпеса, полученные от пациенток с продолжающимися рецидивами генитального герпеса на фоне длительной супрессивной терапии (более 4 месяцев), обладают резистентностью по отношению к ацикловиру [10].
К тому же ни ацикловир, ни другие противовирусные агенты — фамцикловир, валацикловир — не предотвращают перехода вируса в латентное состояние, возникновения рецидивов после их отмены либо передачи инфекции, а также, к сожалению, не влияют на естественное течение этой инфекции, то есть не гарантируют полного излечения. Поэтому на протяжении последних двух десятилетий ученые изыскивают методы непосредственного воздействия на иммунную систему больных генитальным герпесом с целью стимуляции специфических и неспецифических ее факторов, тем самым способствуя блокаде репродукции вируса [1].
Главной мишенью применения иммуномодулирующих препаратов служат вторичные иммунодефициты, которые проявляются частыми, рецидивирующими, трудно поддающимися лечению инфекционно-воспалительными процессами разной локализации [7]. Именно к таким процессам, требующим иммунокоррекции, и относится хроническая рецидивирующая герпесвирусная инфекция (ХРГВИ), в частности ее генитальная форма. Иммуномодуляторы назначают в комплексной терапии одновременно с противовирусными средствами.
Полиоксидоний — отечественный иммуномодулятор с широким спектром фармакологического действия, не имеющий аналогов в мире [3]. Опыт применения полиоксидония начиная с 1996 года показал его высокую клиническую эффективность в комплексном лечении многих вторичных иммунодефицитных состояний, проявляющихся хроническими, рецидивирующими, вялотекущими инфекционно-воспалительными процессами различной локализации, в том числе в ходе терапии вирусных инфекций [4].
У нас также имеется определенный позитивный опыт применения полиоксидония у пациентов, резистентных к ацикловиру [9].
Мы проводили исследование открытым методом у 50 пациентов с ХРГВИ. В исследование включались пациенты (возрастной интервал от 18 до 65 лет) мужского и женского пола с достоверным диагнозом ХРГВИ. К исследованию не допускались пациенты с гиперчувствительностью к полиоксидонию и беременные женщины. Все пациенты, включенные в исследование, находились в периоде продрома или обострения не более 48 часов от момента появления высыпаний. Обязательным условием для женщин детородного возраста было соблюдение полноценной контрацепции.
На предварительном этапе были сформированы две равнозначные группы пациентов по 25 человек. Пациенты, вошедшие в изучаемые группы, отбирались методом произвольной выборки. Все пациенты предъявляли жалобы на пузырьковые или эрозивные высыпания в области гениталий, зуд, жжение. До лечения всем пациентам проводилась ПЦР-диагностика ВПГ-2 (мазок) — положительный результат получен в 98,3 %.
Возрастной состав пациентов, страдающих генитальной формой герпесвирусной инфекции, в обеих группах был приблизительно одинаковым (43,6 года в первой группе и 38,9 — во второй), в то время как в первой группе средний возраст женщин и мужчин был несколько выше по сравнению со второй группой.
Дозировка и схемы введения. Всем пациентам производилась в/м инъекция препарата утром, под контролем врача. 1-я схема: терапия проводилась в течение 45 дней: пациенты получали по 6 мг полиоксидония в день в/м в течение 5 дней и по 6 мг в/м через день в течение 10 дней. Поддерживающая терапия — по 6 мг в/м 2 раза в неделю в течение месяца. 2-я схема: 6 мг полиоксидония в/м через день в течение 10 дней (всего 5 инъекций на курс).
Обследование проводилось до приема препарата и на 12—14-й день от начала приема препарата, а также на 3—6-й день после окончания приема препарата. Обследование включало общее клиническое, иммунологическое исследования крови, исследование мочи (общее), объективное исследование. Накануне приема препарата собирался подробный анамнез пациента. В состав исследуемых включались совершеннолетние пациенты мужского и женского пола с достоверным диагнозом ХРГВИ.
Объем сопутствующей терапии: все пациенты получали стандартную сопутствующую терапию (ацикловир по 0,2 г 5 раз в день в течение 5 дней и антиоксиданты).
Критериями оценки эффективности являлись следующие параметры: первичные критерии — время достижения полного выздоровления (полная реэпитализация); вторичные критерии — длительность ремиссии и частота рецидивов в ближайшем и отдаленном периоде после терапии полиоксидонием. С целью оценки местных симптомов проводился наружный осмотр места поражения. Оценивалось состояние кожных покровов и слизистых: наличие пузырьков, язвочек, корочек, гиперемии; выяснялись жалобы пациента (зуд, жжение, общее состояние, температура, миалгия).
На фоне лечения полиоксидонием по первой схеме длительность течения рецидива и период реэпителизации сократились в среднем с 6,44 до 3,5 дня, в то время как на фоне стандартной терапии (ацикловир и антиоксиданты) те же показатели изменились с 6,44 до 5,16 дня соответственно. После курса терапии в ближайшем и отдаленном периоде длительность рецидива и быстрота наступления реэпителизации в среднем составляла 4 дня. В процессе лечения препаратом свежие высыпания ни у одного пациента не появились. 76% (19 человек) отметили уменьшение тяжести течения рецидива; остальные — 24% (6 человек) — не отметили разницы по сравнению с периодом до получения препарата. На фоне лечения полиоксидонием по второй схеме длительность течения рецидива и период реэпителизации сократились в среднем с 6,72 до 4,24 дня вместо 6,72 — 5,04 дня соответственно. После лечения полиоксидонием в ближайшем и отдаленном периоде длительность рецидива и быстрота наступления реэпителизации в среднем также составляли 4 дня. 64 % (16 человек) отметили уменьшение тяжести течения рецидива; остальные — 36% (9 человек) — не отметили никаких изменений по сравнению с периодом до получения препарата.
Частота рецидивов у пациентов, получавших полиоксидоний по первой схеме в течение 6 месяцев после лечения, уменьшилась в среднем с 6,5 до 3 раз по сравнению с показателями ближайших шести месяцев перед получением препарата. Длительность ремиссии возросла в среднем с 27 до 75 дней. Максимальная длительность ремиссии увеличилась в среднем с 45 до 180 дней (у отдельных пациентов максимальная ремиссия достигала 190–220 дней, что связано с неравномерностью возникновения рецидивов в исследуемом временном интервале). У 84% пациентов (21 человек) отмечалось ослабление клиники течения рецидива; у 16% (4 человека) после лечения клиника не изменилась. Ухудшения течения заболевания отмечено не было. Частота рецидивов у пациентов, получавших полиоксидоний по второй схеме, в течение 6 месяцев после лечения уменьшилась в среднем с 6 до 3,6 раза по сравнению с показателями ближайших шести месяцев перед получением препарата. Длительность ремиссии возросла в среднем с 33 до 62 дней. Показатель максимальной длительности ремиссии в обеих группах вырос в среднем примерно одинаково — с 45 до 180 дней. У 72% пациентов (18 человек) отмечалось ослабление клиники течения рецидива; у 28% (7 человек) после лечения клиника не изменилась. Как и в первой группе, ухудшений течения заболевания отмечено не было.
Максимальная длительность ремиссии за период наблюдения (2 года) составила 1,9 года в первой группе (у 9 пациентов — 36 %) и 1,1 года во второй группе (у 4 пациентов — 16 %).
До лечения полиоксидонием в обеих группах частота встречаемости и выраженность местных и общих клинических проявлений ХРГВИ была выше по сравнению с теми же показателями на фоне лечения полиоксидонием.
Парентеральное (в/м) введение полиоксидония в соответствии со схемами (см. выше) не вызывало аллергических реакций, не оказывало гепатонефротоксического действия и токсического действия на кроветворные органы; пациенты отмечали хорошую переносимость препарата.
По данным общеклинических и лабораторных методов исследования, побочных эффектов и осложнений при приеме полиоксидония не было.
Использование полиоксидония в комплексной терапии пациентов с генитальной формой хронической рецидивирующей герпесвирусной инфекции является эффективным способом уменьшения клинических проявлений в фазе обострения, сокращения длительности рецидивов и заметного уменьшения их частоты в отдаленном периоде.
Раннее назначение полиоксидония способствует более быстрой реэпителизации и более стойкой ремиссии.
Использование инъекционной формы полиоксидония не вызывает аллергических реакций, а также других побочных эффектов и осложнений.
При соблюдении указанного режима дозирования препарат не обладает нефро- и гепатотоксическим действием.
А. Е. Шульженко, кандидат медицинских наук ГНЦ — Институт иммунологии МЗ РФ, Москва
Читайте также:

