Какие клетки осуществляют иммунную функцию кожи
Обновлено: 27.04.2024
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения г.Москвы
Наряду со слизистыми оболочками кожа как основной барьер с внешним миром создает сис-тему защиты от любых воздействий окружающего мира. Она является не только местом реа-лизации иммунологических процессов, но и активно участвует в них благодаря наличию собственных элементов иммунной системы, которые способны активно принимать участие в развитии воспалительных реакций и неопластических процессов. Клетки кожи взаимодействуют между собой и с клетками иммунной системы либо устанавливая прямой контакт, либо секретируя некоторое число растворимых факторов, называемых цитокинами и другие белковые компоненты, например белки системы комплемента.
Главными составляющими иммунной системы кожи являются клетки Лангерганса, клетки Гранстейна, кератиноциты, эпидермальные Т-лимфоциты, эндотелиальные клетки, тканевые макрофаги и тучные клетки. Для кооперации различных клеток на разных стадиях иммунно-го ответа требуется идентичность в отношении антигенов HLA-системы. Такая кооперация имеет место, например, когда макрофаги или дендритные клетки (например, клетки Лангер-ганса), будучи первыми антигенсвязывающими клетками, передают этот антиген Т-лимфоцитам, а затем Т- и В-лимфоциты совместно инициируют формирование антител. Та-кие специфические иммунологические реакции с антителообразованием способствуют осво-бождению организма от антигена-мишени как экзогенного, так и эндогенного происхожде-ния. Однако при нарушении какого-либо звена иммунологической защиты происходит за-медление процесса элиминации антигена, результатом которой является повреждение струк-туры собственной ткани. Взаимодействие с чужеродными антигенами (химическими, инфекционными и др.), денатурация собственных белков, ранее не контактировавших с иммунокомпетентными клетками, способствуют образованию аутоантигенов и выработку аутоантител против них.
Таким образом, кожа представляет собой сложноорганизованную структуру с сетью имму-нокомпетентных клеток и растворимых медиаторов. Внедрение молекулярно-биологических методов как инструмента познания, непрерывно расширяет сведения о коже как об органе иммунной системы. Полученные знания, безусловно, будут способствовать разработке новых методологических терапевтических подходов при кожных заболеваниях.
Кожа является крупнейшим специализированным органом человека, площадь которого составляет 2 м 2 , а масса — почти 3 кг. Она выполняет ряд важнейших функций. В частности, кожа — это барьерный орган и, что особенно важно отметить, подобно тимусу, она является местом, где созревают некоторые типы иммунных клеток и протекают иммунологические реакции. В принципе, в кожном барьере представлены все типы клеток, способные осуществлять широкий спектриммунных реакций. Это дает основание считать кожу органом иммунной системы.
В начале 80х гг. XX века была сформулирована концепция лимфоидной ткани кожи — skin-associated lymphoid tissue (SALT), которая продолжает развиваться и в наши дни. В соответствии с современными взглядами наряду с лимфоцитами к иммунной системе кожи следует отнести нейтрофилы, тучные клетки и эозинофилы, клетки Лангерганса и кератиноциты [3, 4, 20].
Лимфоциты
Для лимфоидных клеток характерна рециркуляция — постоянный обмен между кровью, лимфой и органами, содержащими лимфоидную ткань. Другой особенностью данной клеточной популяции является хоминг — заселение определенных участков лимфоидных органов и тканей. Поэтому внутридермальные лимфоциты отличаются от циркулирующих в периферической крови. Для изучения популяционного состава лимфоцитов кожи были использованы методы иммуногистохимии и «кожного окна» (определение процентного содержания клеток на отпечатке с небольшого участка кожи после удаления поверхностного слоя эпидермиса). Это позволило установить, что в норме лимфоидные клетки кожи являются преимущественно Т-лимфоцитами: CD5+ — 19%, CD3+ — 48%, CD25+ — 26%, CD4+ — 33%, CD22+ — 18% [7, 14]. Все они имеют достаточно специфичный общий маркер — кожный лимфоцитарный антиген (CLA), который считается рецептором, контролирующим сродство Т-клеток к коже. CLA — это адгезивная молекула на мембране, которая обеспечивает связывание Т-лимфоцита с эндотелием посткапиллярных венул кожи и переход его в дерму. CLA-позитивные T-клетки составляют 10—15% циркулирующих клеток крови. Популяция CLA-позитивных Т-клеток представлена несколькими субпопуляциями, различающимися по рецепторному статусу и функциональной активности [10, 11, 12]. Для всех CLA-позитивных Т-клеток характерна экспрессия кожного Т-клеточного хемоаттрактанта (CTACK), который «привлекает» в кожу Т-лимфоциты из циркуляции, прежде всего при различных воспалительных процессах. Совокупность накопленных сегодня клинико-экспериментальных данных показывает, что CTACK играет важную роль в иммунном ответе кожи. Наиболее значима его патогенетическая роль как провоспалительного фактора при таких заболеваниях, как атопический и контактный дерматиты [13].

Кроме того, большинство Т-лимфоцитов нормальной кожи здорового человека имеют рецепторы к другим хемокинам — биологически активным веществам, контролирующим миграцию клеток, в частности лимфоцитов. Это способствует их активному участию в различных иммунологических реакциях, как физиологических, так и патологических [1, 6, 21].
Т-клетки кожи способны дифференцироваться в цитотоксические клетки или клетки памяти (CD45RO). Клетки памяти экспрессируют также кожный лимфоцитарный антиген (CLA), образуются в лимфатических узлах, дренирующих кожу, и возвращаются в кожу при воспалении. В норме они участвуют в формировании иммунитета в коже, а при патологии принимают участие в патогенезе кожной Т-клеточной лимфомы, отторжения трансплантата, атопического дерматита и т. д. [2, 5, 10, 17]. Около трети лимфоцитов кожи являются Т-хелперами (СD4+). В последние годы показано, что данная субпопуляция клеток представлена двумя разновидностями —Th1 и Th2, которые различаются прежде всего по спектру продуцируемых цитокинов. В норме между этими клетками существует определенный баланс; при заболеваниях кожи соотношение Th1/Th2 меняется. Например,при воспалительных процессах повышается активность Th1-лимфоцитов [1, 8, 12, 15]. Таким образом, лимфоциты кожи представляют собой гетерогенную клеточную популяцию, в которой присутствуют клетки рециркулирующего пула и специфические кожные лимфоциты. Для последних характерен своеобразный набор клеточных рецепторов, обусловливающих их тропность к коже, а также определенный набор продуцируемых цитокинов, позволяющий им участвовать в различных клеточных реакциях, которые обеспечивают репарацию кожи.
Нейтрофилы
Нейтрофилы содержатся в нормальной коже в незначительном количестве, а при острых воспалительных процессах их число существенно возрастает. Кроме того, нейтрофильные гранулоциты участвуют в регуляции репаративных процессов путем взаимодействия с другими клетками (макрофагами, кератиноцитами). Одним из механизмов этого взаимодействия является продукция нейтрофилокинов, стимулирующих секрецию фибробластами и лимфоцитами факторов роста, которые в свою очередь индуцируют пролиферативную активность клеток регенерирующей ткани [3, 18].
Тучные клетки и эозинофилы
Тучные клетки (ТК) и эозинофилы кожи участвуют в различных патологических процессах, прежде всего — в аллергических. При внедрении аллергена в кожу он взаимодействует с эозинофилами и ТК, несущими на своей поверхности IgE-антитела. В результате этого взаимодействия происходит активация и дегрануляция клеток с последующим высвобождением различных медиаторов (субстанции Р, интерлейкинов 1 и 6, хемокинов). Они способствуют миграции в очаг патологического процесса других иммунокомпетентных клеток и поддерживают активность воспалительной реакции. Количество и функциональная активность этих клеток по-разному меняются при различных кожных заболеваниях. Кроме того, ТК и эозинофилы играют определенную роль в реализации патогенных эффектов стресса на кожу [2, 6, 9].
Клетки Лангерганса

Клетки Лангерганса (КЛ) относятся к специализированным клеткам эпидермиса и составляют 2-3% от общего числа его клеток. Они представляют собой одну из форм дендритных клеток, имеющих моноцитарно-макрофагальное происхождение и выполняющих в организме важнейшие иммунные функции, прежде всего — как антигенпрезентирующие клетки. Дендритные клетки являются ключевым звеном, связывающим приобретенный и врожденный иммунитет [16].
При воспалении и других процессах, связанных с антигенной стимуляцией, КЛ приобретают двигательную активность, покидают эпидермис с током тканевой жидкости и, перемещаясь по лимфе, претерпевают определенные морфологические трансформации, в результате чего становятся так называемыми «вуалевыми» клетками. Достигая лимфатических узлов, они активно взаимо действуют с другими иммунокомпетентными клетками и осуществляют презентацию им антигенов. КЛ способны взаимодейство вать с различными типами Т-клеток, модулируя таким образом различные типы иммунных реакций (воспаление, аутоиммунитет). Кроме того, КЛ непосредственно участвуют в уничтожении бактерий в коже.
Кератиноциты
Кератиноциты также следует отнести к иммунной системе кожи. Они продуцируют широкий спектр регуляторных молекул (ростовых факторов, цитокинов), чем обусловлено их участие в иммунной защите кожи [2, 8, 16, 21]. Нарушение взаимодействия молекул адгезии на поверхности кератиноцитов с рецепторами лимфоцитов является важным механизмом патогенеза ряда заболеваний, например псориаза [5, 7, 17, 19].
Меланоциты
В последние годы эти пигмент-продуцирующие клетки кожи стали относить и к иммунокомпетентным, поскольку они, как и кератиноциты, способны продуцировать ряд цитокинов (интерлейкины 1, 3 и 6, фактор некроза опухолей, трансформирующий фактор роста и другие), которые выступают в роли медиаторов иммунного ответа в дерме [2].
Цитокины — биорегуляторы иммунных реакций
Последние десятилетия характеризовались бурным накоплением данных о новом классе иммунорегуляторных молекул — цитокинов. Они включают в себя огромное количество различных веществ, в том числе интерлейкинов, которые выполняют коммуникативную функцию между иммуноцитами и оказывают различные регуляторные влияния как в рамках иммунной системы, так и в других органах и тканях. В настоящее время в коже обнаружено большинство известных интерлейкинов: их функции связаны с кожей, а нарушение продукции лежит в основе патогенеза ряда кожных заболеваний, в частности псориаза и атопического дерматита [2, 6, 7].
Иммунная система кожи при инфекционном и неинфекционном поражении
Иммунная система кожи участвует в реализации и врожденного, и приобретенного иммунитета. Наиболее значимо ее роль проявляется при нарушении целостности барьера и проникновении в дерму микро организмов. При этом SALT реагирует как единая функциональная система. В анти-генпрезентирующих клетках происходят процессинг и презентация антигена, в ходе которых КЛ превращаются в дендритные клетки и перемещаются по дерме в лимфатические узлы. В результате они приобретают способность взаимодействовать с Т-хелперами, которые затем активируют В-клетки и частично дифференцируются в эффекторные лимфоциты и клетки памяти. Т-клетки памяти, несущие CLA, способны из кровотока мигрировать в эпидермис; именно они и преобладают в коже. В результате увеличения числа Т-клеток, контактирующих с наиболее «актуальными» антигенами, вносится поправка в антигенраспознающий репертуар Т- лимфоцитов. Этим определяется активность иммунного ответа.
При неинфекционном поражении кожи, например при травме, иммунная система активно участвует в заживлении кожной раны. Заживление кожной раны — это динамичный интерактивный процесс с участием медиаторов, клеток крови, межклеточного матрикса и мезенхимальных клеток, который состоит из трех фаз: воспаление, образование грануляционной ткани и тканевое ремоделирование. Воспаление является реакцией организма в целом и кожи в частности на травму. Ведущая роль в его развитии принадлежит клеткам крови — нейтрофилам. Они не только участвуют в гемостазе, но и выделяют биологически активные вещества.

В результате происходит активация моноцитов-макрофагов, которые служат связующим звеном между воспалением и регенерацией. Активация этих клеток приводит к индукции пролиферации эпидермиса. Необходимо отметить, что реэпителизация начинается уже через несколько часов поле нанесения травмы. Первоначально она идет за счет сокращения внутриклеточных тонофиламентов, что повышает миграционную способность эпидермальных клеток. Примерно через четверо суток в ране определяется новообразованная строма (грануляционная ткань). Под влиянием различных цитокинов, продуцируемых иммунокомпетентными клетками, в ней происходят дифференцировка фибробластов, синтез коллагена, новообразование сосудов. Активное участие в этих процессах принимают цитокины, и в том числе — ростовые факторы (эпидермальный, трансформирующий, тромбоцитарный, эндотелиальный и другие). Метаболизм коллагена, появление в грануляционной ткани миофибробластов, пролиферация кератиноцитов и целый ряд других клеточных событий, завершающих «созревание» грануляционной ткани, приводят к формированию кожного рубца, что свидетельствует о восстановлении целостности ткани и завершении репаративного процесса [19, 21].
Таким образом, в коже представлены все типы иммунного ответа — врожденный и приобретенный (адоптивный), клеточный и гуморальный. Благодаря этому возможны и неспецифическая защитная функция (иммуноглобулины, лизоцим, лактоферрин, дефенсины, фагоцитоз), и первичное распознавание антигена с последующей его презентацией и пролиферацией антиген-специфических Т-клеток. В результате в дерме осуществляются как цитотоксические реакции, так и антителообразование. Необходимо подчеркнуть, что особенностью кожи как иммунного органа является относительное преобладание врожденного иммунитета над приобретенным, а в системе врожденного иммунитета кожи в свою очередь превалируют клеточные факторы. Анализ многочисленных научных данных позволяет полагать, что иммунные реакции имеют отношение к большинству физиологических и патологических процессов, происходящих в коже.

Нарушения функции SALT
На обширном экспериментальном и клиническом материале показано, что нарушения функций SALT — реактивности Т-клеток, продукции цитокинов, экспрессии хемокинов на клетках, межклеточных взаимодействий и других иммунологических реакций — приводят к развитию ряда заболеваний, любое из которых сопровождается изменением внешнего вида кожи. Это могут быть воспалительные заболевания кожи (фурункулы, акне), атопический дерматит, псориаз, Т-клеточная кожная лимфома [5, 16, 17]. Известно, что возрастные изменения кожи также связаны с изменением ее иммунологических функций. В стареющей коже наблюдаются мононуклеарная инфильтрация, снижение числа клеток Лангерганса и изменение продукции иммунокомпетентными клетками цитокинов, влияющих на пролиферацию и дифференцировку клеток кожи.
Разнообразие клеток, входящих в иммунную систему кожи, а также многообразие их функций объясняют тот факт, что на уровне кожи возможно проявление всех типов иммунопатологических синдромов (иммунодефицитный, аутоиммунный, аллергический, лимфопролиферативный). Иммунодефицитный синдром проявляется, например, фурункулезом и другими гнойно-воспалительными процессами. При дефектах фагоцитоза кожа становится чувствительной ко многим бактериальным и грибковым инфекциям, но иммунный ответ нарушается на любой антиген, поскольку страдает антигенная презентация.
Аллергический (гиперергический) синдром встречается достаточно часто и имеет место при контактном и атопическом дерматитах. Явления гиперергии характерны и для псориаза. Аутоиммунный синдром также имеет кожные проявления (склеродермия, системная красная волчанка). Примером лимфопролиферативного синдрома служит Т-клеточная лимфома кожи (грибовидный микоз).
Диагностика всех этих состояний основана на клинических признаках. Например, для иммунодефицитного заболевания это будут такие критерии, как рецидивирующее течение инфекционного поражения кожи, его затяжное течение несмотря на проведение адекватной фармакотерапии, тенденция к генерализации инфекционно-воспалительного процесса в коже, резистентность к антимикробной терапии, преобладание в очаге поражения некротических изменений над воспалительными, несоответствие локальных и системных проявлений кожной инфекции. Специфических тестов, характеризующих состояние иммунитета кожи, в практической медицине не существует. Дерматолог может ориентироваться на стандартные иммунологические показатели крови. В научных же исследованиях используют морфологическую (гистологическую) оценку иммунокомпетентных структур кожи, метод «кожного окна» и некоторые другие.
Как улучшить иммунитет кожи?
Патология иммунной системы приводит к развитию иммунозависимой патологии. Поэтому потребность в стимуляции иммунитета кожи при его угнетении патогенетически обоснована. Для этих целей могут быть рекомендованы такие препараты, как Полиоксидоний и Ликопид. Некоторые иммуномодуляторы (например, Рибоксин) могут использоваться как для системного, так и для местного применения, в том числе в мезотерапевтических методиках. При этом интрадермальные иньекции оказывают влияние преимущественно на иммунную систему кожи, а системное применение приводит к активации лимфопоэза в тимусе и лимфатических узлах. Другими словами, выбор способа введения препарата (местное или системное) должен базироваться на характере иммунных нарушений — как в коже, так и в организме в целом.

Умеренным иммунотропным действием обладают и неспецифические адаптогены (витаминно-микроэлементные комплексы, настойка аралии и т. п.). Мы обнаружили иммуноактивные свойства у органического кремния, который широко используется в мезотерапевтической практике. В лечении заболеваний, вызванных повышенной реактивностью иммунной системы (псориаз, лимфомы), используют иммунодепрессанты (циклоспорин). Последним достижением иммунофармакологии является использование в качестве ингибиторов иммунной системы моноклональных (высокоспецифичных) антител.
Улучшая иммунный статус кожи, следует помнить о том, что иммунная система кожи, морфологически представленная SALT, с одной стороны, является достаточно автономным отделом иммунной системы организма, с другой — имеет с ней тесные морфофункциональные и регуляторные взаимоотношения. Нарушения нормальных иммунных реакций в коже приводят к развитию многих дерматологических заболеваний и подавляющего большинства эстетических проблем, в том числе к преждевременному старению кожи. Неудивительно, что кожа является мишенью для иммунотерапевтических вмешательств, в частности иммуномезотерапии. Более подробно этот вопрос мы планируем рассмотреть в следующих публикациях.
Кожа – это не только физический барьер между внешней и внутренней средой, активно защищающий от стресса, вызванного травмой или микробным воздействием, ультрафиолетовым излучением и токсинами окружающей среды.
Долгое время кожа представлялась только в виде своеобразного щита, отделяющего организм от внешней среды. Концепция кожного иммунитета была введена Streilein в 1983 году, эта концепция была дополнена Egawa и соавт. в 2011 и Ono и соавт. в 2015 г.
Иммунная система кожи расположена в двух основных структурных отделах – эпидермисе и дерме – и состоит из нескольких важных типов иммунокомпетентных клеток. Основные резидентные иммунные клетки – клетки Лангерганса – вместе с меланоцитами, которые продуцируют меланин, занимают область эпидермиса, в то время как другие типы специализированных иммунных клеток, такие как различные субпопуляции дендритных клеток, макрофаги и несколько типов T-клеток, находятся в более глубоком слое – в дерме.
В их перечень также внесены:
антигенные клетки, локализующиеся в эпидермисе,
гранулоциты и другие виды.
Эффективность иммунной системы кожи сильно зависит от тесного взаимодействия и связи между иммунными клетками и клетками кожи, например, кератиноцитами и фибробластами. Кожный иммунитет зависит также от кровеносных и лимфатических сосудов, которые дренируют кожу.
В последние годы появился новый вклад в иммунный ответ кожи для нескольких популяций клеток, находящихся в разных слоях кожи.
Иммунная система кожного покрова, морфологически представленная salt (skin – associated lymphoid tissue), участвует в реализации врожденных и приобретенных защитных функций организма. Значимая ее роль становится заметной при проникновении в дерму патогенной микрофлоры и нарушении целостности барьера между окружающей средой и человеком. Кожный покров, состоящий из эпидермиса, дермы и подкожно-жировой клетчатки, является одним из важнейших и уникальных органов человеческого организма.
Иммунная система кожи принимает участие в противостоянии различным инфекционным агентам в виде вирусов, бактерий, грибков и т. д. Кожа способна за счет микроциркуляторного русла вмещать до 1 дм³ крови и выполняет широкий спектр функций. К основным из них относится барьерная, обменная, терморегуляторная, защитная, осязательная, а также образующая витамин D под воздействием ультрафиолетового излучения.
Рассмотрим более подробно основные клетки, которые влияют на иммунитет кожи.
Кератиноциты составляют основной структурный элемент наружного слоя кожи и в зависимости от уровня созревания создают четыре слоя эпидермиса. Помимо их структурной функции, недавние исследования показали роль кератиноцитов во врожденном и адаптивном иммунитете. Модуляция иммунной системы и иммунного статуса кожи сильно зависит от функциональных кератиноцитов. Кератиноциты вместе с нейтрофилами и эпителиальными клетками создают основной источник антимикробных пептидов (AMП), небольших катионных и амфипатических молекул, выступая в качестве первой линии защиты. Аберрантная экспрессия АМП приводит к развитию воспалительных заболеваний кожи и восприимчивости к микробным инфекциям. Снижение экспрессии AMП приводит к повышенной предрасположенности к кожным инфекциям при атопическом дерматите, тогда как высокая экспрессия AMП наблюдается в псориатических поражениях. Кератиноциты продуцируют широкий спектр регуляторных молекул (ростовых факторов, цитокинов), чем обусловлено их участие в иммунной защите кожи. Нарушение взаимодействия молекул адгезии на поверхности кератиноцитов с рецепторами лимфоцитов является важным механизмом патогенеза ряда заболеваний. Кроме того, пластичность кератиноцитов в продукции хемокинов и хемокиновых рецепторов дает им возможность «общаться» и взаимодействовать с другими типами клеток во время иммунного ответа. Кератиноциты не способны праймировать наивные Т-клетки; однако они могут стимулировать опытные антигены клетки CD4 и CD8. Нарушение работы кератиноцитов приводит к патологическим состояниям, таким как аутоиммунные состояния и онкология.
Клетки Лангерганса (КЛ)
КЛ относятся к специализированным клеткам эпидермиса и составляют 2–3 % от общего числа его клеток. Они представляют собой одну из форм дендритных клеток, имеющих моноцитарно-макрофагальное происхождение и выполняющих в организме важнейшие иммунные функции, прежде всего – как антигенпрезентирующие клетки. Дендритные клетки являются ключевым звеном, связывающим приобретенный и врожденный иммунитет. При воспалении и других процессах, связанных с антигенной стимуляцией, КЛ приобретают двигательную активность, покидают эпидермис с током тканевой жидкости и, перемещаясь по лимфе, претерпевают определенные морфологические трансформации. Достигая лимфатических узлов, они активно взаимодействуют с другими иммунокомпетентными клетками и осуществляют презентацию им антигенов. КЛ способны взаимодействовать с различными типами Т-клеток, модулируя таким образом различные типы иммунных реакций (воспаление, аутоиммунные реакции).
Рассматривая локализацию КЛ, которая является внешней частью, можно предположить их роль в качестве «бойцов» первой линии. Супрессивное действие КЛ на контактную гиперчувствительность зависит от их продукции IL-10 и индукции CD4 + регуляторных Т-клеток и толерантность к CD8+ Т-клеткам. Тем не менее роль КЛ в иммунных реакциях кожи остается несколько загадочной. Интересной особенностью КЛ в стационарном состоянии является их способность к репопуляции локально независимо от циркулирующих предшественников. Скорость их миграции через кожные лимфатические сосуды к дренирующим кожу лимфатическим узлам увеличивается во время воспаления. При стимуляции КЛ удлиняют свои дендриты, которые входят в эпидермальные плотные соединения для захвата антигенов. Они созревают и, наконец, локализуются в области Т-клеток путем усиления регуляции молекул MHC класса II, ко-стимулирующих молекул (CD40) и необходимых для миграции хемокиновых рецепторов CCR7. КЛ имеют решающее значение для захвата белковых антигенов и опосредования локальной среды Th2. Постоянное истощение КЛ приводит к снижению уровня IgE в сыворотке крови.
Дендритные клетки (ДК)
В отличие от КЛ, которые занимают эпидермис, ДК находятся в дерме ниже эпидермально-дермального перехода и отличаются экспрессией молекулы адгезии эпителиальных клеток, IL-10, и способностью стимулировать в плазматические клетки секретирующие IgM. Экспрессия связанного с липопротеидами низкой плотности белка 1 (или CD91) также характерна для ДК. Пластичность этих клеток замечательна, и в зависимости от функции, сублокализации и окружающей среды они создают фенотипически разнообразную группу клеток. Основная роль ДК заключается в обеспечении иммуносупрессии против патогенов путем участия в воспалительных реакциях. ДК, продуцирующие как ФНО-α, так и другие цитокины, могут играть важную роль в индукции псориаза. Также было обнаружено, что при псориазе важную роль играет LL37, АМП, который нарушает толерантность к собственной ДНК. В результате активируются миелоидные ДК и индуцируются адаптивные иммунные реакции. Было установлено, что ДК и тканерезистентные макрофаги имеют общих предшественников. Сложность сети, созданной дендритными клетками, моноцитами и макрофагами в коже, обеспечивает эффективную иммуносупрессию и весьма разнообразный иммунный ответ.
Тучные клетки (ТК)
Тучные клетки (ТК) и эозинофилы кожи участвуют в различных патологических процессах, прежде всего – в аллергических. При внедрении аллергена в кожу он взаимодействует с эозинофилами и ТК, несущими на своей поверхности IgE-антитела. В результате этого взаимодействия происходит активация и дегрануляция клеток с последующим высвобождением различных медиаторов (субстанции Р, интерлейкинов 1 и 6, хемокинов). Они способствуют миграции в очаг патологического процесса других иммунокомпетентных клеток и поддерживают активность воспалительной реакции. Количество и функциональная активность этих клеток по-разному меняются при различных кожных заболеваниях. Кроме того, ТК и эозинофилы играют определенную роль в реализации патогенных эффектов стресса на кожу. ТК в основном расположены в верхнем слое кожи, где они могут легко сталкиваться, реагировать и защищать от инфекций, токсинов и стресса, вызванных заживлением ран. Тучные клетки содержат гистамин, поэтому они известны как типичные аллергические клетки. Тем не менее недавние исследования доказывают их замечательную внутреннюю и внешнюю пластичность и решающую роль в таких жизненно важных процессах, как заживление ран, воспаление кожи, ангиогенез и т. д. В коже человека наблюдается преобладание тучных клеток типа ТС (триптаза-положительные, химаза-положительные), которые являются самыми богатыми по содержанию протеиназ. Триптаза действует на фибронектин и разрушает белки внеклеточного матрикса, позволяет иммунным клеткам, таким как нейтрофилы, мононуклеарные клетки и лимфоциты, проникать в эпидермис. Его функция в активации иммунокомпетентных клеток дополнительно подтверждается его активирующим действием на кератиноциты и металлопротеиназы. Этот фермент обладает также сильной проангиогенной активностью. Подобное провоспалительное действие характерно и для другого мощного фермента тучных клеток – химазы. Было показано, что химаза привлекает и активирует несколько иммунных клеток и усиливает воспаление за счет его влияния на IL-1β и IL-18. В дополнение к пластичности тучных клеток было обнаружено, что оба фермента снижают регуляцию иммунного ответа за счет способности разрушать несколько провоспалительных факторов, таких как цитокины и хемокины. Помимо непрямой модуляции иммунного ответа тучными клетками с помощью секретируемых ферментов они также воздействуют на иммунокомпетентные клетки путем прямого клеточного контакта или цитокинов. При хроническом воспалении кожи, таком как псориатическое поражение и атопический дерматит, тучные клетки секретируют другие цитокины, такие как IL-4 и/или IFN-γ, которые формируют иммунный ответ. При онкологии тучные клетки могут экспрессировать CD30L, что приводит к неконтролируемому иммунному ответу. Помимо известных рецепторов FceRI, участвующих в аллергическом ответе, тучные клетки кожи также экспрессируют рецепторы FcyRI и FcyRIIa, участвующие в ответах IgG.
Общеизвестно, что кожа является резервуаром приблизительно 20 миллиардов Т-клеток, что почти в два раза превышает их количество во всем объеме крови. Первоначально восприятие иммуносупрессии кожи основывалось на Т-клетках, которые мигрируют между дренирующими кожу лимфатическими узлами и периферическими тканями. Локальная дефектная миграция специфических Т-клеток, а не системное снижение опосредованного Т-клетками иммунитета, ответственна за более слабые реакции на бактериальные, грибковые и вирусные антигены. Исследования показывают, что снижение секреции ФНО-α макрофагами ингибирует активацию эндотелиальных клеток путем подавления е-селектина, молекулы адгезии сосудистых клеток, что приводит к трансмиграции Т-клеток в кожу. Было обнаружено, что витамин D ингибирует реактивность эффекторных Т-клеток и индуцирует регуляторные Т-клетки. Эпидермальные CD8+ αβ Т-клетки имеют фенотип памяти и живут среди кератиноцитов с преимущественной локализацией вблизи КЛ.
Т-клетки кожи способны дифференцироваться в цитотоксические клетки или клетки памяти (CD45RO). Клетки памяти экспрессируют также кожный лимфоцитарный антиген (CLA), образуются в лимфатических узлах, дренирующих кожу, и возвращаются в кожу при воспалении. В норме они участвуют в формировании иммунитета в коже, а при патологии принимают участие в патогенезе кожной Т-клеточной лимфомы, отторжения трансплантата, атопического дерматита и т.д. Около трети лимфоцитов кожи являются Т-хелперами (СD4+). В последние годы показано, что данная субпопуляция клеток представлена двумя разновидностями – Th1 и Th2, которые различаются прежде всего по спектру продуцируемых цитокинов. В норме между этими клетками существует определенный баланс; при заболеваниях кожи соотношение Th1/Th2 меняется. Например, при воспалительных процессах повышается активность Th1-лимфоцитов. Таким образом, лимфоциты кожи представляют собой гетерогенную клеточную популяцию, в которой присутствуют клетки рециркулирующего пула и специфические кожные лимфоциты. Для последних характерен своеобразный набор клеточных рецепторов, обусловливающих их тропность к коже, а также определенный набор продуцируемых цитокинов, позволяющий им участвовать в различных клеточных реакциях, которые обеспечивают репарацию кожи.
Современные знания об иммунокомпетентных клетках кожи подчеркивают важность кожи как части лимфатической системы. Иммунные реакции, которые имеют место в периферическом органе, таком как кожа, одинаково важны с теми реакциями, которые происходят в классических лимфоидных органах. В эпоху вакцинации и растущей осведомленности об онкологии, аутоиммунных процессах и процессах старения знание иммунитета кожи имеет принципиальное значение.
Больше внимания следует уделять таким факторам окружающей среды, как гипоксия, которая может присутствовать в разных слоях кожи и регулировать иммунные реакции в коже. Гипоксия кожи ингибирует эффекторные функции лимфоцитов. Фактор транскрипции, индуцируемый гипоксией фактор (HIF)-1α, является ключевым регулятором клеточной адаптации к гипоксии. HIF-1α играет роль в бактерицидной способности макрофагов и нейтрофилов. Было показано, что HIF-1α регулирует выработку кателицидина кератиноцитами, поэтому имеет решающее значение для их антибактериальной функции. В случае ДК гипоксическая микросреда оказывает резкое давление для обеспечения провоспалительных и антимикробных функций. Гипоксия также оказывает сильное влияние на сахаросвязывающие свойства лектинов, которые влияют на механизмы иммунного распознавания, а в случае галектина-1 усиливает связывание углеводов.
Другим влиятельным фактором, который следует учитывать в нашем понимании иммунитета кожи, является старение. Старение кожи является многофакторным процессом, который включает в себя нарушение функции иммунных клеток кожи. Увеличение кожных инфекций и онкологии становится заметным у пожилых людей. Предполагается, что с возрастом нарушаются как приобретенный, так и врожденный иммунитет. Понимание механизмов кожного иммунитета в различных условиях окружающей среды позволит улучшить терапевтические подходы как в дерматологии, так и в косметологии.
Каким же образом укрепить иммунитет кожи?
В первую очередь, необходимо нормализовать режим питания, обогатить рацион здоровой пищей: для этого лучше всего подходят все овощи и фрукты зеленого цвета, злаки, каши. Цитрусовые прекрасно поддерживают организм и улучшают структуру кожи. Витамины для иммунитета кожи – это А, Е, С, В, К, кислоты.
Витамин А поддерживает и восполняет водный баланс кожи, предохраняет от пересыхания и улучшает эластичность. Витамином А богаты продукты животного происхождения.
Витамин Е защищает от воздействия ультрафиолетовых и солнечных лучей, принимает участие в обновлении клеток, питает и смягчает кожу. Витамин Е присутствует в зелени и фруктах.
Витамин С принимает участие в образовании коллагена в организме человека, укрепляет стенки кровеносных сосудов и улучшает цвет лица. Рекордсменами по количеству витамина С являются цитрусовые.
Витамины группы В улучшают цвет и эластичность, препятствуют преждевременному старению, благоприятно воздействуют на процесс обновления клеток кожи, способствует быстрому заживлению ран и синяков.
Никотиновая кислота и витамин К препятствуют старению организма, при достаточном количестве этих витаминов в организме человека существенно замедляется процесс старения, и кожа выглядит молодой.
Для поддержки иммунитета кожи, кроме продуктов питания, можно использовать витамины в чистом виде, как правило, в таблетках, ампулах или капсулах, которые можно приобрести в аптеке.
Витамины принимают в чистом виде как инъекции или маски: они наносятся на лицо и остальные части тела. Витаминные растворы можно добавлять в ванную при купании.
Чтобы внешне воздействовать на кожу и питать ее полезными микроэлементами, используют витаминные комплексы и кремы, в состав которых входят коллаген, воды горных источников и лечебные грязи. Такие препараты очищают верхние слои кожных покровов, способствуя проникновению полезных веществ глубоко под кожу, восстанавливают питание клеток, замедляют процесс старения и разглаживают морщины.
В ряде случаев тусклый землистый цвет лица, дряблость кожи, пигментации, сосудистые патологии и т. д. могут свидетельствовать о том, что ее иммунитету нужна «тяжелая артиллерия». Тогда возникает необходимость проконсультироваться у косметолога насчет различных инъекционных или аппаратных процедур. Еще один важный момент: если вы все делаете правильно, но кожа все равно сигнализирует о серьезных проблемах организма (это может выражаться в раздражениях, акне, красноте и т. д.), стоит обратиться к иммунологу. Он поможет разобраться, как повысить иммунитет кожи, назначит анализы, соберет данные о состоянии здоровья и назначит курс препаратов или инъекций.

Кожа, подобно тимусу, является важным иммунным органом. В структурах кожи созревают некоторые типы иммунных клеток и протекают иммунологические реакции.
В кожном барьере представлены все типы клеток, способные осуществлять широкий спектр иммунных реакций.
Кожный покров является первым барьером на пути проникновения чужеродных элементов.
Кожа первая реагирует на внедрение антигенов и может сигнализировать о наличии воспалительного процесса в организме.
Читайте в этой статье о главных иммунных клетках кожи, механизмах иммунного ответа, а также способах улучшить иммунитет кожи.
Анатомическое и функциональное подобие клеток тимуса с клетками кожи
Кожа играет немаловажную роль в процессах иммунитета. Иммунная функция кожи обеспечивается рядом специализированных клеток.
Основные элементы иммунной системы кожи составляют кератиноциты, эпидермальные Т-лимфоциты клетки Лангерганса, нейтрофилы, базофилы и эозинофилы.

Кератиноциты способствуют созреванию Т-лимфоцитов путем влияния на них фермента дезоксирибонуклеотидилтрансферазы (ДРНТ).
Кератиноциты продуцируют ряд важных биологически активных веществ, которые участвуют в иммунных и воспалительных реакциях.
К ним относятся:
• гидроксиды жирных кислот;
• активатор и ингибитор плазминогена.
Подобие кератиноцитов с эпителиальными клетками тимуса подтверждается общими гетероантигенами, которые находятся в базальных клетках эпидермиса и гормональном эпителии тимуса.
В глубоких структурах телец тимуса обнаружены антигены, характерные для шиповатого, зернистого и рогового слоев эпидермиса.
Из этого следует, что иммунная функция кожи анатомически и функционально подобна к вилочковой железе.
Читайте нас в Telegram
Лимфоцитарная система кожи: основные иммунные маркеры и клетки
Иммунная функция кожи невозможна без самых главных клеток гуморального иммунитета – лимфоцитов.
В норме лимфоидные клетки кожи представлены преимущественно Т-лимфоцитами. Около трети лимфоцитов кожи являются Т-хелперами (СD4+). Все они имеют достаточно специфичный общий маркер — кожный лимфоцитарный антиген (CLA). Рецептор является адгезивной молекулой на мембране, которая обеспечивает связывание Т-лимфоцита с эндотелием посткапиллярных венул кожи и переход его в дерму.
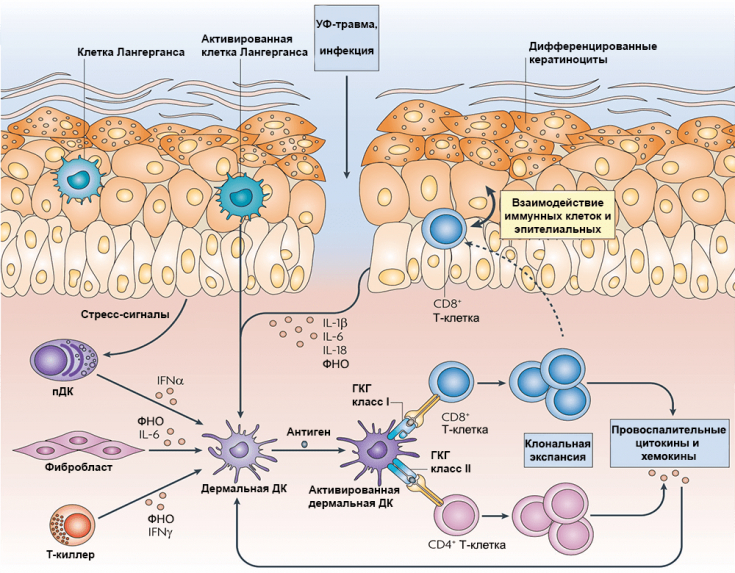
Антигенспецифический Т-клеточный ответ состоит в образовании бластных форм Т-лимфоцитов, которые возвращаются в участки кожи, содержащие антиген.
Иммунные нарушения играют патогенетическую роль при различных заболеваниях кожи, в том числе при буллезных дерматозах, аллергодерматозах, псориазе, Т-лимфоме кожи.
Т-клетки кожи способны дифференцироваться в цитотоксические клетки или клетки памяти (CD45RO). Клетки памяти образуются в лимфатических узлах, дренирующих кожу, и возвращаются в кожу при воспалении. В норме они участвуют в формировании кожного иммунитета, а при патологии принимают участие в патогенезе таких состояний, как кожная Т-клеточная лимфома, отторжение трансплантата, атопический дерматит и других иммунопатологических заболеваний.
Как улучшить иммунитет кожи: эффективные методики и препараты
При условии угнетения иммунитета кожи, необходима стимуляция ее иммунных и защитных свойств.
Для этих целей рекомендуется применять препараты, содержащие полиоксидоний и глюкозаминилмурамилдипептид.
Хорошо себя зарекомендовали некоторые иммуномодуляторы (например, инозин). Они могут использоваться как для системного, так и для местного применения, в том числе в мезотерапевтических методиках. Интрадермальные инъекции оказывают влияние преимущественно на иммунную систему кожи, а системное применение приводит к активации лимфопоэза в тимусе и лимфатических узлах.

Иммунная функция кожи значительно повышается при использовании неспецифических адаптогенов (витаминные комплексы, настойка аралии и т. п.). В лечении заболеваний, вызванных повышенной реактивностью иммунной системы (псориаз, лимфомы), используют иммунодепрессанты (циклоспорин).
Последним достижением иммунофармакологии является использование в качестве ингибиторов иммунной системы моноклональных антител.
Иммунная функция кожи зависит от многих факторов: эндогенных и экзогенных. Негативное влияние на защитные способности кожного покрова имеет ультрафиолетовое излучение в высоких дозах, агрессивные косметические средства, вредные привычки, стрессы, хронические инфекции, а также несоблюдение сбалансированного питания.
Нарушения нормальных иммунных реакций в коже приводят к развитию многих дерматологических заболеваний и подавляющего большинства эстетических проблем, в том числе к преждевременному старению кожи. Поэтому своевременная диагностика и лечение иммунопатологических состояний кожи обеспечит пациента от серьезных последствий и осложнений.
Во время пандемии иммунитету стало уделяться в разы больше внимания, а с наступлением холодов мы уже привыкли запасаться витаминами и включать в рацион иммуностимулирующие продукты. Но существует и другой иммунитет — кожи, и ему тоже нужна поддержка. Что такое иммунитет кожи и как о нем позаботиться, разбираемся вместе с к.м.н., врачом-косметологом, дерматовенерологом клиники Remedy Lab Еленой Клюзко.

Елена Клюзко
Что такое иммунитет кожи и за что он отвечает?
Кожа — крупнейший орган человека массой около 3 кг, который выполняет ряд очень важных функций. Она действует как физический барьер для внешней среды и защищает организм от различных физических и химических факторов: ультрафиолетовое излучение, проникновение микробов и паразитов, потеря воды, попадание внутрь организма различных химических агентов. Один из факторов защиты — иммунная функция кожи. В ней присутствуют защитные клетки — иммуноциты, такие как кератиноциты, лимфоциты, клетки Лангерганса, тучные клетки. Они обеспечивают первые механизмы защиты против многочисленных инфекционных агентов путем захвата и последующей активации иммунологических реакций. Поэтому кожа считается органом иммунной системы, которая отвечает как за врожденный, так и за приобретенный иммунитет.
Что может негативно повлиять на иммунитет кожи?
Важным фактором иммунитета является нормальная микрофлора кожи — микробиом кожи, или совокупность микроорганизмов, которые живут на ее поверхности. Микробиом — уникальная изменяющаяся экосистема. Он разнообразен, индивидуален и зависит от множества факторов: pH, влажности, температуры, количества и качества кожного сала, оксидативного стресса, инфекций, ухода за кожей.
Иммунная система кожи, в свою очередь, является частью общего иммунитета организма. Поэтому кожные иммунологические процессы могут быть подавлены многочисленными внутренними и внешними факторами. К ним относятся: условия окружающей среды (УФ-излучение и загрязнение воздуха поллютантами, вредными химическими веществами), вредные привычки (курение, алкоголь, неправильное питание с избытком сахаров и фаст-фуда), стресс и усталость, особенно хронические, различные заболевания (нарушение работы желудочно-кишечного тракта, ожирение и дисбактериоз кишечника).
Что будет, если он нарушится?
При нарушении кожа может стать чувствительной и раздраженной. Характерны воспалительные реакции, появление прыщей, красных пятен, шелушения и медленно заживающих ранок. Могут появиться преждевременные признаки старения.
Различные кожные заболевания, такие как розацеа, псориаз, атопический дерматит, себорейный дерматит часто являются проявлением нарушенного кожного иммунитета и дисбаланса в микробиоме кожи и требуют консультации и последующего лечения у дерматолога.
Как его восстановить?
Прежде всего, нужно минимизировать негативное воздействие внешних и внутренних факторов. Если вы жалуетесь на проблемы с кожей, волосами или ногтями, то начать восстановление следует с кишечника. Именно желудочно-кишечный тракт в ответе за авитаминоз и слабый иммунитет кожи. Важно придерживаться сбалансированного питания, а при наличии проблем с кожей — «противовоспалительной диеты» с ограниченным употреблением быстрых углеводов. Ведь сахар вызывает процессы гликации — склеивание и патологическое изменение коллагеновых волокон, что приводит к ослаблению иммунитета кожи, образованию морщин и нарушению пигментации.
Своим пациентам мы предлагаем программу ImmunoHealth — тест на основе анализа крови, который позволяет выявлять аномально высокие цифры пищевых антигенов, негативно воздействующих на иммунную систему, и исследовать реакцию иммунной системы на более 100 продуктов питания. Учитывая результаты теста, врач подбирает индивидуальную систему питания, которая снижает нагрузку на иммунную систему, приводит к нормализации обменных процессов и повышает адаптационные возможности организма.
Сдайте анализы и проверьте дефициты витаминов, микроэлементов и гормонов. По результатам исследования и после консультации с врачом начинайте принимать витаминные комплексы и БАДы для восполнения дефицитов и стимуляции иммунитета. Кстати, у нас в клинике пациенты могут сразу пройти комплексный анализ «Check up Essentials», который включает общий анализ крови, определение базовых дефицитов, а также уровня гормонов щитовидной железы. А после консультации можно приобрести назначенные врачом биоактивные комплексы Advanced Nutrition Programme. Они разработаны в Великобритании в 2006 году специально для врачей-косметологов и содержат необходимые для организма витамины и микроэлементы.
Какие вещества наиболее важны для иммунитета кожи?
Все дефициты могут отражаться на иммунитете, красоте и здоровье кожи и организма в целом. Очень важны следующие элементы:
- витамин А — участвует в дифференциации клеток кожи и эпителия слизистых оболочек, повышая сопротивляемость патогенным микроорганизмам. При его дефиците кожа становится сухой и тусклой.
- витамин С — антиоксидант, стимулятор выработки коллагена, повышает сопротивляемость внешним факторам.
- цинк — его дефицит ведет к ослаблению иммунной системы организма, плохому заживлению ран, выпадению волос, акне.
- витамин D — обеспечивает здоровый жизненный цикл клеток и укрепляет иммунитет кожи.
- полиненасыщенные жирные кислоты Омега 3 — составляют основу мембраны клеток иммунной системы.
Нужно ли делать косметические процедуры, направленные на восстановление иммунитета?
Мы можем помочь иммунитету кожи, работая с микробиомом и правильно подбирая уход и косметологические процедуры для кожи. Решающими при сниженном иммунитете кожи станут процедуры по очищению, которые дадут возможность клеткам дышать и полноценно работать. Например, с помощью вакуумного гидропилинга кожи лица HydraFacial можно не только глубоко очистить поры с помощью различных насадок, но и нанести лечебные сыворотки, содержащие антиоксиданты, микроэлементы и витамины. Для стимуляции иммунитета кожи и лечения активно и успешно применяются такие инъекционные процедуры, как мезотерапия (инъекционное введение под кожу коктейлей на основе гиалуроновой кислоты, витаминов, пептидов, аминокислот) или PRP плазмотерапия (инъекционное введение собственной плазмы крови пациента, обогащенной тромбоцитами). На повышение иммунитета кожи также положительно влияет ФДТ (фотодинамическая терапия), основанная на воздействии световой энергии. В комплексном лечении угревых высыпаний успешно применяется широкополосный свет BBL, он воздействует на пропионибактерии акне, возбудители угревой сыпи. Фототерапия убирает воспаления, нормализует микробиом кожи и восстанавливает ее иммунитет.
Читайте также:

