Плоскоклеточный рак пищевода без ороговения что это
Обновлено: 19.04.2024
Рак пищевода 4 стадии диагностируется у каждого третьего больного, самое активное лечение оставляет этим пациентам немного шансов на долгую жизнь. Особенность пищеводной карциномы — высока агрессивность при запоздалом выявлении.
Рак пищевода
На рак пищевода среди всех злокачественных болезней приходится едва ли 3%, заболевает им 9-10 человек из 100 тысяч. В последнее десятилетие частота рака пищевода практически не увеличивается, но и не уменьшается. Опухоль, как правило, развивается у 65-летних мужчин, у женщин на 4 года позже. Это преимущественно мужская патология — женщины болеют в 3.5 раза реже, поскольку ведущая причина развития рака — небрежение собственным здоровьем.
Ранний опухолевый процесс без метастазов в лимфоузлы обнаруживается всего лишь у каждого пятого, подавляющее большинство приходит к врачу с распространенным процессом, когда радикальное лечение технически не выполнимо. Возможности хирургии ограничены даже при 1-2 стадии рака, потому что рядом с пищеводной трубкой располагаются трахея, дуга аорты, грудной проток и сердце, а сформированный из желудка или толстой кишки «новый» орган трудно приживается.

Причины развития опухоли
Доказана связь злокачественных процессов в слизистой оболочке пищевода с постоянным раздражающим действием горячей пищи или токсичных продуктов, к примеру, жевательных наркотиков — наса или бетеля. На пищеводном здоровье отражаются курение и алкоголь, под их влиянием поддерживается хроническое воспаление слизистой с усиленной пролиферацией и развитием дисплазии.
Высока вероятность злокачественного новообразования при частой сегодня ГЭРБ из-за грыжи пищеводного отверстия диафрагмы. симптом которой — заброс содержимого желудка в пищевод. Недостаточность замыкания пищеводно-желудочного мышечного жома приводит к постоянному забросу едкого из-за соляной кислоты желудочного содержимого и хроническому воспалению — эзофагиту с переходом через стадию дисплазии в рак.
Вероятность рака возрастает в 30 раз при смещении слизистой желудка в нижний пищеводный отдел, что именуется пищеводом Барретта и считается предраковым процессом.
Классификация и стадии
Самый частый морфологический вариант опухоли пищевода — плоскоклеточный рак, железистый или аденокарцинома встречается только в 3-5% случаев, другие клеточные варианты крайне редки.
Анатомически пищевод подразделяется на два отдела: шейный и грудной, последний дополнительно делят на верхний, средний и нижний. По частоте развития рака лидирует зона перехода пищевода в желудок — там формируется почти половина всех новообразований, в средней части — чуть больше трети карцином, остальное — в шейном отделе.
Разделение по стадиям рака следующее:
- 0 стадия — дисплазия высокой степени или уже карцинома in situ высокой степени дифференцировки;
- 1 стадия рака всегда без метастазов в лимфоузлы, подгруппа «1А» — малая агрессивность (высокая дифференцировка) клеток, при минимальном поражении слизистой оболочки, стадия усугубляется до «1В» при той же степени злокачественности с большей глубиной проникновения в толщу стенки или при такой же поверхностной опухоли, но большей злокачественности;
- 2 стадия «А» — это глубокое поражение стенки и низкая агрессивность в верхнем и среднем отделах грудной части пищевода или в нижней части рак умеренной и низкой дифференцировки. Высокая агрессивности при том же распространении карциномы в верхнем и среднем отделе пищеводной трубки — уже «2В» стадия, а также меньшая глубина вовлечения стенки с поражением 1-2 лимфоузлов;
- 3 стадия карциномы с тремя подкатегориями от «А» до «С» всегда предполагает метастазы в лимфоузлах или вовлечение в конгломерат рядом располагающихся органов;
- 4 стадия устанавливается при любом местном процессе разной агрессивности с прорастанием метастазов в другие органы.

Особенности рака пищевода на 4 стадии
Рак пищевода 4 стадии проявляется обширным опухолевым поражением пищевода и соседних органов при небольшом числе метастазов в других органах.
Злокачественный процесс в пищеводе распространяется поэтапно. Первоначально раковая опухоль разрастается по пищеводным стенкам, сужая просвет, затем проникает в средостение и вовлекает его органы. Далее присоединяется распространение по лимфатическим сосудам, довольно поздно клетки разносятся кровью, поэтому отдаленные метастазы находят, как правило, при существенном поражении органа и вовлечении соседних структур средостения. Отдаленные метастазы чаще появляются в печени, редко в легочной ткани, костях и мозге.
Симптомы
На ранней стадии рака симптомов практически нет, первые признаки болезни появляются при существенном сужении пищеводной трубки. Часто на симптом сужения — дисфагию не обращают внимания, проталкивая застревающие кусочки еды большим количеством жидкости. Трудности с прохождением пищи тянутся несколько месяцев, пациент ограничивает себя в еде и худеет. Дисфагии сопутствует обильная выработка слюны, позже присоединяется гнилостный запах изо рта из-за застоя пищи над сужением и рвота только что съеденным. Проходимость может улучшиться при распаде опухоли, сузившей просвет.
Прорастание в трахею проявится кашлем с мокротой, содержащей частички пищи. На этом этапе присоединяется высокая температура и симптомы воспаления бронхолегочной системы.
Диагностика
- Первое исследование — эндоскопия пищевода (ЭГДС) с биопсией опухоли.
- Эндо-УЗИ (эндосонография) позволит определить степень поражения пищеводной стенки и расположенных рядом органов и лимфатических узлов.
- Рентген пищевода с барием выявит свищи в трахею.
- КТ грудной полости покажет локализацию метастазов в лимфоузлах и вовлечение в конгломерат соседних структур.
- КТ брюшной полости поможет найти метастазы.
- Бронхоскопия показана при подозрении на вовлечении в опухолевый процесс трахеи и бронхов, во время исследования можно пропунктировать подозрительные на рак лимфоузлы.
- При любых сомнениях в распространенности заболевания необходима МРТ. Вся визуализация обязательно выполняется с контрастом.

Лечение
Без хирургии нет радикального лечения, дефект пищевода замещается отрезком толстой кишки или созданной из желудка трубкой, при метастазах в лимфоузлы до или после проводится химиотерапия.
При невозможности операции единственный выход — облучение с химиотерапией.
При 4 стадии основной метод воздействия — химиотерапия. При выраженной дисфагии до химиотерапии стентом или лазером восстанавливают проходимость пищевода. При плохом самочувствии ограничиваются активной симптоматической терапией.
Прогноз
При минимальном раке 100% выживаемость, при 1 стадии заболевания 5 лет проживает 85%.
Только каждый 5 пациент с 2-3 стадиями карциномы переживет пятилетку, дополнение операции химиотерапии увеличивает группу до 27%. Такие же результаты дает химиолучевое лечение.
Добиться положительных результатов лечения карциномы пищевода на поздних стадиях — крайне сложно, основное направление повышения выживаемости — раннее обнаружение опухоли при эндоскопическом обследовании, а также модификация образа жизни при эзофагите и ГЭРБ. Специалисты нашей Клиники знают, как повысить качество диагностики и помочь при предраковых процессах, какая химиотерапия даст наилучший результат.

Онкологические заболевания органов пищеварения являются частой причиной смерти среди пациентов старше 50 лет. Ранние стадии болезни часто имеют бессимптомное течение, поэтому злокачественные опухоли обнаруживают уже во время метастазирования. Плоскоклеточный рак пищевода является распространенным вариантом онкологии желудочно-кишечного тракта.
Что такое плоскоклеточный рак пищевода?
В медицинской литературе раком пищевода называют онкологическое заболевание, характеризующееся ростом злокачественной опухоли в области эпителия пищевода. Значительная опасность такой патологии обусловлена бессимптомным течением на ранних стадиях и быстрым метастазированием. Низкодифференцированный плоскоклеточный рак пищевода, развивающийся в плоском эпителии, отличается более агрессивным течением.
Основные типы патологии:
- Неороговевающий плоскоклеточный рак пищевода – наиболее распространенный тип опухоли. Характеризуется обильным выделением слизи и нарушением глотания.
- Плоскоклеточный ороговевающий рак пищевода. Такой вариант опухоли обуславливает изменение особенностей пораженного эпителия. Появление рогового слоя способствует нарушению функций клеток слизистой оболочки.
Также в классификации патологии учитывают степень дифференцировки злокачественных клеток. Чем менее клетки дифференцированы, тем быстрее растет опухоль, и распространяются метастазы. Это объясняется тем, что малодифференцированные эпителиальные клетки легко распространяются в другие ткани.
Опухоль может появляться в любой части пищевода, но, как правило, это верхняя часть органа. При этом врачам не всегда удается установить причину возникновения аномального роста клеток. Предполагается, что злокачественный процесс может быть спровоцирован первичными болезнями органов ЖКТ и генетическими факторами.
Анатомические особенности
Пищевод относится к среднему отделу пищеварительного тракта, соединяющему ротоглотку с желудком. Это полая длинная трубка (до 30 см), начинающаяся в шейной области и соединяющаяся с желудком в брюшной полости. Практически сразу после проглатывания пищевая масса попадает в пищевод и желудок. К функциям пищевода относят быстрое перемещение пищи в желудочно-кишечный тракт.
Внутренняя оболочка пищевода образована плоскими эпителиальными клетками, выделяющими слизь для быстрого прохождения пищевых субстратов. Эпителий этого отдела пищеварительного тракта не подготовлен для воздействия агрессивной среды желудка, поэтому в нижней части пищевод изолирован сфинктером. Так, пища в норме передвигается только в сторону желудка, после чего пищеводный сфинктер закрывается.
Недостаточность нижнего пищеводного сфинктера является основной причиной гастроэзофагеальной рефлюксной болезни. При этом из-за неполного закрытия сфинктера кислый желудочный сок попадает в полость пищевода и повреждает плоский эпителий. Длительное воздействие рефлюксной болезни может быть причиной злокачественного перерождения клеток.
Возможные причины и факторы риска
Причины озлокачествления нормальных клеток эпителия не всегда ясны. В норме клеточный цикл контролируется с помощью участков ДНК, ответственных за деление и функциональную активность эпителиоцитов. Строгая регуляция определяет частоту делений клеток, благодаря чему поверхность пищевода периодически обновляется. При воздействии негативных факторов на эпителий клетки начинают видоизменяться. Отдельные клетки начинают делиться бесконтрольно и формировать злокачественную массу, растущую вглубь стенки пищевода и в просвете органа. Иммунная система не всегда справляется со своевременным уничтожением злокачественных элементов.
Плоскоклеточный рак пищевода обычно формируется под воздействием негативных факторов. Опухоль редко является следствием влияния одного заболевания. К самым распространенным факторам риска относят:
- Гастроэзофагеальная рефлюксная болезнь.
- Курение и алкоголизм.
- Наличие предраковых изменений в эпителии (пищевод Барретта).
- Травма пищевода в результате проглатывания острых предметов или оперативного вмешательства.
- Постоянное воздействие слишком острой или горячей пищи.
- Химический ожог эпителия.
- Наличие желчного рефлюкса.
- Ожирение и малоактивный образ жизни.
- Неправильное питание.
- Прохождение лучевой терапии при онкологии органов грудной клетки или живота.
- Генетические мутации.
- Онкология в семейном анамнезе.
- Воспалительные заболевания пищевода.
Перечисленные факторы увеличивают вероятность возникновения болезни, но, как правило, не обуславливают рост опухоли напрямую. Наличие факторов риска должно быть поводом для регулярных скрининговых исследований.
Симптомы и признаки
Как уже было сказано, плоскоклеточный рак пищевода может в течение длительного времени иметь бессимптомное течение. Неприятные ощущения и объективные признаки онкологии обычно появляются при значительном увеличении злокачественной массы и распространении метастазов в другие органы. При этом на ранних стадиях пациент может жаловаться на проявление болезней-предшественников онкологии. Так, например, люди с онкологией пищевода нередко жалуются на постоянную изжогу и трудности с глотанием.
- Необъяснимый дефицит массы тела.
- Различные нарушения процесса пищеварения.
- Боли в загрудинной области, изжога.
- Болезненное затрудненное глотание.
- Приступы удушья во время приема пищи.
- Тошнота и рвота.
- Постоянная усталость.
При появлении перечисленных симптомов рекомендуется обратиться к врачу для прохождения всех необходимых диагностических исследований. Пациенты с рефлюксной болезнью, воспалением пищевода и другими факторами риска должны постоянно проходить обследования для исключения злокачественного роста.
Методы диагностики

При появлении симптомов, указывающих на патологию пищевода, необходимо обратиться к гастроэнтерологу. Врач узнает о жалобах, изучит анамнез для обнаружения факторов риска и проведет физическое обследование. Такой диагноз, как плоскоклеточный рак пищевода, ставится на основе инструментально-лабораторной диагностики, поэтому гастроэнтеролог направит пациента для прохождения необходимых тестов.
- Эндоскопическое исследование пищевода. Для этого врач вводит в ротовую полость пациента гибкую трубку, оснащенную камерой и источником света. Постепенное перемещение камеры в область пищевода позволяет оценить состояние эпителия. Также может быть проведена полноценная гастроскопия, включающая осмотр желудка и начального отдела тонкой кишки, для обнаружения причины поражения пищевода.
- Биопсия – забор участка эпителия пищевода для последующего гистологического исследования. Обычно биопсия производится во время эндоскопического исследования. По результатам такой процедуры врач может определить тип злокачественной опухоли.
- Эндоскопическая ультразвуковая диагностика – визуализация пищевода при введении УЗИ-датчика непосредственно в полость органа.
- Компьютерная и магнитно-резонансная томография – эффективные методы сканирования, позволяющие получать изображения органов в высоком разрешении. Это оптимальный способ поиска очага злокачественного роста.
По результатам всех исследований онколог определит стадию заболевания. Учитывается тип, размер и распространенность опухоли, наличие раковых клеток в лимфатических узлах и метастазирование.
Способы лечения и профилактика
После постановки диагноза, установки типа опухоли и получения результатов дополнительной диагностики онколог определяется со схемой лечения. В первую очередь необходимо устранить злокачественный очаг, восстановить естественную анатомию органа и предотвратить распространение раковых клеток. Наибольшую эффективность показывают хирургические методы лечения.
При незначительном размере опухолевой массы возможен вариант эндоскопической хирургии. В более серьезных случаях, когда опухоль распространилась на лимфатические узлы, требуется открытая операция с удалением части органа и окружающих лимфоидных тканей. После этого может потребоваться реконструкция пищевода с использованием тканей желудка или толстого кишечника. В зависимости от распространенности злокачественного роста может потребоваться частичная резекция желудка.
Другие способы лечения:
-
– введение препаратов, избирательно уничтожающих злокачественные клетки. Как правило, такой метод терапии назначается после операции для профилактики рецидива. Также это может быть единственный вариант лечения при неоперабельной опухоли. К распространенным побочным эффектам химиотерапии относят выпадение волос, тошноту, рвоту и усталость. – уничтожение злокачественных клеточных элементов с помощью рентгеновского излучения. Специальное оборудование прицельно воздействует на определенную анатомическую область для устранения опухоли. Зачастую лучевую терапию используют в комбинации с химиотерапией.
Плоскоклеточный рак пищевода может быть предотвращен с помощью профилактических мер. Врачи рекомендуют отказаться от курения и алкоголя, а также включить в диету больше овощей и фруктов. Своевременное лечение рефлюксной болезни значительно уменьшает вероятность развития болезни.
Таким образом, плоскоклеточный рак пищевода, прогноз при котором зависит от стадии, является опасным вариантом злокачественного роста в органах пищеварения. Своевременное обращение к врачу даже с незначительными симптомами позволяет обнаружить ранний этап роста опухоли или предраковые изменения.
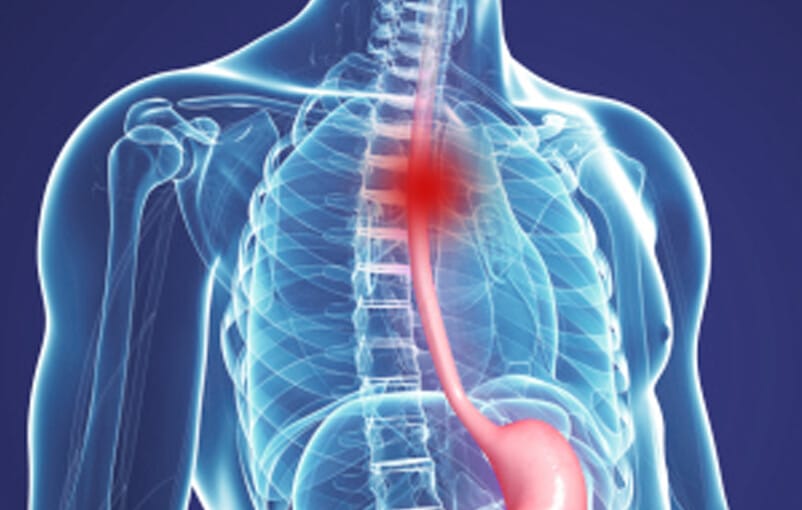
Рак пищевода – злокачественное заболевание, исходящее из его слизистой оболочки. Рак является наиболее частым заболеванием пищевода. Болеют преимущественно мужчины (3:1), у женщин рак пищевода не входит в список 10 наиболее распространённых онкологических заболеваний. Учитывая анатомическую структуру пищевода, самой частой формой рака пищевода в мире является плоскоклеточный рак.
На втором месте — аденокарцинома пищевода — рак, исходящий из железистого эпителия.
Анатомия пищевода
Пищевод представляет собой полую мышечную трубку, которая соединяет глотку и ротовую полость с желудком. Стенка пищевода построена из слизистой оболочки, подслизистой основы, мышечной и адвентициальной оболочек. Мышечная оболочка пищевода состоит из двух слоев: наружного продольного и внутреннего циркулярного. В верхней части пищевода мышечная оболочка образована поперечно-мышечными волокнами. Примерно на уровне одной трети пищевода (считая сверху) поперечно-полосатые мышечные волокна постепенно заменяются гладкомышечными. В нижней части мышечная оболочка состоит только из гладкомышечной ткани.
Слизистая оболочка покрыта многослойным плоским эпителием, в подслизистой оболочке находятся слизистые железы, открывающиеся в просвет органа.
В пищеводе слизистая оболочка кожного типа. Эпителий многослойный плоский неороговевающий, лежит на тонковолокнистой соединительной ткани — собственном слое слизистой оболочки, состоящем из тонких пучков коллагеновых волокон; содержит также ретикулиновые волокна, соединительнотканные клетки. Собственный слой слизистой оболочки вдаётся в эпителий в виде сосочков.
Особенностью пищевода является отсутствие у него серозной оболочки, наружной слой представлен адвентицией, рыхлой соединительной тканью. Лишь в нижней трети пищевод, точнее его абдоминальный отдел, покрыт серозой.
Распространенность рака пищевода
Примерно 80% всех случаев рака пищевода диагностируются в развивающихся странах, где доминирующей гистологической формой является плоскоклеточный рак. В то же время аденокарцинома, за редким исключением, встречается только в индустриально развитых странах.
Для заболеваемости раком пищевода характерна выраженная географическая вариабельность со 100- и более кратной разницей между высшими и низшими показателями. Самая высокая заболеваемость (>150) отмечена в Иране и других странах т.н. Каспийского пояса, а именно, в некоторых районах Туркменистана и Казахстана, прилегающих к Каспийскому морю, а также в Каракалпакии, причем в этих эндемических по раку пищевода регионах заболеваемость высока как среди мужчин, так: и среди женщин. Заболеваемость раком пищевода в Муйнакском районе Каракалпакии составляет 126 – среди мужчин и 150 — среди женщин. Другие очаги высокой заболеваемости – некоторые регионы Китая. Высокая заболеваемость отмечается также в Зимбабве среди чернокожих мужчин (19). В развитых странах относительно высокая заболеваемость раком пищевода (>10) регистрируется во Франции (Кальвадос –17) и в США среди чернокожих мужчин (11).
В России заболеваемость раком пищевода относительно невысока и сравнима с аналогичными показателями в других странах Европы. Однако в некоторых регионах, например в Якутии, заболеваемость раком пищевода значительно выше. Очень высокая частота развития рака пищевода (более 150) отмечается среди малочисленных народов Севера и Дальнего Востока России. Смертность от рака пищевода коррелирует с показателями заболеваемости и имеет те же географические особенности.
Заболеваемость раком пищевода снижается в большинстве стран мира, в том числе и в России. Однако в ряде развитых стран за последние годы наметился рост заболеваемости аденокарциномой кардиального отдела пищевода, которая, но данным ряда канцер-регистров, составляет более 50% всех случаев рака пищевода.
При раке пищевода 5-летняя выживаемость колеблется в пределах 5–12% и остается без изменения в течение двух десятилетий.
Причины и факторы риска
Этиология рака пищевода имеет региональные особенности, а также зависит от локализации и гистологического типа опухоли. Основными факторами риска плоскоклеточного рака пищевода в развитых странах являются курение табака и чрезмерное потребление алкогольных напитков. Для аденокарциномы кардии, наряду с этими двумя факторами, важное значение имеет гастроэзофагеальный рефлюкс, который приводит к постоянному раздражению и повреждению слизистой оболочки кардии, ее метаплазии и дисплазии.
Этиология рака пищевода в регионах с очень высокой заболеваемостью до конца не ясна. Скорее всего, очень высокий риск развития рака пищевода в эндемических регионах, а именно в Иране, Центральной Азии и Китае, связан с дефицитом овощей и фруктов и, соответственно, витаминов и других микроэлементов в питании. Кроме того, предполагают, что риск развития рака пищевода повышен в связи с употреблением очень горячих напитков – чая в Иране и Центральной Азии и мате – в Южной Америке. Высказаны предположения о возможной роли орального потребления некоторых форм табака, например бетеля, а также опия. Рассматривается роль ВПЧ и загрязнения продуктов питания канцерогенными грибами.
Развитее плоскоклеточного рака пищевода связано также с другими его заболеваниями, такими как:
- стриктуры (сужение пищевода) на фоне употребления агрессивных жидкостей или длительного пищеводно-желудочного рефлюкса,
- ахалазия кардии,
- склеродермия,
- синдром Пламмера-Вильсона (развитие пищеводных мембран у женщин с железодефицитный анемией).
У пациентов с таким заболеванием как гиперкератоз (ладоней и стоп), имеющего аутосомно-доминантный тип наследования, к 45 годам плосколеточный рак пищевода развивается у 50% больных, а к 55 годам – у 95%.
Рак пищевода симптомы
Ранние формы рака протекают бессимптомно, поскольку для появления затруднения проглатывания пищи (дисфагии) необходимо сужение просвета пищевода менее 15 мм.
К сожалению, более половины пациентов (60%) к моменту установления диагноза имеют распространённую стадию заболевания.
Основными симптомами при раке пищевода являются:
- Дисфагия.
- Боли при проглатывании пищи.
- Спрыгивание съеденной пищей (регургитация).
- Боли и дискомфорт в грудной клетке.
- Чувство инородного тела в пищеводе.
- Осиплость голоса (при вовлечении в процесс возвратного гортанного нерва).
- Появление увеличенных лимфоузлов на шее.
- Снижение массы тела.
Для плоскоклеточного рака характерно развитие местно-распространённого процесса с вовлечением в опухоль прилегающих жизненно-важных анатомических структур, таких как аорта, трахея, главные бронхи, сердце.
Метастазирование плоскоклеточного рака пищевода происходит лимфогенным путём с развитием отдалённых метастазов в печени, легких, костях.
Диагностика
- Основными диагностическими инструментами у больных плоскоклеточным раком пищевода является рентгенография пищевода с барием (выявление злокачественной стриктуры пищевода, ее протяженности и степени сужения пищевода) и эндоскопическое исследование пищевода и желудка с проведением биопсии новообразования.
- С целью установления стадии заболевания, исключения отдалённых метастазов и оценки местной распространенности процесса необходимо проведение МСКТ органов грудной клетки и брюшной полости с внутривенным контрастированием.
- С целью оценки глубины инвазии опухоли проводят эндосонографическое эндоскопическое исследование (одномоментное проведение эндоскопии и ультразвукового исследования).
- У больных с раком пищевода средней трети необходимо проведение фибробронхоскопиидля исключения вовлечения в опухолевый процесс трахеи и главных бронхов.
- ПЭТ/КТ (с 18F-дезоксиглюкозой) мало информативна для определения состояния первичной опухоли (Т) и регионарных лимфатических узлов (N), но по сравнению с КТ демонстрирует более высокую чувствительность и специфичность в обнаружении отдаленных метастазов; ПЭТ/КТ рекомендуется выполнять в том случае, если у пациента нет отдаленных метастазов по данным КТ.
Классификация
Система стадирования рака пищевода по TNM (UICC, 8‐е издание)
Первичная опухоль
Тх Первичная опухоль не может быть оценена;
Т0 Нет признаков первичной опухоли;
Tis Карцинома in situ/дисплазия высокой степени;
Т1 Прорастание опухоли в собственную пластинку или подслизистый слой;
Т1а Опухоль вовлекает собственную пластинку или мышечную пластинку слизистой оболочки Т1b Опухоль прорастает подслизистый слой;
Т2 Прорастание мышечного слоя;
Т3 Прорастание адвентиции;
Т4 Прорастание прилегающих структур;
Т4а Плевра, брюшина, перикард, диафрагма, вена azygos;
Т4b Прилежащие анатомические структуры: аорта, позвонки, или трахея.
Регионарные лимфатические узлы
Nx Регионарные лимфатические узлы не могут быть оценены;
N0 Нет метастазов в регионарных лимфатических узлах;
N1 Поражение 1–2 регионарных лимфатических узлов;
N2 Поражение 3–6 регионарных лимфатических узлов;
N3 Поражение 7 и более регионарных лимфатических узлов.
Отдаленные метастазы
М0 Отдаленных метастазов нет;
М1 Отдаленные метастазы есть.
Регионарными являются следующие группы лимфатических узлов:
- прескаленные;
- внутренние яремные;
- верхние и нижние шейные;
- шейные околопищеводные;
- претрахеальные (билатеральные);
- лимфатические узлы корня легкого (билатеральные);
- верхние параэзофагеальные (выше v. azygos);
- бифуркационные;
- нижние параэзофагеальные (ниже v. azygos);
- задние медиастинальные;
- диафрагмальные;
- перигастральные (правые и левые кардиальные, лимфатические узлы, вдоль малой кривизны, вдоль большой кривизны, супрапилорические, инфрапилорические, лимфатические узлы вдоль левой желудочной артерии).
Категория pN0 может быть установлена только после лимфодиссекции с патоморфологическим изучением не менее 7 удаленных лимфоузлов (при отсутствии в них метастазов).
Рак пищевода лечение
Основным методом лечения является хирургический. Лишь при невозможности хирургического лечения (отказ пациента или функциональные противопоказания) проводится химиолучевая терапия в самостоятельном варианте.
При росте опухоли в пределах слизистой оболочки (T1) возможно выполнение эндоскопической резекции в пределах слизистой оболочки или подслизистого слоя. Эндоскопическая резекция является методом выбора при РП in situ и при тяжелой дисплазии. Кроме того, метод успешно применяется при опухолях пищевода, не выходящих за пределы слизистой оболочки, у больных, имеющих значительный риск хирургических осложнений. При этом 5-летняя выживаемость достигает 85–100%.
Виды операций
- Основным видом операции при РП является трансторакальная субтотальная резекция пищевода с одномоментной внутриплевральной пластикой стеблем желудка или сегментом толстой кишки с билатеральной двухзональной медиастинальной лимфодиссекцией из комбинированного лапаротомного и правостороннего торакотомного доступов (операция типа Льюиса).
- При локализации опухоли в верхнегрудном или шейном отделах возможно выполнение трансторакальной резекции пищевода с анастомозом на шее (операция типа Мак Кейна).
- В некоторых клиниках в качестве альтернативы выполняются трансхиатальные резекции пищевода, которые не могут претендовать на радикальность. Они не должны применяться у пациентов раком грудного отдела пищевода, поскольку из лапаротомного доступа невозможна адекватная медиастинальная лимфодиссекция выше бифуркации трахеи.
- Другим путем уменьшения частоты хирургических осложнений является минимально инвазивная (торако-лапароскопическая) или гибридная (торакотомия + лапароскопия или торакоскопия + лапаротомия) эзофагэктомия или роботассистированная резекция пищевода.
Выбор метода хирургического лечения при опухоли пищеводно-желудочного перехода определяется ее локализацией согласно классификации Зиверта:
- при I типе выполняется операция Льюиса или операция Гэрлока в зависимости от размеров опухоли, в исключительных случаях (при невозможности торакотомии) – трансхиатальная резекция пищевода;
- при II типе выполняется чресплевральная проксимальная резекция (операция Гэрлока) либо чрезбрюшинная проксимальная резекция с широкой диафрагмотомией и высоким анастомозом в средостении (у соматически отягощенных больных);
- при III типе выполняется чрезбрюшинная проксимальная резекция или гастрэктомия.
При клинической стадии II-III вариантами лечения являются:
- предоперационная ХТ + хирургическое лечение;
- предоперационная химиолучевая терапия + хирургическое лечение;
- хирургическое лечение;
- самостоятельная химиолучевая терапия.
Химио и лучевая терапия
Результаты хирургического лечения РП данных стадий остаются неудовлетворительными, 5 лет переживают лишь около 20% больных. В целях улучшения результатов лечения используются различные сочетания лекарственной и лучевой терапий (предоперационная ХТ, предоперационная химиолучевая терапия, самостоятельная химиолучевая терапия).
При клинической стадии IVa (Т4 или множественные метастазы в регионарных лимфатических узлах средостения) основным методом лечения является самостоятельная химиолучевая терапия. Однако вовлечение перикарда, плевры, легкого и диафрагмы не исключает возможности хирургического лечения в случае объективного ответа на предоперационную терапию.
Основными задачами лечения больных РП с отдаленными метастазами являются улучшение качества жизни путем устранения симптомов, обусловленных ростом опухоли, и увеличение продолжительности жизни. Оценка эффективности различных режимов ХТ этой категории больных затруднена в связи с отсутствием рандомизированных исследований, особенно при плоскоклеточном раке. По этой же причине сложно оценить и тот выигрыш, который дает ХТ по сравнению с симптоматической терапией.
Химиотерапия рекомендуется пациентам в удовлетворительном общем состоянии (по шкале ECOG 0–2 балла) при отсутствии выраженной (III–IV степени) дисфагии, затрудняющей адекватное питание пациента. В последнем случае на первом этапе показано восстановление проходимости пищевода (стентирование, реканализация). При дисфагии I–II степени ХТ позволяет добиться уменьшения степени ее выраженности у ряда больных уже к концу первого курса.
Наиболее эффективными препаратами при обоих гистологических вариантах являются цисплатин, фторпиримидины, таксаны.
При плоскоклеточных раках стандартным режимом ХТ остается комбинация цисплатина с инфузией 5‐фторурацила или капецитабином, частота объективных эффектов при использовании подобных режимов составляется около 35%, а продолжительность жизни не превышает 6–8 мес. Карбоплатин уступает цисплатину по непосредственной эффективности, что ограничивает его применение вне программ химиолучевой терапии.
Применение таксанов возможно в составе двухкомпонентных схем с цисплатином или трехкомпонентных комбинаций (с цисплатином и фторпиримидинами). В последнем случае ценой большей токсичности удается повысить объективный эффект до 48%, однако к удлинению продолжительности жизни это, по-видимому, не приводит.
Паллиативное лечение
Наиболее частым симптомом РП является дисфагия. Необходимость в ее устранении может возникать на всех этапах лечения. Для устранения дисфагии используются различные методы:
- эндоскопические процедуры (баллонная дилатация, электро-, аргонно-плазменная или лазерная деструкция, фотодинамическая терапия),
- лучевая терапия (дистанционная или брахитерапия),
- постановка внутрипросветных стентов.
Эндоскопические процедуры дают быстрый, но кратковременный эффект и подходят в тех случаях, когда в ближайшее время будет начато лечение с предполагаемой высокой эффективностью (хирургическое, лекарственное, лучевое).
В том случаях, когда излечение больного невозможно, оптимальными вариантами коррекции дисфагии является брахитерапия, стентирование пищевода или дистанционная лучевая терапия.
Паллиативная химиолучевая терапия не имеет явных преимуществ по сравнению с ЛТ (без ХТ) и сопряжено с большей токсичностью. По результатам исследования стентирование пищевода позволяет быстрее достичь желаемых эффектов, однако при большем сроке наблюдения в сравнении с брахитерапией частота осложнений (миграция стента, боли, перфорация, желудочно-пищеводный рефлюкс) оказалась выше, а частота полного купирования дисфагии – несколько ниже. При развитии пищеводно-бронхиальных или медиастинальных свищей постановка покрытых стентов позволяет купировать данные осложнения у 70–100% больных.
Наблюдение
Активное наблюдение показано больным для раннего выявления рецидива в пищеводе с целью выполнения хирургического вмешательства либо рецидива в средостении с целью проведения химиолучевой терапии. Объем обследования зависит от стадии болезни и предшествующего лечения:
Стадия I (после эндоскопических резекций слизистого/подслизистого слоя) и стадии II–III (после химиолучевой терапии, имеется перспектива для эзофагэктомии в случае рецидива):
- ЭГДС – каждые 3–4 мес. в течение первых двух лет, каждые 6 мес. – в течение третьего года, далее ежегодно до общей продолжительности наблюдения 5 лет.
- КТ органов грудной клетки и органов брюшной полости – каждые 6 мес. в течение первых 2 лет, далее – ежегодно до общей продолжительности наблюдения 5 лет;
Стадия I–III (после хирургического лечения):
- КТ органов грудной клетки и органов брюшной полости – каждые 6 мес. в течение первых 2 лет, далее – ежегодно до общей продолжительности 5 лет.
Другие методы обследований у остальных категорий пациентов рекомендуется выполнять при наличии клинических показаний. Выполнение ПЭТ/КТ и определение маркеров в сыворотке крови для наблюдения за пациентами не рекомендуется.
Хирургическое лечение в отделении торакоабдоминальной хирургии и онкологии РНЦХ
Лечение в отделении проводится по программам ОМС, ДМС, ВМП, а также на коммерческой основе.
Читайте, как попасть на лечение в отделение торакоабдоминальной хирургии и онкологии РНЦХ.
Для записи на консультацию позвоните по телефонам:
Отправьте заявку на консультацию, заполнив форму на нашем сайте и прикрепив необходимые документы.
Плоскоклеточный рак, или плоскоклеточная карцинома – это гистологический тип злокачественных опухолей, такой диагноз устанавливают по результатам биопсии после исследования образца опухолевой ткани под микроскопом. Новообразование формируется из плоских клеток эпидермиса, которые выглядят как чешуйки. Оно может возникать на коже, в полости рта, в гортани, трахее, бронхах, пищеводе, на половых органах, в прямой кишке.
В «Евроонко» диагностикой и лечением плоскоклеточного рака занимаются врачи экспертного уровня, за плечами которых обширный опыт работы в ведущих онкологических центрах Москвы. С пациентом работает команда, в которую входят онкологи, дерматоонкологи, хирурги, химиотерапевты, радиотерапевты и другие специалисты. Мы применяем инновационные методы лечения, препараты последнего поколения, проводим противоопухолевую терапию в соответствии с ведущими международными рекомендациями. «Евроонко» – первый российский частный онкологический центр, в котором можно получить эффективное паллиативное лечение на поздних стадиях, даже в случаях, когда от пациента отказались в других клиниках.
Причины возникновения плоскоклеточного рака
Причины плоскоклеточного рака те же, что и для других типов злокачественных опухолей. В клетках происходят определенные мутации, которые приводят к злокачественному перерождению. «Неправильные» клетки утрачивают внешние черты и функции нормальных, начинают бесконтрольно размножаться, приобретают способность распространяться в организме.
Основные факторы риска плоскоклеточного рака:
- На коже такие опухоли часто возникают из-за действия ультрафиолетовых лучей. Наиболее уязвимы открытые участки тела.
- Плоскоклеточный рак половых органов, головы и шеи вызывают некоторые типы вируса папилломы человека.
- Риск развития плоскоклеточного рака повышен у курильщиков и людей, которые употребляют много алкоголя.
- Вероятность развития онкологического заболевания повышается с возрастом, так как в клетках тела накапливаются мутации.
- Шрамы, ожоги, хронический воспалительный процесс.
- Воздействие некоторых канцерогенных веществ, например, если человек работает на производстве и контактирует с химикатами.
- Снижение иммунитета.
Ни один из этих факторов не приводит гарантированно к заболеванию – каждый из них лишь в определенной степени повышает вероятность.
Какие бывают виды плоскоклеточного рака?
Злокачественные новообразования данного гистологического типа встречаются на разных частях тела. В зависимости от локализации, могут несколько различаться их свойства, подходы к диагностике и лечению, прогноз для пациента.

Рак кожи
Злокачественные опухоли кожи представлены плоскоклеточным раком примерно в 20% случаев. Намного чаще пациенты страдают базальноклеточным раком, который происходит из клеток, находящихся в нижнем слое эпидермиса.
Плоскоклеточный рак более агрессивен по сравнению с базальноклеточным. Он с большей вероятностью прорастет в глубокие слои кожи, будет распространяться в организме с образованием отдаленных метастазов. Тем не менее, это происходит довольно редко. Чаще всего опухоль удается обнаружить и удалить на ранней стадии.
Как правило, плоскоклеточный рак возникает на коже лица, ушей, шеи, тыльной стороне рук, реже – в области половых органов. Нередко новообразование развивается там, где находятся шрамы и хронические повреждения.
Плоскоклеточный рак красной каймы губ
Злокачественные опухоли губ составляют не более 1–3% от всех онкологических заболеваний. В большинстве случаев (95%) они представлены плоскоклеточным раком, который бывает двух типов:
- Плоскоклеточный ороговевающий рак ведет себя не так агрессивно, медленно растет, редко образует отдаленные метастазы.
- Плоскоклеточный неороговевающий рак растет быстро, раньше приводит к изъязвлению и чаще метастазирует.
Исследования показывают, что у мужчин этот тип рака встречается в 3–13 раз чаще, чем у женщин. Вероятно, это связано с тем, что представители мужского пола чаще подвергаются воздействию солнечных лучей на рабочем месте, среди них более распространено курение, употребление алкоголя.
Рак полости рта
Раком ротовой полости называют злокачественные опухоли, которые возникают на слизистой оболочке губ, щек, десен, передних двух третей языка, неба, дна ротовой полости (находится под языком). В 90% случаев они представлены плоскоклеточным раком, из них 5% – плоскоклеточный ороговевающий рак, который менее агрессивен, реже прорастает в окружающие ткани, распространяется в лимфатические узлы и метастазирует.
Рак пищевода
Слизистая оболочка пищевода выстлана многослойным плоским эпителием, и из него может развиваться плоскоклеточный рак. Чаще всего такие опухоли находятся в шейном отделе пищевода и верхних двух третях грудного отдела. В нижней трети органа чаще встречаются аденокарциномы – злокачественные опухоли из железистых клеток.
Рак гортани
При раке гортани опухоль практически всегда развивается из плоского эпителия и представляет собой плоскоклеточную карциному. Обычно возникновению опухоли предшествуют предраковые изменения – дисплазия. Клетки, которые находятся в очаге, внешне не похожи на нормальные, но отличаются и от раковых. В ряде случаев дисплазия не приводит к развитию рака и даже проходит самостоятельно, особенно если устранена ее причина, например, человек бросил курить. Но у некоторых людей предраковые изменения приводят к возникновению «рака на месте» (in situ), а затем инвазивной опухоли.

Рак трахеи и бронхов
Плоскоклеточный рак – наиболее распространенный тип злокачественных опухолей в трахее. Обычно он возникает в нижней части трахеи, довольно быстро растет, прорастает ее стенку, приводит к изъязвлениям и кровотечению. Это редкий тип рака, его основной причиной является курение.
Наиболее распространенным раком легкого является немелкоклеточный рак – он встречается в 80% случаев и в 30% случаев представлен плоскоклеточной карциномой. Нередко эти опухоли находятся в бронхах.
Рак шейки матки
Шейка матки состоит из двух частей. Экзоцервикс находится снаружи, во влагалище, это то, что видит гинеколог во время осмотра. Эндоцервикс – канал шейки матки, он соединяет матку с влагалищем. В норме экзоцервикс выстлан плоским эпителием, а эндоцервикс – железистым. Место, где они встречаются, называется зоной трансформации.
Плоскоклеточным раком представлены 90% злокачественных опухолей шейки матки. Чаще всего новообразование возникает в области зоны трансформации. Раки, которые развиваются из железистых клеток эндоцервикса, называются аденокарциномами.
В редких случаях в шейке матки встречается железисто-плоскоклеточный рак.
Рак вульвы
Вульвой называют наружные женские половые органы: преддверие влагалища, большие и малые половые губы, клитор. Большинство типов рака, которые развиваются в этой области, представлены плоскоклеточным раком (70–90%). Они делятся на две группы:
- Большая группа – опухоли, происхождение которых неизвестно. Чаще всего их диагностируют у женщин старшего возраста.
- Меньшая группа – злокачественные опухоли, вызванные вирусом папилломы человека.
Рак прямой кишки
В большинстве случаев злокачественные опухоли прямой кишки представлены аденокарциномами – железистым раком. Плоскоклеточный рак в этом органе встречается очень редко и составляет от 10 до 25 случаев на каждые 100 тысяч случаев колоректального рака.
Плоскоклеточный рак составляет 90% от всех злокачественных новообразований анального канала – узкого прохода, который соединяет прямую кишку с анусом.
Рак миндалин
У человека есть четыре вида миндалин: небные (при их воспалении развивается тонзиллит), трубные (находятся в глотке возле отверстий слуховых труб), язычная (позади языка) и глоточная (у детей из-за нее бывают аденоиды). Чаще всего злокачественные опухоли развиваются в небных миндалинах. В большинстве случаев это плоскоклеточный рак. Его сложно диагностировать, поэтому зачастую он выявляется на поздних стадиях.

Виды диагностики заболевания
Врач-онколог назначает пациенту те или иные виды диагностики, в зависимости от того, в каком органе находится злокачественная опухоль:
Место локализации рака
Методы диагностики
- Осмотр дерматолога.
- Дерматоскопия.
- В «Евроонко» применяется современная дерматоскопическая установка — ФотоФайндер. Она позволяет составить «карту родинок» и выявить мельчайшие изменения на коже.
- Осмотр ЛОР-врача.
- Фарингоскопия.
- Ларингоскопия.
- Бронхоскопия.
- Эзофагоскопия.
- Исследование на ВПЧ.
- Эндоскопическое исследование, в том числе эндоУЗИ.
- Рентгенография с контрастным усилением.
- КТ, МРТ.
- Рентгенография грудной клетки.
- Бронхоскопия.
- Осмотр гинеколога
- Осмотр гинеколога.
- Кольпоскопия.
- Осмотр врача-проктолога.
- Проктоскопия.
- Колоноскопия.
- Анализ кала на скрытую кровь.
Во всех случаях, когда обнаружено патологическое образование, проводят биопсию – исследование, во время которого получают фрагмент подозрительной ткани и отправляют в лабораторию для гистологического и цитологического исследования. Биопсия – самый точный метод диагностики рака. Она помогает не только достоверно установить диагноз, но и определить гистологический тип новообразования.Для того чтобы проверить степень распространения рака в организме и уточнить стадию, врач может назначить дополнительные исследования:
- компьютерную томографию, МРТ;
- рентгенографию грудной клетки, костей;
- ПЭТ-сканирование;
- УЗИ и эндоскопические исследования органов, в которые мог прорасти рак.
Лечение плоскоклеточного рака
Лечение зависит от локализации, стадии рака, общего состояния пациента, наличия у него сопутствующих заболеваний и других факторов.
Лучевая терапия
Ионизирующее излучение повреждает опухолевые и другие быстро размножающиеся клетки. Этот вид лечения плоскоклеточного рака может быть назначен до или после операции, либо на поздних стадиях в паллиативных целях.

Хирургия
Радикальные операции возможны, если нет метастазов, и не произошло сильное прорастание рака в окружающие ткани. В одних случаях таким пациентам показано только хирургическое лечение, в других его дополняют противоопухолевыми препаратами, лучевой терапией – это помогает снизить риск рецидива.
При запущенном плоскоклеточном раке может быть выполнено паллиативное хирургическое вмешательство, направленное на ликвидацию симптомов, восстановление проходимости и функции пораженного органа.
Медикаментозное лечение плоскоклеточного рака
Химиотерапия при плоскоклеточном раке может быть адъювантной (после операции), неоадъювантной (до хирургического вмешательства) или применяется в качестве самостоятельного метода лечения на поздних стадиях.
Если опухоль обладает определенными молекулярно-генетическими характеристиками, назначают таргетную терапию. Таргетные препараты прицельно воздействуют на молекулы, которые помогают раку расти и поддерживать свою жизнедеятельность.
Врачи «Евроонко» применяют при плоскоклеточном раке оригинальные противоопухолевые препараты последнего поколения, назначают их в соответствии с современными международными протоколами.
Симптоматическое лечение при плоскоклеточном раке
Лечение при плоскоклеточном раке и любых других злокачественных новообразованиях должно быть направлено не только на борьбу с самой опухолью, но и на купирование симптомов, улучшение состояния пациента. В «Евроонко» пациент может получить все виды симптоматической терапии при раке:
- Купирование болевого синдрома в соответствии с трехступенчатой схемой ВОЗ.
- Восстановление проходимости пищевода, кишечника, дыхательных путей.
- Устранение кровотечений, при необходимости – переливание крови.
- Купирование тошноты.
- Устранение сдавления опухолью внутренних органов, нервов, сосудов.
- Лечение экстренных состояний в условиях палаты интенсивной терапии, оснащенной современной аппаратурой.
- Контроль и коррекция нутритивного статуса.
- Поддерживающая терапия помогает комфортно перенести курс химиотерапии, предотвратить и купировать побочные эффекты.

Прогноз выживаемости при плоскоклеточном раке
Прогноз зависит от того, в каком месте начался рост рака, на какой стадии установлен диагноз и начато лечение. Например, зачастую выживаемость при раке кожи и красной каймы губ стремится к 100%, потому что такие опухоли, как правило, удается обнаружить достаточно рано, и они не очень агрессивны. Если появились отдаленные метастазы, шансы на ремиссию становятся крайне низкими. Но таким пациентам все еще можно помочь: затормозить прогрессирование плоскоклеточного рака, продлить жизнь, улучшить общее состояние, купировать мучительные симптомы.
Мы в «Евроонко» считаем, что безнадежных больных не бывает. Помочь можно всегда. Никогда не стоит сдаваться. Мы знаем, как помочь.

Аденокарцинома пищевода – форма рака, при которой раковые клетки развиваются из железистых, продуцирующих слизь клеток. Болезнь обычно развивается в нижней трети, в области желудочно-пищеводного перехода.
Рак пищевода является одним из самых агрессивных злокачественных новообразований и занимает восьмое место в структуре смертности в мире. Наиболее частыми морфологическими формами являются плоскоклеточный рак (95%) и аденокарцинома (3%). Крайне редко встречаются, карциносаркома, мелкоклеточный рак и меланома. По расчётам Росстата Минздрава РФ заболеваемость среди мужчин и женщин составляет 7.6 и 2.4 случая на 100 тыс. населения соответственно.
Аденокарцинома считается одной из быстро распространяющихся форм рака пищевода в странах Северной Америки и Европы, в то время как плоскоклеточный рак преобладает в развивающихся странах. Это связано с реализацией факторов риска развития данных форм рака пищевода.
Факторы риска
- Пищевод Барретта – заболевание, при котором нормальный плоскоклеточный эпителий пищевода замещается железистыми клетками. Этот процесс называется кишечная метаплазия и развивается в результате хронического агрессивного воздействия желудочного сока на слизистую пищевода у пациентов с гастроэзофагеальной рефлюксной болезнью и грыжами пищеводного отверстия диафрагмы.
- Ожирение.
- Ахалазия кардии и кардиоспазм.

Фото. Эндоскопическая картина при пищеводе Барретта
Классификация
T
- Tis карцинома in situ/дисплазия высокой степени;
- Т1 прорастание опухоли в собственную пластинку или подслизистый слой:
- Т1а собственная пластинка или мышечная пластинка слизистой оболочки;
- Т1b подслизистый слой.
- Т4а плевра, брюшина, перикард, диафрагма;
- Т4b – прилежащие органы: аорта, позвонки, трахея.
N
- N0 нет метастазов в регионарных лимфоузлах;
- N1 поражение 1-2 регионарных лимфоузлов;
- N2 поражение 3-6 регионарных лимфоузлов;
- N3 поражение 7 и свыше регионарных лимфоузлов.
М
- М1 наличие отдаленных метастазов.
Регионарными являются следующие группы лимфатических узлов:
- прескаленные,
- внутренние яремные,
- верхние и нижние шейные,
- шейные околопищеводные,
- надключичные (билатеральные),
- претрахеальные (билатеральные),
- лифоузлы корня легкого (билатеральные),
- верхние параэзофагеальные (выше v. azygos),
- бифуркационные,
- нижние параэзофагеальные (ниже v. azygos),
- задние медиастинальные,
- диафрагмальные,
- перигастральные (правые и левые кардиальные, лимфоузлы вдоль малой кривизны желудка, вдоль большой кривизны желудка, супрапилорические, инфрапилорические, лимфоузлы вдоль левой желудочной артерии).
Поражение чревных лимфоузлов не является противопоказанием к проведению химиолучевой терапии и решению вопроса об оперативном лечении.
Степень дифференцировки опухоли
GX – степень дифференцировки опухоли не может быть определена;
G1 – высокодифференцированная опухоль;
G2 – умеренно дифференцированная опухоль;
G3 – низкодифференцированная опухоль;
G4 – недифференцированная опухоль.
В классификации аденокарциномы пищевода выделяют кардиоэзофагеальный рак, т.е. рак, развивающийся в области пищеводно-желудочного перехода и кардии.
Классификация Зиверта
Аденокарцинома пищеводно-желудочного перехода, согласно классификации Зиверта, подразделяется на 3 типа:
I тип – аденокарцинома дистального отдела пищевода (часто ассоциируется с пищеводом Баррета), центр опухоли расположен в пределах 1–5 см выше кардии (зубчатой линии);
II тип – истинная аденокарцинома зоны пищеводно-желудочного пере хода (истинный рак кардии), центр опухоли расположен в пределах 1 см выше и 2 см ниже кардии (зубчатой линии);
III тип – рак с локализацией основного массива опухоли в субкардиальном отделе желудка в пределах 2–5 см ниже зубчатой линии и возможным вовлечением дистальных отделов пищевода.
Опухоли пищеводно-желудочного перехода I и II типа подлежат лечению согласно алгоритмам, соответствующим РП. Опухоли III типа подлежат лечению согласно алгоритмам, соответствующим раку желудка.
Классификация рака пищеводно-желудочного перехода по Siewert
Классификация аденокарциномы пищевода по стадиямКлиническая картина и симптомы
Ранние стадии аденокарциномы пищевода при отсутствии сужения просвета пищевода часто протекают бессимптомно и являются случайной находкой при проведении эндоскопического исследования в связи с другими заболеваниями пищевода или обследовании. Отдельно следует обратить внимание на проведение планового динамического эндоскопического исследования у пациентов с гастроэзофагеальной рефлюксной болезнью и пищеводом Барретта, входящими в группу риска по развитию аденокарциномы пищевода.
При развитии опухоли, суживающей просвет пищевода (обычно, при сужении менее 15 мм), основным клиническим проявлением является синдром дисфагии, который включает в себя:
- Затруднение при проглатывании пищи, застревание пищи в пищеводе (дисфагия);
- Немотивированное снижение массы тела на фоне уменьшения питания;
- Срыгивание (регургитация) съеденной пищей;
- Чувство давления и дискомфорта в грудной клетке;
- Боли при проглатывании пищи (редко);
- Слюнотечение (редко).
К признакам распространенного заболевания относятся:
- Прогрессирующая дисфагия (от затруднения при проглатывании твердой пищи до невозможности проглотить жидкости и слюну);
- Значительное снижение массы тела вплоть до развития кахексии (крайнего истощения);
- Лихорадка;
- Боли в костях;
- Одышка;
- Загрудинная боль или боль в спине;
- Признаки кровотечения из желудочно-кишечного тракта (рвота с кровью, черный стул (мелена), анемия в общем анализе крови).
Диагностика заболевания
Оптимальный план обследования для постановки диагноза, определения клинической стадии и выработки лечебного плана должен включать в себя следующие процедуры:
- Основным методом диагностики является эзофагогастродуоденоскопия. Она позволяет получить материал для морфологического подтверждения диагноза, а также оценить распространенность первичной опухоли по пищеводу. С целью повышения информативности метода в настоящее время могут применяться такие методики, как хромоэндоскопия, эндоскопия в узко-спектральном пучке света, аутофлюоресценция.
- Эндосонография (Эндо-УЗИ) является наиболее информативным методом в оценке глубины инвазии опухоли в стенку пищевода (символ Т). Также она позволяет с высокой точностью (чувствительность 0,8 и специфичность 0,7) оценить состояние регионарных лимфоколлекторов. Для более точного предоперационного стадирования и определения тактики лечения возможно выполнение пункционной биопсии медиастинальных лимфатических узлов.
- Рентгеноконтрастное исследование пищевода.
Рентгенография пищевода с барием у больного раком пищевода
![рентген рак пищевода]()
- КТ органов грудной клетки и брюшной полости с внутривенным контрастированием. Выполняется для оценки состояния регионарных лимфоузлов и исключения отдаленных метастазов. По сравнению с эндо-УЗИ она обладает меньшей чувствительностью (0,5), но большей специфичностью (0,83) в диагностике регионарных метастазов. Для отдаленных метастазов этот показатель составляет 0,52 и 0,91 соответственно.
- Совмещенная позитронно-эмиссионная компьютерная томография с 18F дезоксиглюкозой (ПЭТ/КТ) малоинформативна для определения T и N-статуса. Но она демонстрирует более высокую чувствительность и специфичность в обнаружении отдаленных метастазов по сравнению с КТ. ПЭТ/КТ рекомендуется выполнять в случае, если у пациента по данным КТ нет отдаленных метастазов (М1).
- Фибробронхоскопия выполняется для исключения инвазии в трахею и главные бронхи при опухолях пищевода, расположенных на уровне или выше ее бифуркации.
При подготовке к хирургическому лечению с целью оценки функционального статуса по показаниям проводят дополнительные функциональные тесты: эхокардиографию, холтеровское мониторирование, исследование функции внешнего дыхания, УЗДГ сосудов, исследование свёртывающей системы крови, анализы мочи, консультации врачей-специалистов (кардиолога, эндокринолога, невропатолога и т.п.).
Хирургическое лечение
Показаниями к проведению хирургического лечения являются локализованные (ранние) формы рака пищевода без поражения окружающих структур: I-IIA (Т1-3N0M0). Также операция показана с высокой степенью дисплазии при пищеводе Барретта, которая рассматривается как cr in situ.
Хирургическое лечение включает проведение:
- Эндоскопической мукозэктомии (удаление слизистой пищевода) при расположении злокачественных клеток в пределах слизистой. Эндоскопическая резекция является методом выбора при carcinoma in situ и при тяжелой дисплазии. Кроме того, метод успешно применяется при опухолях пищевода, не выходящих за пределы слизистой, у больных, имеющих значительный риск хирургических осложнений. При этом 5-летняя выживаемость достигает 85-100%.
- Субтотальную резекцию пищевода с одномоментной пластикой желудочной трубкой или сегментом толстой кишки.
Основным видом операции является трансторакальная субтотальная резекция пищевода с одномоментной внутриплевральной пластикой стеблем желудка или сегментом толстой кишки с билатеральной двухзональной медиастинальной лимфодиссекцией из комбинированного лапаротомного и правостороннего торакотомного доступов (типа Льюиса).
В некоторых клиниках в качестве альтернативы выполняются трансхиатальные резекции пищевода, которые не могут претендовать на радикальность. Они не должны применяться у пациентов раком грудного отдела пищевода, поскольку из лапаротомного доступа невозможна адекватная медиастинальная лимфодиссекция выше бифуркации трахеи.
Другим путем уменьшения числа хирургических осложнений является минимально инвазивная (торако-лапароскопическая) или гибридная (торакотомия+лапаросокопия или торакоскопия + лапаротомия) эзофагэктомия или робот-ассистированная резекция пищевода.
Подробнее про операцию читайте по ссылке. Предупреждаем, что материалы содержат изображения натуралистического характера.
Комбинированное лечение. Химио- и лучевая терапия
Результаты одного хирургического лечения более распространенных стадий остаются неудовлетворительными, 5 лет переживают лишь около 20% больных. В целях улучшения результатов используются различные сочетания лекарственной и лучевой терапий (предоперационная химиотерапия, предоперационная химиолучевая терапия, самостоятельная химиолучевая терапия).
Химиотерапия
А. Предоперационная (неоадъювантная) химиотерапия;
Б. Послеоперационная (адъювантная) химиотерапия.
При аденокарциноме нижнегрудного отдела пищевода или пищеводно-желудочного перехода наиболее оправдано проведение периоперационной химиотерапии, когда 2-3 курса химиотерапии назначаются до операции, а 3-4 курса – после нее. При выявлении гиперэкспрессии HER 2neu в режимы терапии включается трастузумаб в стандартных дозах.
При аденокарциноме нижнегрудного отдела пищевода или пищеводно-желудочного перехода послеоперационная химиотерапия показана, если она проводилась и предоперационно. Адъювантная химиотерапия в самостоятельном виде при аденокарциноме пищевода в настоящее время не рекомендуется.
Лучевая терапия
Проведение одной лучевой терапии (без химиотерапии) до или после хирургического лечения не показано по причине малой эффективности.
А. Предоперационная химиолучевая терапия
Перед химиолучевой терапией возможно проведение 1-2 курсов химиотерапии, что позволяет у большинства больных уменьшить дисфагию и заранее запланировать лучевую терапию.
Хирургическое вмешательство обычно производится через 6-8 недель после завершения химиолучевой терапии.
Оптимальным режимом химиолучевой терапии представляется еженедельное введение паклитаксела и карбоплатина на фоне 5 недель лучевой терапии. Такой предоперационный режим (по сравнению с только хирургией) позволяет достигнуть полного патоморфоза у 23% больных аденокарциномой. Послеоперационная летальность составляет 4%, а 5-летняя выживаемость улучшена с 34% до 47%.
Б. Послеоперационная химиолучевая терапия
Послеоперационная химиолучевая терапия может быть проведена пациентам в удовлетворительном состоянии при наличии микро или макроскопической резидуальной опухоли (после R1 или R2-резекции). Режимы и дозы аналогичные предоперационным.
Самостоятельная химиолучевая терапия
Альтернативой хирургическому лечению операбельных местно-распространенных форм рака пищевода является химиолучевая терапия, которая позволяет достичь сравнимой 5-летней общей выживаемости 20-27%. В прямом сравнительном исследовании самостоятельной химиолучевой терапии на основе цисплатина и инфузии 5-фторурацила и одной операции не было достигнуто достоверных различий в отдаленных результатах, а токсичность и летальность консервативного лечения были значительно ниже.
Во время лучевой терапии проводится химиотерапия, чаще на основе цисплатина и инфузий 5-фторурацила. При наличии выраженной дисфагии, перед началом облучения производят эндоскопическую электрореканализацию пищевода или пункционную микрогастростомию. Химиолучевая терапия нередко осложняется развитием лучевых эзофагитов и усилением степени выраженности дисфагии, что усугубляет нутритивный дефицит пациента и ухудшает переносимость лечения. В таких ситуациях возможен частичный или полный переход на парентеральное питание, постановка временной пункционной микрогастростомы.
Выбор между самостоятельной химиолучевой терапией или хирургическим лечением (с или без предоперационной химиолучевой терапией) зависит от локализации первичной опухоли, функционального состояния больного и опыта хирурга. Так, у сохранных пациентов с локализацией опухоли в средней или нижней трети пищевода предпочтительнее включение в план лечения операции.
При сохранении жизнеспособной опухоли после химиолучевого лечения или местном рецидиве возможно выполнение так называемой «спасительной эзофагэктомии».
Паллиативное лечение неоперабельных больных
Основными задачами лечения пациентов с метастатическим раком пищевода являются устранение болезненных симптомов, увеличение продолжительности жизни.
Оценка эффективности различных режимов химиотерапии рака пищевода затруднена отсутствием рандомизированных исследований. По этой причине даже сложно оценить и тот выигрыш, который дает химиотерапия по сравнению с поддерживающей терапией.
Проведение химиотерапии рекомендуется пациентам в удовлетворительном состоянии и отсутствием выраженной (III-IV) дисфагии, затрудняющей адекватное питание пациента. В последнем случае на первом этапе показано восстановление проходимости пищевода (стентирование, реканализация). При дисфагии I-II степени начало химиотерапии позволяет добиться уменьшения степени ее выраженности у ряда больных уже к концу первого курса.
![Стентирование]()
Стентирование пищевода при раке
Наиболее активными препаратами при обоих гистологических вариантах являются цисплатин, фторпиримидины, таксаны. Кроме того, при аденокарциномах также эффективны оксалиплатин, иринотекан, трастузумаб (при гиперэкспрессии HER-2 neu).
После лечения
Осмотр
Пациенты после радикального лечения (хирургия или химиолучевая терапия) должны осматриваться каждые 3-6 мес. в первые 2 года, далее каждые 6-12 мес. в последующие 3-5 лет, затем ежегодно.
Анализы
Анализы крови и инструментальные обследования назначаются только по клиническим показаниям (появление жалоб или симптомов прогрессирования).
ЭГДС
Пациенты с ранним раком, которые подверглись эндоскопической резекции слизистой, должны выполнять ЭГДС каждые 3 мес. в первый год, каждые 6 мес. на второй и третий годы, далее – ежегодно.
Прогноз
Прогноз при аденокарциноме пищевода определяется стадией заболевания. К сожалению, особенности строения пищевода, высокий риск метастазирования, отсутствие специфической клинической картина на ранних стадиях заболевания, приводят к тому, что 2/3 пациентов к моменту установки диагноза имеют 3 или 4 стадию. Это либо местно-распространенный неоперабельный процесс либо отдаленные метастазы в легких, печени, костях. В данном случае 12-месячная выживаемость составляет лишь 38%.
При локализованных стадиях 5-летняя выживаемость может достигать 47%, при поражении регионарных лимфоузлов – 25%, при наличии отдаленных местастазов не превышает 5%.
Хирургическое лечение в отделении торакоабдоминальной хирургии и онкологии РНЦХ
Лечение в отделении проводится по программам ОМС, ДМС, ВМП, а также на коммерческой основе.
Читайте, как попасть на лечение в отделение торакоабдоминальной хирургии и онкологии РНЦХ.Для записи на консультацию позвоните по телефонам:
Отправьте заявку на консультацию, заполнив форму на нашем сайте и прикрепив необходимые документы.
Читайте также:



