Как лечить трофическую язву бобровой струей
Обновлено: 27.04.2024
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для ингибирования соляной кислоты париетальными клетками слизистой оболочки желудка чаще всего используются блокаторы Н2-рецепторов гистамина второго (ранитидин) и третьего (фамотидин) поколений, несколько реже — ингибиторы протонного насоса (омепразол, рабепразол), а для нейтрализации уже выделенной в полость желудка соляной кислоты — антацидные препараты. Антацидные препараты иногда применяются в лечении больных, страдающих так называемыми «кислотозависимыми» заболеваниями, в сочетании с Н2-блокаторами рецепторов гистамина; иногда в качестве терапии по «требованию» в сочетании с ингибиторами протонного насоса. Одна или две «разжеванные» антацидные таблетки не оказывают значительного эффекта [10] на фармакокинетику и фармакодинамику фамотидина, применяемого в дозе 20 мг.
Между этими медикаментозными препаратами существуют определенные различия, перечислим основные из них: различные механизмы действия; скорость наступления терапевтического эффекта; продолжительность действия; разная степень эффективности их терапевтического действия в зависимости от времени приема препарата и приема пищи; стоимость медикаментозных препаратов [1]. Вышеперечисленные факторы не всегда учитываются врачами при лечении больных.
В последние годы в литературе все чаще обсуждаются вопросы фармакоэкономической эффективности использования в терапии «кислотозависимых» заболеваний различных медикаментозных препаратов, применяющихся по той или иной схеме [2, 7]. Стоимость обследования и лечения больных особенно важно учитывать в тех случаях, когда больные в силу особенностей заболевания нуждаются в продолжительном лечении [4, 6], например при гастроэзофагеальной рефлюксной болезни (ГЭРБ). Это весьма распространенное заболевание, обследование и лечение таких пациентов требуют значительных расходов.
Как известно, у большей части больных ГЭРБ отсутствуют эндоскопические признаки рефлюкс-эзофагита. Однако по мере прогрессирования ГЭРБ появляются патологические изменения слизистой оболочки пищевода. Симптомы этого заболевания оказывают на качество жизни такое же воздействие, что и симптомы других заболеваний, включая и ишемическую болезнь сердца [5]. Замечено [8] отрицательное воздействие ГЭРБ на качество жизни, особенно на показатели боли, психическое здоровье и социальную функцию. У больных, страдающих ГЭРБ, высок риск появления пищевода Барретта, а затем и аденокарциномы пищевода. Поэтому при первых же клинических симптомах ГЭРБ, особенно при возникновении эндоскопических признаков эзофагита, необходимо уделять достаточное внимание своевременному обследованию и лечению таких больных.
В настоящее время лечение больных ГЭРБ проводится, в частности, препаратом фамотидин (гастросидин) в обычных терапевтических дозировках (по 20 мг или по 40 мг в сутки). Этот препарат обладает рядом достоинств: удобство применения (1-2 раза в сутки), высокая эффективность в терапии «кислотозависимых» заболеваний, в том числе и по сравнению с антацидными препаратами [9], а также большая безопасность по сравнению с циметидином. Однако наблюдения показали [1], что в ряде случаев для повышения эффективности терапии целесообразно увеличение суточной дозы гастросидина, что, по некоторым наблюдениям [1], снижает вероятность появления побочных эффектов по сравнению с использованием в повышенных дозах блокаторов Н2-рецепторов гистамина первого (циметидин) и второго (ранитидин) поколений. Преимущество фамотидина [11] перед циметидином и ранитидином заключается в более продолжительном ингибирующем эффекте на секрецию соляной кислоты обкладочными клетками слизистой оболочки желудка.
Существуют и другие преимущества блокаторов Н2-рецепторов гистамина (ранитидина или фамотидина) перед ингибиторами протонного насоса; в частности, назначение этих препаратов на ночь позволяет эффективно использовать их в лечении больных из-за отсутствия необходимости соблюдать определенную «временную» связь между приемом этих препаратов и пищи. Назначение некоторых ингибиторов протонного насоса на ночь не позволяет использовать их на полную мощность: эффективность ингибиторов протонного насоса снижается, даже если эти препараты приняты больными вечером и за час до приема пищи. Однако суточное мониторирование рН, проведенное у больных, лечившихся омезом (20 мг) или фамотидином (40 мг), свидетельствует [3] о том, что продолжительность действия этих препаратов (соответственно 10,5 ч и 9,4 ч) не перекрывает период ночной секреции, и в утренние часы у значительной части больных вновь наблюдается «закисление» желудка. В связи с этим необходим и утренний прием этих препаратов.
Определенный научно-практический интерес вызывает изучение эффективности и безопасности использования фамотидина и омеза (омепразола) в более высоких дозировках при лечении больных, страдающих «кислотозависимыми» заболеваниями верхних отделов желудочно-кишечного тракта.
Нами изучены результаты клинико-лабораторного и эндоскопического обследования и лечения 30 больных (10 мужчин и 20 женщин), страдающих ГЭРБ в стадии рефлюкс-эзофагита. Возраст больных — от 18 до 65 лет. При поступлении в ЦНИИГ у 30 пациентов выявлены основные клинические симптомы ГЭРБ (изжога, боль за грудиной и/или в эпигастральной области, отрыжка), у 25 больных наблюдались клинические симптомы, в основном ассоциируемые с нарушением моторики верхних отделов желудочно-кишечного тракта (чувство быстрого насыщения, переполнения и растяжения желудка, тяжесть в подложечной области), обычно возникающие во время или после приема пищи. Сочетание тех или иных клинических симптомов, частота и время их возникновения, а также интенсивность и продолжительность у разных больных были различными. Каких-либо существенных отклонений в показателях крови (общий и биохимический анализы), в анализах мочи и кала до начала терапии не отмечено.
При проведении эзофагогастродуоденоскопии (ЭГДС) у 21 больного выявлен рефлюкс-эзофагит (при отсутствии эрозий), в том числе у 4 больных обнаружена рубцово-язвенная деформация луковицы двенадцатиперстной кишки и у одного больного — щелевидная язва луковицы двенадцатиперстной кишки (5 больных страдали язвенной болезнью двенадцатиперстной кишки, сочетающейся с рефлюкс-эзофагитом). Кроме того, у одной больной обнаружена пептическая язва пищевода на фоне рефлюкс-эзофагита и у 8 больных — эрозивный рефлюкс-эзофагит. У всех больных, по данным ЭГДС, обнаружена недостаточность кардии (в сочетании с аксиальной грыжей пищеводного отверстия диафрагмы или без нее).
В лечении таких пациентов использовался гастросидин (фамотидин) в дозировке 40-80 мг в сутки в течение 4 недель (первые 2-2,5 недели лечение проводилось в стационаре ЦНИИГ, в последующие 2 недели пациенты принимали гастросидин в амбулаторно-поликлинических условиях). Терапию гастросидином всегда начинали и продолжали при отсутствии выраженных побочных эффектов, пациентам назначали по 40 мг 2 раза в сутки в течение 4 недель; лишь при появлении диареи и крапивницы дозировку гастросидина уменьшали до 40 мг в сутки.
Исследование было выполнено с учетом критериев включения и исключения больных из исследования согласно правилам клинической практики.
При проведении ЭГДС определяли НР, используя быстрый уреазный тест (один фрагмент антрального отдела желудка в пределах 2-3 см проксимальнее привратника) и гистологическое исследование биопсийного материала (два фрагмента антрального отдела в пределах 2-3 см проксимальнее привратника и один фрагмент тела желудка в пределах 4-5 см проксимальнее угла желудка). При обследовании больных при необходимости проводили УЗИ органов брюшной полости и рентгенологическое исследование желудочно-кишечного тракта. Полученные данные, включая и выявленные побочные эффекты, регистрировали в истории болезни.
В период проведения исследования больные дополнительно не принимали ингибиторы протонного насоса, блокаторы Н2-рецепторов гистамина или другие так называемые «противоульцерогенные» препараты, включая антацидные препараты и средства, содержащие висмут. 25 из 30 пациентов (84%) из-за наличия клинических симптомов, ассоциируемых чаще всего с нарушением моторики верхних отделов пищеварительного тракта, дополнительно получали прокинетики: домперидон (мотилиум) в течение 4 недель или метоклопрамид (церукал) в течение 3-4 недель.
Лечение больных ГЭРБ в стадии рефлюкс-эзофагита всегда начинали с назначения им гастросидина по 40 мг 2 раза в сутки (предполагалось, что в случае появления существенных побочных эффектов доза гастросидина будет уменьшена до 40 мг в сутки). Через 4 недели от начала лечения (с учетом состояния больных) при наличии клинических признаков ГЭРБ и (или) эндоскопических признаков эзофагита терапию продолжали еще в течение 4 недель. Через 4-8 недель по результатам клинико-лабораторного и эндоскопического обследования предполагалось подвести итоги лечения больных ГЭРБ.
При лечении больных гастросидином (фамотидином) учитывались следующие факторы: эффективность гастросидина в подавлении как базальной и ночной, так и стимулированной пищей и пентагастрином секреции соляной кислоты, отсутствие изменений концентрации пролактина в сыворотке крови и антиандрогенных эффектов, отсутствие влияния препарата на метаболизм в печени других лекарственных средств.
Двое из 30 больных (6,6%) через 2-3 дня от начала лечения отказались от приема гастросидина, с их слов, из-за усиления болей в эпигастральной области и появления тупых болей в левом подреберье, хотя объективно состояние их было вполне удовлетворительным. Эти больные были исключены из исследования.
По данным ЭГДС, через 4 недели лечения у 17 пациентов из 28 (60,7%) исчезли эндоскопические признаки рефлюкс-эзофагита, у 11 — отмечена положительная динамика — уменьшение выраженности эзофагита. Поэтому в дальнейшем этих больных лечили гастросидином в амбулаторно-поликлинических условиях в течение еще 4 недель по 40 мг 2 раза в сутки (7 больных) и по 40 мг 1 раз в сутки (4 больных, у которых ранее была снижена дозировка гастросидина).
Весьма спорным остается вопрос — рассматривать ли рефлюкс-эзофагит, нередко наблюдаемый при язвенной болезни (чаще всего при язвенной болезни двенадцатиперстной кишки), как осложнение этого заболевания или же считать его самостоятельным, сопутствующим язвенной болезни заболеванием? Наш многолетний опыт наблюдений показывает, что, несмотря на некоторую связь ГЭРБ и язвенной болезни (их относительно частое сочетание и даже появление или обострение рефлюкс-эзофагита в результате проведения антихеликобактерной терапии), все же язвенную болезнь и ГЭРБ (в том числе и в стадии рефлюкс-эзофагита) следует считать самостоятельными заболеваниями. Мы неоднократно наблюдали больных с частыми обострениями ГЭРБ в стадии рефлюкс-эзофагита (при наличии у них рубцово-язвенной деформации луковицы двенадцатиперстной кишки). Последнее обострение язвенной болезни (с образованием язвы в луковице двенадцатиперстной кишки) у этих больных отмечалось 6-7 и более лет назад (значительно реже, чем рецидивы ГЭРБ в стадии рефлюкс-эзофагита), однако при очередном обострении язвенной болезни с образованием язвы в луковице двенадцатиперстной кишки всегда при эндоскопическом исследовании выявляли и рефлюкс-эзофагит. Мы уверены, что при наличии современных медикаментозных препаратов лечить неосложненную язвенную болезнь значительно легче, чем ГЭРБ: период терапии при обострении язвенной болезни двенадцатиперстной кишки занимает значительно меньше времени по сравнению с терапией ГЭРБ; да и в период ремиссии этих заболеваний пациенты с язвенной болезнью двенадцатиперстной кишки чувствуют себя более комфортно, в то время как больные ГЭРБ вынуждены для улучшения качества жизни отказываться от приема значительно большего количества продуктов и напитков.
При обследовании (через 8 недель лечения) трое из 11 больных по-прежнему предъявляли жалобы, ассоциированные с нарушением моторики верхних отделов желудочно-кишечного тракта. Трое больных при хорошем самочувствии отказались от проведения контрольной ЭГДС через 8 недель. По данным ЭГДС, у 7 из 8 больных отмечено исчезновение эндоскопических признаков эзофагита (в том числе у одной больной — заживление пептической язвы пищевода).
Определение НР проводилось у всех 30 больных: в 11 случаях выявлена обсемененность НР слизистой оболочки желудка (по данным быстрого уреазного теста и гистологического исследования материалов прицельных гастробиопсий). Антихеликобактерная терапия в период лечения больным ГЭРБ в стадии рефлюкс-эзофагита не проводилась.
При оценке безопасности проведенного лечения каких-либо значимых отклонений в лабораторных показателях крови, мочи и кала отмечено не было. У 4 больных (13,3%), у которых ранее наблюдался «нормальный» (регулярный) стул, на 3-й день лечения гастросидином (в дозе 40 мг 2 раза в сутки) был отмечен, с их слов, «жидкий» стул (кашицеобразный, без патологических примесей), в связи с чем доза гастросидина была уменьшена до 40 мг в сутки. Через 10-12 дней после снижения дозы стул нормализовался без какой-либо дополнительной терапии. Интересно отметить, что еще у 4 больных, которые ранее страдали запорами, на фоне проводимого лечения стул нормализовался на 7-й день. У 3 из 30 больных (10%) на 3-4-й день приема гастросидина появились высыпания на коже туловища и конечностей (крапивница). После уменьшения дозировки гастросидина до 40 мг в сутки и проведения дополнительного лечения диазолином (по 0,1 г 3 раза в день) высыпания на коже исчезли.
Проведенные исследования показали целесообразность и эффективность терапии ГЭРБ в стадии рефлюкс-эзофагита гастросидином по 40 мг 2 раза в сутки, особенно при лечении больных с выраженными болевым синдромом и изжогой. Такое лечение может успешно проводиться в стационарных и амбулаторно-поликлинических условиях. Изучение отдаленных результатов проведенного лечения позволит определить продолжительность периода ремиссии этого заболевания и целесообразность лечения гастросидином в качестве «поддерживающей» терапии или же терапии «по требованию».
Трофические язвы – это тяжело заживающие раны, образующиеся на нижних конечностях в области голени или стопы. Причиной их появления зачастую выступает нарушение кровообращения в тканях. В 90% язвы на ногах возникают именно из-за сбоев в работе венозных клапанов. Чаще всего от этого осложнения, вызванного венозной (80% случаев) или артериальной (20% случаев) недостаточностью, страдают пациенты в возрасте 60 лет и старше.
В России проживает 35 миллионов человек с венозной недостаточностью, из которых у 5 миллионов впоследствии развиваются трофические язвы.
Причины развития трофических язв
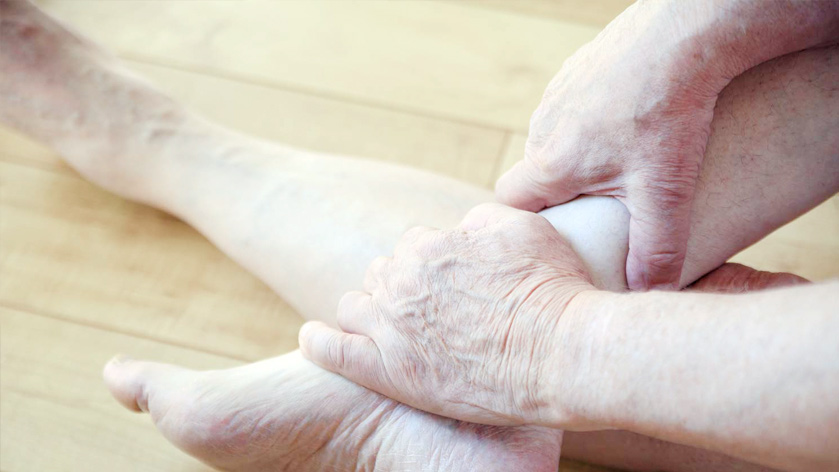
В норме кровь из нижних конечностей гонится по направлению к сердцу с помощью мышечной помпы. Венозные клапаны на этом пути препятствуют обратному кровотоку. Если клапан смыкается не полностью, тогда происходит рефлюкс крови в полость вены, которая начинает увеличиваться, образуя застой, что впоследствии приводит к образованию язвы.
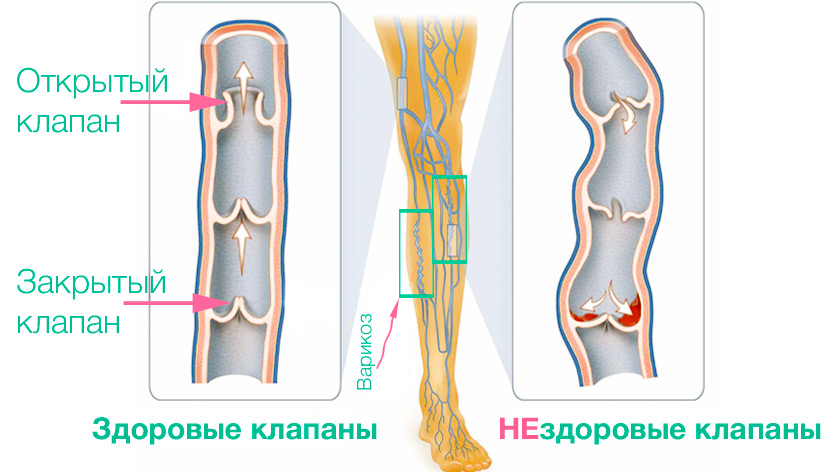
Факторы, повышающие риск появления венозных трофических язв:
- варикоз, флебит, тромбоз глубоких вен,
- травмы или операции,
- наследственность,
- венозная недостаточность.
Определить наличие такого типа недостаточности можно по боли, тяжести, зуду и отеку ноги, пигментации, разрушению и экземе кожи.
Факторы риска для развития артериальных язв:
- артериосклероз сосудистой стенки – образование бляшки, сужающей просвет сосуда,
- ишемия сердца, инсульт, сахарный диабет,
- ожирение,
- малоподвижный образ жизни.
Артериосклероз внешне проявляется в истончении кожи на ногах, потере волос, а ногти становятся толще. Из-за атрофии мышц и подкожной жировой клетчатки ноги бледные и прохладные, болят при нагрузке.
Чем опасно такое осложнение?
Если пациент игнорирует трофические язвы на ногах и их лечение, тогда ему предстоит столкнуться с рядом негативных последствий:
- сильная боль,
- развитие дерматита вокруг пораженного участка кожи,
- инфицирование раны,
- перетекание заболевания в хроническую стадию, что грозит более частыми рецидивами и более длительной терапией, которая длится от полугода.
Лечение трофических язв нижних конечностей включает 2 аспекта: работу врача и уход пациента за ногами. Как правило, доктор прибегает к консервативному способу лечения, который в каждом случае индивидуальный:
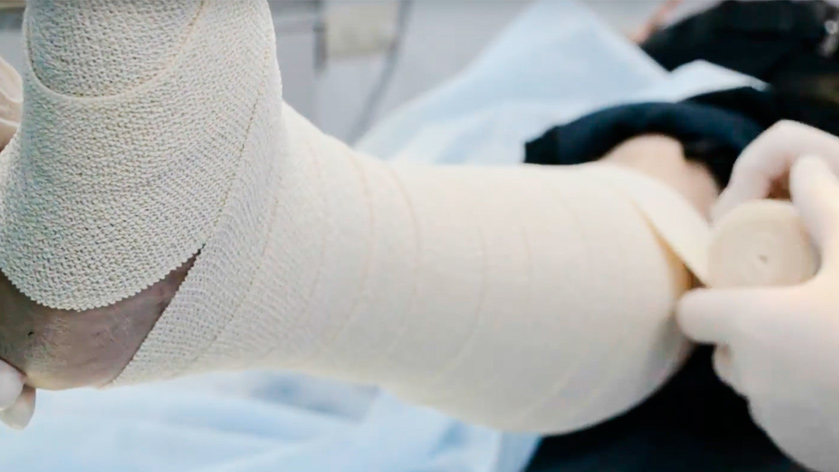
- компрессионная терапия – для возвращения к норме венозного кровотока, что приводит к закрытию язв даже без хирургии:
-
из воздухопроницаемых бинтов и бинтов с окисью цинка,
- специальные компрессионные гольфы,
- промывание и накладывание повязок (сорбционных, интерактивных и т.д.),
- подбор препаратов против воспаления, инфекций, для ускорения заживления тканей.
Домашнее лечение трофических язв, помимо выполнения всех указаний врача, подразумевает:
Настоящая работа посвящена исследованию возможности повышения эффективности комплексной терапии трофических язв и послеоперационных ран нижних конечностей с помощью топического иммуномодулятора. В исследовании приняли участие 44 больных
Настоящая работа посвящена исследованию возможности повышения эффективности комплексной терапии трофических язв и послеоперационных ран нижних конечностей с помощью топического иммуномодулятора.
В исследовании приняли участие 44 больных от 30 до 81 года (30 женщин, 14 мужчин) с хроническими трофическими язвами нижних конечностей. Трофические язвы развились из-за нарушения кровообращения в нижних конечностях по причине тромбофлебита или диабетической ангиопатии. У большинства больных тромбофлебит возник как осложнение варикозной болезни. Диагноз «варикозная болезнь, посттромбофлебитический синдром (ПТФС)» был постановлен 41 больному. На момент исследования признаки острого тромбофлебита на фоне ПТФС имелись у 9 человек, признаки рожистого воспаления кожи — у 5 человек. У 1 больного трофическая язва сочеталась с остеомиелитом большой берцовой кости, у двоих — с начинающейся гангреной пальцев ноги. В анамнезе трое больных перенесли флебэктомию, 1 больная — склерозирующую терапию по поводу варикозного расширения вен.
У подавляющего большинства исследованных больных имелась 1 трофическая язва и лишь у двоих больных были 2 язвы. В большинстве случаев язвы располагались на передней, внутренней или внешней поверхности голени, у 2 больных диабетической ангиопатией язвенный процесс локализовался на стопе. Размеры трофических язв варьировали от 0,5х0,5 см до 3х4,5 см. Кратер язвы был заполнен фибринозными массами у 30 больных, фибринозно-гнойными — у 6 больных, гнойно-некротическими фрагментами ткани — у 5 пациентов. В трех случаях на момент поступления больного язва выглядела чистой, без фибринозных, гнойных или некротических масс.
У 5 больных некротически-буллезной формой рожи на коже голени были признаки острого воспаления, пузыри с серозно-гнойным содержимым. У 2 других больных отмечались признаки начинающейся гангрены: соответственно I и III пальцы правой стопы были синюшно-черного цвета.
Лечение
При лечении всех 44 больных соблюдались следующие принципы лечения:
- постельный режим с приподнятым положением больной конечности для устранения застоя крови и лимфы;
- тщательный туалет кожи вокруг язвы;
- создание тока тканевой жидкости из язвы в повязку в начале лечения. Для этой цели использовали повязки с гипертоническим раствором NaCl в сочетании со спиртовым раствором хлорофиллипта, что обеспечивало очищение язвы, улучшение питания живых тканей дна и стенок язвы;
- активация регенеративных способностей организма после очищения кратера язвы.
Все больные ПТФС получали общее и местное лечение. Общими составляющими лечения были инфузионная (реополиглюкин 200 мл + трентал 5 мл + аскорбиновая кислота 5 мл в/в капельно, через день № 5), эскузан по 15 капель 3 раза в сутки, аспирин 0,5 г — 1 раз в сутки, троксевазин по 2 капсулы 3 раза в сутки в течение 15 дней или диовенор 600 мг по 1 табл. 1 раз в сутки в течение 30 дней. В дополнение к вышеописанному лечению пациенты с признаками острого тромбофлебита получали инъекции раствора гепарина 5000 ЕД п/к 4 раза в сутки в течение 6 дней.
Местное лечение в первые дни (от 1 до 4 дней) — хлорофиллипт спиртовой в сочетании с гипертоническим раствором, перевязки делались каждый день. После очищения язвы накладывались повязки с мазью гепона или солкосерил (контрольная группа, 10 человек). Как отмечалось выше, у 3 больных язва не содержала фибринозных, гнойных или некротических элементов. У этих больных сразу начинали лечение мазью гепона — иммуномодулятора, обладающего способностью повышать эффективность иммунной защиты, а также прямым противовирусным действием.
Мазь изготавливалась непосредственно в аптеке ГКБ №1 и имела следующий состав: гепона 0,006; ланолина 10,0; масла оливкового 10,0; воды для инъекций 10,0. Готовую мазь хранили при +4°С, использовали в течение 10 дней.
Мазь наносили тонким слоем на поверхность трофической язвы, повязки с мазью гепона меняли через день. Лечение проводилось в течение 10 дней (5 перевязок).
Лечение неосложненных трофических язв
В контрольной группе 10 больных получали такую же общую терапию, но местное лечение после очищения язвы проводили мазью солкосерил. Заживление язв у больных этой группы происходило на 5–15 дней дольше, чем при применении мази гепона. У 1 больной контрольной группы в ходе лечения мазью солкосерил произошло ухудшение, развилось рожистое воспаление кожи (некротически-буллезная форма). Этой пациентке было назначено адекватное хирургическое лечение, в дополнение к общему лечению применялись антибиотик и бисептол, для местного лечения вместо солкосерила использовалась мазь гепона.
Лечение язвенных дефектов кожи после некрэктомии по поводу некротически-буллезной формы рожи
Больные с некротически-буллезной формой рожи в дополнение к инфузионной терапии получали инъекции цефазолина по 1 г в/м 3 раза в сутки в течение 7 дней, а также бисептол 480 мг по 1 табл. 3 раза в сутки в течение 10 дней. На фоне консервативного лечения проводили оперативное вмешательство — некрэктомию. Пузыри вскрывались, некротизированные ткани удалялись, открытая рана обрабатывалась раствором перманганата калия. Далее открывшиеся после некрэктомии большие дефекты кожи лечили гепоном, как трофические язвы. У всех больных отмечались хорошие результаты лечения. Через 3–4 дня после начала применения мази гепона наблюдался выраженный рост грануляционной ткани с последующим формированием соединительнотканного рубца в кратчайшие сроки.
Лечение послеоперационных ран нижних конечностей у больных диабетической ангиопатией
При лечении больных диабетической ангиопатией консервативное лечение дополняли адекватными дозами инсулина (п/к). В качестве антибиотика использовали линкомицин по 600 мг в/м 2 раза в сутки в течение 14 дней. При начинающейся гангрене пальца на фоне консервативного лечения проводили адекватное оперативное вмешательство — ампутацию или ограниченное иссечение некротизированных элементов. В послеоперационном периоде промывали рану и свищевые ходы раствором гепона (0,002 г в 10 мл физиологического раствора), а также накладывали повязки с мазью гепона, как описано выше. Результаты лечения свидетельствуют о значительной активации роста грануляционной ткани и ускоренном заживлении послеоперационной раны под влиянием гепона.
Очевидно, что применение гепона в описанных выше клинических случаях стимулировало активный рост грануляционной ткани. Обычно у больных диабетической ангиопатией проходимость капиллярного русла оказывается минимальной, во время хирургических манипуляций кровь выделяется, как правило, только из подкожных сосудов, внутренние ткани практически обескровлены, имеют бледно-розовый цвет. Рост грануляционной ткани у таких больных либо не отмечается вовсе, либо протекает очень вяло, послеоперационные раны хронически не заживают, остаются трофические язвы. Применение гепона позволило добиться ускоренного заживления послеоперационных ран и незаживающих язв у больных диабетической ангиопатией.
Литература
Клинический пример
Больная О. Л. О., 52 года (ИБ № 5039).
Диагноз при поступлении: варикозная болезнь, посттромбофлебитический синдром, трофическая язва правой голени.
Диагноз окончательный: варикозная болезнь, посттромбофлебитический синдром, трофическая язва правой голени. Рожистое воспаление правой голени (некротически-буллезная форма).
Жалобы при поступлении: боли в области правой голени, усиливающиеся при ходьбе, наличие трофической язвы на передней поверхности нижней трети правой голени.
Anamnesis morbi: считает себя больной в течение 20 лет, когда впервые появились варикозные расширения вен правой голени. Неоднократно лечилась по поводу данного заболевания у ангиохирурга по месту жительства, от оперативного лечения отказывалась. Трофическая язва появилась около месяца назад, попытки самостоятельно лечиться облегчения не принесли, обратилась в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: детских болезней не помнит, болезнь Боткина, туберкулез, наличие венерических заболеваний у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен.
Status praesens objectivus: общее состояние больной удовлетворительное, сознание ясное, положение в постели активное. Больная повышенного питания, костно-мышечная система без патологии. Кожа и видимые слизистые обычной окраски. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких дыхание везикулярное, ЧДД 16 в 1 мин. Тоны сердца ритмичные, пульс 68 уд. в 1 мин, АД 130/80 мм рт. ст. Язык влажный, розовый, живот мягкий, безболезненный, печень — по краю реберной дуги, селезенка не пальпируется, симптом «поколачивания» отрицателен с обеих сторон. Физиологические отправления в норме.
Locus morbi: правая нижняя конечность отечна, голень синюшного цвета, болезненна при пальпации. На передней поверхности нижней трети голени трофическая язва 2х2 см, края гиперемированы, в кратере фибринозное отделяемое.
Анализы: кровь на RW — отрицательная; биохимический анализ крови — белок 54 г/л, креатинин 76 мкмоль/л, мочевина 5,5 ммоль/л, остаточный азот 25 ммоль/л, диастаза 20 г/(ч/л), билирубин 16 — 4 — 12 мкмоль/л, глюкоза 3,2 ммоль/л; коагулограмма — протромбин 85%, фибриноген 3,2 мкмоль/л, время рекальцификации 90 с; общий анализ крови: Э — 5,5 млрд./мл, Л — 6,4 млн./мл, Hb — 115 г/л, цветной показатель — 0,92, СОЭ — 25 мм/ч; общий анализ мочи — норма.
Лечение: раствор гепарина по 5000 ЕД п/к каждые 6 ч, аспирин 0,25 г по 1 табл. 1 раз в день; местно трофическую язву обрабатывали спиртовым раствором хлорофиллипта, поверхность язвы 2 раза в день смазывали мазью троксевазин, на ночь — мазью солкосерил. Через 5 дней лечения общее состояние пациентки значительно ухудшилось, температура тела повысилась до 39,5°С. Кожные покровы правой нижней конечности резко гиперемированы, гипертрофированы, болезненны. Установлен диагноз: рожистое воспаление правой нижней конечности.
Коррекция лечения: цефазолин по 1 г 2 раза в сутки, бисептол 480 мг по 1 табл. 3 раза в сутки. Через двое суток в области пораженной конечности появились пузыри с серозной жидкостью, под которыми впоследствии образовались участки некроза дермы (некротически-буллезная форма рожи).
Ввиду отсутствия положительного эффекта от предшествующей терапии, у больной проведено лечение с применением гепона.
Местно — произведено рассечение пузырей, удаление некротических элементов тканей. Были назначены ванны с перманганатом калия, инфузионная терапия (реополиглюкин 200 мл + трентал 5 мл + аскорбиновая кислота 5 мл в/в капельно, через день № 5), эскузан по 15 капель 3 раза в сутки, аспирин 0,5 г — по 1 табл. 1 раз в сутки, троксевазин по 2 капсулы 3 раза в сутки в течение 15 дней или диовенор 600 мг по 1 табл. 1 раз в сутки в течение 30 дней.
Locus morbi на момент начала терапии гепоном: по передней поверхности правой голени 3 язвенных дефекта кожи 10х10 см, раны заполнены фиброзно-гнойным отделяемым. После санации раневой поверхности раствором риванола применялись повязки с гепоном. Смена повязок проводилась через день. Уже после второй перевязки появился значительный рост грануляционной ткани, к концу лечения (всего 5 перевязок в течение 10 дней) раны очистились. Проведена операция аутодермопластики марочным способом (15 марок). Гепон в виде мази продолжали применять на всей послеоперационной поверхности. На фоне применения гепона «прижились» все 15 марок, в кратчайшие сроки сформировался рубец.
Клинический пример
Больная К. Л. Н. , 78 лет (ИБ № 6784).
Диагноз при поступлении: облитерирующий атеросклероз сосудов нижних конечностей. Сахарный диабет.
Диагноз окончательный: сахарный диабет III степени. Диабетическая ангиопатия нижних конечностей. Начинающаяся гангрена III пальца (ногтевая фаланга) правой стопы.
Жалобы при поступлении на постоянные боли в нижних конечностях, особенно в области III пальца правой стопы, общую слабость, недомогание.
Anamnesis morbi: считает себя больной около 20 лет, когда впервые был обнаружен сахарный диабет. Неоднократно лечилась в эндокринологическом и хирургическом стационарах. Последнее обострение началось 3 недели назад, когда появились перечисленные выше жалобы. Попытки самостоятельного лечения оказались безрезультатными, обратилась в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: аппендэктомия в 1950 году. Болезнь Боткина, туберкулез, венерические заболевания у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен. Отмечает длительно протекающие гнойные процессы при любых незначительных травмах.
Status praesens objectivus: общее состояние средней тяжести, сознание ясное, положение в постели активное. Больная обычного питания, костно-мышечная система без патологии. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких — везикулярное дыхание, ЧДД 16 в 1 мин. Тоны сердца ритмичны, слегка приглушены, Ps 68 уд. в 1 мин, АД 130/90 мм рт. ст. Язык слегка суховат, живот правильной формы, участвует в акте дыхания, при пальпации безболезненный. Симптомы раздражения брюшины отрицательны. Печень по краю реберной дуги, селезенка не пальпируется. Симптом «поколачивания» отрицателен с обеих сторон. Физиологические отправления в норме.
Locus morbi: кожные покровы обеих нижних конечностей бледные, сухие. На стопах кожа прохладная на ощупь. Кожа III пальца правой стопы в области ногтевой фаланги синюшно-черного цвета. Движения в пальце сохранены.
Анализы: RW — отрицательная. Общий анализ крови: Э — 4,2 млрд./мл, Л — 9,2 млн./мл, Hb — 105 г/л, цветной показатель — 0,95, СОЭ — 17 мм/ч. Биохимия крови: глюкоза (при поступлении) 18,5 ммоль/л, глюкоза (после коррекции) 5,4 ммоль/л; билирубин 20,3–5,8–14,5 мкмоль/л, АЛТ — 0,43 ммоль/(ч/л), АСТ — 0,3 ммоль/(ч/л). Общий анализ мочи — норма. Коагулограмма: протромбиновый индекс 90%, фибриноген 8,8 мкмоль/л, время рекальцификации 100 с.
Лечение: инъекции инсулина (п/к) 28 ЕД утром, 16 ЕД вечером, раствора линкомицина 600 мг в/м 3 раза в сутки в течение 14 дней. Инфузионная терапия (реополиглюкин 200 мл + трентал 5 мл + актовегин 5 мл в/в капельно, через день № 5).
Местно — в III палец правой стопы под жгутом ввели линкомицин. Ночью после инъекции в области III пальца появились «дергающие» боли. Утром в области некроза кожи произведен овальный разрез длиной около 2,5 см, иссечены некротические элементы в области лизированного участка ногтевой фаланги, удалены секвестры, поставлен резиновый выпускник, наложена асептическая повязка. Со следующего дня начали накладывать повязки с мазью гепона, перевязки проводили через день №5. Во время перевязок удалялись некротические элементы до «живой» ткани. Ампутации пальца удалось избежать. Последующее лечение прошло успешно по типу лечения костного панариция. Отмечались быстрое очищение раны, энергичный рост грануляционной ткани и формирование рубца из соединительной ткани.
Клинический пример
Больная Б. Л. А., 65 лет (ИБ № 4571).
Диагноз при поступлении: диабетическая ангиопатия сосудов нижних конечностей, начинающаяся гангрена I пальца правой стопы.
Диагноз окончательный: сахарный диабет II типа средней тяжести в стадии декомпенсации. Диабетическая ангиопатия нижних конечностей. Начинающаяся гангрена I пальца правой стопы. Диабетическая нефропатия I степени.
Жалобы при поступлении: постоянные боли в области правой стопы, черный цвет кожных покровов I пальца правой стопы, общая слабость и недомогание.
Anamnesis morbi: считает себя больной около 20 лет, когда впервые был выявлен сахарный диабет. Неоднократно лечилась в эндокринологическом отделении. Перечисленные выше жалобы появились около 2 недель назад. Пыталась лечиться самостоятельно — без результата. Обратилась за помощью в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: детских болезней не помнит. Болезнь Боткина, туберкулез, венерические заболевания у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен. Периодически отмечает боли в области сердца, повышения АД.
Status praesens objectivus: общее состояние удовлетворительное, сознание ясное, положение в постели активное. Больная повышенного питания. Кожные покровы бледные, костно-мышечная система без патологии. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких — везикулярное дыхание, ЧДД 16 в 1 мин. Тоны сердца приглушены, ритмичны, Ps 82 удара в 1 мин, АД 140/80 мм рт. ст. Живот мягкий, при пальпации безболезненный. Печень по краю реберной дуги, селезенка не пальпируется. Симптом «поколачивания» с обеих сторон отрицателен. Физиологические отправления в норме.
Locus morbi: обе голени и стопы прохладные на ощупь. Пульсация на A.dorsalis pedis значительно ослаблена. I палец правой стопы в области ногтевой и средней фаланг синюшно-черного цвета, движения в пальце сохранены.
Анализы: RW — отрицательная; Э — 3,2 млрд./мл, Л — 13,5 млн./мл; Hb — 104 г/л, цветной показатель — 0,97; СОЭ — 56 мм/ч; протромбин — 100%, фибриноген 4,8 мкмоль/л, время рекальцификации 90 с: глюкоза крови 12,5 ммоль/л; общий анализ мочи — Л на все поле зрения.
Реовазография — общий кровоток правой голени снижен, левой голени достаточный. Тонус сосудов повышен. Затруднен венозный отток, больше справа.
Лечение: операция — ампутация I пальца правой стопы с головкой I плюсневой кости.
Режим II, диета 9. Инъекции инсулина (п/к) 26 ЕД утром, 16 ЕД вечером. Инъекции раствора линкомицина 600 мг в/м 3 раза в сутки в течение 14 дней. Местно — перевязки со спиртовым раствором хлорофиллипта, затем мазью левомиколь.
Locus morbi на момент начала лечения гепоном: послеоперационная рана в области I пальца правой стопы до 3 см в диаметре, имеется свищевой ход к культе плюсневой кости с гнойным отделяемым. Лечение препаратом гепон включало промывания свищевого хода и послеоперационной раны раствором гепона (0,002 г в 10 мл физиологического раствора). Процедуры с использованием гепона повторяли через день, всего 5 процедур в течение 10 дней. На 6-й день лечения гепоном из свищевого хода был извлечен секвестр. На 10-е сутки рана очистилась и уменьшилась в диаметре до 1,5 см. Края раны сцеплены лейкопластырем по типу наводящих швов. Продолжено лечение мазью гепона. К 14-му дню появилась грануляционная ткань, но из свищевого хода продолжали выделяться секвестры культи плюсневой кости. К 30-му дню рана зажила вторичным натяжением.
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
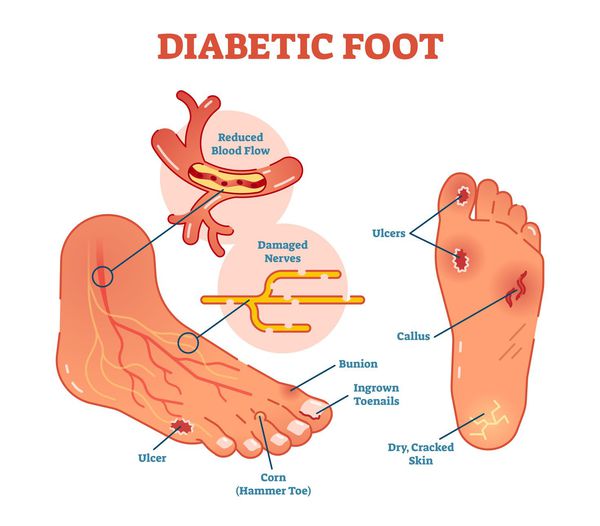
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
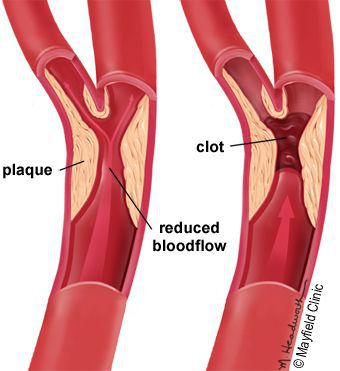
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
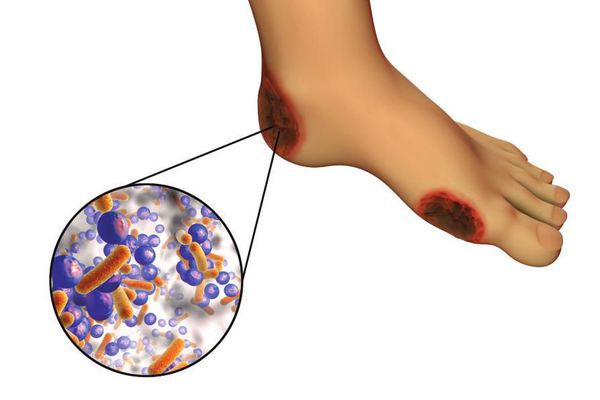
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
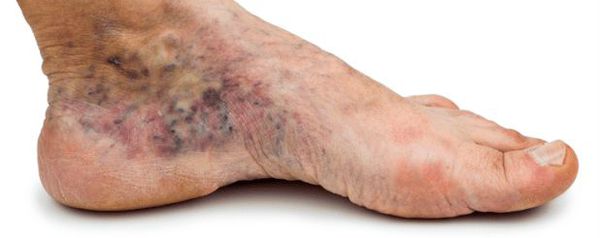
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
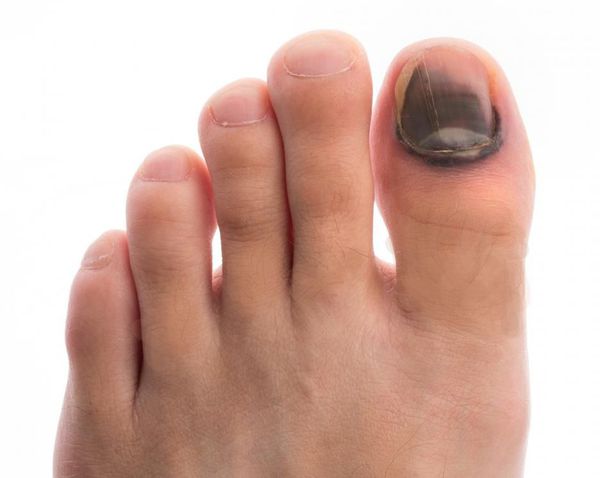
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
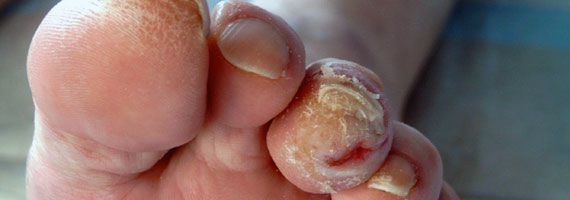
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
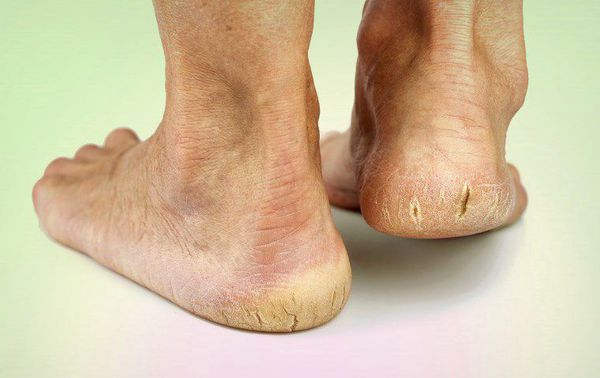
- трофические язвы, длительно не заживающие на стопах.
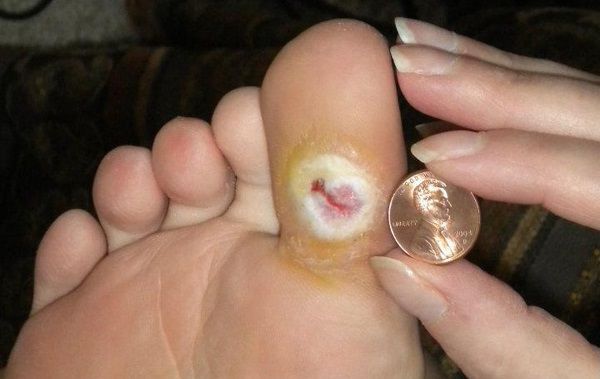
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
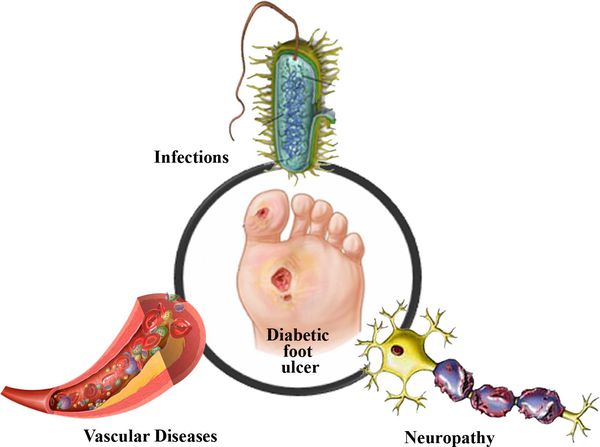
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
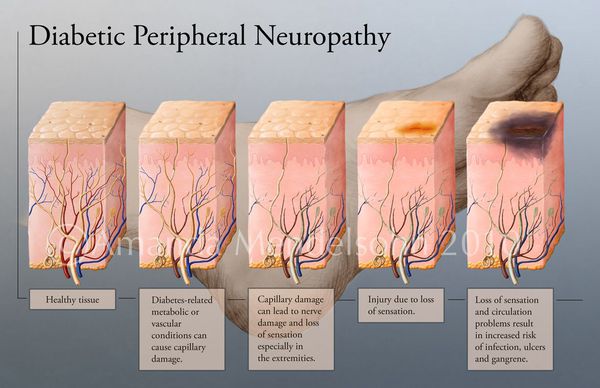
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
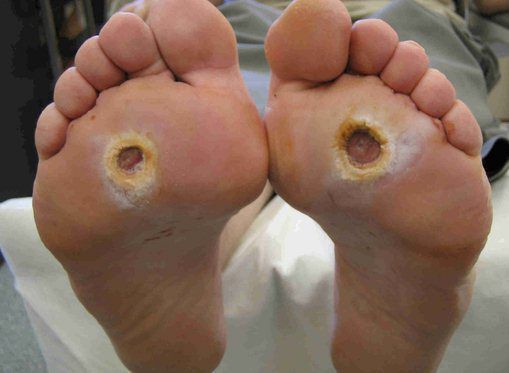
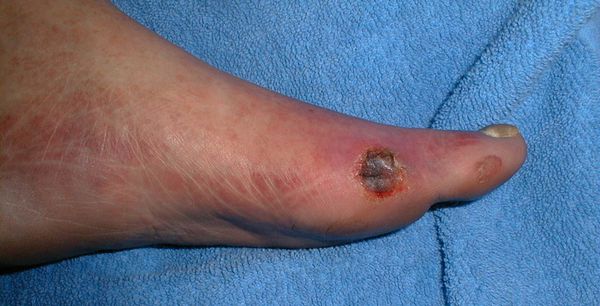
Классификация Вагнера
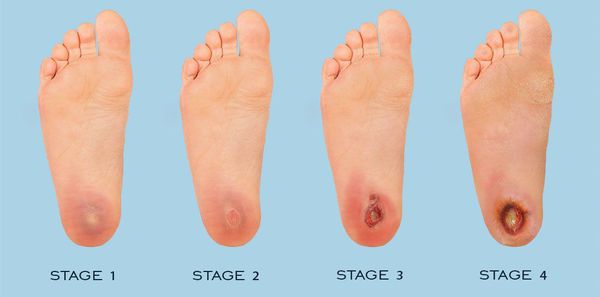
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.

Трофическая язва – крайне неприятное и опасное заболевание, требующее немедленного лечения. Однако терапия для каждого случая индивидуальна, так как причин возникновения патологии очень много. Чтобы избавиться от симптомов заболевания, необходимо пройти качественную диагностику, обратившись к квалифицированным специалистам.
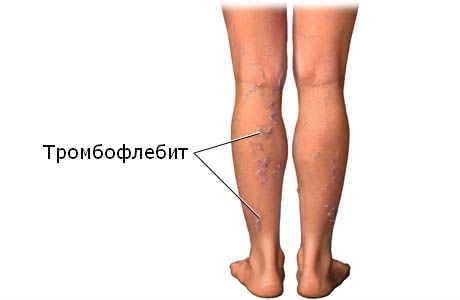
Тромбофлебит – что это?
Болезнь представляет собой нарушение кровотока или лимфатической системы, которые характеризуются образованием открытой раны преимущественно на нижних конечностях. Они, в свою очередь, заживляются крайне сложно, местная терапия практически не помогает. Осложнения происходят в случае присоединения инфекции, что приводит к более серьёзным последствиям заболевания.
Патология склонна к рецидивам и показывает малую способность к заживлению.
Чаще всего люди приходят на приём к доктору с язвами, локализующимися в области стопы, голени или лодыжки. Он жалуется на использование различных способов лечения, но. Как правило, ни один из способов не приносит ожидаемого облегчения. Наоборот, язва становится только больше и глубже.
Болезнь наиболее часто диагностируется у пациентов пожилого возраста, а также у людей, страдающих сахарным диабетом, варикозным расширением вен и другими патологиями, которые характеризуются нарушением кровообращения в области образования дефекта.
Чтобы устранить трофические язвы на ногах, требуется незамедлительно посетить врача и пройти полную диагностику состояния здоровья. Доктор не только качественно обработает рану, но и назначит соответствующую терапию, способную заживить рану и наладить кровообращение в области поражения тканей.

Симптомы
Трофические язвы конечностей не образуются одномоментно. Они проходят несколько этапов, прежде чем появится кровоточащая рана, которая быстро покрывается гноем.
- Сначала проявляется отёчность, которая сильно чешется и зудит.
- Кожа становится похожа на тонкий пергамент.
- Проявляется синюшность и несвойственная пигментация тканей.
- Часто наблюдается озноб во время сна.
- Появляются судороги мышц икр в ночные часы, во время сна.
- На истончившейся коже возникают капли желтоватой, прозрачной жидкости типа сукровицы.
Далее появляется язва с острыми и уплотнёнными краями. Очень быстро в незаживающую рану поселяются патогенные микроорганизмы, что приводит к нагноению раны.
Ноги более подвержены образованию сложных и глубоких язв, так как здесь часто происходит замедление движения крови в сосудах и венах. Ограниченное питание тканей и нарушения лимфатической системы приводит к образованию открытых ран.
Причины
Основной причиной развития открытых ран называют нарушение кровоснабжения в определённой части организма. Чаще всего это нижние конечности, так как замедленный кровоток и образование тромбов характерны для этой области.
У пациентов, страдающих сахарным диабетом, трофические язвы главным образом локализуются на большом пальце стопы или пятках.
Распространёнными причинами возникновения дефектов называют:
- Недостаточность венозная в хроническом виде, развивающаяся из-за варикоза вен, посттромботического заболевания, после некоторых операций или в результате аномального строения вен с рождения;
- Хроническая форма артериальной недостаточности, развивается в результате заболевания сахарным диабетом, гипертонической болезни или патологий артерий ног;
- нейротрофические расстройства, которые формируются в результате серьёзных травм позвоночника;
- свищи вен и артерий, они бывают врождённые и приобретённые;
- лимфедема;
- изменения травматического характера, к примеру после обморожения, радиационного воздействия или ожога;
- инфекции, в том числе вирус герпеса, туберкулез или гнойные воспаления;
- опухоли различной этиологии, как доброкачественные, так и злокачественные;
- внешнее воздействие, в том числе употребление наркотических и психотропных препаратов.
Также причиной развития трофических язв нижних конечностей может стать совокупность нескольких причин из перечисленного списка.
Далеко не у всех пациентов с перечисленными заболеваниями и патологиями возникают трофические язвы. Существует ещё ряд факторов, которые могут стать решающими в развитии кожного дефекта. К примеру, избыточная масса тела, а также чрезмерные физические нагрузки или долгое пребывание в одном положении. Последнее относится не только к «сидячей» работе, но и к людям, которые по причине травм, операций или нарушений деятельности организма вынуждены лежать.
Пожилые люди чаще страдают данной проблемой, так как в силу возраста нарушается кровообращение в нижних конечностях, образ жизни малоподвижен, а также существует ряд хронических заболеваний. Кроме того, с течением лет иммунная система организма ослабевает.
Патогенез

Чаще всего болезнь наблюдается в результате нарушения естественного кровотока в венах и артериях нижних конечностей, а также проблемах с течением лимфы. Кровь становится гуще, медленнее передвигается по сосудам, продукты обмена скапливаются в мелких капиллярах. В результате ткани истончаются, нарушается система регенерации клеток. Возникает ситуация. Когда даже малейшая царапина может стать причиной разрастания трофической язвы.
Повреждённые клетки тканей и некроз становится благоприятный средой для размножения патогенной микрофлоры. Бактерии вызывают нагноение, а также распространяют инфекцию по организму. Это может приводить к таким осложнениям как гангрена и сепсис, с последующей ампутацией конечности.
У людей с низким порогом чувствительности, к примеру, страдающих диабетом, повышен риск развития трофических язв, так как они могут вначале не замечать ран на ногах.
Классификация и стадии
Лечение трофических язв связано с особенностями их происхождения. При этом применяют обширную классификацию, по которой делят патологии на многочисленные разновидности. Патологию делят на несколько групп, которые формируются в зависимости от причины возникновения болезни, а также интенсивности её течения и заживления при квалифицированной терапии.

Классификация трофических язв, следующая:
- Венозные. Их развитие связано с варикозом и образованием тромбов в глубоких венах.
- Артериальные. Связаны с развитием атеросклеротических бляшек.
- Диабетические. Они связаны с повышенным содержанием сахара, нарушениями кровообращения в капиллярах, патологии нервов.
- Гипертонические. Наблюдаются при течении синдрома Мартореля.
- Системные. Появляются при системных нарушениях организма, к примеру, нарушениях обмена веществ, васкулите и других заболеваниях.
- Нейротрофические. Возникают на фоне патологий или травмирования нервных стволов.
- Рубцовые. Образуются в местах, где проводились оперативные вмешательства и остались шрамы.
- Застойные. Происходят в результате недостаточного кровоснабжения и предельной отёчности конечностей, чаще это случается при сердечно-сосудистых патологиях.
- Пиогенные. Запущенные состояния гниения, когда человек не следит за собственной гигиеной.
- Специфические и инфекционные. Связаны с параллельным течением опасных заболеваний пациента, к примеру, туберкулёзом или сифилисом.
- Малигнизированные. Образованы опухолями на коже.
- Лучевые.
- Возникшие в результате внешнего воздействия, например, ожогов или обморожения.
Также существует разновидность трофических язв, которые образуются в результате самостоятельного членовредительства пациента самому себе. Их называют искусственными. Чаще всего пациент пытается симулировать состояние болезни таким образом.
Согласно официальным классификациям, выделяют несколько основных стадий заболевания. Первая стадия предполагает возникновение поверхностной раны. Она располагается на нижней конечности, ткани вокруг синюшные, кожа истончена, наблюдается отёчность и боль в центре дефекта. Сама рана сухая и пока не загноившаяся.
Вторая стадия обусловлена ухудшением состояния раны. Она увеличивается в размерах, появляются бугры и неровности, края синюшного цвета. Язва мокнущая с гнойным налётом, затрагивает все слои кожи.
На третьей стадии уплотняется дно язвы и её стенки, кожа вокруг становится болезненной и сильно отёчной. Четвёртая стадия характеризуется постоянно мокнущей раной, при нажатии на края которой проявляется кровь. Кожные покровы бледные, тонкие, неживые.
Пятая стадия предполагает начало процесса заживления раны. Она очищается от гноя и начинает затягиваться. На шестой стадии трофическая язва заживляется, образуется плотный рубец.
Диагностика
Пациент, заметивший на своих конечностях язву, должен незамедлительно обратиться к врачу. Это может быть хирург или флеболог. В первую очередь квалифицированный доктор проводит визуальный осмотр и собирает анамнез пациента. Затем назначаются стандартные анализы и изучается карта пациента.
Только после установления причин возникновения трофических язв назначаются специальные анализы и проводятся специфические диагностические мероприятия.
Для назначения анализов учитывается возраст пациента, его хронические и сопутствующие патологии, учитывается количество язв и места их локализации. Для начала доктор назначает стандартные виды анализов: моча, биохимический и общий анализ крови. В рамках анализа крови определяется количество сахара и холестерина. Это очень важные показатели.
Если рана мокнущая, можно взять выделяемую жидкость на бакпосев, а также провести гистологию и цитологию. Это позволяет определить агрессивность трофических язв, а также определить тип присоединившейся патогенной микрофлоры.
Для верности диагноза также проводится ультразвуковое исследование венозного кровотока. Если предполагается нарушение артериального потока, направляют на МРТ с введением контрастного вещества, чтобы определить место нарушения.
Лечение
Спрашивая, как лечить трофическую язву, пациент должен понимать, что это не просто использование препаратов и мазей. Здесь важен комплексный подход, чтобы искоренить причину возникновения дефектов тканей, восстановить кровообращение и улучшить регенерацию. В противном случае предполагается возникновение рецидивов.
В зависимости от сложности заболевания применяют консервативное лечение мазями и другими препаратами, возможно, с использованием физиотерапии и рецептов народной медицины. При запущенных случаях показанием может стать оперативное вмешательство.
Трофическую язву можно также вылечить при помощи ЭВЛК. Данный способ лечения актуален, если причина недуга заключается в больной вене, которая нарушает кровоток и тем самым провоцирует развитие язвы на нижних конечностях
Консервативная терапия

Если человеку не требуется срочное хирургическое вмешательство, как правило, врач назначает консервативное лечение. Оно включает использование компрессионного белья для восстановления нормального кровообращения в конечностях. А также применение широкого спектра лекарственных препаратов.
В качестве компрессии используют специальные чулки или эластичные бинты.

Медикаментозная терапия включает регулярные профессиональные обработки раны, а также использование веществ против воспаления, инфицирования раны и стимулирующих заживление дефекта. В комплексе назначаются антибиотики широко спектра, препараты для восстановления нормального тока венозной крови, противовоспалительные и трофические вещества.
Антибиотикотерапию применяют при явных признаках инфекции: покраснение раны, гнойные выделения, повышение температуры тела пациента.
Длительность приёма антибиотиков варьируется в зависимости от запущенности патологии и ответа патогенной микрофлоры на применение препаратов против трофических язв. Курс длится от 2–3 недель вплоть до двух месяцев непрерывного приёма таблеток или инъекций. При сильных болях используются подходящие пациенту обезболивающие.
Показано также использование средств против свёртываемости крови, препаратов, улучшающих приток венозной крови и её нормальную циркуляцию. Не менее важно использовать мази против варикозного расширения вен. На фоне общей терапии используют местные обработки, обязательно антисептиком, а затем нетугая повязка с мазями для трофических язв. Они заживляют и способствуют регенерации клеток.
По мере заживления начинают применять специальные пластыри для данного заболевания.
Нельзя перетягивать область поражения, применяя тугие повязки. К ране нужно обеспечить свободный доступ кислорода, чтобы заживление происходило быстрее.
Хирургическое вмешательство
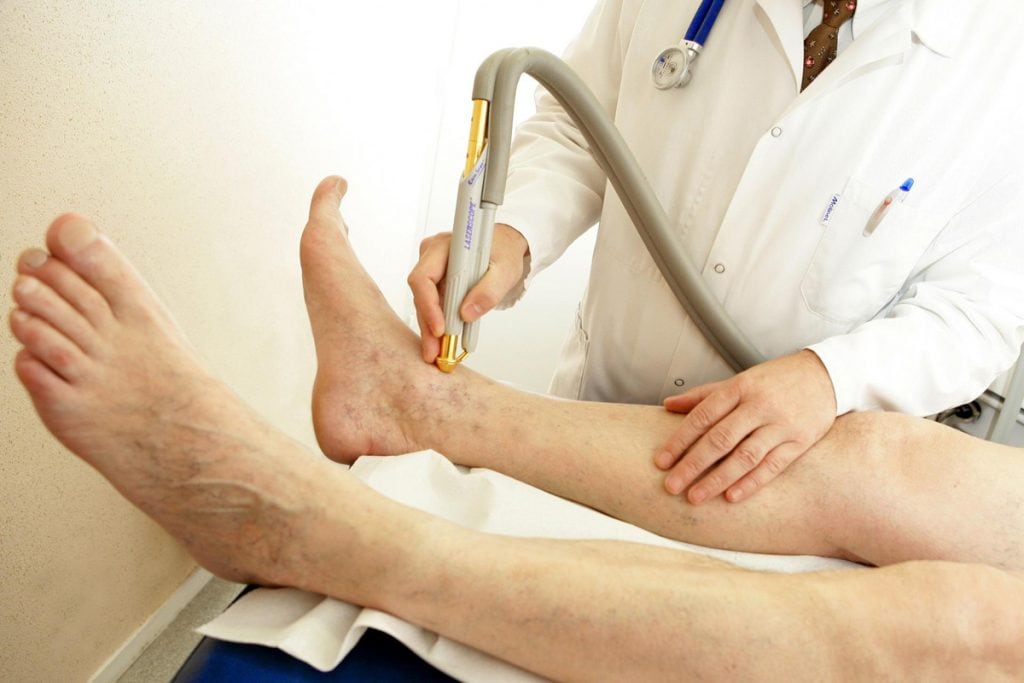
Если размеры поражения превышают показатели 50–70 мм требуется помощь хирурга. Он убирает некротические ткани, зачищает гной и при необходимости проводит замещение отсутствующего кожного покрова путём трансплантации.
Операция по восстановлению кровообращения в повреждённом сосуде проводится одновременно с лечением трофической язвы.
Если язва осложнена обширным некрозом, особенно это касается пальцев ног, назначается ампутация части конечности. В настоящее время существуют щадящие методы восстановления кровотока с помощью лазера или специального клея, однако положительный исход применения подобной процедуры может предусмотреть только врач.
В рамках лечения и восстановления пациенту назначаются физиотерапевтические процедуры. К примеру, лечение дарсонвалем, озонотерапеия, СУФ и инфракрасное облучение, лазерная корректировка и магнитотерапия. При домашних обработках, наряду с антисептиками, используются примочки с отварами трав.
Лекарства и препараты

В каждом индивидуальном случае лекарственные средства подбираются для конкретного пациента. В начале терапии доктор может назначить антибиотики широкого спектра, но после получения результатов биохимии и бакпосева назначения могут быть скорректированы.
В качестве веществ, способствующих ускорению процесса восстановления тканей и обменных процессов, применяют Актовегин или Пентоксифиллин. Для заживления и устранения варикоза применяют венотоники. Это мази для лечения варикоза – Флебодия 600, Детралекс или Троксевазин. Для местных обработок можно использовать Мирамистин или Хлоргексидин.
Курс лечения и особенности обработок назначается только наблюдающим доктором. Самолечение в этом случае недопустимо и не принесёт желаемого выздоровления. Заживление у всех проходит по-разному. Первые улучшения пациент заметит спустя 2 – 3 недели с момента начала терапии. Стойкий эффект можно увидеть спустя три месяца, а при обширных поражениях тканей – через полгода.
Профилактика

Предупредить развитие незаживающих язв на ногах можно только своевременным лечением болезней, способствующих нарушению кровообращения нижних конечностей. Важно наладить качественный режим жизни с достаточными физическими нагрузками, сбалансированным питанием и контролем веса. Не стоит забывать о регулярном посещении доктора для контроля состояния пациента.
Если имеются предпосылки к образованию варикоза, следует подобрать подходящий компрессионный трикотаж, выбрать удобную обувь, защитную одежду, чтобы предотвратить мелкие травмы. Обязательно соблюдать режим труда и отдыха.
Вопрос – Ответ
Несмотря на обилие информации, многие пациенты до сих пор не могут вовремя определить образование трофических язв и обращаются в кабинет доктора слишком поздно. Мы ответим на ряд самых популярных вопросов об этом заболевании.
Ангелина Б., 68 лет, г. Минск
Страдаю трофическими язвами несколько лет. Хотелось бы узнать, можно ли применять для местной обработки перекись и зелёнку?

Применение перекиси водорода возможно при ежедневных обработках и очищения ран перед наложением чистого бинта. Манипуляции важно проводить пару раз в сутки, утром и вечером после душа. Вместо перекиси водорода рекомендуют более щадящий раствор хлоргексидина. Зелёнка – популярное средство в медицинских аптечках россиян. Её также можно использовать при обработках, но наносить её исключительно на края раны, чтобы избежать инфицирования. Мазать саму рану не нужно, такое лечение неэффективно. В случае с трофическими язвами лучше применить мази для лечения конкретно этой патологии.
Вера Борисовна П., 52 года, г. Гродно
Страдаю сахарным диабетом и хотелось бы спросить, можно ли мазать трофические язвы инсулином?
Применение инсулина необоснованно. Нет никаких научных данных об эффективности данного препарата на открытых ранах. Кроме того, использование терапевтических средств без назначения доктора способно привести к различным осложнениям и ухудшению состояния пациента.
Виктор С., 62 года, г. Минск
Как проводить гигиену ран?
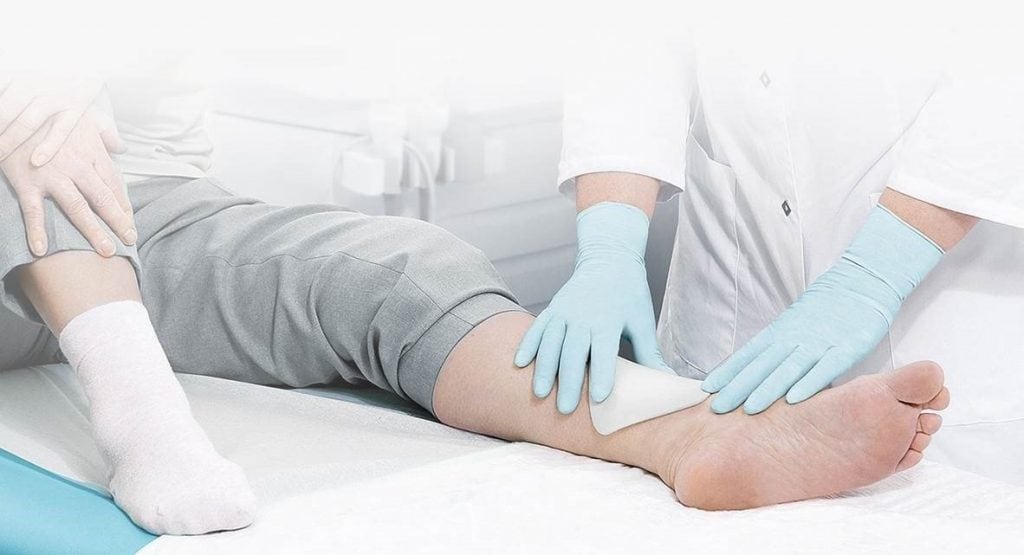
Достаточно подставить ногу под струю чистой воды и подержать в течение пары минут. Иногда рекомендуется использовать брусок хозяйственного мыла, но не каждый способен спокойно перенести эту процедуру. После промывания рану слегка просушивают и обрабатывают антисептиками, а затем накладывают чистую повязку. Подобные обработки проводятся дважды в сутки. Желательно, чтобы пациенту помогал кто-то из близких, чтобы не упустить развитие некроза и загноение.
Читайте также:

