Как лечить свищ на ноге при сахарном диабете
Обновлено: 01.05.2024
Синдром диабетической стопы (СДС) — очень серьезное осложнение сахарного диабета (СД). Это осложнение (в 85% случаев представленное трофическими язвами стоп разной тяжести) выявляется у 4—10% от общего числа пациентов с СД.
Синдром диабетической стопы (СДС) — очень серьезное осложнение сахарного диабета (СД). Это осложнение (в 85% случаев представленное трофическими язвами стоп разной тяжести) выявляется у 4—10% от общего числа пациентов с СД. Бытует мнение, что эффективность лечения язвенных дефектов стоп при СД низка, однако это не соответствует действительности. На самом деле при нейропатической форме (50—70% всех больных СДС) заживление трофической язвы происходит в 80—90% случаев. Для этого необходимо соблюдение нескольких обязательных условий (см. таблицу 1), тогда как низкая эффективность лечения часто связана с тем, что условия соблюдаются не полностью. Как показывает практика последних 10 лет, появление специализированных отделений и кабинетов «Диабетической стопы» значительно повысило эффективность лечения этих пациентов и снизило число ампутаций. Одна из не решенных пока проблем, актуальных для таких специализированных отделений, — низкая эффективность консервативного лечения диабетических язв при (нейро)ишемической форме СДС.
Ишемическая и нейроишемическая формы составляют менее половины всех случаев СДС (5—10% и 25—40%, соответственно) (Дедов, 1998, Shаw, 1996; Международная рабочая группа по диабетической стопе, 2000; Staroverova, 2001). Однако наличие выраженной ишемии принципиально меняет прогноз лечения у этих пациентов: вероятность заживления язвенных дефектов без восстановления магистрального кровотока составляет 10—30% (Международная рабочая группа по диабетической стопе, 2000). Следует помнить, что назначение большинства вазоактивных средств не повышает вероятность заживления язвенных дефектов. Согласно данным метаанализа (Loosemore, 1994), непростаноидные препараты (эффективные при II стадии хронической артериальной недостаточности, ХАН) неэффективны при III-IV стадиях. Простаниоды (алпростадил, илиопрост) влияют на прогноз при III-IV стадиях ХАН, но в основном — у больных с умеренными проявлениями критической ишемии (tcpO2>20 mmHg). Прогрессирование поражения и отсутствие заживления ран после малых ампутаций на фоне критической ишемии приводят к высокой ампутации у значительной части пациентов. Однако хорошо известно, что проведенное в таких условиях реконструктивное вмешательство на артериях нижних конечностей кардинально меняет прогноз лечения, позволяет избежать высокой, а в ряде случаев — и малой ампутации. Это привело к тому, что в последние годы хирургическая реконструкция артерий (путем шунтирования или эндоваскулярных вмешательств) рассматривается в качестве метода выбора при лечении как перемежающейся хромоты, так и язвенных дефектов ишемического происхождения при СД (American Diabetes Association, 1999; Международная рабочая группа по диабетической стопе, 2000). Была показана высокая эффективность реконструктивных операций у пациентов с СД, в ряде случаев сопоставимая с таковой у пациентов без нарушений углеводного обмена. Результатом широкого внедрения этих методов в зарубежных странах явилось значительное снижение числа ампутаций при ишемической форме синдрома диабетической стопы в Европе. Реконструктивные операции на артериях у больных сахарным диабетом проводятся и в России (Покровский, 2002; Гавриленко, 2002; Мухамадеев, 2002).
Еще один недавно вошедший в практику метод лечения — иммобилизирующая разгрузочная повязка (ИРП), в зарубежной литературе — Total Contact Cast. Такая фиксирующая повязка на голень и стопу представляет собой более или менее жесткий «сапожок» (из гипса или современных полимерных материалов, съемный или несъемный), переносящий нагрузку с области язвы на другие участки. Важно, что этот метод позволяет ходить по улице, работать и т. п., не подвергая при этом рану механической нагрузке. В большинстве зарубежных стран ИРП стал «золотым стандартом» разгрузки, но в России он практически не применялся из-за боязни возникновения осложнений (не всегда обоснованной). В нашей стране основным, хорошо себя зарекомендовавшим методом разгрузки сегодня является «полубашмак». Однако в ряде ситуаций «полубашмак» оказывается неэффективен либо существуют противопоказания к его применению. Это расположение язвы в средней части стопы или пяточной области, необходимость выходить на улицу, работать, а также несоблюдение пациентом предписанного режима разгрузки. В этих случаях требуется использование ИРП.
Пациент В., 57 лет, обратился за консультацией в отделение «Диабетическая стопа» ЭНЦ РАМН 15.04.2003. Диагноз: сахарный диабет 2 типа, тяжелого течения, декомпенсация. Диабетическая дистальная полинейропатия. Диабетическая макроангиопатия: атеросклероз артерий нижних конечностей, критическая ишемия левой нижней конечности (ХАН IV ст). Синдром диабетической стопы, нейроишемическая форма: инфицированный язвенный дефект левой пяточной области II-III cт. по Wagner. Диабетическая микроангиопатия: диабетическая нефропатия в стадии протеинурии с сохранной азотовыделительной функцией почек (IV ст. по Morgensen); диабетическая ретинопатия II ст. ИБС, стенокардия напряжения I ф. к. Многоузловой эутиреоидный зоб 0 ст. (ВОЗ).
СД 2 типа диагностирован в 1990 г. Пациент получал лечение диабетоном 80 мг 1-2 таб/сут (принимал препарат нерегулярно), контроль гликемии был нерегулярным. На момент осмотра уровень гликемии достиг 17,5 ммоль/л натощак.
Перемежающуюся хромоту не отмечал (однако вел малоподвижный образ жизни, редко проходил более 500 м).
23.02.2003 появился язвенный дефект левой пяточной области. Рана не заживала, несмотря на проводившееся амбулаторное и стационарное лечение (включавшее вазапростан 40 мкг/сут N 15), осложнилась раневой инфекцией (St. aureus, Enterococcus).
На момент осмотра: рана 4,5 х 3,5 см, глубиной до 3 см (см. рисунок 1). Стопа отечна, теплая на ощупь. Вибрационная чувствительность на стопах = 0-1 балл, пульсация на артериях правой стопы ослаблена, левой — не определяется.
Общее состояние: относительно удовлетворительное, температура тела в норме. ЧСС = 70 уд/мин, АД = 140—150/80—90 mmHg.
Рентгенологически: дефект мягких тканей пяточной области, признаков деструкции пяточной кости нет.
УЗДГ: справа — признаки стеноза ~50% бедренно-подколенного сегмента, артерий голени. Слева — стенотические изменения бедренно-подколенного сегмента (~50%), окклюзия передней тибиальной артерии, субтотальный стеноз задней большеберцовой артерии.
Дуплексное сканирование брюшного отдела аорты и артерий нижних конечностей (в ГКБ №81): сосудистая стенка неровная, утолщена в дистальных сегментах обеих задних большеберцовых артерий (ЗББА) с медиокальцинозом. Толщина комплекса «интима-медиа» до 1,2 мм. В просвете дистальных сегментов ЗББА — множественные микрокальцинаты, стенозирование ЗББА справа до 90%, слева до 80%.
Восстановление артериального кровотока
На основании данных обследования и с учетом неэффективности проводившейся консервативной терапии, пациент был направлен к ангиохирургу для проведения реконструктивного вмешательства на артериях нижней конечности. Указанное лечение осуществлялось в 25-м Центральном военном клиническом госпитале РВСН с 13.05.03 по 02.06.03.
При обследовании в стационаре были получены следующие данные.
Клинический анализ крови: гемоглобин — 128 г/л, эритр. — 4,36*10 12 /л, лейк. — 6,8*10 9 /л (пал. — 2%, сегм. — 62%, эоз. — 2%, лимф. — 28%, мон. — 6%), СОЭ — 23 мм/ч.
Клинический анализ мочи: уд. вес — 1014, белок — 1,22%, цил. — нет, лейк. — 2—4 в п/зр, эритр. — 3—5 в п/зр.
Биохимический анализ крови: общий белок — 69,0 ммоль/л, билирубин — 10,0 ммоль/л, креатинин — 120 мкмоль/л, мочевина — 6,1 ммоль/л, холестерин — 4,8 ммоль/л, β-липопротеиды — 40%, триглицериды — 1,0 ммоль/л, АЛТ, АСТ — в норме.
ЭКГ: ритм синусовый, правильный, 68 уд/мин. Горизонтальное положение электрической оси сердца.
Ro-графия органов грудной клетки: легочные поля прозрачны. Корни фиброзные, с петрификатами. Гипертрофия левого желудочка, уплотнена дуга аорты.
УЗИ органов брюшной полости: печень, селезенка, желчный пузырь, поджелудочная железа, почки — без патологических изменений.
Ангиография артерий нижних конечностей: абдоминальный отдел аорты с неровными контурами, просвет ее сохранен. Контуры магистральных артерий нижних конечностей неровные, просвет сохранен, выраженный кальциноз стенок артерий. Магистральные артерии обеих голеней с неровными контурами, резко истончаются ниже уровня щели голеностопных суставов. В дистальном отделе левой задней большеберцовой артерии определяются два тандемных критических стеноза. Подошвенные артериальные дуги разомкнуты.
Проведенное лечение
Антибиотикотерапия (офлоксацин 200 мг два раза в день), хирургическая обработка раны (иссечение некротизированных тканей из кармана глубиной до 3 см), дезинтоксикационная терапия, дезагреганты в/в. Пациент переведен на инсулинотерапию (актрапид 8 ЕД п/з, 6 ЕД п/о, 6 ЕД п/у; монотард 8 ЕД п/з, 8 ЕД — 22.00), достигнута компенсация углеводного обмена (гликемический профиль 25.06.03: 8,9–6,5–4,7–7,4–5,1 ммоль/л). В связи с диабетической нефропатией IV ст. пациент постоянно получает эналаприл 10 мг/сут.
20.05.03 произведена рентгеноэндоваскулярная ангиопластика задней большеберцовой артерии слева, восстановлен артериальный кровоток.
Операция проводилась под местной анестезией 0,5%—20,0 Sol. Novocaini, левосторонним чрезбедренным доступом антеградно пунктирована бедренная артерия. Через интродюсер диаметром 5F введен коронарный проводник в заднюю большеберцовую артерию дистальнее стенозов. В область критических стенозов подведен баллонный сегмент катетера размерами 2, 5x20, 0 мм. Выполнена ангиопластика под рабочим давлением до 5 атм. На контрольной ангиограмме стеноз устранен, препятствий для кровотока не определяется. Проводник удален. Интродюсер подшит к коже. Асептическая повязка. За период вмешательства больному внутриартериально введено 7 тыс. ЕД гепарина. Состояние пациента не изменилось.
После выписки: при допплеровском исследовании магистрального кровотока справа и слева в задних большеберцовых артериях — магистральный измененный кровоток (ЛПИ > 1), в тыльных артериях стопы — коллатеральный кровоток, но ЛПИ > 1 (возможно завышение лодыжечно-плечевого индекса, вследствие артериосклероза Менкеберга).
Чрескожное напряжение кислорода (tcpO2) на тыльной стороне левой стопы (через три месяца после ангиопластики): лежа — 19 mmHg, сидя — 20 mmHg (возможно занижение показателя вследствие отека стопы). По совокупности клинических данных, состояния раны и результатов инструментального обследования было сделано заключение, что явления критической ишемии устранены.
Применение индивидуальной разгрузочной повязки (Total Contact Cast)
Пациент был выписан для амбулаторного лечения, которое включало:
- ежедневные перевязки с промыванием раны раствором диоксидина, фурацилина, наложением атравматической повязки (Atrauman, Branolind);
- регулярное удаление гиперкератоза с краев раны;
- разгрузку пораженной конечности (костыли);
- компенсацию углеводного обмена (инсулинотерапия).
Признаков ишемии конечности не наблюдалось, рана заполнилась полноценной грануляционной тканью (см. рисунок 2), но скорость сокращения размеров раны оказалась ниже расчетной (см. рисунок 3).
Известно, что скорость заживления соответствует расчетной при отсутствии значимой ишемии, инфекции и механической нагрузки на рану. Учитывая, что разгрузка конечности с применением костылей не является оптимальной, было решено изготовить иммобилизирующую разгрузочную повязку.
Эквивалентный радиус раны рассчитывается как (d1+d2)/4, где d1 и d2 — соответственно максимальный и перпендикулярный ему минимальный диаметр раны.
Расчетная скорость заживления (черная линия) определяется по формуле Cavanagh: r = -0.74 + 1.04*r0 — 0.1*t — 0.012*r0*t, где r — эквивалентный радиус раны в данный момент, r0 — исходный эквивалентный радиус раны, а t — время с начала лечения (дни) (Cavanagh, 2001).
Реальные размеры раны наносились на график (красная линия) при каждом осмотре пациента (точка «0» — 1 месяц после баллонной ангиопластики). Из графика видно, что после изготовления ИРП скорость заживления (угол наклона графика) значительно выросла и достигла расчетной.
При применении этого метода разгрузки рана начала затягиваться гораздо быстрее, и к 10.09.03 было достигнуто заживление язвы (см. рисунок 4).
Основными методами реваскуляризации нижних конечностей являются шунтирующие операции и чрескожная транслюминальная баллонная ангиопластика (ЧТБА). Зачастую ЧТБА считают недостаточно эффективной и предлагают не использовать у пациентов с СД. Известно, что долговременный эффект шунтирования выше, чем у баллонной ангиопластики, причем у больных с СД эта разница выражена сильнее (Dyet, 2000). Но в критических ситуациях (язвенные дефекты, критическая ишемия) ангиопластика представляет собой малоинвазивный метод, позволяющий стабилизировать ситуацию и избежать ампутации, что зачастую более важно, чем отдаленные результаты вмешательства. Это так называемая limb-saving angioplasty — ангиопластика для спасения конечности.
История болезни, представленная выше, демонстрирует также, как важна постоянная оценка эффективности проводимого лечения (в нашем случае — сопоставление динамики размеров язвы с результатами расчета по формуле Cavanagh). Если эффект от лечения недостаточен, необходимо выявить причину, по которой это происходит. В нашем случае отсутствие оптимального режима разгрузки оказалось достаточной причиной для замедленного заживления раны, и эта проблема могла быть решена только с помощью нового метода — иммобилизирующей разгрузочной повязки. Следует особенно отметить, что для приближения к «идеальной» скорости заживления не потребовалось использования ни «стимуляторов заживления» (солкосерил, актовегин, метилурацил и т. п.), ни «сосудистых» средств. Эти препараты широко применяются, однако их эффективность в отсутствии необходимых условий для заживления (см. таблицу 1) крайне низка.
В настоящее время становятся доступными новые методы лечения СДС, внедрение которых в повседневную практику вполне возможно и крайне необходимо. Только адекватное комбинированное лечение позволяет достичь оптимальных результатов, особенно в сложных случаях, таких, как синдром диабетической стопы.
По вопросам литературы обращайтесь в редакцию
О. В. Удовиченко, кандидат медицинских наук
Г. Р. Галстян, кандидат медицинских наук
И. А. Ерошкин, кандидат медицинских наук
А. А. Ефимов, О. В. Носов
Ю. Г. Васильев, кандидат медицинских наук
Эндокринологический научный центр РАМН (Москва), 25-й Центральный военный клинический госпиталь РВСН (Одинцово)
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
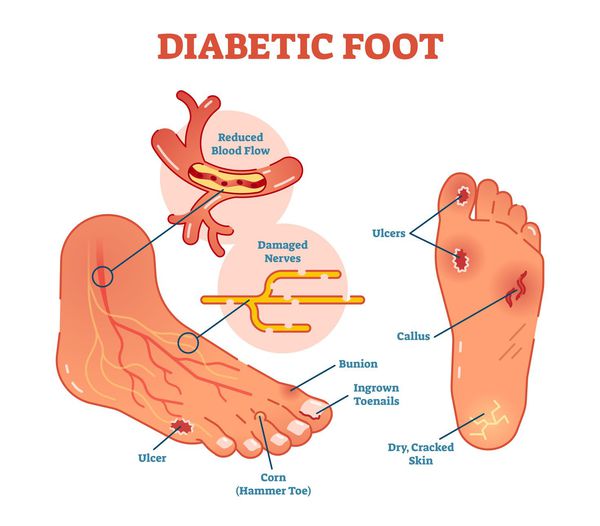
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
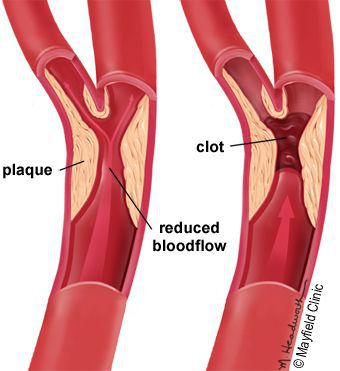
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
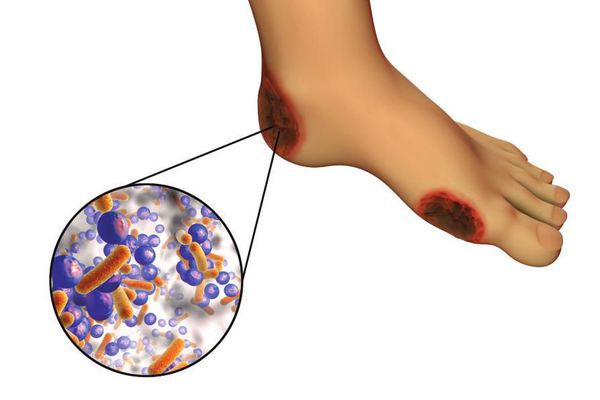
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
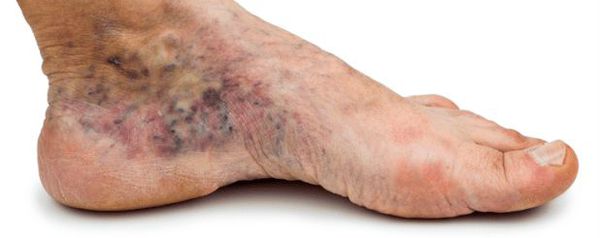
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
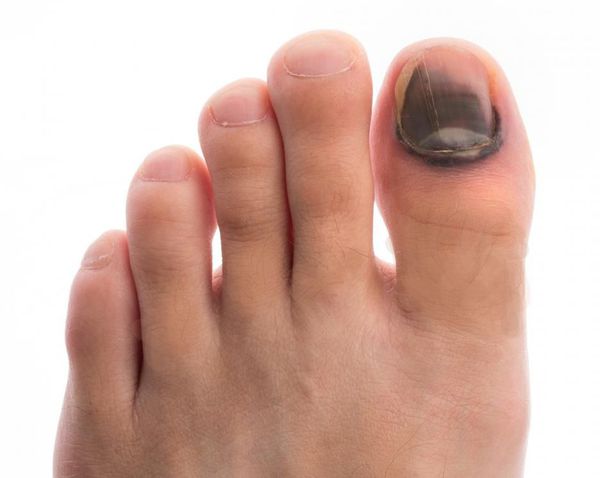
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
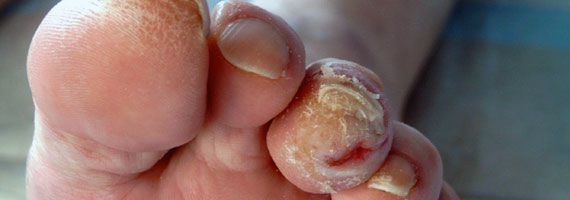
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
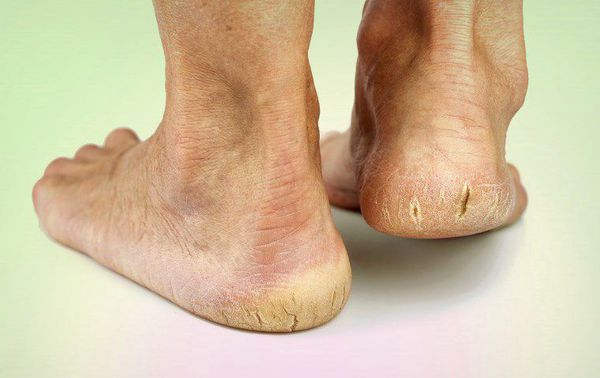
- трофические язвы, длительно не заживающие на стопах.
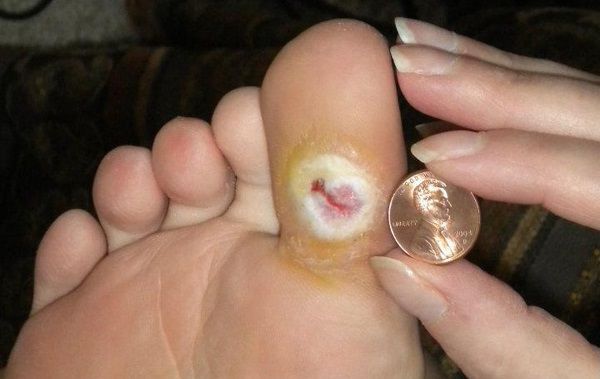
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
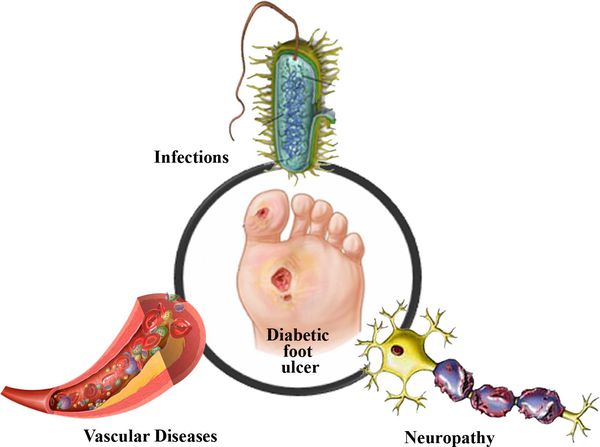
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
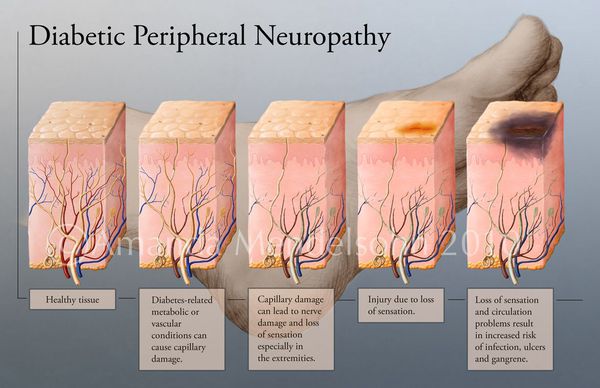
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
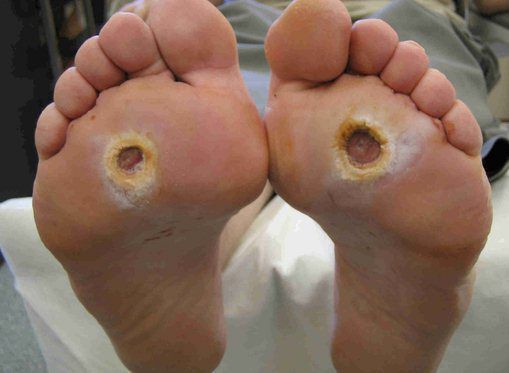
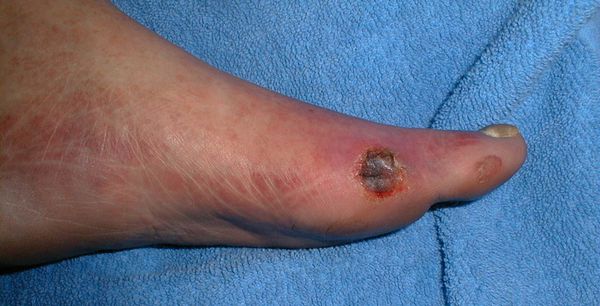
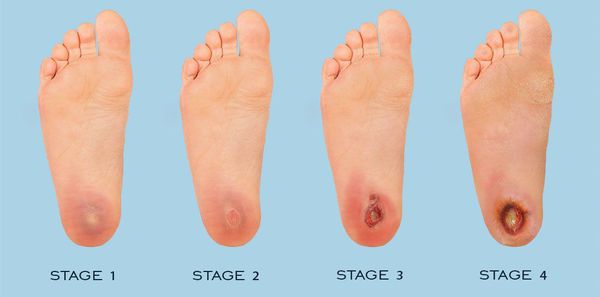
Классификация Вагнера
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Свищ всегда приходит внезапно, когда воспаление уже вылечено или операционная рана давно зажила. Его появление нельзя предугадать, хоть его формирование проходит не без симптомов, но то, что в этом месте случится именно свищ, догадаться невозможно. Зато появившийся свищ спутать с чем-то другим очень сложно.
Что такое свищ?
Свищ — это сформировавшееся в результате патологического процесса соустье между полыми органами желудочно-кишечного тракта и/или мочеполовой системы. Свищ — это также и извитой трубчатый ход от органа, проходящий через мягкие ткани с выходом на кожу.
Более благозвучное название свища, заимствованное из латыни, — фистула, но это медицинское понятие более широкое. Оно включает также искусственно сформированные соустья, как оперативно создаваемая фистула между веной и артерией у диализных пациентов. В одной ипостаси фистула — это свищ, в другой — искусственно созданное соустье, свищ же — всегда нерукотворная патология.
Свищ всегда имеет начало — внутреннее отверстие, локализующееся в первичном очаге воспаления с нагноением. Началом свища может быть незаживающая рана от травмы или операции, что особенно характерно для органов желудочно-кишечного тракта, продуцирующих секреты: желудочный, кишечный или панкреатический сок, желчь.
Наружное отверстие свища может открываться в другой орган или на кожу, как при свище прямой кишки, но это отверстие не обязательно — некоторые свищевые ходы слепо заканчиваются в мягких тканях, мышцах или клетчатке, образуя там гнойные кистообразные полости — затёки.
Виды свищей
Классификация свищей многообразна, у каждого органа — собственная градация свищей по локализации, иногда степени вовлечения окружающих тканей и даже по объему через свищ выделяемого секрета.
Полные свищи имеют наружное и внутреннее отверстие, неполные — только внутреннее.
Открывающиеся в коже называются наружными свищами, соединяющие органы свищи — внутренние.
Внутренние свищи по числу вовлеченных в процесс органов бывают комбинированными и изолированными. Изолированные свищи называются по органу, давшему ему начало: панкреатический, желчный, кишечный, вагинальный, мочеточниковый и так далее.
При соустье двух или нескольких органов, комбинированном виде свища, используется «объединённое» название. Так при свищевом ходе между прямой кишкой и влагалищем — свищ ректовагинальный, при свищевом ходе от желчного пузыря к желудку — свищ холецистогастральный, между поджелудочной железой и стенкой желудка — панкреатогастральный или поджелудочно-желудочный свищ.
По количеству ходов свищи делятся на одноканальные или простые и многоканальные или сложные, а также разветвленные или непрямые и неразветвленные или прямые.
По состоянию тканей и хода — инфицированные или осложненные свищи, как правило, гнойные и «чистые» неинфицированные или неосложненные свищи с выделением, к примеру, желчи или панкреатического сока.
| В зависимости от количества отверстий | Полные свищи | Имеют два отверстия – соединяют два органа между собой или один орган с поверхностью кожи |
| Неполные свищи | Имеют только одно отверстие | |
| В зависимости от локализации второго отверстия (для полных свищей) | Внутренние свищи | Соединяют внутренние органы |
| Наружные свищи | Соединяют внутренние органы с поверхностью кожи | |
| В зависимости от количества вовлеченных органов | Изолированные свищи | Получают название только по одному органу, давшему начало свищу |
| Комбинированные свищи | Вовлечено два и более органов | |
| В зависимости от хода свища | Одноканальные (простые) | Один свищевой ход |
| Многоканальные (сложные) | Несколько свищевых ходов | |
| Разветвленные (непрямые) | Имеется разветвление свища | |
| Неразветвленные (прямые) | Нет разветвлений | |
| В зависимости от наличия осложнений | Неосложненные (неинфицированные) | Признаки инфекции отсутствуют |
| Осложненные (инфицированные) | Имеются признаки инфекционного процесса в свище | |
| В зависимости от течения | Первичные | Свищ обнаружен впервые |
| Рецидивирующие | Процесс то утихает, то вновь активируется: развивается воспаление, появляются новые свищевые ходы или открываются старые |
Свищи делятся на первичные и хронически протекающие — рецидивирующие, когда процесс то затухает, то вновь воспаляется с образованием новых ходов и иногда закрытием старых.
Свищ прямой кишки классифицируют по отношению к анальному сфинктеру, а свищи, локализующиеся над анусом и подковой огибающие его, с открытием внутрь прямой кишки ещё и градуируют по 4 степеням сложности.
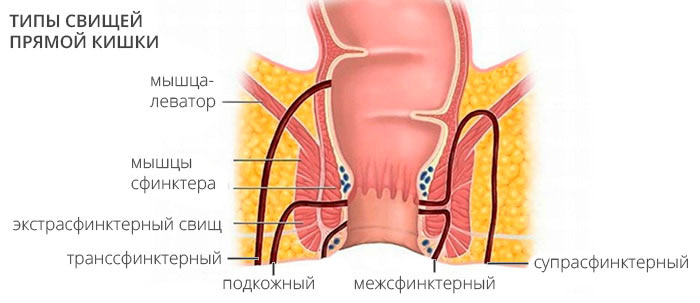
Поджелудочные полные свищи могут быть малыми с выделением до полстакана сока, средними — до 700 миллилитров и большими.
Вариантов классификаций столько, сколько существует в человеческой природе видов свищей.
Причины появления свищей
Большинство свищей формируется в результате осложненного течения воспалительного процесса: при остром панкреатите, воспалении окружающей прямую кишку клетчатке — парапроктите, язвенно-некротическом колите — болезни Крона, остеомиелите.
Деструктивные процессы внутренних органов тоже могут положить начало формированию свищевого хода, так происходит при пролежнях стенки желчного пузыря крупным камнем, когда сдавливание тканей приводит к их истончению и последующему разрыву. У трёх их четырёх женщин с желчнокаменной болезнью пролежни — ведущая причина формирования желчного свища.
Аналогичный механизм локальной деструкции тканей включается при прободении или пенетрации язвы желудка в поджелудочную железу, завершающийся открытием желудочно-поджелудочного свищевого хода.
Некоторые исследователи причиной образования свища считают ишемические изменения стенки прямой кишки при частом использовании ректальных свечей с НПВС.
Травмы операционные, родовые и спонтанные — одна из ведущих причин образования свища. Операционные травмы могут быть случайными — не замеченными при ревизии и практически микроскопическими рассечениями тканей в зоне операции и отсроченными, когда отторгаются организмом используемые в хирургии материалы: шовный шёлк или скобки степлера.
Кроме случайной хирургической травмы к свищам может привести оперативная помощь при вскрытии гнойного парапроктита. Речь не идет о неадекватной хирургии, просто это такое неблагоприятное место: плохое кровоснабжение клетчатки — основного места действия при невозможности прекращения транзита через кишку каловых масс, изобилующих кишечной микрофлорой. Нет стерильности и всегда присутствуют патогенные микроорганизмы — нет условий для заращения операционной раны.
Травмы при родах, особенно разрывы при неадекватной акушерской помощи, а также незамеченные при послеродовом осмотре повреждения — самая частая причина влагалищных фистул.
Изменение мягких тканей после давней лучевой терапии, особенно при сочетанном облучении рака шейки или тела матки, рака прямой кишки тоже может привести к формированию свищей. К формированию хода предрасполагает несколько факторов: нарушение питания тканей в результате постлучевого фиброза при наличии обильной кишечной и влагалищной микрофлоры. Постлучевые свищи довольно сложно дифференцировать с истинными злокачественными свищами, формирующимися при некрозе прогрессирующей или рецидивной злокачественной опухоли.
Кисты поджелудочной железы, наполненные едким панкреатическим секретом, способны самопроизвольно находить выход своему содержимому, расплавляя ткани ферментами и формируя свищевые ходы из брюшной полости в грудную — между поджелудочной железой и плеврой или бронхами.
Аналогичный результат, только с выходом на кожу, возможен при пункционном дренировании кистозных полостей поджелудочной железы, выполняемом с лечебной целью у ослабленного пациента, или при дренировании перекрытого камнем или опухолью общем желчном протоке.
Каждый свищ имеет свою конкретную причину и комбинацию неблагоприятных условий для заживления.
Симптомы появления
Процесс формирования свища сложно отследить, он может занимать от нескольких дней, как случается при остром панкреатите, так и несколько месяцев, как при постлучевых изменениях тканей.
Проявления на начальном этапе формирования свища обусловлены его первопричиной, как правило, местным воспалительным процессом с исходом в гнойное расплавление тканей с болью и инфильтрацией, часто интоксикацией и лихорадкой.
Вне обострения воспалительной реакции свищевой ход прощупывается как тяж. Размеры уплотнения вокруг свищевого хода обусловлены воспалительной инфильтрацией и разветвлением самих свищевых ходов, рубцовыми изменениями окружающих тканей, ранее вовлекавшимися в воспалительный конгломерат.
Сформированный свищ имеет вход и иногда выход, ткани вокруг него уплотнены, из отверстия можно выдавить отделяемое: гной, желчь, панкреатический сок и так далее. При свищевом ходе из кишки во влагалище из половых органов может вытекать кал, при соустье кишки с мочевым пузырём из ануса подтекает моча. Отделяемое из кишечного свища имеет каловый запах, гнойный секрет из влагалища тоже специфически пахнет. Особенно тяжёлым окружающим кажется запах отделяемого свища, ведущего из зоны распада злокачественной опухоли.
Воспаление вызывает болевой синдром от небольшого дискомфорта до невыносимых болей. Опухолевые свищи не болят, поскольку формируются внутри распадающегося новообразования.
При активизации инфекции с формированием затеков гнойного содержимого присоединяется общая реакция: интоксикация, высокая температура, потливость и бледность, сердцебиение и учащённое дыхание.
Методы диагностики
Диагностика простого неразветвленного одноканального свища несложна — достаточно прощупать в локальном уплотнении тяж, из которого при надавливании может потечь содержимое.
Все наружные выходы свища исследуются пуговчатым зондом, так определяется локализация ходов. Зонд вводят со стороны кожи, осторожно продвигая его до упора, если исследуется прямокишечный свищ, то внутри прямой кишки прохождение зонда определяют указательным пальцем.
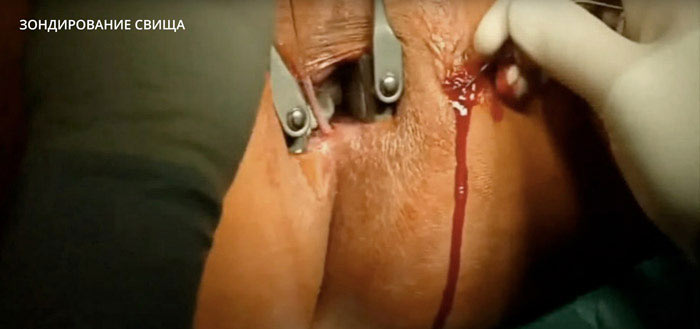
Дальше проводится проба с красящим веществом — метиленовым синим, который шприцем вводится в наружное отверстие. При ректальном свище до пробы в кишку вставляют ватный тампон, по отметкам красителя на нем определяют точное место внутреннего отверстия.
При любом свище можно фиксировать выход краски при эндоскопии: аноскопии, ректоскопии, колоноскопии, цистоскопии, кольпоскопии и так далее. Эндоскопическое обследование одно из ведущих и в процессе диагностики и лечения выполняется неоднократно.
В некоторых случаях выполняется фистулография — рентген анатомической области до и после введения в свищ контрастного вещества. Процедура не требуется только при простых и коротких свищах прямой кишки вне обострения воспаления.
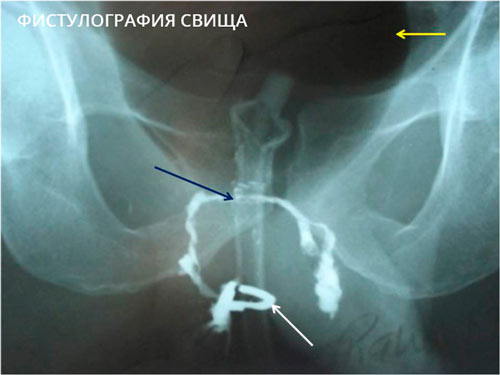
Методы визуализации, КТ и МРТ, также позволяют уточнить локализацию ходов и затеков, разветвленность и первопричину заболевания.
При вовлечении прямой кишки информативна ультрасонография (УЗИ) специальным ректальным датчиком, когда компьютерная программа позволяет увидеть патологию в трёхмерном изображении. При планировании операции дополнительно определяется функция анального сфинктера.
- Пальпация (ощупывание),
- осмотр отверстия на коже,
- исследование свища с помощью зонда,
- проба с метиленовым синим.
- Установить предварительный диагноз,
- оценить состояние пациента,
- оценить ход свища,
- выявить ответвления, карманы.
- Общий анализ крови,
- общий анализ мочи,
- биохимическое исследование крови,
- бактериологическое исследование отделяемого.
- Оценить общее состояние здоровья пациента,
- выявить возбудителей инфекционного процесса в свище, чтобы правильно подобрать антибиотики.
- Эндоскопическая диагностика: аноскопия, ректоскопия, колоноскопия, цистоскопия, кольпоскопия,
- фистулография – рентгенография после введения в свищ контрастного раствора,
- УЗИ,
- КТ,
- МРТ.
- Детально оценить свищевой ход,
- установить окончательный диагноз,
- уточнить детали в сложных случаях.
Способы лечения свищей
Свищи редко закрываются самостоятельно, на это можно надеяться только при создании благоприятных условий, к примеру, ограничении и отчасти контроле движения кала по прямой кишке с помощью очистительных клизм. В подавляющем большинстве случаев консервативная терапия неэффективна, единственный радикальный способ лечения — хирургический, то есть иссечение патологического участка в том числе и с реконструкцией недостающих тканей.
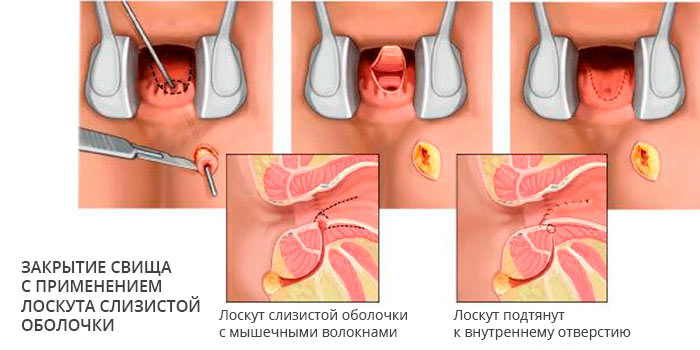
Технически простое оперативное вмешательство, в том числе эндоскопическое, и добрая сотня хирургических модификаций не может вылечить около половины пациентов, которых преследуют рецидивы. Особенно сложно добиться успеха при кишечных и мочевых свищах, поскольку они всегда контаминированы микрофлорой. В некоторых случаях приходится прибегать к формированию кишечной стомы, временно — на несколько месяцев прекращая движение каловых масс по патологически измененному участку кишки.
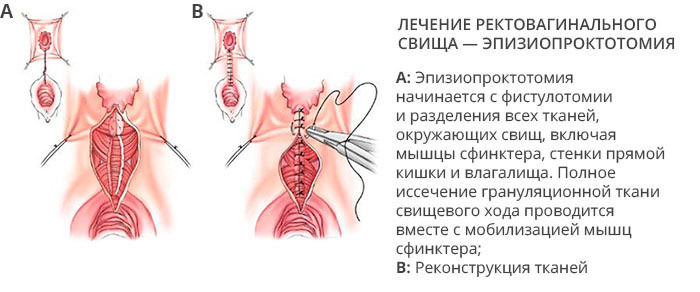
В единичных случаях прибегают к «дедовским методам» лечения с выскабливанием слизистой оболочки хода, обжигают её химическими реагентами и ферментами, добиваясь слипания стенок. Большего результата, приблизительно у 50%, добиваются введением в свищевой ход фибринового клея, склеивающего стенки.
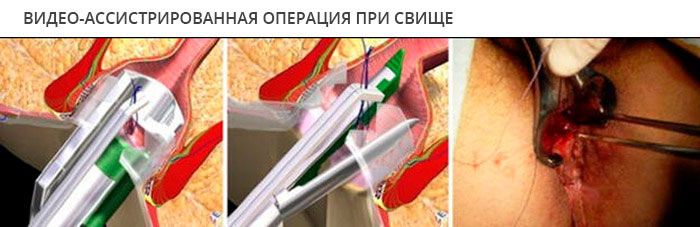
Аналогично клею действуют тампоны из биоматериалов, герметизирующие внутреннее отверстие, запустевание хода способно вызвать слипание стенок и закрытие свища.
До настоящего времени не определились с ролью антибиотиков в лечении свищей, вызванных воспалением, поскольку лекарства не способны проникнуть внутрь инфильтрата из-за массивных рубцовых изменений. Тем не менее, при свищевых ходах на фоне болезни Крона специфическая медикаментозная терапия проводится обязательно и небезуспешно.
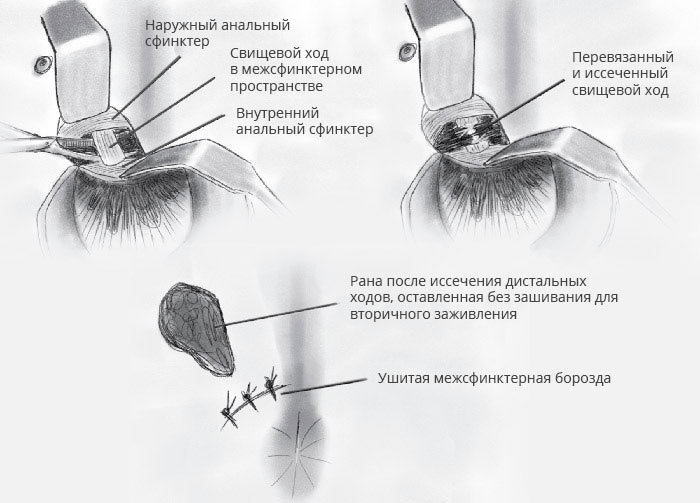
Операция при свищах методом LIFT
Профилактика свищей
Не все болезни поддаются профилактике, особенно свищи, осложнившие течение гнойного парапроктита. Тем не менее возможно адекватное лечение приводящих к парапроктиту заболеваний — геморроя и трещин, и именно это будет профилактикой образования свищей.
Осложненное течение родов не предотвратить, но качественная и своевременная акушерская помощь, внимательное отношение к женщине и тщательный послеродовый осмотр — доступная профилактическая мера.
Высокая частота постлучевых поражений тканей, прогрессирующий с течением времени фиброз, заставил онкологов отказаться от высоких доз лучевой терапии и даже изменить подходы к лечению злокачественных опухолей половой сферы.
Особое значение придается правильному выбору способа хирургического лечения заболеваний полых органов и адекватному ведению послеоперационного периода.
В нашей клинике осложненное течение заболевания — большая редкость, потому что мы не только знаем о способах профилактики, но и активно их используем.
Трофические язвы на ногах (ТЯ) являются одним из наиболее опасных осложнений сахарного диабета (СД). Они несут реальную угрозу ампутации конечности, поэтому требуют тщательно продуманного подхода к терапии. Лечение трофической язвы при сахарном диабете народными средствами не является достаточным и эффективным. Заболевание отличается склонностью к хроническому и длительному течению. Поэтому даже при использовании самых современных протоколов терапии полного заживления удается добиться только в 25-30% клинических случаев. 114
Почему при сахарном диабете появляются трофические язвы нижних конечностей?
Диабетические ТЯ возникают в результате специфического поражения микроциркуляторного русла или периферических нервов. При сахарном диабете 2 типа на стопах часто появляются натоптыши (мозоли), повреждение которых способствует образованию плохо заживающих ран. 115,116
ТЯ, как правило, локализуются на конечных фалангах пальцев стопы и могут достигать значительных размеров, глубины. Из-за большой вероятности инфицирования раны увеличивается риск ампутации конечности. 115,116
Процесс образования трофических язв при сахарном диабете начинается с гибели нервных окончаний, вследствие чего чувствительность кожи снижается. Со временем в клинической картине появляется болевой синдром (при поражении периферических нервов он отсутствует). 115,116

Лечение трофических язв на ногах при диабете
В зависимости от стадии язвенного процесса лечащий врач подбирает методы консервативной терапии.
Фаза экссудации
На начальной стадии развития лечение трофических язв направлено на санацию раны (удаление некротических тканей, патогенной микрофлоры), а также подавление воспалительной реакции. Пациентам показан полупостельный режим (10-14 дней) и постоянный контроль уровня сахара в крови.
Лечение проводится при помощи флеботоников в сочетании с дезагрегантами, а также антибактериальных и противовоспалительных препаратов. Особую важность имеет местное лечение, которое предусматривает освобождение раны от фибриновых масс и некротических тканей минимум 2-3 раза в день.
Дебридмент может быть химический, механический, биологический. На этом этапе лечения трофической язвы при сахарном диабете целесообразно применение биоразлагаемых покрытий с антибактериальными компонентами, а также антисептиков пролонгированного действия. При отсутствии артериальной недостаточности, которая характерна для венозных ТЯ, допустимо применение компрессионного трикотажа. 116

Фаза репарации
На этом этапе раневая поверхность очищается, стихает воспаление, появляются грануляции, сокращается образование экссудата. Лечение направлено на стимуляцию роста и созревания соединительной ткани. Поэтому желательно ведение раны во влажной среде с обязательным применением эластической компрессии. 116
Фаза эпителизации
Чтобы обеспечить правильную эпителизацию и рубцевание тканей, рану необходимо защитить от механических повреждений. Поэтому крайне важным становится постоянное ношение бандажа (накладывается на 5-7 дней). Рациональным считается применение раневых покрытий, которые стимулируют эпителизацию, флеботоников (курс не менее 3-х месяцев), а также проведение физиотерапевтических процедур. 116
Терапия должна быть патогенетической, своевременной, комплексной. Но чем лечить трофические язвы при сахарном диабете, может определить только специалист с учетом фазы ее развития.
Крем Акриол Про для безболезненной обработки трофических язв
Механическая обработка трофических язв – один из важнейших компонентов лечения. Но для диабетических язв типичным является выраженный болевой синдром, поэтому процедура причиняет пациентам дискомфорт.
Использование крема Акриол Про перед механической чисткой раневой поверхности позволяет достичь обезболивающего эффекта, облегчает санацию трофической язвы при сахарном диабете. В состав средства входят прилокаин, лидокаин. Оба анестетика амидные. При их использовании вероятность развития аллергической реакции крайне мала по сравнению с эфирными анестетиками – тетракаином, новокаином, пр.
Крем Акриол Про наносится на раневую поверхность толстым слоем (1-2 г/10 см 2 ) не позднее, чем за 30-60 минут до механической обработки. Обязательным является использование окклюзионной повязки. Процедуру следует начинать не позднее, чем через 10 минут после снятия повязки, при этом анестезирующий эффект сохраняется до 4 часов.


- АКРИОЛ ПРО / Статьи / Как лечить трофические язвы при сахарном диабете
Приглашаем вас посетить наш стенд на выставке InterCHARM !
Номер стенда: 14 С28

«АКРИХИН» – одна из ведущих российских фармацевтических компаний, выпускающая высококачественные и доступные по цене лекарственные препараты наиболее востребованных российскими пациентами терапевтических групп.
- Компания по объему продаж входит в пятерку ведущих локальных фармацевтических производителей на российском рынке
- Производственная площадка «АКРИХИНа» – это современный комплекс на участке площадью 36 га в 20 км от Москвы, в городе Старая Купавна
- В 2015 году «АКРИХИН» получил заключение Минпромторга РФ о соответствии требованиям надлежащей производственной практики (GMP)
- «АКРИХИН» успешно прошел более 30 международных и российских аудитов качества
1 ГРЛС, р/у ЛП-004175 от 03.03.2017
2 Сертификат GMP-0036-000221/18
3 Greveling K, Prens EP, Ten Bosch N, van Doorn MB. Comparison of lidocaine/tetracaine cream and lidocaine/prilocaine cream for local anaesthesia during laser treatment of acne keloidalis nuchae and tattoo removal: results of two randomized controlled trials. Br J Dermatol. 2016 Jul 5. doi:10.1111/bjd.14848 Hernandez E.;
4 J.Cassuto, R.Sinclair, M.Bonderovic, Anti-inflammatory properties of local anesthetics and their present and potential clinical implications. Acta Anaesthesiol Scand 2006; 50; 265-282]
5 На основании отчета IQVIA март 2018 - сентябрь 2021 г.
6 Русский медицинский журнал. Жигульцова Т.И., Паркаева Л.В., Ильина Е.Э., Виссарионов В.А.: «Опыт применения 5% крема «Эмла» в практике дерматокосметологов»
7 Инструкция по применению лекарственного препарата для медицинского применения Акриол Про
8 Т.Н. Калви, Н.Е. Уильямс. Фармакология для анестезиологов. Издательство Бином, Москва, 2007, 119-128
9 На основании отчета «анестетики в инъекционной косметологии за 2016 г.» Аналитического центра Vademecum по объему продаж.
10 Т.И. Жигульцова, к.м.н. Л.В. Паркаева, Е.Э. Ильина, профессор В.А. Виссарионов: «Опыт применения 5% крема «Эмла в практике дерматокосметологов» Косметология и пластическая хирургия. Том 16, № 9, 2008
12 В качестве окклюзионной повязки может быть использована пищевая пленка
13 Drug Release Studies on an Oil-Water Emulsion Based on a Eutectic Mixture of Lidocaine and Prilocaine as the Dispersed Phase
15 ФЗ- 532, Технический регламент Таможенного союза о безопасности парфюмерно-косметической продукции, ФЗ 61, ФЗ 532, УК РФ, ст. 235, 238, 227
16 В.В. Осипова.ММА им. И.М.Сеченова. Психологические аспекты боли. Лекция. №1/2010
17 По данным GMP News. Анализ рынка местных анестетиков, применяемых при косметологических инъекциях в 2020 году.
18 Один из видов окклюзионной повязки, а именно: бинт, пищевая пленка, лейкопластырь или прорезиненная ткань
19 Комбинация лидокаин и прилокаин в концентрации выше 0,5-2% обладают бактерицидным и противовирусным свойствами. В Акриол Про концентрация равна 5 %.
20 А.А. Степанов, Г.В. Яцык, Л.С. Намазова Метод профилактикиболи у детей раннего возраста при вакцинации //В практику педиатров- 14.09.2006 –
21 Н.В.Клипинина, РМЖ, Некоторые особенности восприятия и переживания боли детьми: взгляд психолога, репринт. 2007 .1-7
23 Gonzalez S. Evaluation of Topical Anesthetics by Laser-Induced Sensation. Lasers in Surgery and Medicine 23:167–171(1998));
24 В.Г.Лебедюк с соавторами. Анестезия в дерматокосметологии. Экспериментальная и клиническая дерматокосметология, 2010 г. № 5
25 Meltem F. Söyleva Nilüfer Koçaka Bahar Kuvakia Seyhan B. Özkanb Erkin Ki˙rb; Anesthesia with Cream for Botulinum A Toxin Injection into Eyelids. Ophthalmologica 2002;216:355–358
26 Е.В. Матушевская и авторы. Топические местные анестетики в косметологии. Клиническая Дерматология и Венерология. 03.2017 стр. 89-96
27 Therapeutics and Clinical Risk Management 2006:2(1) 99 – 113
28 Ф. Майкл Ферранте, Тимоти Р. Вейд Бопкор Послеоперационная боль. Руководство. Пер. с англ./ Под ред.. М.: Медицина, 1998.- 640 с., стр. 243
30 Wetter DA et al. J American Acad Dermatol. 2010;63(5):789-98
32 ПРИКАЗ МИНЗДРАВА РОССИИ от 08.10.2015 № 707н
34 J. ALASTAIR CARRUTHERS, MD, JEAN D.A. CARRUTHERS, MD. Safety of Lidocaine 15% and Prilocaine 5% Topical Ointment Used as Local Anesthesia for Intense Pulsed Light Treatment. Dermatologic Surgery 2010;36:1130–1137
35 Ya-Xian et al. Количество клеток в роговом слое нормальной кожи в зависимости от анатомического расположения на теле, возраста, пола и физических параметров Archives Dermatol Res 1999; 291 :555–559.
36 Дж Морган, Мэгид С.Михаил. Клиническая анестезиология, Книга 1. Бином. Москва Санкт-Петербург, 2001 г.
37 Arendt-Nielsen L, Bjerring P, Nielsen J. Acta Derm Venereol 1990;70:314-318
38 Белорусский государственный медицинский университет. 2-я кафедра терапевтической стоматологии. Терапевтическая Стоматология. Часть 1. Под ред. А.Г.Третьяковича, Л.Г.Борисенко.
39 Dermatol Surg 1999;25:950-954
40 К. Greveling et al. Br J Dermatol 176 (1), 81-86. 2016 Dec 10
41 Juhlin and Evers Adv Dermatol 1990;5:75-92
42 Arendt-Nielsen L, Bjerring P, Nielsen J. Acta Derm Venereol 1990;70:314-318
43 Study Desensor 001. Wahlgren CF, Quiding H. J Am Acad Dermatol 2000;42:584-8.
45 Руководство по дерматокосметологии под редакцией Е.Р.Аравийской и Е.В.Соколовского. СПБ: ООО "Издательство Фолиант", 2008 - 632 с
51 Radman et al.2002, Yamashita., 2003
54 МАСМИ. Исследование пользователей анестетиков для кожи. Июнь 2018 г.
55 О.М.Бурылина, А.В.Карпова. Косметология. Клиническое руководство. ГЭОТАР-Медиа. Москва, 2018
57 Paul M. Friedman, MD, Jushua P.Fogelman, MD and others. Comperative Study of the Efficacy of Four Topical Anesthetics. Dermatolog Surg 1999; 25:950-954
63 Comparison of Topical Anesthetics for Radiofrequency Ablation of Achrocordons: Eutectic Mixture of Lignocaine/Prilocaine versus Lidocaine/Tetracaine Pratik Gahalaut,1 Nitin Mishra,1 Sandhya Chauhan,2 and Madhur Kant Rastogi11Department of Dermatology, Venereology and Leprosy, Shri Ram Murti Smarak Institute of Medical Sciences, Nainital Road, Bareilly 243001, India2Department of Pediatrics, Shri Ram Murti Smarak Institute of Medical Sciences, Nainital Road, Bareilly 243001, India
76 Моррисон А.В., Бочарова Ю.М., Моррисон В.В. Токсин ботулизма — лечебный эффект в косметологии (обзор). Саратовский научно-медицинский журнал 2016; 12 (3): 521–524.
77 А.В. Гара, В.Г. Золотарева, Особенности проведения ботулинотерапии по эстетическим показаниям пациенткамстарше 45 лет, Инъекционные методы в косметологии No 4-2011 – 54-60 с
78 Методическое пособие по мезотерапии для слушателей послевузовского и дополнительного профессионального образования. / Шамов Б. А., Дядькин В.Ю., Желонкина Т.И./ – Казань: КГМУ, 2011. – 60с.
98. Внутриочаговая интерферонотерапия рецидивирующих бородавок, Г. Э. Баграмова, Т.Г. Седова, А.Н. Хлебникова // Российский журнал кожных и венерологических заболеваний №1, 2013 – 23-26 с.
99. Королькова Т.Н., Гома С.Е. Изучение влияния мезотерапии пептидами эпифиза на влажность и эластичность кожи, Российский журнал кожных и венерических болезней. 2017; 20(5) – 305-310 с.
100. С.В. Ключарева, С.М. Никонова, И.В. Пономарев, Лечение лазерами доброкачественных пигментных новообразований кожи, экспериментальная и клиническая дерматокосметология №3, 2006 – 22-31 с.
101. Фотоомоложение в комплексной коррекции возрастных изменений кожи, Н.И. Цисанова, Журнал по прикладной эстетике №1, 2007г
119. Аралова М.В. Персонализированная технология регионального лечения больных с трофическими язвами нижних конечностей. Дис. на соискание ученой степени д.м.н. Воронеж, 2019
121. Hansson C et al. Acta Derm Venereol (Stockh) 1993;73:231-233.
122. Приказ Минздрава России от 13.10.2017 № 804н «Об утверждении номенклатуры медицинских услуг.
123. Приказ Министерства здравоохранения от 08.10.2018 № 707н «Об утверждении Квалификационных требований к медицинским и фармацевтическим работникам с высшим образованием по направлению подготовки «Здравоохранение и медицинские науки»
124. 124. Старостина Л.С. Помощь в контроле боли у детей: советы педиатра. Медицинский совет. 2021;(1):263–268. doi: 10.21518/2079-701X-2021-1-263-268
Большинство хирургических вмешательств заканчивается наложением швов. В ряде случаев вокруг шовных нитей, лигатур, развивается гнойное воспаление с последующим формированием свищей, которые необходимо удалять.

Лигатурный свищ, согласно статистическим данным, диагностируется у 5% пациентов, перенесших различные хирургические операции. Определенно чаще возникает после оперативных вмешательств, проводимых на полых органах малого таза и брюшной области, что вызвано высокими рисками инфицирования окружающих здоровых тканей даже при неукоснительном соблюдении требований асептики. Так, распространенность глубоко лигатурного свища после гинекологических операций составляет 9%, после вмешательств в связи с язвенной болезнью желудка и двенадцатиперстной кишки – 7,8%.
Характерные особенности глубоких лигатурных свищей:
- возникают в абсолютно любой части человеческого тела;
- образуются во всех видах ткани (мышечная ткань, эпидермис);
- возникают в любое время после проведения оперативного вмешательства;
- имеют разное течение клинической картины (отторжение швов может протекать как с заживлением раны, так и с интенсивным развитием воспалительного процесса и нагноением раневой области);
- образуются при любом материале лигатурных нитей.
Лигатурные свищи при использовании разных видов шовного материала
Глубокие лигатурные свищи образуются преимущественно при отторжении организмом нерассасывающихся лигатурных нитей, однако зафиксированы случаи развития данной патологии и при применении рассасывающегося шовного материала. Чаще всего патологическое состояние вызывается шелковыми, капроновыми и лавсановыми нитями. Реже лигатурные свищи вызываются проленовыми или викриловыми нитями.
- Реакция иммунного отторжения. Для иммунных клеток нить, которую они рассматривают в качестве инородного, потенциально опасного тела, выступает в качестве мишени. В этой связи шовный материал не покрывается капсулой.
- Прошивание полого органа. Возникает при нарушении техники проведения оперативного вмешательства, в ходе которого нить попадает в просвет полого органа. В результате контакта с содержимым органа, которое априори является нестерильным, происходит инфицирование нити с последующим распространением патогенных микроорганизмов по всей ее длине.
Возможные осложнения глубокого лигатурного свища:
- Абсцесс. Гнойное воспаление тканей, приводящее к образованию гнойной полости.
- Флегмона. Протекающий в жировой клетчатке гнойный процесс, склонный к стремительному распространению на окружающие здоровые ткани.
- Сепсис. Второе название – заражение крови. Представляет собой инфекционное заболевание, характеризующееся проникновением патогенных микроорганизмов из первичного очага инфекции в кровяное русло.
Показания к вскрытию

Образованию свища предшествует воспалительное уплотнение вокруг шовного материала, обусловленное миграцией лейкоцитов и усиленным образованием коллагена. Затем на фоне уплотнения образуется небольшая замкнутая полость с серозным экссудатом, воспалительным выпотом. На фоне воспаления отмечается покраснение и отек кожи, местное повышение температуры, нередко – повышением температуры тела и ухудшение общего состояния.
Затем полость самопроизвольно вскрывается с образованием свищевого хода, который включает в себя фрагмент лигатуры. Через свищевой ход выделяется серозный экссудат. Спустя некоторое время экссудат становится гнойным. Образованию свищей способствуют:
- несоблюдение правил асептики;
- индивидуальная непереносимость шовного материала;
- обменные расстройства – сахарный диабет, авитаминозы, общее истощение (кахексия) с дефицитом белка;
- сопутствующие тяжело протекающие заболевания внутренних органов;
- иммунодефицитные состояния или наоборот, высокая иммунореактивность;
- общее тяжелое состояние пациента;
- пожилой возраст.
Сроки формирования лигатурных свищей варьируют в широких пределах, от нескольких месяцев до нескольких лет, и даже до года после операции. Свищи могут развиваться повсеместно: на коже и на слизистых оболочках, а также в подкожном слое, мышцах, фасциях, и на внутренних органах. При этом частота их возникновения не зависит от лигатурного материала.
В некоторых случаях свищевые ходы закрываются самопроизвольно без лечения, что может быть истолковано как заживление свища. Однако спустя некоторое время свищ рецидивирует, его ход открывается, и гной вновь выходит наружу. Хроническое гнойное воспаление может полечь за собой формирование гнойных очагов – абсцессов и флегмон с дальнейшим развитием сепсиса.
Если лигатурный свищ возник на брюшной стенке после операции на органах брюшной полости, возможна эвентерация – расхождение швов и выпадение наружу внутренних органов. Все это указывает на невозможность самостоятельного излечения лигатурного свища и необходимость хирургического вмешательства.
Методика

Сначала врач осматривает место болезни и оценивает характер и протяженность гнойного воспаления, наличие гнойных очагов и затеков. С этой целью иногда прибегают к фистулографии – в свищевые ходы вводят рентгенконтрастное вещество, а затем выполняют рентгенографию.
Вскрытие свища осуществляется под местной анестезией. После предварительной обработки кожи антисептиком врач рассекает рану и удаляет имеющийся шовный материал. Попутно коагулируют кровоточащие сосуды. Свищевое образование вместе со стенками и ходами удаляют полностью в пределах здоровых тканей. Имеющиеся гнойные затеки обязательно вскрывают. Образовавшуюся рану полностью промывают растворами антисептиков и дренируют.
Вторичные отсроченные швы накладывают лишь после того как прекратится отхождение серозного и гнойного отделяемого по дренажам. До этого времени проводятся ежедневные перевязки со сменой дренажей, пациент принимает антибиотики, противовоспалительные и общеукрепляющие средства, витамины.
Лигатурный свищ далеко не всегда обусловлен нарушением асептики, неправильной техникой наложения швов, и другими врачебными ошибками. Поэтому даже грамотное удаление свища не всегда гарантирует от рецидивов.
Особенности лечения
Чем более длительнее период существования глубокого лигатурного свища, тем сложнее добиться полного излечения пациента. Для эффективности лечения, наряду с проведением оперативно вмешательства, показано проведение комплексной терапии с использованием препаратов различных групп:
- антибактериальные средства;
- местные антисептики;
- ферментативные препараты, направленные на деструкцию омертвевших тканей.
Нередко в дополнении к оперативному и медикаментозному методам терапии специалист назначает проведение физиотерапевтических процедур:
- УВЧ-терапия. Процедура оказывает благоприятное воздействие на процессы микроциркуляции лимфы и крови, что позволяет добиться снижения отека и предотвращает распространение инфекции.
- Кварцевание поверхности раны. Процесс кварцевания оказывает пагубное воздействие на представителей патогенной микрофлоры, тем самым способствуя достижению стойкой ремиссии. Однако данный метод физиотерапии не может гарантировать полное выздоровление пациента.
Особенности послеоперационного периода

В послеоперационном периоде важно строго соблюдать все данные врачом рекомендации. Послеоперационная рана должна подлежать регулярной обработке антисептиками и медикаментами, ускоряющими регенерацию тканей. Кроме того, в это время необходимо:
- принимать назначенные врачом лекарственные препараты;
- выполнять перевязку раневой области;
- контролировать чистоту повязки (загрязненная повязка может стать причиной инфицирования раны);
- не допускать попадания на рану воды (при намокании повязки показана незамедлительная перевязка);
- посещать врача для оценки состояния процесса заживления раневой области;
- соблюдать диету, рекомендованную специалистом;
- отказаться от посещения бассейна, сауны, бани, солярия;
- исключить физическую активность;
- воздержаться от употребления спиртных напитков.
Когда требуется врачебная помощь?
В послеоперационном периоде пациенту необходимо особенно внимательно относится к своему состоянию, ведь любые негативные изменения могут свидетельствовать о течении воспалительного процесса. К числу общих тревожных симптомов относятся:
- повышение показателей температуры тела;
- слабость, головокружение, обмороки;
- рвота, тошнота.
Также пациенту надлежит следить за состоянием послеоперационной раны. Негативными проявлениями в этот период считаются:
- покраснение кожи в области раны;
- отечность пораженной зоны;
- гнойные или кровяные выделения из раны;
- усиливающаяся боль в области раны;
- расхождение медицинских швов.
Сколько длится период заживления и когда показано снятие швов
Снятие медицинских швов производится исключительно при условии полного заживления раневой области, которое диагностируется при плотном срастании краев раны. На продолжительность периода заживления оказывают влияние такие факторы как:
Читайте также:

