Как измеряют билирубин через кожу
Обновлено: 05.05.2024
Оценка способности печени транспортировать органические анионы и метаболизм ксенобиотиков
Билирубин
Билирубин — продукт катаболизма гемовых соединений. Ежедневно вырабатывается 250-350 мг билирубина. Его концентрация в сыворотке зависит от:
- эффективность сосудистого полюса печеночной клетки;
- усиление этерификации билирубина (глюкуроновой, серной, тауриновой кислотами);
- эффективность желчного полюса гепатоцитов;
- желчная непроходимость.
Причины повышения билирубина
Нарушения образования или метаболизма билирубина приводят к повышению уровня билирубина в сыворотке крови. Наиболее частые причины:
- Чрезмерный распад эритроцитов (гемолиз) или образование непрямого билирубина из негемоглобинового гема или его предшественников в обход основного пути метаболизма (так называемая шунтирующая гипербилирубинемия);
- Нарушение всасывания билирубина клеткой печени из-за нарушения функции сосудистого полюса гепатоцита.
Это происходит при следующих состояниях:
- Негемолитическая врожденная гипербилирубинемия (синдром Жильбера);
- Токсическое поражение печени;
- Вирусное поражение печени;
- Нарушение конъюгации билирубина с гликуроновой, серной, тауриновой кислотами в гепатоците в результате:
- Дефицит UDP-глюкуронилтрансферазы при негемолитической врожденной гипербилирубинемии (синдром Криглера-Наджара типа II);
- Прием некоторых лекарств (включая хлорамфеникол, хлорамбуцил, стрептомицин, прогестерон, рифампицин);
- Повреждение печени токсинами или вирусами;
- Нарушение транспорта глюкуронатов, сульфатов и тауратов билирубина при негемолитической врожденной гипербилирубинемии (синдром Дубина-Джонсона, синдром Ротора);
- Повреждение гепатоцитов и их секреторного полюса из-за:
- Воспаление (вирусное, токсическое или лекарственное);
- Жирная печень;
- Цирроз печени;
- Нарушение транспорта билирубина во внутри- и внепеченочном тракте, вызванное холестазом (поражение более 2/3 желчных протоков проявляется желтухой).
Свободный и связанный билирубин
Биохимическая реакция Ван ден Берга позволяет идентифицировать две фракции билирубина:
- Свободный (неконъюгированный, переносится в крови с альбумином) — иначе известный как непрямой;
- Связанный (конъюгированный с глюкуроновой, серной, тауриновой кислотами) — иначе известный как прямой.
В нормальных условиях общий билирубин сыворотки составляет 0,2–1,2 мг / дл (3,4–20,5 мкмоль / л); > 80% — это непрямой билирубин. Причины повышения непрямого билирубина в сыворотке крови это:
- усиление распада красных кровяных телец;
- нарушение всасывания билирубина в печеночную клетку;
- нарушение кислотно-билирубиновой конъюгации.
Другие нарушения, особенно заболевания печени и желчевыводящей системы с холестазом, характеризуются гипербилирубинемией со значительным повышением прямого билирубина.
В клинической практике чаще всего определяют концентрацию общего билирубина, определение концентрации отдельных фракций важно при диагностике негемолитической врожденной гипербилирубинемии:
- При синдроме Криглера-Наджара I и II типа и при синдроме Жильбера наблюдается гипербилирубинемия с избытком непрямого билирубина;
- При синдроме Дубина-Джонсона и синдроме Ротора, характеризующемся гипербилирубинемией с преобладанием прямого билирубина.
Соотношение концентрации прямого и общего билирубина
Отношение концентрации прямого билирубина к уровню общего билирубина оказалось важным при диагностике острого поражения печени. Используется как прогностический фактор при остром поражении печени (независимо от этиологии): прогноз неблагоприятный, если он превышает 0,3.
Желчные кислоты
Общая концентрация желчных кислот (первичная и вторичная) более чувствительна при оценке транспортной способности печени, а также процессов секреции и резорбции. Общие концентрации желчных кислот в сыворотке крови определяют натощак (в норме
Повышение концентрации желчных кислот происходит при:
- Паренхиматозные заболевания печени;
- Внепеченочный холестаз;
- Внутрипеченочный холестаз у беременных (характерны высокие значения, превышающие норму в 10-100 раз).
Аммиак
При тяжелом поражении печени наблюдаются нарушения выведения аммиака из организма и повышение его сывороточной концентрации. Аммиак — продукт дезаминирования аминокислот; служит субстратом для производства мочевины и, таким образом, устраняется.
- 27-102 мкг / дл (16-60 мкмоль / л) у мужчин;
- 19-87 мкг / дл (11-51 мкмоль / л) у женщин.
Концентрация аммиака определяется при диагностике печеночной энцефалопатии. Симптомы энцефалопатии при тяжелом поражении печени появляются, когда концентрация аммиака превышает 150 мкг / дл и коррелируют с тяжестью заболевания. При печеночной коме концентрация аммиака превышает 300 мкг / дл.
Оценка дезинтоксикационной активности и лекарственной трансформации
Дыхательный тест на аминопирин
Этот тест очень чувствителен при диагностике метаболической функции печени. Аминопирин метаболизируется почти исключительно микросомальной окислительной системой гепатоцитов.
После перорального приема аминопирина, меченного углеродом, через различные интервалы времени определяют концентрацию радиоактивного диоксида углерода в выдыхаемом воздухе. Поскольку это нетипичный биохимический тест, его рассмотрение выходит за рамки данной главы.
Оценка метаболизма соединительной ткани
Концентрация проколлагенового пептида III типа (P-III-P) используется для оценки фиброза и используется для определения степени тяжести цирроза.
Диагностика рака печени
При диагностике гепатоцеллюлярной карциномы измеряется α-фетопротеин (AFP). Это α 1 -глобулин, продуцируемый в печени плода и в небольших количествах другими клетками желудочно-кишечного тракта плода, а у взрослых — опухолевыми клетками, происходящими из гепатоцитов, но также встречается при остром и хроническом гепатите, циррозе и метастазах рака в печень. Норма ≤5 нг / мл, концентрация> 20 нг / мл — показание к ультразвуковому исследованию печени,> 400 нг / мл — гепатоцеллюлярная карцинома.
Диагностика асцита
Биохимические лабораторные тесты полезны для диагностики этиологии асцита при асците
- Количество гранулоцитов; например, идиопатическое бактериальное воспаление диагностируется не только на основании бактериологических тестов — асцитическая жидкость, собранная во время диагностического парацентеза, показывает высокий плеоцитоз (> 250 нейтрофилов с полиморфным ядром в мм 3). Причем источник инфекции не может быть обнаружен в брюшной полости;
- Активность ЛДГ — помогает различать экссудат (высокая активность ЛДГ) и транссудат (низкая активность ЛДГ);
- Уровни белка и холестерина (в асцитной жидкости и сыворотке); отношение концентрации белка и холестерина в плазме к их концентрации в перитонеальной жидкости> 4 указывает на транссудатный характер жидкости, значения
- Сывороточный альбумин и асцитная жидкость; градиент альбумина (SAAG), то есть разница в концентрации альбумина в сыворотке и асцитической жидкости — это важный биохимический индикатор портальной гипертензии. SAAG> 11 г / л предполагает асцит, связанный с портальной гипертензией (обычно при циррозе, патологии сосудов печени или сердечной недостаточности). Значения
Серологические исследования

Серологические исследования
Серологические тесты проводятся для выявления этиологических факторов заболевания печени. Наиболее часто ищутся серологические маркеры вирусных гепатитов HAV, HBV, HCV, HDV, HEV, цитомегаловирус (CMV) и вирус Эбштейна-Барра (EBV).
Инфекция HAV
Диагноз гепатита А основан на определении наличия в сыворотке крови:
- РНК ВГА;
- Анти-ВГА IgM (анти-ВГА IgG указывают на инфекцию и служат свидетельством приобретенного иммунитета).
Инфекция HBV
Диагноз гепатита В ставится на основании ряда серологических тестов, включая определение в сыворотке крови:
- ДНК ВГВ;
- HBsAg;
- HBeAg;
- IgM и IgG анти-HBs;
- IgM и анти-HBc IgG.
Инфекция ВГС
Диагностика ВГС-инфекции включает определение:
Инфекция HDV
Диагноз гепатита D предполагает определение:
- РНК HDV;
- HDAg;
- IgM к HDV;
- IgG к HDV.
Инфекции другими гепатотропными вирусами
При серологической диагностике других вирусных гепатитов определяются специфические IgM и IgG (например, анти-CMV IgM и IgG, анти-EBV IgM и IgG).
Аутоиммунный гепатит
При диагностике аутоиммунного гепатита в сыворотке измеряют неспецифические антитела, при рутинной диагностике это:
- Антиядерные антитела (ANA);
- Антитела против гладких мышц (ASMA — антитела против гладких мышц);
- Антитела к микросомальным антигенам печени и почек (LKM-1 — антитела к микросомам печени и почек);
- Растворимые антитела печени (SLA).
Иногда дополнительно отмечают:
- Антитела против цитоплазматических антигенов нейтрофилов (ANCA — антинейтрофильные цитоплазматические антитела);
- (Относительно редко) антитела против рецепторов асиалогликопротеинов (ASGP-R — антитела к рецепторам асиалогликопротеинов);
- (Также редко) антитела против цитозоля печени (LC1).
Антимитохондриальные антитела (АМА) — это основной параметр иммунологической диагностики первичного билиарного цирроза.
Резюме
Лабораторная диагностика заболеваний верхних и нижних отделов желудочно-кишечного тракта носит вспомогательный характер, в основе лежат визуальные и морфологические исследования.
Биохимическая основа диагностики целиакии — серологические тесты, то есть определение антител:
- против эндомизма (EmA);
- против тканевой трансглутаминазы (тТГ).
Биохимические тесты, включая определение активности липазы и амилазы в сыворотке и моче, играют ключевую роль в диагностике острого панкреатита.
Диагноз хронического панкреатита основывается в основном на визуализирующих исследованиях, при этом лабораторные тесты имеют второстепенное значение.
Диагностика патологии печени во многом основывается на лабораторных показателях. Высокая активность индикаторных ферментов свидетельствует о поражении паренхимы печени, а повышенная активность выделительных ферментов — о патологии желчевыводящей системы, например, холестазе.
Обратный индекс де Ритиса (АСТ / АЛТ> 1) может указывать на алкогольную болезнь печени.
Серологические тесты проводятся для поиска причины заболевания печени.
Чрескожное исследование билирубина у новорожденных. Показания
1. Желтуха возникает у большинства новорожденных. Билирубин в высоких концентрациях оказывает токсическое действие на нервную систему, вызывая билирубиновую энцефалопатию и ядерную желтуху.
2. Обязательное обследование следует проводить у всех новорожденных перед выпиской в целях выявления тяжелой гипербилирубинемии и обеспечения соответствующего наблюдения. Для этого проводят измерение общего билирубина сыворотки (ОБС) или чрескожное измерение билирубина.
3. Клиническое наблюдение за течением желтухи дает неточную оценку.
4. Чрескожное измерение отраженного от кожи и подкожных тканей света с помощью билирубинометров — объективный неинвазивный способ оценки степени желтухи новорожденных, косвенно свидетельствующий о величине ОБС.
5. Чрескожные билирубинометры используют преимущественно для скрининга выраженной гипербилирубинемии у доношенных и недоношенных новорожденных.
6. В США в настоящее время разрешено использование двух чрескожных билирубинометров. Несмотря на разные технологии, используемые при создании этих приборов, принципы их работы в целом сходны:
а. Аппарат для исследования выраженности желтухи «Konica Minolta/Air-Shields JM-103» (Drager Medical, Telford, PA, USA).
б. Аппарат для неинвазивного исследования концентрации билирубина «BiliChek» (Children's Medical Ventures/Respironics, Norwell, MA, USA).
7. С помощью обоих билирубинометров проводят чрескожное измерение билирубина. Их данные коррелируют со значениями ОБС при уровне меньше 15 мг/дл у доношенных и недоношенных новорожденных, возможны более широкие вариации при более высоких уровнях билирубина.

Показания для чрескожного исследования билирубина
1. Чрескожное измерение билирубина проводят в следующих случаях:
а. В качестве рутинного обследования перед выпиской на 1-4-й день жизни у доношенных и недоношенных новорожденных для оценки риска развития тяжелой гипербилирубинемии с помощью использования номограммы почасового (от рождения) уровня билирубина.
б. Для повторной неинвазивной оценки прогрессирования желтухи у доношенных и недоношенных новорожденных.
в. При развитии желтухи в первые сутки жизни.
г. При клинических проявлениях желтухи, не соответствующих возрасту данного новорожденного.
2. Исследование ОБС в дополнение к другим исследованиям при диагностике патологии, вызвавшей гипербилирубинемию, показано в следующих случаях:
а. Во время фототерапии или при быстром увеличении ОБС.
б. Концентрация ОБС соответствует уровню для проведения обменного переливания крови или при отсутствии эффекта от фототерапии.
в. Повышенный уровень прямого билирубина.
г. Развитие желтухи в возрасте 3 нед или старше.
д. При других заболеваниях или у недоношенных новорожденных при сроке гестации 35 нед и меньше.
Ограничения чрескожного исследования билирубина
1. Чрескожное измерение билирубина — скрининговый метод, необходим для выявления тех новорожденных, которым показано исследование ОБС. На основании его результатов не следует принимать решения о лечении.
2. На основании двух крупных исследований пациентов со значениями ОБС более 15 мг/дл с помощью устройств «BiliChek» и «JM-103» показано, что точность чрескожного измерения билирубина недостаточна.
3. Достоверность данных чрескожного измерения билирубина снижается при фототерапии или после операции заменного переливания крови. Не рекомендуется использовать чрезкожное измерение билирубина в течение суток после одного из этих методов лечения:
а. Под воздействием фототерапии изменяется химическая структура билирубина в подкожных тканях, превращая его в водорастворимое вещество. Результаты чрескожного измерения билирубина после фототерапии могут быть недостоверны, так как значительное снижение количества подкожного билирубина не всегда сопровождается его снижением в сыворотке.
б. Данные исследования показали, что коэффициент корреляции снижается от 0,90 перед фототерапией до 0,85 после ее начала.
Эта тенденция сохраняется на протяжении всего курса фототерапии, при этом коэффициент корреляции достигает значения 0,33 у новорожденных, получающих фототерапию дольше 48 ч.
4. Результаты чрескожного измерения билирубина менее точные у недоношенных новорожденных:
а. При сравнении результатов системы «BiliChek» с измерением ОБС коэффициент корреляции составляет 0,86 у недоношенных, не получавших фототерапии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Методика чрескожного исследования билирубина. Рекомендации
1. В нашей стране в настоящее время используют две модели билирубинометров для чрескожного измерения билирубина:
а. Измеритель «Konica Minolta/Air-Shields JM-103» (Drager Medical, Telford, PA, USA):
- Принцип работы основан на измерении разницы между оптическими плотностями света в синем и зеленом частях спектра.
- Измерительный датчик имеет два оптических канала.
- На основании расчета разницы между оптическими плотностями вычисляют части, общие для эпидермиса и дермы. В итоге могут быть получены различия только для подкожных тканей.
- Теоретически позволяет измерять степень желтизны кожи и подкожных тканей при минимальном влиянии меланинового пигмента и зрелости кожи.
- Линейная корреляция данных с ОБС — основание для перевода полученных измерений в ОБС прибором, что отражается на цифровом экране.
б. Неинвазивный анализатор билирубина «BiliChek» (Children's Medical Ventures/Respironics, Norwell, MA, USA):
- Устройство состоит из источника света, микроспектрофотометра, оптоволоконного датчика и микропроцессорной схемы управления.
- Используется весь спектр видимого света, отраженного от кожи.
- Отраженный от кожи свет воспринимается и анализируется.
- В алгоритме вычисления учитывают действие гемоглобина, меланина и толщины кожи.
- Поглощение света билирубином в капиллярном ложе и подкожных тканях рассчитывают с помощью спектрального вычитания.
На что обратить внимание при организации чрескожного исследования билирубина у новорожденных?
1. Во внутрибольничном протоколе должны быть определены состояния, при которых необходимо проводить чрескожное измерение билирубина и исследование ОБС.
2. При тяжелой желтухе обоснованием обменного переливания крови является только уровень ОБС.
3. Чрескожное измерение билирубина — менее точный метод исследования после фототерапии. В целях мониторинга значений билирубина следует измерять ОБС.
4. Результаты измерений, полученные с помощью «BiliChek», не зависят от расы и цвета кожи. У чернокожих новорожденных корреляция значений чрескожного измерения билирубина, полученных с помощью «JM-103», и уровня ОБС менее тесная. Считают, что чрескожное измерение билирубина имеет большее значение по сравнению с ОБС.
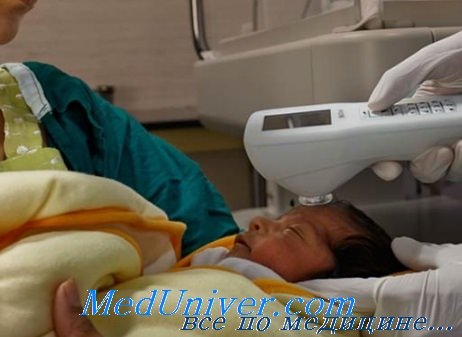
Методика чрескожного исследования билирубина:
1. Калибруют устройство чрескожного измерения билирубина в соответствии с инструкциями производителя.
2. Проводят измерение. Для этого нажимают на кнопку запуска и осторожно прижимают кончик устройства ко лбу младенца или грудине до окончания измерения и получения данных.
3. По данным некоторых исследований, корреляция результатов чрескожного измерения билирубина, полученных с грудины, и уровня ОБС несколько выше по сравнению с данными с лобной области. Возможно, на результат измерения со лба влияет окружающий свет. Однако в других исследованиях разницы в месте измерения не обнаружено.
4. Повторные измерения следует проводить в том же месте размещения датчика и с одинаковой силой давления на прилагаемое устройство.
Минимизировать влияние на результат можно с помощью соответствующих тренировок.
5. Исследование с помощью системы «BiliChek» занимает приблизительно 20-80 с. За это время аппарат производит пять измерений и высчитывает среднее значение. Анализатор «JM-103» выполняет двойное измерение и расчет примерно за 10 с.
6. Не следует использовать повторно одноразовые датчики.
Осложнения чрескожного исследования билирубина
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Причина желтухи у новорожденного младенца. Как определить?
У более 60% новорождённых отмечается видимая желтушность. Это является следствием того, что:
• имеется значительный физиологический выброс Нb из разрушенных эритроцитов (в результате повышается концентрация Нb) при рождении;
• период жизни эритроцитов у новорождённых (70 дней) значительно короче, чем у взрослых (120 дней);
• метаболизм билирубина печени в первые дни жизни недостаточно эффективен.
Желтуха новорождённых имеет большое значение.
• Она может быть признаком другого заболевания, например, гемолитической анемии, инфекции, метаболических нарушений.
• Неконьюгированный билирубин может откладываться в головном мозге, особенно в базальных ганглиях, приводя к ядерной желтухе.
Ядерная желтуха - это энцефалопатия в результате отложения неконъюгированного билирубина в базальных ганглиях и ядрах ствола головного мозга. Она может происходить, если уровень неконъюгированного билирубина превышает альбуминсвязывающую способность билирубина в крови. Поскольку свободный билирубин жирорастворим, он может проникать через гематоэнцефалический барьер. Нейротоксические эффекты варьируют в тяжести от транзиторного нарушения до катастрофического повреждения и смерти. Острыми проявлениями являются летаргия и низкое питание.
В тяжёлых случаях отмечается раздражительность, увеличение мышечного тонуса, что приводит к тому, что ребёнок лежит с выгнутой спиной (опистотонус), развитию судорог и комы. У выживших младенцев могут развиваться хореоидатетоидный церебральный паралич (в результате повреждения базальных ганглиев), нарушения обучения и нейросенсорная тугоухость.
Ядерная желтуха ранее была важным фактором поражения головного мозга у младенцев с тяжёлой резус-гемолитической болезнью, однако после введения в профилактических целях анти-D иммуноглобулина матерям с отрицательным резус-фактором она стала редкой.
Клинически желтуха проявляется у младенцев, если уровень билирубина достигает 80-120 ммоль/л. Лечение варьирует в зависимости от гестационного возраста младенца, возраста начала, уровня билирубина, темпа подъёма и общеклинического состояния.

Возраст начала проявления указывает на вероятную причину желтухи:
I. Желтуха до 24 ч после рождения:
Гемолитические нарушения
Резус-конфликт
Несовместимость АВО
Дефицит Г-6-ФД
Сфероцитоз, дефицит пируват-киназы
Врождённые инфекции
II. Желтуха между 24 ч и 3 нед после рождения:
Физиологическая желтуха
Желтуха от грудного молока
Инфекции, например ИМП
Гемолиз, например, дефицит
Г-6-ФД, несовместимость АВО
Кровоизлияния
Полицитемия
Синдром Криглера-Найяра
III. Желтуха через 3 нед после рождения:
Неконъюгированная гипербилирубинемия
Физиологическая желтуха или желтуха от грудного молока
Инфекции (особенно ИМП)
Гипотиреоз
Гемолитическая анемия, например дефицит Г-6-ФД
Высокая обструкция ЖКТ
Конъюгированный (>20% общего билирубина)
Обструкция желчевыводящих путей
Неонатальный гепатит
Желтуха менее 24 ч после рождения
Желтуха, возникающая в первые 24 ч после рождения, обычно является результатом гемолиза. Её особенно важно выявить, поскольку билирубин является неконъюгированньш и уровень его может возрастать очень быстро и достигать чрезвычайно высоких значений.
Резус-гемолитическая болезнь. Поражённые младенцы обычно выявляются в антенатальном периоде, контролируются и лечатся, если возможно. Рождение ребёнка с тяжёлым поражением, анемией, водянкой и гепатоспленомегалией с быстроразвивающейся тяжёлой желтухой стало редкостью. Могут появляться антитела к резус-антигенам, отличным от D, и к группам крови Келли и Даффи, однако гемолиз обычно менее выражен.
Несовместимость АВО. Сейчас это более распространено, чем резус-конфликт. Большинство антител к АВО являются IgM и не проникают через плаценту, однако у некоторых женщин с группой крови «0» имеются анти-А-гемолизиновые IgG в крови, которые могут проникать через плаценту и приводить к гемолизу эритроцитов у младенцев с группой крови «А».
Иногда у младенцев с группой крови «В» может быть поражение анти-В гемолизинами. Гемолиз может вызвать тяжёлую желтуху, однако обычно менее тяжёлую, чем при резус-конфликте. Уровень Нb у младенцев обычно нормальный или незначительно снижен и, в отличие от резус-конфликта, при нём отсутствует гепатоспленомегалия. Желтуха обычно достигает пика в первые 12-72 ч.
Дефицит глюкозо-6-фосфатдегидрогеназы (Г-6-ФД). Средиземноморские и средне- и дальневосточные и афро-американские варианты заболевания могут вызывать желтуху в неонатальном периоде. Родителям поражённых детей должен быть выдан список препаратов, которые необходимо исключить, поскольку они могут спровоцировать желтуху.
Сфероцитоз. Значительно менее распространён по сравнению с дефицитом Г-6-ФД. Часто, но не всегда, имеется семейный анамнез. Это нарушение можно установить при выявлении сфероцитов в мазке крови.
Врождённые инфекции. Желтуха при рождении может быть также следствием врождённой инфекции. В этом случае билирубин является конъюгированным и у младенцев имеются другие клинические признаки.

Желтуха между 24ч и 3 нед после рождения
Физиологическая желтуха. У большинства младенцев, у которых выявляется лёгкая или умеренная желтуха в течение этого периода, отсутствуют какие-либо причины для этого и билирубин повышен, поскольку младенец адаптируется к переходу от внутриутробной жизни. Термин «физиологическая желтуха» может применяться только после исключения других причин.
Желтуха от грудного молока. Это не означает, что грудное молоко содержит токсины. Тем не менее имеется эпидемиологическое наблюдение о том, что желтуха более распространена и держится более длительное время у младенцев на грудном вскармливании. Гипербилирубинемия имеет характер неконъюгированной. Причины мультифакторные, в том числе увеличение энтерогепатической циркуляции билирубина.
У некоторых младенцев желтуха явно усиливается при недостаточном поступлении грудного молока из-за трудностей, возникающих с налаживанием грудного питания, у некоторых младенцев даже развивается дегидратация. Потеря веса указывает на тяжесть дегидратации. Грудное вскармливание необходимо продолжать, даже несмотря на то что уровень билирубина снижается при его прекращении. Некоторым младенцам необходима внутривенная инфузионная терапия для коррекции дегидратации.
Инфекции. У инфицированных младенцев может развиваться неконъюгированная гипербилирубинемия в результате низкого всасывания жидкости, гемолиза, снижения функции печени и увеличения энтерогепатической циркуляции. При подозрении на инфекцию необходимо провести соответствующие исследования и лечение. В этом случае можно выявить особенно ИМП.
Другие причины. Несмотря на то что желтуха в результате гемолиза обычно отмечается в первый день жизни, она может наблюдаться в течение первой недели. Кровоподтёки и полицитемия (венозный гематокрит >0,65) усиливают желтуху у новорождённых. При очень редком синдроме Кригера-Найяра, когда имеется дефицит или отсутствие фермента глюкуронил-трансферазы, может отмечаться чрезвычайно высокий уровень неконъюгированного билирубина.
Желтуха через 3 нед после рождения (персистирующая желтуха новорождённых)
Желтуха у младенцев в возрасте более 3 нед от рождения называется персистирующей, или пролонгированной, желтухой новорождённых. У большинства новорождённых гипербилирубинемия остаётся неконъюгированной, однако это необходимо подтвердить лабораторными исследованиями.
Для пролонгированной неконъюгированной гипербилирубинемии характерно следующее:
• наиболее распространённой причиной является желтуха от грудного молока, которая наблюдается у 15% здоровых младенцев на грудном вскармливании; она постепенно уменьшается и исчезает к 4-5 нед жизни;
• необходимо обследование на наличие инфекции, особенно ИМП;
• необходимо исключить врождённый гипотиреоз, поскольку он может присутствовать при пролонгированной желтухе до формирования клинических признаков в виде «обветренного» лица, сухой шершавой кожи, гипотонии и запора. Поражённые младенцы должны выявляться при неонатальном биохимическом скрининге (проба Гатри). Конъюгированная гипербилирубинемия предполагается у ребёнка, у которого наблюдаются тёмная моча и непигментированный серый стул.
К другим вывляемым клиническим признакам относятся гепатомегалия и недостаточное увеличение веса. Причины патологии включают синдром неонатального гепатита и атрезию жёлчных путей, которую важно диагностировать немедленно, поскольку задержка хирургического вмешательства неблагоприятно влияет на исход.
Тяжесть желтухи у новорожденного. Желтуху легче всего наблюдать при натягивании кожи пальцем. Желтуха обычно проявляется на коже головы и лица, затем распространяется вниз по туловищу и на конечности. В некоторых центрах используется транскутанный измеритель желтухи, однако если изменение окраски кожи клинически значимо или имеются сомнения относительно её тяжести, необходимо проверить уровень билирубина в крови.
Легко недооценить желтуху у недоношенных детей и младенцев из афро-карибских, азиатских этнических групп. Для них необходимо установить низкие пороговые значения для измерения билирубина. Увеличение селезёнки или печени указывает на то, что желтуха не является физиологической.
Скорость изменений желтухи у новорожденного. Кривая скорости изменений имеет линейный характер до достижения плато, поэтому серийные измерения могут отмечаться на графике и использоваться для прогнозирования необходимости лечения до того, как он поднимется до опасного уровня.
Недоношенные дети более чувствительны к повреждению, вызванному повышенным уровнем билирубина (более низкий уровень альбумина), таким образом, порог для вмешательства ниже.
Младенцы, страдающие тяжёлой гипоксией, гипотермией или другим тяжёлым заболеванием, могут быть более подвержены осложнениям тяжёлой желтухи. Препараты, способные вытеснить билирубин из альбумина, например сульфаниламиды и диазепам, редко используются у новорождённых.
Оценка желтухи у новорождённых
• Тяжесть?
- Клиническая оценка — надавите на кожу для оценки тяжести желтухи, которая распространяется от головы до конечностей; может недооцениваться у лиц с тёмной кожей и недоношенных.
- По мере необходимости определите уровень билирубина (транскутанный или в крови).
• Гестация?
- Более низкий порог для лечения у недоношенных.
• Возраст?
- Если - Если >3 нед — необходимо проверить, является она неконъюгированной или конъюгированной.
- Хорошее или плохое самочувствие?
- Проверить на наличие клинических признаков сепсиса и имеется ли дегидратация.
• Факторы риска?
- Гемолиз — проверить на наличие антенатальных антител, если мать имеет группу крови «О» (АВО-несовместимость) или если относится к средиземноморской, дальневосточной или афро-карибской этнической группе (дефицит Г-6-ФД).
- Сепсис, тяжёлое состояние, ацидоз, низкий уровень альбумина плазмы (если измеряется).
• Необходимость лечения?
- Отметить значения билирубина на диаграмме, соотносящей уровень билирубина с возрастом.
- Также отметить темп изменения билирубина.
- Оценить срок гестации, возраст и имеющиеся факторы риска.
Видео этиология, патогенез желтухи (повышения билирубина)
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
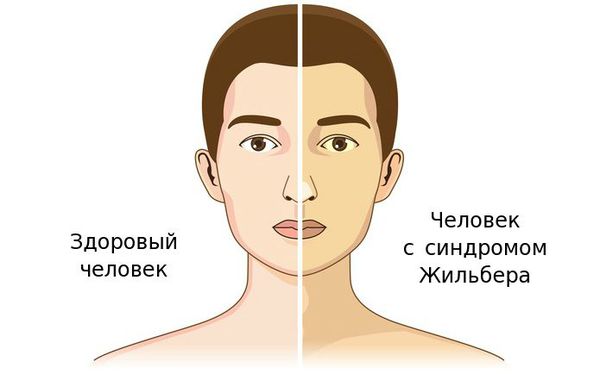
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.
К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .
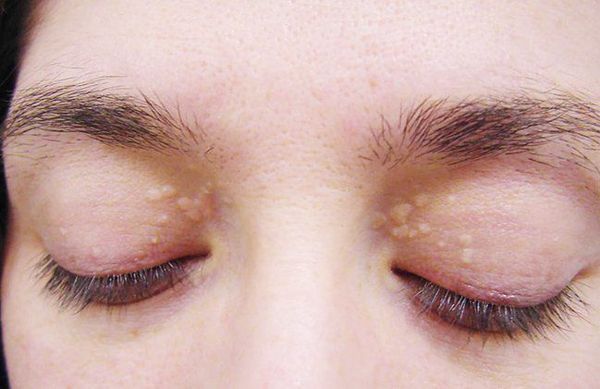
Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.
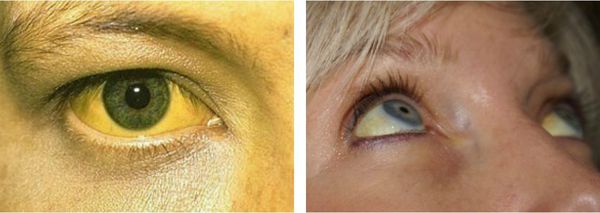
Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).
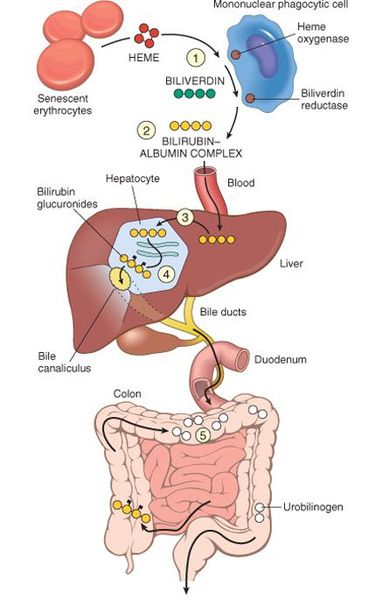
У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.
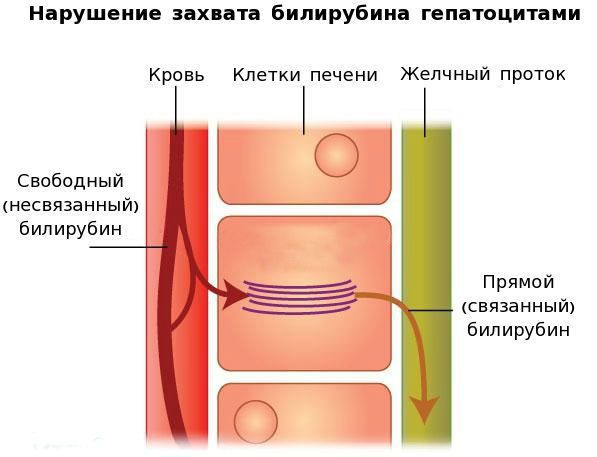
В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.
Читайте также:

