Как долго может длится заболевание склероатрофический лихен
Обновлено: 28.04.2024
Первый МГМУ им. И.М. Сеченова
Первый МГМУ им. И.М. Сеченова
Первый московский государственный медицинский университет им. И.М. Сеченова
Первый МГМУ им. И.М. Сеченова, Москва, 119991, Российская Федерация
Полиморфный вариант склероатрофического лихена
Журнал: Клиническая дерматология и венерология. 2014;12(2): 35‑40
Потекаев Н.С., Плиева Л.Р., Теплюк Н.П., Сергеев Ю.Ю. Полиморфный вариант склероатрофического лихена. Клиническая дерматология и венерология. 2014;12(2):35‑40.
Potekaev NS, Plieva LR, Tepliuk NP, Sergeev IuIu. A polymorphic variant of lichen sclerosus. Klinicheskaya Dermatologiya i Venerologiya. 2014;12(2):35‑40. (In Russ.).
Первый МГМУ им. И.М. Сеченова
Склероатрофический лихен (lichen sclerosus et atrophicus, каплевидная склеродермия, болезнь белых пятен, белый лишай Цумбуша, крауроз вульвы, крауроз полового члена) представляет собой редкий хронически протекающий воспалительный дерматоз неясной этиологии, поражающий кожно-слизистые покровы. В статье приводятся краткие сведения о патогенезе, клинике, диагностике и лечении данного дерматоза. Описано клиническое наблюдение склероатрофического лихена с вовлечением кожного покрова и слизистой оболочки полости рта. Особенностью клинических проявлений является полиморфизм высыпаний: папулы, бляшки, пузыри и эрозии. Диагноз подтвержден дерматоскопическим и гистологическим методами исследования. Имеется полное описание дерматоскопической и гистологической картин. Авторами подчеркивается важная роль дерматоскопии в диагностике заболевания и успешное применение системной глюкокортикостероидной терапии.
Первый МГМУ им. И.М. Сеченова
Первый МГМУ им. И.М. Сеченова
Первый московский государственный медицинский университет им. И.М. Сеченова
Первый МГМУ им. И.М. Сеченова, Москва, 119991, Российская Федерация
Склероатрофический лихен - САЛ - (lichen sclerosus et atrophicus, каплевидная склеродермия, болезнь белых пятен, белый лишай Цумбуша, крауроз вульвы, крауроз полового члена) представляет собой редкий хронически протекающий воспалительный дерматоз неясной этиологии, поражающий кожно-слизистые покровы [1].
САЛ был впервые описан Hallopeau в 1887 г. как атрофическая форма плоского лишая [2]. Однако в дальнейшем он различал две формы склерозирующего лишая: первично-склерозирующую и вторичную, развивающуюся из обычного плоского лишая. До сих пор нозологическая принадлежность дерматоза четко не определена: большая часть авторов считают САЛ разновидностью ограниченной склеродермии, некоторые - вариантом красного плоского лишая, а сторонники третьей точки зрения (Л.Н. Машкилейсон, 1965 г.) рассматривают САЛ как самостоятельный дерматоз, занимающий промежуточное положение между красным плоским лишаем и склеродермией [1, 3].
В патогенезе САЛ предполагается роль различных факторов:
1) аутоиммунного - в 79% случаев у больных САЛ обнаруживаются аутоантитела [4, 5], а в 20-34% случаев отмечается связь между САЛ и рядом аутоиммунных заболеваний, таких как очаговая алопеция, витилиго, аутоиммунный тиреоидит, сахарный диабет 1-го типа, пернициозная анемия [4, 6];
2) генетического - отмечаются семейные случаи дерматоза, имеется достоверная связь с антигеном DQ7 главного комплекса гистосовместимости класса II [4];
3) инфекционного - предполагается участие спирохет вида Borrelia и вируса папилломы человека как возможных причинных факторов САЛ [4];
4) гормонального - у больных отмечаются дисгормональные сдвиги в системе гипофиз-надпочечники-яичники; у девочек с САЛ вульвы в связи с низким уровнем эстрогенов характерны более поздние сроки полового созревания, менструальная дисфункция, у женщин в период менопаузы САЛ принимает упорный рецидивирующий характер.
САЛ чаще страдают женщины - соотношение больных женщин и мужчин составляет от 6:1 до 10:1. Пик заболеваемости у женщин приходится на 5-6-й десяток жизни, на 2-м месте - препубертатный период у девочек между 8 и 13 годами [4, 6, 7].
Клинически САЛ проявляется мелкими, 3-6 мм в диаметре, четко отграниченными плоскими полигональными папулами асбестовидного цвета с перламутровым блеском или ливедным оттенком, напоминающими папулы красного плоского лишая [3, 7, 11]. По периферии папул может быть тонкий сиреневый венчик как при бляшечной склеродермии. Высыпания располагаются изолированно или группируются с образованием бляшек молочно-белого цвета или цвета слоновой кости. Поверхность бляшек сначала располагается вровень с окружающей кожей или слегка возвышается над ней, но со временем становится вогнутой. Устья волосяных фолликулов в пределах бляшек расширены, заполнены роговыми пробками серо-коричневого цвета и имеют комедоноподобный вид. Если пробок много, поверхность бляшки выглядит бородавчатой. Кожный рисунок сглажен. Субъективные ощущения отсутствуют. Высыпания имеют склонность к спонтанному разрешению, оставляя атрофические гипо- или депигментированные пятна, имеющие сходство с витилиго. Весьма характерно обнаружение в очагах атрофии телеангиэктазий и петехий. Поражение гениталий может быть изолированным и отличаться большим разнообразием клинических форм: папулезной, эритематозно-отечной, витилигинозной, буллезной, атрофической, эрозивно-язвенной [3]. В отличие от поражения кожного покрова, САЛ гениталий сопровождается выраженными субъективными ощущениями в виде длительно существующего, упорного, мучительного зуда. Отмечается положительный феномен Кебнера [1, 4]. Изредка, в основном у женщин, САЛ половых органов приводит к плоскоклеточному раку [1].
На слизистой оболочке полости рта САЛ бывает представлен перламутрово-белыми пятнами [5] или ороговевающими мацерированными бляшками с сетчатым рисунком, напоминающими красный плоский лишай.
Наиболее характерными дерматоскопическими признаками САЛ являются роговые пробки (комедоноподобные структуры) и бесструктурные зоны белого цвета. Гистологически роговые пробки представляют собой кератотические массы, заполняющие устья волосяных фолликулов, а бесструктурные зоны белого цвета соответствуют участкам атрофии эпидермиса [12]. Было отмечено, что для очагов САЛ, существующих менее 1,5 лет, более характерно обнаружение роговых пробок, в то время как для более старых очагов характерны зоны атрофии. При дерматоскопии возможно обнаружение чешуек, структур по типу хризалид (признак, определяющийся только при проведении дерматоскопии в поляризованном свете и представляющий собой отдельные блестящие линии ярко-белого цвета) и эрозий [13]. По периферии некоторых очагов можно обнаружить эритематозный венчик, состоящий из телеангиэктазий, являющийся признаком прогрессирующей стадии заболевания [14].
Гистологическая картина при САЛ характеризуется атрофией эпидермиса, особенно его шиповатого слоя, гиперкератозом с роговыми пробками, вакуольной дистрофией базального слоя, выраженным отеком и гомогенизацией коллагена в верхней части и воспалительным лимфоцитарным инфильтратом с примесью гистиоцитов в средней части дермы. Капилляры расширены [3].
САЛ следует дифференцировать с ограниченной склеродермией, красным плоским лишаем, витилиго (впрочем, САЛ нередко сосуществует с этими дерматозами [3,15]), лейкоплакией, простым лишаем Видаля, экстрамамиллярным раком Педжета, опрелостью, кандидозом и др.
Лечение САЛ проводится аналогично терапии склеродермии: применяются антибактериальные, аминохинолоновые препараты, ферментные, сосудорасширяющие, биостимулирующие средства, витаминотерапия, местно - глюкокортикостероидные мази, ингибиторы кальциневрина (такролимус, пимекролимус), ретиноиды, аналоги витамина D3, а при генерализованных формах, торпидных к лечению, - системные глюкокортикостероиды, цитостатики [3, 4, 6, 7]. Из физиотерапевтических методов лечения применяются ПУВА-терапия, фонофорез, ультразвуковая терапия, лазеротерапия, оксигенотерапия (гипербарическая оксигенация).
Ниже приводим клиническое наблюдение полиморфного варианта САЛ.
Больная П., 57 лет, пенсионерка, жительница Владимирской области, поступила под наше наблюдение в мае 2013 г. с диагнозом «Локализованная склеродермия». Из анамнеза стало известно, что около 5 лет назад на фоне менопаузы и перенесенного стресса больная П. отметила появление высыпаний на коже голеней без субъективных ощущений. Дерматологом по месту жительства был поставлен диагноз «Красный плоский лишай» и была назначена системная терапия (названий препаратов не помнит, однако предполагает, что антибактериальные) - без положительного эффекта. Со временем высыпания увеличились в количестве, появились буллезные элементы. В 2010 г. в Государственном научном центре дерматовенерологии и косметологии Минздрава России проведена диагностическая биопсия кожи и по результатам гистологического исследования поставлен диагноз САЛ. Тогда же была проведена терапия системными антибиотиками (пенициллин), системными глюкокортикостероидами - дипроспан 2,0 мл внутримышечно 2 инъекции, преднизолон 30 мг внутримышечно 3 инъекции, сосудистыми препаратами - с временным положительным эффектом. В последующие 2 года дерматоз периодически обострялся, а с конца 2012 г. распространился на кожу верхних конечностей, живота, пояснично-крестцовой области, наружных гениталий. Пациентка самостоятельно применяла мазь левомеколь на область гениталий и голеней, так как поражение этих областей сопровождалось субъективными ощущениями в виде сильного зуда (гениталии) и болезненности (вскрывшиеся пузыри с образованием эрозий в области нижних конечностей). В ноябре 2011 г. проконсультирована ревматологом, который не обнаружил данных за наличие системной склеродермии. В том же году анализ крови на антитела к боррелиям Бургдорфера дал отрицательный результат. В мае 2012 г. проведен курс комбинированной кислородно-озоновой терапии - без эффекта.
Аллергоанамнез и наследственность не отягощены. Из сопутствующей патологии - гипертоническая болезнь II стадии.
Лабораторно-диагностические исследования: в клиническом и биохимическом анализах крови - без патологии; результаты исследования крови на сифилис, ВИЧ-инфекцию, гепатиты В и С - отрицательные; общий анализ мочи - без патологических отклонений. Электрокардиограмма - синусовый ритм, горизонтальное положение электрической оси сердца, гипертрофия левого желудочка с изменениями миокарда.
Локальный статус: поражение кожи разгибательной поверхности предплечий, тыльной поверхности кистей, лучезапястных сгибов, правой боковой поверхности живота, пояснично-крестцовой области, передних поверхностей голеней с переходом на тыл и внутреннюю поверхностью стоп носит хронический характер и представлен полиморфными высыпаниями (рис. 1). Рисунок 1. Клинико-морфологическая картина САЛ у пациентки П. а - поражение разгибательной поверхности левого предплечья в виде плоских полигональных и овальных папул. Видны расширенные волосяные фолликулы; б - классические проявления склероатрофического лишая: на поверхности атрофической бляшки отчетливо визуализируются роговые пробки; в - поражение кожи нижних конечностей: сочетание бляшечной и буллезной форм САЛ; вокруг большинства бляшек наблюдается венчик гиперемии; г - эрозивный элемент в области левой стопы; д - поражение слизистой оболочки правой щеки. На коже верхних конечностей - высыпания в виде плоских полигональных и овальных папул, диаметром от 1 до 3 см, с четкими границами, белесоватого цвета с ливедным оттенком и перламутровым блеском, в пределах которых отчетливо визуализируются фолликулярные роговые пробки. Большинство папул расположены изолированно, но некоторые из них группируются с образованием бляшек. На тыле кистей часть папул разрешилась вплоть до образования белесоватых пятен. По периферии папул отмечается тонкий сиреневый венчик. На коже правой боковой поверхности живота и пояснично-крестцовой области визуализируются продолговатые белесоватые бляшки округлых очертаний с четкими границами диаметром 7 и 2 см. Большая по размерам бляшка имеет поверхность «папиросной бумаги» с многочисленными роговыми пробками. Меньшая в размерах бляшка плотной консистенции, с бородавчатой поверхностью, рядом с ней наблюдаются две плоские папулы. По периферии бляшек, как и папул, отмечается сиреневый венчик. На коже пояснично-крестцовой области имеется пятно молочно-белого цвета, в пределах которого наблюдаются телеангиэктазии и единичные геморрагические пятна. В области нижних конечностей эффлоресценции представлены буллезными и эрозивными элементами с четкими границами и периферическим ливедным венчиком. Пузыри имеют плотную покрышку, местами с бородавчатой поверхностью, и серозное содержимое. На слизистой оболочке правой щеки имеется довольно крупная бляшка белесоватого цвета, причудливых очертаний и четким сетчатым рисунком. На коже наружных гениталий и перианальной области наблюдаются участки атрофии белесоватого цвета, эритематозные пятна и небольшие трещины. Ногтевые пластинки кистей и стоп не поражены. Волосы не изменены. Субъективно: зуд в аногенитальной области и болезненность в области эрозий на стопах при ходьбе.
При дерматоскопическом исследовании различных элементов САЛ определяются бесструктурные зоны белого цвета, роговые пробки, телеангиэктазии по периферии некоторых бляшек и структуры по типу хризалид, что соответствует описанным в литературе данным (рис. 2). Рисунок 2. Дерматоскопическое исследование очагов поражения у пациентки П. а - стационарная стадия склероатрофической бляшки: роговые пробки и бесструктурные зоны белого цвета (звездочка); б - первоначальные проявления склероатрофической папулы: волосяной фолликул (белая стрелка), роговая пробка (черная стрелка); в - прогрессирующая стадия склероатрофической бляшки. По периферии образования четко определяется эритематозный венчик. Телеангиэктазии (овал), роговые пробки (стрелка); г - регрессирующая стадия склероатрофической бляшки характеризуется бесструктурными зонами белого цвета (звездочка), отсутствием роговых пробок и телеангиэктазий.

Учитывая клиническую картину поражения кожно-слизистого покрова был поставлен диагноз САЛ, полиморфного варианта. Была произведена диагностическая биопсия кожи. Гистологическое описание: «Эпидермис с выраженным гиперкератозом, небольшим акантозом, резко атрофирован, местами отслаивается от дермы с образованием полости. Зернистый слой атрофирован. Сально-волосяные фолликулы расширены, заполнены кератотическими массами - роговыми пробками. В дерме - отек верхнего слоя, периваскулярные лимфомакрофагальные инфильтраты и очаговый склероз - в нижнем слое. Заключение: картина укладывается в морфологию старых изменений САЛ» (рис. 3). Рисунок 3. Гистологические препараты с очага поражения на коже пациентки П. Эпидермис с выраженным гиперкератозом, атрофирован. Сально-волосяные фолликулы расширены, заполнены кератотическими массами (роговые пробки). В дерме - отек верхнего слоя, дезорганизация коллагеновых волокон нижнего слоя. Окрашивание гематоксилином и эозином.
Была назначена терапия: пенициллин 500 000 ЕД внутримышечно 4 раз в день в течение 10 дней, трентал 200 мг внутримышечно 5 инъекций, актовегин 5,0 мл внутримышечно 5 инъекций, веторон Е 10 капель в день, местно - промывание эрозий раствором хлоргексидина биглюконата, перевязки с ксероформной мазью с анестезином, аэрозоль пантенол, аппликации мази элоком на папулы. На фоне проводимого лечения не отмечалось существенного терапевтического эффекта и больной был назначен системный глюкокортикостероидный препарат метипред в дозе 32 мг/сут (8 таблеток). К 14-му дню лечения метипредом наблюдалось выраженное улучшение в виде эпителизации большинства эрозий, разрешения периферического венчика роста вокруг большинства высыпаний, частичного регресса папул, уплощения бляшек и уменьшения выраженности фолликулярного гиперкератоза, купирования субъективных ощущений. Лечение метипредом в дозе 32 мг/сут было продолжено до 21-го дня с последующим снижением до 24 мг/сут. Пациентка была выписана для дальнейшего лечения и наблюдения дерматологом по месту жительства.
Интерес данного клинического наблюдения полиморфного варианта САЛ заключается в разнообразии проявлений данного дерматоза, редком поражении слизистой оболочки полости рта, важной роли дерматоскопии в диагностике заболевания и в успешном применении системной глюкокортикостероидной терапии.
Склероатрофический лишай – дерматологическое заболевание неясной этиологии, при котором наблюдается атрофия различных участков кожи, в основном в области половых органов, реже других регионов тела. Симптомом этого состояния является образование светлых, почти белых бляшек и папул вокруг гениталий, изредка на шее и около подмышечных впадин, которые со временем трансформируются в атрофические очаги. Диагностика склероатрофического лишая осуществляется на основании результатов дерматологического осмотра больного, в спорных случаях может производиться биопсия кожных покровов в области поражения с последующим гистологическим исследованием. Этиотропное лечение заболевания не разработано, назначают общеукрепляющие средства, витаминотерапию и лекарства для улучшения микроциркуляции. Имеются указания на положительный эффект от использования противомалярийных средств.
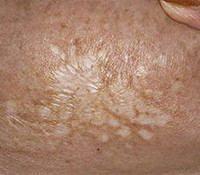
Общие сведения
Склероатрофический лишай (болезнь белых пятен, каплевидная склеродермия, крауроз вульвы/полового члена) – атрофическое заболевание кожи неопределенного генеза, которое преимущественно поражает зону гениталий, но может располагаться и на иных участках кожных покровов. Это состояние было впервые описано еще в 1889 году французским дерматологом Франсуа Аллопо, принявшем заболевание за разновидность обычного плоского лишая. Лишь дальнейшие исследования позволили определить, что патология, описанная Аллопо, разделяется на два типа – первичный склероатрофический лишай и последствия красного плоского лихена (стадия атрофии). Это дерматологическая заболевание в несколько раз чаще встречается у женщин, особенно экстрагенитальные формы – последние практически никогда не наблюдаются у мужчин. Наблюдения по поводу возрастного распределения несколько разнятся – по одним данным, склероатрофический лишай в основном поражает лиц старшего возраста и крайне редко возникает у девочек в подростковый период. Согласно мнению иных исследователей, нередки случаи развития этого состояния у молодых женщин – такие различия в описании многих специалистов объясняют путаницей, при которой за болезнь белых пятен принимают застарелые формы красного плоского лишая.

Причины склероатрофического лишая
Этиология и патогенез склероатрофического лишая в данный момент изучены недостаточно, имеется лишь несколько гипотез по поводу развития этого дерматологического заболевания. Наибольшим признанием пользуется патогенетическая теория – описаны как наследственные случаи данного состояния, так и их схожее развитие у однояйцовых близнецов. Однако при этом ни дефектные гены, ни другие молекулярные механизмы возникновения склероатрофического лишая не изучены. Другая популярная теория указывает на аутоиммунные факторы развития этой патологии, поскольку ее проявления схожи с другими поражениями кожи подобного типа (склеродермией, некоторыми формами псориаза). Но и эта версия не объясняет все проявления склероатрофического лишая, кроме того, заболевание очень слабо реагирует на лечение иммуносупрессивными средствами.
Имеются указания на роль инфекционных факторов, например, боррелиоза (болезни Лайма). После перенесенной инфекции такого типа у ряда лиц возникают типичные проявления склероатрофического лишая. Не исключено влияние и других вирусных или бактериальных инфекций, также эта теория некоторыми дерматологами сочетается с аутоиммунной по причине возможной перекрестной реакции на антигены возбудителей и собственных тканей человека. Практически доказано, что предрасполагающую роль в развитии склероатрофического лишая играют гормональный дисбаланс, поражения эндокринной системы, частые психоэмоциональные стрессы. Изучение этого заболевания, попытки объяснения причин его возникновения и использования этих данных в лечении патологии продолжаются до сих пор.
Симптомы склероатрофического лишая
Большинство случаев склероатрофического лишая регистрируется у женщин в возрасте 35-50 лет, иногда наблюдается развитие заболевания у молодых девушек и даже подростков. Высыпания могут локализоваться на шее, груди, около подмышечных впадин, на лобке, бедрах и в области половых органов – при этом так называемые экстрагенитальные формы болезни белых пятен (наличие высыпаний на теле при отсутствии их на вульве и близлежащих участках) составляют только 20% от всех случаев. Наиболее часто склероатрофический лишай проявляется именно поражением генитальной области и собственно вульвы. Для начала заболевания характерно появление на поверхности кожных покровов папул белого цвета, которые достаточно быстро трансформируются в светлые или розовые бляшки. Поверхность бляшек несколько приподнята над здоровой кожей, шелушится, из субъективных симптомов отмечается выраженный зуд. При дальнейшем развитии склероатрофического лишая на месте бляшек образуются гипопигментированные атрофические участки кожи, поверхность которых напоминает папиросную бумагу.
Мужчины страдают от этой патологии в несколько раз реже, при этом у них практически всегда наблюдается поражение кожных покровов в области половых органов (в 90% случаев поражается крайняя плоть и поверхность головки полового члена). В остальном развитие кожных проявлений склероатрофического лишая не имеет особенностей, отмечается появление бляшек или папул с дальнейшей атрофией кожи и появлением белых пятен. Поражение крайней плоти может приводить к развитию рубцового фимоза. Как у мужчин, так и у женщин генитальные формы склероатрофического лишая могут осложняться вторичной инфекцией бактериального или вирусного генеза. Также эта форма заболевания опасна тем, что является предраковым состоянием – по статистике, примерно в 3-5% случаев болезнь белых пятен перерождается в плоскоклеточный рак кожи или половых органов.
Диагностика склероатрофического лишая
Выявление склероатрофического лишая в дерматологии не представляет особой сложности из-за выраженных проявлений заболевания – белых атрофических участков кожи, локализующихся вокруг половых органов и на вульве. При осмотре могут обнаруживаться относительно свежие очаги патологии в виде светло-розовых папул или бляшек. Однако дифференциальная диагностика склероатрофического лишая несколько затруднена, поскольку схожими проявлениями обладают склеродермия, застарелые формы красного плоского лишая, некоторые разновидности псориаза. Главной особенностью патологии является преимущественная локализация высыпаний вокруг и на половых органах, поэтому при экстрагенитальных формах наиболее часто возникают диагностические ошибки.
Патогистологические изменения при склероатрофическом лишае неодинаковы на различных стадиях процесса. На начальных этапах выявляют выраженный отек дермы, умеренную лимфогистиоцитарную инфильтрацию, расширение кровеносных сосудов. Эпидермис утолщен, наблюдается нарушение процессов ороговения, роговые массы могут забивать волосяные фолликулы, протоки потовых и сальных желез. При дальнейшем развитии склероатрофического лишая определяется атрофия эпидермиса, гомогенность коллагеновых волокон дермы. На поздних этапах в некоторых случаях могут наблюдаться признаки метаплазии клеток и начальных проявлений плоскоклеточного рака.
Лечение склероатрофического лишая
Из-за неясности причин склероатрофического лишая этиотропного лечения этого дерматологического заболевания на сегодняшний день не существует. Применяют различные симптоматические методы терапии, а также препараты, относительная эффективность которых была доказана эмпирическими клиническими наблюдениями. Из наружных средств назначают иммуносупрессивные мази (на основе кортикостероидов или такролимуса), однако они могут уменьшить выраженность симптомов лишь на стадии развития бляшек и папул. Аналогично в лечении склероатрофического лишая используют и противомалярийные средства – их не назначают при развившейся атрофии кожи. Препараты, улучшающие местное кровоснабжение и процессы микроциркуляции (например, на основе витаминов), также позволяют значительно уменьшить выраженность симптомов. Некоторые специалисты указывают на необходимость лечения основного заболевания, которое могло быть провоцирующим для склероатрофического лишая – эндокринных нарушений, сахарного диабета и пр.
Иногда в терапии болезни белых пятен применяют хирургические методики. Операции могут производиться как по эстетическим показаниям (устранение чрезмерно больших участков атрофии и дальнейшая пластика), так и по медицинским. В тяжелых случаях склероатрофического лишая возникают спайки, приводящие к сращению малых половых губ, сужению мочеиспускательного канала, фимозу. Все эти осложнения могут быть устранены только хирургическим путем – пластикой вульвы и мочеиспускательного канала, обрезанием (циркумцизио) у мужчин. Кроме того, хирургическое лечение показано при трансформации склероатрофического лишая в плоскоклеточный рак кожи.
Прогноз и профилактика склероатрофического лишая
Большинство дерматологов склонны относить склероатрофический лишай к заболеваниям с относительно неблагоприятным прогнозом. Это связано с неопределенным генезом патологии, в результате чего, несмотря на все терапевтические мероприятия, у больных остаются атрофические участки кожи различного размера. Всегда имеется риск таких осложнений, как развитие спаек, сужение мочеиспускательного канала, вторичная инфекция, злокачественное перерождение. Больные склероатрофическим лишаем должны каждые 2-3 месяца посещать дерматолога или онколога с целью как можно более раннего выявления вышеперечисленных грозных осложнений.
Облитерирующий ксеротический баланит – это склеротически-фиброзный и атрофический процесс со слабо выраженным воспалительным компонентом, поражающий головку полового члена. Характеризуется появлением белесоватых пятен и гиперкератотических очагов в области головки и внутреннего листка крайней плоти, сморщиванием кожи, вследствие чего возможно развитие стеноза крайней плоти, фимоза, сужения устья уретры. Распознавание производится на основании осмотра, биопсии и установления гистологического диагноза. Выполняется циркумцизио, меатотомия, при необходимости - пластика уретры, назначается местная терапия глюкокортикоидами.
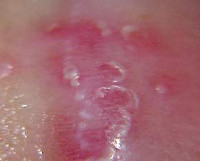











Общие сведения
Облитерирующий ксеротический баланит (склерозирующий лихен) может развиваться в любом возрасте: у детей, мужчин среднего и пожилого возраста, но чаще встречается у пациентов старше 50 лет. Специалисты расценивают облитерирующий ксеротический баланит как состояние, предрасполагающее к развитию рака полового члена.
По гистологическим признакам облитерирующий ксеротический баланит сходен со склероатрофическим лишаем и некоторыми локальными формами склеродермии. В гинекологии ограниченная склеродермия может выявляться в области наружных гениталий у женщин при отсутствии данных за крауроз вульвы. Эти наблюдения позволяют объединить кожные и урогенитальные склерозирующие процессы в одну группу, имеющую дистрофическую природу.

Причины
Этиология склерозирующего лихена неясна. Считается, что к развитию заболевания может приводить широкий круг факторов – генетические, аутоиммунные, инфекционные, механические, гормональные. В современной андрологии, дерматологии и гинекологии имеются наблюдения семейных случаев склеротического лишая и склерозирующего лихена гениталий. Проводимые в данном направлении исследования позволили выявить ряд генов, ответственных за развитие наследуемого облитерирующего ксеротического баланита и степени его выраженности.
Данные некоторых научных изысканий указывают на связь между данной формой баланита и аутоиммунными поражениями – витилиго, псориазом, ревматической полимиалгией, системной красной волчанкой, сахарным диабетом, микседемой, первичным билиарным циррозом печени, алопецией и др. Кроме того, местные проявления патологии сходны с характерными изменениями тканей при аутоиммунных заболеваниях. Не исключается роль вирусных агентов, в частности, в тканях крайней плоти после выполнения циркумцизио, нередко обнаруживаются возбудители генитального герпеса и папилломавирусной инфекции.
В ряде случаев прослеживается зависимость возникновения болезни от местных повреждений кожи – механической, химической или термической травмы, потертостей, хронического раздражения мочой, радиационного облучения при лучевой терапии. Ряд исследователей отмечают связь склеротически-фиброзных изменений в области головки полового члена с предшествующим хирургическим обрезанием крайней плоти по поводу фимоза. Предполагается, что развитие патологии может быть связано с возрастным падением уровня тестостерона или нарушением чувствительности тканей к мужским половым гормонам.
Симптомы ксеротического баланита
Поражается головка полового члена и внутренний листок кожи крайней плоти – вначале появляются белесоватые пятна, пузыри с геморрагическим содержимым и атрофические участки, которые затем трансформируются в склеротические бляшки. В дальнейшем образуется циркулярное склеротическое кольцо, по мере уплотнения которого выведение головки затрудняется. На этом фоне дополнительное инфицирование может приводить к бактериальному воспалению головки полового члена - баланиту. В конечной стадии баланита с развитием рубцового фимоза головка совсем перестает открываться.
У мужчин, ранее перенесших обрезание, облитерирующий ксеротический баланит обычно начинается в зоне постоперационного кожного рубца. Снижение эластичности кожи крайней плоти может сопровождаться ее надрывами, особенно во время полового акта. При рубцевании наружного отверстия уретры и части мочеиспускательного канала в области ладьевидной ямки развивается затрудненное мочеиспускание, требующее натуживания; струя мочи становится тонкой и прерывистой. Течение патологии рецидивирующее, длительное.
Осложнения
Склеро-атрофические и гиперкератотические процессы при облитерирующем ксеротическом баланите не только ухудшают качество жизни, но и могут стать причиной рецидивирующих инфекций мочевых путей (уретрита, цистита, пиелонефрита), мочекаменной болезни, гидронефроза и даже почечной недостаточности.
Диагностика
В ходе диагностики необходимо исключить другие заболевания со сходной симптоматикой – бактериальный и грибковый баланопостит, герпетическую, хламидийную инфекцию, приобретенный фимоз, крауроз и лейкоплакию полового члена. В комплексе диагностики выполняется бактериологическое и ПЦР исследование мазков. Окончательное подтверждение получают с помощью биопсии измененных очагов кожи полового члена и уретры и их морфологического изучения.
При гистологическом исследовании выявляются участки фолликулярного гиперкератоза, истончение слоя росткового эпидермиса, гомогенный склероз коллагена, сокращение или атрофия эластических волокон, густая лимфоплазмоцитарная инфильтрация. Кроме верификации данной разновидности баланита, биопсия позволяет исключить рак полового члена и мочеиспускательного канала. С целью выявления стриктур уретры показано выполнение уретрографии и уретроскопии.
Лечение облитерирующего ксеротического баланита
Тактика лечения определяется распространенностью склерозирующих изменений. В начальной I стадии склерозирующего лихена, когда в патологические изменения вовлекается только крайняя плоть, производится операция обрезания крайней плоти (циркумцизио) с последующим наблюдением.
При II стадии, характеризующейся сужением отверстия уретры, требуется выполнение меатотомии – хирургического рассечения меатуса. В дальнейшем назначаются длительные курсы местной терапии глюкокортикоидными кремами. В III и IV стадии, протекающей с тотальнам вовлечением крайней плоти, головки члена, мочеиспускательного канала, необходимо широкое иссечение рубцовых тканей проведение реконструктивной пластики уретры на протяжении, затем – локальной глюкокортикоидной терапии.
Прогноз и профилактика
При своевременном лечении прогноз благоприятный, на поздних стадиях наблюдаются нарушения мочеиспускания, увеличивается вероятность развития рака полового члена. Специальная профилактика не выработана. Рекомендуется избегать травматизации половых органов и ЗППП, регулярно выполнять гигиенические процедуры, своевременно обращаться к специалистам по поводу экстрагенитальной патологии. При обнаружении любых изменений в области головки полового члена необходима консультация врача-андролога. Раннее иссечение пораженных тканей, консервативная терапия и наблюдение позволяют избежать грозных осложнений.
Очаговая склеродермия – это хроническое заболевание соединительной ткани, характеризующееся преимущественным поражением кожных покровов. Клинически проявляется уплотнением (индурацией) различных участков кожи с последующей атрофией и изменением пигментации, образованием контрактур. Диагноз ставится на основании симптоматики, обнаружения в крови антинуклеарного фактора и антицентромерных антител. В сомнительных случаях проводится гистологическое исследование кожи. Лечение заключается в применении глюкокортикостероидов, иммунодепрессантов, антифиброзных средств, блокаторов кальциевых каналов и проведении ПУВА-терапии. В ряде случаев выполняются хирургические операции.
МКБ-10
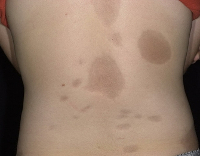
Общие сведения
Очаговая (локализованная, ограниченная) склеродермия – хроническое аутоиммунное заболевание из группы диффузных болезней соединительной ткани. Патология встречается повсеместно, распространенность составляет от 0,3 до 3 случаев на 100 000 человек. Чаще страдают женщины европеоидной расы. Возраст манифестации очаговой склеродермии зависит от формы. Бляшечная склеродермия чаще встречается у взрослых (30-40 лет), линейная - у детей от 2 до 14 лет, склероатрофический лихен – у женщин старше 50 лет. При локализованной форме, в отличие от системной, поражение внутренних органов в большинстве случаев либо минимально, либо отсутствует. Имеется ассоциация склеродермии с патологиями щитовидной железы (тиреоидитом Хашимото, болезнью де Кервена).

Причины
Точная причина заболевания неизвестна. Предполагается этиологическая роль бактерии Borrelia burgdorferi, вызывающей лайм-боррелиоз, однако убедительных данных за эту теорию на сегодняшний день нет. В развитии склеродермии важную роль играет наследственная предрасположенность. Были выявлены более частые случаи очаговой склеродермии среди близких родственников. При проведении генетических исследований обнаружена взаимосвязь между определенными генами гистосовместимости (HLA – DR1, DR4) и локализованной формой заболевания. Провоцирующими факторами, способствующими возникновению склеродермии, являются переохлаждения, травмы, постоянные вибрационные воздействия на кожу, прием лекарственных препаратов (блеомицина). Триггерными эффектами также обладают различные химические соединения (хлорвинил, кремний, нефтепродукты, сицилий, эпоксидная смола, пестициды, органические растворители).
Патогенез
Выделяют три основных патогенетических механизма склеродермии – фиброз (разрастание соединительной ткани), аутоиммунное повреждение и сосудистые нарушения. Иммунная аутоагрессия заключается в выработке лимфоцитами антител к соединительной ткани и ее компонентам. Также лимфоциты синтезируют интерлейкины, которые стимулируют пролиферацию фибробластов, гладкомышечных клеток и образование коллагена. Разрастающаяся при этом соединительная ткань замещает нормально функционирующую ткань. В результате повреждения эндотелия сосудов антителами и пролиферирующими гладкомышечными клетками снижается уровень простациклина (вещества, обладающего антиагрегантными и вазодилатирующими свойствами). Это приводит к спазму микрососудов, повышению адгезии и агрегации форменных элементов крови, внутрисосудистой коагуляции и микротромбозу.
Классификация
Очаговая склеродермия подразделяется на множество форм. Наиболее распространенными являются бляшечная и линейная. У ряда пациентов могут наблюдаться одновременно несколько вариантов заболевания. Существует целый ряд классификаций, но наиболее оптимальной и широко используемой считается классификация клиники Мэйо, включающей следующие разновидности очаговой склеродермии:
- Бляшечная. Данная форма в свою очередь подразделяется на поверхностную (морфеа) и узловатую (келоидоподобную). Характерны типичные участки уплотнения кожи с атрофией и нарушением пигментации.
- Линейная. К ней относятся полосовидная, саблевидная формы, а также прогрессирующая гемиатрофия лица Парри-Ромберга. Очаги располагаются в виде линий по ходу сосудисто-нервного пучка.
- Генерализованная (многоочаговая). Проявляется сочетанием бляшечного и линейного вариантов. Очаги распространены по всему телу.
- Буллезная. При данной разновидности на коже возникают пузыри с жидкостным содержимым, оставляющие после себя эрозии.
- Пансклеротическая инвалидизирующая. Наиболее неблагоприятная форма очаговой склеродермии. Характеризуется тяжелым, прогрессирующим течением, плохо поддается лечению. Поражаются все слои кожи и ткани, лежащие под ней. Развиваются грубые контрактуры суставов и длительно незаживающие язвы на коже.
- Склероатрофический лихен Цумбуша (болезнь белых пятен). Характерно образование пятен белого цвета, сопровождающихся нестерпимым зудом. Преимущественная локализация пятен – половые органы.
Симптомы
Для клинической картины типично образование на коже очагов, которые проходят три последовательных стадий развития – отек, индурацию (уплотнение) и атрофию. В начале заболевания на коже конечностей, шеи или туловища появляются пятна сиреневого или лилового цвета, имеющие нечеткие края. Размер пятен может сильно варьировать – от просяного зерна до размеров ладони и больше. На этом этапе пациент не испытывает каких-либо неприятных ощущений или боли. Затем пятна начинают отекать, кожа в центре очага уплотняется, становится блестящей, приобретает цвет слоновой кости. Пациент начинает ощущать зуд, покалывания, стянутость кожи, болезненность. Далее наступает стадия атрофии. Кожа в очагах истончается, прекращается рост волос, нарушается потоотделение, возникает стойкая дисхромия (гипер- или депигментация) и телеангиэктазии. Иногда развивается атрофодермия (участки западения кожи).
При линейной склеродермии очаги расположены по ходу нервов и сосудов. В случае локализации на коже лица очаги по внешнему виду напоминают рубец от удара саблей (саблевидная форма). Прогрессирующая гемиатрофия представляет собой глубокий процесс с поражением всех тканей половины лица - кожи, подкожной клетчатки, мышц и костей лицевого скелета, что приводит к выраженной деформации лица, обезображивающей внешний вид пациента. Также происходит атрофия половины языка и снижение вкусовой чувствительности.
Из внекожных признаков очаговой склеродермии стоит отметить офтальмологические и неврологические проявления при гемиатрофии Парри-Ромберга. Они включают выпадение ресниц и бровей на стороне поражения, западение глазного яблока из-за атрофии глазных мышц и орбитальной клетчатки, нейропаралитический кератит, головокружения, когнитивные нарушения, мигренозные головные боли, эпилептические припадки. Также возможно развитие феномена Рейно. Симптомы синдрома Рейно следующие – стадийное изменение окраски кожи пальцев рук вследствие вазоспазма и последующей гиперемии (бледность, цианоз, покраснение), сопровождающееся онемением, болью и покалыванием в пальцах рук. Остальные экстрадермальные проявления, характерные для системной склеродермии, встречаются крайне редко.
Осложнения
Наиболее распространенная проблема рассматриваемого заболевания – косметические дефекты. Серьезные осложнения, представляющие угрозу для жизни больного, возникают редко. К ним относятся нарушение мозгового кровообращения при гемиатрофии лица, ишемия и гангрена пальцев рук при феномене Рейно, выраженные контрактуры суставов, инвалидизирующие пациента. Через несколько лет после дебюта болезни могут развиться тяжелые поражения внутренних органов – фиброз легких, легочная гипертензия, фиброз миокарда, перикардит, стриктуры пищевода, острая нефропатия, почечная недостаточность.
Диагностика
Пациентов с очаговой склеродермией курируют врачи ревматологи и дерматологи. При постановке диагноза учитывается клиническая картина, семейный анамнез. Все методы диагностики направлены в первую очередь на определение степени вовлечения внутренних органов и исключение системной склеродермии. С этой целью применяются следующие исследования:
- Лабораторные. В анализах крови выявляются эозинофилия, повышение уровня ревматоидного фактора, гаммаглобулинов, высокие титры антицентромерных антител и антинуклеарного фактора (АНФ). Наличие антител к топоизомеразе (анти-Scl 70) свидетельствует в пользу системного процесса. При развитии «склеродермической почки» в моче появляются белок и эритроциты.
- Инструментальные. При капилляроскопии наблюдается дилатация капилляров без участков некроза. По данным ФЭГДС могут встречаться признаки эзофагита, стриктуры пищевода. При фиброзе миокарда на ЭКГ иногда обнаруживаются нарушения ритма сердца, на ЭхоКГ – зоны гипокинеза, выпот в перикардиальную полость. На рентгенографии или компьютерной томографии легких отмечаются интерстициальные изменения.
- Гистологическое исследование биоптата кожи. Заключительный этап, позволяющий достоверно поставить диагноз. Проводится при сомнительных результатах предыдущих исследований. Характерны следующие признаки - инфильтрация лимфоцитами, плазмоцитами и эозинофилами в ретикулярном слое дермы, утолщенные коллагеновые пучки, набухание и склероз сосудистой стенки, атрофия эпидермиса, сальных и потовых желез.
Очаговую склеродермию дифференцируют с другими формами склеродермии (системной, склеродермой Бушке), дерматологическим заболеваниями (саркоидозом кожи, липонекробиозом, склеродермоподобной формы поздней кожной порфирии, базально-клеточным раком), поражением мягких тканей (панникулитом, липодерматосклерозом, эозинофильным фасциитом). В дифференциальной диагностике принимают участие онкологи, гематологи.
Лечение
Этиотропной терапии не существует. Метод лечения и вид лекарственного средства необходимо подбирать с учетом формы заболевания, тяжести течения и локализации очагов. При линейной и бляшечной формах используются топические глюкокортикостероиды высокой и сверхвысокой активности (бетаметазон, триамцинолон), синтетические аналоги витамина Д. При выраженной индурации кожи эффективны аппликации с диметилсульфоксидом. В случае поражений внутренних органов с целью уменьшения фиброзообразования назначаются пеницилламин и инъекции гиалуронидазы.
При неглубоких процессах хорошим терапевтическим действием обладает ПУВА-терапия, которая включает облучение кожи ультрафиолетовыми волнами длинного спектра с одновременным пероральным или наружным применением фотосенсибилизаторов. Тяжелое поражение кожи служит показанием к применению иммунодепрессантов (метотрексата, такролимуса, микофенолата), синдром Рейно - блокаторов кальциевых каналов (нифедипина) и препаратов, улучшающих микроциркуляцию (пентоксифиллина, ксантинола никотината). При склероатрофическом лихене проводится низкоинтенсивная лазеротерапия. В случае развития контрактур суставов, значительно затрудняющих движения, или грубых деформаций скелета и косметических дефектов лица требуется хирургическая операция.
Профилактика и прогноз
В подавляющем большинстве случаев очаговая склеродермия имеет доброкачественное течение. Правильно подобранная терапия позволяет добиться регресса симптомов. Иногда наступают спонтанные ремиссии заболевания. Неблагоприятные исходы возникают при тяжелых формах (прогрессирующей гемиатрофии лица, пансклеротической инвалидизирующей склеродермии), а также поражении внутренних органов. Эффективных методов профилактики не разработано. Рекомендуется избегать или максимально ограничить контакт кожи с химическими соединениями (кремнием, сицилием, хлорвинилом, нефтепродуктами, органическими растворителями, пестицидами, эпоксидной смолой).
2. Ревматические заболевания/ Под ред. Дж.Х. Клиппела, Дж.Х. Стоуна, Л.Дж. Кроффорд, П.Х. Уайт – 2012.
3. Диффузные болезни соединительной ткани: руководство для врачей/ под ред. проф. Мазурова В.И. –2009.
ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России
ГКБ №14 им. В.Г. Короленко Департамента здравоохранения Москвы
Первый МГМУ им. И.М. Сеченова
Клиническая характеристика склероатрофического лихена у детей
Журнал: Клиническая дерматология и венерология. 2015;14(1): 75‑78
ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России
Представлены краткие исторические сведения о склероатрофическом лихене. Авторы обращают внимание на тенденцию увеличения случаев заболевания в детском возрасте с запоздавшей диагностикой. Это связано с многообразием клинических проявлений дерматоза и редкой встречаемостью данной патологии в практике детских гинекологов, дерматовенерологов и педиатров. Подробно представлены возрастные особенности клинических проявлений и течения заболевания у детей, особенно в случаях вовлечения в патологический процесс области гениталий. Рассматриваются вопросы диагностики и его лечения. Описаны собственные клинические наблюдения развития склероатрофического лихена гениталий (САЛГ) у детей в возрасте 8 и 12 лет. Комплексная терапия САЛГ позволила достичь клинически положительный эффект. Представленные сведения касаются особенностей локализации, клинического полиморфизма и подходов к лечению склероатрофического лихена в детском возрасте. Систематизация клинических проявлений данного заболевания представляет интерес не только для практических дерматологов, но и детских гинекологов, урологов и педиатров.
ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздрава России
ГКБ №14 им. В.Г. Короленко Департамента здравоохранения Москвы
Первый МГМУ им. И.М. Сеченова
Склероатрофический лихен (САЛ) (синонимы: болезнь «белых пятен», белый лихен Цумбуша) — редко встречающееся заболевание с малоизученными этиологией и патогенезом. Его клиника и течение у детей характеризуется рядом особенностей, к которым можно отнести редкость заболеваемости мальчиков, преимущественную локализацию очагов поражения в области кожно-слизистых покровов гениталий, выраженность субъективных ощущений, полиморфизм клинических проявлений. Клиническая картина САЛ впервые была описана F. Hallopeau (1887), а патоморфологическая характеристика — J. Darier (1892) [1]. Ряд авторов, например Л.Н. Машкилейсон (1965), С.И. Довжанский (1979), Ю.К. Скрипкин, В.Н. Мордовцев (1999), В.А. Волнухин (2002) [2—4] рассматривают САЛ как один из вариантов течения ограниченной склеродермии. Это предположение основывается на нередком сочетании САЛ с различными формами склеродермии, сходной гистологической картиной заболевания и подходами к лечению. Описаны случаи сочетания типичных очагов бляшечной склеродермии на коже туловища и конечностей с САЛ половых органов [5—6]. В то же время другие исследователи, например, О.Л. Иванов (1997) [7], Т. Фицпатрик и др. (1999) считают САЛ нозологически самостоятельным заболеванием с четко очерченными клинической и гистологической картинами.
В литературе различные аспекты данной патологии (особенно у детей) освещены недостаточно. В последнее время отмечается тенденция к увеличению случаев заболевания в детском возрасте с запоздавшей диагностикой. Это связано с многообразием клинических проявлений дерматоза и редкой встречаемостью данной патологии в практике детских гинекологов, дерматовенерологов и педиатров [8].
К этиопатогенетическим механизмам развития САЛ относят ряд эндогенных (наследственная предрасположенность, нейроэндокринные и дисгормональные нарушения, хронические воспалительные заболевания, стрессы) и экзогенных (переохлаждение, инфекции вирусной и бактериальной природы, механические повреждения) факторов. Описан случай локализованной буллезно-геморрагической формы САЛ у мальчика после проведения обряда ритуальной циркумцизии [9].
Клинические проявления и течение заболевания у детей имеют ряд возрастных особенностей. Заболевание начинается в возрасте 5—8 лет. Очаги поражения локализуются преимущественно в области половых органов и в перианальной зоне. Клинически в области вульвы наблюдается нечетко ограниченная эритема и беловатые склерозирующиеся бляшки, образующие фигуру «восьмерки». У этих больных можно обнаружить экскориации в области клитора и малых половых губ. У мальчиков поражается в основном головка полового члена. Если в процесс вовлекается препуций, может развиться вторичный фимоз. САЛ у мальчиков может сочетаться со стенозом мочеиспускательного канала или его наружного отверстия, что влечет за собой вторичные осложнения вплоть до почечной недостаточности [10]. Пораженные участки кожи легко травмируются. Пациенты жалуются на дизурию или болезненную дефекацию, что в дальнейшем может быть связано с формированием у детей невротических реакций [1]. Описан феномен Кебнера при САЛ, особенно выраженный в детском возрасте. В качестве травмирующих агентов в области гениталий у детей могут выступать глистные инвазии, аллергические проявления, сопровождающиеся зудом, инфекции мочевыводящих путей.
Для экстрагенитальной локализации характерны плоские папулы, которые могут возвышаться, несколько западать или находиться на уровне здоровой кожи, размером от нескольких миллиметров в диаметре, оттенком от розового до цвета слоновой кости. Папулы могут сливаться в поверхностные бляшки различных размеров, по периферии которых иногда наблюдается эритематозный или гиперпигментированный венчик. По мере прогрессирования процесса развивается атрофия, появляются коричневые фолликулярные роговые пробки.
Характерны полиморфные клинические формы склероатрофического лихена гениталий (САЛГ) у детей [1, 10].
1. Папулезный САЛГ — отдельные изолированные плоские папулы, оставляющие после своего разрешения белесоватые участки поверхностной атрофии. Высыпания у девочек, как правило, располагаются на внутренней поверхности больших половых губ, в области задней комиссуры, не распространяясь на перианальную область. Субъективные ощущения выражены слабо. Папулезная форма САЛГ наблюдается в более позднем возрасте по сравнению с другими вариантами, является более резистентной к проводимому лечению.
2. Эритематозно-отечный САЛГ характеризуется преобладанием воспалительных явлений в очаге: выраженной гиперемией, отечностью в области больших половых губ, препуции, а в ряде случаев и вокруг анального отверстия. На фоне выраженных воспалительных явлений имеются участки поверхностной атрофии белесоватого цвета. Эта форма САЛГ часто встречается у детей с отягощенным аллергологическим анамнезом. У девочек нередко сопровождается вульвовагинитом.
3. Витилигинозный САЛГ — распространенная форма, проявляющаяся очагами поверхностной атрофии, трещинами, депигментациями, локализующимися в области задней спайки, головки полового члена, крайней плоти. Субъективные ощущения обычно отсутствуют, а изменения на коже часто обнаруживаются случайно. Детские гинекологи и урологи наиболее часто расценивают эти изменения как лейкоплакию или витилиго.
4. Буллезный САЛГ характеризуется появлением пузырьков с серозным или геморрагическим содержимым, расположенных на фоне очагов атрофии и гиперемии. Буллезные элементы располагаются субэпидермально. После их вскрытия обнаруживаются эрозии, соответствующие очертаниям пузырей, с обрывками эпидермиса по периферии. Больных беспокоят зуд, жжение при мочеиспускании, болезненность. Буллезный вариант САЛГ отличается крайне упорным течением, резистентностью к проводимой терапии [9]. Наиболее часто описанные нарушения расцениваются детскими гинекологами и дерматологами как проявления герпеса. При локализации атрофического процесса в области полового члена развивается кольцевидное сужение крайней плоти, а уплотнение слизистой оболочки приводит к формированию фимоза. Появление пузырей является симптомом прогрессирования атрофического процесса.
5. Для атрофической формы САЛГ характерны четкие границы очагов поражения, частое распространение на перианальную область. В очагах преобладают явления атрофии по типу «папиросной бумаги».
6. Эрозивно-язвенный САЛГ характеризуется спонтанным образованием болезненных кровоточащих эрозий на фоне выраженной гиперемии и атрофии без предшествующего образования пузырей. Больных беспокоит зуд и болезненность в очагах поражения.
САЛГ независимо от клинической разновидности отличается длительным хроническим течением с повторяющимися обострениями вплоть до пубертатного периода. В пубертатный период часто происходит спонтанное разрешение САЛ или значительное улучшение (наступление периода половой зрелости, возрастные физиологические изменения гормонального фона), что в большинстве случаев и объясняет благоприятный исход САЛГ у детей.
Гистологически САЛ характеризуется атрофией эпидермиса, вакуольной дистрофией клеток базального слоя, отеком и полосовидным лимфоцитарным инфильтратом. В сосочковом слое дермы обнаруживается гомогенизация коллагеновых волокон. Наблюдается гиперкератоз, значительно превосходящий атрофичный мальпигиев слой, с образованием роговых кератотических пробок.
Диагноз основывается на данных клинической картины заболевания. В круг болезней для дифференциальной диагностики включают витилиго, красный плоский лишай, идиопатическую атрофию кожи, ксеротический облитерирующий баланит, синехии крайней плоти (рис. 1).

Рис. 1. Синехии крайней плоти у ребенка 4 лет.
Подход к лечению САЛ у детей неоднозначен. В основном используют средства, имеющие патогенетическую направленность. Однако главная цель терапии — замедлить прогрессирование болезни, достичь стабилизации процесса, а в дальнейшем — регресса клинической картины [1, 10, 11]. Лечение проводят повторными курсами (не менее 3) антибиотиков (пенициллин, тетрациклин и другие), сосудистыми препаратами, улучшающими трофику, микроциркуляцию (например, ксантиноланикотинат, никошпан, теоникол), экстрактом алоэ и плаценты, солкосерилом. Местно применяются мази, стимулирующие репаративные процессы, оказывающие противовоспалительное действие. Мальчикам с САЛГ при недостаточном эффекте терапии рекомендуют раннее обрезание.
Приводим клинические наблюдения пациентов.
Больная Ж., 8 лет, родилась от первой беременности с массой тела 3800 г. Развитие до года без особенностей. Наследственность не отягощена.
Перенесенные заболевания: ОРВИ, хронический тонзиллит с последующей тонзилэктомией в 6 лет, аденоиды II степени.
Больна в течение 1,5 лет, когда впервые возникли упорный зуд, краснота, трещины в области наружных половых органов, жжение при мочеиспускании. Детским гинекологом диагностирован вульвовагинит, лейкоплакия вульвы. Проведенное лечение было неэффективным. Со стороны внутренних органов и систем патологии не выявлено. Направлена на консультацию к дерматовенерологу.
При осмотре: большие половые губы развиты правильно. Патологический процесс локализуется в области передней и задней промежности, до ануса. На внутренней поверхности больших половых губ определяются участки поверхностной атрофии белесоватого цвета со сглаживанием рельефа слизистой и нечеткой дифференцировкой малых половых губ и клитора. В задней спайке трещины, мацерация (рис. 2).

Рис. 2. Больная Ж., 10 лет. Склероатрофический лихен вульвы до лечения.
Диагноз: «Склероатрофический лихен аногенитальной области, атрофическая форма».
Пациентке проведены три курса стационарного лечения в клинике им. В.Г. Короленко. Получала пенициллин, актовегин, трентал, витамин Е, наружную мазевую терапию. В результате проведенного лечения субъективные ощущения значительно уменьшились, трещины эпителизировались.
Больной М., 10 лет, родился от первой беременности. Масса тела при рождении 3500 г. Наследственность не отягощена.
Перенесенные заболевания: краснуха, ОРВИ, ветряная оспа. Сопутствующие: диффузный нетоксический зоб 0—I ст.
Болен около года, когда родителями впервые было замечено белесоватое пятно на головке полового члена. Обследован дерматологом и урологом. При обращении: общее состояние удовлетворительное, патологии внутренних органов и систем не выявлено.
При осмотре: патологический процесс локализован в области головки полового члена, а также наружного и внутреннего листка крайней плоти, представлен очагами атрофии и склероза. Кожа крайней плоти сужена, головка выводится с трудом. Определяется сужение переднего отверстия уретры.
Диагноз: «Склероатрофический лихен аногенитальной области, атрофическая форма. Стриктура переднего отверстия уретры».
Пациенту проведены пять курсов стационарного лечения в клинике им. В.Г. Короленко. Получал пенициллин, актовегин, трентал, ксантиноланикотинат, кокарбоксилазу, пиридоксин, аевит. Наружно: мазь актовегин. В результате проведенного лечения наблюдалось заметное улучшение: уменьшение очагов рубцовой атрофии, их размягчение, свободное открытие головки (рис. 3).

Рис. 3. Больной М., 12 лет. Склероатрофический лихен головки полового члена после лечения.
Таким образом, вышеизложенные сведения свидетельствуют об особенностях локализации, клиническом полиморфизме и подходах к лечению САЛ в детском возрасте. Систематизация клинических проявлений данного заболевания несомненно представляет интерес не только для практических дерматологов, но и детских гинекологов, урологов и педиатров.
Читайте также:

