Гипертермия при меланоме кожи
Обновлено: 04.05.2024
Традиционно радиотерапию не принято включать в программу лечения первичных очагов кожных форм меланомы. Облучение если и назначают, то проводят его в рамках адъювантного лечения после удаления лимфоузлов (операции лимфодиссекции) с целью уменьшения риска рецидива заболевания.
Во всем мире чаще всего к радиотерапии специалисты прибегают при рецидиве меланомных опухолей и с целью воздействия на метастазы, в частности лучевая терапия помогает облегчить симптомы при метастатических поражениях меланомой головного мозга и костных тканей.
При меланомах используются как контактные, так и дистанционные техники облучения, для каждой из которых существует перечень своих определенных показаний. К примеру, максимальный лечебный эффект дистанционного γ-излучения наблюдается именно на глубине около четырех-пяти миллиметров, близкофокусная рентген-терапия дает неплохие результаты при поверхностных поражениях слизистых оболочек и кожи и т.д.
Высокодозное (4-8 Гр за 1 фракцию) облучение практически у 70% больных эффективно при метастазах в мозг и в каждом втором случае, когда вторичные очаги обнаружены в костях, в подкожной клетчатке, в лимфоузлах.
Причем сочетание радиотерапии с гипертермией способствует повышению эффективности проводимого лечения до 75-80%. При крупных (свыше 10 мм) меланомных опухолях доктора практикуют комбинированную химиолучевую терапию в дооперационный период.
Уменьшение объема (регресс) опухоли в подобных ситуациях отмечается в среднем у 60% пациентов. Благодаря методике крупного фракционирования выполнять запланированное хирургическое вмешательство можно буквально сразу же после завершения курса радиотерапии.
При данной технике облучения сама первичная опухоль получает суммарную дозу около 60-70 Гр, а вовлеченные в метастатический онкопроцесс лимфоузлы – приблизительно 40-45 Гр-экв.
Необходимо отметить, что в последние годы доказана целесообразность проведения радиохирургических вмешательств (с-ма «Гамма-нож») при наличии небольших (менее 30 мм) метастазов меланомы в тканях мозга (стереотаксическое сфокусированное облучение злокачественного образования суммарной дозой до 30 Грей).
И, конечно, нельзя не сделать акцент на протонной терапии, которая считается сейчас самым перспективным и многообещающим методом лечения, дающим возможность успешно справляться даже с радиорезистентными опухолями. Она основана на использовании положительно заряженных частиц – протонов, пучки которых направляются на патологический очаг подобно всем известным рентген-лучам.
Важным преимуществом протонной терапии служит большая энергия, направляемая во время сеанса облучения непосредственно на меланомную опухоль и не травмирующая здоровые ткани. При протонной терапии можно не только регулировать направленность доз радиоактивного излучения на пораженный онкопроцессом участок, но и рационально распределять дозы внутри новообразования.
Кстати, лечение посредством протонной терапии может быть в числе прочего применено и тогда, когда речь идет о четко ограниченных опухолях, находящихся очень близко к радиочувствительным структурам. Сама процедура облучения протонами не сопровождается каким бы то ни было дискомфортом, минимально допустимые повреждения интактных тканей не вызывают тошнот, рвот и диареи.
Благодаря беспрецедентно высокой точности воздействия на опухоли протонное излучение позволяет сократить курс лечения меланомы за счет уменьшения количества лечебных сеансов и применения более высоких доз радиации при самой минимальной нагрузке на здоровые ткани.
Длится процедура всего лишь несколько минут, при этом основное время у специалистов уходит на настройку аппаратуры и расположение пациента в правильной позиции. Назначаться протонная терапия может не только взрослым, но и детям, в т.ч. при рецидивах меланомы после ранее проведенного хирургического лечения и для уничтожения отдаленных метастатических очагов.
г. Москва, Духовской переулок, 22б
Что такое меланома? Причины возникновения, диагностику и методы лечения разберем в статье доктора Беляниной Елены Олеговны, онколога со стажем в 25 лет.
Над статьей доктора Беляниной Елены Олеговны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Меланома (от греч. melanos – "чёрный", "тёмный") — это злокачественная опухоль, развивающаяся из меланоцитов (клеток, синтезирующих меланин). Чаще всего она образуется из кожных меланоцитов, то есть располагается на коже. В 7% случаев меланома локализуется на сетчатке глаза и в 1-3% случаев — на слизистых оболочках прямой кишки, полости рта, оболочках головного и спинного мозга. [1] [2]
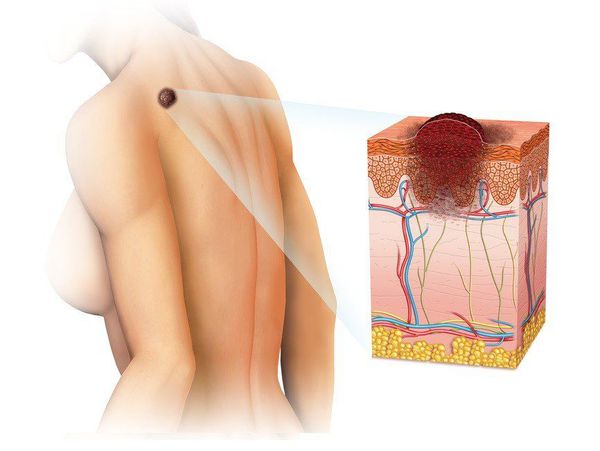
Эта болезнь — одна из наиболее злокачественных опухолей, которая часто метастазирует в разные органы.
Заболеваемость меланомой продолжает увеличиваться. По росту смертности эта патология занимает второе место после рака лёгкого. [3]
В настоящее время и звестно значительное количество факторов, которые повышают вероятность заболевания меланомой. Ни один из них не может быть признан главным или обязательным дл я возникновения заболевания. Однако современные исследования чётко установили, что основная причина меланомы — воздействие ультрафиолетовых лучей естественного солнечного света (а также излучения солярия) на кожу человека. [1] [4]
Другие факторы риска развития меланомы:
- светлая кожа (склонность к солнечным ожогам, светлые или рыжие волосы, голубой цвет глаз);
- большое количество невусов (родинок), в том числе наличие атипичных;
- меланома в личном анамензе, а также наличие меланомы у кровных родственников;
- солнечные ожоги с образованием пузырей, наличие солнечных ожогов в детстве;
- существование врождённого невуса (риск возрастает пропорционально увеличению его размера).
Особенности меланомы у детей
У детей меланома бывает редко. Однако беспигментная меланома у детей может выглядеть как обычная бородавка. Также часто встречается разновидность невусов — невус Шпитц (резко очерченная куполообразная розовато-красная папулу или бляшку), который также не всегда можно отличить от меланомы. Для уточнения необходимо наблюдение и цифровая дерматоскопия.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы меланомы
Первые признаки меланомы — появление на коже образования, непохожего на остальные по размеру, цвету и форме.
Меланома отличается от родинки следующими признаками: образование асимметричное по цвету и структуре, его края неправильные и зубчатые, оттенки в пределах одного образования отличаются, размер образования более 4 мм. С течением времени меланома изменяется по одному или нескольким ранее перечисленным критериям.
При обследовании важно учитывать, насколько пигментное образование отличается от остальных. Выявление "гадкого утёнка" среди родинок является причиной его более детального осмотра.
Клиническая картина меланомы достаточна разнообразна. Внешне она может представлять собой как незначительное пигментное пятно, так и узловое образование с изъязвлением. Цвет варьируется от светло-коричневого до чёрного.
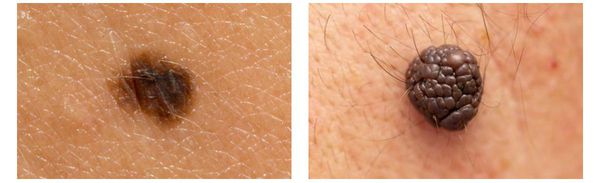
Зачастую меланома возникает у взрослых, но иногда встречаются случаи врождённой формы заболевания. В детском возрасте меланома развивается редко.
Меланома локализуется на любых участках кожи, в том числе и на ногтевой ложе.
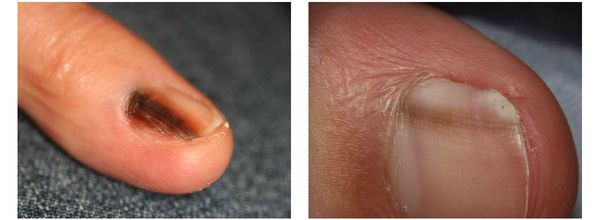
Различают четыре основных типа меланомы в зависимости от клинической картины, течения заболевания, анатомического расположения и гистологических параметров.
1. Поверхностно-распространяющаяся меланома встречается в 65-75% случаев. Для неё характерно длительное течение. Сначала это пятно коричневого цвета, которое постепенно растёт и становится асимметричным по структуре и цвету (появляются вкрапления тёмно-коричневого, чёрного и розового цвета). При переходе в вертикальную фазу роста на пятне появляется утолщение — бляшка. Наиболее часто встречаемая локализация у мужчин — на спине, а у женщин — преимущественно на нижних конечностях.
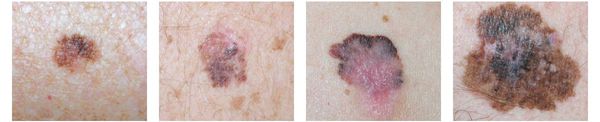
2. Лентиго-меланома представлена в виде пятна неправильной формы и окраски. Она развивается у лиц пожилого возраста. Чаще всего локализуется на лице, шее и тыле конечностей. Лентиго-меланома растёт на фоне длительно существующего злокачественного лентиго (предракового меланоза Дюбрейля). При инвазии клеток меланомы за пределы эпидермиса на пятне появляются возвышающиеся участки.
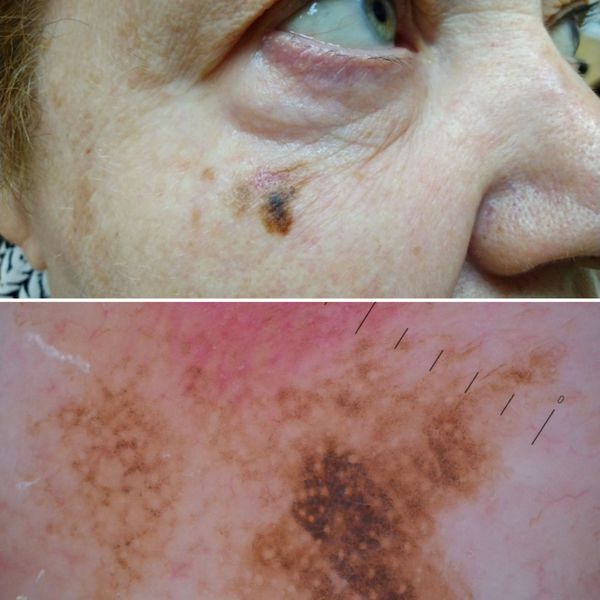
3. Узловая меланома представлена выступающим над поверхностью кожи образованием тёмно-коричневого или чёрного цвета. Часто эти образования симметричны и не вызывают подозрений. Однако, как правило, такая меланома характеризуется быстрым ростом и плотные на ощупь. С ростом опухоли она может изъязвляться. Чаще всего располагается на спине, голове и шее.
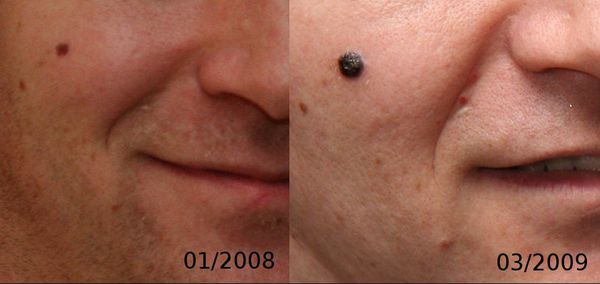
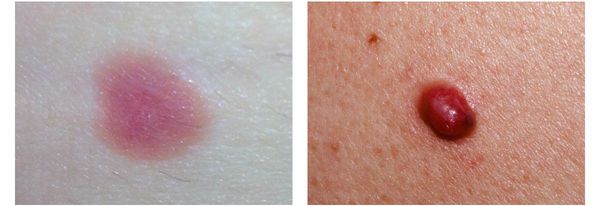
4. Во всех формах возможны беспигментные варианты (около 2%). Беспигментная (амеланотическая) меланома достаточно сложна для диагностики, так как сначала выглядит как безвредная розово-красная папула.
Поздние симптомы меланомы. Появление метастазов
Признаки метастазов зависят от того, в каком органе они появились:
- головной мозг — головные боли, неврологические симптомы (нарушение чувствительности к теплу, боли, расстройства памяти, координации и подвижности и т. п.);
- кости — боли в спине;
- лимфатические узлы — их увеличение и болезненность;
- на коже вблизи первичного очага — одновременное появление множества чёрных образований.
Патогенез меланомы
Патогенез меланомы, как и всех злокачественных опухолей, весьма сложный. Результат воздействия ультрафиолета на кожу человека (лучей А и В, длиной 280-340 нм) зависит от многих факторов, включающих дозу облучения и индивидуальный ответ организма (особенности иммунного ответа и генетическую предрасположенность).
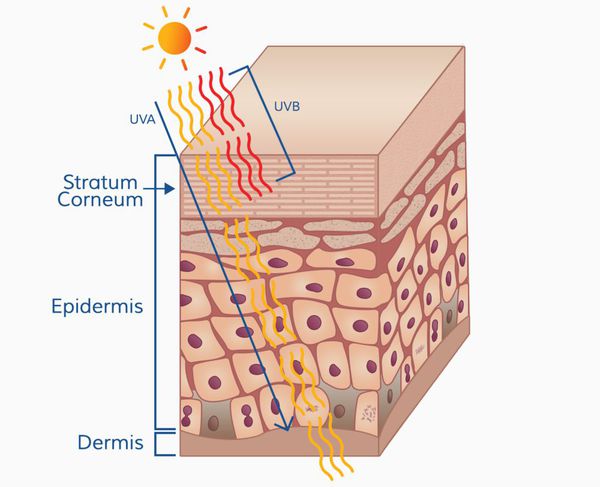
Ультрафиолетовое облучение вызывает:
- фотохимические реакции;
- повреждение молекулы ДНК (иногда повреждение восстанавливается);
- мутации (когда повреждение ДНК "не лечится" организмом);
- иммунные нарушения.
Образование пиримидиновых димеров (т. е. дефектов ДНК) под действием УФО — основная причина мутаций. [5]
Роль диспластических невусов в развитии меланомы недостаточно ясна. Проводимые исследования пока не ответили на вопрос, являются ли эти образования предраковым состояниям, или развитие меланомы в их зоне является статистически случайным событием.
По данным многочисленных гистологических исследований, около 30% меланом развиваются в области меланоцитарных невусов , остальные 70% развиваются на неизменённой коже. [6] [7] [8]
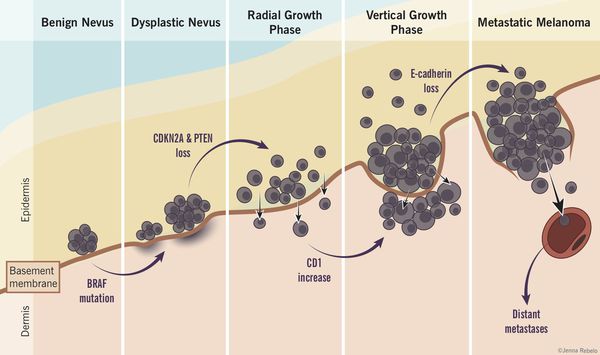
Таким образом, по имеющимся данным, на фоне невусов развивается небольшой процент всех случаев злокачественной меланомы. [4]
Атипичные невусы в первую очередь являются важными маркерами повышенного риска меланомы. При этом профилактическое удаление таких невусов нецелесообразно (они не являются 100% предшественником меланомы)
Пациенты с диспластическими невусами представляют собой группу повышенного риска и должны находиться под постоянным врачебным наблюдением.
В 7-15% всех случаев меланома является наследственной патологией. При этом обнаруживаются мутации в генах-супрессорах опухолевого роста.
Классификация и стадии развития меланомы
Стадию опухолевого процесса меланомы определяют в соответствии с классификацией TNM. Она зависит от толщины первичной опухоли, а также наличия или отсутствия регионарных и/или отдалённых метастазов.
Для определения стадии меланомы необходимо гистологическое исследование. Оценку состояния лимфоузлов для установления стадии выполняют при помощи клинического осмотра и ультразвукового исследования.
Критерий Т говорит о распространённости первичной опухоли (для классификации по этому критерию необходимо удалить первичную опухоль и провести её гистологическое исследование):
- pТis — первичная (неинвазивная) меланома (I уровень инвазии);
- pТ1 — толщина опухоли ≤ 1 мм:
○ pТ1а — II уровень прорастания опухоли в соседние ткани или III уровень без изъязвления опухоли;
○ pТ1b — IV или V уровень прорастания опухоли в соседние ткани или присутствие её изъязвления;
○ pТ2а — без изъязвления опухоли;
○ pТ2b — с изъязвлением;
○ pТ3а — без изъязвления;
○ pТ3b — с изъязвлением;
○ pТ4а — без изъязвления;
○ pТ4b — с изъязвлением.
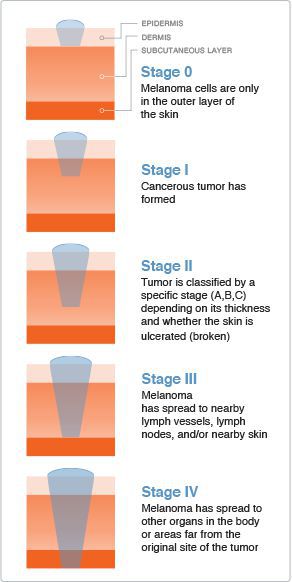
Критерий N говорит о существовании или отсутствии метастазов в регионарных лимфоузлах :
Иммунотерапия меланомы и ее эффективность
При рецидивирующих поражениях кожи и лимфатических узлов местная обработка опухоли противотуберкулезной вакциной Кальметта-Герена (БЦЖ) приводит к развитию локального иммунного ответа. Для этой цели используется также б-интерферон.
К сожалению, в большинстве случаев достигается лишь кратковременный ответ, и процедура оказывается неэффективной для больных с метастазами во внутренние органы и в кости.
Обнаружение пептидов, специфических для клеток меланомы, позволило разработать новый подход к созданию вакцины, эффективной в лечении первичных и вторичных опухолей. Наиболее широко известный пептид (из семейства антигенов (генов) меланомы, MAGE) представляет собой рекомбинантный эпитоп, обладающий иммуногенными свойствами. Есть основания предполагать, что он окажется эффективным.
Модификаторы биологического ответа и гипертермия в лечении меланомы
После разработки методов иммунотерапии меланомы в 1970-х годах, внимание клиницистов привлек модификатор биологического ответа, интерферон, который оказался эффективным в лечении других раков (а именно В-клеточных лимфом).
Оказалось, что у 10-20% больных все интерфероны (а, b, у) проявляют терапевтическое действие, хотя в большинстве случаев оно проявляется в отношении небольших опухолей и носит кратковременный характер. При местном применении а-интерферона иногда наблюдается полное исчезновение опухоли на коже.
В одном из последних исследований а-интерферон применяли или изолированно в высоких дозах, или совместно с химиотерапией. Иногда лечебный эффект проявлялся, иногда отсутствовал.
В течение последних пяти лет для лечения меланомы применяется интерлейкин-2. Препарат назначается изолированно или совместно с культурой аутологичных лимфоцитов, которые при этом начинают проявлять цитотоксическое действие по отношению к опухолевым клеткам. Эти киллерные клетки, активированные лимфокинами (LAK), дают лишь кратковременные воспалительные осложнения и оказываются эффективными примерно у 25% больных.
К сожалению, при применении интерлейкин/LAK возникают многочисленные побочные эффекты, связанные с дозировкой, что затрудняет их применение.
Как при других раках, в лечении меланомы совместно с перфузией раствором мелфалана использовалась тепловая энергия (метод гипертермии). Хотя при температуре 41-45 °С погибает большее количество клеток опухоли, при этом проявляется сильная токсическая реакция. Поэтому, чаще используют более мягкие условия (39-40 °С).
В настоящее время исследование возможностей гипертермии в лечении меланомы проводятся в рамках программ Европейской организации исследования и лечения рака и ВОЗ.

Реаферон - препарат интерферона-а
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лучевая терапия меланомы и ее эффективность
Однако она может оказаться полезной для больных, у которых патологический процесс зашел слишком далеко, особенно в случае меланомы lentigo maligna, когда хирургическое лечение оказывается невозможным.
Поскольку в основном поражается кожа на конечностях, можно давать достаточно высокие дозы радиации, не опасаясь действия облучения на внутренние органы.
Для преодоления эффекта плеча, который, в основном, определяет радиоустойчивость клеток, обычно используют большие фракции дозы (более 5 Гр).
Паллиативная лучевая терапия меланомы
Паллиативное облучение показано для отдельных больных с метастазами в головной мозг и в кости. Хотя меланома не относится к числу наиболее радиочувствительных опухолей, ее устойчивость можно преодолеть используя большие фракции дозы.
При этом примерно у 25% больных в течение продолжительного времени удается контролировать процессы роста первичной опухоли и метастазирования. Исследуется эффективность новейших методов, таких как облучение нейтронами и заряженными частицами, а также применение радиосенсибилизаторов и гипертермии.
К числу новых интересных подходов локальной терапии относится борнейтронзахватная терапия. Метод основан на способности опухоли усваивать фени-лаланин, необходимый для синтеза меланина. При этом в качестве субстрата используется фенилаланин, содержащий ко-валентно-связанный изотоп бора, 10 B1-n-баренилфенилаланин.
Если затем клетки облучить достаточно безопасными тепловыми нейтронами, то происходит их захват ядром 10В, которое при этом распадается с образованием ядра лития и а-частицы. Энергия излучения избирательно высвобождается внутри опухолевых клеток, синтезирующих меланин, и вызывает их гибель. Метод использовался для лечения больных с меланомой, причем были получены обнадеживающие результаты.
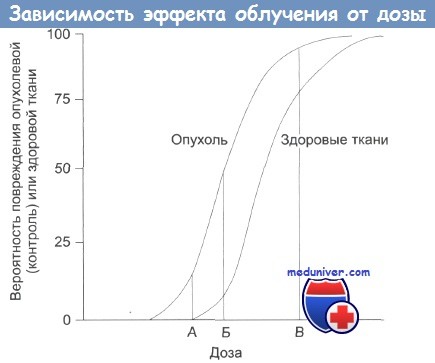
Зависимость терапевтического эффекта от дозы облучения.
А — нижняя безопасная доза;
Б — увеличение дозы: растет поражение здоровых тканей;
В — наивысшая вероятность успешного лечения, но и высокая вероятность поражения здоровых тканей, многочисленные побочные эффекты, некоторые из которых могут проявиться в отдаленном будущем
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Локальная гипертермия при лечении опухоли. Химиотерапия опухоли кожи.
Что касается локальной гипертермии, то ее нельзя рассматривать как самостоятельный метод лечения опухолей кожи. Она используется в комплексе с химиотерапией или лучевой терапией, позволяя не только повысить эффективность, но и уменьшить частоту побочных эффектов этих методов. Метод гипертермии в СВЧ-, УВЧ- и ВЧ-диапазонах основан на том. что микрососудистая система опухолей в большей степени подвержена деструктивному воздействию гипертермии, чем микрососудистая система нормальной ткани.
Гипертермию с успехом использовали в комплексном лечении метастатической меланомы, болезни Боуэна, метастазов плоскоклеточного рака внутренних органов в кожу. Курс лечения продолжался до 3-4 мес. Клинический эффект (например, прилечении гипертермией болезни Боуэна) наступал через 2-4 нед., очаги, оставшиеся после курса гипертермии, были удалены хирургическим путем в пределах окружающих здоровых тканей; рецидив отмечался в 1 из 6 случаев. При гистологическом исследовании в регрессирующем очаге болезни Боуэна оказались более выраженными инфильтрация Т-лимфоцитами, васкуляри-зация, экспрессия рецепторов к Fas-антигену и фактору некроза опухоли.
В некоторых случаях при новообразованиях кожи возможно применение общей химиотерапии. Для введения химиопрепаратов в организм используют пероральный, внутривенный, внутримышечный, внутриартериальный регионарный, эндолимфатический пути. Цитостатические средства, используемые в дермато-онкологической практике, представлены несколькими группами.
Первая группа химиопрепаратов — апеллирующие вещества. Они обладают цитостатической активностью, так как способны образовывать ковалентные связи с нуклеофильными соединениями, в том числе со структурными элементами ДНК, что приводит к блокаде митоза и нарушению жизнедеятельности клетки. В эту группу включают производные бисфхлорэтиламина, этиленамины и этилендиамины, алкилсульфонаты, производные нитрозомочевины и триазена. Обычно они используются при лечении множественной базалиомы и метатипического рака (проспидин), лимфомы кожи (проспидин, фотрин, хлорамбуцил, циклофосфамид, эмбихин, сарколизин, дакарбазин, дегранол, допан), саркомы Капоши (проспидин, циклофосфамид, фотрин), меланомы (дакарбазин).
Вторая группа химиопрепаратов — антиметаболиты — соединения, нарушающие синтез нуклеиновых кислот и представленные аналогами фолиевой кислоты (метотрексат, используемый, например, при лечении кератоакантомы), пуринов (фопурин, используемый для лечения лимфомы кожи и саркомы Капоши) и пиримидинов (фторофур, применяющийся для лечения лимфомы кожи).
В состав третьей группы химиопрепаратов входят алкалоиды (винбластин и винкристин, применяемые при лимфоме кожи), антибиотики: блеомицин (применяемый при лимфоме кожи, плоскоклеточном раке кожи, болезни Боуэна, бородавках); брунеомицин и доксорубицин (при лимфомах кожи); дактиномицин (при саркоме Капоши и меланоме).
Четвертая группа химиопрепаратов — синтетические вещества разного химического строения: производные мочевины (гидроксикарбамид, применяющийся при меланоме и болезни Ходжкина), а также рад других соединений.
Все перечисленные группы цитостатических средств обладают способностью оказывать действие не только на клеточные популяции, характеризующиеся злокачественным ростом, но и на другие тканевые системы, обладающие быстрой пролиферацией (иммунную систему, клетки слизистой оболочки желудочно-кишечного тракта, кожу и ее придатки). Многие из них высокотоксичны. Среди осложнений химиотерапии наиболее часто описываются: тошнота, рвота, диарея, анорексия, стоматит, алопеция, геморрагический синдром, анемия, тромбоцитопения, лейкопения, гепатит, нефрит, дерматит. Профилактика и лечение осложнений проводятся так же, как при лучевой терапии.
Химиотерапия противопоказана при выраженном истощении больного, диссеминации опухолевого процесса, особенно с метастазами в головной мозг, печень, почки; исходном угнетении гемопоэза (менее 3,0 х 10 9 \л лейкоцитов и 100 х 10 9 \л тромбоцитов), патологии сердечнососудистой системы, активном туберкулезе.

Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

