Эритематозно-сквамозные высыпания что это
Обновлено: 01.05.2024
Атопический дерматит (АД) — наследственное, иммунонейроаллергическое, хроническое рецидивирующее воспалительное заболевание кожи, обусловленное атопией, проявляющееся интенсивным зудом, симпатергической реакцией кожи (белым дермографизмом), преимущественно эритематозно-лихеноидными высыпаниями, в сочетании с другими признаками атопии.
В 1923 г. американские аллергологи Coca A. F. и Cooke R. A., желая описать необычный тип гиперчувствительности к различным веществам окружающей среды, который возникал только у людей и чаще встречался в семьях без явной предшествовавшей сенсибилизации, обратились за помощью к филологу Perry из Колумбийского университета. Он и предложил ученым использовать термин «атопия», в переводе означающий «не на своем месте» или «странный» [29]. Под атопией понимают наследственную предрасположенность к аллергическим реакциям в ответ на определенные антигены. Первым описанным в литературе «атопиком» был император Октавий Август, у которого был описан крайне выраженный зуд, сезонный ринит и стесненность дыхания. Кроме того, детально описан и семейный анамнез: его внук, император Клавдий, страдал от симптомов риноконъюнктивита, а внучатый племянник, Британик, — от аллергии на эпителий лошади [41]. Уже более 80 лет термин «атопия» используется во всем мире, хотя и является порой предметом дискуссий.
АД является чрезвычайно распространенным и зачастую тяжело протекающим дерматозом. Его частота в структуре кожных заболеваний, по разным данным, составляет от 20 до 40%. Результаты эпидемиологических исследований показывают, что АД чаще встречается среди молодых людей, чем среди взрослых. Болеют оба пола, несколько чаще женщины. АД возникает у людей всего мира и у всех рас. В течение последних десятилетий распространенность заболевания значительно увеличилась. Например, в Дании общая заболеваемость близнецов в возрасте до 7 лет, рожденных с 1960 по 1964 гг., составляла 3%. А у близнецов, рожденных с 1970 по 1974 гг., этот показатель уже увеличился до 10% [44].
Возникновение и хроническое течение АД обусловливают наследственная предрасположенность, функциональные нарушения нервной системы, влияние неблагоприятных условий окружающей среды, психоэмоциональные расстройства и патология внутренних органов, обменные, нейрогуморальные, нейрососудистые нарушения, аллергические заболевания, нерациональное питание, различные интоксикации [14].
Клинические проявления АД разнообразны, однако достаточно типичны и хорошо изучены. Заболевание обычно начинается в раннем детском возрасте, чаще во втором полугодии жизни. Может продолжаться долгие годы, характеризуясь ремиссиями, в основном в летний, и рецидивами в весенне-осенний периоды года. Со временем острота заболевания ослабевает, и в возрасте 30–40 лет у большинства больных наступает спонтанное излечение. В течении заболевания выделяют три фазы: младенческую (обычно с 7–8 недели жизни до 3 лет), детскую (с 3 до 7 лет) и взрослую. В младенческой и детской фазах чаще наблюдаются очаговые эритематозно-сквамозные высыпания со склонностью к экссудации (везикуляция, мокнутие) на коже лица, ягодицах, конечностях. Во взрослой фазе преобладают зудящие эритематозно-лихеноидные высыпания на сгибательных поверхностях конечностей, на шее с развитием лихенизации (кожа становится утолщенной, грубой на ощупь, кожный рисунок резко выражен). Степень выраженности и распространенности процесса может быть различной — от ограниченных (периоральных) высыпаний до обширного поражения кожного покрова по типу эритродермии. Непременный признак АД, независимо от фазы течения или клинического варианта, — интенсивный зуд, составляющий основу страданий больного, в значительной мере утяжеляющий течение заболевания и снижающий качество жизни [6, 15, 42].
В соответствии с клинической классификацией Сергеева Ю. В. [14], выделяют пять форм АД: лихеноидная, эритематозно-сквамозная, пруригинозная форма, экзематозная, атипичная.
Диагноз АД основывается на комплексе диагностических признаков АД, который получил название критериев Hanifin а. Rajka, 1980 (табл. 1) [37]. Диагноз АД требует наличия по крайней мере трех из четырех главных критериев и трех малых критериев.
Для объективной оценки степени тяжести и распространенности кожного процесса и выраженности зуда при АД группой исследователей Европейского центра по изучению АД была разработана унифицированная шкала симптомов (SCORAD), представляющая собой многопараметровую балльную оценку степени тяжести АД, которая может быть использована в качестве наиболее объективного («золотого») стандарта при научных исследованиях и в клинической практике [32].
Как заболевание, обострения которого могут быть спровоцированы психогенно, АД был отнесен к классическим психосоматическим заболеваниям Францем Александером в 1950 году [21]. С тех пор было проведено большое количество отечественных [3, 4, 5, 8, 9, 10, 11, 12, 13, 18] и зарубежных [19, 20, 37, 22, 23, 28, 30, 33] исследований, посвященных изучению роли психогенных воздействий как провоцирующих обострения АД факторов, а также психических расстройств у больных АД. На модели АД представляется возможным изучение психических расстройств, развивающихся у пациентов с хроническими зудящими дерматозами. Считается, что локализация высыпаний на видимых участках кожного покрова и выраженный зуд приводят не только к снижению качества жизни, но и к развитию патологических психических реакций на болезнь, значительно влияющих на комплаентность пациента в процессе терапии и дополнительно утяжеляющих состояние больных.
Согласно проведенным исследованиям, АД нередко обостряется после психогенных воздействий и зачастую сопровождается психическими нарушениями [24, 25, 26, 27, 34, 35, 38, 39]. Так, ассоциация АД и депрессивных расстройств установлена в исследованиях коморбидности обсуждаемого дерматоза и аффективной патологии. Согласно когортному исследованию, проведенному Timonen М., у 30% больных АД отмечаются эпизоды депрессии в течение жизни [45], что значительно превышает этот показатель в общей популяции (от 5% до 10%) [43]. В исследованиях других авторов депрессии выявлялись у 23–80% пациентов с АД [1, 5, 11, 12, 13, 18]. Коморбидность тревожных расстройств и АД отмечалась почти у половины исследованных больных [4, 46]. Приводятся данные о том, что психологический профиль «атопика» характеризуется депрессией, напряженностью, тревогой и агрессивностью [25, 28, 33]. При этом частое развитие психических расстройств объясняется, как правило, характером кожного заболевания (хроническое течение, интенсивный, в том числе ночной, зуд и локализация высыпаний на видимых участках кожного покрова).
Однако проведенные психосоматические исследования больных АД в большинстве своем основываются либо на использовании формализованных психометрических методик диагностики, либо психологического консультирования и не позволяют оценить долю истинно нозогенных психических девиаций и долю расстройств, развившихся вне зависимости от АД.
В последние годы была создана систематика психодерматологических расстройств (табл. 2). Согласно этой классификации АД относится, с одной стороны, к группе психосоматических болезней, с другой стороны, как хронический дерматоз может быть причиной развития нозогенных реакций и патологических развитий. Однако исследований особенностей психических расстройств при АД с этих позиций не проводилось.
Целью настоящего исследования явилось комплексное клиническое изучение психических расстройств при АД и их связи с особенностями клиники и течения заболевания кожи, направленное на разработку их типологической дифференциации.
Материал и методы исследования
Материал исследования составили 97 пациентов (73 женщины и 23 мужчины; средний возраст 26,9 ± 10,2 года).
Критерии включения: верифицированный диагноз АД согласно международным диагностическим критериям J. M. Hanifin и G. Rajka [37], возраст пациентов от 18 до 65 лет.
Критерии исключения: манифестный шизофренический/шизоаффективний/аффективный психоз, органическое поражение ЦНС, деменция, зависимость от психоактивных веществ, другие тяжелые соматические заболевания в стадии обострения или декомпенсации.
Исследование проведено клиническим методом, предусматривающим комплексное дерматологическое и психопатологическое обследование. Дерматологическое обследование предусматривало анализ анамнестических и клинических показателей, подтверждение диагноза АД. Степень тяжести и распространенность кожного процесса у всех пациентов оценивались при помощи индекса SCORAD (метод, рекомендованный Европейской рабочей группой по АД [32], учитывающий распространенность высыпаний, характер сыпи (эритема, отек, мокнутие, экскориации, лихенификация, сухость) и выраженность субъективных симптомов — зуд, обусловленная АД бессонница.
Психопатологическое обследование проводилось сотрудниками отдела по изучению пограничной психической патологии и психосоматических расстройств (руководитель — академик РАМН А. Б. Смулевич) НЦПЗ РАМН, кафедры психиатрии и психосоматики ФППОВ ММА им. И. М. Сеченова, к. м. н. Дороженком И. Ю., к. м. н. М. А. Терентьевой, к. м. н. В. И. Фроловой, К. А. Батуриным. Экспериментально-психологическое обследование проводилось О. В. Петуховой, Д. А. Бесковой, Л. Т. Козловской. Окончательная квалификация психопатологических расстройств проводилась академиком РАМН А. Б. Смулевичем в рамках клинических разборов, на которые были представлены все пациенты.
Код вставки на сайт
Атопический дерматит (АД) — наследственное, иммунонейроаллергическое, хроническое рецидивирующее воспалительное заболевание кожи, обусловленное атопией, проявляющееся интенсивным зудом, симпатергической реакцией кожи (белым дермографизмом), преимущественно эритематозно-лихеноидными высыпаниями, в сочетании с другими признаками атопии.
В 1923 г. американские аллергологи Coca A. F. и Cooke R. A., желая описать необычный тип гиперчувствительности к различным веществам окружающей среды, который возникал только у людей и чаще встречался в семьях без явной предшествовавшей сенсибилизации, обратились за помощью к филологу Perry из Колумбийского университета. Он и предложил ученым использовать термин «атопия», в переводе означающий «не на своем месте» или «странный» [29]. Под атопией понимают наследственную предрасположенность к аллергическим реакциям в ответ на определенные антигены. Первым описанным в литературе «атопиком» был император Октавий Август, у которого был описан крайне выраженный зуд, сезонный ринит и стесненность дыхания. Кроме того, детально описан и семейный анамнез: его внук, император Клавдий, страдал от симптомов риноконъюнктивита, а внучатый племянник, Британик, — от аллергии на эпителий лошади [41]. Уже более 80 лет термин «атопия» используется во всем мире, хотя и является порой предметом дискуссий.
АД является чрезвычайно распространенным и зачастую тяжело протекающим дерматозом. Его частота в структуре кожных заболеваний, по разным данным, составляет от 20 до 40%. Результаты эпидемиологических исследований показывают, что АД чаще встречается среди молодых людей, чем среди взрослых. Болеют оба пола, несколько чаще женщины. АД возникает у людей всего мира и у всех рас. В течение последних десятилетий распространенность заболевания значительно увеличилась. Например, в Дании общая заболеваемость близнецов в возрасте до 7 лет, рожденных с 1960 по 1964 гг., составляла 3%. А у близнецов, рожденных с 1970 по 1974 гг., этот показатель уже увеличился до 10% [44].
Возникновение и хроническое течение АД обусловливают наследственная предрасположенность, функциональные нарушения нервной системы, влияние неблагоприятных условий окружающей среды, психоэмоциональные расстройства и патология внутренних органов, обменные, нейрогуморальные, нейрососудистые нарушения, аллергические заболевания, нерациональное питание, различные интоксикации [14].
Клинические проявления АД разнообразны, однако достаточно типичны и хорошо изучены. Заболевание обычно начинается в раннем детском возрасте, чаще во втором полугодии жизни. Может продолжаться долгие годы, характеризуясь ремиссиями, в основном в летний, и рецидивами в весенне-осенний периоды года. Со временем острота заболевания ослабевает, и в возрасте 30–40 лет у большинства больных наступает спонтанное излечение. В течении заболевания выделяют три фазы: младенческую (обычно с 7–8 недели жизни до 3 лет), детскую (с 3 до 7 лет) и взрослую. В младенческой и детской фазах чаще наблюдаются очаговые эритематозно-сквамозные высыпания со склонностью к экссудации (везикуляция, мокнутие) на коже лица, ягодицах, конечностях. Во взрослой фазе преобладают зудящие эритематозно-лихеноидные высыпания на сгибательных поверхностях конечностей, на шее с развитием лихенизации (кожа становится утолщенной, грубой на ощупь, кожный рисунок резко выражен). Степень выраженности и распространенности процесса может быть различной — от ограниченных (периоральных) высыпаний до обширного поражения кожного покрова по типу эритродермии. Непременный признак АД, независимо от фазы течения или клинического варианта, — интенсивный зуд, составляющий основу страданий больного, в значительной мере утяжеляющий течение заболевания и снижающий качество жизни [6, 15, 42].
В соответствии с клинической классификацией Сергеева Ю. В. [14], выделяют пять форм АД: лихеноидная, эритематозно-сквамозная, пруригинозная форма, экзематозная, атипичная.
Диагноз АД основывается на комплексе диагностических признаков АД, который получил название критериев Hanifin а. Rajka, 1980 (табл. 1) [37]. Диагноз АД требует наличия по крайней мере трех из четырех главных критериев и трех малых критериев.
Для объективной оценки степени тяжести и распространенности кожного процесса и выраженности зуда при АД группой исследователей Европейского центра по изучению АД была разработана унифицированная шкала симптомов (SCORAD), представляющая собой многопараметровую балльную оценку степени тяжести АД, которая может быть использована в качестве наиболее объективного («золотого») стандарта при научных исследованиях и в клинической практике [32].
Как заболевание, обострения которого могут быть спровоцированы психогенно, АД был отнесен к классическим психосоматическим заболеваниям Францем Александером в 1950 году [21]. С тех пор было проведено большое количество отечественных [3, 4, 5, 8, 9, 10, 11, 12, 13, 18] и зарубежных [19, 20, 37, 22, 23, 28, 30, 33] исследований, посвященных изучению роли психогенных воздействий как провоцирующих обострения АД факторов, а также психических расстройств у больных АД. На модели АД представляется возможным изучение психических расстройств, развивающихся у пациентов с хроническими зудящими дерматозами. Считается, что локализация высыпаний на видимых участках кожного покрова и выраженный зуд приводят не только к снижению качества жизни, но и к развитию патологических психических реакций на болезнь, значительно влияющих на комплаентность пациента в процессе терапии и дополнительно утяжеляющих состояние больных.
Согласно проведенным исследованиям, АД нередко обостряется после психогенных воздействий и зачастую сопровождается психическими нарушениями [24, 25, 26, 27, 34, 35, 38, 39]. Так, ассоциация АД и депрессивных расстройств установлена в исследованиях коморбидности обсуждаемого дерматоза и аффективной патологии. Согласно когортному исследованию, проведенному Timonen М., у 30% больных АД отмечаются эпизоды депрессии в течение жизни [45], что значительно превышает этот показатель в общей популяции (от 5% до 10%) [43]. В исследованиях других авторов депрессии выявлялись у 23–80% пациентов с АД [1, 5, 11, 12, 13, 18]. Коморбидность тревожных расстройств и АД отмечалась почти у половины исследованных больных [4, 46]. Приводятся данные о том, что психологический профиль «атопика» характеризуется депрессией, напряженностью, тревогой и агрессивностью [25, 28, 33]. При этом частое развитие психических расстройств объясняется, как правило, характером кожного заболевания (хроническое течение, интенсивный, в том числе ночной, зуд и локализация высыпаний на видимых участках кожного покрова).
Однако проведенные психосоматические исследования больных АД в большинстве своем основываются либо на использовании формализованных психометрических методик диагностики, либо психологического консультирования и не позволяют оценить долю истинно нозогенных психических девиаций и долю расстройств, развившихся вне зависимости от АД.
В последние годы была создана систематика психодерматологических расстройств (табл. 2). Согласно этой классификации АД относится, с одной стороны, к группе психосоматических болезней, с другой стороны, как хронический дерматоз может быть причиной развития нозогенных реакций и патологических развитий. Однако исследований особенностей психических расстройств при АД с этих позиций не проводилось.
Целью настоящего исследования явилось комплексное клиническое изучение психических расстройств при АД и их связи с особенностями клиники и течения заболевания кожи, направленное на разработку их типологической дифференциации.
Материал и методы исследования
Материал исследования составили 97 пациентов (73 женщины и 23 мужчины; средний возраст 26,9 ± 10,2 года).
Критерии включения: верифицированный диагноз АД согласно международным диагностическим критериям J. M. Hanifin и G. Rajka [37], возраст пациентов от 18 до 65 лет.
Критерии исключения: манифестный шизофренический/шизоаффективний/аффективный психоз, органическое поражение ЦНС, деменция, зависимость от психоактивных веществ, другие тяжелые соматические заболевания в стадии обострения или декомпенсации.
Исследование проведено клиническим методом, предусматривающим комплексное дерматологическое и психопатологическое обследование. Дерматологическое обследование предусматривало анализ анамнестических и клинических показателей, подтверждение диагноза АД. Степень тяжести и распространенность кожного процесса у всех пациентов оценивались при помощи индекса SCORAD (метод, рекомендованный Европейской рабочей группой по АД [32], учитывающий распространенность высыпаний, характер сыпи (эритема, отек, мокнутие, экскориации, лихенификация, сухость) и выраженность субъективных симптомов — зуд, обусловленная АД бессонница.
Психопатологическое обследование проводилось сотрудниками отдела по изучению пограничной психической патологии и психосоматических расстройств (руководитель — академик РАМН А. Б. Смулевич) НЦПЗ РАМН, кафедры психиатрии и психосоматики ФППОВ ММА им. И. М. Сеченова, к. м. н. Дороженком И. Ю., к. м. н. М. А. Терентьевой, к. м. н. В. И. Фроловой, К. А. Батуриным. Экспериментально-психологическое обследование проводилось О. В. Петуховой, Д. А. Бесковой, Л. Т. Козловской. Окончательная квалификация психопатологических расстройств проводилась академиком РАМН А. Б. Смулевичем в рамках клинических разборов, на которые были представлены все пациенты.
Для характеристики кожного поражения в виде папулезно-везикуальных высыпаний, гиперемии, инфильтрации, сухости, шелушения, лихенификации чаще используются термины «атопический дерматит» и «нейродермит». По клиническому течению атопический дермат
 |
Диффузный атопический дерматит отличается от ограниченного более распространенным процессом. Иногда процесс принимает генерализованный характер. Наряду с нерезко ограниченными буровато-красными участками инфильтрированной и лихенизированной кожи, которые могут охватывать обширные поверхности, отмечаются отдельные плоские блестящие узелки, множественные экскориации. Кожа больных диффузным атопическим дерматитом отличается сухостью. У некоторых больных наблюдается везикуляция и мокнутие. При этом в клинической картине заболевания преобладают, наряду с инфильтрацией и лихенизацией, отечность кожи, папулы, везикулы, эрозии и эритема островоспалительного характера. Больных беспокоит непрекращающийся зуд. На участках разрешившихся высыпаний остается временная гиперпигментация кожи. При диффузном атопическом дерматите отмечается хронически рецидивирующее течение с частыми и длительными обострениями. Очень часто у больных атопическим дерматитом наблюдаются респираторные проявления атопии: бронхиальная астма, риноконъюнктивит.
| Наряду с атопическим дерматитом, или нейродермитом, который хорошо известен дерматологам, встречается тяжелый, генерализованный атопический дерматит, который протекает с постоянными явлениями экзематизации и пиодермии. Для него характерно сочетание с атопическими заболеваниями респираторного тракта в виде аллергических риносинуситов, конъюнктивитов и атопической бронхиальной астмы. Тяжелое течение заболевания нередко приводит к инвалидности. Лечение этих больных представляется крайне затруднительным, что обусловлено часто встречающейся лекарственной непереносимостью |
Одна из особенностей течения атопического дерматита — гнойная кожная инфекция, проявляющаяся в виде пиодермии, для которой характерны мелкие пустулезные высыпания, носящие поверхностный характер. Типичным для этих больных является герпес симплекс, который может локализоваться на коже лица, рук, ягодиц, на слизистых оболочках и способен мигрировать на новые участки. Предрасположенность больных атопическим дерматитом к стафилодермии, герпетической инфекции считается клиническим признаком недостаточности иммунитета. Конъюнктивит при атопическом дерматите иногда носит сезонный характер и является проявлением поллиноза, хотя в большинстве случаев он наблюдается круглогодично. При посеве содержимого с конъюнктивы часто идентифицируется золотистый стафилококк.
Таким образом, можно выделить синдром, который характеризуется сочетанием тяжелого генерализованного атопического дерматита с чередованием распространенной экзематизации и пиодермии и респираторных проявлений атопии. При этом отмечается чрезвычайно высокий уровень IgE, сенсибилизация почти ко всем атопическим аллергенам. Сочетание аллергических IgE опосредованных реакций и иммунодефицита, клинически проявляющегося в рецидивирующей пиодермии, герпетической инфекции и подтвержденного результатами иммунологического исследования, является одним из патогенетических механизмов развития этого синдрома. Особая тяжесть заболевания, молодой возраст больных, неэффективность традиционных методов терапии позволили выделить это заболевание и назвать его тяжелым атопическим синдромом (Ю. А. Порошина, Е. С. Феденко, В. Д. Прокопенко, 1985 год).
К сожалению, традиционные методы терапии недостаточно эффективны при лечении тяжелого атопического синдрома. Глюкокортикостероиды, обладающие выраженным противовоспалительным, антиаллергическим действием, нередко приводят к стероидозависимости и вызывают ряд тяжелых осложнений в виде обострений очагов инфекции и пиодермии. Обострение пиодермии вызывает необходимость антибактериальной терапии, которая, как правило, обостряет атопический дерматит или осложняется в связи с наличием у больного лекарственной непереносимости. В связи с неэффективностью традиционной терапии в Институте иммунологии МЗ РФ разработаны и проводятся методы экстракорпоральной иммунофармакотерапии (ЭИФТ, плазмоцитоферез с диуцифероном, преднизолоном и др. препаратами).
За период 1995–1997 гг. в Клинике неврозов обследовано 2686 больных, обратившихся к аллергологу по поводу различных зудящих высыпаний на коже. Из них у 612 был выявлен атопический дерматит (205 мужчин и 405 женщин в возрасте от 16 до 35 лет, средний возраст — 22–25 лет).
Ограниченный атопический дерматит наблюдался у 319 пациентов, распространенный – у 205, а у 88 был выявлен тяжелый атопический синдром. Диагноз ставился на основании клинического, аллергологического и иммунологического обследования.
Всем больным проводилось общеклиническое, в том числе функциональное, лабораторное инструментальное обследование, консультации специалистов (ЛОР, гастроэнтеролог, окулист и др.).
Кроме тщательно собранного аллергологического, фармакологического и пищевого анамнеза по специально разработанной схеме, аллергологическое обследование производилось со стандартными отечественными наборами бытовых, пыльцевых, эпидермальных и пищевых аллергенов и включало кожные тесты — уколом или скарификационные (у больных с выраженным поражением кожи в области предплечий тесты выполнялись на спине), провокационные назальные и конъюнктивальные тесты, а также тест торможения естественной эмиграцией лейкоцитов (ТТЕЭЛ) in vivo по Адо А. Д. с медикаментами.
Иммунологическое обследование предусматривало определение общего и специфических IgE в сыворотке крови и исследование показателей первичного иммунного статуса: количества лейкоцитов, лимфоцитов, Т- и В-лимфоцитов, Т-хелперов и Т-супрессоров, иммуноглобулинов класса А, М, G, а также нейтрофильного фагоцитоза.
Клинически кожные проявления характеризовались наличием папулезно-везикулярных высыпаний, местами с геморрагическими корочками на поверхности, выраженной сухостью, распространенной эритемой, лихинизацией. В локтевых сгибах и подколенных областях отмечались очаги яркой гиперемии, отечности и экcсудации. Субъективно беспокоил мучительный зуд. У 28 из 88 больных тяжелым атопическим синдромом наблюдалась пиодермия – поверхностные пустулы с гнойным отделяемым. Пиодермия носила распространенный характер у 9 больных, ограниченный у 19, сочеталась с фурункулезом у 5 больных. 82 человека страдали рецидивирующим герпес симплекс.
Таблица 1. Респираторные проявления атопии у 365 больных атопическим дерматитом
Кроме проявлений атопического дерматита и пиодермии, у многих пациентов (365) имелись респираторные проявления атопии, которые представлены в таблице 1.
Большинство больных (427) страдали сопутствующими заболеваниями желудочно-кишечного тракта (хронический гастрит, язвенная болезнь желудка и 12-перстной кишки, дискинезия желчных путей и толстой кишки, дисбактериоз кишечника и др.).
У 362 пациентов выявлена патология ЛОР-органов (хронический гайморит, полипозный этмоидит, хронический тонзиллит, хронический субатрофический фарингит).
Как видно из таблицы 1, у значительного числа больных (41%) атопическим дерматитом был выявлен поллиноз. У половины пациентов (49,1%) отмечались респираторные проявления бытовой аллергии.
При аллергологическом обследовании 612 человек, страдающих атопическим дерматитом, у 428 пациентов была выявлена сенсибилизация к небактериальным аллергенам. В таблице 2 представлены результаты аллергологического обследования этих пациентов по данным кожных (prick и скарификационных), назальных и конъюнктивальных тестов, а также по определению специфических IgE в сыворотке крови.
Как видно из таблицы 2, наибольшее число положительных тестов было получено с бытовыми и пыльцевыми аллергенами, что, как говорилось выше, обусловлено наличием не только кожных, но и респираторных проявлений атопии.
Таблица 2. Результаты аллергологического обследования 428 больных атопическим дерматитом
105 больным, у которых в анамнезе имелись указания на медикаментозную непереносимость, проводился ТТЕЭЛ с лекарственными средствами. У 38 человек он оказался положительным.
Клиническое течение распространенного атопического дерматита и тяжелого атопического синдрома с рецидивами пиодермии и герпеса при наличии хронических очагов инфекции (хронический гайморо-этмоидит, хронический тонзиллит, дисбактериоз кишечника и пр.) позволило предположить, что у этой категории больных имеется сочетание аллергии и иммунодефицита. При иммунологическом обследовании были выявлены следующие изменения гуморального и клеточного иммунитета: снижение количества лимфоцитов периферической крови за счет уменьшения популяций Т-клеток, снижение нейтрофильного фагоцитоза. Отмечено увеличение продукции иммуноглобулинов класса А, М, и особенно IgE. У всех обследованных больных было зафиксировано значительное повышение уровня общего IgE, иногда в 10–30 раз по сравнению с уровнем у здоровых людей.
Наряду с термином атопический дерматит, отражающим аллергическую природу данного заболевания, по-прежнему широко используется (особенно дерматологами) более старое определение – нейродермит. Такое название было дано недаром, так как практически у всех больных обострение кожного процесса вызывается эмоционально-стрессовыми факторами, психотравмирующей ситуацией. В свою очередь, постоянный зуд, беспокоящий больного, вызывает раздражительность, вспыльчивость, приводит к бессоннице.
Пример
Больная Ч. 1972 года рождения находилась в клинике на лечении с 18.02.93 по 29.04.93 по поводу невротической депрессии, выраженного астено-депрессивного синдрома.
Сопутствующий диагноз: атопический дерматит, распространенная форма в стадии обострения (при выписке ремиссия). Поллиноз. Аллергический риноконъюнктивит. Сенсибилизация к пыльце деревьев. Пищевая аллергия к орехам, яблокам, моркови. Хронический гастрит со сниженной секреторной функцией. Дискинезия толстой кишки.
Жалобы на постоянный зуд кожи, высыпания, раздражительность, вспыльчивость, плаксивость, нарушение сна, головные боли, повышенную утомляемость, снижение настроения.
Из анамнеза: бабушка страдала экземой. У тети бронхиальная астма. Родилась первым ребенком, в срок. Со слов матери, беременность и роды протекали без осложнений. С пяти месяцев находилась на искусственном вскармливании – почти сразу появилась детская экзема. В пять лет диагностирован нейродермит. Наблюдалась дерматологами. Были длительные периоды относительного благополучия, когда оставался ограниченный дерматит (в области локтевых суставов, кистей). Летом всегда улучшение, обострение в сентябре—октябре. С 1992 года в мае появились явления ринита. Отмечалось обострение дерматита после употребления в пищу орехов, шоколада, яиц, цитрусовых. В августе 1993 года отек Квинке после употребления яблок, после этого яблоки не ела. С детства отмечено резкое обострение дерматита на фоне стрессовых ситуаций. Последнее ухудшение около года на фоне психотравмирующей ситуации в семье (развод с мужем). Распространились кожные высыпания, беспокоит постоянный зуд, из-за этого нарушился сон. За год похудела на 7 кг. Принимала супрастин и димедромл с незначительным эффектом. Местное лечение, назначенное дерматологом (названия мазей больная не знает), давало только кратковременное улучшение.
При поступлении: общее состояние удовлетворительное. Кожа сухая, на фоне участков гиперемии множественные расчесы, мелкопапулезные, везикулярные рассеянные высыпания, корочки. В области шеи, локтевых суставов, запястий выраженная лихенификация. Отеков нет. Явлений ринита, конъюнктивита нет. Слизистая полости рта и зева не изменена. В легких везикулярное дыхание, хрипов нет. Тоны сердца ясные, ритмичные, АД – 110/70. Пульс 88 в минуту, удовлетворительных свойств. Живот мягкий, безболезненный во всех отделах. Печень не увеличена. Дизурии нет. Стул не регулярный, склонность к запорам. Астенизирована. Настроение снижено. Фиксирована на своем состоянии и на психотравмирующей ситуации в семье.
Результаты клинико-лабораторного обследования: кл. ан. крови – HB-124, Л-5,0; п.1, с.46, э.12, л.36, м.5, соэ-8 мм/час. Биохим. ан. крови: общий белок 80,0; мочевина 4,4; креатинин 89,1, холестерин 6,1; бета-липопротеиды 6,1; билирубин общ. 14,8; АЛТ–0,25; АСТ-0,34; глюкоза 4,7; серомукоид 0,10. СРБ – отрицат., р-ция Вассермана отрицат.
Ан. мочи – без особенностей.
ЭКГ: без патологии.
Рентгенография ППН – прозрачность пазух не нарушена.
ЭГДС: гастрит, дуодено-гастральный рефлюкс.
Конс. ЛОР: здорова.
Конс. гинеколога: здорова
Конс. гастроэнтеролога: хронический гастрит со сниженной секреторной фукцией. Дискинезия толстой кишки.
Конс. невропатолога: вегето-сосудистая дисфункция по гипотоническому типу.
Иммунный статус: Л:5,0; Лф-36%, — 1,9; фагоцитоз 74%, Тлф-61%-1,1; Влф 5%-0,09; IgА 230, IgM 110, IgG 1400, IgG- общ. больше 1000.
Аллергологическое обследование: скарификационные тесты положительные с аллергенами из пыльцы березы +++, ольхи +++, орешника +++, дуба ++, ясеня ++, тополя +, с эпидермальными и бытовыми аллергенами – отрицательные. Сертификационные тесты с пищевыми пассивными аллергенами – орехи (грецкий, фундук, миндаль, арахис), морковь, яблоки (старкин, гольден) — положительные. Тестирование проводилось на спине.
Лечение: индивидуальная гипоаллергенная диета, в/в капельно дексона 8 мг на физ. р-ре, два дня; в/в кап. дексона 4 мг. На физ. р-ре – 3 дна, всего 28 мг; в/в кап. Аскорбиновая кислота 5,0 на физ. р-ре 5 дней; задитен 1 т. х 2 раза, фестал 1 т. х 3 раза во время еды, интал 2 кап. х 3 раза (растворенный в воде) за 20 мин. до еды, активированный уголь 1 т. х 3 раза через 1, 5 часа после еды; в/в кап. тавегил 2,0 на физ. р-ре – 2 дня, тавегил 2,0 в/м на ночь – 5 дней, ретаболил 1 т. на ночь, местная обработка кожи мазью целестодерм и мазью Унна, физиотерапия, (электросон, УФО), иглорефлексотерапия, комплексная психотерапия, лечебная релаксационная гимнастика, групповые и индивидуальные занятия с психологом. ГБО – 5 сеансов.
В результате проведенного лечения отмечена выраженная положительная динамика: высыпания на коже полностью исчезли, остается лихенификация в области локтевых сгибов и запястий, зуд почти не беспокоит. Нормализовался сон. Стала спокойнее, бодрее, активнее. Улучшилось настроение.
Что такое многоформная экссудативная эритема (МЭЭ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Фоминых Софьи Юрьевны, дерматолога со стажем в 23 года.
Над статьей доктора Фоминых Софьи Юрьевны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
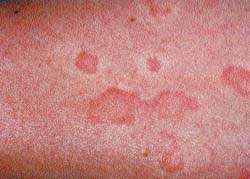
Многоформная экссудативная эритема (МЭЭ) — это острое аллергическое заболевание, при котором на коже и слизистых оболочках появляются различные по виду высыпания — пятнистые, папулёзные и пузырные.
МЭЭ обычно болеют люди молодого и среднего возраста. У пациентов мужского пола это заболевание встречается несколько чаще, чем у женщин.
Известны две основные разновидности МЭЭ:
- инфекционно-аллергическая (идиопатическая или истинная) — составляет около 80 % всех случаев МЭЭ и является следствием аллергической реакции на хронический очаг инфекции в организме;
- токсико-аллергическая — развивается, как правило, на фоне применения некоторых лекарственных средств, таких как амидопирин, барбитураты, сульфаниламиды и тетрациклины [7] .
Для инфекционно-аллергической МЭЭ характерна весенне-осенняя сезонность. Одного очага хронической инфекции недостаточно, чтобы данное заболевание развилось или обострилось. Для этого необходимо определённое сочетание триггерных, т. е. провоцирующих факторов, например:
- иммунодефицит (обратимый, преходящий, циклический);
- переохлаждение;
- ультрафиолетовое облучение;
- некоторые консерванты в составе пищевых продуктов (бензоаты, формальдегид и т. д.);
- психоэмоциональный стресс;
- патология пищеварительного тракта (хронический гастрит, дисбактериоз);
- аутоиммунные заболевания и онкопатология; , ангина и другие заболевания.
Не исключается и наличие наследственной предрасположенности к ММЭ.
Причиной инфекционно-аллергической МЭЭ, которая приводит к развитию болезни, чаще всего является герпесвирус человека, вирус Эпштейна — Барр, цитомегаловирус, а также возбудители вирусных гепатитов, микобактерии, микоплазменная, стрептококковая и грибковые инфекции, паразиты. Наиболее распространённый вид инфекционно-аллергической МЭЭ — герпес-ассоциированная МЭЭ [4] [12] [13] .
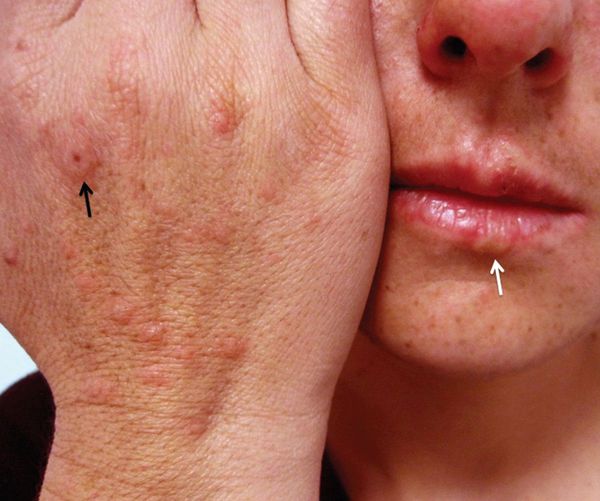
Считается, что герпесвирусная инфекция [1] [2] [5] становится причиной подавляющего большинства случаев МЭЭ. Чаще всего обнаруживается связь с вирусом простого герпеса первого типа [8] [10] [11] , реже — второго.
В пользу инфекционно-аллергической формы МЭЭ свидетельствует наличие продромального периода (предшествующего болезни), склонности к сезонности высыпаний и хроническое рецидивирующее течение.
Эксперты ВОЗ отмечают, что рост заболеваемости простым герпесом в настоящий момент заставляет рассматривать его в числе первоочередных проблем, наряду с ВИЧ-инфекцией и гриппом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы многоформной экссудативной эритемы
Для инфекционно-аллергической МЭЭ, включая герпес-ассоциированную [13] , характерно острое начало заболевания. Оно может проявляться повышением температуры, общей слабостью, ломотой в теле, головной болью, болезненными ощущениями в горле и другими симптомами.
Нередко за несколько дней до обострения МЭЭ у пациентов активируется герпетическая инфекция — проявляется герпес на губах или возникает рецидив генитального герпеса [8] .
Высыпания, характерные для МЭЭ, обычно начинают появляться через 1-2 дня после начала продромальных явлений. При этом общие симптомы обычно идут на спад.
Локализация сыпи весьма разнообразна. Она может появиться как на коже, так и на слизистых оболочках.
Кожные проявления
На коже обычно отмечаются чётко очерченные округлые красно-розовые пятна и плоские отёчные папулы, которые увеличиваются в размерах от 2-3 мм до 3 см в диаметре. При инфекционно-аллергической форме пятна обычно несколько мельче и не склонны к слиянию. Они могут доставлять зуд и жжение.
Преимущественная локализация высыпаний — на разгибательной стороне рук и ног, тыльной стороне стоп и кистей, на лице и в области гениталий. В основном они располагаются на теле симметрично, часто группами в виде дуг, гирлянд.
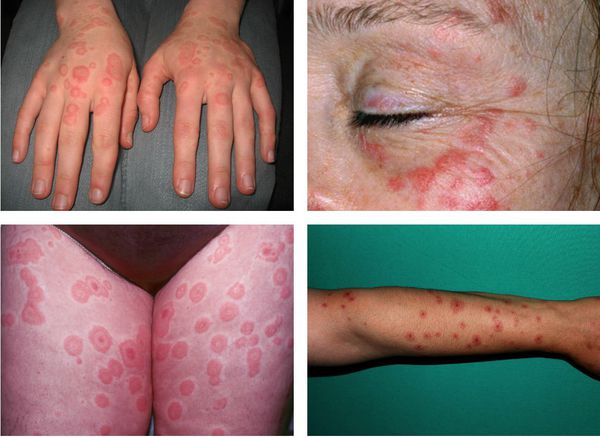
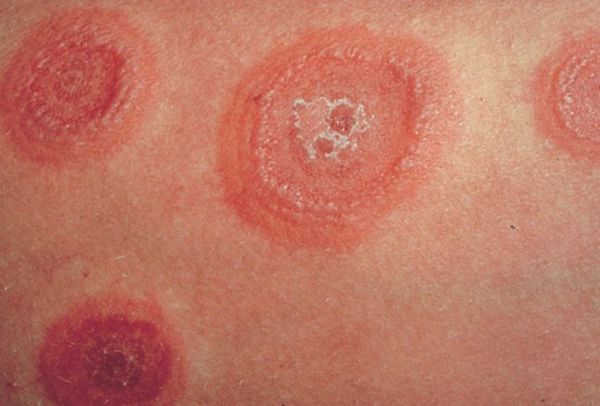
По мере роста папулы её центр начинает западать и менять окраску на более синюшную, по периферии остаётся красно-розовый ободок — таким образом элементы сыпи приобретают характерный вид "мишени" (иногда их сравнивают с "бычьим глазом" или "кокардой") [4] .
После в их центре образуются пузыри — везикулы и буллёзные элементы. Они содержат серозный или кровянистый экссудат. Лопаясь, пузыри формируют желтоватые или коричнево-бурые корочки, эрозированные поверхности.
В итоге на теле пациента одновременно присутствуют элементы разной степени развития — пятна, папулы и пузыри, переходящие в корочки и эрозии. Именно поэтому эритема именуется многоформной.
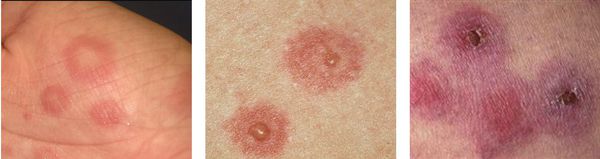
С интервалами в несколько дней могут образовываться новые группы высыпаний. Это может затянуть процесс. Но обычно окончательный регресс наступает приблизительно в течение двух недель.
Частота обострений может варьировать от 1-2 до 5-12 раз в год. В редких тяжёлых случаях одно обострение может переходить в другое, практически без светлого промежутка. За это время предыдущие высыпания полностью не разрешаются.
Высыпания на слизистых оболочках
Могут появляться единичные элементы на слизистой полости рта, который не причиняют особого беспокойства. В более тяжёлых случаях поражения бывают настолько обширными и болезненными. Они затрудняют речь и приём даже однородной и жидкой пищи [12] [13] .
Образующиеся пузыри лопаются довольно быстро, поэтому пациент не успевает их заметить — обычно обнаруживаются уже эрозии, на которых иногда можно увидеть плёнчатые фибринозные налёты светлого или бурого оттенка.
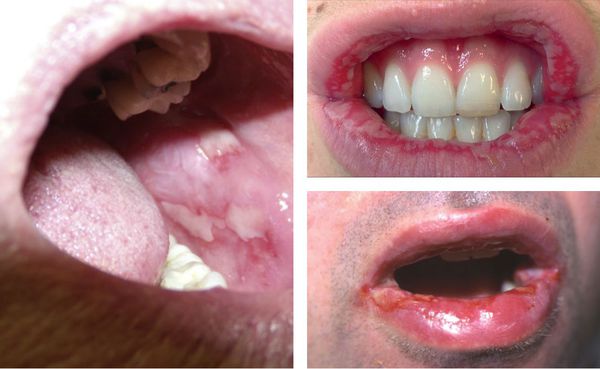
В области красной каймы губ могут возникнуть весьма болезненные, растрескивающиеся кровянистые корки, которые не позволяют больному полноценно открывать рот.
Реже высыпания обнаруживаются на слизистых глаз и половых органов. В осложнённых случаях возможно присоединение вторичной инфекции, образование рубцов и синехий (спаек).
Патогенез многоформной экссудативной эритемы
На современном этапе любая разновидность мультиформной экссудативной эритемы рассматривается как сдвиг адаптации защитных механизмов в сторону гиперчувствительности [4] .
МЭЭ — это смешанная аллергическая реакция, в которой просматриваются особенности, характерные для гиперчувствительности как немедленного, так и замедленного типа. Зачастую у пациента явно прослеживается так называемая общая атопическая предрасположенность — исходно у него могут отмечаться, к примеру, признаки пищевой аллергии, атопический ринит, бронхиальная астма и дерматит.
При герпес-ассоциированной МЭЭ у пациентов резко повышается уровень иммуноглобулинов класса Е (IgE) и снижается продукция иммуноглобулинов класса А (IgA), которые обеспечивают "первую линию" защиты кожи и слизистых оболочек. Также отмечается понижение выработки альфа- и гамма-интерферона и образование циркулирующих иммунных комплексов с вирусом простого герпеса.
Вирус повреждает генетический аппарат не только клеток эпидермиса, но и иммунокомпетентных клеток, изменяет состояние их рецепторов, выработку специфических ферментов и провоспалительных цитокинов. В то же время может наблюдаться Т-клеточный и нейтрофильный иммунодефицит, повышение количества В-лимфоцитов. Всё это нарушает связь между различными звеньями иммунитета, искажает нормальный иммунный ответ, заставляет организм проявлять агрессию к собственным тканям, в данном случае — к клеткам эпидермиса и эндотелия сосудов кожи.
Всё вышеперечисленное приводит к образованию лимфоцитарного инфильтрата вокруг кровеносных сосудов кожи, иногда с признаками геморрагии. В базальном слое эпидермиса развивается внутри- и внеклеточный отёк. Сам слой расслаивается, в нём возникают некротические изменения с образованием толстостенных булл.
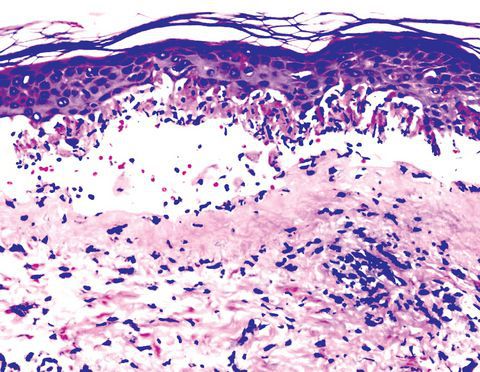
Степень тяжести патологических проявлений при герпес-ассоциированной МЭЭ во многом зависит от выраженности имеющихся иммунных сдвигов, которые, в свою очередь, могут являться причиной наличия хронического инфекционного очага в организме.
Классификация и стадии развития многоформной экссудативной эритемы
В зависимости от степени выраженности симптомов [3] [12] выделяют две формы МЭЭ:
- малая — поражений слизистых нет или они очень слабо выражены, почти нет общих симптомов;
- большая — протекает с тяжёлым поражением слизистых оболочек, ярко выраженными общими симптомами.
По первичным элементам сыпи, преобладающим в клинической картине МЭЭ, различают пять форм заболевания:
- эритематозная — ограниченное покраснение кожи;
- папулёзная — появление красноватых плотных узелков;
- эритематозно-папулёзная — образование папул с ярко-красными краями и потемневшим центом;
- везикуло-буллёзная — формирование эритематозных бляшек с пузырьком в центре;
- буллёзная — превращение пузырьков в эрозии, которые покрываются корочками.
Воспалительный процесс в зависимости от гистопатологической картины поражения кожи разделяют на три типа [3] :
- эпидермальное воспаление — нарушается наружный слой кожи;
- дермальное воспаление — изменяется толстый слой кожи под эпидермисом;
- смешанное (эпидермо-дермальное) воспаление.
По степени тяжести МЭЭ может быть лёгкой, средней, среднетяжёлой и тяжёлой. В качестве критериев тяжести рассматривают количество и размер буллёзных элементов, наличие поражений слизистых оболочек полости рта и гениталий, температуру тела. Отдельно выделяют часто рецидивирующую форму.
Общепринятой классификации герпес-ассоциированной МЭЭ в настоящее время не существует. В её развитии, как и в развитии МЭЭ, различают два периода:
- продромальный — период активации вирусного процесса;
- буллёзный — период разгара заболевания.
Осложнения многоформной экссудативной эритемы
Осложнения чаще всего развиваются при тяжёлых формах заболевания, а также у людей, организм которых по различным причинам ослаблен [12] [13] .
При обширных поражениях слизистой полости рта резкая болезненность высыпаний затрудняет нормальный гигиенический уход. Когда во рту изначально присутствовали очаги инфекции, возможно развитие такого осложнения, как фузоспирохетоз. Это стоматологическое заболевание характеризуется образованием толстого желтоватого дурно пахнущего налёта на слизистой полости рта, языке и зубах.
Затруднённый приём пищи при генерализованном поражении слизистой полости рта может приводить к истощению пациента.
При локализации высыпаний на слизистой носа возможно развитие ринита с носовыми кровотечениями.
Эрозии на слизистой половых органов могут заживать с образованием синехий (спаек, сращений).
В 22% случаев через эрозивные дефекты покровов проникает вторичная бактериальная инфекция. Это чревато гнойно-септическими осложнениями, образованием более глубоких поражений, на месте которых в редких случаях могут образовываться рубцы.
Поражение слизистой оболочки глаз может осложняться конъюнктивитом и кератитом (кератоконъюнктивитом) [3] .
К числу редких и наиболее серьёзных осложнений можно также отнести постгерпетическую невралгию, пневмонию, почечную недостаточность.
Диагностика многоформной экссудативной эритемы
Для постановки диагноза "МЭЭ" в типичном случае врачу-дерматологу достаточно характерной клинической картины и данных опроса пациента. Имеют значение сведения о хронических очагах инфекции, недавних рецидивах герпетических высыпаний и провоцирующих факторах.
Лабораторные анализы (например, общий анализ крови) в нетяжёлых случаях могут не показать никаких отклонений. При тяжёлых формах отмечается повышение СОЭ и умеренный лейкоцитоз — небольшое повышение уровня лимфоцитов в крови.
Для уточнения диагноза нужно исключить другие, схожие по симптоматике заболевания — пузырчатку, узловатую эритему, системную красную волчанку, вторичный сифилис и другие. С этой целью выполняют цитологическое исследование мазков-отпечатков, взятых с поверхности высыпаний, а также изучение клеток поражённой ткани под микроскопом.
Наличие герпетической инфекции в организме при необходимости можно подтвердить несколькими способами:
- ПЦР-диагностика на инфекции, передающиеся половым путём;
- серологическое обследование на наличие антител к вирусу простого герпеса;
- оценка иммунного статуса.
Дифференциальную диагностику герпес-ассоциированной МЭЭ необходимо проводить с узловатой и кольцевидной эритемой Дарье, токсидермиями, вторичным сифилисом, системной красной волчанкой, герпетическим стоматитом, болезнью Кавасаки, уртикарным васкулитом, красным плоским лишаем (эрозивной формой).
Лечение многоформной экссудативной эритемы
Основные задачи лечения:
- уменьшить тяжесть общих проявлений и количество высыпаний во время обострений;
- сократить длительность рецидивов;
- предотвратить осложнения;
- в межрецидивный период повысить сопротивляемость организма, сократить частоту рецидивов.
При любой форме МЭЭ используют десенсибилизирующую терапию и антигистаминные (противоаллергические) препараты.
При поражении слизистых оболочек рта и половых органов назначаются орошения и полоскания составами, успокаивающими воспаление и подавляющими инфекцию — "Ротокан", настой ромашки и т. п.
Ускорить очищение эрозий от налётов и некротических тканей помогают местные ферментные препараты. Также применяются кератопластические средства и препараты, способствующие регенерации и ускорению эпителизации повреждений.
Показаниями для госпитализации может послужить тяжёлое течение заболевания, а также неэффективность амбулаторного лечения. В нетяжёлых случаях вполне допустимо лечение в домашних условиях, без особых ограничений.
Изоляции больного не требуется, так как он не представляет опасности для здоровья окружающих. Пациенту рекомендуется гипоаллергенная диета, химически и термически щадящая, гомогенная пища (особенно при высыпаниях на слизистой рта), пить достаточное количество воды.
Лечение герпес-ассоциированной МЭЭ
Тактика лечения при герпес-ассоциированной МЭЭ зависит от степени выраженности тех или иных симптомов, стадии развития процесса, частоты и тяжести обострений [3] [4] . Например, если рецидивы возникают часто, высыпания обильны и им характерны некротические изменения, то нередко применяются глюкокортикоиды [14] .
Когда в возникновении заболевания очевидна роль герпесвируса, показан приём синтетических ациклических нуклеозидов — ацикловир, валацикловир [14] , фамцикловир.
В случае торпидного (вялого) течения герпес-ассоциированной МЭЭ рекомендовано профилактическое, противорецидивное и превентивное (предупреждающее) лечение. Для этого длительными курсами применяют препараты, содержащие ацикловир.
Применение антибиотиков в лечении герпес-ассоциированной МЭЭ оправдано лишь при наличии признаков вторичной бактериальной инфекции — нарастание интоксикации и появление гнойного отделяемого.
Чтобы предупредить присоединение вторичной инфекции, эрозированные участки и пузыри обрабатывают растворами антисептиков, например, фукорцином, фурацилином или хлоргексидином.
Прогноз. Профилактика
В большинстве случаев МЭЭ прогноз для жизни и здоровья благоприятный, за исключением редких особо тяжёлых форм болезни у людей с пониженной резистентностью организма.
Рубцы при заживлении повреждений не образуются, за редким исключением. Иногда на месте бывших элементов сыпи изменяется окрас кожи.
Рецидивировать МЭЭ может приблизительно в 30 % случаев. Особое внимание следует уделять тяжёлым поражениям слизистой оболочки и бактериальной суперинфекции [15] .
В качестве первичной профилактики рекомендуется минимизировать риск заражения герпетической инфекцией:
- соблюдать нормы личной гигиены;
- избегать случайных половых связей;
- практиковать защищённый секс.
Чтобы сохранить сопротивляемость организма инфекциям в норме, нужно рационально питаться, соблюдать оптимальный режим труда и отдыха, полноценно спать, регулярно закаляться, отказаться от вредных пристрастий.
Меры неспецифической вторичной профилактики формируются с учётом возможных триггерных факторов. Целесообразно обратить внимание на следующие моменты:
- регулярное прохождение профилактических осмотров и своевременная санация (очищение) хронических очагов инфекции, при ассоциации с герпесвирусной инфекцией — противовирусная терапия;
- защита от избыточного облучения солнечным светом и ультрафиолетового облучения;
- уменьшение вероятности переохлаждения;
- исключение стрессовых воздействий и т. п.
Для предупреждения рецидивов герпес-ассоциированной МЭЭ применяется герпетическая поливакцина, которая вводится по особой схеме. Её эффективность достигает более 70 %: она в 2-4 раза уменьшает частоту рецидивов.
Сокращению числа рецидивов также способствует длительный превентивный приём синтетических ациклических нуклеозидов, препаратов интерферона [6] , его индукторов и целого ряда неспецифических иммуномодуляторов [9] .
Читайте также:

