Эпителий фолликула при гипофункции щитовидной железы
Обновлено: 28.04.2024
Щитовидная железа. Развитие щитовидной железы. Строение щитовидной железы. Гормоны щитовидной железы.
Щитовидная железа вырабатывает тиреоидные гормоны тироксин и трийодтиронин, а также тирокальцитонин (кальцитонин).
Тироксин и трийодтиронин являются мощными стимуляторами окислительных процессов в клетках, причем трийодтиронин в 5-10 раз активнее тироксина. Эти гормоны усиливают обмен веществ, синтез белков, газообмен, обмен углеводов и жиров. Тиреоидные гормоны оказывают значительное влияние на развитие, рост и дифференцировку клеток и тканей. Они ускоряют развитие костной ткани. Особенно большое влияние гормоны щитовидной железы оказывают на гистогенез нервной ткани. При недостаточности щитовидной железы тормозится дифференцировка клеток и тканей головного мозга, нарушается психическое развитие человека.
Тиреоидные гормоны оказывают стимулирующее действие на регенерационные процессы в тканях. В состав тироксина и трийодтиронина в качестве обязательного ингредиента входит йод, поэтому поступление йода с питьевой водой и пищей в организм необходимо для нормальной деятельности щитовидной железы. Не содержащий йода третий гормон щитовидной железы — тирокальцитонин участвует в регуляции кальциевого и фосфорного обмена.
Развитие щитовидной железы.
Зачаток щитовидной железы появляется на 4-й неделе эмбриогенеза в виде выпячивания вентральной стенки глоточной кишки между 1-й и 2-й парами жаберных карманов. Выпячивание это превращается в эпителиальный тяж с утолщением на конце. Щитовидная железа вначале закладывается как экзокринная железа. Позднее проток, соединяющий железу с глоткой, редуцируется, и от этого протока остается лишь foramen cecum. Эпителиальный тяж раздваивается на конце. В течение 3-го месяца по ходу эпителиальных тяжей образуются перетяжки. В четкообразных сегментах этих тяжей появляются просветы. По мере углубления перетяжек эпителиальные тяжи распадаются на отдельные фолликулы и клеточные островки.
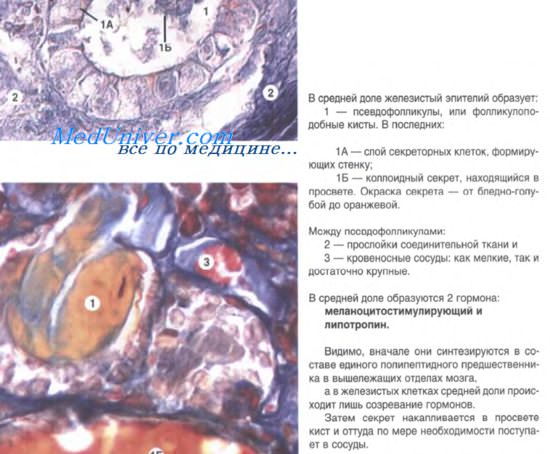
В конце 3-го месяца эпителий фолликулов дифференцируется. Клетки его — фолликулярные эндокриноциты (тироциты) — начинают вырабатывать гормоны, которые накапливаются в полости фолликула. Образование новых фолликулов и их развитие происходят гетерохронно. К моменту рождения отмечается наличие фолликулов с коллоидом ("коллоидный тип строения") и без коллоида с десквамацией эпителия ("десквамативный тип строения"). Между фолликулами встречаются межфолликулярные островки клеток. В процессе развития железы наряду с дифференцировкой эпителия происходит разрастание мезенхимы, преобразующейся в соединительную ткань. Формируется строма железы, содержащая густую сеть капилляров. В строму проникают нервные волокна.
В зачаток железы врастают также производные 5-й пары жаберных карманов — клетки так называемых ультимобранхиальных телец. Это С-клетки, вырабатывающие кальцитонин. Это клетки нейроэктодермальной природы, и в закладку щитовидной железы они внедряются через ультимобранхиальные зачатки.
Таким образом, в формировании структурно-функциональных единиц щитовидной железы участвуют следующие клеточные диффероны: это ведущие клетки эпителия фолликулов — фолликулярные эндокриноциты, вырабатывающие тироксин и трийодтиронин; кальцитониноциты, или С-клетки, продуцирующие кальцитонин и другие пептиды (соматостатин, тиролиберин, серотонин и др.).
Строение щитовидной железы.
Железа, состоящая из двух долей, снаружи покрыта соединительнотканной капсулой, от которой отходят перегородки, подразделяющие паренхиму на дольки. Структурно-функциональной единицей щитовидной железы является фолликул. Средний диаметр фолликулов около 50 мкм. Форма их преимущественно округлая. Фолликулы представляют собой замкнутые пузырьки. Стенка их образована однослойным эпителием, состоящим из фолликулярных эндокриноцитов (тироцитов). Среди этих клеток в виде небольших скоплений находятся С-клетки. Они могут быть и около фолликулов, и между фолликулами.
Полость фолликула заполнена продуктом секреции тироцитов — коллоидом, содержащим белки — тироглобулины. Снаружи фолликулы оплетают сети кровеносных и лимфатических капилляров. Между соседними фолликулами встречаются интерфолликулярные островки, состоящие из малодифференцированных эндокриноцитов.
Фолликулярные эндокриноциты имеют кубическую форму и округлое ядро. На апикальной поверхности их имеются микроворсинки. В цитоплазме хорошо развиты органеллы, обеспечивающие синтез белков. Много свободных рибосом, образующих полисомы. Соседние эндокриноциты в стенке фолликула соединяются при помощи плотных контактов, десмосом и интердигитаций.
Особенностью гистофизиологии щитовидной железы является различно направленное движение секреторных продуктов: вначале в полость фолликула, а затем в противоположном направлении — в кровь. Происходит это благодаря активной деятельности фолликулярных эндокриноцитов. Секреторный цикл этих клеток состоит из следующих фаз: поглощение исходных веществ, синтез секрета, выделение его в полость фолликула в виде коллоида, иодирование коллоида, эндоци-тоз иодированного коллоида и его модификация и выведение гормона через ба-зальную часть клетки в окружающие ткани и кровеносные и лимфатические капилляры. Выработка тиреоидных гормонов начинается с синтеза тиреоглобули-на в базальной части эндокриноцитов.
Содержащие тиреоглобулин продукты синтеза из эндоплазматической сети поступают в комплекс Гольджи и далее в виде секреторных гранул путем экзоцитоза выводятся в полость фолликула. К нейодированному тиреоглобулину присоединяется сначала один атом йода, а затем и второй, в результате чего образуются моно- и дийодтиронины. Последующая комплексация дает тетрайодтиронин, или тироксин. При отщеплении одного атома йода от тироксина образуется трийодтиронин.
В нормальных условиях процессы образования коллоида и его резорбции уравновешены. Это равновесие, однако, нарушается при гипо- и гиперфункции щитовидной железы. При гипофункции задерживается выведение гормона. При этом фолликулы обычно имеют большие размеры, в полости фолликула коллоида много, он густой, не имеет резорбционных вакуолей, эпителий представлен плоскими эндокриноцитами. При гиперфункции, наоборот, усиливается выведение гормона-коллоида в кровь. Коллоид разжижается, количество его невелико, эпителий стенки фолликула становится высоким призматическим.
Парафолликулярные эндокриноциты (С-клетки, или кальцитониноциты) вырабатывают белковый гормон кальцитонин. Он понижает уровень кальция в крови и является антагонистом паратирина. Кальцитонин действует на остеокласты костной ткани, уменьшая их резорбтивную активность. С-клетки — это более светлые и более крупные, чем фолликулярные эндокриноциты, и доля их составляет 0,1%. Обычно они лежат поодиночке или мелкими группами. В цитоплазме парафолликулярных эндокриноцитов много аргирофильных или осмиофильных секреторных гранул, содержащих кальцитонин и другие пептиды.
Строма железы состоит из рыхлой волокнистой соединительной ткани, в которой часто обнаруживаются тучные клетки, макрофаги, лимфоциты. Фибробласты щитовидной железы обладают рядом уникальных свойств, что определяется особенностями рецепторно-трансдукторной системы клеток. В частности, они могут участвовать в развитии воспаления наряду с иммунокомпетентными клетками. Хорошо развиты капилляры фенестрированного типа. Нервные волокна содержат пептиды, характерные для С-клеток.
Реактивность. Физиологическая регенерация щитовидной железы происходит путем обновления клеток эпителия фолликулов за счет их митоза. Источником развития новых фолликулов могут быть интерфолликулярные клеточные островки. Интоксикации, травмы, аутоиммунные процессы, наследственные факторы и др. могут приводить к тиреотоксикозу или к гипотиреозу. Следует иметь в виду, что для нормального функционирования щитовидной железы необходимо достаточное поступление в организм йода. Щитовидная железа обладает высокой способностью к регенерации после травм. Примером аутоиммунного заболевания щитовидной железы является болезнь Хашимото. Она возникает вследствие того, что тироглобулин проникает в строму щитовидной железы и, являясь антигеном, вызывает иммунную реакцию организма.
При этом сильно разрастается строма железы, она инфильтрируется лимфоцитами и плазмоцитами, а фолликулы щитовидной железы содержат мало коллоида и постепенно атрофируются.
Патологическая анатомия гипотиреоза. Морфология микседемы
Длительное и стойкое гипотиреоидное состояние организма может привести к микседеме.
S. Reichlin, J. Heyman, L. Lauriand, Z. Lewitus, И. Б. Хавин описали клинические случаи микседемы с выраженным отсутствием способности паренхимы щитовидной железы синтезировать активные тиреоидные гормоны из дийодтирозина.
Многие фолликулярные полости но имеют коллоида, соединительнотканная основа избыточно развита, часто уплотнена, местами фиброзирована и гиалинизирована. Склеротическим изменениям при этом заболевании подвергаются также стопки кровеносных сосудов. Щитовидная железа при гипотиреозе и микседеме чаще уменьшена, эластической, иногда плотноватой консистенции, бурого, серого или розового цвета. На разрезе по своей структуре этот орган напоминает диффузный, роже узловатый зоб.
При гипотиреозе, кроме симптомов, непосредственно обусловленных функциопальпой недостаточностью тиреоидной паренхимы, возникают патологические изменения как со стороны кожи, так и некоторых внутренних органов. К характерным патоморфологическим изменениям, обнаруживаемым при выраженных формах гипотиреоза и микседемы, в первую очередь относятся трофические поражения кожи и ее придатков. В основе этих нарушений лежит извращение местного углеводного обмена (накопление в различных участках кожи, а также в некоторых внутренних органах особого слизистого вещества белково-полисахаридного комплекса — муцина).
Указанные специфические изменения со стороны кожи и ее придатков при гипотиреозе и микседеме принято определять как кожный муцииоз (Г. Цондек, J. Gabrilove, A. Ludwig).
Муцин накапливается также в сердце, почках, поджелудочной железе, надпочечниках, а также вокруг кровеносных сосудов в периваскулярной соединительной ткани. Отложения муцина в щитовидной железе, мозгу, лимфатических узлах, печени и желчных путях не наблюдается. Муцин хорошо выявляется различными гистологическими красителями (муцикармином по Мейеру, а также тионином или толуидиновым синим по Гойеру).
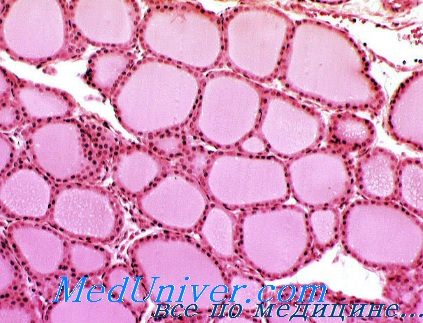
Среди специфических кожных изменений при гипотиреозах следует отметить наличие умеренного гиперкератоза, паракерато-за и акантоза эпидермиса. Расширяются мелкие кровеносные сосуды сосочкового слоя кожи, нарушается структура волосяных и сальных луковиц; волосы на голове становятся редкими и ломкими. Иногда возникает диффузная плешивость; волосы растут очень медленно, ногти при этом заболевании становятся толстыми и легко ломаются.
У больных микседемой нередко наблюдается ожирение, которое характеризуется равномерным распределением жира по всему телу, однако иногда в более выраженной степени он откладывается на тыльной стороне кистей, нижней части шеи и вокруг лодыжек.
Запущенные формы микседемы нередко сопровождаются различными нарушениями со стороны внутренних паренхиматозных органов: анацидным гастритом, атонией кишечника, функциональной недостаточностью печени и поджелудочной железы, а также желчнокаменной болезнью. При микседеме и гипотиреозе довольно часто поражается сердце, в частности миокард правого желудочка (при наличии дистрофических изменений и в других отделах этого органа). Чаще всего изменения в миокарде вызваны как накоплением в нем муцина, так и развивающимся атеросклеротическим кардиосклерозом с признаками расширения полостей сердца.
Указанные изменения, подтверждаемые обычно электрокардиографически или обнаруживаемые на секции, характеризуют этот орган как «микседематозное сердце».
Наконец, при микседеме происходят глубокие нарушения в некоторых органах эндокринной системы, проявляющиеся в первую очередь компенсаторной гипертрофией передней доли гипофиза (с появлепием в пей отчетливо вакуолизированных и резко гипертрофированных хромофобных клеток, так называемых клеток тиреоидэктомии).
В передней доле гипофиза при этом заболевании значительно увеличивается количество базофильных клеток и уменьшается число эозинофильных. В промежуточной доле мозгового придатка иногда накапливается коллоид, который, по мере увеличения его количества, проникает в заднюю долю. Иногда при микседеме и гипотиреозе наблюдаются стертые формы сахарного диабета, а также признаки вирилизации, гипоплазия лоловых и околощитовидных желез.
Препарат 26.
| Щитовидная железа. Окраска гематоксилин-эозином. |
(Нижеследующее описание основывается на материале раздела 22.3.1.)
А. Общее описание
гистологическое строение всех её долей одинаково.
это преобладающие структуры железы;
их стенку составляет один слой клеток на базальной мембране,
внутри фолликулов содержится гомогенный коллоид (2).

а) (Малое увеличение)
это компактные скопления клеток вне фолликулов.
паращитовидная железа (I) - одна или несколько.
Б. Эндокриноциты : два типа клеток
составляют большинство железистых клеток;
в фолликуле образуют всю внутреннюю поверхность его стенки;
продуцируют й одсодержащи е гормон ы ( тироксин и трийодтиронин).

их доля в общем числе железистых клеток невелика;
если они находятся в фолликуле, то
тоже (как и тироциты) прилегают к базальной мембране,
но не достигают своей апикальной частью просвета фолликула;образуют кальцитонин - гормон, понижающий содержание Са 2+ в крови .
В. Функционирование тироцитов
тироциты поглощают из крови аминокислоты и ионы иода ;
с их участием
вначале на рибосомах синтезируется белок тиреоглобулин ,
а затем происходит модификация этого белка (так, что в составе белка образуются тиреоидные гормоны);
такой модифицированный тиреоглобулин выделяется в просвет фолликула, образуя коллоид (3) -
2. Фаза выведения :
затем тироциты (1) реабсорбируют тиреоглобулин (путём пиноцитоза) обратно из коллоида;
при этом возле них в коллоиде появляются светлые полости - ресорбционные вакуоли (4);
в) (Среднее увеличение)

пиноцитозные пузырьки сливаются в клетках с лизосомами, после чего тиреоглобулин расщепляется лизосомальными ферментами ;это приводит к высвобождению из его состава тиреоидных гормонов;
последние выделяются в кровеносные капилляры (2А на снимке в; 2 на снимке г), оплетающие фолликулы.
г) (Большое увеличение)

Г. Гипо- и гиперфункция железы
А как по морфологии железы определить её функциональную активность?
тироциты уплощены , отчего стенка фолликулов утончается;
реабсорбирующая функция тироцитов страдает сильней, чем синтетическая; поэтому
ресорбционные вакуоли почти исчезают ;
объём коллоида (а значит, и полостей фолликулов) увеличивается ;
коллоид из-за застоя уплотнён .
тироциты - высокие, т.е. стенка фолликулов утолщена;
ресорбционные вакуоли в коллоиде - очень крупные,
объём же коллоида (и полостей фолликулов) уменьшается.
Что такое аутоиммунный тиреоидит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сивова А. А., эндокринолога со стажем в 13 лет.
Над статьей доктора Сивова А. А. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Хронический аутоиммунный (лимфоматозный) тиреоидит (ХАИТ) — хроническое заболевание щитовидной железы аутоиммунного происхождения, было описано Х. Хасимото в 1912 г. Заболевание чаще наблюдается у женщин и наиболее часто диагностируется среди известных патологий щитовидной железы. Аутоиммунный тиреоидит выявляется у одной из 10-30 взрослых женщин. [1]
Рассматриваемое заболевание аутоиммунной природы, и для него обязательно присутствие антител. Впервые опубликовали данные об обнаружении антител к ткани щитовидной железы в сыворотке у пациентов с аутоиммунным тиреоидитом в 1956 году. Впоследствии выяснилось, что аутоиммунный тиреоидит подразумевает наличие антител к тиреоглобулину, второму коллоидному антигену и тиреопероксидазе (микросомальному антигену).
Провоцирующие факторы
Сегодня принято считать, что апоптоз, то есть программируемая гибель фолликулярных клеток щитовидной железы — одна из главных причин аутоиммунного тиреоидита и других патологий щитовидной железы. [2] Предполагается, что запуску апоптоза способствуют вирусы и генетические нарушения.
Чем опасен тиреоидит во время беременности
Аутоиммунный тиреоидит у женщины никак не отражается на возможности забеременеть и родить здорового ребёнка при условии, что у пациентки нормальный уровень гормонов — тиреотропный гормон (ТТГ) до 2,5 мЕд/л, в том числе в первом триместре беременности.
При гормональном нарушении возможны следующие осложнения:
-
;
- выкидыш;
- преждевременные роды;
- проблемы со сном;
- поздний токсикоз; ;
- кровотечения после родов;
- гипоксия плода;
- неонатальный тиреотоксикоз.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы аутоиммунного тиреоидита
Изначально, на протяжении некоторого времени, больные не высказывают никаких жалоб. Постепенно с течением времени регистрируют медленное развитие клинической картины снижения функции щитовидной железы, вместе с тем в части ситуаций будет отмечаться прогрессирующее уменьшение размеров железы или же наоборот ее увеличение. [3]
Клинические проявления при хроническом аутоиммунном тиреоидите начинают появляться с нарушением функции щитовидной железы, но в части ситуаций симптомов может и не быть. Все симптомы аутоиммунного тиреоидита щитовидной железы неспецифические, т. е. могут быть при многообразных заболеваниях. Но несмотря на это, все же обозначим клинические проявления, имея которые следует обратиться к эндокринологу для обследования.

Патогенез аутоиммунного тиреоидита
Эндогенный (внутренний) критерий наследования аутоиммунных заболеваний взаимосвязан с клонами Т-лимфоцитов.
- Чтобы произошло развитие хронического заболевания с учетом имеющейся наследственной предрасположенности, нужно влияние экзогенных факторов (вирусных и любых других инфекций, фармпрепаратов), которые способствуют активации Т-лимфоцитов, те впоследствии активируют В-лимфоциты, запуская цепную реакцию.
- Далее Т-клетки, кооперируясь с антитиреоидными антителами, воздействуют на эпителиальные клетки фолликулов, содействуя их деструкции, вследствие чего снижается численность правильно функционирующих структурных единиц щитовидной железы. [1][4]
Количество антитиреоидных антител при этом заболевании непосредственно отражает выраженность аутоиммунного процесса и иногда имеет склонность уменьшаться по мере увеличения продолжительности заболевания. Только присутствия антитиреоидных антител недостаточно, чтобы травмировать структурные элементы щитовидной железы.
Для реализации токсических свойств имеющимся антителам необходимо вступить во взаимодействие с Т-лимфоцитами, которые чувствительны к антигенам щитовидной железы при ХАИТ, чего не бывает при наличии обычного зоба или если патология щитовидной железы не выявлена.
В норме все клетки имеют иммунологическую нечувствительность к другим клеткам собственного организма, которая приобретается во время внутриутробного развития (еще до рождения), во время взаимодействия зрелых лимфоцитов со своими антигенами. Любые нарушения в данном взаимодействии и синтез особых клонов Т-лимфоцитов, которые вступают во взаимодействие со своими же антигенами, и могут стать той причиной, которая приводит к нарушению иммунологической нечувствительности и впоследствии привести к формированию любых аутоиммунных патологий, включая и ХАИТ.
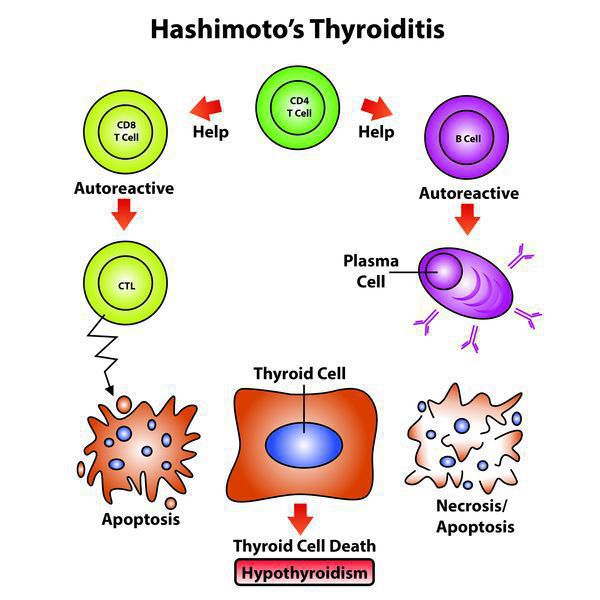
Классификация и стадии развития аутоиммунного тиреоидита
Формы ХАИТ с учетом объема железы и данных клиники:
- Гипертрофическая (тиреоидит Хасимото). Наиболее распространена. Щитовидная железа отличается плотностью, увеличена до II или III степени. Функция железы чаще не изменена, однако в большинстве ситуаций регистрируют тиреотоксикоз или гипотиреоз. Встречается у 15-20% больных.
- Атрофическая. Щитовидная железа в норме или незначительно увеличена, а на момент осмотра может быть даже уменьшена. Функционально — гипотиреоз. Встречается у 80-85% пациентов.
Еще одна классификация аутоиммунного тиреоидита щитовидной железы: [2]
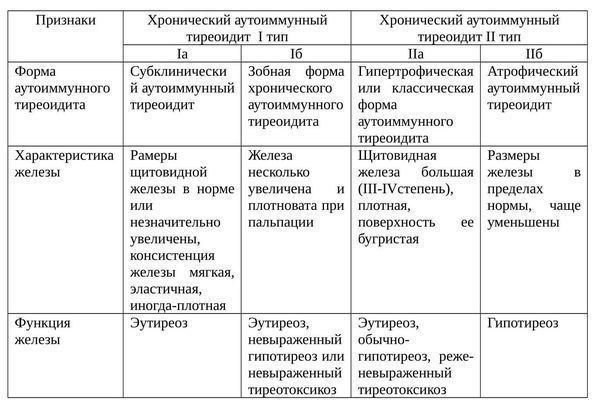
Фазы ХАИТ с учетом клинической картины заболевания:
- Эутиреоидная. Бессимптомное продолжительное (иногда пожизненное) течение, без изменений в функции щитовидной железы.
- Субклиническая. Если заболевание прогрессирует, то поскольку происходит деструкция клеток щитовидной железы и уменьшается уровень тиреоидных гормонов, повышается синтез тиреотропного гормона (ТТГ), который в свою очередь чрезмерно стимулирует щитовидную железу, благодаря чему организм поддерживает на нормальном уровне секрецию Т4.
- Фаза тиреотоксикоза. Поскольку заболевание продолжает развиваться, в кровь высвобождаются имеющиеся тиреоидные гормоны и формируется тиреотоксикоз. Не считая этого, в кровь попадают разрушенные части внутренних структур фолликулярных клеток, в результате образуются антитела к клеткам щитовидной железы. Когда при прогрессирующей деструкции щитовидной железы концентрация гормонопродуцирующих клеток снижается ниже допустимого предела, концентрация в крови Т4 стремительно уменьшается, развивается стадия явного гипотиреоза.
- Фаза гипотиреоза. Продолжается приблизительно в течение года, чаще всего после этого происходит восстановление функции щитовидной железы. Иногда гипотиреоидная фаза продолжается всю жизнь.
ХАИТ преимущественно протекает только с одной фазой заболевания. [5]
Осложнения аутоиммунного тиреоидита
ХАИТ — условно безопасное заболевание, не приводящее к осложнениям только при условии сохранения необходимой концентрации гормонов в крови, т. е. эутиреоидного состояния. И, соответственно, тогда никаких осложнений не развивается. Но при наступлении гипотиреоза могут наблюдаться осложнения. При отсутствии лечения гипотиреоза могут возникать осложнения: нарушение репродуктивной функции, выраженное снижение памяти, вплоть до слабоумия, анемия, но самое грозное и тяжелое осложнение гипотиреоза — гипотиреоидная или мексидематозная кома — возникает при резкой недостаточности гормонов щитовидной железы. [5] [6]
Диагностика аутоиммунного тиреоидита
Диагностика ХАИТ состоит из нескольких пунктов. Для определения данного заболевания у больного необходим минимум один большой критерий, если таких критериев не обнаружено, то диагноз лишь вероятен. [1]
Большие диагностические критерии:
- первичный гипотиреоз (причем возможен как манифестный, так и устойчивый субклинический);
- присутствие антител к ткани щитовидной железы;
- ультразвуковые критерии аутоиммунной патологии.
Пальпация щитовидной железы
Какие анализы нужны, чтобы определить АИТ
Для установления аутоиммунного тиреоидита необходимо сдать кровь на тиреотропный гормон ( ТТГ), тироксин свободный (Т4 свободный) и антитела к тиреопероксидазе (ТПО). Если антитела к ТПО повышены, но ТТГ в пределах нормы, то диагноз АИТ носит вероятный характер.
Нужно заметить, что при обнаружении у больного гипотиреоза манифестного или стабильного субклинического, диагностирование аутоиммунного тиреоидита важно для установления причины уменьшения функции железы, но несмотря на это постановка диагноза никак не меняет терапевтических методов. Лечение заключается в употреблении заместительной гормональной терапии препаратами тиреоидных гормонов.
Использование пункционной биопсии щитовидной железы не показано для установления хронического аутоиммунного тиреоидита. Ее необходимо проводить, только если имеются узлы щитовидной железы, более 1 см в диаметре.
Важно отметить, что нет надобности контролировать в течение болезни количество имеющихся антител к щитовидной железе, потому что данная процедура не имеет диагностической роли для анализа прогрессирования аутоиммунного тиреоидита. [7]
Лечение аутоиммунного тиреоидита
Терапия аутоиммунного тиреоидита щитовидной железы неспецифическая. При формировании фазы тиреотоксикоза достаточно применения симптоматической терапии. При формировании гипотиреоза главным вариантом медикаментозной терапии является назначение тиреоидных гормонов. Сейчас в аптечной сети РФ возможно приобрести только таблетки Левотироксина натрия (L-тироксин и Эутирокс). Применение таблетированных препаратов тиреоидных гормонов нивелирует клинику гипотиреоза и при гипертрофической форме аутоиммунного тиреоидита вызывает уменьшение объема щитовидной железы до допустимых значений.
В случае обнаружения у пациента манифестного гипотиреоза (повышение уровня тиреотропного гормона и снижение концентрации Т4 свободного) необходимо использование в лечении левотироксина натрия в средней дозе 1,6 – 1,8 мкг/кг массы тела пациента. Показателем правильности назначенного лечения будет являться уверенное удержание в пределах референсных значений тиреотропного гормона в крови больного.
Когда у больного диагностирован субклинический гипотиреоз (увеличена концентрация ТТГ в совокупности с неизмененной концентрацией Т4 свободного), необходимо:
- Спустя 3–6 месяцев вторично провести гормональное обследование для доказательства наличия изменения функции щитовидной железы;
- Когда в течение беременности у пациентки обнаружено увеличение уровня тиреотропного гормона, даже при сохраненной концентрации Т4 свободного, назначить левотироксин натрия в полной расчетной заместительной дозе сразу же;
- Лечение левотироксином натрия нужно при постоянном субклиническом гипотиреозе (увеличение концентрации тиреотропного гормона в крови свыше 10 мЕд/л, и еще в ситуациях не менее двукратного определения концентрации тиреотропного гормона между 5 – 10 мЕд/л), но если этим больным более 55 лет и у них имеются сердечно-сосудистые патологии, лечение левотироксином натрия назначается только при отличной переносимости лекарства и при отсутствии сведений о декомпенсации данных болезней на фоне приема тироксина;
- Показатель достаточности лечения субклинического гипотиреоза представляет собой стабильное удержание уровня ТТГ в пределах референсных значений в крови.
Если у женщин перед планированием беременности, выявлены антитела к ткани щитовидной железы и/или ультразвуковые признаки аутоиммунного тиреоидита, нужно определить гормональную функцию щитовидной железы (концентрацию тиреотропного гормона и концентрацию Т4 свободного) и обязательно определять уровень гормонов в каждом триместре беременности. [8]
Если поставлен диагноз аутоиммунный тиреоидит, но не выявляются изменения в работе щитовидной железы, применение препаратов левотироксина натрия не показано. [9] Оно возможно иногда в исключительных ситуациях внушительного увеличения объема щитовидной железы, спровоцированного аутоиммунным тиреоидитом, при этом решение принимается по каждому пациенту индивидуально. [10]
Физиологическое количество калия йодита (приблизительно 200 мкг/сутки) не могут спровоцировать формирование гипотиреоза и не осуществляют негативного воздействия на функцию щитовидной железы при ранее развившемся гипотиреозе, вызванном аутоиммунным тиреоидитом.
Питание при аутоиммунном тиреоидите
Продуктов, которые влияют на течение аутоиммунного тиреоидита, не существует. Глютен или лактоза не имеют отношения к гипотиреозу на фоне АИТ. Поэтому рекомендации по питанию для людей с аутоиммунным тиреоидитом такие же, как и для всех остальных: разнообразное сбалансированное питание с достаточным употреблением воды.
Существуют ли народные способы лечения
Аутоиммунный тиреоидит лечат только медицинскими препаратами, которые назначает эндокринолог. Отсутствие адекватной терапии может грозить опасными осложнениями: нарушением репродуктивной функции, выраженным снижением памяти (вплоть до слабоумия), анемией и комой, которая возникает при резкой недостаточности гормонов щитовидной железы.
Прогноз. Профилактика
Хронический аутоиммунный тиреоидит прогрессирует обычно крайне медленно, с развитием гипотиреоидного состояния спустя несколько лет. В отдельных ситуациях состояние и трудоспособность сохраняются в течение 15-18 лет, даже с учетом непродолжительных обострений. В фазе обострения тиреоидита регистрируются симптомы невыраженного либо гипотиреоза, либо тиреотоксикоза.
Сегодня методов профилактики хронического аутоиммунного тиреоидита не найдено.
Что такое гипотиреоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 28 лет.
Над статьей доктора Курашова О. Н. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Гипотиреоз — это заболевание эндокринной системы, возникающее из-за длительно низкого уровня тиреоидных гормонов, вырабатываемых щитовидной железой, и проблем с их воздействием на организм преимущественно на тканевом уровне.
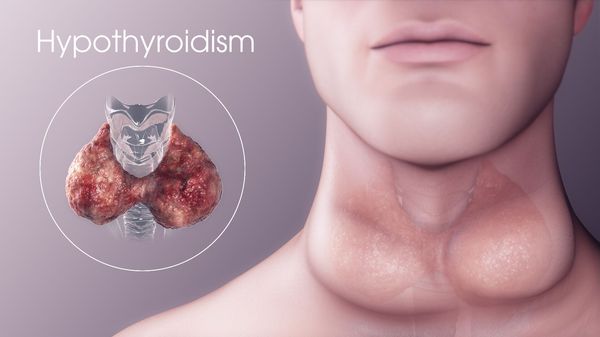
Ежегодно на каждую тысячу человек приходится 0,6-3,5% заболевших гипотиреозом. [3] [6] [8] Данное нарушение может возникнуть в любом возрасте, но обычно оно возникает у пожилых людей старше 60 лет. [14] Среди новорождённых гипотиреоз встречается в одном случае из 4-5 тысяч.
К факторам риска относятся:
-
; ;
- подострый и послеродовой тиреоидит;
- аутоиммунные заболевания (B1-дефицитная анемия, болезнь Аддисона, сахарный диабет I типа);
- рак тканей головы и шеи (леченый);
- курение;
- болезни щитовидной железы у родственников;
- применение радиоактивного йода при лечении рака щитовидной железы ;
- приём некоторых препаратов (амиодарон, α-интерферон, карбонат лития, йод-, бромсодержащие и другие лекартсва). [15]
В 80% случаев гипотиреоз связан с поражением защитных сил организма, т. е. аутоиммунным тиреоидитом. Он является ведущей причиной первичного гипотиреоза у взрослых людей. [3]
Риск возникновения аутоиммунного тиреоидита зависит от возраста и пола пациента: у женщин в возрасте 40-50 лет он возникает в 10-15 раз чаще, чем у мужчин. [6] [9]
При аутоиммунном тиреоидите даже на фоне длительной ремиссии функциональное состояние щитовидной железы в разное время может значительно различаться. Так, с возрастом деструктивные изменения в щитовидной железе постепенно нарастают. Этот фактор, а также наличие тиреоидных аутоантител могут спровоцировать переход субклинического (скрытого) гипотиреоза, протекающего на фоне аутоиммунного тиреоидита, в явный. Частота таких случаев составляет около 5 % в год.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гипотиреоза
Симптомы гипотиреоза крайне обманчивы, разнообразны и не всегда заметны. Их проявление зависит от степени выраженности заболевания.
К основным клиническим проявлениям относятся: [9] [11] [14]
- Обменно-гипотермический синдром. Характерно постоянное чувства холода, снижение температуры тела, увеличение веса.
- Нарушение нервной системы и органов чувств. Человек становится заторможенным, вялым, появляется сонливость, ухудшается память, нарушается носовое дыхание и слух, голос становится низким и грубым, а речь замедленной. На лице и конечностях может возникнуть плотный отёк. Кожа утолщается, становится сухой и холодной, приобретает бледный окрас с желтоватым оттенком, волосы становятся тусклыми и ломкими, подверженными выпадению.
- Нарушение сердечно-сосудистой системы. Наблюдается пониженное или нормальное артериальное давление. У части пациентов возникает мягкая диастолическая гипертензия.
- Изменения со стороны ЖКТ. Замедляется перистальтика кишечника, возникают запоры, изменения желчного пузыря и его протоков, снижается аппетит, вплоть до развития анорексии.
- Анемический синдром. Из-за недостатка гормонов щитовидной железы возникает депрессия костно-мозгового кроветворения, нередко развивается В12-дефицитная и постгеморрагическая анемия, время кровотечения увеличивается.
- Дисфункция почек. Почечный кровоток и скорость клубочковой фильтрации снижаются, как и эффективность почечного плазмотока, уровень глюкозы и натрия в крови становится ниже нормы.
- Сбои репродуктивной системы. У женщин происходит нарушение овуляции, менструальные циклы становятся короткими и редкими, возникает бесплодие. В большинстве случаев развивается вторичная гиперпролактинемия, которая сопровождается самопроизвольным вытеканием молока из молочной железы и отсутствием месячных. На фоне декомпенсированного гипотиреоза беременность наступает крайне редко. Снижение либидо наблюдается у лиц обоего пола. У мужчин может развиваться эректильная дисфункция, нарушение сперматогенеза.
- Нарушение опорно-двигательной системы. Как правило, замедляется костное ремоделирование, снижается интенсивность резорбции (рассасывания) кости и костеобразования. Часто возникает снижение плотности костной ткани и рабдомиопатия, причём как с гипертрофией (увеличением) мышц, так и с их атрофией.
Патогенез гипотиреоза
Тиреоидные гормоны, которые вырабатывает щитовидная железа, называются "трийодтиронин" (Т3) и "тироксин" (Т4). Они влияют практически на все процессы, протекающие в организме. Стимулирующее влияние на них оказывает тиреотропный гормон гипофиза (ТТГ).
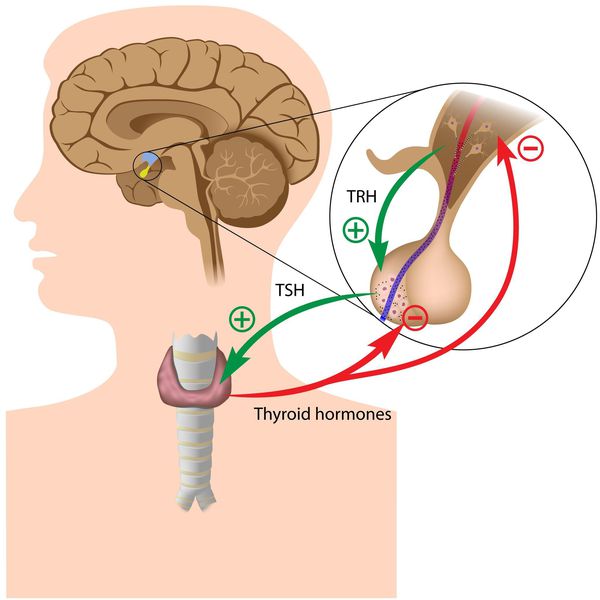
Синтез тиреоидных гормонов начинается после того, как щитовидная железа захватывает йод. Он является регулятором гормоногенеза и размножения тиреоцитов — клеток эпителия щитовидной железы. Попав в тиреоциты, йодид окисляется до активной формы при помощи тиреопероксидазы — микросомального антигена, к которому образуются антитела, в частности при аутоиммунном тиреоидите. [4] [6] [7] Уровень поступления йода изменяет чувствительность тиреоцитов к воздействию ТТГ, которая усиливается при дефиците йода. [3] [6]
Исходя из этого механизма возникновения гормонов щитовидной железы, патогенетически гипотиреоз делится на три типа:
- первичный (тиреогенный);
- вторичный (гипофизарный);
- третичный (гипоталамический);
- периферический (тканевой).
Первичный гипотиреоз возникает в 80-95% случаев и чаще всего обусловлен нарушениями общей структуры щитовидной железы, которые являются врождёнными или приобретёнными, а также сбоем секреторной функции её клеток.
Вторичный и третичный гипотиреоз возникают в 3-4% случаев. Они связаны с заболеваниями таких участков головного мозга, как аденогипофиз или гипоталамус в результате которых наблюдается стойкая нехватка гормонов щитовидной железы и нарушение секреции ТТГ гипофиза. [4] [6]
Периферический гипотиреоз развивается крайне редко — в 0-1% случаев. Основным фактором его возникновения является резистентность (сопротивляемость) тканей-мишеней (например, мозга, гипофиза, сердца, костей, печени) гормонам Т4 и Т3. [5] [6] [7]
В патогенезе аутоиммунных заболеваний щитовидной железы взаимодействуют генетические и средовые факторы. Однако точная роль тех и других не определена. Ведущее значение в гибели тиреоцитов при этих заболеваниях придают клеточным механизмам, т.е. цитотоксическим эффектам аутореактивных Т- лимфоцитов. [3] [5] Отсутствие при аутоиммунных поражениях щитовидной железы классических признаков гнойного воспаления (боли, отёка и других), обычно сопровождающих массивный некроз ткани, указывает в таких случаях на иной механизм гибели тиреоцитов. В последние годы установлено, что Т-лимфоциты способны вызывать гибель клеток-мишеней не только путём некроза, но в основном путём индукции их разрушения. [3] [5] [7] [9]
Классификация и стадии развития гипотиреоза
В Международной классификации болезней десятого пересмотра выделены две формы гипотиреоза:
- Субклинический (скрытый) гипотиреоз, развившийся в результате йодной недостаточности.
- Иные формы гипотиреоза:
- врожденный гипотиреоз с диффузным зобом;
- врождённый гипотиреоз без зоба;
- гипотиреоз, возникший по причине приёма лекарств и других экзогенных веществ;
- постинфекционный гипотиреоз;
- атрофия щитовидной железы (приобретённая);
- другие уточнённые гипотиреозы;
- неуточнённый гипотиреоз.
Первичный гипотиреоз подразделят на три большие группы:
- Врождённый гипотиреоз.
- Гипотиреоз, связанный с уменьшением количества функционирующей ткани щитовидной железы:
- возникающий после операции
- развивающийся после облучения
- вызванный аутоиммунным нарушением щитовидной железы
- связанный с вирусным заболеванием щитовидной железы
- возникающий на фоне новообразований щитовидной железы.
- Гипотиреоз, связанный с нарушением выработки тиреоидных гормонов:
- эндемический зоб — возникает в районах с йододефицитом;
- спорадический зоб с гипотиреозом — развивается в случае дефектов биосинтеза гормонов;
- медикаментозный гипотиреоз — появляется в результате приёма тиреостатиков и других препаратов;
- зоб и гипотиреоз, развившиеся в связи с употреблением продуктов, содержащих вредные вещества. [3][5][7][9]
В последнее время разработана классификация первичного гипотиреоза, которая основывается на выраженности симптомов и результатах гормональных исследований (определяющий показатель — уровень ТТГ). В неё включают:
- Субклинический (скрытый) гипотиреоз — симптомы размыты или отсутствуют, уровень ТТГ повышен, содержание Т4 в норме.
- Манифестный — возникает типичная клиническая картина гипотиреоза, уровень ТТГ повышен, концентрация Т4 снижена:
- компенсированный.
- декомпенсированный.
- Осложнённый — развивается кретинизм, сердечная недостаточность, выпот в серозные полости, вторичная аденома гипофиза. [2]
Осложнения гипотиреоза
Гипотиреоидная кома ("спячка") — это угрожающее жизни состояние, которое чаще развивается у пожилых людей, которые долгое время не лечили тяжёлый гипотиреоз, который был у них довольно долгое время. [3] [5] [7] [9]
К основным провоцирующим факторам такого осложнения относят:
- охолаждение;
- сердечно-сосудистые заболевания;
- острые инфекции;
- травмы;
- кровопотерю;
- хирургические вмешательства;
- приём алкоголя или лекарств, угнетающих функцию центральной нервной системы;
- стрессовые ситуации. [6][7][8]
При гипотиреоидной коме температура тела, как правило, снижается до 24-32,2°С, возникают судороги и угнетение дыхания. Лечение такого состояния нужно начинать незамедлительно. [14] Но даже при своевременном обнаружении осложнения и незамедлительном лечении смерть может наступить в 25-60% случаев. [15]
Но появление осложнений может вызвать не только отсутствие лечения, но и неграмотная медикаментозная терапия. Например, передозировка лекарствами может привести к избыточному синтезу гормонов щитовидной железы и патологиям со стороны сердечно-сосудистой системы. В связи с этим крайне важно соблюдать все рекомендации врача по лечению заболевания и ни в коем случае не лечиться самостоятельно.
Диагностика гипотиреоза
Диагностика гипотиреоза включает в себя подробный опрос пациента, осмотр и лабораторные исследования.
Так как симптомы гипотиреоза неспецифичны, он может скрываться под масками других заболеваний. Поэтому по проявлениям его иногда можно спутать с железодефицитной анемией, депрессией, аменореей, невритом и другими нарушениями. [15] [16] В связи с этим важную роль в определении гипотиреоза играют лабораторные исследования. Они показаны всем пациентам с нарушениями щитовидной железы и предполагают оценку уровня ТТГ и свободного Т4. [2] [12] Определение уровня Т3 в крови, как правило, не является информативным, так как при первичном гипотиреозе этот показатель находится в норме. [14]
На явное наличие гипотиреоза будет указывать высокий уровень ТТГ и низкий уровень свободного Т4 в крови. При субклиническом гипотиреозе уровень ТТГ также будет повышен, а уровень свободного Т4 будет находиться в пределах нормы.
После того как наличие гипотиреоза подтверждено, при помощи показателя ТТГ также определяется характер заболевания и наличие возможных осложнений. Уровень ТТГ также позволяет в значительном большинстве случаев оценить адекватность проводимой терапии: об этом будет свидетельствовать стойкий уровень ТТГ в крови в пределах нормы. [6] [7] [8]
В достаточно редких случаях проводят пробу с тиреолиберином для оценки аутоиммунных заболеваний щитовидной железы. [6] [9] [15]
Дополнительные методы диагностики, такие как УЗИ щитовидной железы, сцинтиграфия или пункционная биопсия, используются для уточнения характера и степени выраженности заболевания. [6] [11] [12] [16]
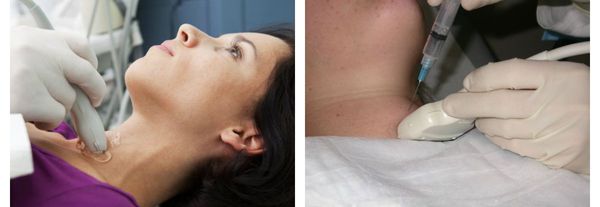
Так как с возрастом учащаются случаи узлового зоба, выраженный шейный кифоз может смещать трахею кзади и вниз, что затрудняет пальпаторную оценку состояния щитовидной железы, в результате чего своевременная диагностика заболевания не проводится. [4] [5] [6] [7] [8]
В связи с тем, что гипотиреоз не всегда проявляет себя, среди населения принято проводить массовую диагностику данного заболевания — скрининг. Так, определение уровня ТТГ позволяет обнаружить первичный гипотиреоз у людей без каких-либо других его проявлений, а также у новорождённых (исследование проводится на 4-5 сутки жизни). При планировании беременности и на ранних её сроках также важно пройти исследование на гипотиреоз. [3] [5] [7] [9]
Лечение гипотиреоза
Цель лечения гипотиреоза — это поддержание уровня ТТГ в пределах 0,5-1,5 мМЕ/л.
Единственным методом лечения является пожизненная заместительная терапия. Начинать её стоит при уровне ТТГ более 10 мЕД/л, высоких титрах антител к ТПО и других показателях. Для этого предпочтительны препараты левотироксина натрия. Его применение противопоказано лишь в случае нелеченого тиреотоксикоза и недостаточности коры надпочечников, остром инфаркте миокарда, аллергии и индивидуальной непереносимости препарата. [16]
Обычно лечение проводится в условиях стационара. Показаниями к госпитализации пациентов с гипотиреозом служат:
- тяжёлая степень заболевания;
- наличие выраженной сердечной патологии;
- гипотиреоидная кома.
Заместительная терапия первичного (манифестного) гипотиреоза показана пожизненно с назначением тироксина в средней дозе 1,6-1,8 мкг/кг. Пациентам с кардиальной патологией доза рассчитывается, исходят из расчёта 0,9 мкг/кг. Стоит отметить, что в связи с уменьшением метаболизма тиреоидных гормонов потребность в них с возрастом снижается. [5] [7] [9]
Дозы тироксина зависят от причин и патогенеза заболевания. Потребность в препарате у людей со спонтанным гипотиреозом выше, чем у пациентов с гипотиреозом, возникшим после хирургического лечения и применения радиоактивного йода.
Уровень ТТГ при диагностике гипотиреоза напрямую связан с оптимальной заместительной дозой тироксина: у большинства женщин она составляет 75-100 мкг, а у мужчин — до 150 мкг в день приёма.
Первый контроль уровня ТТГ после начатого лечения проводят через 2-3 месяца, затем один раз в шесть месяцев (при обязательном условии соблюдения пациентом схемы лечения). [6] [9] [13]
При субклиническом гипотиреозе существует риск развития манифестной формы заболевания со всеми характерными проявлениями. Так, явный гипотиреоз возникает у 20-50% пациентов в течение 4-8 лет, а присутствие антитиреоидных антител увеличивает риск до 80%. [8] [9] [10] Потому людям со скрытым гипотиреозом следует длительно наблюдаться у специалистов.
Проблемы при лечении гипотиреоза
Лечение тироксином безопасно, просто и сравнительно дешево. Но, несмотря на многолетний опыт его использования, при нём всё же могут возникать многие проблемы. Основная из них связана с несоблюдением пациента схемы лечения. Так, одновременное повышение уровней Т4 и ТТГ, по всей вероятности, будет указывать на то, что за несколько дней до визита к врачу пациент не выполнял его назначений.
Снижение эффективности установленной дозы тироксина часто связано с меньшим содержанием гормона в таблетках (например, в непатентованных препаратах) или взаимодействием лекарств при одновременном приёме других препаратов. [9] [13]
Недостаточность дозы также может быть связана с уменьшением всасывания тироксина, нарушением энтеропечёночного кровотока, ускорением кругооборота или выделением гормона с мочой, медленным снижением тиреоидной функции после лечения гипертиреоза.
Существуют и другие особенности и проблемы при лечении гипотиреоза. [6]
Лучшим критерием подбора дозы тироксина при аутоиммунном тиреоидите является исследование ТТГ и свободного Т4. При этом лечение нацелено на компенсацию гипотиреоза благодаря той же заместительной терапии и редукция зоба при помощи супрессивной терапии. [6] [9] Критериями эффективности лечения при этом будут служить:
- уменьшение зоба в объёме;
- снижение плотности щитовидной железы;
- уменьшение титра антител до нормы;
- поддержание уровня ТТГ в пределах нормы.
Назначение препаратов тиреогормонов при аутоиммунном тиреоидите без нарушения функции щитовидной железы нецелесообразно, а операция может привести к состоянию, способному значительно ухудшить качество жизни пациента с возможностью развития тяжёлого гипотиреоза и инвалидизации. [9] [13]
Прогноз. Профилактика
Прогноз заболевания при своевременной диагностике и лечении благоприятный. [10] Осложнить его, особенно в отношении трудоспособности и состояния здоровья в целом, могут фибрилляция предсердий и выраженная сердечная недостаточность, развивающиеся на фоне тиреотоксикоза. [5]
Специфической профилактики заболевания не существует. Снизить риск развития гипотиреоза можно только при помощи сбалансированного правильного питания , употребления достаточного количества йода с пищей (включения в рацион морепродуктов) и контроля гормонального баланса. Крайне важно проходить профилактические осмотры и являться на контрольные приёмы к лечащему врачу. [5] [11] [12]
В качестве неспецифической профилактики патологий щитовидной железы стоит проходить санаторно-курортное лечение по показаниям врача.
Доказано, что медикаментозная терапия при гипотиреозе становится более эффективной в сочетании с радоновыми процедурами, а азотные ванны, не содержащие радон, оказывают профилактическое воздействие. [1] [5] Благодаря этому удаётся добиться стойкости ремиссии заболевания.

Рекомендуется проведение до трёх курсов таких процедур с интервалом от 8 до 12 месяцев. Подбор схем лечения в санатории (в т.ч. медикаментозных), рациональное использование природных и климатических факторов определяют ближайший и отдалённый результат оздоровления.
Читайте также:

