Элидел при поствоспалительной пигментации
Обновлено: 28.04.2024
БЕСПЛАТНАЯ КОНСУЛЬТАЦИЯ: поможем врачам и владельцам клиник выбрать оборудование для лечения сосудистых дисхромий
Оглавление
Посттравматические и поствоспалительные сосудистые дисхромии — это приобретенные расстройства пигментации, в патогенезе которых задействован сосудистый компонент кожи на фоне острого или хронического воспаления, либо травмы.
В нашей компании Вы можете приобрести следующее оборудование для лечения посттравматических и поствоспалительных сосудистых дисхромий:
Этиология и патогенез
Кровеносные и лимфатические сосуды кожи в норме
Артериолы и венулы образуют в дерме два сплетения (рис. 1):
- Верхнее горизонтальное — находится в папиллярной дерме, из него выходят капиллярные петли дермальных сосочков.
- Нижнее горизонтальное — расположено на границе дермы и подкожно-жировой клетчатки. Оно образовано сосудами, идущими со стороны мышц и подкожного жира.
Артериолы и венулы нижнего горизонтального сплетения соединяются с верхним горизонтальным сплетением, а также формируют боковые оттоки, кровоснабжающие луковицы волос и потовые железы.
Внешний диаметр артериальных сосудов папиллярной дермы варьируется от 17 до 26 мкм — они называются терминальными артериолами. Их стенка состоит из непрерывного монослоя эндотелиальных клеток с базальной мембраной, которые снаружи покрыты перицитами (рис. 2). В нормальных условиях эндотелиоциты подавляют коагуляцию крови и предотвращают попадание белков плазмы в окружающую ткань.
Лимфатические сосуды кожи образуют два сплетения, аналогичные верхнему и нижнему горизонтальному сплетению кровеносных сосудов и располагающиеся вблизи них. Ветви от верхнего лимфатического сплетения проходят в дермальные сосочки и дренируются в более крупные лимфатические сосуды глубокой дермы и верхней части ПЖК.
В отличие от эндотелиальных клеток кровеносных сосудов, эндотелиальные клетки лимфатических сосудов наслаиваются друг на друга, почти не имея плотных соединений и обладая рудиментарной базальной мембраной (либо вообще без нее). К тому же просвет лимфатических сосудов значительно шире, а стенка тоньше — это позволяет тканевой жидкости беспрепятственно попадать в них (рис. 3).
Рис. 1. Верхнее (papillary plexus) и нижнее (cutaneous plexus) горизонтальные сосудистые сплетения в коже (Elsevier)
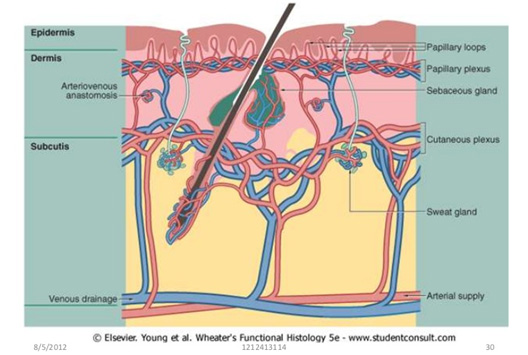
Рис. 2. Кожная биопсия терминальной артериолы (слева) и венулы (справа) кожи. У артериолы обращает на себя внимание более толстая стенка и фрагментированная эластичная пластинка (темно-синие точки) (Saara T. et al. Diagnosing vascular dementia by skin biopsy — Uniqueness of CADASIL. Skin Biopsy — Perspectives 2011)
Кровеносные и лимфатические сосуды кожи при воспалении
Кровеносные и лимфатические сосуды вносят существенный вклад в патогенез воспалительного процесса и его клинические проявления. Расширенные артериальные и венозные капилляры с усиленным кровотоком лежат в основе rubor и calor — покраснения и местного повышения температуры. Избыток экссудата, вызванный ростом проницаемости кровеносных сосудов и дренажной способности лимфатических сосудов, приводит к tumor — отеку. Наконец, dolor и functio laesa (боль и нарушение функции) возникают после притока лейкоцитов в область воспаления.
Активация эндотелия медиаторами воспаления (VEGF, TNF-α, IL-6, IL-1β и др.) усиливает его чувствительность к веществам, которые обеспечивают взаимодействие с лейкоцитами: E-селектин, молекула межклеточной адгезии 1 (ICAM-1), молекула адгезии сосудистых клеток 1 (VCAM-1) (рис. 3). При хроническом воспалении сеть кровеносных сосудов долгое время остается активированной и высокопроницаемой, что поддерживает накопление жидкости в тканях. Под ее влиянием эндотелиальные клетки лимфатических капилляров расходятся, и жидкость из тканей начинает просачиваться в лимфатическую сеть. Механизмы, контролирующие увеличение лимфатического просвета, в настоящее время неизвестны, как не изучена и функция расширенных лимфатических капилляров. Считается, что они способствуют подавлению воспалительного процесса.
Воспалительные заболевания и состояния, в которые вовлекается сосудистый компонент кожи (Huggenberger R., Detmar M.. The cutaneous vascular system in chronic skin inflammation. J Investig Dermatol Symp Proc 2011; 15(1): 24–32):
- Розацеа
- Атопический дерматит
- Гнездная алопеция
- Буллезный пемфигоид
- Герпетиформный дерматит
- Экссудативная эритема
- Системный склероз
Здесь также следует отметить атеросклероз, бронхиальную астму, ревматоидный артрит и воспалительные заболевания кишечника. Ниже будут описаны заболевания и состояния кожи, в патогенезе которых лучше всего изучено участие сосудистого компонента кожи.
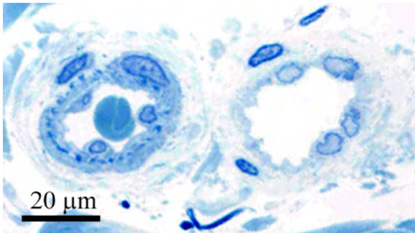
Рис. 3. Современные представления о роли кровеносных и лимфатических сосудов в хроническом воспалении кожи (Huggenberger R., Detmar M. The cutaneous vascular system in chronic skin inflammation. J Investig Dermatol Symp Proc 2011; 15(1): 24–32)
Кровеносные сосуды кожи (справа) состоят из монослоя эндотелиальных клеток (красные) с непрерывной базальной мембраной (серая), которые снаружи покрыты перицитами (синие). Эндотелиальные клетки лимфатических сосудов (зеленые, слева) не имеют плотных соединений, накладываются друг на друга «внахлест» и обладают рудиментарной базальной мембраной. Они связаны с внеклеточным матриксом через фибриллиновые филаменты (зеленые нити). Просвет лимфатических сосудов значительно шире, а стенка тоньше, чем у кровеносных сосудов.
Эндотелиальные клетки кровеносных сосудов экспрессируют рецепторы к фактору роста эндотелия сосудов (VEGF) — VEGFR-1 и VEGFR-2. В то же время эндотелиальные клетки лимфатических сосудов экспрессируют VEGFR-2 и VEGFR-3. Ключевой «игрок» хронического воспаления — VEGF-A — может связываться с VEGFR-1 и VEGFR-2, т.е. влиять и на кровеносные, и на лимфатические сосуды. Длительная стимуляция VEGF-A и VEGF-С приводит к ремоделированию сосудов, увеличению их проницаемости, повышенной экспрессии молекул адгезии и хроническому воспалению кожи. На этом фоне лимфатические сосуды расширяются, что, вероятно, подавляет воспаление. Его угнетению также способствует связывание хемокинов с рецептором D6.
Поствоспалительные сосудистые дисхромии на примере розацеа
Розацеа характеризуется выраженными сосудистыми изменениями в коже. Все механизмы данной патологии пока не изучены, но считается, что в ее патогенезе участвуют:
- врожденный иммунитет;
- активные формы кислорода;
- ультрафиолетовое излучение;
- микробиом кожи;
- сосудистые изменения.
Локально в коже усиливается кровоток, что вместе с дилатацией сосудистых сплетений в дерме приводит к типичным клиническим проявлениям розацеа (см. ниже). Сообщалось, что у пациентов с розацеа повышены уровни фактора роста эндотелия сосудов А (VEGF-A), усилен ангиогенез и лимфангиогенез. Клинически это подтверждается эпизодами «приливов» и эритемы. Ультрафиолетовое облучение усугубляет течение розацеа — вероятно, путем стимуляции кератиноцитов к еще большему синтезу VEGF-A.
Интересно, что роль лимфатических сосудов в патогенезе розацеа в настоящее время неизвестна. У ряда пациентов наблюдается отек кожи, напоминающий лимфедему, а при фиматозных изменениях может отмечаться выраженная лимфедема кожи. Это указывает на важную роль нарушения лимфатической дисфункции в патогенезе розацеа, но какую именно — пока неясно.
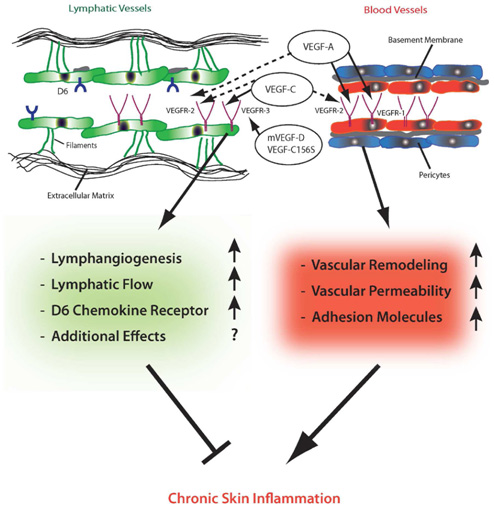
Клинические проявления розацеа состоят из целого спектра симптомов и признаков. На щеках и лбу пациентов время от времени появляется эритема с телеангиэктазиями — обычно после определенных триггеров. На носу, лбу и щеках могут наблюдаться воспалительные папулы и гнойнички (рис. 4). В отличие от акне, пациенты с розацеа не сообщают о повышенной жирности кожи — вместо этого они чувствуют сухость и шелушение. Отсутствие комедонов также говорит в пользу розацеа при дифференциальной диагностике с обыкновенными угрями. Наконец, розацеа почти никогда не приводит к образованию рубцов на коже.
На финальных стадиях у пациентов может возникать ринофима — утолщенный и деформированный нос. Хотя в ряде случаев ринофима появляется изолированно, без других клинических признаков розацеа.
Рис. 4. Розацеа (Danish national service on dermato-venereology)
Посттравматические сосудистые дисхромии
Посттравматическим сосудистым дисхромиям предшествует какая-либо травма — ушиб, инъекция кожи, надрез и др. В результате кровь попадает в мягкие ткани, где происходит окисление гемоглобина и ферритина с последующим накоплением гемосидерина. Предрасполагающие факторы:
- отек нижних конечностей;
- сахарный диабет;
- болезни сердечно-сосудистой системы;
- повышенное артериальное давление;
- венозная гипертензия;
- хроническая венозная недостаточность;
- липодерматосклероз.
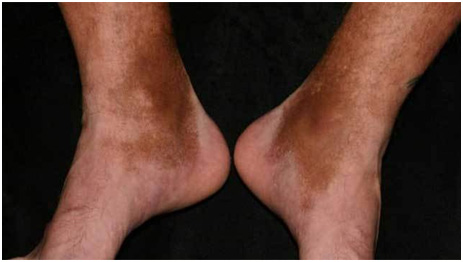
Посттравматические сосудистые дисхромии проявляются пятнами любого размера и формы, цвета от желтого до коричневого или черного, возникающими в любой области тела, но чаще на нижних конечностях (рис. 5).
Рис. 5. Посттравматическая гиперпигментация на ногах из-за повреждения сосудов и скопления гемосидерина под кожей (Photo: MavCure)
Принципы лечения
Лечение посттравматических и поствоспалительных сосудистых дисхромий зависит от конкретного заболевания или состояния кожи. Например, для пациентов с розацеа важным условием является избегание триггерных факторов. У каждого человека набор таких факторов индивидуален и выясняется он опытным путем. В качестве профилактического средства рекомендуется солнцезащитная косметика с UVA и UVB фильтрами. Пациенты с розацеа лучше переносят физические фильтры — оксид цинка и диоксид титана.
При посттравматических сосудистых дисхромиях определенную пользу могут принести местные кортикостероидные средства, гризеофульвин, циклоспорин А, витамин С и биофлавоноиды.
Эффективным методом лечения поствоспалительных и посттравматических сосудистых дисхромий является IPL-терапия — применение интенсивного импульсного света (Intense Pulsed Light). IPL-модуль входит в универсальный аппарат-платформу М22 (Lumenis). Его положительное действие основано на селективном фототермолизе — поглощении света определенной длины волны гемоглобином крови. Параметры IPL подбираются таким образом, чтобы находящийся в расширенных сосудах гемоглобин накапливал максимум световой энергии. В результате происходит локальный нагрев и разрушение патологических капилляров, которые питают участок дисхромии.
Весомым преимуществом IPL перед лазерами является площадь воздействия — интенсивный импульсный свет обладает широким пучком, что позволяет быстро и качественно обрабатывать большие участки сосудистых сеточек, мальформаций, гемангиом, телеангиэктазий, варикозно расширенных капилляров и др.
Определенную сложность для IPL представляет меланин, который скапливается в коже над областью дисхромии и действует как экран, затрудняя прохождение света к гемоглобину крови. Для решения этой проблемы IPL-модуль аппарата-платформы М22 имеет несколько светофильтров, которые «отсекают» лишнее световое излучение, чтобы селективно нагревать только гемоглобин в расширенных сосудах. Для повышения эффективности воздействия также используется несколько проходов IPL-модулем.
в тубах алюминиевых по 15, 30 или 100 г; в пачке картонной 1 туба.
Описание лекарственной формы
Гомогенный крем от белого до почти белого цвета.
Фармакологическое действие
Фармакодинамика
Пимекролимус является производным макролактама аскомицина и обладает противоспалительным действием. Пимекролимус селективно ингибирует продукцию и высвобождение цитокинов и медиаторов воспаления из Т-лимфоцитов и тучных клеток.
Пимекролимус специфично связывается с цитозольным рецептором макрофилином-12 и ингибирует кальцийзависимую фосфатазу — кальциневрин. Ингибирование кальциневрина приводит к подавлению пролиферации Т-лимфоцитов и предотвращает транскрипцию и выработку в Т-хелперах типов 1 и 2 ранних цитокинов, таких как ИЛ-2, γ-интерферон, ИЛ-4, ИЛ-5, ИЛ-10, фактор некроза опухоли (ФНОα) и гранулоцитарно-макрофагальный колониестимулирующий фактор. Пимекролимус и такролимус в равной степени подавляют вторичный иммунный ответ в изолированных клеточных колониях Т-хелперов кожи, полученных у больных с атопическим дерматитом.
Кроме того, in vitro после взаимодействия с комплексом антиген/IgE пимекролимус предотвращает антиген/IgE-опосредованное высвобождение цитокинов и медиаторов воспаления из тучных клеток. Пимекролимус не влияет на рост кератиноцитов, фибробластов и эндотелиальных клеток и, в отличие от кортикостероидов, оказывает селективное действие на клетки иммунной системы и не вызывает нарушений функции, жизнеспособности, процессов дифференциации, созревания клеток Лангерганса мышей и дендритных клеток моноцитарного происхождения у человека. Препарат не оказывает влияния на дифференцировку «наивных» Т-лимфоцитов в Т-эффекторные клетки под действием клеток Лангерганса и дендритных клеток, являющуюся одним из основных механизмов специфического иммунного ответа.
На экспериментальных моделях кожного воспаления была продемонстрирована высокая противовоспалительная активность пимекролимуса после его местного и системного применения. При местном применении на экспериментальных моделях аллергического контактного дерматита (АКД) пимекролимус сопоставим по эффективности с высокоактивными кортикостероидами: клобетазолом-17-пропионатом и флутиказоном, ингибирует воспалительную реакцию в ответ на воздействие кожных раздражителей, не вызывая изменения консистенции и атрофии кожи.
Кроме того, при местном и пероральном применении пимекролимус на экспериментальных моделях АКД эффективно уменьшает кожное воспаление, зуд и выраженность гистопатологических изменений. При местном применении степень проникновения в кожу такролимуса и пимекролимуса одинаково хорошая. Однако способность пимекролимуса проникать через кожу меньше, чем у такролимуса и ГКС . Таким образом, пимекролимус обладает селективным действием на кожу.
Уникальность механизма действия пимекролимуса состоит в сочетании селективного противовоспалительного действия на кожу с незначительным влиянием на системный иммунный ответ.
При применении в течение 6 нед у детей в возрасте от 3 мес до 17 лет пимекролимус эффективно уменьшает зуд и кожное воспаление (эритему, инфильтрацию, экскориацию и лихенизацию). При длительном применении в течение 12 мес пимекролимус эффективно снижает частоту возникновения внезапных обострений АКД, не вызывая атрофии, раздражения и повышения чувствительности кожи, не обладая фототоксическим или фотосенсибилизирующим действием.
Фармакокинетика
У 98% из 40 взрослых больных с исходным поражением 14–62% площади поверхности тела после 1 года лечения кремом Элидел концентрации пимекролимуса в крови оставались на низком уровне и в большинстве случаев были ниже минимальной определяемой концентрации.
У 8 пациентов с содержанием пимекролимуса в крови выше минимальной определяемой концентрации значение AUC составляло 2,5–11,4 нг/мл.
Дети. Фармакокинетические исследования пимекролимуса были проведены у 58 детей в возрасте от 3 мес до 14 лет с атопическим дерматитом (экземой) при поражении 10–92% площади поверхности тела, получавших лечение кремом Элидел 2 раза в сутки на протяжении 3 нед. Пятеро детей получали лечение в течение 1 года по мере необходимости.
У 8 детей в возрасте от 2 до 14 лет с содержанием пимекролимуса в крови выше минимальной определяемой концентрации при трехкратном измерении значение AUC составляло от 5,4–18,8 нг/мл. Значения AUC у пациентов с площадью поражения кожных покровов менее или более 40% были сопоставимы.
В исследованиях in vitro связывание пимекролимуса с белками плазмы (в основном с различными липопротеинами) составило 99,6%.
Поскольку при местном применении концентрации пимекролимуса в крови очень низкие, определение параметров метаболизма не представляется возможным.
Фармакокинетика в особых клинических случаях
Атопический дерматит (экзема) редко наблюдается у больных в возрасте 65 лет и старше. Количество пациентов такого возраста в клинических исследованиях 15% крема Элидел было недостаточным, чтобы выявить какие-либо различия в эффективности лечения по сравнению с молодыми пациентами.
Рекомендации по дозированию для младенцев (3–23 мес), детей (2–11 лет) и подростков (12–17 лет) не отличаются от рекомендаций для взрослых пациентов.
Показания
Атопический дерматит (экзема) — для кратковременного и длительного применения у взрослых, подростков и детей (в возрасте от 3 мес).
Крем для наружного применения от белого до почти белого цвета, гомогенный.
| 1 г | |
| пимекролимус | 10 мг |
Вспомогательные вещества: натрия гидроксид - 0.2 мг, лимонная кислота безводная - 0.5 мг, бензиловый спирт - 10 мг, натрия цетостеарилсульфат - 10 мг, моно- и диглицериды - 20 мг, цетиловый спирт - 40 мг, стеариловый спирт - 40 мг, пропиленгликоль - 50 мг, олеиловый спирт - 100 мг, триглицериды среднецепочечные - 150 мг, вода очищенная - 569.3 мг.
15 г - тубы алюминиевые (1) - пачки картонные.
30 г - тубы алюминиевые (1) - пачки картонные.
Фармакологическое действие
Пимекролимус – производное макролактама аскомицина, обладает противовоспалительным действием. Селективно ингибирует продукцию и высвобождение цитокинов и медиаторов из Т-лимфоцитов и тучных клеток.
Пимекролимус специфично связывается с цитозольным рецептором макрофилином-12 и ингибирует кальцийзависимую фосфатазу - кальциневрин. Ингибирование кальциневрина приводит к подавлению пролиферации Т-лимфоцитов и предотвращает транскрипцию и выработку в Т-хелперах 1 и 2 типа ранних цитокинов, таких как интерлейкин-2, интерферона гамма, интерлейкин-4, интерлейкин-5, интерлейкина-10, фактор некроза опухоли-α и гранулоцитарно-макрофагальный колониестимулирующий фактор. Пимекролимус и такролимус в равной степени подавляют вторичный иммунный ответ в изолированных клеточных колониях Т-хелперов кожи, полученных у больных с атопическим дерматитом.
In vitro пимекролимус также предотвращает антиген/IgE-опосредованное высвобождение цитокинов и медиаторов воспаления из тучных клеток. Пимекролимус не влияет на рост кератиноцитов, фибробластов и эндотелиальных клеток и, в отличие от кортикостероидов, оказывает селективное действие на клетки иммунной системы и не вызывает нарушений функции, жизнеспособности, процессов дифференциации, созревания клеток Лангерганса мышей и дендритных клеток моноцитарного происхождения у человека. Препарат не оказывает влияния на дифференцировку "наивных" Т-лимфоцитов в Т-эффекторные клетки под действием клеток Лангерганса и дендритных клеток, являющуюся одним из основных механизмов специфического иммунного ответа.
На экспериментальных моделях кожного воспаления была продемонстрирована высокая противовоспалительная активность пимекролимуса после его местного и системного применения. При местном применении на экспериментальных моделях аллергического контактного дерматита (АКД) пимекролимус сопоставим по эффективности с высокоактивными кортикостероидами: клобетазолом-17-пропионатом и флутиказоном, ингибирует воспалительную реакцию в ответ на воздействие кожных раздражителей, не вызывая изменения консистенции и атрофии кожи.
Кроме того, при местном и пероральном применении на экспериментальных моделях АКД острого течения пимекролимус эффективно уменьшает кожное воспаление, зуд и выраженность гистопатологических изменений. При местном применении степень проникновения в кожу такролимуса и пимекролимус одинаково хорошая. Однако способность пимекролимуса проникать через кожу меньше, чем у такролимуса и ГКС. Таким образом, пимекролимус обладает селективным действием на кожу.
Уникальность механизма действия пимекролимуса состоит в сочетании селективного противовоспалительного действия на кожу с незначительным влиянием на системный иммунный ответ.
При применении в течение 6 недель у детей в возрасте от 3 месяцев до 17 лет пимекролимус эффективно уменьшает зуд и кожное воспаление (эритему, инфильтрацию, экскориацию и лихенизацию). При длительном применении в течение 12 месяцев пимекролимус эффективно снижает частоту возникновения внезапных обострений АКД, не вызывая атрофии, раздражения и повышения гиперчувствительности кожи, не обладая фототоксическим или фотосенсибилизирующим действием.
Фармакокинетика
У 98% из 40 взрослых больных с исходным поражением 14-62% площади поверхности тела после 1 года лечения Элиделом концентрации пимекролимуса в крови оставались на низком уровне и в большинстве случаев были ниже минимальной определяемой концентрации.
У 8 пациентов с содержанием пимекролимуса в крови выше минимальной определяемой концентрации значение AUC составляло 2.5-11.4 нг×ч/мл.
Фармакокинетические исследования пимекролимуса были проведены у 58 детей в возрасте от 3 до 14 лет с атопическим дерматитом (экземой) при поражении 10-92% площади поверхности тела, получавших лечение кремом Элидел 2 раза/сут на протяжении 3 недель. 5 детей получали лечение в течение 1 года по мере необходимости.
У 8 детей в возрасте от 2 до 14 лет с содержанием пимекролимуса в крови выше минимальной определяемой концентрации при трехкратном измерении значение AUC составляло от 5.4-18.8 нг×ч/мл. Значения AUC у пациентов с площадью поражения кожных покровов менее 40% и более 40% были сопоставимы.
В исследованиях in vitro связывание пимекролимуса с белками плазмы (в основном с различными липопротеинами) составило 99.6%.
Поскольку при местном применении концентрации пимекролимуса в крови очень низкие, определение параметров метаболизма не представляется возможным.
Показания препарата Элидел
Препарат показан для кратковременного и длительного применения у взрослых, подростков и детей (в возрасте от 3 мес).

Медикаментозное средство наружного применения для избавления от кожных заболеваний. Не содержит гормонов, хорошо переносится, разрешено к использованию с раннего возраста.
Состав и форма выпуска
Лекарственный препарат Элидел содержит пимекролимус — вещество, быстро подавляющее воспалительные процессы в тканях кожи без влияния на местный и системный иммунитет. Фактически это — уникальное, не имеющее аналогов соединение избирательного действия, которое справляется с обширными дерматитами и экземами, не нанося вреда организму.
Элидел выпускается в единственной фармацевтической форме — в виде 1-процентного крема, упакованного в металлические тубы по 15 и 30 г. Кроме активного компонента в составе медикамента:
цетиловый, бензиловый, олеиловый, стеариловый спирты;
Тубы с кремом пакуются в картонные коробки, снабжены инструкцией по применению.
Механизм действия препарата
При контакте с кожей помикролимус избирательно блокирует выделение медиаторов воспаления и цитокинов, не подавляя полностью активность иммунную систему и не накапливаясь в тканях, в отличие от гормонов. Элидел не взаимодействует с эндотелиальными клетками, не уменьшает синтез фибробластов и керациноцитов, не вызывает нарушения целостности кожных покровов.
Препарат действует местно, эффективно подавляет воспалительные процессы, препятствует распространению патологии. В системный кровоток вещества крема всасываются в микроскопических дозах, метаболиты Элидела в организме практически не обнаруживаются.
В течение 5–7 дней с начала лечения препарат снимает кожный зуд, жжение, уменьшает покраснения и отеки. Полное излечение воспалительного процесса занимает, в среднем, 2–3 недели.
Лечебное средство не оказывает агрессивного воздействия на ткани, помогает сократить применение глюкокортикостероидов при обширных воспалениях. В некоторых случаях Элидел можно применять в качестве монотерапии длительное время без негативных последствий для организма.
Когда и как нужно использовать Элидел: инструкция
Крем необходимо применять для лечения экзем и дерматитов неинфекционного характера, в том числе атопического. Препарат разрешен для устранения высыпаний на коже у младенцев с 3 месяцев.
Наносить Элидел на пораженные участки рекомендуется не менее 2 раз в сутки: кожу предварительно вымыть и осушить мягкой салфеткой, выдавить и распределить крем тонким слоем, слегка втирая в поверхность до полного впитывания;
для участков кожи 25 см² достаточно около 1 г. средства;
окклюзионных повязок после использования Элидела не требуется;
при необходимости повторять нанесение средства можно чаще.
При острых дерматитах препарат применяют короткими курсами, пока воспаление, жжение и отечность не исчезнут. В случае регулярных или хронических признаках патологии разрешено использовать Элидел в течение длительного времени ежедневно.
Крем подходит лечения любых частей тела, включая кожу шеи и лица, внутренние стороны бедер. Он хорошо справляется с опрелостями у детей и взрослых. Чем раньше начать его использование, тем быстрее удается устранить все неприятные симптомы. При рецидивах дерматитов применять Элидел можно повторно. Рекомендации по терапии для пациентов разного возраста одни и те же. При необходимости разрешено сочетать препарат с гормональными медикаментами.
В период лечения нанесение крема можно совмещать с уходовыми и косметическими средствами, соблюдая перерыв между медикаментом и ими в 15–20 минут. На всем протяжении курса нежелательно подвергать кожу открытым солнечным лучам. Выходя на улицу нужно закрывать очаги поражения одеждой, не посещать солярий, отказаться от посещений пляжей.
Побочные эффекты
В первые дни использования крема вероятно кратковременное усиление жжения, снижение чувствительности кожи. По мере продолжения лечения неприятные ощущения у продаются и проходят. Под воздействием ультрафиолетовых лучей возможно появление пигментных пятен, чрезмерной сухости, шелушения.
При аллергической реакции на крем усиливаются симптомы воспаления, увеличивается местный отек, появляется сильное раздражение.
Противопоказания
Отказаться от терапии кремом Элидел необходимо если:
возраст больного не достиг 3 месяцев;
есть склонность к индивидуальной непереносимости компонентов средства;
в местах предполагаемого нанесения крема есть крупные родинки, вирусные папилломы, повреждения покровов: глубокие царапины, ссадины, трещины или ранки, кожа кровоточит;
дерматит осложнен грибковой, паразитарной или бактериальной инфекцией;
имеются опухолевые процессы.
Элидел нельзя применять при генерализованной эритродермии, выраженном иммунодефицитном состоянии, наносить его на слизистые оболочки. Запрещено мазать на область сосков. В период беременности или лактации препарат разрешен, если отсутствуют патологические признаки и противопоказания к его использованию. Кормящим женщинам во время лечения необходимо наблюдать за поведением ребенка, так как неизвестно, проникают ли частицы крема в грудное молоко, впитываясь в организм с кожного покрова.
В случаях, когда на фоне применения Элидела обнаруживается кожная инфекция, курс прерывают. Возобновить его можно после лечения соответствующими противомикробными препаратами.
Стоимость
Купить Элидел можно в аптечных сетях и заказать в интернет-аптеках. Цена одной тубы крема весом 15 г. варьируется в пределах 800–920 рублей. Упаковка весом в 30 г. стоит от 1300 до 1460 рублей.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
БЕСПЛАТНАЯ КОНСУЛЬТАЦИЯ: поможем врачам и владельцам клиник выбрать оборудование для лечения поствоспалительных дисхромий
Оглавление
Поствоспалительные дисхромии (поствоспалительная гиперпигментация, поствоспалительная гипопигментация) — приобретенные расстройства пигментации, возникающие из-за склонности меланоцитов к избыточному или недостаточному синтезу пигмента, а также вследствие накопления в коже патологического пигмента (например, липофусцина при старении).
В нашей компании Вы можете приобрести следующее оборудование для лечения поствоспалительных дисхромий:
Поствоспалительная гиперпигментация является одним из наиболее распространенных дерматологических состояний, которое чаще развивается на темной коже. В одном из исследований было установлено, что пигментация при акне наблюдается у 65,3% афроамериканцев, 52,7% латиноамериканцев и 47,4% азиатов. Она может возникать в любом возрасте, ей в равной степени подвержены как женщины, так и мужчины.
Что касается гипопигментации, то в одной из работ с участием 423 здоровых людей у 20 (4,7%) был выявлен хотя бы один очаг осветления кожи. Локальное обесцвечивание особенно заметно на темных фототипах кожи вследствие контраста с окружающими здоровыми тканями.
Этиология и патогенез
Поствоспалительные дисхромии могут возникать после перенесенных инфекций, аллергических реакций, механических повреждений кожи, реакций на лекарства, фототоксического дерматита, ожогов и воспалительных заболеваний (системная красная волчанка, атопический дерматит и др.), а также при длительном применении гидрохинона или химических пилингов. Состояние поражений может усугубляться под влиянием ультрафиолета, различных химических веществ и лекарств — тетрациклины, доксорубицин, блеомицин и 5-фторурацил (цитостатики), клофазимин (противотуберкулезный препарат), серебро, золото, противомалярийные препараты, гормоны.
Интересно, что у разных людей под действием одних и тех же факторов может развиваться как гипер-, так и гипопигментация — некоторые специалисты связывают это с тяжестью воспалительного процесса в каждом конкретном случае. Однако есть более глубокая теория, которая называется индивидуальной хроматической склонностью (individual chromatic tendency). Она отталкивается от положения о том, что у каждого человека могут быть «сильные» и «слабые» меланоциты, число и тип которых передаются по наследству. На любое внешнее воздействие «сильные» меланоциты реагируют избыточной продукцией пигмента, что выражается гиперхромией, тогда как «слабые» меланоциты практически перестают синтезировать пигмент, что создает гипохромные участки кожи. При этом «слабые» (лабильные) меланоциты подвержены деструкции, поэтому воспалительный процесс может просто уничтожить их, в результате чего некоторые участки лица и тела станут значительно светлее окружающей кожи.
Что касается поствоспалительной гиперпигментации, то одним из патогенетических механизмов ее развития является избыток на коже сквалена вследствие гиперпродукции себума сальными железами. Попадающее на кожу ультрафиолетовое излучение генерирует в коже синглетный кислород, который под действием сквалена превращается в пероксид сквалена. В свою очередь, он стимулирует выработку простагландина Е2, который запускает меланогенез. Избыточное количество себума вырабатывается, например, при акне — соответственно, при данном заболевании содержание сквалена в поверхностных липидах повышено. Кроме того, в воспалительных очагах процессы окисления протекают особенно активно, поэтому после акне может возникать поствоспалительная гиперпигментация.
В основном поствоспалительная гиперпигментация локализуется в эпидермисе (коричневая пигментация), однако иногда пигмент может захватываться макрофагами и переносится в дерму — в этом случае участок кожи приобретает серовато-голубую окраску. Дермальная пигментация может существовать много лет или даже оставаться на всю жизнь.
Клинические проявления
Различные дерматологические заболевания и состояния с возможными исходами в гипер- или гипопигментацию представлены в табл. 1.
Табл. 1. Возможные исходы дерматологических заболеваний и состояний кожи
Читайте также:

