Дерматиты при диабете на ногах
Обновлено: 25.04.2024
Своевременное выявление и лечение ксероза кожи у больных сахарным диабетом необходимо для предупреждения развития и прогрессирования ряда осложнений, в частности синдрома диабетической стопы.
Основным методом устранения сухости кожи у данной категории пациентов считается применение наружных средств с мочевиной и витаминами, таких как Бальзамед и Бальзамед интенсив. Средства указанной серии получили высокую оценку как врачей, так и пациентов.
- КЛЮЧЕВЫЕ СЛОВА: сахарный диабет, ксероз кожи, нейропатия, синдром диабетической стопы, Бальзамед, Бальзамед интенсив
Своевременное выявление и лечение ксероза кожи у больных сахарным диабетом необходимо для предупреждения развития и прогрессирования ряда осложнений, в частности синдрома диабетической стопы.
Основным методом устранения сухости кожи у данной категории пациентов считается применение наружных средств с мочевиной и витаминами, таких как Бальзамед и Бальзамед интенсив. Средства указанной серии получили высокую оценку как врачей, так и пациентов.
Сахарный диабет (СД) уже многие годы остается значимой медико-социальной проблемой. Он является одной из важнейших причин инвалидизации и смертности. Кроме того, отмечается его высокая распространенность. Так, по данным Международной диабетической федерации (International Diabetes Federation – IDF), в 2017 г. в мире насчитывалось 425 млн страдающих СД, к 2030 г. их количество может достичь 600 млн [1]. Возрастание заболеваемости наблюдается и в нашей стране. Встречаемость СД за последние 15 лет увеличилась более чем в два раза и в настоящее время составляет 2–5% популяции. Согласно данным государственного регистра больных СД, на 31 декабря 2016 г. таковых было 4,35 млн, у 4 млн (92%) диагностирован СД 2 типа. Однако, по мнению экспертов, реальное количество пациентов гораздо больше. Согласно результатам эпидемиологических исследований, не все страдающие СД стоят на учете, у значительной части лиц с метаболическим синдромом и нарушением толерантности к углеводам высок риск развития патологии в ближайшем будущем [2].
Патогенез СД сложен и многофакторен. Инсулинорезистентность, дисфункция бета-клеток поджелудочной железы, наследственность, гиподинамия, неправильное питание обусловливают различные метаболические изменения. Однако одну из ведущих ролей в развитии СД играет оксидативный стресс. Антиоксидантная система организма не способна противостоять этому патологическому процессу.
Вследствие гипергликемии снижается эндоневральный кровоток, нарушается капиллярная проницаемость, увеличивается эндоневральная васкулярная сопротивляемость, уменьшается эндоневральное кислородное напряжение. Это приводит к гипоксии, ухудшению кровоснабжения нервных волокон, нарушению их функции и развитию диабетической нейропатии.
Метаболические изменения, оксидативный стресс, снижение антиоксидантной защиты, микро- и макроангиопатии, нейропатия вызывают осложнения, которые на доклинической стадии практически не диагностируются, а на клинической – лечатся, но с определенными трудностями.
Известно, что одной из первых на происходящие в организме процессы реагирует кожа. Изменение ее состояния может быть одним из признаков развития СД.
Эпидермис состоит из нескольких слоев эпителиальных клеток, которые непрерывно делятся, благодаря чему кожа быстро обновляется. При этом ороговевшие клетки постоянно отшелушиваются. При изменениях в эпидермисе деление эпителиальных клеток и, следовательно, обновление кожи замедляется. На некоторых участках кожа истончается. В результате ее защитные функции снижаются и повышается риск травматизации. На коже кистей и стоп в области максимального трения и давления процесс отшелушивания замедляется, роговой слой утолщается. Снижение скорости клеточного обмена приводит к дефициту натурального увлажняющего фактора. Последний состоит из свободных аминокислот, мочевины и других компонентов, создающих гидролипидную мантию. Кроме того, в норме кожа на 70% состоит из воды. Изменения, ассоциированные с СД, обусловливают ее обезвоживание. При длительно протекающем патологическом процессе появляются шелушение, ощущение стянутости, сухость кожи (ксероз), зуд.
Дерма содержит тонкие пучки эластической ткани, коллагена, мышечных волокон, нервные окончания, сосуды. При СД обновление структур дермы нарушается, кожа теряет эластичность. Снижаются ее тургор, увлажнение и тонус. Вследствие нейропатии и ишемии нарушается функция структур жировой клетчатки – потовых и сальных желез. Меняется кислотность эпидермиса, снижаются барьерные свойства и создаются предпосылки для развития инфекций. Нарушается процесс терморегуляции. Усиливается выпадение волос.
Изменения со стороны кожи, в частности ксероз, у больных СД являются одним из факторов развития синдрома диабетической стопы [3, 4]. Для него характерна определенная стадийность: микротрещины, язвы на стопах, гангрена, остеомиелит. При последних состояниях может потребоваться госпитализация и ампутация конечности [3–8]. Как было отмечено ранее, лечить клиническую стадию и осложнения синдрома диабетической стопы сложно.
Терапевтические и профилактические мероприятия при ксерозе кожи позволяют избежать или отсрочить развитие синдрома диабетической стопы. На начальной стадии ксероза широко применяются наружные средства в виде кремов, бальзамов, увлажняющих препаратов. Результаты сравнительных исследований их эффективности у больных СД оказались противоречивыми. Однако большинство исследователей отдали предпочтение кремам с мочевиной (карбамидом). Мочевина способствует увлажнению кожи, удалению ороговевших частиц.
Более высокий комплаенс отмечен при применении средств серии Бальзамед и Бальзамед интенсив вследствие достаточно быстрого противовоспалительного, увлажняющего и регенерирующего действия [9, 10].
В состав данных средств входят 10%-ная мочевина, витамины А, Е, F, масла авокадо и жожоба, которые улучшают трофику кожи, нормализуют процесс заживления, положительно влияют на микроциркуляцию.
Опыт применения средств Бальзамед и Бальзамед интенсив
Нами оценена эффективность Бальзамеда и Бальзамеда интенсив при лечения ксероза кожи у больного СД.
Пациент 68 лет обратился к врачу общей практики с жалобами на жажду, общую слабость, быструю утомляемость, онемение и зуд в области стоп и голеней после ночного сна и в течение дня, ощущение неуверенности при ходьбе.
Из анамнеза: сахарный диабет 2 типа установлен в 63 года после обращения по поводу учащенного мочеиспускания. Назначены метформин 850 мг/сут и препарат для снижения уровня холестерина. Кроме того, рекомендованы специальная диета, физическая нагрузка, регулярный контроль глюкозы в крови, периодическое посещение врача. Пациент регулярно принимал только метформин, диету не соблюдал, самоконтроль глюкозы в крови не проводил, врача не посещал. Артериальная гипертензия – десять лет, регулярно принимал гипотензивные препараты. Артериальное давление в пределах 140–150/90–95 мм рт. ст., измеряется по требованию – один-два раза в месяц при болях в голове и головокружениях. Максимальные цифры артериального давления – 180/100 мм рт. ст. Больной курит (по пачке сигарет в день), употребляет алкоголь (по несколько раз в месяц). Имеет отягощенный семейный анамнез в отношении артериальной гипертензии по линии отца и СД 2 типа по материнской линии. Аллергологический анамнез не отягощен.
Физикальный осмотр: состояние удовлетворительное. Телосложение гиперстеническое. Ожирение третьей степени (индекс массы тела > 42 кг/м²). Частота дыхательных движений – 18 в минуту. Над всей поверхностью легких ясный легочный звук. Дыхание везикулярное, хрипы отсутствуют. Частота сердечных сокращений – 76 в минуту, пульс ритмичный. Тоны сердца ритмичные. Артериальное давление в положении сидя – 145/95 мм рт. ст. Пульсация на периферических артериях стоп сохранена. Живот мягкий, безболезненный при пальпации. Симптом Пастернацкого отрицательный с обеих сторон. Периферические лимфатические узлы не увеличены. Периферических отеков нет.
Осмотр и оценка состояния кожных покровов и внешнего вида нижних конечностей: кожа нижних конечностей бледная, сухая, шершавая на ощупь, покраснение отсутствует. Эластичность снижена. Патологический кожный процесс симметричный, локализуется на подошвах в области пяток и больших пальцев, представлен гиперкератозом, многочисленными мелкими чешуйками, подчеркнутым кожным рисунком. Мозолей, натоптышей, трещин и язвенных дефектов не обнаружено. Суставы стоп не деформированы. Волосы на голенях отсутствуют. Ногтевые пластины не изменены.
Неврологическое обследование: пациент ориентирован в месте и времени, в отношении текущих и отдаленных событий память не нарушена, внимание значительно снижено. Эмоционально лабилен, неопрятен. Выраженные рефлексы орального автоматизма. Сила в конечностях удовлетворительная. Парезы не наблюдаются. Мышечный тонус несколько повышен в конечностях по пластическому типу. Мышечная атрофия не выявлена. Сухожильные рефлексы умеренной живости в руках (S = D), коленные – торпидные, ахилловы – отсутствуют. Неустойчивость в позе Ромберга. Интенционное дрожание и атаксия при выполнении координаторных проб. Вибрационная чувствительность снижена на больших пальцах обеих ног – 4–5 усл. ед., на обеих лодыжках – 5 усл. ед. Мышечная и суставная (проприоцептивная) чувствительность сохранна. Болевая и тактильная чувствительность снижена: гипестезия в дистальных отделах нижних конечностей по типу носков. Температурная чувствительность сохранна.
Необходимо отметить, что исследование вибрационной чувствительности проводили с помощью градуированного камертона по Рюдель – Сейфферу, частота колебаний – 128 Гц. Рукоятку вибрирующего инструмента поочередно прикладывали к большим пальцам и лодыжкам ног. Для получения достоверных результатов замеры проводили не менее трех раз. Когда пациент переставал ощущать колебания камертона, отмечали показания шкалы. В норме вибрационная чувствительность должна быть более 6 усл. ед.
Проприоцептивная чувствительность определялась в положении лежа с закрытыми глазами. Пациент определял направление сгибания пальцев ног – вверх или вниз.
Поверхностная чувствительность также исследовалась в положении лежа с закрытыми глазами. Чувствительность сравнивалась на симметричных участках в направлении от дистальных отделов к проксимальным. Для оценки болевой чувствительности использовали одноразовую зубочистку, для тактильной – кусочек ваты, для температурной – пробирки с теплой и холодной водой.
Клинический анализ крови: гемоглобин в норме – 120 г/л.
Биохимический анализ крови: глюкоза – 10,2 ммоль/л, гликозилированный гемоглобин – 10%, холестерин – 7,8 ммоль/л, холестерин липопротеинов низкой плотности – 4,5 ммоль/л, липопротеинов высокой плотности – 0,5 ммоль/л, триглицериды – 2,3 ммоль/л.
Общий анализ мочи: уровень глюкозы в пределах нормы, белок – отрицательно.
Электрокардиограмма: ритм синусовый, правильный, гипертрофия левого желудочка.
На основании характера жалоб больного, данных анамнеза, оценки состояния кожных покровов стоп, результатов неврологического обследования и лабораторных исследований поставлен диагноз: инсулиннезависимый сахарный диабет средней степени тяжести c множественными осложнениями (E11.7), диабетическая сенсорная полинейропатия (G63.2), дерматит сухой кожи (L85.8), артериальная гипертензия второй степени второй стадии.
Для лечения ксероза был назначен Бальзамед интенсив. Режим применения: несколько раз в день и на ночь в течение месяца или до клинического улучшения. Кожа предварительно должна быть очищена и обработана пемзой.
Исходя из данных статистики и собственного опыта, у пациентов с СД отмечается низкий комплаенс лечению. Для повышения такового обсуждался возможный риск развития осложнений при отказе больного от лечения, было обосновано назначение средства Бальзамед интенсив. Для профилактики сухости кожи пациента обучили правильному уходу за кожей стоп (гигиене стоп), проинформировали о внешних факторах, способных усилить ксероз кожи: сухость воздуха, особенно в помещении в зимнее время, высокая температура и ультрафиолетовое излучение, горячие ванны, использование щелочных моющих средств, ношение тесной обуви, синтетического белья.
Для оценки эффективности лечения раз в десять дней проводился осмотр кожи стоп.
Кроме того, пациент вел дневник наблюдения.
Положительный эффект лечения отмечался уже через десять дней. Максимальный результат достигнут через 30 дней. Внешне кожа стоп выглядела мягкой, гладкой, увлажненной и эластичной, исчезли чешуйки, сгладился кожный рисунок. В дневнике самоконтроля пациент отметил удобство применения бальзама, приятные ощущения после его нанесения и эффективность.
По окончании лечения для профилактики сухости кожи был рекомендован Бальзамед. В отличие от Бальзамеда интенсив данное средство обладает более легкой текстурой.
Полученные нами результаты согласуются с результатами ряда исследований. В частности, сравнительное исследование эффективности Бальзамеда интенсив и препарата, содержащего мочевину, проводили О.В. Удовиченко и Е.В. Бублик [11]. В исследовании участвовали 45 пациентов с СД 1 и 2 типов, у которых была выявлена сухость кожи стоп. Средний возраст больных – 60 ± 12 лет, длительность заболевания – 13 ± 7 лет. Пациенты были разделены на две группы: первая получала Бальзамед интенсив, вторая – препарат сравнения. Средства наносили два раза в день в течение одного месяца.
Состояние кожи оценивалось при осмотре пяточных областей, выраженность ксероза кожи определялась по шкале Exelbert. Ноль баллов по указанной шкале означает нормальное состояние кожи, один балл – наличие нерезко выраженных чешуек, два балла – множества чешуек, три – небольшого количества многоугольников, четыре – умеренного количества многоугольников, пять – выраженной сети многоугольников, шесть – поверхностных трещин, семь – трещин умеренной глубины, восемь баллов – глубоких трещин (кровоточащие и т.п.). На фоне применения Бальзамеда интенсив проявления ксероза в среднем снизились на 44%, при использовании препарата сравнения – только на 22%.
В исследование Л.С. Кругловой и соавт. было включено 60 пациентов с различными хроническими дерматозами, локализующимися на стопах. Возраст больных варьировался от 12 до 74 лет, в среднем – 42,6 ± 5,7 года. Всем участникам исследования было назначено комплексное лечение в соответствии с медицинскими стандартами. В качестве базовой терапии рекомендован Бальзамед интенсив два раза в день на протяжении одного – полутора месяцев. Для оценки состояния кожи использовали дерматологический индекс шкалы симптомов. С его помощью по трехбалльной системе определяют выраженность таких симптомов, как ксероз, гиперкератоз, десквамация, трещины, эритема, болезненность, зуд.
После наступления клинической ремиссии всем пациентам был рекомендован Бальзамед. Схема применения: четыре раза в день в течение шести месяцев.
По результатам исследования был сделан следующий вывод: средства Бальзамед интенсив и Бальзамед характеризуются высокой терапевтической и профилактической эффективностью. Они восстанавливают водно-липидный барьер и функции кожи [10]. Согласно результатам исследований, а также нашего наблюдения, на фоне применения Бальзамеда интенсив и Бальзамеда развития аллергических и других побочных реакций не выявлено.
Таким образом, средства серии Бальзамед могут быть рекомендованы больным СД для лечения дерматита сухой кожи и регулярного ухода за кожей стоп.
У пациентов с СД большое внимание следует уделять профилактике таких осложнений, как диабетическая нейропатия, синдром диабетической стопы. Для таких больных разработана методика ухода за кожей ног. При первых симптомах сухости кожи рекомендовано наносить средства с мочевиной. К таким средствам, в частности, относятся Бальзамед и Бальзамед интенсив.
Нарастание частоты заболеваемости инсулинзависимым сахарным диабетом (ИЗСД) у детей и подростков требует расширения исследований по профилактическому и раннему выявлению как доклинических стадий сахарного диабета (СД), так и его осложнений, своевременное
Ряд авторов не только признают, что поражение кожи при ИЗСД является наиболее доступным признаком для клинической оценки врачом, но и прослеживают связь между поражением кожи при ИЗСД и такими осложнениями этого заболевания, как нефропатия, нейропатия, ретинопатия, развитие ограничения подвижности суставов (ОПС) — артропатия (хайропатия)
В настоящее время поражение кожи при ИЗСД у детей может быть классифицировано следующим образом: первичное, вторичное и смешанное (сочетанное) поражения кожи; метаболические нарушения кожи; поражение кожи, связанное с лечением ИЗСД
Нарастание частоты заболеваемости инсулинзависимым сахарным диабетом (ИЗСД) у детей и подростков требует расширения исследований по профилактическому и раннему выявлению как доклинических стадий сахарного диабета (СД), так и его осложнений, своевременное обнаружение и лечение которых являются основными факторами, позволяющими предотвратить инвалидизацию и сократить смертность больных. При ИЗСД поражаются все органы и ткани организма, наиболее общим механизмом поражения является формирование диабетической микроангиопатии. Ряд авторов не только признают, что поражение кожи при ИЗСД является наиболее доступным признаком для клинической оценки врачом, но и прослеживают связь между поражением кожи при ИЗСД и такими осложнениями этого заболевания, как нефропатия, нейропатия, ретинопатия, развитие ограничения подвижности суставов (ОПС) — артропатия (хайропатия). Большинство исследований, проведенных в основном у взрослых больных, страдающих как инсулиннезависимым сахарным диабетом (ИНСД), так и ИЗСД, статистически достоверно показывают, что частота встречаемости симптомокомплекса поражения кожи, чаще всего описываемого как «диабетическая дермопатия», возрастает с повышением частоты других специфических осложнений СД. Все исследователи отмечают, что своевременная диагностика и лечение, включающее повышение уровня гликемического контроля, уменьшают проявления осложнений, а на ранних стадиях делают возможным их обратное развитие.
Особенностью кожных покровов ребенка, обусловливающей их повышенную чувствительность к патологическим изменениям, является более тонкий, чем у взрослых, и более рыхлый слой эпидермиса за счет большего содержания воды. Граница между эпидермисом и дермой неровная, связь между ними слабее, чем у взрослых. Дерма имеет преимущественно клеточную структуру, особенно у детей до шести лет; коллагеновые волокна очень тонкие, эластические, слабо развиты, тогда как волокнистая структура у взрослых имеет малое количество клеточных элементов. За счет этих особенностей защитная функция кожи у детей ослаблена — кожа более ранима, склонна к инфицированию (недостаточная кератинизация рогового слоя, его тонкость, незрелость местного иммунитета), эпидермолизу (легкое отделение эпидермиса от дермы), особенно у детей до трех лет. Поверхность детской кожи суше, чем у взрослых, имеет более выраженную склонность к шелушению вследствие физиологического паракератоза и более слабого функционирования железистого аппарата кожи.
Большинство исследователей считают, что поражения кожи при СД встречаются довольно часто, и, учитывая микроскопические изменения, они могут достигать даже 100% при манифестации заболевания. С помощью гистологических и электронно-микроскопических исследований доказано сходство морфологического строения кожи больных СД в возрасте моложе 40 лет и практически здоровых людей старше 60 лет. У них исчезают эластические волокна и активируются фибробласты, отмечаются разрывы коллагеновых пучков, снижение синтеза эластина и полимеризации коллагена при повышении количества коллагеновых белков, глюкозоаминогликанов, структурных гликопротеинов. При этом установлено, что снижение количества эластических волокон на всех стадиях старения кожи обычно предшествует изменениям коллагена.
У детей, в отличие от взрослых, практически не встречаются такие разнообразные, распространенные при СД первичные формы поражения кожи микроангиопатического и макроангиопатического генеза (в связи с резистентностью к инсулину), как генерализованная кольцевидная гранулема (granuloma annulare), папуллезно-роговой дерматоз Карле (hyperkeratosis follicularis et parafollicularis in cutem penetrans), папиллярно-пигментная дистрофия кожи (acanthosis nigricans), эруптивные ксантомы (xantoma papuloeruptivum), склередема (scleredema), кальцифилаксия (calcifilaxia), а также исчезающие гранулемы, резипелоидоподобная эритема, пигментный пурпурный дерматоз, периунгвальные телеангиоэктазии. Также крайне редки у детей и такие вторичные инфекционные поражения, в том числе кожи, как злокачественный наружный отит — тяжелая инфекция, вызываемая Pseudomonas; неклостридиальная газовая гангрена, как правило вызываемая Proteus, Klebsiella, E. coli, Pseudomonas; некротизирующий фасциит — смертельная инфекция, поражающая поверхностную фасцию. Из метаболических нарушений кожи, сопровождающих СД, практически не встречаются у детей гемохроматоз и порфирия.
- классическая — единичные крупные очаги поражения, чаще встречаемые на коже голеней, нередко с изъязвлениями;
- атипичная — с двумя вариантами течения — склеродермоподобным и поверхностно-бляшечным.
Никакое современное лечение, направленное либо на коррекцию углеводного обмена и метаболических нарушений, либо на улучшение микроциркуляции и тканевой резистентности (лазеротерапия, рентгенотерапия, криодеструкция и др.), не позволяет добиться стойких радикальных результатов. В настоящее время большинство исследователей все же рассматривают ЛН как самостоятельное заболевание — хронический дерматоз.
Таким образом, в настоящее время поражения кожи при ИЗСД у детей может быть классифицированы следующим образом:
- первичное, вторичное и смешанное (сочетанное) поражение кожи;
- метаболические нарушения кожи;
- поражение кожи, связанное с лечением ИЗСД.
Первичное поражение кожи — это сосудистые поражения (осложнения) микроангиопатического генеза — структурные и функциональные нарушения в мелких кровеносных сосудах (артериолы, венулы, капилляры). Клинически проявляются эритемой конечностей, внешне напоминающей рожу, иногда с изъязвлениями. Микроскопически характерны утолщение базальных мембран сосудов и пролиферация эндотелиальных клеток. К ним относится диабетическая дермопатия и рубеоз. Собственно диабетическая дермопатия — одна из самых распространенных форм поражения кожи — выражается в образовании множественных бессимптомных двухсторонних атрофических гиперпигментированных пятен, чаще всего на голенях. Их присутствие свидетельствует о возможности микрососудистых изменений в других тканях. Специфическое лечение дермопатии не проводится. Также имеет место рубеоз — розовый оттенок кожи лица у больных ИЗСД, обусловленный функциональной микроангиопатией или повышенным сродством гликированного гемоглобина к кислороду.
Вторичное поражение кожи включает: кожные инфекции — бактериальные и грибковые; неврологические нарушения — сенсорные, моторные и автономные.
Больные СД склонны к развитию инфекционно-воспалительных заболеваний, особенно при неудовлетворительном контроле гликемии. На поверхности кожи больных СД выявляется в 2,5 раза больше микроорганизмов, чем у здоровых лиц, а бактерицидная активность кожи у больных СД ниже, чем у здоровых, в среднем на 20%, и это снижение прямо коррелирует с тяжестью течения СД, в связи с чем при СД, в том числе ИЗСД, часто наблюдаются различные инфекционно-воспалительные и инфекционно-грибковые заболевания кожи. Прежде всего они развиваются на коже нижних конечностей, пораженных нейропатией и ишемией. Это обычно полимикробные инфекции: золотистый стафилококк, гемолитический стрептококк, грамотрицательные аэробные бактерии и множество анаэробов. На ногах, в области мозолей или в других местах трения и нарушения целостности кожи, в области ногтевых лож образуются язвы или нагноения. Инфекция может распространиться на окружающие ткани, вызывая некротизирующий целлюлит, лимфангит, гнойный миозит, некротизирующий фасциит, остеомиелит или даже газовую гангрену (такие исходы распространения инфекции у детей практически не встречаются). Пиодермии, фурункулы, карбункулы, флегмоны, рожа, дерматиты, эпидермофития, кандидомикоз, хронические паронихии и панариции, инфицированная гангрена встречаются у больных СД значительно чаще, чем в популяции. По принятой нами классификации ИЗСД у детей и подростков инфекционно-воспалительные и инфекционно-грибковые заболевания, в том числе кожи, отнесены не к сопутствующим ИЗСД заболеваниям, а к неспецифическим осложнениям ИЗСД, что правомерно, так как распространенность, тяжесть этих поражений, сложность их лечения у детей обусловлена именно наличием ИЗСД. Фурункулез у больных СД протекает тяжело и длительно, а подкожные абсцессы головы могут привести даже к тяжелым поражениям мозга. У взрослых больных СД встречается и гангрена Фурнье, для которой характерно поражение подкожных тканей в области полового члена, мошонки и промежности, реже — стенки живота. Возбудителем этого поражения является смешанная аэробная и анаэробная микрофлора. Микробно-воспалительные процессы при СД могут привести к сепсису. Присоединение инфекционно-воспалительных и грибковых заболеваний кожи, как правило, приводит к тяжелым и длительным декомпенсациям СД и увеличивает потребность организма в инсулине. У лиц с хорошим контролем СД фурункулез и карбункулы встречаются не чаще, чем в популяции здоровых. Из грибковых поражений у детей с ИЗСД наиболее распространены кандидозы, чаще всего вызывающие ангулярные стоматиты, паронихии, вульвовагиниты или баланиты.
Эпидермофитии у детей с ИЗСД довольно редки, но часто осложняются вторичной бактериальной инфекцией. Крайне редки у детей трудно поддающиеся терапии фикомикоз, мукормикоз, при которых в процесс могут вовлекаться мозговые оболочки. У детей с ИЗСД довольно распространены дерматомикозы, особенно стоп и ладоней, кожа которых становится сухой и чешуйчатой.
Широко распространены вторичные нарушения кожи, связанные с неврологической патологией при СД. Среди них: сенсорные нарушения — онемение пальцев ног, постепенно распространяющееся выше, захватывающее стопы, способствующее развитию травматических язвенных поражений, вторичных инфекций и гангрены, особенно при наличии сосудистых изменений; моторные нарушения — слабость межкостных мышц вызывает уплощение стоп с потерей смягчающей функции подошвы стоп; автономные (вегетативные) нарушения — гипергидроз верхней половины тела и сухость кожи нижней части туловища. Эти проявления относятся к диабетической нейропатии, поражающей 5-50% больных СД. У детей с ИЗСД наиболее часто встречается дистальная симметричная сенсорно-моторная полинейропатия с минимальными кожными проявлениями (сухость кожи, гиперкератоз, мозоли, вторичное инфицирование пораженных участков кожи, нарушения роста ногтей), обратимая в фазе начальных проявлений. Именно нейропатия — один из ведущих патогенетических факторов развития в дальнейшем синдрома «диабетической стопы» (ДС). Среди больных СД, осложненным синдромом ДС, частота ампутации нижних конечностей в 15 раз выше, чем у остального населения. При преобладании нейропатических изменений над изменениями периферического кровотока развивается нейропатическая форма ДС, одним из вариантов течения которой является поражение кожи — нейропатическая язва. Она чаще возникает на участках стопы, испытывающих давление, — плантарной поверхности и межпальцевых промежутках. Длительно протекающая сенсорно-моторная нейропатия приводит к деформации стопы с перераспределением и повышением давления на ее отдельные участки. В этих местах отмечается утолщение кожи, гиперкератоз с высокой плотностью. В дальнейшем развивается аутолиз подлежащих мягких тканей с формированием язвенного дефекта, при этом больной может ничего не замечать из-за снижения болевой чувствительности. Язвенный дефект может вторично инфицироваться, в том числе анаэробной микрофлорой, с развитием гипертермии, лейкоцитоза, требующих срочного хирургического лечения с некроэктомией, антибактериальной терапией, улучшением гликемического контроля. У детей все формы ДС встречаются крайне редко, но начальные проявления имеют место в детском возрасте, что требует адекватного обучения, обследования и лечения больных, в том числе прицельного осмотра состояния кожи при ИЗСД.
К смешанному (сочетанному) поражению кожи при СД относятся: утолщение кожи (синдром «диабетической руки» — ОПС с утолщением кожи и склеродермоподобным синдромом), желтый цвет кожи и ногтей, синдром «диабетических пузырей», пруригус и повреждения волос. К нему же следует отнести склеродермоподобные изменения кожи пальцев и тыльной части кистей рук, снижающие их подвижность. Кожа утолщается в области пальцевых суставов и периунгвально. Эти изменения, иногда в сочетании с артропатией (ОПС), описываются некоторыми исследователями как синдром «диабетической руки». Часто с утолщением кожи ассоциируется гиперкератоз. Желтый цвет кожи и ногтей (ксантохромия) ранее связывался с гиперкаротинемией, но сейчас доказано, что при СД в крови сохраняется нормальный уровень каротина. В настоящее время этиология и патогенез не выяснены. Синдром «диабетических пузырей» возникает редко, как правило на коже конечностей. Выявляются одиночные или множественные пузыри, заживающие без рубцевания через две—пять недель. Возможна симптоматическая терапия. Пруригус — поражение кожи в аногенитальной области на фоне кандидоза (гиперемия, трещины, шелушения, вторичное инфицирование). Иногда при плохо контролируемом СД может быть диффузное выпадение, а у больных пониженного питания — избыточный рост волос (лануго) на коже рук и спины. Редко, обычно при плохом уровне гликемического контроля, наблюдаются повышенное шелушение кожи, себорейный дерматит, ихтиозоподобный синдром, особенно в области голеней.
К метаболическим нарушениям кожи при СД относится ксантоматоз, редко встречающийся в детском возрасте и являющийся следствием гиперлипидемии. Клинически ксантоматоз проявляется в виде плотных желтых папул с эритематозным ободком, чаще на кистях, стопах, ягодицах, разгибательных поверхностях верхних и нижних конечностей. Купируется адекватной инсулинотерапией.
Специфическими кожными осложнениями лечения ИЗСД являются липодистрофии, образующиеся в местах инъекций инсулина. Встречаются в виде липом или липогипертрофий (плюс-ткань) и липоатрофий (минус-ткань). В связи с широким применением в настоящее время хорошо очищенных биосинтетических человеческих инсулинов липоатрофии встречаются крайне редко. В настоящее время именно липогипертрофии, или липомы, представляют собой наиболее распространенную проблему для больных ИЗСД, даже при небольшом сроке заболевания. Они возникают в результате некорректной техники введения инсулина (нарушения схем ротаций мест инъекций инсулина, несоблюдение техники и правил введения препаратов), а иногда и без видимых причин; затрудняют абсорбцию и метаболизм инсулина, ухудшают компенсацию заболевания, увеличивают потребность в инсулине, создают косметические дефекты на коже. Кроме вышеописанных правил профилактики липодистрофий, в случае их появления дополнительно и с хорошим эффектом применяется массаж липом, физиотерапия. Также у некоторых больных периодически возникают кровоподтеки в местах инъекций инсулина. Эти места, как правило, теплее на ощупь, чем окружающая кожа.
Обобщая вышеизложенное, можно сказать, что исследование кожи, представляющей собой наиболее доступную неинвазивному клиническому осмотру систему организма, имеет огромное клиническое значение. Знание особенностей поражения кожи у детей при ИЗСД не только помогает в оценке фазы течения заболевания, но и имеет непреходящее значение для решения вопросов о направлении диагностического поиска, коррекции лечения и прогнозе течения ИЗСД.
Диабетическая стопа Cиндром диабетической стопы (СДС) объединяет патологические изменения периферической нервной системы, артериального и микроциркуляторного русла, явления остеоартропатии, представляющие непосредственную угрозу развития я
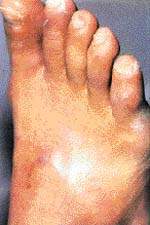 |
| Диабетическая стопа |
Cиндром диабетической стопы (СДС) объединяет патологические изменения периферической нервной системы, артериального и микроциркуляторного русла, явления остеоартропатии, представляющие непосредственную угрозу развития язвенно-некротических процессов и гангрены стопы. СДС — одно из наиболее грозных осложнений сахарного диабета (СД), развивающееся более чем у 70% больных. Несмотря на то что поражение нижних конечностей достаточно редко является непосредственной причиной смерти пациентов, оно в большинстве случаев ведет к инвалидизации. Частота ампутаций конечностей у больных СД в 15 — 30 раз превышает данный показатель в общей популяции и составляет 50 — 70% общего количества всех нетравматических ампутаций. Однако следует особо отметить, что при СД II типа (инсулин-независимом) уже на момент постановки диагноза от 30% до 50% больных имеют признаки поражения нижних конечностей той или иной степени.
Достаточно велики и экономические затраты, необходимые для проведения адекватного лечения этой большой категории пациентов, но следует помнить, что при использовании оперативных методов эти затраты возрастают в 2 — 4 раза. Это связано как с более высокой стоимостью самого хирургического лечения, так и с увеличением затрат на последующую реабилитацию (протезирование, полная потеря трудоспособности). Ампутация одной конечности ведет к возрастанию нагрузки на другую, и, как следствие этого, многократно увеличивается риск развития язвенных дефектов и на контралатеральной конечности.
 |
| Алгоритм обследования больных с синдромом диабетической стопы |
В мировой клинической практике как терапевтов, так и хирургов принята единая классификация синдрома диабетической стопы, согласно которой различают три основные клинические формы:
- нейропатическую;
- ишемическую;
- нейроишемическую (смешанную).
В основу данной классификации положены современные представления о патогенезе СДС и преобладании одного из его основных звеньев (нейропатия, микро- и макроангиопатия) в конкретном клиническом случае. Каждая клиническая форма СДС требует различных терапевтических подходов.
Одним из проявлений диабетической нейропатии является диабетическая остеоартропатия. Наиболее выраженные изменения костных структур и связочного аппарата стопы называются суставом или стопой Шарко. Кроме собственно сустава Шарко выделяют и другие формы костно-суставных поражений при СД: остеопороз, гиперостоз, остеолиз, патологические переломы и спонтанные вывихи. На практике наблюдаются различные сочетания вышеуказанных форм у одного и того же пациента, что связано с общностью их патогенетических и реализующих факторов. Учитывая этот момент, многие авторы предлагают объединить разновидности патологических изменений костей и суставов под термином «стопа Шарко».
Для раннего выявления поражения нижних конечностей у больных СД необходимо проведение определенного комплекса диагностических мероприятий, состоящих из следующих этапов.
1. Тщательный сбор анамнеза. Имеют значение длительность заболевания, тип СД ( I тип или II тип), проводимое ранее лечение, а также наличие у больного на момент осмотра или ранее таких симптомов нейропатии, как колющие или жгущие боли в ногах, судороги в икроножных мышцах, чувство онемения, парастезии. Жалобы больного на перемежающуюся хромоту являются характерным признаком макроангиопатии. Учитываются время появления болей, расстояние, которое больной проходит до появления первых болей, наличие болей в покое. В отличие от ишемических болей, которые могут также возникать ночью, нейропатически обусловленный болевой синдром купируется при ходьбе. Ишемические боли несколько ослабевают при свешивании ног с края постели. Наличие в анамнезе язв или ампутаций является важным прогностическим признаком в плане развития новых поражений стоп. При имеющихся других поздних осложнениях СД, таких как ретинопатия и нефропатия (особенно ее терминальная стадия), высока вероятность развития язвенного дефекта. Наконец, при сборе анамнеза необходимо определить информированность больного о возможности поражения стоп при СД, ее причинах и мерах профилактики.
2. Осмотр ног — наиболее простой и эффективный метод выявления поражений стопы. При этом важно обратить внимание на такие признаки, как цвет конечности, состояние кожи и волосяного покрова, наличие деформаций, отеков, участков гиперкератоза и их расположение, язвенных дефектов, состояние ногтей, особенно в межпальцевых промежутках, зачастую остающихся незамеченными. Пальпаторно определяется пульсация на артериях стопы.
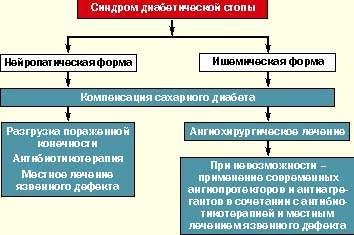 |
| Алгоритм лечения больных с различными клиническими формами синдрома диабетической стопы |
3. Оценка неврологического статуса включает:
а) Исследование вибрационной чувствительности, проводимое с помощью градуированного камертона. Для нейропатического поражения характерно повышение порога вибрационной чувствительности, для ишемической — показатели соответствуют возрастной норме.
б) Определение болевой, тактильной и температурной чувствительности по стандартным методикам. В последние годы большую популярность приобрели неврологические наборы монофиламентов, позволяющих с большой степенью точности определить степень нарушения тактильной чувствительности.
в) Определение сухожильных рефлексов.
г) Электромиография является наиболее информативным методом оценки состояния периферических нервов, однако ее применение ограничено из-за трудоемкости и высокой стоимости исследования.
4. Оценка состояния артериального кровотока. Наиболее часто используются неинвазивные методы оценки состояния периферического кровотока — допплерометрия, допплерография. Проводится измерение систолического давления в артериях бедра, голени и стопы — по градиенту давления определяется уровень окклюзии. Показатели лодыжечно-плечевого индекса (ЛПИ) отражают степень снижения артериального кровотока (ЛПИ = РАГ/РПА, где PАГ — систолическое давление в артериях стоп или голеней, PПА — систолическое давление в плечевой артерии). Показатели систолического давления и ЛПИ определяют дальнейший ход диагностического поиска. При необходимости проводится определение насыщения тканей кислородом, а для решения вопроса о возможности проведения ангиохирургического лечения — ангиография. Показатели систолического давления могут служить определенным ориентиром в плане возможности консервативного лечения, они также позволяют прогнозировать вероятность заживания язвенных дефектов стоп.
 |
| Диабетическая стопа: рентгенограмма |
5. Рентгенография стоп и голеностопных суставов позволяет выявить признаки диабетической остеоартропатии, диагностировать спонтанные переломы мелких костей стопы, заподозрить наличие остеомиелита, исключить или подтвердить развитие газовой гангрены.
6. Бактериологическое исследование имеет первостепенное значение для подбора адекватной антибиотикотерапии.
В группу риска развития СДС входят следующие категории пациентов:
- страдающие дистальной полинейропатией;
- страдающие заболеваниями периферических сосудов;
- имеющие язвы стоп в анамнезе;
- перенесшие ампутации;
- страдающие гипертонией и гиперхолестеринемией;
- слабовидящие и слепые;
- страдающие диабетической нефропатией, особенно на стадии ХПН;
- одинокие пожилые люди;
- злоупотребляющие алкоголем, курильщики.
Пациенты, входящие в группу риска, должны проходить указанные выше обследования не реже одного раза в шесть месяцев. Обследование должно проводиться специально обученным эндокринологом или группой специалистов (эндокринолог, хирург, рентгенолог, специалист функциональной диагностики) в поликлиниках по месту жительства. Больные, имеющие различные клинические формы синдрома диабетической стопы, должны направляться в специализированные отделения стационаров или в центры «Диабетическая стопа», организованные на базе городских многопрофильных больниц и специализированных центров. Тактика лечения каждого конкретного больного определяется в зависимости от формы и тяжести СДС, наличия других осложнений СД и сопутствующих заболеваний.
Таблица 1. Дифференциальная диагностика основных клинических форм синдрома диабетической стопы
В случае нейропатической формы СДС должно проводиться консервативное лечение больного с использованием разгрузки пораженной конечности (постельный режим, костыли, кресло-каталка, ношение специальной разгрузочной обуви), массивной антибиотикотерапии (с учетом данных бактериологического исследования отделяемого), проводимой до полной эпителизации дефекта, ежедневного местного лечения язвенного дефекта, включая хирургическую обработку раны с удалением гноя и некротических масс, орошением растворами антисептиков, применением современных перевязочных средств (в зависимости от стадии раневого процесса). Лечение проводится под строгим контролем гликемии с ежедневной коррекцией дозы инсулина и пероральных сахароснижающих препаратов. Большинству больных СД I типа требуется интенсификация инсулинотерапии, а больным СД II типа — перевод с приема таблетированных препаратов на инсулинотерапию. При наличии диабетической остеоартропатии в комплекс лечебных средств включаются препараты кальция, витамина Д, бифосфонаты.
При ишемической форме СДС предпочтение должно отдаваться современным методам сосудистых реконструкций для восстановления нормального кровотока в поврежденной конечности. Лечение таких больных должно проводиться совместно ангиохирургом и эндокринологом. В случае невозможности проведения оперативного лечения рекомендуется медикаментозная терапия (ангиопротекторы в эффективных дозах, вазапростан). Абсолютно необходимым является поддержание хорошей компенсации сахарного диабета.
В случае диагностики нейроишемической (смешанной) формы синдрома диабетической стопы должна проводиться комплексная терапия, влияющая на оба патогенетических звена.
Вопросы реабилитации особенно важны для больных, перенесших ампутации пальцев или части стопы по поводу диабетической гангрены, а также для пациентов с выраженными деформациями стоп. Для таких больных в обязательном порядке должны изготавливаться ортопедическая обувь и другие ортопедические приспособления.
Диспансерное наблюдение за больными с нейропатической формой синдрома осуществляется районными эндокринологами или специалистами кабинетов и центров «Диабетическая стопа». Наблюдение за пациентами с ишемической и смешанной формами синдрома должно осуществляться совместно эндокринологами и ангиохирургами центров «Диабетическая стопа» или профильных отделений городских больных. Профилактика развития поражений стоп при СД обязательно должна включать обучение пациентов правилам подбора обуви и ухода за ногами.
Проведение лечебных и профилактических мероприятий по приведенному плану позволяет снизить риск ампутации конечности у больных СД в два и более раза.
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
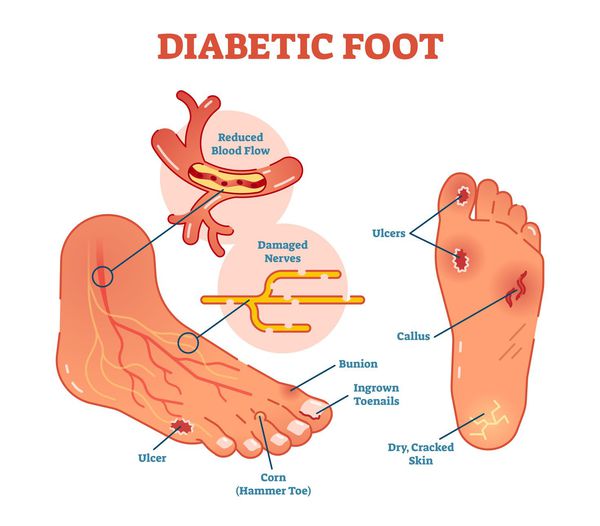
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
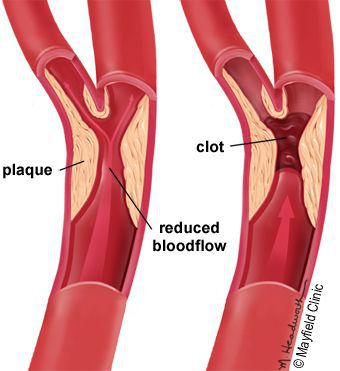
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
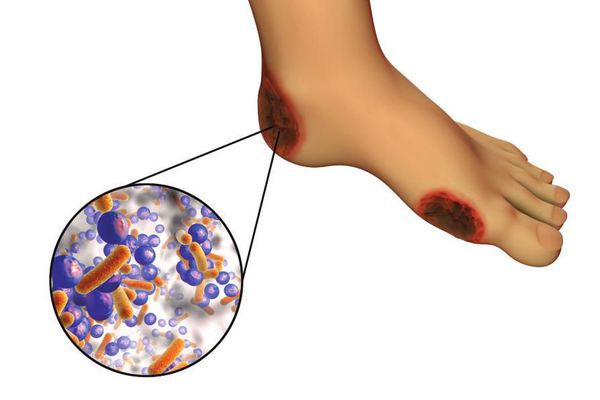
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
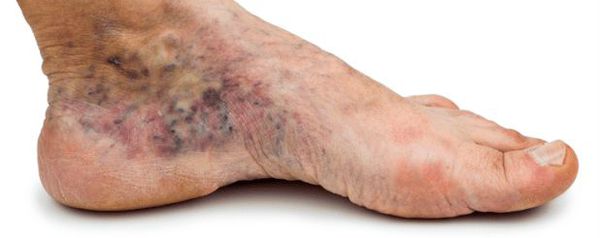
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
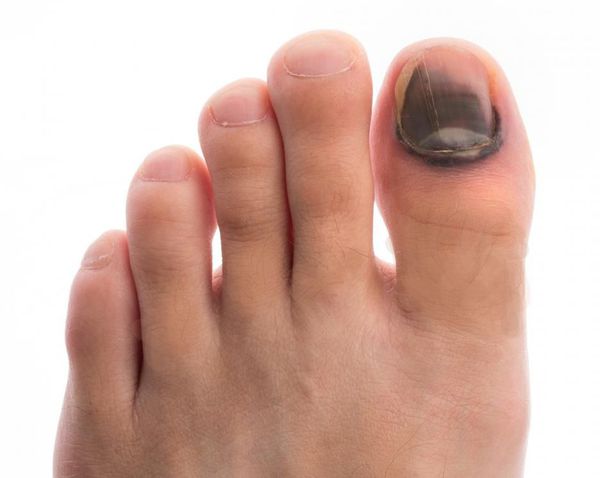
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
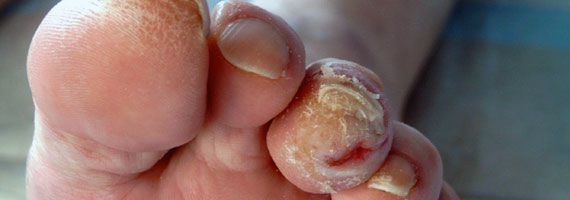
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
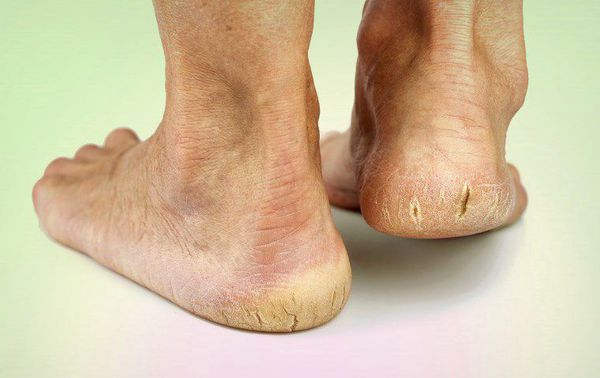
- трофические язвы, длительно не заживающие на стопах.
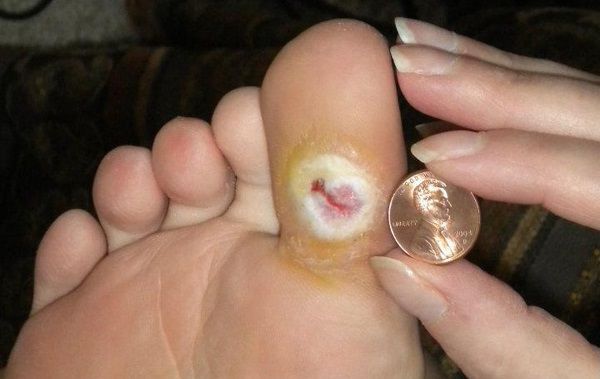
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
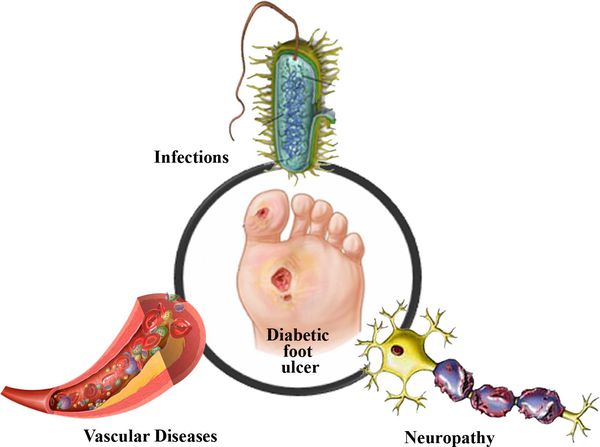
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
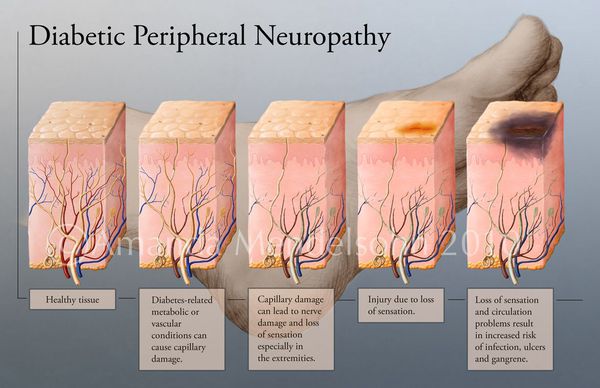
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
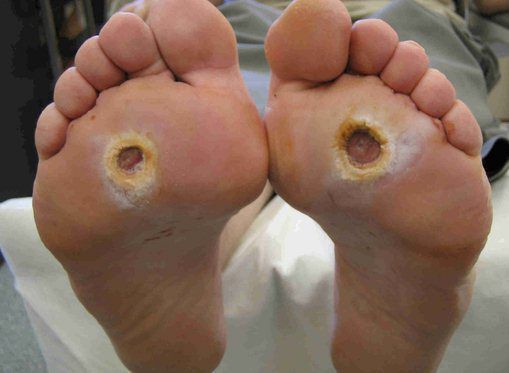
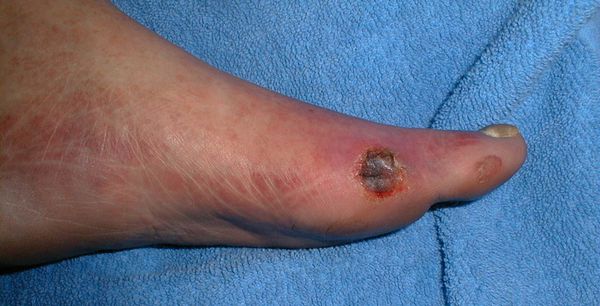
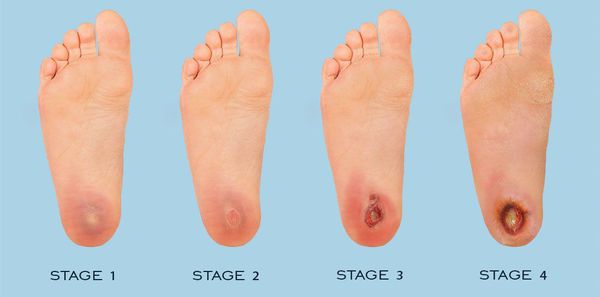
Классификация Вагнера
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения
Российский государственный медицинский университет
ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова», Москва, Россия, 117997
Хроническая экзема у пациентки с сахарным диабетом 2-го типа, ассоциированная с инфекцией, обусловленной Klebsiella spp.
Журнал: Клиническая дерматология и венерология. 2017;16(5): 12‑15
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения
Различные формы экземы могут осложняться вторичной инфекцией. Описано выявление S. aureus, Str. faecalis, Str. pyogenes, Candida. В литературе представлены результаты многочисленных исследований развития экземы при сахарном диабете (СД). Показано значительное распространение аллергических заболеваний у пациентов от 4 до 18 лет с СД 1-го типа. Патологические изменения сосудов и нарушения иммунного статуса могут приводить к возникновению и развитию экземы при СД 2-го типа. В статье представлено описание хронической экземы у пациентки, страдающей СД 2-го типа и другими тяжелыми коморбидными состояниями. Интерес данного случая заключается в выявлении Klebsiella spp. в очагах поражения при хронической экземе. Обсуждаются различные патологические состояния, когда была выявлена Klebsiella. Высказывается предположение, что инфицирование Klebsiella spp. способно значительно затруднить терапию хронической экземы при СД.
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения
Российский государственный медицинский университет
ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова», Москва, Россия, 117997
В настоящее время накоплен обширный материал по обнаружению сопутствующей инфекции при разных формах экземы [1—5]. Наибольшее количество исследований было проведено при микробной экземе. При обострении заболевания возрастает частота идентификации грибов преимущественно в ассоциации со S. aureus, Str. faecalis, Str. pyogenes при практически неизмененной микробиоте кожи [2]. Представлены особенности течения дерматоза, осложненного кандидозом [3]. При обследовании пациентов с микробной экземой в очагах поражения отмечен значительный рост грамположительных микроорганизмов, представленных бактериями рода Staphylococcus, в меньшей степени Streptococcus. Плотность грамотрицательных бактерий в зоне поражения значительно возрастала. Численность грамотрицательных палочек также увеличивалась. Показано, что патогенные микроорганизмы S. aureus и S. pyogenes вытесняют представителей нормальной микробиоты, что свидетельствует об участии патогенной микрофлоры в патологическом процессе [4]. Перифокальная варикозная экзема нередко ассоциируется с микотической инфекцией [5].
В литературе [6—8] представлены описания многочисленных исследований по клиническим проявлениям экземы у пациентов, страдающих сахарным диабетом (СД). Показано значительное распространение аллергических заболеваний у пациентов в возрасте от 4 до 18 лет с СД 1-го типа [9]. Распространенность экземы у пожилых лиц с СД и при его отсутствии существенно не различается в возрастной группе от 65 лет [10]. В то же время патологические изменения сосудов и нарушения иммунного статуса могут приводить к возникновению и развитию экземы при СД 2-го типа [11].
Представляем клиническое наблюдение развития осложненной хронической экземы у пациентки, страдающей СД 2-го типа.
Пациентка К., 75 лет, обратилась с жалобами на высыпания на коже нижних конечностей, сопровождающиеся сильными болями и постоянным интенсивным зудом в местах высыпаний.
Считает себя больной в течение 2 лет, когда впервые без видимой причины отметила появление высыпаний на коже туловища, ног. В течение 13 лет наблюдалась флебологом по поводу хронической лимфовенозной недостаточности. Двадцать лет назад выявлен СД 2-го типа, на период обращения эндокринолог по месту жительства оценивал это заболевание как средней степени тяжести в состоянии компенсации. Кроме того, в последнее время наблюдалась по поводу ожирения II степени, эутиреоза, диффузного узлового зоба, нефросклероза смешанного генеза, диабетической полинейропатии, деформирующего остеоартроза коленных суставов, хронической болезни печени (III стадия), цереброваскулярной болезни (хроническая ишемия головного мозга сложного генеза), дорсопатии вне обострения, пресбиопии слабой степени, осложненной катарактой, ангиопатии сетчатки обоих глаз, хронической венозной недостаточности III степени. Сенсибилизацию к пищевым продуктам и лекарственным препаратам не отмечала.
По поводу высыпаний на коже обращалась к дерматологу по месту жительства: диагностирована экзема, рекомендованы наружные средства для применения в амбулаторных условиях. В дальнейшем периодически отмечала обострения кожного процесса, получала лечение амбулаторно и стационарно. Настоящее обострение — в течение 1 мес. В связи с отсутствием эффекта от проводимого амбулаторного лечения была госпитализирована.
Патологический процесс на коже носит распространенный островоспалительный характер. Очаги локализуются на коже туловища, ног (преимущественно в средней и нижней трети). Высыпания полиморфны, представлены округлыми папулами ярко-красного цвета до 0,2 см в диаметре, эритематозно-сквамозными очагами с нечеткими границами и очертаниями, в пределах которых отмечаются точечные и линейные экскориации, эрозии, покрытые серозно-геморрагическими и серозно-гнойными корочками, линейные трещины, очаги мокнутия. На коже ног расположены симметричные участки отечно-инфильтрированной застойной эритемы с участками индурации и фиброза синюшно-багрового цвета, в пределах которых отмечаются эрозивные дефекты, массивные рыхлые серозно-геморрагические корки, очаги рубцовой атрофии (рис. 1); на левой голени — эрозивно-язвенные дефекты от 3 до 6 см в диаметре (рис. 2). Дермографизм смешанный. Видимые слизистые чистые. Выражена отечность в области голеностопных суставов. Отмечает болезненность крупных и мелких суставов верхних и нижних конечностей при активных и пассивных движениях.

Рис. 1. Пациентка К. до лечения.

Рис. 2. Очаги поражения пациентки К. до лечения.
Диагноз клинический: «хроническая распространенная экзема, стадия обострения (простой раздражительный контактный дерматит, причина не уточнена, L24.9). Вторичная инфекция (импетигинизация других дерматозов Д01.1)».
Данные лабораторной диагностики. В общем анализе крови отмечено повышение СОЭ до 36 мм/ч. В анализе мочи лейкоцитов 5—8 в поле зрения. Основные биохимические показатели в пределах нормы. Уровень гликемии натощак и после нагрузки: в 8:00 — 5,9 ммоль/л, в 11:00 — 6,8 ммоль/л.
Проведено бактериологическое исследование отделяемого эрозивно-язвенных дефектов на условно-патогенную микрофлору воспалительных процессов: идентифицирована Klebsiella spp., чувствительная к цефуроксиму, цефтриаксону, эритромицину, азитромицину, левофлоксацину, мупироцину, фузидиевой кислоте.
В соскобе с кожи стоп патогенные грибы не обнаружены.
— 2% раствор пентоксифиллина 5,0 + раствор актовегина 5,0 + раствор натрия хлорида 200,0 внутривенно капельно № 10;
— раствор цефтриаксона 1 г внутримышечно № 10 (после курса азитромицина);
— 30% раствор тиосульфата натрия 10,0 внутривенно струйно № 10;
— раствор баралгина внутримышечно № 5 (по требованию).
— азитромицин 500 мг 2 раза в день курсом 5 дней (перед курсом цефтриаксона);
— клемастина гидрофумарат (тавегил) 1 мг 1 раз в день;
— полиметилсилоксана полигидрат (энтеросгель) 1 столовая ложка;
— комбинированный препарат, содержащий алкалоиды белладонны + фенобарбитал + эрготамин (Alcaloida belladonnae + Phenobarbitalum + Ergotaminum) (беллатаминал) 2 раза в день.
— влажно-высыхающие повязки с 2% водным раствором ихтиола 2 раза в день на голени;
— 1% раствор метиленового синего на экскориации, трещины, на очаги на туловище;
— мазь, содержащую 0,64 мг бетаметазона дипропионата;
— 30 мг салициловой кислоты (акридерм).
За 3 нед, проведенные в стационаре, эрозивно-язвенные дефекты эпителизировались, большинство высыпаний регрессировали до поствоспалительных пятен (рис. 3). При выписке зуд отсутствовал, болевые ощущения значительно уменьшились, сохранялась незначительная инфильтрация очагов поражения, свежих высыпаний не отмечали.

Рис. 3. Очаги поражения пациентки К. после проведенного лечения.
Таким образом, в приведенном нами наблюдении хроническая экзема протекала на фоне тяжелой коморбидной патологии. Интерес данного случая заключается в выявлении Klebsiella spp. в очагах поражения при хронической экземе.
Klebsiella относится к семейству Enterobacteria-ceae. Эти грамотрицательные палочки являются факультативными анаэробами, способны образовывать капсулу, благодаря которой устойчивы в окружающей среде. В клинической практике известны различные поражения, обусловленные клебсиеллами. Так, при ангиоматозе кожи со вторичными кишечными изъязвлениями у 63-летней пациентки была обнаружена Klebsiella pneumoniae [12]. Данный возбудитель нередко обладает резистентностью ко многим лекарственным препаратам (РМЛП).
При обследовании взрослых 235 пациентов, приехавших в Швейцарию или наблюдавшихся в других странах, у 43 (18%) обнаружена РМЛП. У 42 (98%) пациентов были обнаружены грамнегативные возбудители, в большинстве случаев Escherichia coli и K. pneumoniae [13]. С другой стороны, K. pneumoniae оказалась на втором месте после Streptococcus agalactiae среди причин неонатального сепсиса на Гаити [14]. K. rhinoscleromatis является возбудителем риносклеромы, эндемичной для Египта [15]. У пациентов, страдающих СД, описаны различные патологические состояния, обусловленные клебсиеллами. В частности K. pneumoniae, продуцирующая карбапенемазу, при колонизации прямой кишки рассматривается как фактор риска, увеличивающий летальность пациентов с инфицированной диабетической стопой [16]. K. oxytoca с пониженной чувствительностью к хлоргексидину была обнаружена в материале с поверхности язвы при диабетической стопе [17].
В представленном нами наблюдении Klebsiella spp. обнаружена в экзематозных очагах у пациентки с СД 2-го типа и тяжелой коморбидной патологией. Процесс на коже носил распространенный характер, очаги поражения на коже туловища наиболее соответствовали клинической характеристике идиопатической экземы, процесс на нижних конечностях — варикозной экземе. Для достижения терапевтического эффекта потребовалось последовательное назначение двух антибиотиков (азитромицин и цефтриаксон). В результате проведенной терапии было достигнуто улучшение состояния, но полного регресса не наблюдалось. По-видимому, инфицирование Klebsiella spp. способно значительно затруднить терапию хронической экземы при СД.
Представляется целесообразным изучение частоты инфекций, обусловленных клебсиеллами, и разработка методов лечения пациентов, страдающих экземой и СД.
Читайте также:

