Что у человека больше кожа или кишечник
Обновлено: 04.05.2024
В чем заключаются трудности диагностики гельминтозов? Какова терапия гельминтозов? На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов
В чем заключаются трудности диагностики гельминтозов?
Какова терапия гельминтозов?
На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов (болезни адаптации), постоянного стресса, повышения уровня образованности и культуры населения многие давно известные заболевания человека изменили свою клиническую картину. Некоторые симптомы практически перестали встречаться, другие, наоборот, стали выходить на первый план. Это относится и к заболеваниям, вызываемым гельминтами, в частности, круглыми паразитическими червями (нематодами). В умеренном поясе наиболее широко распространенные нематоды — аскарида и острицы.
Гельминты могут вызывать нарушения функции желудочно-кишечного тракта (ЖКТ), быть причиной аллергических (или псевдоаллергических) реакций или усугублять их, вызывать интоксикацию, а также быть фактором, ослабляющим иммунитет [2]. В настоящее время редко встречаются случаи массивной инвазии, когда диагностика не вызывает затруднений, а клубки гельминтов вызывают обтурации кишечника, — значительно чаще гельминты стали являться причиной развития аллергических проблем. При этом гельминтозы относятся к тем заболеваниям, которые трудно диагностировать в связи с объективными и субъективными трудностями (длительные периоды отсутствия яйцекладки, возможность отсутствия среди паразитирующих особей самок, вероятность технических ошибок). Поэтому важно знать клиническую картину данных заболеваний, чтобы иметь возможность назначать углубленное обследование или эффективную терапию по совокупности косвенных признаков, даже не имея прямых доказательств наличия гельминтоза.
С целью оценить клиническую картину при нематодозах проанализированы жалобы, анамнез и результаты осмотра 150 детей, у которых были обнаружены аскариды (116 детей), острицы (27 детей), аскариды и острицы (7 детей). Гельминты выявлены стандартными методами: обнаружение яиц аскарид в фекалиях методом мазка или яиц остриц в соскобе на энтеробиоз, а также визуальное обнаружение аскарид или остриц в фекалиях, рвотных массах или при оперативном или эндоскопическом вмешательстве в брюшной полости или в области прямой кишки [3].
Среди детей было 67 мальчиков, 83 девочки. Распределение по возрасту представлено в табл. 1. Преобладали дети младшего дошкольного возраста (от одного до трех лет), их количество составило 63%. Именно в этом возрасте — наибольшие эпидемиологические предпосылки появления нематодозов.
У 150 детей с доказанными инвазиями аскаридами и/или острицами отмечались следующие клинические проявления.
У 107 детей (71,3%) были аллергические проблемы: кожные высыпания, диатез, атопический дерматит, нейродермит — у 99 (66%), из них у 18 эти проблемы носили периодический характер, у двух детей, кроме кожных высыпаний, отмечались конъюнктивиты; у десяти (6,7%) отмечалась доказанная пищевая аллергия на какие-то продукты с высоким уровнем специфических IgE в сыворотке крови; у шести детей (4%) отмечался астматический компонент или был установлен диагноз бронхиальная астма.
У 113 детей (75,3%) отмечались нарушения функции желудочно-кишечного тракта: неустойчивый стул, непереваренный стул, наличие в кале «зелени», слизи — у 66 (44%); запоры или склонность к запорам — у 55 (36,7%), у 17 детей (11,3%) отмечался неустойчивый стул со склонностью к запорам, т. е. периоды нормального или разжиженного стула чередовались периодами запоров; метеоризм, проявляющийся повышенным газообразованием, вздутием живота, урчанием, отрыжками, проявлялся у 30 детей (20%); тошнота, рвота, регургитация отмечались у 29 детей (19,3%).
У 60 (40%) детей, которые по возрасту могли пожаловаться на боли в животе, отмечался болевой абдоминальный синдром: чаще всего отмечались так называемые «летучие боли», которые возникали независимо от еды, периодически, как правило, без конкретной локализации или локализованные вокруг пупка (в параумбиликальной зоне). Такие боли проходили сами по себе без медикаментов или на фоне приема сорбентов, спазмолитиков, некоторым детям нужно было какое-то время полежать; болевой синдром такого характера отмечался у 54 детей (36%). У восьми детей (5,3%) боли в животе носили постоянный характер, часто были связаны с едой (возникали после еды), были интенсивными, часто требовали медикаментозного лечения и госпитализации для исключения острой хирургической патологии; одному ребенку была проведена по этому поводу аппендэктомия, и в аппендиксе с катаральными изменениями обнаружены аскариды; у двух детей отмечался болевой абдоминальный синдром обоих типов.
У 66 детей (44%) отмечались нарушения аппетита: у 54 (36%) аппетит был чаще снижен или избирательный; у 12 (8%) — повышен (ребенок постоянно хочет есть). Часто на вопрос об аппетите родители отвечали «когда как», т. е. были периоды нормального аппетита и снижения или повышения аппетита. В оценке данного показателя не обходится без большой доли субъективности, т. к. родители по-разному оценивают аппетит своих детей.
Бруксизм (скрежетание зубами) — симптом, который часто связывается с глистными инвазиями, но фактически является неспецифическим признаком интоксикации центральной нервной системы и может сопровождать любые хронические интоксикации — отмечался у 25 детей (16,7%).
Нарушения ночного сна отмечались у 81 ребенка (54%): беспокойство к вечеру, затруднения засыпания — у 15 детей (10%); беспокойный ночной сон (вскрикивания, постанывания, метания во сне, пробуждения, плач, бессонница, кошмарные сновидения) — у 76 (50,7%). Некоторые родители старших детей затруднялись охарактеризовать ночной сон ребенка, т. к. ребенок спит в другой комнате. Проблемы с засыпанием и ночным сном — важный симптом глистных инвазий, т. к. известно, что кишечные нематоды (в том числе аскариды и острицы) часто активизируются именно ночью.
У 54 детей (36%) отмечались зуд и/или покраснения в области заднего прохода (анальная эскориация) — у 43 детей (28,7%); зуд — у 38 (25,3%); оба симптома — у 27 (18%). Анальная эскориация и зуд считаются симптомами энтеробиоза (острицы), но при этом из 54 детей, у которых отмечались данные симптомы, энтеробиоз был доказан у 17 детей (31,5% от числа детей с этими симптомами). У других 37 детей (68,5% от числа детей с данными симптомами) было доказано наличие аскаридоза, но ни визуально, ни в анализах не были обнаружены острицы. Это может свидетельствовать либо о том, что в данных случаях присутствовали острицы, которые не были диагностированы, т. е. гельминтоз был смешанным, либо о том, что анальная эскориация и зуд — симптомы, характерные не только для энтеробиоза, но и аскаридоза.
У 29 детей (19,3%) отмечались признаки общего ослабления иммунитета: часто или длительно болеющие дети (по общепринятой классификации Monto J. et al., 87) — 18 детей (12%); рецидивирующие стоматиты, гингивиты отмечались у 13 детей (8,7%); кариес зубов — у шести (4%); рецидивирующие гнойные заболевания кожи или слизистых — у трех (2%).
У 15 детей (10%) имелись результаты исследования иммунного статуса по крови: у 13 детей было снижено количество Т-клеток; у всех 15 детей было снижено количество Т-хелперов, причем у шести из них — существенно; у 12 детей было снижено хелперно-супрессорное соотношение; у семи детей отмечалось снижение уровня IgA (секреторный иммуноглобулин), в том числе у трех — существенное, у остальных же восьми детей уровень IgA в сыворотке крови был либо нормальным, либо повышенным; у шести детей отмечалось снижение количества лимфоцитов, в том числе у одного ребенка была выраженная лимфо- и нейтропения. Эти результаты подтверждают известные данные о том, что аскариды и острицы угнетающе влияют на функции иммунитета, а также что у людей с ослабленным иммунитетом большая вероятность появления гельминтоза [1].
У 49 детей (32,7%) отмечались различные симптомы, которые также можно связать с воздействием гельминтов на организм: «географический» язык — у 12 детей (8%); отставание в физическом развитии, недостаточная прибавка в весе или похудание за какой-то период времени — у 21 ребенка (14%); болезненный вид (синева под глазами, бледность) выявлен при осмотре у семи детей (4,7%); неприятный запах изо рта, особенно по утрам, отмечался у десяти детей (6,7%); повышенная утомляемость, астенический синдром — у восьми детей (5,3%); эмоциональная лабильность, капризность, раздражительность ребенка — у четырех (2,7%), причем этот показатель субъективен, как и оценка родителями аппетита; гиперсаливация — еще один симптом, который обычно ассоциируют с гельминтозами, отмечался у трех детей (2%); различные проявления гиповитаминозов, в том числе рахит — у пяти детей (3,3%). Нередко при осмотре выявлялись изменения кожного покрова в виде «гусиной кожи».
У большинства детей отмечалось более одного симптома. Обобщенные данные по клинической картине представлены в табл. 2.
Терапия во всех случаях состояла из двух этапов: сначала — антигельминтная терапия, причем назначались два разных препарата (декарис и вермокс) с интервалом три — пять дней между ними, чтобы максимально охватить различные стадии жизни гельминтов; через некоторое время после антигельминтной терапии — препараты для микробиологической и функциональной коррекции. Соответственно оценивались результаты противоглистной терапии, результаты всего лечения, а также катамнез в течение шести месяцев после терапии. В большинстве случаев улучшение наступало быстро в процессе лечения. У 36 детей только после антигельминтной терапии существенно уменьшились или полностью исчезли аллергические проявления, у 39 детей после первого этапа терапии нормализовалась работа ЖКТ, у 41 ребенка сразу прекратились боли в животе, по остальным симптомам также наступало улучшение после противоглистных препаратов. Это подтверждает то, что симптомы были вызваны наличием гельминтов.
У 92 детей после всего лечения не было никаких жалоб; о 37 нет данных об изменениях состояния в процессе и после лечения; у 16 детей эффект был неполным, т. е. какие-то симптомы сохранялись и после окончания лечения; у четырех детей эффект от терапии оказался нестойким, поскольку возникли рецидивы после окончания лечения; у трех детей эффекта от терапии не было.
От состояния желудочно-кишечного тракта зависит не только характер пищеварения, но и внешний вид кожных покровов. Если кишечник функционирует некорректно, то происходит накопление токсических веществ, которые образовались в процессе переваривания пищи. Данный процесс чреват развитием аутоинтоксикации организма, которая в свою очередь влияет на внешний вид кожных покровов. Бесполезно прибегать к косметическим методам, если первопричиной неудовлетворительного состояния кожи является неудовлетворительное состояние желудочно-кишечного тракта.
Почему кишечник и кожа взаимосвязаны?
Организм человека представляют собой единую сложную систему, поэтому кожа и ЖКТ связаны. Если происходят структурно-функциональные изменения в пищеварительной системе, то человек может столкнуться с такими вероятными кожными проявлениями:
- сухость кожи и снижение её эластичности;
- прыщи и угревая сыпь (акне);
- кожная пигментация.
Сбой в работе желудочно-кишечного тракта может проявляться одним из перечисленных симптомов или их совокупностью. Если человек замечает неудовлетворительное состояние кожи, то ему рекомендована консультация не только дерматолога, но и гастроэнтеролога.
Какие заболевания кишечника приводят к ухудшению состояния кожи
Негативно отразится на состояние кожных покровов могут такие отклонения со стороны желудочно-кишечного тракта:
- синдром раздражённого кишечника;
- неспецифический язвенный колит;
- проктосигмоидит;
- хронические запоры;
- синдром мальабсорбции;
- хронический гастрит.
Кроме того, одной из наиболее распространенных причин появления проблем с кожей, является дисбактериоз. При нарушении баланса кишечной микрофлоры нарушается процесс всасывания питательных компонентов и витаминов, а также снижается иммунитет, что априори негативно отражается на состоянии кожных покровов. Послужить причиной развития кишечного дисбактериоза и других заболеваний кишечника, могут такие факторы, как нерациональное питание, злоупотребление алкоголем, преобладание в рационе однотипной пищи и продуктов, которые богаты простыми углеводами. Очень часто проблемы с кожей на фоне дисбактериоза кишечника возникают при прохождении антибиотикотерапии, так как эта группа препаратов не обладает избирательным воздействием, и уничтожает как отрицательную так и положительную микрофлору.
Как распознать проблемы с ЖКТ
Обнаружив у себя кожные дефекты, угревую сыпь, пигментные пятна и другие негативные изменения на коже, необходимо обратить внимание на наличие симптомов, которые указывают на сбой в работе желудочно-кишечного тракта. Во внимание берется набор таких клинических симптомов:
- дискомфорт и боль в правой или левой подвздошной области, а также вокруг пупка;
- повышенное газообразование в кишечнике (метеоризм);
- расстройства стула (чередование запоров и диареи);
- боль в подложечной области;
- отрыжка кислым;
- присутствие фрагментов слизи, гноя или крови в испражнениях.
Кишечник и зуд кожи также взаимосвязаны. Кроме ранее перечисленных кожных проблем, которые развиваются на фоне структурно-функциональных изменений в системе пищеварения, расстройства пищеварительной деятельности могут приводить к появлению симптомов местной аллергической реакции. К симптомам аллергической реакции можно отнести сыпь по типу крапивницы, покраснение кожных покровов, шелушение кожи, зуд, отёчность. Прием противоаллергических препаратов поможет снять только симптомы аллергии, но не решит проблему в полной мере, так как аллергические реакции, связанные с некорректной работой ЖКТ необходимо лечить комплексно.
Диагностика
Если возникли высыпания на коже, кишечник должен быть комплексно осбледован. Комплексная диагностика включает такие методы исследования:
- ультразвуковое исследование органов брюшной полости;
- копрограмма;
- лабораторный анализ на дисбактериоз;
- колоноскопия.
В качестве дополнительных методов обследования может быть назначен общий и биохимический анализ крови.
Лечение
Добиться эффекта оздоровления кожи можно только через здоровый кишечник. При заболеваниях кишечника, которые спровоцировали проблемы с кожей, могут быть назначены такие группы лекарственных медикаментов:
- Противовоспалительные препараты в форме таблеток, капсул и ректальных суппозиториев.
- Спазмолитики. Эта группа лекарственных средств является своего рода скорой помощью, к которой прибегают для снятия спазмов в кишечнике.
- Энтеросорбенты. Кишечные сорбенты назначаются для очищения кишечника от токсических компонентов и продуктов метаболизма.
- Пробиотики. Эта группа средств назначается при дисбактериозе и синдроме раздраженного кишечника для восстановления микрофлоры кишечника.
- Пребиотики. Назначаются чаще в комбинации с пробиотиками, так как представляют собой питательную среду для кишечных бактерий.
Улучшить состояние желудочно-кишечного тракта и соответственно кожных покровов помогает прием метапребиотика Стимбифид Плюс. Метапребиотик содержит фруктополисахариды, фруктоолигосахариды, а также лактат кальция. Каждый компонент по отдельности и все в комбинации создают максимально благоприятные условия для роста и размножения нормальной кишечной микрофлоры. Даже лучший пребиотик не создаст того эффекта стимуляции роста кишечных бактерий, который обеспечивает метапребиотик.
В отличие от пробиотиков, которые являются уязвимыми перед кислотной средой желудка и не в полном объеме попадают в кишечник, метапребиотик Стимбифид Плюс эффективно восстанавливает популяцию собственных бактерий в кишечнике человека. По мере восстановления нормального баланса кишечных бактерий будет улучшаться состояние кожи и произойдет ее общее оздоровление. Стимбифид Плюс может быть использован как при уже возникших дерматологических проблемах, так и для профилактики заболеваний кожных покровов. Чистый кишечник – здоровая кожа, и этот факт подтвержден как гастроэнтерологами, так и дерматологами.
С ростом интереса к лечению природными средствами, растёт и популярность пробиотиков. В 2012 г. почти 4 млн взрослых американцев принимали пробиотики или пребиотики, что в 4 раза превышает показатель 2007 г. Пробиотики использовали в более чем 50 000 случаях госпитализации в 139 американских лечебных учреждениях в 2012 г. В одном только прошлом году американские потребители потратили, по приблизительным расчётам, 2,4 млрд долларов на пищевые добавки.
Однако недавно были опубликованы два исследования, в которых учёные из Израиля задаются вопросом: действительно ли столь широкое применение пробиотиков с целью улучшения общего самочувствия и восстановления микрофлоры кишечника после применения антибиотиков целесообразно.
Первое исследование показало, что бактерии из пробиотические микроорганизмы, содержащиеся в пищевой добавке, не способны колонизировать надлежащие отделы кишечника, и, предположительно, они могут миновать ЖКТ без всякого на него влияния. В другом исследовании, те же бактерии поселялись в кишечнике после курса антибиотиков, однако при этом наблюдалась задержка восстановления собственной микробиоты. Оба исследования, проведённые на здоровых добровольцах, были опубликованы в журнале Cell в октябре 2018 года.
Термин «пробиотики» означает «живые микроорганизмы, которые при их введении в адекватной дозе, способствуют полезны для здоровья организма-хозяина». Однако некоторые эксперты заявляют, что любые доказательства пользы, ограниченны незначительным количеством показаний, являются спорными, а их качество зачастую неудовлетворительно. Проведённый в 2018 г. Кокрановский анализ показал, что в данные 10 из 14 систематичного обзоров клинических исследований, были недостаточными для определения того, чтобы установить улучшают ли пробиотики состояние ЖКТ.
Казалось бы, что лучше дела должны обстоять у пациентов с диареей. Несмотря на то, что многие исследования свидетельствуют о том, что прием пробиотиков может предотвращать или лечить антибиотико-ассоциированную диарею и инфекцию Clostridium difficile, в других исследованиях (как детей, так и взрослых) не было отмечено эффектна при этих состояниях. Два последних, наиболее актуальных исследования, опубликованных в конце предыдущего года в журнале New England Journal of Medicine, не показали эффективности пробиотиков Lactobacillus rhamnosus для детей с гастроэнтеритом или желудочным гриппом.
Среди учёных и практикующих врачей, использующих бактериальную терапию, такая неопределённость «вызвала крайне большую путаницу», как заявляет Эран Элинав (Eran Elinav), доктор медицинских наук, профессор Института имени Вецмана в Реховоте (Израиль), ведущий автор нового исследования в опубликованного в Cell.
Оценка колонизации
В 2015 г. Элинав со своим коллегой Эраном Сегалом (Eran Segal), специалистом в области вычислительной биологии, продемонстрировали, что одна и та же пища может по-разному влиять на сахар крови у различных лиц, не страдающих диабетом, что частично зависит от микрофлоры их кишечника.
Эти учёные разработали метод прогнозирования пиков глюкозы в крови после приёма пищи, основанный на широком наборе клинических и лабораторных показателей, в т. ч. микробиоты стула. Прогнозируемуые изменения глюкозы в крови использовали для разработки персонализированного режима питания, способствующего снижению пиков глюкозы крови после приёма пищи. Впоследствии, данный подход зарегистрировали в качестве инновации в области питания.
Элинав и Сегал, в своей последней работе, предполагают, что наиболее эффективным средством восстановления микрофлоры кишечника является тот, который является персонализированным. В своём новом исследовании они, вместе с Замиром Хальперн (Zamir Halpern), главным терапевтом гастроэнтерологического института при медицинском центре Сураски в Тель-Авиве (Израиль), вновь рассмотрели основные вопросы, которые, как им кажется, они в недостаточной мере осветили в своих предыдущих работах: в какой степени пробиотики колонизируют кишечник человека и какой эффект они на него оказывают?
В первом исследовании девятнадцать здоровых добровольцев принимали либо представленную на рынке пробиотическую добавку с 11 штаммами, либо плацебо дважды в день в течение 4 недель. По словам Элинав, добавка включала 4 основных рода бактерий, используемых в пробиотиках по всему миру.
Не полагаясь только на исследования кала (что являлось обычной практикой при исследованиях кишечной микрофлоры), учёные также изучили участки на всём протяжении ЖКТ, как до, так и во время курса пробиотиков. С помощью колоноскопии и глубокой эндоскопии верхних отделов пищеварительного тракта учёные собрали пробы содержимого и слизистой оболочки кишечника, а также провели биопсию его ткани. Затем, пробы подвергли тщательному генетическому секвенированию для определения состава микробиоты, её фунционирования и экспрессии генов клеток кишечника организма-хозяина
Пробы оболочки кишечника, отобранные спустя 3 недели после начала курса пробиотиков, показали, что субъектов, принимавших антибиотики, можно разделить на 2 лагеря: «восприимчивых» и «резистентных». Восприимчивые добровольцы продемонстрировали значительное содержание пробиотических штаммов в оболочке кишечника, тогда как в кишечниках резистентных добровольцев значительной колонизации выявлено не было. У восприимчивых лиц также отмечали изменения индигенного микробиома и профиля экспрессии генов по всей длине кишечника, чего не отмечали у резистентных субъектов, а также в группе плацебо.
По словам Колин Келли (Colleen Kelly), врача-гастроэнтеролога и профессора Медицинской школы Уоррена Альперта Брауновского Университета, не привлечённой к данному исследованию, данная работа первой продемонстрировала, что у некоторых людей слизистая оболочка кишечника резистентен к пробиотической колонизации, «где и происходит всё действие».
Исходная естественная микробиом кишечника добровольцев во многом определяет, будут ли они восприимчивы или резистентны к пробиотикам. Интересно отметить, что в пробах кала не было обнаружено подобной разницы: как у восприимчивых, так и у резистентных субъектов выявили сравнимое количество пробиотических бактерий, причём большее количество бактерий было обнаружено в стуле добровольцев, получавших плацебо.
Согласно Элинав, данные результаты позволяют предположить, что «наш текущий подход к пробиотикам, вероятно, неправильный». Такая вариабельность между индивидуумами означает, что некоторые люди могут выиграть от приёма пробиотиков, а другие — нет.
Такой результат не удивителен, заявляет Роб Найт (Rob K, доктор наук, руководитель Инновационного микробиома при Университете Калифорнии (г. СанДиего), не принимавший участия в исследовании. Он отметил, что разные люди по-разному реагируют на те же самые продукты питания, лекарственные средства и патогены. «Это распространяется и на полезные организмы», — сказал он относительно данного исследования и добавил, что в предшествующей работе была выявлена аналогичная вариабельность.
Среди врачей и общественности сложилось мнение, что употребление внутрь «хороших» бактерий может вытеснить «плохие» бактерии и улучшить состояние кишечника даже у здорового человека. В большинстве опубликованных до сих пор клинических исследований на здоровых добровольцах не было выявлено значительных изменений микрофлоры кишечника. С публикацией исследования Института Вейцмана, заявление о пользе пробиотиков вызывает ещё больше сомнений, чем когда-либо. Келли говорит: «Идея того, что люди принимают пробиотики только для улучшения общего самочувствия может быть пустой тратой денег».
После антибиотиков
В своём втором исследовании учёные рассмотрели, что происходит в кишечнике, когда человек принимает пробиотики после курса антибиотиков. Двадцать один здоровый доброволец прошёл лечение антибиотиками широкого спектра (ципрофлоксацин и метронидазол) в течение одной недели. После чего они либо в течение 4-х недель, дважды в день принимали ту же добавку, что и в первом исследовании, либо аутологичный трансплантат фекальной микробиоты, представляющий образец собственной микрофлоры субъектов до приема антибиотиков, взятый с помощью эндоскопии верхней части ЖКТ, либо ничего и составляли группу контроля.
На этот раз никто из субъектов, принимавших пробиотики не был резистентен к колонизации. Антибиотики убили большую часть естественного микробиома, что позволило экзогенным штаммам распространиться. Однако за это пришлось заплатить: естественные бактерии кишечника восстанавливались в течение более длительного периода в группе, принимавшей пробиотики, по сравнению с группой контроля. Возврат к исходному показателю экспрессии генов клеток кишечника организма-хозяина также подавлялся в группе пробиотиков в течение шестимесячного периода последующего наблюдения.
Александр Хоруц (Alexander Khoruts), врач-гастроэнтеролог и руководитель медицинской программы по кишечной микрофлоре Университета Миннесоты, не принимавший участия в исследовании, заявил, что был удивлен, что пробиотики продемонстрировали вообще сколь-нибудь явный эффект, даже столь незначительный. Он отметил: «Я не ожидал, что эти микробы были активны настолько, чтобы повлиять на восстановление микробиома».
В основном, Хоруц занимается пациентами с инфекцией, вызванной C. difficile и с трудом поддающейся лечению, и едва ли не все его пациенты заявляют, что принимали пробиотики. Хотя он и не спорит с ними, а лишь подталкивает к употреблению большего количества ферментируемых продуктов питания, Хоруц всё же говорит, что доказательства, подтверждающие пользу применения пробиотиков, слабее, чем многие думают. «В своём литературном обзоре (хотя многие могут с ним не согласиться), я не обнаружил никаких убедительных доказательств, по меньшей мере в отношении инфекции C. difficile, о каком-либо положительном влиянии приёма пробиотиков», — заявляет врач.
Одним из значительных недостатков является очевидная нехватка рандомизированных исследований, предоставляющих данные по безопасности пробиотиков — именно эту тему поднимает системный обзор, представленный в журнале Annals of internal medicine.
Несмотря на результаты исследования Института Вейцмана, до сих пор неизвестно действительно ли приём пробиотиков во время или после курса антибиотиков замедляет восстановление естественного микробиома, и могут ли подобные пертурбации вызвать проблемы. Состав пробиотиков различен и, согласно Найту, исследователи вводили чрезвычайно высокую дозу. К тому же, дизайн исследования не включал анализ клинических результатов.
Тем не менее, длительные нарушения после курса антибиотиков связаны с рядом проблем со здоровьем, в т. ч. с инфекциями, ожирением, аллергией и хроническими воспалениями, заявляет Элинав. По его мнению, длительные нарушения, вызванные пробиотиками, исследованием которых занималась его команда, «потенциально могут привести к долгосрочным побочным эффектам у потребляющих их лиц».
Найт отмечает, что исследование проводили на здоровых добровольцах, которым вводили антибиотики только для целей научного исследования. В действительности же люди принимают антибиотики, страдая от какого-либо заболевания. Замедлят ли пробиотики восстановление естественной микрофлоры кишечника в этом случае?
«В этом исследовании абсолютно не рассматривается данный вопрос», — говорит Найт. — «В нём обсуждают введение антибиотиков здоровым субъектам, ситуация с которыми может в корне отличаться от клинической популяции пациентов».
Хоруц полагает, что ущерб от приёма большинства пробиотиков, вероятно, будет минимальным. Однако для него «и этого вполне достаточно, чтобы прекратить их назначение и задуматься над тем, чему верить. Полагаю, лечащий врач должен обладать здоровой степенью скептицизма в отношении заявлений, которые делают касательно подобных продуктов».
Применение результатов
Как и Хоруц, Келли занимается пациентами с инфекцией C. difficile, лечение которых затруднительно. В прошлом она советовала им принимать пробиотики, если лечение включало антибиотики. Ныне она стала сомневаться в таком подходе: «Правильно ли я поступаю? Выписывая им пробиотики, не замедляю ли я восстановление естественных бактерий?» Аналогично Найту, она полагает, что для окончательного решения вопроса необходимо провести исследование на клинической популяции. В настоящее время Американская гастроэнтерологическая ассоциация рекомендует «в целом, воздержаться от неизбирательного применения пробиотиков».
Тем не менее, в исследовании был и светлый момент. У субъектов, которым их собственную микрофлору пересаживали с помощью аутологичного фекального трансплантата, микрофлора возвращалась к состоянию до приёма антибиотиков и исходному профилю экспрессии генов клеток кишечника в течение нескольких дней, «что доказывает эффективность персонализированного подхода к вмешательству в микрофлору», — отмечает Элинав
Однако размножение аутологичной фекальной микробиоты может стать проблемой: необходимо собрать образцы, когда человек ещё здоров, и после хранить его в течение неограниченного срока. Но в этом случае, можно будет создать персонализированный банк пробиотических бактерий с индивидуально подобранными характеристиками.
Элинав полагает, что в не столь отдалённом будущем станет возможным использовать алгоритмы машинного обучения для индивидуального подбора специфических пробиотических штаммов для пациента на основании исходной микробиоты кишечника и профиля экспрессии генов, что повысит шансы оказания клинического эффекта пробиотиками. Так как вероятно, что универсальную пробиотическую колонизацию отмечают только после курса антибиотиков, такой подход применим только к лицам, не принимающим антибиотики.
Элинав также отмечает в результатах позитивный момент касательно торможения пробиотиками восстановления микрофлоры после антибиотиков. Почему бы не использовать комбинацию антибиотиков и пробиотиков для перезапуска экосистемы кишечника и, в идеале, лечения заболеваний, связанных с микрофлорой (например, воспаления кишечника), и даже ожирения? «Полагаю, это крайне перспективный и интересный аспект, требующий дополнительных исследований», — заявляет учёный.
Синдром недостаточности пищеварения или синдром мальдигестии не является редким явлением в современном мире. Одной из главных причин нарушения пищеварения принято считать недостаточную выработку пищевых ферментов, которые расщепляют компоненты пищи. Это состояние сопровождается выраженными клиническими проявлениями, которые заставляют человека обратиться за медицинской помощью.
Характеристики состояния
Синдром мальдигестии обусловлен функциональной недостаточностью поджелудочной железы, желудка или кишечника. Независимо от степени вовлеченности одного из органов пищеварительной системы, данное состояние приводит к нарушению процесса всасывания нутриентов, включая витамины и минералы. За короткий промежуток времени, расстройства пищеварения вызывают потерю массы тела, ухудшение состояния кожи и волос, негативно отражается на иммунитете человека, и провоцирует обострение любых хронических заболеваний.
Кроме того, остатки непереваренной пищи (химус) являются благоприятной средой для размножения болезнетворных организмов, с последующим развитием тяжелого кишечного дисбактериоза и аллергических реакций.
Несмотря на то, что существует отдельная (инволютная) форма мальдигестии, связанная с возрастными изменениями в организме пожилых людей, чаще всего с этим состоянием сталкиваются люди молодого и среднего возраста.
Причины развития
Одной из главных причин развития данного состояния является нарушение работы желудка или кишечника, а также поджелудочной железы с уменьшением продукции пищеварительных ферментов. К другим потенциальным факторам развития синдрома недостаточности пищеварения, можно отнести:
Нарушение процесса желчеобразования и желчевыделения.
- Замедление кишечной перистальтики.
- Дисбактериоз кишечника.
- Эндокринные патологии.
Синдром недостаточности пищеварения условно делится на полостную, пристеночную и внутриклеточную мальдигестию. Полостная мальдигестия развивается при таких состояниях, как муковисцидоз, хроническое воспаление поджелудочной железы, а также после операций на данном органе. Снижение функциональности ферментов, ответственных за расщепление компонентов пищи, наблюдается при хроническом гастрите. Кроме того, развитию мальдигестии способствует язва желудка и синдром раздраженного кишечника, при котором наблюдается нарушение транзита химуса. Пристеночное пищеварение нарушается в том случае, если наблюдается повреждение клеток эпителия кишечника (энтероцитов). Повреждение эпителия кишечника наблюдается при целиакии, болезни Крона, а также при энтеритах различной этиологии.
Непереваренные остатки пищи, которые остаются длительное время в просвете кишечника провоцируют не только развитие дисбактериоза, но и приводят к образованию токсических компонентов (скатол, аммиак, индол), которые оказывают местнораздражающий эфеект и повреждают слизистую оболочку кишечника.
Клинические симптомы
Распознать расстройства кишечника при мальдигестии можно по таким характерным клиническим признакам:
-
(метеоризм).
- Расстройства стула (диарея).
- Урчание в животе.
- Боль в околопупочной области.
- Тошнота.
- Отрыжка с неприятным запахом.
Кроме того, для мальдигестии характерны такие симптомы, как общая слабость, частичная или полная утрата аппетита, а также снижение массы тела. У пациентов с мальдигестией наблюдается увеличение объема испражнений, при этом меняется их цвет и запах. В испражнениях наблюдается маслянистые включения (стеаторея). Синдром недостаточности пищеварения очень часто протекает в комбинации с непереносимостью лактозы (молочного сахара) или других пищевых компонентов.
При тяжелом течении, у пациентов с синдромом мальдигестией резко ухудшается общее состояние, нарушается процесс всасывания биологически-значимых компонентов и развивается мальабсорбция. На фоне данного состояния снижается масса тела, у женщин могут пропадать менструации, наблюдается ухудшение состояния кожи, волос и ногтей.
Лечение
Одним из главных условий правильного и результативного лечения мальдигестии является коррекция рациона. Из ежедневного меню исключают те продукты, которые плохо переносятся организмом. Питание усиливают продуктами, богатыми белком, углеводами и микроэлементами, при этом жиры урезают до минимума. Также, из меню исключают сырые фрукты и овощи. Стандартная терапия синдрома недостаточности пищеварения включает приём медикаментов, содержащих пищеварительные ферменты. Перестальтика кишечника восстанавливается с помощью приёма медикаментов из группы регуляторов моторики.
Для восстановления структурно-функционального состояния ЖКТ при мальдигестии и лечения дисбактериоза целесообразно использовать метапребиотики, которые бережно и эффективно нормализуют баланс кишечной и желудочной микрофлоры, подавляют рост и развитие болезнетворных микроорганизмов, а также восстанавливает поврежденный эпителий желудочно- кишечного тракта. Метапребиотик Стимбифид Плюс содержит фруктополисахариды и фруктоолигосахариды, которые являются ценным питательным субстратом для кишечной и желудочной микробиоты. Кроме того, Стимбифид Плюс дополнен лактатом кальция, стимулирующим рост и размножение полезных кишечных бактерий.
Комбинация из перечисленных компонентов позволяет добиться эффекта быстрого, безопасного и полного восстановления пищеварительной системы, пострадавшей от мальдигестии. Рациональное питание и приём метапребиотика Стимбифид плюс с профилактической целью, позволит избежать дисбиоза кишечника, расстройств пищеварительной деятельности и тяжелых осложнений, развивающихся на фоне синдрома недостаточности пищеварения. Метапребиотик может быть использован в любом возрасте.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Прыщи на лице: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
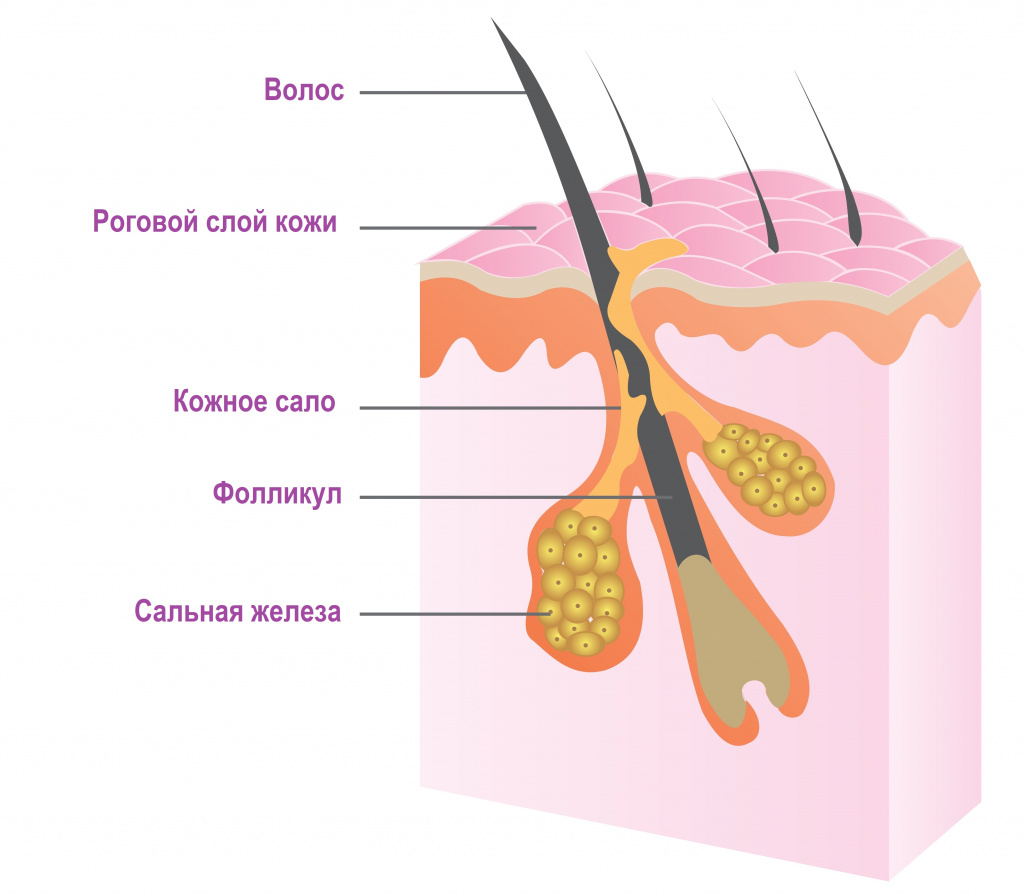
Сальные железы в коже человека располагаются у основания волосяного фолликула. Они продуцируют кожное сало, которое увлажняет кожу и защищает от негативного влияния окружающей среды, бактерий и грибов. Гиперсекреция сальных желез провоцирует формирование прыщей (акне, угрей). На лице они чаще всего локализуются в местах расположения крупных сальных желез (на лбу, висках, щеках, на носу и подбородке).
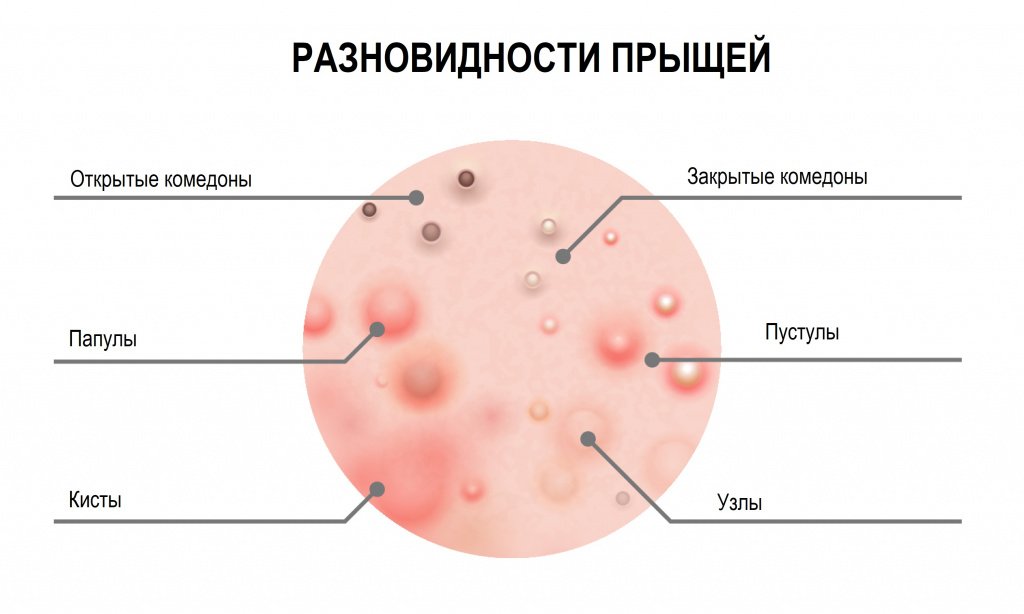
Разновидности прыщей на лице
В самом общем виде прыщи относятся к одному из двух типов:
Невоспалительные элементы (комедоны) – выглядят как небольшие бугорки или точки различного цвета. Комедоны могут быть открытыми или закрытыми.
- Открытые комедоны выглядят как плотные высыпания поверхностного типа, обычно серого или черного цвета, который придает им окислительная реакция их содержимого с кислородом.
- Закрытые комендоны, подкожные прыщи (милиумы) имеют вид белых бугорков или точек, похожих на маленькие крупинки проса. Скопившееся кожное сало не имеет выхода наружу, что приводит к болезненному воспалению. Закрытые комедоны чаще превращаются в классические красные прыщи.
- Папулы (красные прыщи) представляют собой воспалившиеся комедоны без явного гнойного содержания. Имеют вид мелких красных или розовых шариков, выступающих над поверхностью кожи, белой головки нет. Если папула сформировалась на месте открытого комедона, то сквозь кожу часто можно разглядеть темную пробку.
- Пустулы – это инфицированные папулы или, проще говоря, прыщи с гнойным содержимым и белой головкой, окруженные воспаленной кожей. Они появляются, когда помимо кожного сала и бактерий в поры попадают омертвевшие клетки кожи. По форме пустулы бывают конусообразными, плоскими или сферическими. Их цвет может варьировать от белого до желтого или зеленого.
Зеленый цвет означает присоединение вторичной инфекции, и при самостоятельном выдавливании велика вероятность ее проникновения в кровь.
Кистозные прыщи тяжело поддаются лечению и всегда оставляют на коже заметные следы.
Возможные причины появления прыщей на лице
Итак, прыщи появляются как результат избыточной продукции кожного сала, которое закупоривает кожные поры. Если пора закрыта частично и в нее есть доступ воздуха, начинается образование прыщей. Сначала они выглядят как черные точки, окруженные воспаленной кожей, – так называемые угри. В полностью закупоренной поре, как в контейнере, быстро размножаются анаэробные бактерии (Propionibacterium acnes или Malassezia), провоцирующие воспалительный процесс и нагноение.
Но что заставляет сальные железы работать столь активно? Считается, что одна из причин кроется в высоком уровне андрогенов (мужских половых гормонов), которые стимулируют выработку кожного сала. Развитию гиперандрогении могут способствовать проблемы пищеварения, стрессы, болезни почек и надпочечников, эндокринной и половой системы.
Важно упомянуть, что высыпания на лице, внешне похожие на прыщи, могут быть симптомом и проявлением других, порой очень серьезных дерматологических заболеваний (акнеформных дерматозов), которые никак не связаны с работой сальных желез.
Прыщи на лице могут оказаться симптом целого ряда заболеваний (нарушения функции внутренних органов, гормональной дисфункции, недостатка витаминов, снижения иммунитета), а также плохой экологической обстановки, неправильного ухода за кожей. Перечислим основные заболевания, состояния и факторы, результатом воздействия которых становятся высыпания на коже.
- Физиологические изменения гормонального статуса: половое созревание, вторая фаза менструального цикла, беременность, лактация, менопауза.
- Заболевания эндокринной системы: синдром поликистозных яичников, гипотиреоз, опухоли эндокринных желез.
- Утолщение рогового слоя эпидермиса (гиперкератоз), когда мертвые клетки эпидермиса не отшелушиваются, а остаются на коже, закупоривая сальные железы.
- Заболевания печени и вызванная ими интоксикация.
- Неправильное питание и авитаминоз:
- Преобладание в рационе быстрых углеводов (фастфуда, хлебобулочных изделий, жареной, жирной пищи) провоцирует повышение уровня глюкозы в крови и резкий выброс инсулина, что, в свою очередь, влияет на повышение уровня тестостерона.
- Избыток омега-6 жирных кислот может усугубить воспалительные процессы в коже (такие явления могут наблюдаться при употреблении большого количества рыбы и птицы, выращенной на комбикормах).
- Злоупотребление молочными продуктами, подсолнечным, арахисовым, соевым маслами и маргарином нередко вызывает гиперфункцию сальных желез.
- Дефицит цинка, витаминов А и Е, Омега-3 жирных кислот.
Заболевания желудочно-кишечного тракта, нарушение моторики и перистальтики кишечника, частые запоры способствуют интоксикации и появлению прыщей.
При наличии высыпаний на коже следует обратиться к врачам-дерматологам и косметологам. Однако часто лечение требует комплексного подхода, подразумевающего терапию заболевания, симптомом которого стали прыщи. В таком случае необходимы консультации гинеколога , эндокринолога , гастроэнтеролога , аллерголога , психоневролога.
Диагностика и обследования при появлении прыщей
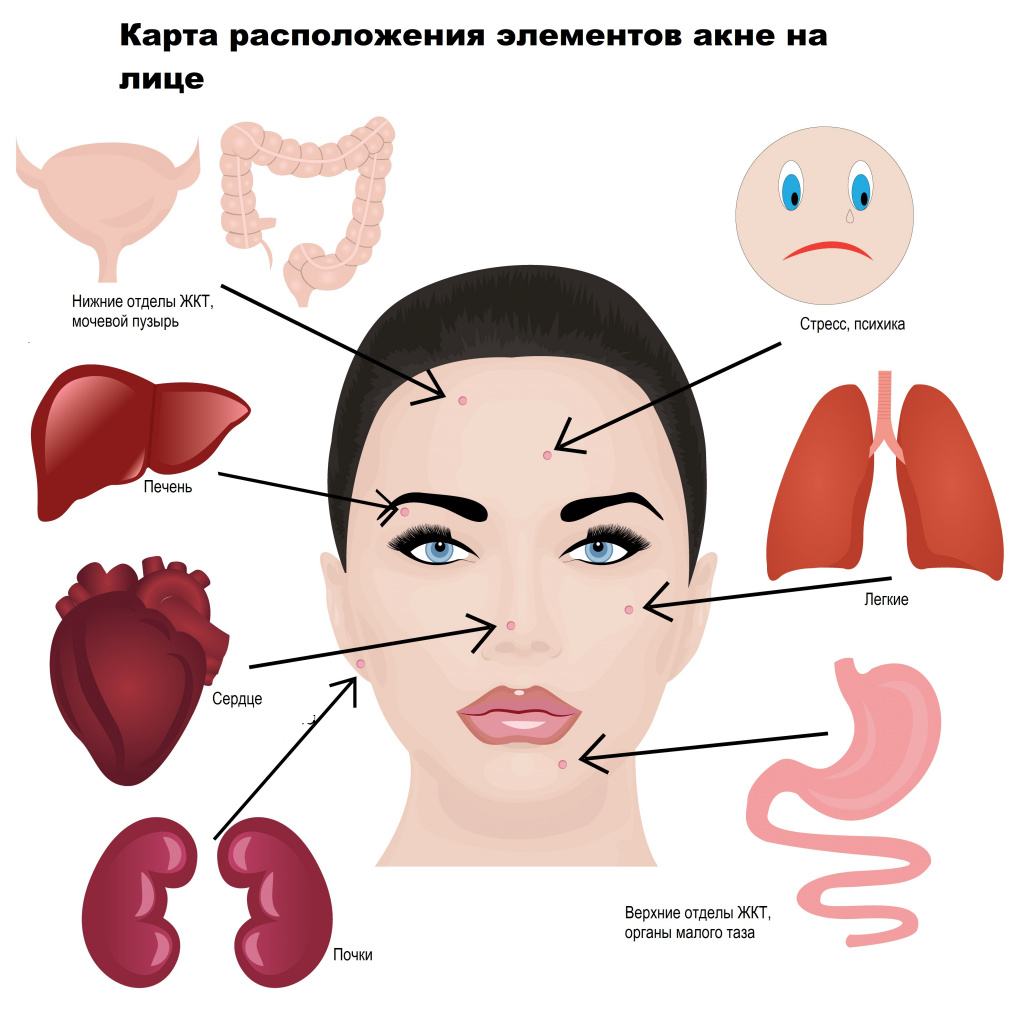
Прыщи и их локализация являются своеобразным мессенджером, передающим информацию о нарушениях работы органов или систем. Чаще всего прыщи возникают в так называемой Т-зоне (лоб, нос, подбородок) – здесь сальные железы наиболее активны, а поры – расширены. Но нередко прыщи встречаются и на щеках, скулах (U-зоне). Это обусловлено разными причинами и состоянием организма. Составлена специальная карта-путеводитель «Виды прыщей и что они означают». Так, средняя часть лба соответствует нижнему отделу пищеварительного тракта, тонкому кишечнику и мочевому пузырю, область возле ушных раковин – почкам, веки и область вокруг глаз – печени, височная область – желчному пузырю, средняя треть лица, скулы – легким, подбородок – желудку, органам малого таза, нос – поджелудочной железе и сердцу, а нижняя часть щек и нижняя челюсть – нижним отделам ЖКТ.
![Карта.jpg]()
Диагностика начинается с тщательного осмотра кожи, сбора анамнеза (сведений о перенесенных болезнях, операциях, хронических заболеваниях, наследственности) и установления связи между высыпаниями и образом жизни, питанием, привычками.Если природа заболевания неочевидна, назначаются лабораторные исследования.
-
Клинический анализ крови.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также: