Что такое изъявление эпителия
Обновлено: 29.04.2024
Неоплазии кишечника – это группа доброкачественных или злокачественных новообразований, которые могут располагаться в разных отделах толстой кишки. Чаще всего развиваются они развиваются из слизистой оболочки кишечника, но источником роста может стать и другая ткань.
Доброкачественные новообразования довольно распространены. По некоторым данным частота их встречаемости достигает 40% у людей старше 50 лет. Как правило, они никак не беспокоят человека. Главная их опасность заключается в злокачественном перерождении и возникновении рака, поэтому необходима их своевременная диагностика и удаление.
Злокачественные опухоли занимают третье место в структуре онкопатологии и представляет серьезную проблему для экономически развитых стран. Заболевания могут приводить к инвалидизации и гибели больного, а результаты лечения не всегда удовлетворительны.
Причины неоплазии кишечника
На данный момент принято считать, что неоплазии кишечника – это полиэтиологичное заболевание. К их развитию может привести несколько причин:
- Особенности питания: переедание, употребление в пищу большого количества мяса, пряных, маринованных, копченых и соленых блюд, злоупотребление алкоголем, недостаток в рационе пищевых волокон, растительной клетчатки и витаминов.
- Воспалительные заболевания кишечника – неспецифический язвенный колит, болезнь Крона.
- Наследственная предрасположенность – описано несколько синдромов, при которых развиваются множественные новообразования кишечника, которые склонны к малигнизации.
- Возраст. Чем старше человек, тем выше вероятность развития у него неоплазии.
Доброкачественные опухоли кишечника
Полипы. Это относительно доброкачественные новообразования, произрастающие из слизистой оболочки кишечника. Выглядят как шаровидные, грибовидные или ветвистые разрастания. Некоторые полипы располагаются на тонкой ножке, другие – на широком основании. Главной опасностью данных новообразований является их возможная малигнизация (злокачественное перерождение), поэтому их рекомендуют своевременно удалять.
Липома кишечника. Это очень редкое новообразование, встречается в 0,035-0,4% случаев всех доброкачественных новообразований кишки. Обычно липома представлена единичным новообразованием, но могут быть варианты мультифокального поражения.
Диагностика данных новообразований на дооперационном этапе является сложной задачей. Как правило, ее обнаруживают при морфологическом исследовании материала, удаленного во время операции по поводу других заболеваний кишечника.
Морфологически липома представлена хорошо дифференцированной жировой тканью с фиброзной стромой. Обычно поверхность гладкая и покрыта неизмененной слизистой оболочкой. При больших размерах опухоли на слизистой могут быть эрозии и язвы (их связывают с ишемическими поражениями и травматизацией каловыми массами).
Гемангиомы кишечника. Строго говоря, гемангиома не является опухолевым образованием. По сути это результат изменений кровеносных сосудов (мальформация). Условно ее можно разделить на две категории:
- Капиллярная, представленная сетью кровеносных сосудов наименьшего калибра – капилляров, выстланных гиперплазированным эпителием.
- Кавернозная – образована более крупными кровеносными сосудами, которые располагаются между соединительнотканной стромой.
Основным симптомом гемангиомы является кровотечение. При крупных новообразованиях возможна обтурация просвета кишки с развитием кишечной непроходимости.
Злокачественные образования кишечника
Злокачественные новообразования кишечника делят на опухоли эпителиального и неэпителиального происхождения. Эпителиальные опухоли развиваются из эпителия слизистой оболочки кишки (колоректальный рак). Чаще всего, это аденокарциномы, плоскоклеточный рак, реже встречается мелкоклеточный, перстневидноклеточный, медуллярный и недифференцированный рак. Раку всегда предшествуют доброкачественные неоплазии или хронические воспалительные процессы – полипы, болезнь крона, неспецифический язвенный колит.
Из неэпителиальных опухолей встречаются лейомиосаркома, ангиосаркома и саркома Капоши.
По характеру роста злокачественного новообразования выделяют:
- Экзофитные опухоли – растут в просвет кишки.
- Диффузно-инфильтративные опухоли – распространяются внутри стенки кишки.
- Аннулярные новообразования – охватывают стенку кишки по ее окружности.
Симптоматика
Симптомы новообразования зависит от его вида, размера и локализации. Мелкие новообразования, не превышающие 2-3 см, никак себя не проявляют клинически. И только при их увеличении появляются признаки:
- Боль в животе неясной локализации.
- Кишечная непроходимость. Она может развиваться на фоне обтурации или инвагинации кишечной стенки из-за нарушения ее перистальтики.
- Полипы, гамангиомы и рак кишечника могут кровоточить. При профузных кровотечениях из заднего прохода будет выделяться алая кровь или мелена. При незначительной кровоточивости могут быть прожилки крови в кале, при скрытых кровотечениях развиваются железодефицитные анемии.
- Выделение слизи из заднего прохода – ворсинчатые полипы, рак.
- Диспепсические расстройства: запоры, диареи, вздутие живота.
- Чувство инородного тела в прямой кишке.
Стадии опухолевого процесса
При диагностике злокачественной неоплазии кишечника большое значение имеет стадия распространения опухоли. От этого зависит прогноз течения заболевания и схема его лечения. Здесь выделяют следующие стадии:
Рак in situ – злокачественные клетки обнаруживаются только в слизистой оболочке кишки.
1 стадия – опухоль прорастает подслизистый слой.
2 стадия – опухоль распространяется на мышечный слой кишечной стенки.
3 стадия – опухоль прорастает всю толщину кишечной стенки, может распространяться на висцеральную брюшину и жировую клетчатку. Обнаруживаются метастазы в регионарных лимфатических узлах.
4 стадия – опухоль любых размеров с отдаленными метастазами (печень, легкие, головной мозг).

Диагностика
Для обнаружения неоплазии кишечника применяются следующие методы диагностики:
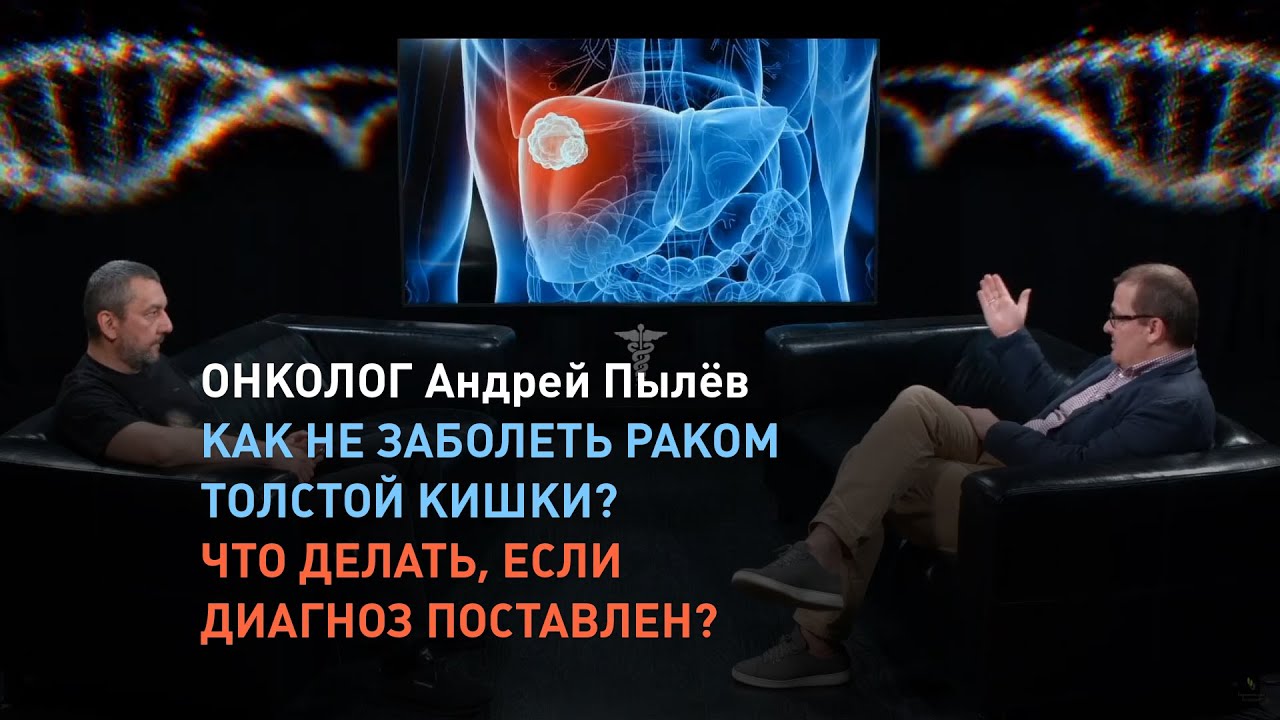
- Эндоскопическое обследование кишки – тотальная колоноскопия (осмотр всей поверхности толстой кишки) и ее сокращенный вариант – ректоскопия и ректосигмоскопия – осмотр прямой и сигмовидной кишки. Этот метод позволяет визуализировать новообразования на ранних стадиях, еще до развития симптомов, провести их удаление, а если это невозможно, выполнить биопсию. В настоящее время колоноскопия является золотым стандартом диагностики неоплазий толстой кишки.
- Анализ кала на скрытую кровь. Этот метод применяется для обнаружения полипов и опухолей, которые имеют изъязвленную поверхность и кровоточат. Как правило, речь идет о достаточно крупных новообразованиях. Это обследование проводят в рамках скрининга колоректального рака. При положительном результате показана дальнейшая колоноскопия.
- Ирригоскопия – рентгенологическое исследование толстой кишки. В первую очередь позволяет обнаружить экзофитные новообразования и опухоли, деформирующие просвет кишки и кишечную стенку.
При обнаружении злокачественной неоплазии кишечника проводится дополнительное обследование для определения стадии заболевания. Сюда входят УЗИ, КТ, МРТ, ряд лабораторных анализов.
Лечение
Новообразования кишечника подлежат удалению, независимо от того, злокачественное оно или доброкачественное.
При небольших размерах неоплазии ее удаляют во время колоноскопии, и полученный материал отправляют на морфологическое исследование. При злокачественных опухолях кишечника проводят обширные операции, направленные на радикальное удаление опухоли. Это может быть резекция фрагмента кишки или удаление кишки (колэктомия). В ряде случаев требуется наложение колостомы – выведение надопухолевого отдела кишки на переднюю брюшную стенку.
При распространенных опухолях лечение дополняют химиотерапией, а для проксимальных отделов кишечника и лучевой терапией.
Прогностические данные
Прогноз будет определяться видом неоплазии кишечника. Например, липомы и ангиосаркомы не склонны к малигнизации, но удалять их нужно, чтобы предотвратить развитие осложнений – кишечной непроходимости и кровотечений. С полипами ситуация иная. Рекомендуют проводить полипэктомию, поскольку есть риск злокачественного перерождения. Наибольший риск малигнизации наблюдается в следующих случаях:
- Ворсинчатые полипы.
- Полипы более 1 см.
- Полипы на широком основании.
- Множественный полипоз.
Прогноз при раке кишечника определяется стадией заболевания. При начальных этапах прогноз благоприятный, есть вероятность полного выздоровления, 5-летняя выживаемость достигает 90%. На второй стадии – 50-70%, на третьей – 50%, и при метастатической форме рака пятилетний рубеж переживают только 10% больных.
Профилактика неоплазий кишечника
Снизить риски развития неоплазии кишечника помогут следующие рекомендации:
- Нормализация питания. Необходимо употреблять в пищу достаточное количество витаминов, клетчатки и пищевых волокон. Не переедайте, ограничьте употребление канцерогенных продуктов: копчености, маринады, легкоусвояемые углеводы, жирные сорта мяса, жареные блюда, пряности, алкоголь.
- Соблюдайте режим физической активности.
- Не допускайте возникновения хронических запоров и диарей, своевременно лечите заболевания ЖКТ.
Учитывая то, что рак кишечника развивается из полипов, необходимо их своевременное удаление. С этой целью всем людям старше 50 лет рекомендуют проводить колоноскопию хотя бы раз в десятилетие. Эта процедура позволит осмотреть слизистую кишки и одновременно удалить обнаруженные новообразования.
Возникновение и развитие патологических состояний экзо- и эндоцервикса — это сложный и не достаточно изученный процесс. За весь период изучения патологии шейки матки выдвигалось несколько концепций развития заболеваний шейки матки: роль воспалительных процессов половых органов, нарушений менструального цикла, травм (роды, аборты), нарушений местного иммунитета. Впервые роль воспалительных процессов в развитии патологии шейки матки отметил R.Meyer в 1910г.
Число инфекций, передающихся половым путем, в последнее время неуклонно возрастает. Это способствует не только увеличению воспалительных заболеваний внутренних половых органов, но и приводит к развитию патологических процессов на шейке матки.
В настоящее время технические возможности и наши знания о воспалительном процессе изменились, а роль воспаления в механизме развития патологии шейки матки представляется иначе, чем об этом писал Меуег. Однако в последнее время воспалительному процессу, способствующему развитию патологии шейки матки, стали придавать большое значение.
Воспаление — это реакция живой ткани на повреждение, заключающаяся в определенных изменениях терминального сосудистого ложа, крови, соединительной ткани, направленная на уничтожение агента, вызывающего повреждение, и на восстановление поврежденной ткани.
О воспалении можно говорить в том случае, когда имеется сочетание альтерации, нарушений крово- и лимфообращения, ведущих к экссудации, и пролиферации клеточных элементов, завершающейся чаще всего репаративной регенерацией. В очаге воспаления возникает гамма чрезвычайно сложных процессов, которые не могут протекать автономно, не являясь сигналом для включения в воспалительную реакцию различных систем организма.
Фото 1. Зона трансформации с явлениями воспаления
Фото 2. Экзоцервицит
Фото 3. Картина воспаления на пробе Шиллера
Фото 4. Экзоцервицит
Включение в процесс воспаления иммунной, нервной, эндокринной и других систем обеспечивает ряд изменений,оказывающих большое влияние на поврежденную ткань.
Шейка матки и влагалище — это экологические ниши, анатомическое строение и функции которых способствуют поддержанию нормального биоценоза, что защищает половую систему от внедрения специфических или неспецифических возбудителей и, таким образом, от прогрессирования воспалительного процесса.
Система сомоочищения влагалища функционирует благодаря циклическому влиянию эстрогенов в первую фазу цикла и прогестерона — во вторую. Под действием эстрогенов происходит рост многослойного плоского эпителия, синтез гликогена в нем, продукция слизистого секрета в шейке матки. Многослойный плоский эпителий, насыщенный гликогеном, и слизистая пробка в цервикальном канале выполняют барьерную функцию — преграждают путь повреждающему агенту (специфической или неспецифической инфекции), препятствуют развитию воспаления.
Под действием прогестерона происходит десквамация и цитолиз многослойного плоского эпителия. Палочки Дедерлейна способствуют расщеплению гликогена в отторгнутом многослойном эпителии до молочной кислоты, что в свою очередь приводит к поддержанию нормальной рН влагалищной среды. Если самоочищающая система влагалища и шейки матки не способствует разрешению острого воспаления, то возникает хронический воспалительный процесс, который способствует развитию в многослойном плоском эпителии дистрофических изменений, инфильтрации стромы лейкоцитами и лимфоцитами, уменьшению количества гликогена и нарушению дифференциации клеток в процессе метаплазии. Все эти изменения являются фоном для развития патологии шейки матки.
Для диагностики заболеваний шейки матки используют комплекс различных методов — кольпоскопия, цитологическое исследование (pap-smear test), гистологическое исследование биоптата шейки матки и соскоба цервикального канала, а также специальные исследования, направленные на выявление инфекционного агента — бактериоскопия, бактериологическое исследование, ПЦР, ДНК-гибридизация.
Как известно, в задачи кольпоскопии входит:
1) оценка состояния эпителия шейки матки;
2) выявление патологического очага;
3) дифференцировка доброкачественных изменений от подозрительных в отношении малигнизации;
4) выбор наиболее измененного участка экзоцервикса для прицельной биопсии.
Критериями оценки состояния экзоцервикса при кольпоскопии является наличие того или иного типа эпителия, состояние сосудов шейки матки и их рисунок, цвет и поверхность шейки матки, характер стыка многослойного плоского эпителия и цилиндрического, реакция на уксусную пробу и пробу Шиллера. Наличие воспаления может приводить к отеку ткани шейки матки, что изменяет вид поверхности экзоцервикса и изменяет цвет (как правило, бледно-розовый на ярко-красный или бордовый). Ткань экзоцервикса становится рыхлой с выраженными и легко кровоточащими сосудами, которые бывают резко увеличенными. При пробе Шиллера могут обнаруживаться немые иоднегативные участки. Такая кольпоскопическая картина характеризует атипические изменения на шейке матки, что может способствовать гипердиагностике CIN или даже рака шейки матки.
Фото 5. Атрофический вагинит и экзоцервицит
Фото 6. Зона трансформации. Йоднегатив. Явление экзоцервицита
Фото 7. Атрофический экзоцервицит
Несмотря на то, что цитологический и гистологический методы исследования являются более достоверными, чем кольпоскопия, морфолог так же бывает в затруднении при дифференциальной диагностике изменений на шейке матки, обусловленных воспалением или цервикальной интраэпителиальной неоплазией, так как они сходны с картиной воспалительного процесса. Поэтому раннее выявление инфекционного процесса и проведение своевременной адекватной терапии, способствующей санации влагалища перед проведением pap-smear test и биопсии шейки матки, дает возможность получить более достоверные данные как в процессе кольпоскопии, так и цитологического и гистологического исследований. Кроме того, это позволяет, в зависимости от результата, выбрать наиболее эффективный и обоснованный метод лечения в каждом конкретном случае.
Таким образом, адекватная противовоспалительная терапия определяет возможность в короткие сроки эффективно подготовить пациентку к проведению цитологического исследования и биопсии шейки матки, чтобы получит реальные данные о состоянии шейки матки.
На этапе проведения деструкции патологически измененного экзоцервикса также необходимо учитывать наличие воспалительного процесса. Если на подготовительном этапе не удалось добиться хороших результатов, то деструкция шейки матки длительное время не будет завершаться нормальной эпителизацией, и это может способствовать возникновению осложнений (эндометриоз шейки матки, рубцовые изменения экзоцервикса, стриктуры цервикального канала, множественные наботовы кисты, экзоцервициты и др.).
Лечение воспалительного процесса, особенно обусловленного инфекциями, передающимися половым путем, обязательно должно быть комплексным. Кроме используемых современных антибактериальных препаратов, назначаемых в соответствии с выявленным патогенным агентом, при наличии патологии шейки матки особое значение приобретает применение препаратов местного действия. Для местного антибактериального лечения кольпитов и экзоцервицитов используется большое количество разнообразных влагалищных лекарственных средств широкого спектра действия — Тержинан, Макмирор, Клион-Д, Бетадин и др.
Учитывая, что чаще всего у пациенток наблюдаются смешанные инфекции, большое значение приобретает сочетание в одном препарате нескольких действующих компонентов, что позволяет добиваться хорошего лечебного эффекта.
Проведенные нами исследования показали, что в большом количестве случаев монокомпонентная антибиотикотерапия инфекционных процессов сопровождается развитием дисбиоза влагалищной флоры. При этом во влагалищном содержимом преобладает сочетание анаэробной и грибковой флоры. Применение в комплексе лечения местно антибиотика широкого спектра действия, метронидазолового компонента, воздействующего на анаэробную флору, противогрибкового составляющего максимально способствует не только санации влагалища, но и предотвращает развитие бактериального вагиноза, обеспечивает поддержание во влагалище нормальной кислотности и флоры. Использование одного лекарственного средства, обладающего всеми составляющими, особенно ценно в плане диагностики и лечения патологии шейки матки.
Мы имеем большой опыт применения в процессе диагностики и лечения патологии шейки матки, сопровождающейся воспалительным процессом, такого препарата широкого спектра действия как Тержинан.
Тержинан — это влагалищные таблетки, которые содержат тернидазол, нистатин, неомицина сульфат и преднизолон. Столь многокомпонентный состав обеспечивает воздействие на патологическую флору, которая может способствовать возникновению и персистенции воспалительного процесса.
Отличительной особенностью данного препарата является наличие в его составе малой дозы преднизолона — глюкокортикоида, обладающего выраженным противовоспалительным, противоаллергическим, иммунодепрессивным, антиэкссудативным, противозудным действием, а также снижающим проницаемость сосудов и улучшающим микроциркуляцию. Препарат не оказывает побочного системного влияния, отличается высокой эффективностью. В зависимости от выраженности процесса можно использовать Тержинан в течение 6 или 10 дней, после чего проводить диагностические исследования. Такая тактика резко повышает достоверность исследований и способствует правильному выбору дальнейшей тактики лечения заболеваний шейки матки.
Таким образом, воспаление в строме шейки матки играет большую роль в развитии патологического процесса на шейке матки, определяет возможности диагностики и терапии заболеваний шейки матки. Точность диагностики и эффективность лечения зависит во многом от своевременно проведенной адекватной противовоспалительной терапии.
Литература
1. Воспаление: Руководство для врачей / Под ред. В.В.Серова, В.С.Паукова. — М.: Медицина, 1995.
2. Патология шейки матки и вульвы / Под ред. В.Н.Прилепской. — 1999.
3. Патология влагалища и шейки матки / Под ред. В.И.Краснопольского.— 1997.
4. Intergrated Colposcopy. — Second edition Malcolm Anderson.— 1996.
5. Vaginal Ecosystem. — M.: Vignali, 1995.
Что такое аденокарцинома желудка? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бондаренко Юлии Сергеевны, хирурга со стажем в 16 лет.
Над статьей доктора Бондаренко Юлии Сергеевны работали литературный редактор Юлия Липовская , научный редактор Вячеслав Михайличенко и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Аденокарцинома желудка (Gastric adenocarcinoma) — это злокачественная опухоль, которая развивается из железистых клеток внутренней стенки желудка — эпителиального слоя. На её долю приходится 90–95 % от всех типов рака желудка [1] .
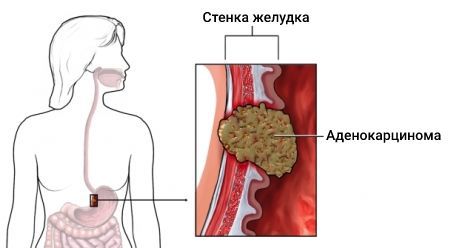
К основным симптомам аденокарциномы относятся: боль в верхних отделах живота («под ложечкой»), снижение веса, тошнота, рвота и потеря аппетита.
Причины аденокарциномы желудка
Причины заболевания окончательно не изучены. Известны только факторы риска, которые могут привести к развитию болезни. Их наличие не гарантирует, что со временем у человека сформируется рак желудка.
Различают внешние и внутренние факторы риска аденокарциномы.
Внешние факторы риска:
- нездоровый образ жизни и нерациональное питание: курение, употребление алкоголя, большого количества копчёностей, консервантов и нитритов, диета с низким содержанием овощей и фруктов; ;
- операции на желудке: ушивание прободной язвы и резекция желудка — удаление его части;
- профессиональные вредности: вдыхание угольной пыли, лаков и красок, производство резины, металлургические работы;
- инфекции, например вирус Эпштейна — Барр и Helicobacter pylori.
Внутренние факторы риска:
-
, которая развивается из-за дефицита витамина В12; ;
- аденоматозные полипы желудка;
- болезнь Мене́трие — переразвитие слизистой оболочки желудка с её последующим утолщением, появлением аденом и кист;
- наследственные факторы: мутация гена CDH1 и/или развитие рака желудка у родственника повышает вероятность образования опухоли на 80 % [1][2] .
Под влиянием этих факторов железистые клетки желудка начинают мутировать и бесконтрольно делиться, «ускользая» от иммунной системы.
Эпидемиология
Аденокарцинома желудка — наиболее распространённая злокачественная опухоль. В структуре смертности среди онкозаболеваний она занимает второе место.
Ежегодно в России регистрируют около 36 тысяч новых случаев рака желудка и более 34 тысяч человек умирают от этой болезни. Высокая смертность связана с тем, что больные обращаются за медицинской помощью уже на поздних стадиях рака.
Мужчины заболевают аденокарциномой в 1,3 раза чаще женщин. Возможно, это связано с тем, что женщины внимательней относятся к своему здоровью и раньше обращаются к врачу.
Чаще всего болезнь выявляют у людей старше 50 лет [3] . Но аденокарцинома, вызванная наследственными причинами, чаще возникает до 40 лет.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы аденокарциномы желудка
- На ранних стадиях — дискомфорт в животе, изжога, чувство переполнения и распирания вскоре после еды, иногда даже после небольшого перекуса.
- На более поздних стадиях — тошнота и боли в верхней части живота.
- Рвота съеденной пищей из-за поражения выходного отдела желудка.
- Дискомфорт за грудиной при продвижении пищи из-за поражения пищеводно- желудочного перехода.
- Рвота «кофейной гущей» и «чёрный стул» при кровотечении из опухоли желудка.
- Снижение веса, анемия, слабость и кахексия (истощение) из-за проблем с проходимостью пищи, плохого аппетита и быстрой насыщаемости на фоне растущей опухоли.
- Бледность кожи из-за присоединения анемии [2] .
Аденокарцинома желудка проявляет себя не сразу. Первым симптомом чаще всего становится быстрая насыщаемость, дискомфорт и тяжесть в верхних отделах живота. Постепенно болевой синдром прогрессирует, из-за чего снижается аппетит и вес. Признаки кровотечения и рвота также характерны для более поздних стадий болезни.
Патогенез аденокарциномы желудка
Патогенез аденокарциномы желудка до конца не изучен. Существует теория, что под воздействием агрессивных внешних факторов на слизистую оболочку желудка повреждается структура ДНК железистых клеток, которые выстилают желудочные ямки, вырабатывают слизь и гормоны простагландины. Это повреждение приводит к различным мутациям, из-за которых здоровая клетка становится злокачественной [4] .

Изначально агрессивные факторы вызывают воспаление в стенке желудка, которое затем приводит к дисплазии и метаплазии. Клетки начинают быстро делиться, становятся атипичными, из-за чего меняется структура слизистой оболочки желудка. По сути дисплазия — это предраковое состояние.
После образования аденокарцинома начинает расти либо в просвет желудка, либо прорастать во все слои его стенки, соседние ткани и органы, например в поджелудочную железу, печень, переднюю брюшную стенку и поперечный отдел толстой кишки с её брыжейкой. Также опухоль может расти вдоль пищеварительной трубки, распространяясь на пищевод и двенадцатиперстную кишку.
С током лимфы, а на поздних стадиях через кровоток, раковые клетки распространяются в организме и становятся причиной метастазов — образования вторичных очагов опухоли в других органах. Чаще всего аденокарцинома метастазирует в печень, лёгкие, головной мозг и брюшину.
Классификация и стадии развития аденокарциномы желудка
Аденокарцинома может образоваться в любой части желудка. Чаще всего её обнаруживают в пилорическом отделе, чуть реже — в кардиальном.
У каждой локализации есть свой шифр:
- C16.0 — опухоль находится в кардиальном отделе желудка;
- C16.1 — в дне желудка;
- C16.2 — в теле желудка;
- C16.3 — в антральном отделе желудка;
- C16.4 — в пилорическом отделе желудка;
- C16.5 — на малой кривизне желудка;
- C16.8 — на большой кривизне желудка;
- C16.8 — выходит за пределы перечисленных областей;
- C16.9 — опухоль неуточнённой локализации [16] .
В медицинском международном сообществе наиболее признана классификация по TNM, где:
- «T» обозначает «tumor», т. е. глубину прорастания опухоли в стенке желудка;
- «N» — «nodus», т. е. количество поражённых лимфоузлов;
- «М» — «metastasis», т. е. наличие метастазов.
Стадии аденокарциномы желудка по классификации TNM 2018 года представлены ниже в таблице [18] .
В зависимости от того, насколько опухолевые клетки похожи на здоровые, выделяют три формы опухоли:
- высокодифференцированная аденокарцинома желудка (G1) — клетки опухоли похожи на здоровую ткань, сама опухоль обычно растёт медленно, при своевременной диагностике хорошо поддаётся лечению;
- умеренно дифференцированная аденокарцинома (G2) — скорость роста и злокачественность клеток опухоли умеренные;
- низкодифференцированная аденокарцинома (G3) — клетки опухоли не похожи на какую-либо здоровую ткань, сама опухоль наиболее злокачественная, отличается быстрым ростом и метастазированием.
Отдельно стоит сказать о перстневидноклеточной аденокарциноме желудка. Это редкая низкодифференцированная опухоль, одна из самых агрессивных форм рака желудка [19] [21] . Фактически она не поддаётся химио- и лучевой терапии, наиболее эффективным методом лечения на ранних стадиях является операция. Поэтому крайне важно обращаться к врачу при появлении первых симптомов, похожих на признаки гастрита или язвы желудка, особенно если есть предрасположенность к раку желудка.
Осложнения аденокарциномы желудка
Чаще возникает кровотечение и опухолевый стеноз, реже — асцит.
Диагностика аденокарциномы желудка
Обычно пациент с аденокарциномой желудка жалуется на боли в верхней части живота (под «ложечкой»), снижение веса, непроходимость пищи, отвращение к еде, потерю аппетита, рвоту съеденной накануне пищей или кровью.
При подозрении на аденокарциному желудка назначают инструментальное обследование:
- ФГДС с биопсией — обследование пищевода, желудка и двенадцатиперстной кишки с забором и исследованием фрагмента опухоли. Выполняется в первую очередь. Позволяет отличить аденокарциному от других видов опухоли.
- КТ органов брюшной полости, грудной клетки и головы с внутривенным контрастированием — онкопоиск. Позволяет уточнить, поражены ли лимфоузлы, есть ли метастазы в других органах.
- Лапароскопия — обследование желудка с помощью видеолапароскопа. Показано пациентам, у которых по данным эндоУЗИ или КТ есть подозрение на прорастание опухоли в серозную оболочку желудка. Обязательна при тотальном и субтотальном поражении органа. Если местное распространение опухоли подтвердилось, меняется тактика лечения: таким больным сначала будет показана химиотерапия, а затем (при уменьшении опухоли) — хирургическое лечение. В сомнительных случаях в ходе лапароскопии берут смывы с желудка и брюшной полости. Это помогает обнаружить опухолевые клетки и выставить стадию рака перед началом химиотерапии.
- УЗИ брюшной полости и надключичных лимфоузлов — позволяет выявить метастазы печени, асцит и увеличение лимфоузлов (зачастую поражаются лимфоузлы над ключицами, в области яичников, прямой кишки и пупка).
Чаще всего выполняют УЗИ, КТ и ФГДС с биопсией, реже — эндоскопическое УЗИ, так как не все специалисты могут его провести. В крупных онкологических стационарах пациенты проходят все перечисленные исследования и ПЭТ КТ, так как они помогают верно подобрать тактику лечения.
При подготовке к операции обязательно назначают консультацию кардиолога. Чтобы оценить функцию сердца, по показаниям дополнительно проводят эхокардиографию и холтеровское мониторирование. Также выполняют исследование ФВД (функции внешнего дыхания) и УЗДГ вен нижних конечностей, чтобы исключить тромбозы. Иногда может потребоваться консультация эндокринолога, невролога и других врачей [6] .
Лабораторная диагностика включает:
- развёрнутый клинический и биохимический анализ крови;
- коагулограмма — исследование свёртывающей системы крови;
- определение группы крови и резус-фактора с фенотипированием;
- анализ крови на гепатиты В, С, ВИЧ-инфекцию и сифилис;
- общий анализ мочи;
- анализ крови на онкомаркеры (Са 19-9, Са 72-4 и РЭА — раковый эмбриональный антиген).
Все эти анализы также нужны для предоперационной подготовки. Если есть подозрение на аденокарциному желудка, нужно обратить внимание на количество эритроцитов и гемоглобина в общем анализе крови: их снижение может указывать на развитие анемии и внутрижелудочное кровотечение.
Лечение аденокарциномы желудка
Хирургическое лечение на ранней стадии
При выявлении ранних форм рака, т. е. при раке in situ, показано эндоскопическое лечение:
- резекция слизистой (EMR) — удаление опухоли вместе с частью слизистой оболочки желудка;
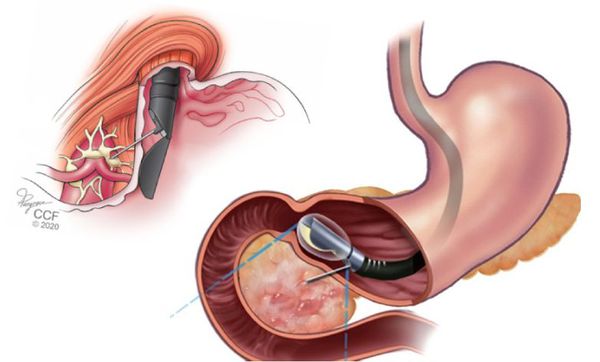
- диссекция в подслизистом слое (ESD) — удаление опухоли вместе с частью подслизистого слоя. Проводится при аденокарциноме до 2 см, позволяет удалить её единым блоком, без разрезов [8] .
Эти операции проводят под общим обезболиванием. Вначале определяют границы опухоли и с помощью электрокоагуляции «маркируют» (прижигают) края резекции, отступая на 3 мм от границы опухоли. Затем в подслизистый слой вводят инъекцию физраствора и Волювена (Гидроксиэтилкрахмала), чтобы отделить опухоль от мышечного слоя. Потом аденокарциному удаляют и смотрят на её «ложе»: нет ли кровотечения или перфорации, удалось ли полностью удалить опухоль. После чего удалённый фрагмент извлекают и отправляют на гистологическое исследование.
![Резекция слизистой желудка [17]](https://probolezny.ru/media/bolezny/adenokarcinoma-zheludka/rezekciya-slizistoy-zheludka-17_s.jpg)
После операции пациентов выписывают на 3–4 сутки. Эффективность лечения при соблюдении всех стандартов составляет 98 %. Рекомендуется:
- через месяц после операции, а затем каждые 3 месяца делать ФГДС;
- через полгода после операции — КТ;
- в течение месяца строго соблюдать диету — питаться жидкой протёртой пищей, исключить алкоголь и горячую еду.
Хирургическое лечение на поздних стадиях
Операция при аденокарциноме желудка проводится в несколько этапов: сначала удаляется сама опухоль, затем восстанавливается пассаж пищи [9] .
Основные радикальные операции при аденокарциноме желудка:
- гастрэктомия — полное удаление желудка;
- субтотальная проксимальная резекция — удаление верхней части желудка вместе с кардиальным отделом;
- субтотальная дистальная резекция — удаление нижних 2/3 или 3/4 желудка.
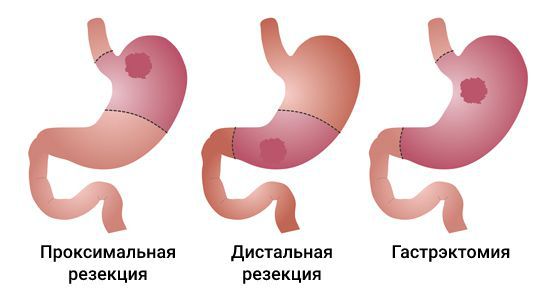
Все виды операций выполняются как «открытым» способом (лапаротомически), так и через небольшие разрезы (лапароскопически), в том числе с помощью робототехники. Выбор хирургического доступа и объёма операции зависит от распространённости процесса: степени поражения стенок желудка, вовлечения пищевода, двенадцатиперстной кишки и наличия метастазов.
После удаления опухоли часто выполняют лимфодиссекцию. Это стандартная операция по удалению лимфоузлов при раке желудка. Она проводится, чтобы снизить риск рецидива, так как аденокарцинома очень часто метастазирует лимфогенным путём , т. е. с током лимфы.
При единичных метастазах в других органах выполняют симультанные операции, т. е. сразу несколько вмешательств.
Если у пациента много отдалённых метастазов, то оперативное лечение, как правило, не проводится. Но при развитии экстренных жизнеугрожающих состояний, таких как перфорация стенки желудка, кровотечение или стеноз, операция выполняется, чтобы спасти жизнь пациента. Объём оперативного вмешательства при этом должен быть минимальным.
Химиотерапия
Основным методом лечения опухоли, которую невозможно удалить, является химиотерапия [12] . Она нужна для того, чтобы убить опухолевые клетки или значительно замедлить их рост.
Доктор может назначить монотерапию, т. е. лечение одним препаратом, или комбинированную химиотерапию с применением нескольких лекарств. Комбинированная химиотерапия позволяет усилить противоопухолевый эффект.
Комбинированные методы лечения включают:
- периоперационную химиотерапию — предпочтительный метод, проводится перед операцией, чтобы уменьшить опухоль, и после операции для борьбы с оставшимися раковыми клетками [10][11] ;
- адъювантную химиотерапию — выполняется после операции;
- адъювантную химиолучевую терапию — проводится после нерадикального удаления опухоли, т. е. когда раковые клетки остаются по краям резекции и продолжают расти.
Выбор конкретной комбинации зависит от состояния пациента, его возраста, а также тяжести и характера сопутствующих заболеваний.
Показания к химиотерапии:
- распространение аденокарциномы за пределы слизистого слоя;
- поражение лимфоузлов;
- наличие метастазов.
Пациент может отказаться от химиотерапии, но он должен понимать, что без лечения опухоль может быстро возникнуть снова и метастазировать.
Симптоматическое лечение (паллиативная помощь)
Симптоматическая терапия проводится на IV стадии рака, когда специальные методы лечения противопоказаны. Она помогает облегчить симптомы болезни с помощью адекватного обезболивания.
Рекомендуется постепенно переходить от слабых обезболивающих (например, Кетопрофена) к более сильным препаратам, вплоть до наркотических (Трамадола или Морфина). При выраженном болевом синдроме их можно использовать в среднем каждые 4 часа.
Прогноз. Профилактика
Прогноз при аденокарциноме желудка зависит от морфологического вида опухоли (дифференцированности), её размеров, наличия и количества метастазов, а также от инвазии в окружающие органы.
Зачастую пациенты с аденокарциномой обращаются к врачу уже на поздних стадиях болезни, когда опухоль проявляет себя осложнениями и её уже нельзя удалить [16] . Всё дело в том, что на ранних стадиях симптомы рака похожи на симптомы гастрита или язвы желудка. При таких проявлениях пациентам не хочется срочно делать гастроскопию. Вместо этого они идут в аптеку и покупают лекарства, после приёма которых жалобы на время стихают, однако опухоль продолжает расти. Поэтому чаще всего при аденокарциноме желудка прогноз неблагоприятный.
У пациентов, которым полностью удалили опухоль, более благоприятный прогноз:
- при первой стадии рака пятилетняя выживаемость отмечается у 80–90 % пациентов;
- при второй стадии рака — у 50–60 % пациентов;
- при третьей стадии рака — у 10–30 % пациентов [13][14] .
Пятилетняя выживаемость — это условный срок. Именно в это время зачастую развиваются рецидивы. Если в течение пяти лет после лечения опухоль не развилась повторно, то прогноз можно считать благоприятным.
Профилактика аденокарциномы желудка
Чт обы предотвратить развитие аденокарциномы, необходимо:
- правильно питаться: меньше употреблять солёных, копчёных и вяленых продуктов, больше — сезонных овощей и фруктов;
- избавиться от вредных привычек: алкоголя и курения;
- при наличии факторов риска регулярно проходить скрининг — 1 раз в год делать ФГДС;
- при появлении жалоб как можно скорее обращаться к врачу и лечить хронические заболевания желудка.
После 45–50 лет профилактически обследовать желудок нужно абсолютно всем: статистически доказано, что с возрастом риск развития аденокарциномы желудка увеличивается [15] .
Доброкачественные опухоли желудка встречаются значительно реже злокачественных новообразований данной локализации. Они часто протекают бессимптомно, «заявляя» о себе различными осложнениями. Многие из них способны приводить к раку желудка. Их своевременное выявление и лечение считается важным направлением современной гастроэнтерологии.
Описание новообразований доброкачественной опухоли желудка
Доброкачественные опухоли желудка различаются по внутренней структуре и внешнему виду. Они могут иметь размеры от нескольких миллиметров до десятков сантиметров в диаметре. Их форма чаще бывает округлая или овальная, поверхность может быть гладкой или неровной, консистенция — твёрдой или мягкой при пальпации.
Эпителиальные опухоли желудка (полипы) бывают единичными или многочисленными (диффузный полипоз). Они могут расти на тонкой ножке, либо иметь массивную основу. В зависимости от строения будет различаться цвет нароста (от бледно-розового до ярко-малинового). Ворсинчатые полипы часто представляют собой папиллярные выросты различной толщины и высоты, напоминающие пальцы. Под микроскопом будут видны ряды изменённых клеток железистого эпителия с ветвящимися тубулярными структурами, участками кишечной метаплазии и дисплазии.
Если произойдёт малигнизация полипов, внешне они станут выглядеть, как неоднородные диффузные разрастания слизистого слоя, с участками изъязвления и выраженным сосудистым компонентом. При микроскопическом исследовании будут видны атипичные клетки.
Неэпителиальные доброкачественные новообразования способны расти в полость желудка или наружу, сдавливая соседние органы и структуры. Опухоли больших размеров могут визуально выделяться и прощупываться при осмотре.
Виды доброкачественных опухолей желудка
Основная классификация доброкачественных образований желудка разделяет их соответственно происхождению на две большие группы:
- эпителиальные опухоли;
- неэпителиальные опухоли.
К первой группе относятся гиперпластические (75%) и аденоматозные полипы (аденомы), а также диффузный полипоз. Слизистые наросты чаще поражают пилороантральный отдел желудка и встречаются у мужчин от 40 до 60 лет. Гиперпластические полипы имеют преимущественно доброкачественное течение. Аденомы желудка в большинстве случаев перерождаются в рак. При полипозе наблюдаются слизистые разрастания обоих типов.
Неэпителиальные доброкачественные опухоли желудка встречаются крайне редко. К ним относятся:
- эндотелиомы (из эндотелия сосудов);
- липомы (из жировых клеток);
- невриномы (из нервной ткани);
- миомы (из мышечных волокон);
- гемангиомы (из кровеносных сосудов);
- лимфангиомы (из лимфатических сосудов);
- фибромы (из волокнистых соединительных структур);
- смешанные опухоли.
Также в желудке бывают дермоиды, гамартомы, хондромы, остеомы и гетеротопии, происходящие из панкреатической ткани и желез двенадцатиперстной кишки. Наиболее часто из неэпителиальных доброкачественных опухолей встречается лейомиома (гладкомышечное новообразование). Последняя склонна к осложнённому течению и озлокачествлению.
Локализация
Опухоли желудка могут поражать любой его отдел. Чаще они располагаются в нижней трети органа.
Причины
Этиология доброкачественных новообразований желудка до конца не известна. Учёные предполагают, что появление и рост полипов взаимосвязан с нарушением процессов регенерации и пролиферации клеток эпителия. Гиперпластические наросты часто начинают развиваться при пониженной продукции соляной кислоты. Аденомы преимущественно возникают на фоне изменений, связанных с атрофическим гастритом, вследствие кишечной метаплазии и дисплазии. Эпителиоциты «теряют» свою дифференцировку и приобретают атипичные свойства, что может дать начало злокачественному процессу.
Опухоли желудка неэпителиальной природы по мнению учёных берут своё начало из гетеротопированной эмбриональной ткани. Причинами данной аномалии могут быть различные патологические процессы во время внутриутробного развития человека.
Факторы риска
Опухоли в желудке чаще возникают у людей, которые:
- страдают хроническими заболеваниями пищеварительной системы;
- имеют активную инфекцию Хеликобактер пилори (микроорганизмы приводят к повреждению слизистых оболочек желудочно-кишечного тракта и снижению их защитных свойств);
- не соблюдают принципов рационального сбалансированного питания;
- имеют генетическую предрасположенность к возникновению опухолей;
- проживают в экологически неблагоприятных районах;
- систематически подвергаются воздействию неблагоприятных факторов (химические соединения, стрессы, травмы и т. д.);
- имеют иммунодефицит;
- имеют вредные привычки (алкоголь, курение и т. п.).
В группу риска попадают люди после 40 лет, которые не проходят ежегодные профилактические осмотры с обязательным исследованием желудка.
Симптомы
Чаще новообразования протекают без специфических клинических симптомов. У большинства пациентов доброкачественные опухоли желудка имеют признаки сопутствующих патологий (хроническое воспаление, язвенная болезнь, гастроэзофагеальный рефлюкс и т.д.). Больной может предъявлять следующие жалобы:
- отрыжка воздухом или кислым содержимым;
- изжога;
- тошнота;
- рвота;
- вздутие живота;
- нарушение стула;
- дискомфорт, тяжесть, давление, ощущение инородного тела в эпигастральной области;
- боли в эпигастрии различной интенсивности и характера, в разной степени зависящие от приёма пищи.
При появлении осложнений, возникает типичная клиническая картина. При выраженном воспалении в желудке боль приобретает постоянный ноющий характер. Особенно сильный болевой синдром и жжение наблюдаются при невриноме. При ущемлении доброкачественных опухолей болезненные ощущения бывают интенсивными, схваткообразными, распространяясь по всему животу. Нередко человек покрывается холодным потом и теряет сознание.
При изъязвлении полипов, может наблюдаться клиническая картина желудочных кровотечений. Возможна рвота с кровью, появление дегтеобразного стула, общее недомогание. При хронической кровопотере развивается анемия. Человек становится бледным, постоянно испытывает усталость, слабость, головокружения.
Если слизистый нарост полностью перекрывает выход из желудка в 12-типерстную кишку, возникает острая кишечная непроходимость. При частичном закрытии просвета опухолью будут беспокоить тошнота, рвота съеденной пищей, тяжесть в эпигастрии и другие симптомы.
Неэпителиальные доброкачественные новообразования различаются по симптоматике, в зависимости от расположения, наличия дефектов поверхности, скорости и типа роста (внутрь желудка или наружу). Чаще они проявляются периодическими болезненными ощущениями после еды, при движениях или смене позы тела. Большие по объёму опухоли могут пальпироваться и «выступать» через брюшную стенку, а также «затруднять» работу соседних органов.
Практически любое неэпителиальное образование желудка способно осложниться кровотечением. Особую опасность представят гемангиома. Она может вызвать массивную кровопотерю, угрожающую жизни пациента. При ущемлении и/или инфицировании опухоли возможно появление кишечной непроходимости и перитонита. Со временем доброкачественные новообразования желудка способны трансформироваться в рак.
Диагностика доброкачественной опухоли желудка
Для обнаружения доброкачественных опухолей желудка используется комплекс диагностических мероприятий. Ведущими методами являются:
- лабораторные исследования (анализ крови, серологические тесты для определения наличия инфекции, оценка желудочного сока и т. д.);
- рентгенологические методы (рентгенография желудка, КТ органов брюшной полости и т.д.);
- УЗИ желудочной стенки и регионарных лимфоузлов;
- эндоскопическое исследование ЖКТ с прицельным забором гистологического материала из 6-8 подозрительных участков.

Часто неэпителиальные образования желудка подтверждаются после операции, когда проводят морфологический анализ удалённой опухоли.
Лечение доброкачественной опухоли желудка
Опухоли желудка незлокачественной природы, как правило, подлежат хирургическому лечению. Наиболее приемлемым способом в отношении эпителиальных образований небольшого размера является их эндоскопическое удаление. Проводят энуклеацию или электрокоагуляцию полипа. Большие и множественные полипозные разрастания оперируют чрезбрюшинным доступом (убирают часть желудка или весь орган). В ряде случаев проводят эндоскопическую резекцию огромной опухоли, чтобы устранить нежелательные симптомы и снизить риск осложнений.
Хирургическое удаление неэпителиальных доброкачественных образований производится различными способами, в зависимости от их особенностей. По показаниям выполняется энуклеация, разные виды резекции желудка или гастрэктомия.
Прогноз
При доброкачественных опухолях, расположенных в желудке, прогноз, как правило, благоприятный. Многое зависит от гистологического типа и размера образования. Оценить риск малигнизации и возникновения осложнений сможет только врач. Аденоматозные полипы и большинство неэпителиальных новообразований характеризуются частым злокачественным перерождением, поэтому они должны быть своевременно диагностированы и удалены.
После радикальной операции на желудке по поводу доброкачественных опухолей не исключён риск рецидива, но в целом отмечается благоприятный прогноз. Пациент должен следовать всем рекомендациям врача и ежегодно проходить контрольные обследования.
Профилактика
Основой профилактических мероприятий при доброкачественных опухолях желудка является систематическое посещение врача-гастроэнтеролога и прохождение назначенных им обследований. Необходимо вовремя диагностировать и лечить хронические заболевания пищеварительной системы. Весомая роль в профилактике опухолей желудка принадлежит сбалансированному рациональному питанию. Также важно придерживаться канонов здорового образа жизни, поддерживать адекватную работу иммунной системы, исключить неблагоприятные факторы внешней среды и т.д.
Доброкачественные опухоли желудка, как правило, не угрожают жизни пациента, однако они требуют высокой квалификации доктора. В нашей клинике имеются различные методы, позволяющие выполнить адекватное лечение даже в самых сложных случаях.
Дисплазия – это нарушение строения тканей организма, с упрощением их структуры, деформацией клеток и их составных частей. Обусловленные генетическими причинами врожденные дисплазии, как правило, имеют многообразные проявления, часто множественные и в разных системах.
Дисплазии слизистых оболочек имеют локальную привязку к определённому органу, как-то желудок, кишечник, шейка матки. В отличии от всех прочих дисплазий этот вид патологии не наследуется и не связан с глобальным генетическим сбоем, а вызывается жизнедеятельностью патологической микрофлоры.
Виды дисплазии
Дисплазии очень разнообразны и разнородны, врожденные и благоприобретенные дисплазии по сути очень разные процессы, одни захватывают несколько систем, другие – только участки слизистой оболочки.
Врожденные дисплазии проявляются аномалиями развития – отклонениям в строении, не мешающими нормальному функционированию, и пороками развития – эти аномалии уже нарушают функционирование анатомической области.
Дисплазии слизистой не формируют пороков и аномалий развития, но способны привести к злокачественным процессам. Абсолютно разные проявления дисплазий не позволяют создать единую классификацию, каждый исследователь проблемы предлагает собственную систематизацию разнородной патологии, не свободную от недостатков.
Врожденные дисплазии формируются во внутриутробном периоде, клинические проявления затрагивают покровные ткани и костно-мышечную систему, разделение их весьма условно.
Выделяют дисплазию эктодермы – поверхностной ткани зародыша, из которой формируются наружные покровы: кожа с ногтями и волосами и слизистая ротовой полости с зубами. Патология может проявиться в любом возрасте, в любом наборе признаков и с любой их выраженностью. Это может быть только сухость кожи с небольшими пятнышками атрофии и почти полным отсутствием зубов или гнездная плешивость с без ногтей и с лунообразными дефектами зубной эмали при полном наборе зубов. Возможно и просто снижение числа потовых желез в коже, что приводит к быстрому перегреванию уже в младенчестве и опасности внезапной смерти.
У подавляющего большинства страдающих генетической дисплазией соединительной ткани возможны нарушения всех систем организма от незначительных до опасных для жизни и с любым набором признаков: неврологические нарушения, пороки сердечных клапанов, изменения скелета, аневризмы сосудов, размягчение колец трахеи, опущение почек, а также приводящие к внезапной смерти сочетанное поражение сердечно-сосудистой и дыхательной систем. Наиболее активный всплеск проявлений отмечается в подростковом возрасте, когда, например, резко прогрессирует сколиоз и плоскостопие, появляется сердечная аритмия и близорукость. Сформировано несколько синдромов с характерными внешними проявлениями, опять-таки с вариабельной выраженностью – от мизерных отдельных проявлений до чрезвычайно выраженных с ранней гибелью от осложнений, как синдром Марфана и несовершенный остеогенез.
Дисплазия суставов проявляется врожденными пороками развития крупных – тазобедренных и коленных, а также мелких суставов кисти и стопы, и по своей сути может считаться все той же дисплазией соединительной ткани, но в отдельно взятой суставной системе. Как правило, патология выявляется у грудничка, но в минимальной форме может проходить незаметно, констатируют которую при обследовании по поводу случайной травмы ноги.
Дисплазию фиброзную выдают одиночные и множественные кисты в костях. Некоторые люди до глубокой старости проживают здоровую жизнь и узнают о генетической патологии в виде небольшой кисточки случайно при рентгене по другому поводу. Другие страдают хроническими болями и деформацией конечности, часто с укорочением, из-за множества кистозных полостей в костной ткани.
Дисплазию слизистых оболочек внутренних органов «зарабатывают» в процессе жизни. В большинстве случаев процесс не проявляется симптомами или имеет нехарактерные и нестабильные минимальные признаки, находят его при микроскопии кусочка ткани. Дисплазия может прогрессировать от легкой степени, через среднюю и тяжелую вплоть до рака нулевой стадии – и в этом её главная опасность. Тяжелую степень дисплазии сложно, а иногда и невозможно достоверно отличить от неинвазивного рака in situ.
Дисплазия желудка клинически может проявляться желудочной патологией, нередко у пациента отмечается инфицирование хеликобактерией. Патология заключается в упрощении клеточного строения – снижении дифференцировки, изменении клеточных ядер и других внутриклеточных структур. Легкая дисплазия не только переходит в среднюю, но и регрессирует, аналогично протекает и средняя, а тяжелая считается предраковым процессом и подлежит серьёзному лечению и наблюдению. Желудочная дисплазия по частоте встречаемости существенно уступает метаплазии – формированию в слизистой участков из клеток очень похожих на клетки толстой или тонкой кишки. При микроскопии вокруг любой дисплазии обязательно находят участки кишечной метаплазии и это тоже предраковый процесс.
Первичная дисплазия уротелия - нечасто встречающаяся патология, проявляющаяся симптоматикой раздраженного мочевого пузыря с частыми и болезненными позывами на мочеиспускание. Этот вариант дисплазии не принято разделять на степени, вероятность развития рака на диспластичном фоне чуть больше 15% и переход в нулевую стадию рака займет от 4 до 8 лет.
Цервикальная или дисплазия слизистой шейки матки очень частая патология, поскольку её ведущая причина – инфицированность вирусом папилломы человека. Сам вирус убить невозможно – он устойчив к любым лекарствам, но он смертен и у подавляющего большинства женщин самостоятельно излечивается в ближайшие два-три года.
Степени дисплазии
На трёх женщин с легкой дисплазией шеечной слизистой приходится одна пациентка со средней и тяжелой дисплазией. У девяти из десяти женщин место патологического изменения слизистой расположено у перехода плоского эпителия в железистый, который в норме находится у начала цервикального канала, но вследствие родов и абортов может перемещаться вглубь канала ближе к полости матки.
Дисплазия характеризуется появлением неправильных клеток – атипичных, но межклеточные структуры совсем не страдают. Клетки изменяют свою форму, ядра в них тоже меняют размер, форму и цвет. Ядра более крупные, неровные с толстой наружной оболочкой, внутриклеточная жидкость светлеет и увеличивается в объёме. Вместо абсолютно одинаковых клеточек эпителия появляется полная клеточная пересортица, усиленно делящаяся на такие же дефектные экземпляры. Вероятность развития рака в этой группе разноразмерных клеток доходит до 50%, правда, на это потребуются многие годы.
Степени дисплазии или по современной классификации, подчеркивающий возможность прогрессии до злокачественного процесса, цервикальной интраэпителиальной неоплазии или CIN градуируются следующим образом:
- Легкая цервикальная дисплазия или CIN I – патология располагается в одной трети пласта эпителия. Исследования показали, что у двух третей женщин в течение трёх лет с момента заражения вирусом папилломы человека 16 и 18 типов (ВПЧ) процесс самопроизвольно разрешится вследствие естественной гибели пораженной вирусом клетки, которую вирус не успеет покинуть и слущится вместе со своим клеточным «домиком». У трёх из десяти зараженных женщин ВПЧ продолжит жить дальше, а у одной перейдёт в среднюю степень дисплазии, тем не менее легкая дисплазия не считается предраком.
- Средняя степень цервикальной дисплазии или CIN II – поражение охватывает больше половины толщины эпителия – до двух третей. У трёх из сотни с течением времени такая дисплазия прогрессирует в тяжелую.
- При тяжелой степени цервикальной дисплазии или CIN III свободным от атипических клеток остается только поверхность эпителия, визуально даже в электронном микроскопе это патологическое состояние очень похоже на рак in situ. Предполагается, что у каждой седьмой женщины с диагностированной CIN III уже есть злокачественные клетки, тем не менее, у каждой третьей пациентки тяжелая дисплазия может уйти в среднюю и легкую степень и даже исчезнуть. Проблема в одном – нельзя сказать у кого в будущем будет рак шейки матки, а кто им не заболеет.
Риск рака реален у женщины с длительной цервикальной неоплазией, поэтому оперируют даже легкую дисплазию, не исчезнувшую после 36 месяцев наблюдения. Кстати, инфицирование ВПЧ не обещает обязательной дисплазии, у каждой четвертой зараженной женщины вирус не внедряется внутрь клеток – «проносится» мимо к выходу из половых путей.
Диагностика заболевания
Дисплазия слизистой не болит, не мешает жить – у неё нет симптомов.
Самый простой способ выявления патологии слизистой шейки матки был придуман Папаниколау в 1940-х годах и состоял он из взятия соскоба поверхностных клеток. Сегодня применяется модифицированный инструментарий, позволяющий собрать больше материала. Исследование клеток под микроскопом – цитология позволяет определиться во следующим диагностическим этапом – кольпоскопией.
Расширенная кольпоскопия – осмотр тканей под большим увеличением от пятикратного до 30-кратного, с дополнительным усилением «картинки» специальными обработками растворами, что помогает выбору оптимального места для взятия кусочка ткани – биопсии участка дисплазии. Кусочки слизистой размером не менее 3 миллиметров отправляются на микроскопию – гистологию. Биопсия исключается при воспалении и инфекциях, но только на время.

Дальше при морфологическом подтверждении дисплазии проводится выскабливание слизистой оболочки цервикального канала для выявления его изменений, у женщины дисплазия может локализоваться в железистых криптах – ямках слизистой и зона эпителиального перехода способна смещаться выше. Выскабливание визуализирует скрытый от глаза патологический субстрат.
Лечение дисплазии
При врожденных дисплазиях радикального лечение не существует, при некоторых опасных для жизни пороках развития проводятся операции, но вся терапия направлена только на уменьшение симптомов с увеличением двигательной активности и паллиативная по своей сути.
При дисплазии суставов разработаны эффективные, но тягостные методики многомесячной фиксации для создания покоя и предоставления времени для не случившегося во внутриутробном периоде развития.
При дисплазии желудка проводится избавление от хеликобактерии, налаживается ритм питания, модифицируется диета и образ жизни в сторону нормального, используются защищающие слизистую от повреждений лекарственные средства.
Лечение дисплазии шейки матки зависит от её выраженности: при легкой степени дисплазии прибегают к консервативным мероприятиям. Вирус папилломы человека устойчив к лекарственному воздействию, но его жизнедеятельность поддерживают нарушения слизистой оболочки при хроническом воспалении, способствует снижение иммунитета при гормональных нарушениях и системных заболеваниях.
Здоровой женщине проще избавится от ВПЧ, но при наличии у неё болезней необходимо помочь организму – излечить острое воспаление, перевести хронический процесс в длительную ремиссию, добиться гормонального баланса, нормализовать сахар и другие элементы крови.
При длительно существующей CIN I, которую наблюдают почти 3 года без тенденции ткани к нормализации структуры, тоже оперируют – удаляют сектор шейки. Сектор похож на геометрическую фигуру – конус, отсюда и название операции – конизация.
Среднюю и тяжелую дисплазию лечат только хирургией – проводится конизация шейки матки радиоволновым или лазерным методами. Операция высокоэффективна, почти не оставляет рубцов и не мешает в дальнейшем забеременеть и выносить ребенка.
Восстановительный период
Биопсия шейки матки для диагностики дисплазии при правильном выполнении не чревата проблемами, но некоторым пациенткам с хроническими воспалительными процессами половой сферы требуется профилактическое применение антибиотиков. Не допускается использование в послеоперационном периоде вагинальных тампонов и промывания влагалища, на 2 недели также исключается половая жизнь.
После конизации по поводу дисплазии несколько дней беспокоят не столько боли, сколь неприятные ощущения внизу живота. Будут и выделения, в первые дни могут быть прожилки крови или окрашивание кровью. С течением времени выделения осветляются и уменьшается их количество. Длительность истечения зависит от скорости заживления. Возможно усиление менструации. На полное восстановление слоя слизистой потребуется несколько недель, период ограничений увеличивается, как минимум до месяца, то есть на это время полностью исключается секс, тампоны, спринцевания и высокие физические нагрузки.
Восстановление обязательно должен контролировать врач. Результат лечения оценивает контрольная кольпоскопия и соскоб слизистой – не должно быть признаков атипии и участков дисплазии.
Предраковые процессы и дисплазии умеют лечить обычные гинекологи, но наблюдение специалиста с онкологической подготовкой, тем более в специализированной онкологической клинике поднимает диагностику и терапию на должный уровень качества.
Читайте также:

