Бобровая струя при лечении свищей
Обновлено: 28.04.2024
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для ингибирования соляной кислоты париетальными клетками слизистой оболочки желудка чаще всего используются блокаторы Н2-рецепторов гистамина второго (ранитидин) и третьего (фамотидин) поколений, несколько реже — ингибиторы протонного насоса (омепразол, рабепразол), а для нейтрализации уже выделенной в полость желудка соляной кислоты — антацидные препараты. Антацидные препараты иногда применяются в лечении больных, страдающих так называемыми «кислотозависимыми» заболеваниями, в сочетании с Н2-блокаторами рецепторов гистамина; иногда в качестве терапии по «требованию» в сочетании с ингибиторами протонного насоса. Одна или две «разжеванные» антацидные таблетки не оказывают значительного эффекта [10] на фармакокинетику и фармакодинамику фамотидина, применяемого в дозе 20 мг.
Между этими медикаментозными препаратами существуют определенные различия, перечислим основные из них: различные механизмы действия; скорость наступления терапевтического эффекта; продолжительность действия; разная степень эффективности их терапевтического действия в зависимости от времени приема препарата и приема пищи; стоимость медикаментозных препаратов [1]. Вышеперечисленные факторы не всегда учитываются врачами при лечении больных.
В последние годы в литературе все чаще обсуждаются вопросы фармакоэкономической эффективности использования в терапии «кислотозависимых» заболеваний различных медикаментозных препаратов, применяющихся по той или иной схеме [2, 7]. Стоимость обследования и лечения больных особенно важно учитывать в тех случаях, когда больные в силу особенностей заболевания нуждаются в продолжительном лечении [4, 6], например при гастроэзофагеальной рефлюксной болезни (ГЭРБ). Это весьма распространенное заболевание, обследование и лечение таких пациентов требуют значительных расходов.
Как известно, у большей части больных ГЭРБ отсутствуют эндоскопические признаки рефлюкс-эзофагита. Однако по мере прогрессирования ГЭРБ появляются патологические изменения слизистой оболочки пищевода. Симптомы этого заболевания оказывают на качество жизни такое же воздействие, что и симптомы других заболеваний, включая и ишемическую болезнь сердца [5]. Замечено [8] отрицательное воздействие ГЭРБ на качество жизни, особенно на показатели боли, психическое здоровье и социальную функцию. У больных, страдающих ГЭРБ, высок риск появления пищевода Барретта, а затем и аденокарциномы пищевода. Поэтому при первых же клинических симптомах ГЭРБ, особенно при возникновении эндоскопических признаков эзофагита, необходимо уделять достаточное внимание своевременному обследованию и лечению таких больных.
В настоящее время лечение больных ГЭРБ проводится, в частности, препаратом фамотидин (гастросидин) в обычных терапевтических дозировках (по 20 мг или по 40 мг в сутки). Этот препарат обладает рядом достоинств: удобство применения (1-2 раза в сутки), высокая эффективность в терапии «кислотозависимых» заболеваний, в том числе и по сравнению с антацидными препаратами [9], а также большая безопасность по сравнению с циметидином. Однако наблюдения показали [1], что в ряде случаев для повышения эффективности терапии целесообразно увеличение суточной дозы гастросидина, что, по некоторым наблюдениям [1], снижает вероятность появления побочных эффектов по сравнению с использованием в повышенных дозах блокаторов Н2-рецепторов гистамина первого (циметидин) и второго (ранитидин) поколений. Преимущество фамотидина [11] перед циметидином и ранитидином заключается в более продолжительном ингибирующем эффекте на секрецию соляной кислоты обкладочными клетками слизистой оболочки желудка.
Существуют и другие преимущества блокаторов Н2-рецепторов гистамина (ранитидина или фамотидина) перед ингибиторами протонного насоса; в частности, назначение этих препаратов на ночь позволяет эффективно использовать их в лечении больных из-за отсутствия необходимости соблюдать определенную «временную» связь между приемом этих препаратов и пищи. Назначение некоторых ингибиторов протонного насоса на ночь не позволяет использовать их на полную мощность: эффективность ингибиторов протонного насоса снижается, даже если эти препараты приняты больными вечером и за час до приема пищи. Однако суточное мониторирование рН, проведенное у больных, лечившихся омезом (20 мг) или фамотидином (40 мг), свидетельствует [3] о том, что продолжительность действия этих препаратов (соответственно 10,5 ч и 9,4 ч) не перекрывает период ночной секреции, и в утренние часы у значительной части больных вновь наблюдается «закисление» желудка. В связи с этим необходим и утренний прием этих препаратов.
Определенный научно-практический интерес вызывает изучение эффективности и безопасности использования фамотидина и омеза (омепразола) в более высоких дозировках при лечении больных, страдающих «кислотозависимыми» заболеваниями верхних отделов желудочно-кишечного тракта.
Нами изучены результаты клинико-лабораторного и эндоскопического обследования и лечения 30 больных (10 мужчин и 20 женщин), страдающих ГЭРБ в стадии рефлюкс-эзофагита. Возраст больных — от 18 до 65 лет. При поступлении в ЦНИИГ у 30 пациентов выявлены основные клинические симптомы ГЭРБ (изжога, боль за грудиной и/или в эпигастральной области, отрыжка), у 25 больных наблюдались клинические симптомы, в основном ассоциируемые с нарушением моторики верхних отделов желудочно-кишечного тракта (чувство быстрого насыщения, переполнения и растяжения желудка, тяжесть в подложечной области), обычно возникающие во время или после приема пищи. Сочетание тех или иных клинических симптомов, частота и время их возникновения, а также интенсивность и продолжительность у разных больных были различными. Каких-либо существенных отклонений в показателях крови (общий и биохимический анализы), в анализах мочи и кала до начала терапии не отмечено.
При проведении эзофагогастродуоденоскопии (ЭГДС) у 21 больного выявлен рефлюкс-эзофагит (при отсутствии эрозий), в том числе у 4 больных обнаружена рубцово-язвенная деформация луковицы двенадцатиперстной кишки и у одного больного — щелевидная язва луковицы двенадцатиперстной кишки (5 больных страдали язвенной болезнью двенадцатиперстной кишки, сочетающейся с рефлюкс-эзофагитом). Кроме того, у одной больной обнаружена пептическая язва пищевода на фоне рефлюкс-эзофагита и у 8 больных — эрозивный рефлюкс-эзофагит. У всех больных, по данным ЭГДС, обнаружена недостаточность кардии (в сочетании с аксиальной грыжей пищеводного отверстия диафрагмы или без нее).
В лечении таких пациентов использовался гастросидин (фамотидин) в дозировке 40-80 мг в сутки в течение 4 недель (первые 2-2,5 недели лечение проводилось в стационаре ЦНИИГ, в последующие 2 недели пациенты принимали гастросидин в амбулаторно-поликлинических условиях). Терапию гастросидином всегда начинали и продолжали при отсутствии выраженных побочных эффектов, пациентам назначали по 40 мг 2 раза в сутки в течение 4 недель; лишь при появлении диареи и крапивницы дозировку гастросидина уменьшали до 40 мг в сутки.
Исследование было выполнено с учетом критериев включения и исключения больных из исследования согласно правилам клинической практики.
При проведении ЭГДС определяли НР, используя быстрый уреазный тест (один фрагмент антрального отдела желудка в пределах 2-3 см проксимальнее привратника) и гистологическое исследование биопсийного материала (два фрагмента антрального отдела в пределах 2-3 см проксимальнее привратника и один фрагмент тела желудка в пределах 4-5 см проксимальнее угла желудка). При обследовании больных при необходимости проводили УЗИ органов брюшной полости и рентгенологическое исследование желудочно-кишечного тракта. Полученные данные, включая и выявленные побочные эффекты, регистрировали в истории болезни.
В период проведения исследования больные дополнительно не принимали ингибиторы протонного насоса, блокаторы Н2-рецепторов гистамина или другие так называемые «противоульцерогенные» препараты, включая антацидные препараты и средства, содержащие висмут. 25 из 30 пациентов (84%) из-за наличия клинических симптомов, ассоциируемых чаще всего с нарушением моторики верхних отделов пищеварительного тракта, дополнительно получали прокинетики: домперидон (мотилиум) в течение 4 недель или метоклопрамид (церукал) в течение 3-4 недель.
Лечение больных ГЭРБ в стадии рефлюкс-эзофагита всегда начинали с назначения им гастросидина по 40 мг 2 раза в сутки (предполагалось, что в случае появления существенных побочных эффектов доза гастросидина будет уменьшена до 40 мг в сутки). Через 4 недели от начала лечения (с учетом состояния больных) при наличии клинических признаков ГЭРБ и (или) эндоскопических признаков эзофагита терапию продолжали еще в течение 4 недель. Через 4-8 недель по результатам клинико-лабораторного и эндоскопического обследования предполагалось подвести итоги лечения больных ГЭРБ.
При лечении больных гастросидином (фамотидином) учитывались следующие факторы: эффективность гастросидина в подавлении как базальной и ночной, так и стимулированной пищей и пентагастрином секреции соляной кислоты, отсутствие изменений концентрации пролактина в сыворотке крови и антиандрогенных эффектов, отсутствие влияния препарата на метаболизм в печени других лекарственных средств.
Двое из 30 больных (6,6%) через 2-3 дня от начала лечения отказались от приема гастросидина, с их слов, из-за усиления болей в эпигастральной области и появления тупых болей в левом подреберье, хотя объективно состояние их было вполне удовлетворительным. Эти больные были исключены из исследования.
По данным ЭГДС, через 4 недели лечения у 17 пациентов из 28 (60,7%) исчезли эндоскопические признаки рефлюкс-эзофагита, у 11 — отмечена положительная динамика — уменьшение выраженности эзофагита. Поэтому в дальнейшем этих больных лечили гастросидином в амбулаторно-поликлинических условиях в течение еще 4 недель по 40 мг 2 раза в сутки (7 больных) и по 40 мг 1 раз в сутки (4 больных, у которых ранее была снижена дозировка гастросидина).
Весьма спорным остается вопрос — рассматривать ли рефлюкс-эзофагит, нередко наблюдаемый при язвенной болезни (чаще всего при язвенной болезни двенадцатиперстной кишки), как осложнение этого заболевания или же считать его самостоятельным, сопутствующим язвенной болезни заболеванием? Наш многолетний опыт наблюдений показывает, что, несмотря на некоторую связь ГЭРБ и язвенной болезни (их относительно частое сочетание и даже появление или обострение рефлюкс-эзофагита в результате проведения антихеликобактерной терапии), все же язвенную болезнь и ГЭРБ (в том числе и в стадии рефлюкс-эзофагита) следует считать самостоятельными заболеваниями. Мы неоднократно наблюдали больных с частыми обострениями ГЭРБ в стадии рефлюкс-эзофагита (при наличии у них рубцово-язвенной деформации луковицы двенадцатиперстной кишки). Последнее обострение язвенной болезни (с образованием язвы в луковице двенадцатиперстной кишки) у этих больных отмечалось 6-7 и более лет назад (значительно реже, чем рецидивы ГЭРБ в стадии рефлюкс-эзофагита), однако при очередном обострении язвенной болезни с образованием язвы в луковице двенадцатиперстной кишки всегда при эндоскопическом исследовании выявляли и рефлюкс-эзофагит. Мы уверены, что при наличии современных медикаментозных препаратов лечить неосложненную язвенную болезнь значительно легче, чем ГЭРБ: период терапии при обострении язвенной болезни двенадцатиперстной кишки занимает значительно меньше времени по сравнению с терапией ГЭРБ; да и в период ремиссии этих заболеваний пациенты с язвенной болезнью двенадцатиперстной кишки чувствуют себя более комфортно, в то время как больные ГЭРБ вынуждены для улучшения качества жизни отказываться от приема значительно большего количества продуктов и напитков.
При обследовании (через 8 недель лечения) трое из 11 больных по-прежнему предъявляли жалобы, ассоциированные с нарушением моторики верхних отделов желудочно-кишечного тракта. Трое больных при хорошем самочувствии отказались от проведения контрольной ЭГДС через 8 недель. По данным ЭГДС, у 7 из 8 больных отмечено исчезновение эндоскопических признаков эзофагита (в том числе у одной больной — заживление пептической язвы пищевода).
Определение НР проводилось у всех 30 больных: в 11 случаях выявлена обсемененность НР слизистой оболочки желудка (по данным быстрого уреазного теста и гистологического исследования материалов прицельных гастробиопсий). Антихеликобактерная терапия в период лечения больным ГЭРБ в стадии рефлюкс-эзофагита не проводилась.
При оценке безопасности проведенного лечения каких-либо значимых отклонений в лабораторных показателях крови, мочи и кала отмечено не было. У 4 больных (13,3%), у которых ранее наблюдался «нормальный» (регулярный) стул, на 3-й день лечения гастросидином (в дозе 40 мг 2 раза в сутки) был отмечен, с их слов, «жидкий» стул (кашицеобразный, без патологических примесей), в связи с чем доза гастросидина была уменьшена до 40 мг в сутки. Через 10-12 дней после снижения дозы стул нормализовался без какой-либо дополнительной терапии. Интересно отметить, что еще у 4 больных, которые ранее страдали запорами, на фоне проводимого лечения стул нормализовался на 7-й день. У 3 из 30 больных (10%) на 3-4-й день приема гастросидина появились высыпания на коже туловища и конечностей (крапивница). После уменьшения дозировки гастросидина до 40 мг в сутки и проведения дополнительного лечения диазолином (по 0,1 г 3 раза в день) высыпания на коже исчезли.
Проведенные исследования показали целесообразность и эффективность терапии ГЭРБ в стадии рефлюкс-эзофагита гастросидином по 40 мг 2 раза в сутки, особенно при лечении больных с выраженными болевым синдромом и изжогой. Такое лечение может успешно проводиться в стационарных и амбулаторно-поликлинических условиях. Изучение отдаленных результатов проведенного лечения позволит определить продолжительность периода ремиссии этого заболевания и целесообразность лечения гастросидином в качестве «поддерживающей» терапии или же терапии «по требованию».
Три четверти пациентов с коронавирусной инфекцией сталкиваются с нарушением обоняния (гипосмией или аносмией) и вкуса. У 10% переболевших способность адекватно различать запахи не восстанавливается больше полугода. Это серьёзная проблема, над её решением работают ведущие учёные.

Почему происходит изменение обоняния и вкуса после ковида?
Врачи часто сталкиваются с заболеваниями, при которых пациент не различает запахи. Вот некоторые примеры.
- Болезнь Паркинсона. Больного беспокоят тремор конечностей, нарушение походки, мышечная скованность. Именно с этими симптомами он обращается к врачу. Но лет за 5 до появления двигательных нарушений пациенты могут отметить, что снижается обоняние.
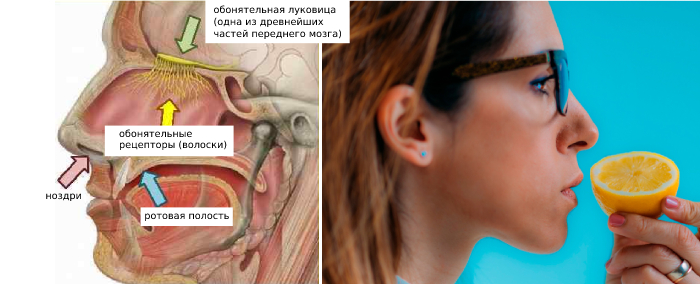
- Опухоли. Ощущение запахов пропадает при поражении мозга, если затронута обонятельная луковица – особая зона, где находятся обонятельные нейроны.
- Муковисцидоз. Наследственное заболевание. Аносмия появляется в первые два года.
- Рецепторы перестают полноценно формировать нервный импульс.
- ОРВИ, аллергический ринит, полипы в носовой полости. Гипосмия связана с отёком слизистой носа. Именно он блокирует чувствительные волоски.
Возможно ли вернуть обоняние и вкус?
Параллельно снижению обоняния происходит нарушение вкусового восприятия. Это логичный процесс. Улавливаемый человеком аромат блюд усиливает вкус, делает его более насыщенным. Когда человек не воспринимает запаха еды, он не может полноценно оценить её вкуса. При восстановлении обонятельной чувствительности возвращается вкусовое восприятие.
Способность различать запахи и вкус можно вернуть. Сделать это тем проще, чем раньше начать лечение. Похоже на ситуацию с инсультом. После сосудистой катастрофы в головном мозге нужно как можно быстрее оказать человеку помощь, приступить к восстановлению двигательной активности в самые ранние сроки.
При коронавирусной инфекции так же – чем быстрее начата реабилитация, тем лучше прогноз. Обонятельные нейроны обладают способностью к восстановлению, обновляясь примерно раз в 40 дней. Для того, чтобы они быстрее заработали, ими нужно активно заниматься.
Почему не все переболевшие коронавирусной инфекцией теряют обоняние?
Аносмия обычно развивается на 4–6 день заболевания. На 10–14 день большинство людей выздоравливают и способность различать ароматы возвращается. Но у некоторых дефект остаётся. Нужно понимать, любое заболевание не может протекать одинаково у разных людей. Нет двух идентичных организмов, соответственно, и болезни будут протекать по-разному.
- Вирусная нагрузка – число микробов, попавших в организм. Чем больше, тем тяжелее протекает заболевание.
- Вирулентность вируса – сила его деструктивного (повреждающего) воздействия. У разных типов и подтипов коронавирусов разная. Не стоит забывать, что вирусы мутируют, меняются.
- Иммунная память. Чем больше ОРВИ в своей жизни перенёс человек, тем легче болеет коронавирусом, тем меньше риск возникновения осложнений.
- Сопутствующие заболевания человека: сахарный диабет, ожирение, тяжёлые формы гипертонии, дыхательная недостаточность. А если эти заболевания сочетаются – коронавирусная инфекция протекает ещё тяжелее.
Что необходимо делать, чтобы вернуть обоняние?
Раздражать рецепторы и восстанавливать цепочку проводящего пути. Заставлять нервные клетки работать, вспоминать свои функции. Для этого хорошо подходят кофе, мелисса, мята, чеснок. Применяется ароматерапия с помощью эфирных масел: гвоздики, цитрусовых, эвкалипта. Вдыхать ароматы надо 5–6 раз в день. При отёке слизистой оболочки помогут орошения полости носа солевыми растворами. Разрешается использовать специальные спреи, даже гормональные. Их должен назначить врач оториноларинголог, потому что есть противопоказания.
Невролог может прописать препараты, улучшающие трофику нервной ткани, в том числе и обонятельных рецепторов, а также порекомендовать рефлексотерапию.
Рефлексотерапия. Что это? Как можно с её помощью вернуть обоняние?
Рефлексотерапию медики относят к физиотерапии. Она улучшает кровоснабжение, иннервацию, лимфоотток, способствует улучшению самочувствия. При помощи рефлексотерапии можно вернуть обоняние. Это не новый метод лечения, он использовался и раньше. Рефлексотерапия хорошо помогает в лечении аллергических ринитов и даже инфекционных.
Иглорефлексотерапия – постановка игл, может сочетаться с прижиганием. Внутренние органы на поверхности кожи имеют свои проекции, которые называются чудесными меридианами. Врач воздействует на биологически активные точки определённой зоны, вследствие чего происходит улучшение микроциркуляции, лимфотока, устранение отёка, улучшение обоняния. Восстанавливая циркуляцию энергии по древнему китайскому учению, мы восстанавливаем здоровье.
ВИДЕО с участием врача-невролога Лебедевой Л.В.
Для пациентов, столкнувшихся с такой проблемой, как коронавирусная инфекция (covid-19) специально разработаны программы постковидной диагностики и реабилитации: ПОСТКОВИДНЫЙ СИНДРОМ и ПОСТКОВИДНЫЙ СКРИНИНГ.
В этом месяце жителям районов Савеловский, Беговой, Аэропорт, Хорошевский» предоставляется скидка 5% на ВСЕ мед.
Скидки для друзей из социальных сетей!
Эта акция - для наших друзей в "Одноклассниках", "ВКонтакте", "Яндекс.Дзене", YouTube и Telegram! Если вы являетесь другом или подписчиком стр.
Гуляев Сергей Викторович
Врач-ревматолог, терапевт, нефролог
Кандидат медицинских наук
Мы в Telegram и "Одноклассниках"
Подагра: диагностика и лечение
Подагра (в переводе с греческого языка – «нога в капкане») – заболевание, возникающее в результате нарушения обмена мочевой кислоты и характеризующееся периодическими атаками острого артрита, чаще всего в области большого пальца стопы. При этой болезни кристаллы мочевой кислоты (моноурат натрия) начинают накапливаться в различных тканях, прежде всего в области суставов, почках и других органах.
Подагра – болезнь достаточно древняя и известна еще со времен Гиппократа, который одним из первых дал подробную характеристику основных симптомов болезни и связал ее развитие с перееданием. В средние века подагра считалась заболеванием королевских особ и аристократии, склонных к обильным застольям.
Сегодня «болезнь аристократии и королей» широко распространена в разных социальных слоях общества, однако всех больных объединяет одно – склонность к чрезмерному употреблению мясных продуктов. По-видимому, это частично объясняет тот факт, что мужчины болеют подагрой в 10 раз чаще, чем женщины. Однако неправильный образ жизни, «перекосы» в питании (в частности увлечение новомодными «белковыми» диетами) делают и современных женщин уязвимыми перед этим заболеванием.

Что такое подагра?
В настоящее время подагра считается системным заболеванием, поскольку помимо суставов поражает практически весь организм.
Нарушение так называемого пуринового обмена приводит к повышению концентрации мочевой кислоты в крови и моче, образованию уратных кристаллов и их отложению в мягких тканях, в том числе в области суставов верхних и нижних конечностей. Со временем отложения кристаллов мочевой кислоты (ураты) формируют узелковые подкожные образования - тофусы, которые хорошо видны невооруженным глазом и позволяют врачу поставить диагноз даже при обычном внешнем осмотре. Однако задолго до образования тофусов болезнь проявляет себя приступообразным, необычно тяжелым воспалением суставов - подагрическим артритом (чаще всего располагающимся в области большого пальца стопы, хотя возможно поражение других суставов, чаще ног).
При подагре поражаются внутренние органы, в частности почки, которые длительное время работают в условиях повышенной нагрузки, связанной с необходимостью выведения мочевой кислоты из крови. Со временем развивается мочекаменная болезнь, усугубляющая негативное действие мочевой кислоты на почечную ткань. Дополнительным повреждающим фактором является частый и как правило бесконтрольный прием обезболивающих средств по поводу болей в суставах. Постепенно функция почек нарушается – формируется почечная недостаточность, которая и определяет окончательный прогноз болезни
Виды подагры
Подагра может быть первичной и вторичной.
Первичная подагра передается по наследству и связана с недостаточной функцией ферментов, участвующих в регуляции уровня мочевой кислоты.
Вторичная подагра развивается на фоне уже имеющегося заболевания, при котором в силу тех или иных причин отмечается повышенное образование мочевой кислоты, например, при заболеваниях крови или хронических болезнях почек. В таких случаях лечение должно быть направлено на лечение болезни, приведшей к развитию вторичной подагры.
Нормальными считаются следующие показатели уровня мочевой кислоты в крови:
- у мужчин моложе 60 лет - 250-450 мкмоль /л; старше 60 лет - 250-480 мкмоль /л;
- у женщин до 60 лет - 240-340 мкмоль /л; в более старшем возрасте – 210-430 мкмоль /л;
- у детей до 12 лет – 120-330 мкмоль /л.
Превышение этих показателей указывает на нарушение обмена мочевой кислоты и повышенный риск развития симптомов, свойственных подагре. В такой ситуации необходимо пройти обследование для уточнения причины такого нарушения, а также своевременного выявления заболеваний, ведущих к повышению уровня мочевой кислоты. Раннее выявление таких фоновых заболеваний в ряде случаев позволяет своевременно начать лечение и избежать опасных для жизни осложнений. При длительном нарушении обмена мочевой кислоты с повышенным выведением ее с мочой неизбежно развивается мочекаменная болезнь и в конечном итоге почечная недостаточность.
Клиническая картина
Классический острый приступ подагры возникает внезапно, как правило, ночью на фоне хорошего общего здоровья. Развитию приступа обычно предшествуют события, предрасполагающие к резкому повышению уровня мочевой кислоты к крови – фуршеты, дни рождения, застолья с обильным употреблением мясных продуктов. Последние, как известно, нередко используются в качестве закуски после приема алкогольных напитков. Сочетание этих факторов крайне неблагоприятно, поскольку алкоголь ухудшает выведение мочевой кислоты с мочой, что быстро приводит к «скачку» мочевой кислоты в крови и созданию необходимых условий для развития подагрического артрита. Еще одним фактором, предрасполагающим к обострению или возникновению приступа суставной подагры, является обезвоживание организма, что нередко случается при обильном потоотделении после посещения бани или сауны. Спровоцировать начало обострения подагры могут также переохлаждение и травма, в том числе незначительная травма, например, ношение тесной обуви. Приступ подагры достаточно однотипен: возникает чрезвычайно интенсивная боль в 1 плюснефланговом суставе (сустав большого пальца), он резко опухает, становится горячим и красным, а затем сине-багрового цвета. Функция сустава нарушается, больной не может даже пошевелить пальцем.
Приступы подагры обычно продолжаются в течение 3-10 дней, затем боли постепенно исчезают, кожа приобретает нормальный цвет, сустав вновь начинает действовать. Следующий приступ подагры может появиться через несколько месяцев или даже лет. Однако со временем «светлые» периоды становятся все короче и короче.
Если подагрический артрит переходит в хроническую форму, то это приводит к деформации суставов и нарушению их функции.
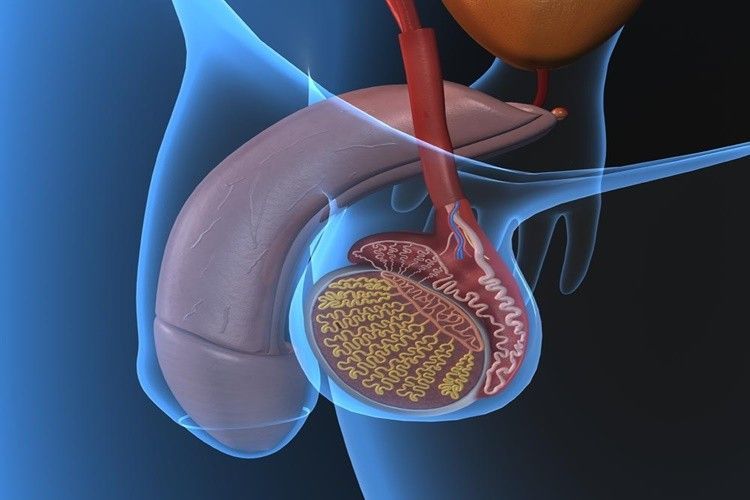
Воспалительные процессы бактериальной и небактериальной этиологии в мужской железе – распространенная патология. Она требует обязательной медицинской помощи, поскольку без адекватной терапии может серьезно подорвать здоровье, привести к бесплодию, импотенции. Что нельзя делать при простатите у мужчин и как правильно проходить лечение, читайте в статье ниже.
Алкоголь
Регулярное употребление алкогольных напитков оказывает разрушительное действие на организм: снижается иммунитет, ухудшается способность тела противостоять инфекциям. Спирт нарушает нормальное кровоснабжение органов малого таза, приводит к застойным явлениям, ухудшает метаболизм предстательной железы.
Многие пациенты интересуются возможностью употребления легкого алкоголя, в частности пива. Его также не рекомендуется пить постоянно и во время лечения. Подобные напитки способствуют изменению гормонального баланса, снижают выработку тестостерона. Это негативно отражается на здоровье мужской железы.
Антибактериальная терапия – еще один ответ на вопрос, почему нельзя пить при простатите. Инфекционное поражение – основание для назначения антибиотиков. Практически все препараты этой группы несовместимы с алкоголем и дают тяжелые побочные реакции, которые могут нести угрозу не только здоровью, но и жизни пациента. Исключение спиртных напитков из рациона –важный фактор успеха в терапии простатита.

Что нельзя есть при простатите
Пациенты часто спрашивают, почему нельзя острое при простатите или существуют другие запреты. Поскольку мужская железа тесно связана с мочевым или желудочно-кишечным трактом, предполагается ряд ограничений в питании. Рацион при заболевании обязан базироваться на разумном балансе белков, жиров и углеводов. В достаточном количестве должны присутствовать клетчатка, витамины и минералы.
В периоды обострения врачи рекомендуют воздержаться от продуктов, способствующих газообразованию: капусты, бобовых, редиса.
Следует ограничить прием продуктов, которые способствуют развитию запоров. Сюда относятся жирное мясо, жареные блюда, копчености, вяленая рыба, выпечка, изделия из белой муки, майонез.
Раздражающее действие на мочеполовую систему может оказывать избыточное содержание соли и кислоты в продуктах питания. Чтобы снизить нагрузку на почки, во время лечения простатита запрещается употребление солений, маринадов, уксуса, пряностей, острых приправ. Избегают приема крепкого чая и кофе.

Интенсивные физические усилия
Хотя малоподвижный образ жизни является одной из причин застойных явлений в малом тазу, однако активные физические нагрузки при воспалении противопоказаны. Стимуляция кровообращения в промежности может интенсифицировать процесс воспаления, усилить болевой синдром, привести к отечности.
В острой фазе рекомендуют воздержаться от следующих видов нагрузки:
поднятие и перемещение тяжестей;
приседания с дополнительным весом;
езда на велосипеде;
Недостаточная активность
Что нельзя при хроническом простатите – частый вопрос, которые задают пациенты. Длительная сидячая работа без смены положения и физической нагрузки приводит к застою кровообращения в малом тазу. Это ухудшает трофику и метаболизм органа, способствует развитию воспалительных процессов.
При патологии рекомендуют плавание, спортивную ходьбу, легкие кардиотренировки. Существует комплекс Кегеля – это специальные упражнения, которые тренируют мышцы тазового дна и улучшают питание мужской железы.

В список того, чего нельзя делать при простатите, уверено попадают такие мероприятия как: баня, сауна и горячая ванна. Перегрев вызывает активный приток крови и способствует разносу инфекции по организму, может развиться отек. При обострении врачи рекомендуют предпочитать душ для поддержания гигиены.
Незащищенный секс
При сильном болевом синдроме с повышенной температурой тела пациент вряд ли будет заинтересован в сексуальном контакте. Однако хроническая стадия протекает в большинстве случаев без выраженных болевых ощущений и изменения соматического состояния.
Регулярная сексуальная жизнь показана при простатите. Сокращение мышц тазового дна во время эякуляции, выделения сока при семяизвержении предупреждают застойные явления. Однако важно соблюдать гигиену сексуальных отношений.
Лечение бактериального простатита следует проводить вместе с партнершей, чтобы не получить вторичное инфицирование. Также во время терапии важно использовать барьерный метод защиты, чтобы предупредить заражение другими патогенами, которые могут спровоцировать рецидив заболевания.
Что нельзя при простатите у мужчин – часто интересует пациентов. Специалисты клиники Dr. AkNer готовы ответить на все ваши вопросы, провести комплексное обследование и назначить адекватную терапию.
Эффективное лечение эректильной дисфункции в клинике Dr. AkNer. Опытный андролог, сексопатолог и уролог со стажем более 40 лет. Новейшие методы терапии.

Лечение эректильной дисфункции: честно об очень деликатной проблеме
Даже полностью здоровые мужчины могут сталкиваться с проблемами с эрекцией, причем по самым разным причинам. Чаще всего в таких случаях имеет место эректильная дисфункция. Нередко ее еще называют импотенцией, но с точки зрения медицины это немного разные проблемы.
Эректильная дисфункция у мужчин проявляется в виде снижения качества и продолжительности эрекции, а также трудностях, которые появляются перед ее возникновение. Это более широкое понятие, нежели импотенция, означающая невозможность совершить половой акт, т. е. полное отсутствие эрекции. В связи с этим лечение эректильной дисфункции и импотенции может отличаться. Все зависит от причины проблемы и того, насколько она запущена, поэтому здесь важно вовремя обратиться к врачу.
Что такое эректильная дисфункция
Эректильной дисфункцией называют состояние, при котором в течение более 3 месяцев мужчине не удается достичь или поддерживать эрекцию полового члена, необходимую для совершения полового акта.
Эрекцией, в свою очередь, называется увеличение полового члена вследствие наполнения его тканей кровью во время возбуждения. Импотенция — это отсутствие эрекции, крайняя степень эректильной дисфункции, при которой половой акт невозможен ни при каких условиях.
Почему может возникать эректильная дисфункция
Все существующие причины импотенции у мужчин делятся на следующие группы:
- Органические. Связаны с состоянием организма, когда для эрекции есть какое-либо физиологическое препятствие. Риск импотенции повышают курение и злоупотребление алкоголем.
- Психогенные. Проблемы с эрекцией обусловлены психологическим состоянием мужчины: сильными переживаниями, стрессом, депрессией, проблемами в отношении с сексуальным партнером.
- Смешанные. Здесь на мужчину влияют как органические, так и психогенные факторы.
Во многих случаях причиной эректильной дисфункции становятся проблемы с сосудами, связанные с возрастными изменениями их стенок. К примеру, при поражении сосудов холестериновыми бляшками появляются препятствия для нормального тока крови, поэтому она не может наполнить кавернозные тела полового члена. Поэтому так важно вовремя посетить врача, поскольку проблемы с сосудами повышают риск инсульта и инфаркта.
Среди сосудистых проблем к эректильной дисфункции и импотенции могут приводить:
- атеросклероз;
- травмы живота и таза, повреждающие сосуды, питающие половой член;
- сахарный диабет;
- гипертония.
Какими симптомами проявляется
Выраженность симптомов эректильной дисфункции может варьироваться от незначительных проявлений до серьезных расстройств. Характерные признаки:
- уменьшение или исчезновение спонтанных эрекций;
- снижение способности к повторным половым актам в течение суток;
- уменьшение числа полноценных половых актов с эякуляцией;
- невозможность вызвать эрекцию при мастурбации;
- необходимость дополнительной эротической стимуляции;
- недостаточная интенсивность эрекции.
Из-за проблем в половой сфере мужчина становится раздражительным и нервозным. У него может развиться депрессия, ухудшиться настроение.
Основным симптомом импотенции у мужчин выступает полное отсутствие эрекции. Еще к признакам можно отнести эякуляцию раньше времени, длительное семяизвержение и ослабленную эрекцию.
Виды эректильной дисфункции
В зависимости причины возникновения выделяют следующие виды импотенции:
- Эндокринная. Связана с недостатком гормона тестостерона.
- Анатомически обусловленная. Возникает из-за искривления полового члена, его частичного или полного удаления, болезненности из-за грыжи в мошонке.
- Нейрогенная. Развивается на фоне заболеваний нервной системы, к примеру, нейропатии или склероза.
- Сосудистая. Объясняется проблемами с сосудами, которые ведут к нарушению кровоснабжения полового члена и невозможности достичь эрекции.
Можно ли вылечить эректильную дисфункцию
Лечение импотенции у мужчин проводится комплексно и обязательно с учетом причины. Для диагностики необходимо обратиться к врачу — сексопатологу. Он проведет осмотр половых органов, задаст интересующие вопросы относительно характера и частоты эрекции, а также назначит нужные обследования: дуплексное УЗИ и компьютерную томографию полового члена, реографию и пр.

Лечение сосудистой импотенции проводится с помощью препаратов, расширяющих сосудов. При недостатке тестостерона назначаются соответствующие заместительные медикаменты. Хороший эффект в лечении эректильной дисфункции пожилых мужчин показывают препараты-ингибиторы фосфодиэстеразы 5-го типа. Они способствуют эрекции, но не влияют на природу возникновения проблемы.
В дополнение к медикаментозному лечению используются:
- психотерапия;
- вакуум-терапия;
- массаж;
- ЛФК.
В клинике Dr. AkNer практикуются наиболее современные и эффективные методы лечения. Здесь мужчинам оказывает помощь уролог, андролог и сексопатолог с опытом более 40 лет. После лечения в клинике 99% мужчин полностью восстановили половую функцию, поэтому и вы можете доверить нам свою деликатную проблему.
Читайте также:

