Антибиотики при цитомегаловирусе и герпесе
Обновлено: 01.05.2024
Цитомегалия – это широко распространенная инфекция вирусного генеза (ЦМВИ), которая характеризуется разнообразными проявлениями: от бессимптомного течения до очень тяжелых, генерализованных форм с поражением внутренних органов и центральной нервной системы. Поскольку данный вирус был открыт сравнительно недавно, в 1956 году, то он считается еще недостаточно изученным, и в научном мире до настоящего времени борьба с ним является предметом активных дискуссий.
Согласно данным ВОЗ, цитомегаловирусная инфекция занимает одно из ведущих мест среди заболеваний, вызываемых герпесвирусами семейства Herpesviridae. Один из видов рода Human betaherpesvirus 5 (вирус герпеса человека 5 типа, общепринятое название – Cytomegalovirus) способен инфицировать человека, вызывая у него цитомегалию. Увеличение распространенности этого заболевания отмечается в настоящее время во всех странах мира. Также встречается такое наименование заболевания, как вирусная болезнь слюнных желез. Раньше цитомегалию называли «болезнью поцелуев» так как она передается в том числе и через слюну.
Суть проблемы ЦМВИ заключается в том, что она относится к так называемым оппортунистическим инфекциям, клиническое проявление которых дает о себе знать лишь в условиях первичного или вторичного иммунодефицита. У лиц с крепкой иммунной системой в подавляющем большинстве случаев инфекция протекает по типу вирусоносительства.
Число больных ЦМВ в разных странах колеблется от 0,2% до 3%, что представляет собой весьма обширную группу жителей нашей планеты. Вирус весьма широко представлен в популяции. Как правило, антитела обнаруживают у 10-15 % подростков и 40 % людей от 30-35 лет. i Распространенность этой инфекции, возможность длительной персистенции (длительного сохранения вируса в организме человека) с поражением различных органов и систем, трудности лабораторной диагностики и отсутствие лекарственных препаратов, которые могли бы раз и навсегда победить эту болезнь, подчеркивают актуальность этой проблемы.
Пути передачи цитомегаловирусной инфекции у взрослых

Современная статистика говорит о том, что на первом году жизни этой инфекцией заражается каждый пятый ребенок. Среди путей заражения наиболее опасным является внутриутробное инфицирование, т.е. во время беременности. Таким образом заражается 5-7% детей. Примерно 30% случаев передачи вируса ребенку происходит во время вскармливания малыша грудью ii . Также дети часто заражаются в детских коллективах. Доля пациентов, у которых можно обнаружить сам вирус в организме, в разных регионах мира колеблется от 44% до 85%. А вот доля болеющих цитомегаловирусной инфекцией людей составляет, по данным из разных источников, 0,2-3%.
Чаще всего заражение происходит при длительных контактах с носителями этого вируса. Он передается следующими путями:
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, а также при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Виды цитомегаловируса
Среди разновидностей цитомегалии выделяют следующие виды:
- Врожденная цитомегаловирусная инфекция, iii которая проявляется в большинстве своем в виде увеличения селезенки и печени. Опасность заболевания также заключается и в возможной желтухе, возникающей на фоне инфекции. Заболевание может привести к нарушению в работе центральной нервной системы, кроме того, у женщин инфекция может спровоцировать внематочную беременность или выкидыш.
- Острая цитомегаловирусная инфекция. В качестве основных путей заражения здесь преимущественно выделяют половые контакты, однако не исключено заражение и при переливании крови. По своим проявлениям цитомегалия в этом случае напоминает обычную простуду, кроме того, отмечается также увеличение слюнных желез и образование на деснах и языке белого налета.
- Генерализованная ЦМВИ. В этом случае заболевание приводит к формированию воспалительных процессов в селезенке, почках, надпочечниках, поджелудочной железе. Как правило, это происходит по причине ослабления иммунитета, при этом заболевание протекает в комплексе с бактериальной инфекцией.
Симптомы цитомегаловируса у мужчин, женщин и детей

ЦМВ инфекция является персистирующей, то есть имеющей хронический характер. Она характеризуется многообразием клинических проявлений, выраженность которых зависит от формы патологии.
При внутриутробном инфицировании могут наблюдаться недоношенность и задержка развития плода, заболевания печени, петехиальная сыпь (мелкие кожные кровоизлияния) и острые воспалительные заболевания сетчатки глаза. Летальность при внутриутробном инфицировании цитомегаловирусом достигает 30%. Из оставшихся в живых детей многим диагностируют отставание в умственном развитии или инвалидность по слуху и зрению. Но все же в большинстве случаев внутриутробное инфицирование не вызывает развития заболевания, а протекает бессимптомно.
У недоношенных младенцев ЦМВИ может привести к увеличению лимфатических узлов, гепатиту, развитию тяжелой пневмонии, к которой часто присоединяется бактериальная инфекция. Таких детей необходимо срочно лечить в условиях стационара.
Цитомегаловирусная инфекция у взрослых приводит к развитию мононуклеозоподобного синдрома, который по своим симптомам напоминает ОРВИ. Заболевание проявляется следующими клиническими признаками:
- повышенная температура тела, которая наблюдается до месяца и более;
- суставные и мышечные боли, головная боль;
- боли в горле;
- выраженные слабость, недомогание, вялость, повышенная утомляемость;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания.
Также могут развиться заболевания печени и редко – пневмония. Длительность течения мононуклеозоподобного синдрома может составлять до 60 и более дней.
Особенно тяжело ЦМВ переносят пациенты, которые страдают синдромом врожденного и приобретенного иммунодефицита (СПИД iv ). Те, кто перенес пересадку внутренних органов и тканей, вынуждены постоянно принимать иммунодепрессанты, что приводит к подавлению иммунных реакций. Это тоже может стать причиной активизации ЦМВИ в организме. Множественное поражение органов этим видом вируса и отсутствие адекватной терапии может привести к их дисфункции и даже гибели пациента.
С целью диагностики данной инфекции проводятся лабораторные исследования и определение в крови специфических антител к цитомегаловирусу – иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении этим заболеванием либо о наличии в организме хронической цитомегаловирусной инфекции. Повышение количества иммуноглобулинов G наблюдается в период затухания активности инфекции. Их наличие в крови говорит о присутствии вируса в организме, но не свидетельствует об активности инфекционного процесса.
Лечение цитомегаловируса: лекарства, применяемые при терапии
На сегодняшний день единого метода лечения и «таблеток», при помощи которых вирус полностью устраняется из организма, не существует. Лекарства от цитомегаловируса, которое позволяло бы навсегда избавиться от заболевания, ученые пока не изобрели. Но все же на сегодняшний день уже существуют противовирусные препараты, применение которых способствует купированию симптомов заболевания и улучшению самочувствия.
Поскольку важным звеном в активации и распространении этой инфекции в организме больного является снижение иммунной защиты, для поддержания иммунитета на необходимом уровне применяются препараты с содержанием интерферонов. Один из таких препаратов – это комплексный противовирусный иммуномодулирующий препарат ВИФЕРОН широкого спектра действия для детей и взрослых. Он обладает двойным действием – способствует блокировке вируса и восстановлению иммунитета. Оригинальная формула препарата включает сочетание интерферона альфа-2b и высокоактивных актиоксидантов (витамины С, Е). Препарат входит в группу цитокинов и обладает универсальным действием при лечении в отношении широкого спектра вирусов и других возбудителей заболеваний.
ВИФЕРОН Свечи при цитомегаловирусе
ВИФЕРОН в виде Свечей (суппозиториев) для лечения цитомегаловируса взрослым можно применять при беременности (с 14-й недели), а также в период грудного вскармливания. Также препарат разрешен детям, в том числе новорожденным и недоношенным. ВИФЕРОН помогает снижать частоту рецидивов 1 и применяется в составе комплексной терапии для борьбы с рядом заболеваний, в том числе инфекционно-воспалительными заболеваниями урогенитального тракта у взрослых (вирус папилломы человека, хламидиоз, цитомегаловирусная инфекция, уреаплазмоз, трихомониаз, гарднереллез, бактериальный вагиноз, рецидивирующий влагалищный кандидоз, микоплазмоз).
Дозировка
Рекомендуемая доза для взрослых – ВИФЕРОН 500 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 5-10 суток. По клиническим показаниям терапия может быть продолжена.
Лечение цитомегаловирусной инфекции - препараты
Подход к лечению ЦМВ-инфекции существенно отличается у реципиентов после аллогенной трансплантации костного мозга (ТКМ) и у больных, подвергающихся химиотерапии (в том числе высокодозной после трансплантации аутологичных стволовых клеток). Больным первой группы необходимо упреждающее лечение, поскольку, несмотря на наличие препаратов, эффективно ингибирующих репликацию вируса, лечение уже развившихся висцеральных поражений эффективно не более чем в половине случаев.
Больным, получающим стандартную химиотерапию, специфическое лечение проводят только при установленном или высоковероятном висцеральном поражении.
Методы контроля ЦМВ-инфекции у реципиентов аллогенного костного мозга зависят от ЦМВ-статуса пары донор — реципиент. При серонегативности как донора, так и реципиента самым надежным способом профилактики ЦМВ-инфекции является использование для трансфузий препаратов крови от серонегативных доноров или лейкодеплеция с помощью фильтров последнего поколения, предназначенных для фильтрации в банках крови. При любом другом сочетании ЦМВ-статусов главные инструменты контроля — еженедельный мониторинг ЦМВ-виремии (методом ПЦР или выявлением антигенемии рр65) и упреждающее лечение ганцикловиром при позитивном результате.
Для начала терапии больных высокого риска (реципиенты неродственной или неполностью совместимой трансплантации, лечение РТПХ антитимоцитарным глобулином) достаточно однократного позитивного анализа. В то же время у больных низкого риска при невысокой вирусной нагрузке назначение специфической терапии можно отложить до повторного позитивного анализа, выполненного с интервалом 3— 5 дней. Этот подход проверен многими исследователями, в том числе нами. Доказано, что такой подход эффективнее и дешевле, чем профилактическое использование высоких доз иммуноглобулина и ацикловира, которое было популярно в конце 80-х — начале 90-х годов.
В настоящее время существует только два препарата, эффективных при лечении ЦМВ-инфекции: ганцикловир (цимевен, фирма «Ф. Хоффманн — Ля Рош») и натрия фосфоноформат (фоскавир, фирма АСТРА). Сидофовир (Vistide, фирма «Пфайзер») активен против резистентных штаммов, удобен тем, что его вводят раз в неделю (5 мг/кг), однако его применение может ограничивать выраженная нефротоксичность. Все остальные препараты (интерфероны, ацикловир и его производные, «иммуномодуляторы») не должны даже рассматриваться как варианты контроля ЦМВ-инфекции.
Из двух указанных препаратов наиболее изучен ганцикловир, коммерчески доступный более 15 лет. Накоплен исчерпывающий опыт его применения при ЦМВ-инфекции.

Ганцикловир (1,3-дигидрокси-пропоксиметил-гуанин) сам по себе не является активным противовирусным агентом, необходимо его фосфорилирование вирусной тимидинкиназой. В форме трифосфата ганцикловир ингибирует вирусную ДНК-полимеразу. Сродство ганцикловира к тимидинкиназам человека значительно меньше, поэтому его токсичность для человеческих клеток относительно невелика.
Доза ганцикловира для курса индукции составляет 10 мг/кг в сутки на два введения. Курс индукции продолжается 2—3 нед, после чего назначают поддерживающую дозу — 5 мг/кг в сутки на одно введение ежедневно или 5—6 раз в неделю. Длительность курса поддерживающей терапии определяют индивидуально. При упреждающем лечении реактивации ЦМВ после аллогенной ТКМ при достижении негативной реакции на антигене-мию или виремию поддерживающее лечение можно не проводить, в то время как при органном поражении (пневмония, ЦМВ-колит) лечение должно быть продолжено до купирования симптомов и негативизации результатов вирусологических исследований, а при ЦМВ-ретините терапия может быть пожизненной.
При длительном профилактическом или упреждающем применении ганцикловира в раннем посттрансплантационном периоде высока частота поздних ЦМВ-пневмоний. Таким пациентам необходимо продолжать мониторинг ЦМВ-виремии или антигенемии и после 100-го дня после трансплантации [11]. Примерно у 20 % больных, леченных ганцикловиром в указанной дозе, развивается гранулоцитопения менее 1000 в 1 м\ во всех случаях обратимая (быстрее под влиянием G-CSF), с медианой длительности 12 дней. Резистентность ЦМВ к ганцикловиру является редкостью.
Отличным от ганцикловира по механизму действия (прямое ингибирование ДНК-полимеразы) является натрия фосфоноформат (фоскарнет, фоскавир), который может быть эффективен при резистентности данного штамма вируса к ганцикловиру. Индукционная доза натрия фосфоноформата 90 мг/кг каждые 12 ч. Продолжительность курса лечения составляет 14 дней, затем проводят поддерживающую терапию в половинной дозе. Побочными реакциями являются нарушение функции почек, гипомагнезиемия, гипокальциемия и изъязвление слизистых оболочек наружных половых органов.
Необходимо отметить коммерчески доступный специфический антицитомегаловирусный иммуноглобулин. Убедительных доказательств его эффективности в лечении вызванных ЦМВ болезней нет. С учетом его дороговизны, а также наличия препаратов, оказывающих специфическое противовирусное действие, дальнейшее применение этого препарата вряд ли оправдано.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инфекции вызванные цитомегаловирусом: диагностика, лечение, профилактика
Вирусы герпеса — большие, покрытые оболочкой, двунитевые ДНК-вирусы (120—200 нм). Геном содержит 120—240 тыс. пар нуклеотидов, кодирующих более 35 белков. Оболочка состоит из гликопротеинов и Fc-рецепторов. Инфекция персистирует у человека на протяжении всей жизни, переходя в латентную форму после острой стадии и периодически рецидивируя (особенно при снижении иммунитета у человека).
Классификация герпес-вирусов
Все вирусы герпеса разделяют на:
• а-герпес-вирусы — быстрорастущие цитолитические вирусы, вызывающие латентную инфекцию и поражающие нейроны (вирусы простого и опоясывающего герпеса);
• бета-герпес-вирусы — медленно растущие вирусы, вызывающие латентные инфекции секреторных желёз и почек (цитомегаловирус);
• у-герпес-вирусы — вирусы, вызывающие латентный инфекционный процесс в лимфоидной ткани (вирус Эпштейна—Барр).
Недавно обнаруженные вирусы герпеса человека типа 6 и 7 (ВГЧ-6 и ВГЧ-7) относят к у-герпес-вирусам, так как они вызывают латентные инфекции лимфатических узлов и имеют генетические сходства именно с этой группой вирусов герпеса. ВГЧ-8, ассоциированный с саркомой Капоши, сходен с вирусом Эпштейна—Барр. Все вирусы герпеса, за исключением вируса простого герпеса типа 1 и 2, различны по антигенной структуре.
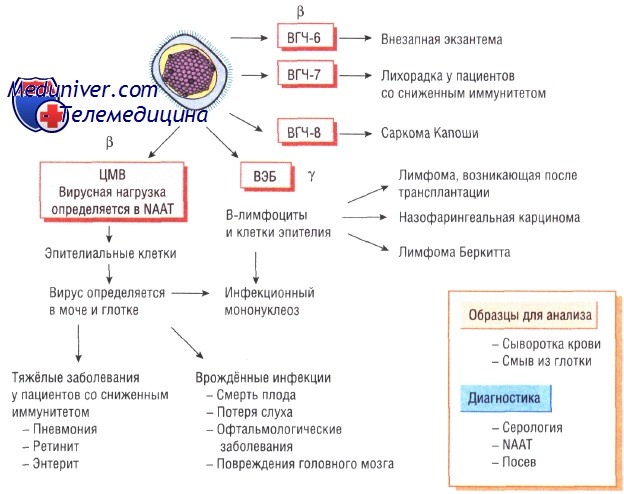
Инфекции вызванные цитомегаловирусом
По своей структуре цитомегаловирус похож на все остальные вирусы герпеса. Обычно он персистирует в организме на протяжении всей жизни. Его обнаруживают в моче и слюне человека. Примерно 50% населения Великобритании инфицированы ВГЧ-5.
Эпидемиология и патогенез цитомегаловирусной инфекции. Механизм передачи инфекции — вертикальный или контактный (от человека к человеку). Чем ниже социально-экономические условия, тем раньше происходит инфицирование. Возможен вертикальный механизм передачи инфекции. Кроме того, заражение может произойти при переливании крови или пересадке органов; в этом случае инфекции свойственно очень тяжёлое течение.
Клинические признаки инфекции вызванной цитомегаловирусом. Врождённая инфекция обычно протекает в тяжёлой форме. В начальном периоде выраженные симптомы заболевания отсутствуют. В дальнейшем возникает прогрессирующая глухота, задержка развития. При заражении после рождения заболевание протекает в лёгкой форме. У пациентов со сниженным иммунитетом (ВИЧ-инфекция, состояние после трансплантации органов) может развиться тяжёлая пневмония, ретинит, поражение кишечника, причём вирусная инфекция может быть приобретённой (от пересаженного органа) или собственной (латентная форма).
Диагностика инфекции вызванной цитомегаловирусом. Врождённую инфекцию диагностируют при проведении анализа мочи через 3 нед после рождения. У взрослых цитомегаловирус может быть культивирован либо определён молекулярно-генетическим методом в образцах мочи и крови. Исследование вирусной нагрузки имеет большое значение для диагностики тяжёлого течения инфекции и назначения своевременного лечения.
Лечение и профилактика инфекции вызванной цитомегаловирусом. При тяжёлой инфекции, угрожающей жизни пациента, а также при риске потери зрения лечение проводят ганцикловиром в комплексе с иммуноглобулином (при развитии пневмонии). Эфир ганцикловира, валганцикловир принимают внутрь, назначают в начале лечения и в качестве поддерживающей терапии. Ещё более токсичные альтернативные препараты (фоскарнет и цидофовир) ингибируют цепочечную ДНК-полимеразу. Важная мера профилактики заболевания — тщательный подбор донорских органов для пересадки и крови для переливания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ЦМВИ у детей. Что делать если у ребенка обнаружили цитомегаловирусную инфекцию?
Цитомегаловирусная инфекция (ЦМВИ) во многом остается "темной лошадкой" для современных инфекционистов. Обладателям вируса-возбудителя в теории может быть кто угодно, но далеко не каждый об этом догадывается. Дело обстоит таким образом, во-первых, потому что довольно часто носительство бывает бессимптомным, во-вторых, в связи с тем что возможности передачи вируса весьма широкие. Возбудитель ЦМВИ попадает в организм через плаценту, вертикально (когда плод проходит через родовые пути), при грудном вскармливании с молоком, при переливании крови и в процессе полового контакта. В отношении детей большую роль играют первые три способа передачи вируса.
Цитомегаловирус в организме может вести себя по-разному, собственно, именно это во многом затрудняет его диагностику. Как уже говорилось выше, он может вообще никак себя не проявлять, но лишь при одном условии - прочной и хорошо функционирующей иммунной системе, которая активное размножение вируса в клетках организма может подавить. Однако в условиях иммунодефицита этот вирус становится по-настоящему опасен. Поэтому от него страдают помимо больных СПИДом и людей пожилого возраста еще и дети.
ЦМВИ выявляется особенно часто у детей до двух лет - это период становления иммунитета ребенка. Его иммунная система не в столько в дефиците, сколько супрессирована, то есть в некоторой степени подавлена, особенно на первых месяцах жизни. Таким образом природа защищает новорожденного от чрезмерно сильных реакций иммунитета на огромное множество чужеродных агентов. После года та защита, которую малыш получал с молоком матери, начинает исчезать, а свои противовирусные частицы вырабатываться в должной мере пока не могут. В связи с этим дети нередко страдают от ЦМВИ.

Проявления ЦМВИ достаточно широко варьируют, так как вирус способен проникать практически во все клетки организма и вызывать цитопатический эффект. Проще говоря, клетки меняются и утрачивают способность нормально функционировать. Что говорит о врожденной ЦМВИ, которую ребенок получил либо через плаценту еще в утробе, либо в процессе родов?
1. У таких детей имеется желтушность кожных покров и склер глаз. Печень значительно увеличена, так как цитомегаловирус имеет склонность поселяться сразу в клетки этого органа.
2. Из-за нарушения работы печени страдает и свертываемость крови, на основании этого дети с ЦМВИ страдают от повышенной кровоточивости (на коже появляются синячки, сыпь, плохо заживает пупочная ранка, кровь может появиться в стуле).
3. Также значительно увеличивается селезенка.
4. Помимо этого есть ряд других признаков: страдают легкие (вплоть до развития пневмонии), нарушена центральная нервная система (менингит, энцефалит, гидроцефалия характеризуются судорогами, повышенной возбудимостью). Изменено состояние органов ЖКТ, что характеризуется колитами, энтеритами, недостаточностью поджелудочной железы. Вирус не обходит стороной и почки, приводя к развитию нефрита.
К сожалению, выхаживать таких новорожденных чрезвычайно трудно, ведь на фоне такого "букета" к ослабленному организму присоединяются другие инфекционные заболевания. Поэтому тяжело текущие ЦМВИ часто заканчиваются гибелью новорожденного еще в первые недели его жизни, либо вовсе приводят к выкидышу, если женщина заразилась на ранних сроках беременности.
К счастью, такое тяжелое течение заболевания бывает далеко не у всех новорожденных (всего у 10 %), так что причина тяжести ЦМВИ в этом случае во многом остается загадкой. Те же дети, которые относительно легко переживают инфекцию, нередко впервые сталкиваются с ней через месяц-два после рождения. И в этом случае симптомы могут быть самыми разными. Обычно снижается слух или зрение, нарушается работа нервной системы, страдает физическое развитие. Вот с такими проблемами родители приходят к педиатру, и установить истинную причину - ЦМВИ удается не всегда.
Стоит помнить о и передаче вируса ребенку с материнским молоком. Когда инфицирование происходит таким путем, у ребенка часто возникает пневмония, которая лечению антибактериальными препаратами не поддается.

Дети старшего возраста и подростки с ЦМВИ сталкиваются еще реже в силу прочности их иммунной системы. Но если вирус все же активизировался, то проявляет он себя обычно снижением работоспособности, болью в суставах, лихорадкой и головными болями. Вывод таков, что по одним признакам установить наличие ЦМВ невозможно, всегда требуется лабораторное подтверждение. Оно заключается в поиске специфических антител, которые наш организм вырабатывает в ответ на наличие конкретных вирусных частиц. Есть специфические антитела - есть и вирус. Что же делать, если у ребенка обнаружили ЦМВИ?
1. Обнаружение ЦМВИ возможно еще в процессе беременности, посредством УЗИ, ведь вирус может приводить к формированию множественных видимых пороков у плода. Поскольку такие дети в будущем практически не жизнеспособны, беременность предлагается прервать.
2. В том случае, когда ЦМВИ выявляется у ребенка через некоторое время после рождения (не в первые дни), тактика врача будет зависеть от течения инфекционного процесса. Есть конкретные лекарственные средства, которые назначают для подавления ЦМВ - Ганцикловир, Фоскарнет. Однако принимать решение об их применении самостоятельно нельзя, так как эти лекарственные средства обладают рядом очень серьезных побочных эффектов. Они негативно сказываются на состоянии крови и токсичны для почек. В связи с этим их применяют только при острой необходимости, когда цитомегаловирус выходит из-под контроля. Новый препарат Цитотект, тоже подходит для лечения ЦМВИ, но вводится он также исключительно по назначению специалиста.
3. Нужно добиваться, чтобы признаки ЦМВИ не появлялись у ребенка. А для этого очень важно укреплять его иммунитет, который самостоятельно способен подавлять вирус и не давать ему негативно влиять на здоровье малыша. Есть множество природных иммуностимуляторов, которые разрешено давать детям (настойка эхинацеи, элеутерококка), Иммунал, Иммудон и другие средства, которые можно использовать курсами после консультации у педиатра с целью улучшения работы иммунной системы. Не последнюю роль играет питание. Не забывайте, что оно должно привносить в организм нужное количество белков, углеводов и жиров, микроэлементов, витаминов. Следите за тем, чтобы ребенок соблюдал режим, не переутомлялся, регулярно бывал на свежем воздухе и физически был активен.
- Вернуться в оглавление раздела "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Рассказывает научный руководитель Кабинета терапии герпесвирусных инфекций и иммунореабилитации Центра здоровья КБ № 122 инфекционист и клинический иммунолог д.м.н. профессор, академик РАЕН и Нью-Йоркской академии наук, Почетный ученый Европы Валерий Александрович Исаков .
– Давайте разберемся с этим «семейством».

– Самый известный представитель этого семейства – вирус простого герпеса 1-го типа. Это наиболее распространенная форма, описанная еще Гиппократом. И хотя внешние проявления мы замечаем на носогубном треугольнике (простуда на губах, крыльях носа или слизистой), вирус поражает организм в целом. Он может проявляться в течение года несколько раз. Но встречаются и более тяжелые формы течения с повторением от 4–5 до 6 и более раз в год. Вирус герпеса 2-го типа, или генитальный герпес, может беспокоить раз в два-три месяца, а то и каждый месяц (особенно женщин). Жить с этим крайне тяжело. Мало того что приходится терпеть неприятные симптомы, частые проявления вируса свидетельствуют о существенных изменениях в иммунном статусе.
– А может, предположим, человек не знать, что страдает герпесом, обусловленным вирусами этих двух типов?
– Может. Например, мы часто видим в уголках губ так называемые заеды – трещинки. Исследования показывают, что у 20% таких пациентов есть вирус простого герпеса 1-го типа. То же самое и с генитальным герпесом: не обязательно будет сыпь и зуд, вполне возможно образуется просто трещинка.
– Я слышала, что вирус ветрянки – тоже герпес.
– Это 3-й тип – герпес Зостера, или ветрянки, который может поражать и после 40 лет. Считается, что у 40% детей, которые перенесли ветрянку, вирус ветряной оспы остается существовать дальше в ганглиях нервной системы (нервном узле – скоплении нервных клеток).
В пожилом возрасте, когда меняется гормональный фон и происходит естественное угнетение иммунологических реакций, создаются условия для реактивации вируса. Клинически это проявляется в виде опоясывающего герпеса – высыпаний на торсе, образующих сплошную ленту по ходу межреберных нервов. Больных беспокоит зуд и невралгические боли. Как вы видите, вирусы герпеса могут долгие годы ждать удобного случая, «укрываясь» в клетках нервной и иммунной систем.
– Почему вирусы герпеса облюбовали именно эти клетки?
– На этот вопрос сложно ответить. Вирусы появились на земле миллиарды лет назад, а человек как биологическое существо – относительно недавно (как считают специалисты, сотни тысяч лет назад). Поэтому вирусы «хитрее» организма человека. Вирус погружается внутрь клетки, сбрасывает свою защитную оболочку – и процесс пошел. ДНК вируса может встраиваться в ДНК клетки хозяина, и с этого момента он живет и размножается. Но инфицирование – не значит болезнь, и не всегда носитель вируса страдает его проявлениями. 10% населения не болеют вообще или болеют редко и в мягкой стертой форме. Ну а остальным везет меньше. Герпесом могут поражаться печень, легкие, органы зрения, половые органы, железистая ткань, стенки сосудов различных органов. Все это – на фоне гибели или снижения функциональной активности клеток иммунной системы и развития вторичных иммунодефицитных состояний.
– Но основным-то источником заражения являются инфицированные люди?
– Да, а механизмы инфицирования – воздушно-капельный, оральный (через рот), контактный (через микротравмы на коже и слизистых оболочках) и гемоконтактный (через кровь). Факторами передачи инфекции могут быть инфицированные слюной или содержимым пузырьков детские игрушки, предметы обихода – полотенце, посуда, дверные ручки. Вирусы герпеса могут содержаться в слюне, крови, слезной жидкости, содержимом везикул, сперме, секрете влагалища и шейки матки, моче, грудном молоке, различных органах и тканях, используемых для пересадки.
– А если в семье кто-то болеет, значит ли это, что и другие больны или заболеют?
– Риск инфицирования внутри семьи гораздо выше, но это не означает, что все будут болеть одинаково. Бывает, у пациента два или три разных вируса герпеса одновременно, а у членов его семьи – другие комбинации. Поэтому каждого пациента надо обследовать и лечить отдельно.
– Мы поговорили лишь о наиболее распространенных вирусах этого семейства. Сколько же их всего?
– Известно восемь разновидностей вируса. Вирус герпеса 4го типа (вирус Эпштейна – Барр, ВЭБ) – единственный онкогенный среди своего семейства. Живет преимущественно в лимфоидной ткани и вызывает воспаление и боль в лимфоузлах шеи, подмышечных, паховых областях. У детей и взрослых острая форма инфекции называется инфекционным мононуклеозом. Как и в случае ветрянки, 30–40% детей, перенесших это заболевание, становятся пожизненными носителями ВЭБ. На долгий срок даже могут забыть о нем. Но в определенный момент наступает сбой в работе иммунной системы, и пациент начинает болеть. Первая реакция – недоумение. Почему? 10–15 лет не болел, а тут – частые ОРЗ, ангины, фарингиты, немотивированная слабость, повышение температуры. И длиться это может годами. Начинаются поиски причины. Пациенту делают мазки из зева, носа, выделяют, к примеру, стрептококки, назначают антибиотики, и на какое-то время эффект есть. А через три недели все повторяется снова: боли, налеты в горле, слабость, увеличение шейных лимфоузлов. В такой ситуации следует задуматься о герпетической природе такого недомогания и сдать анализы на ВЭБ. А поскольку схожую симптоматику дают еще цитомегаловирус и вирус герпеса 6го типа, то лучше подойти к решению проблемы комплексно.
– Цитомегаловирус имеет какие-то свои особенности?
– Это 5-й тип вируса герпеса, который живет в клетках иммунной системы и поражает в основном внутренние органы: щитовидную, поджелудочную, половые железы. Известны случаи аутоиммунного тиреоидита, тяжелого панкреатита вирусной природы. Особенно это опасно у беременных, так как беременность протекает на фоне физиологического подавления иммунитета (чтобы не было конфликта между матерью и развивающимся плодом) и снижения выработки гормонов. Это идеальные условия для его активации. Цитомегаловирус сильнее других вирусов поражает плод и приводит к нарушениям нервной системы, печени, легких.
– А как ведут себя в нашем организме менее известные вирусы герпеса?
– Вирусы герпеса человека 6-го и 7-го типов менее изучены. Вирус герпеса 6-го типа в чем-то похож на цитомегаловирус, вызывает чаще всего внезапную экзантему (острое инфекционное заболевание детей раннего возраста, протекающее с повышенной температурой и кожными высыпаниями). Герпес 6го типа у детей и взрослых вызывает первичную герпетическую инфекцию, проявляющуюся менингоэнцефалитом разной степени тяжести, поражением печени, воспалительными процессами в легких, бронхах и сердечной мышце.
– Герпес так многолик. С ним сталкиваются врачи многих специальностей: гинекологи, урологи, офтальмологи, неврологи, оториноларингологи, педиатры, дерматологи, иммунологи. У кого и как лечиться?
– Надо помнить, что герпесвирусы поражают весь организм в целом. И если необходим результат, нужно выявить причину и пройти комплексное лечение с участием врача-иммунолога, инфекциониста. И уж никак нельзя относиться к этому заболеванию легкомысленно. Герпесвирусы могут быть причиной бесплодия, мертворождения и выкидышей, инициируют процессы атеросклероза и развитие злокачественных новообразований, они могут свести на нет безупречно проведенное хирургическое вмешательство. Например, при протезировании клапанов сердца. Более того, Всемирная организация здравоохранения на ближайшее время поставила проблему борьбы с герпесвирусными инфекциями на первое место. Не ВИЧ и СПИД, не вирусные гепатиты и не грипп. Это такая же реальная опасность.
Поэтому нами создан Кабинет терапии герпесвирусных инфекций и иммунореабилитации. Здесь работают врачи-специалисты доктора и кандидаты медицинских наук: акушеры-гинекологи, инфекционисты, иммунолог, аллерголог. Консультируют терапевт, невролог, оториноларинголог, дерматовенеролог, офтальмолог. Лечение пациента проводится комплексно, применяются новые эффективные технологии с использованием современных противовирусных, иммуномодулирующих и антибактериальных препаратов, вакцин.
– Насколько эффективны эти препараты?
– Полностью уничтожить вирус невозможно. Но можно добиться длительной ремиссии и уменьшить концентрацию вируса во всех биологических жидкостях: слюне, крови, моче. Для этого используются противовирусные препараты последнего поколения, которые обладают «игольчатым» механизмом действия: они менее токсичны и могут применяться годами без негативного воздействия на организм. Также назначается иммуностимулирующая терапия в комплексе с другими местными средствами.
Материал предоставлен газетой «Панацея» (№ 2 (103) февраль 2015 г.)
Читайте также:

