Анализ на гистологию рака кожи что это
Обновлено: 26.04.2024
Плоскоклеточная карцинома кожи - частота, клиника, диагностика
Плоскоклеточный рак кожи в меньшей степени, чем базальноклеточная карцинома, хотя обе имеют много общих черт. Плоскоклеточная карцинома возникает под действием солнечной радиации или рентгеновских лучей, а также при длительном контакте с мышьяковистыми соединениями и промышленными канцерогенами. В самом начале XX в. среди врачей-радиологов многоочаговая плоскоклеточная карцинома представляла собой обычную опухоль.
Позже, когда выяснилась причина этого и были разработаны чувствительные методы дозиметрии, ситуацию удалось поставить под контроль.
Гистологически опухоль представляет собой типичное кератинизирующее плоскоклеточное повреждение кожи. На основании данных гистологического анализа можно предсказать степень риска локального распространения опухоли. Для менее дифференцированных опухолей риск распространения оказывается выше. Так же как базальноклеточная карцинома, опухоль преимущественно развивается на открытых участках кожи, которые подвергаются воздействию солнечных лучей. Это кожа на шее и на голове, особенно в области носа, на висках и на краях ушных раковин, а также вокруг губ.
Характерными местами являются боковые и задняя поверхности шеи, тыльные поверхности кистей рук и предплечья. Обычно опухоль выглядит в виде сквамозных изъязвлений, покрытых струпьями, или представляет собой экзофитное повреждение нодулярной природы, которое при отсутствии лечения может быстро расти. Место расположения опухоли помогает поставить диагноз, поскольку для плоскоклеточной карциномы, хотя она обычно развивается на коже лица, в большей степени, чем для опухоли базальноклеточного типа, характерно расположение на других участках кожного покрова. Для плоскоклеточной карциномы также свойственно быстрое развитие. В большинстве случаев кожные опухоли, возникающие на кистях рук и на предплечье, представляют собой плоскоклеточную карциному.
Иногда, при микроскопическом исследовании, плоскоклеточную карциному трудно отличить от кератоакантомы, кожного заболевания, обычно доброкачественной природы. При этом заболевании на лице или на шее образуется папула, состоящая из нескольких частей и часто достигающая больших размеров. Центральная изъязвленная часть папулы покрыта роговым слоем.
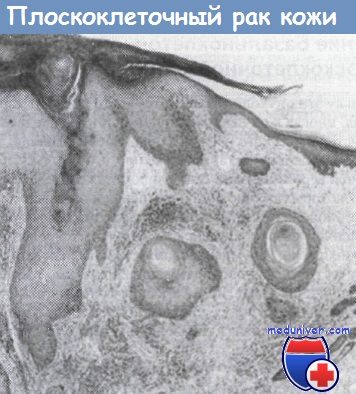
Плоскоклеточная карцинома кожи.
Видны инвазирующие массы чешуйчатого эпителия, образующие «жемчужные» кератино-вые бляшки (х20).
Плоскоклеточная карцинома развивается при радиационных дерматитах. По гистологическим и клиническим показателям эта опухоль более агрессивна, чем другие карциномы, хотя латентный период ее развития может достигать 20 лет. По данным одного из масштабных наблюдений, проведенном примерно на 400 больных, смертность от плоскоклеточной карциномы достигает 10%.
В настоящее время частота заболеваемости плоскоклеточной карциномой сократилась. Это связано с использованием аппаратуры, обеспечивающей возможность получения высокоэнергетических пучков, и с ограниченным применением лучевой терапии для лечения доброкачественных заболеваний кожи и артритов. Сказанное также относится к случаям плоскоклеточной карциномы, возникающей на месте хронической ожоговой язвы, так называемой язвы Маржолена.
Для этих случаев, однако, характерен длительный период покоя, в конце которого наступает агрессивное развитие опухоли, сопровождающееся метастазированием в легкие и другие органы. Аналогичная по типу плоскоклеточная карцинома иногда развивается в синусовых трактах при хроническом остеомиелите и других хронических инфекциях, а также на местах дисплазии или шрамов при хронических кожных болезнях, например, при обычной или при системной красной волчанке.
Плоскоклеточная карцинома образуется в местах контакта кожи со слизистой оболочкой, например в области ануса и вульвы. В этих случаях опухоль проявляет себя так же агрессивно, как и возникающая при лучевых повреждениях кожи, на месте пятен болезни Боуэна или на фоне карциномы in situ. К числу редких опухолей с непредсказуемым прогнозом относится карцинома потовых желез.
Наиболее часто эти опухоли развиваются в подмышечной ямке и в аногенитальной области. Они отличаются от опухолей сальных желез, также очень редких. В заключение отметим, что плоскоклеточная карцинома часто развивается в области депигментированных пятен при витилиго, что особенно характерно для негроидного населения.
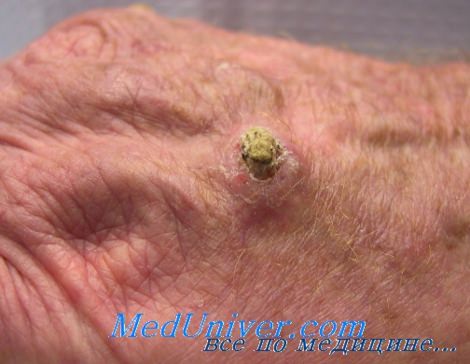
Плоскоклеточный рак кожи - внешний вид
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Биопсия при раке кожи. Гистологическое исследование опухоли кожи.
Результаты гистологического исследования при диагностике опухоли кожи более информативны, чем данные цитологического исследования. Это наглядно продемонстрировано при диагностике метатипического рака кожи, занимающего промежуточное положение между базалиомой и плоскоклеточным раком кожи. Поданным Е.С. Снарской (1994), цитологическая картина в 75% случаев метатипического рака была идентична язвенной база-лиоме и лишь в 25% случаев дала возможность предположить метатипический рак. Гистологическое исследование необходимо проводить, даже если диагноз опухоли кожи кажется ясным.
С целью исключения злокачественной опухоли кожи оно должно проводиться при всех кожных узлах, а также целесообразно при опухолях, которые планируется подвергать лучевой терапии, после которой ткань опухоли становится непригодной для гистологического исследования. Гистологическое исследование дает возможность оценить, удалена ли опухоль в пределах здоровой кожи. В некоторых случаях необходимо проведение микроскопически контролируемой операции по серийным гистологическим срезам. Гистологическое исследование необходимо для определения тактики лечения больного и прогноза заболевания. Повторные биопсии с интервалом в несколько недель или месяцев могут быть использованы для мониторинга прогрессиро-вания лимфомы кожи или эффективности ее лечения. Гистологические препараты могут длительно храниться, пересматриваться в любое время, а также использоваться как документ.
Биопсия — метод получения ткани живого организма для морфологического исследования с диагностической целью. Она должна выполняться в условиях операционной или перевязочной с соблюдением всех правил асептики и антисептики. При этом для установления границы новообразования и видимо интактной ткани необходимо хорошее освещение операционного поля. Биопсия выполняется острым инструментом, рассекающим, а не разминающим кожу.
В дерматоонкологии используются эксцизионная биопсия, при которой иссекается вся опухоль, и инцизионная биопсия, при которой иссекается только часть новообразования (в центре, а не с периферии опухоли и с захватом интактной ткани). Материал для гистологического исследования также может быть получен путем кюретажа с использованием кюретки в форме кольца или хирургической ложки. Пункционная биопсия проводится специальным трубчатым ножом диаметром от 2 до 8 мм (чаще всего диаметром 4 мм). Он представляет собой полый цилиндр с режущим краем, который продвигают в толщу кожи, врашая большим и указательным пальцами. При этом получают столбик ткани, состоящий из эпидермиса, дермы и подкожной жировой клетчатки; основание столбика удаляют ножом. Кожный дефект закрывается швом или проводится гемостаз с помощью давящей повязки либо гемостатической губки. Биопсию путем срезания бритвой, скальпелем или ножницами применяют при узловой базалиоме и керато-мантоме. Разрез следует делать параллельно линиям кожного натяжения.
Разнообразие методов исследования материала (световая, электронная микроскопия, иммунофлюоресцентное окрашивание) делает биопсию кожи одним из самых простых и информативных методов диагностики опухолей кожи.
Для обычного гистологического исследования образец помещается в 10% раствор формалина. Стандартно фиксированные препараты не пригодны для гистохимических, цитохимических, иммуногистохимических и электронномикроскопических исследований.
Для электронной микроскопии используется буфер — глутаральдегид, а перед проведением иммунофлюоресцентного исследования образец опухоли должен быть немедленно заморожен или помещен в специальный транспортный буферный раствор.
Роль гистологического исследования при диагностике доброкачественных и злокачественных опухолей кожи подробно рассматривается в статье «Система кожных покровов». В то же время провести четкое разграничение между доброкачественными и злокачественными новообразованиями кожи может оказаться довольно сложно. При этом, исходя из того, что доброкачественная опухоль — это локализованная пролиферация клеток одного и того же типа с нормальной дифференцировкой и сохранением контроля за автономностью их роста, а злокачественная опухоль способна к ме-тастазированию в лимфатические узлы и внутренние органы, дать заключение о функциональных способностях опухолей по морфологической картине их маленького кусочка сложно. Особенные затруднения возникают в тех случаях, когда результаты гистологического исследования не коррелируют с клинической картиной опухоли. В этой связи может возникнуть проблема отличия доброкачественных опухолей от гамартом и рака in situ. Отличие доброкачественной опухоли от гамартомы основывается на том, что в гамартому включен более, чем один тип клеток. Что касается рака in situ, то этот диагноз устанавливается на основании признаков снижения дифференциров-ки и ядерной атипии клеток, локализованных лишь в пределах эпидермиса, т.е. отграниченных от других здоровых тканей.
Широкое распространение получают методы иммуноморфологического анализа биопсийного материала. С помощью антител к различным компонентам наружной мембраны или цитоплазмы клеток уточняются гистогенез опухоли, степень ее дифференцировки, начальные этапы инвазии. Используемыми с этой целью маркерами могут быть как вещества антигенной природы (белки, полипептиды, полисахариды), так и относительно простые соединения или даже химические группировки, не обладающие антигенными свойствами.
Для выявления клеток плоского эпителия протоков эккринных, апокринных и сальных желёз, а также гистогенетически связанных с ними опухолей кожи, используют антитела к антигенам эпителиальной мембраны (ЕМА), состоящим из гликопротеинов с высокой молекулярной массой.
Цитокератины, представляющие собой группу промежуточных волокон различного молекулярного веса, обнаруживаются в ороговевающем и неороговевающем эпителии. Для идентификации, например, кератинов высокого молекулярного веса, экспрессируемых многослойным плоским эпителием, используются панцитокератины САМ 5.2 и АР34. Ряд антител к кератину распознают уникальные эпи-топы придаточных структур кожи. С их помощью также можно определять гистогенез или направление дифференцировки многих опухолей пилосебоцейного комплекса и потовых желез.
Маркером меланоцитов является кислый протеин S100, антитела к нему реагируют с клетками Шванна, Лангерганса и эккринных потовых желез, а также с опухолями и гамартомами, развившимися из этих клеток. Его целесообразно использовать для отличия мела-номы от других веретеноклеточных опухолей и для определения мелких отсевов меланомы, расположенных на расстоянии от первичной опухоли или в глубоких тканях кожи. Для идентификации доброкачественных и злокачественных меланоцитарных опухолей кожи также используют NK1-C3 и НМВ 45.
Для идентификации мягкотканных опухолей, наряду с антителами к цитокератинам также используют антитела к другим основным типам белков промежуточных волокон — виментину, десмину и белку нейрофиламентов. Виментин присутствует во многих клетках кожи (фибробластах, макрофагах, хондроцитах. эндотелиальных и лимфоидных клетках), поэтому применение его маркеров весьма ограничено. Напротив, десмин (полипептид с молекулярной массой 53 000) характерен для большинства миоцитов и поэтому не обнаруживается в саркомах, возникших без участия мышечной ткани. Нейрофиламенты, варьирующие по молекулярной массе от 68 000 до 200 000, идентифицируются в кожных опухолях из клеток Меркеля и карцино-идных опухолях. Менее целесообразно их использование при фиброгистиоцитарных опухолях. Хотя в некоторых истинных гистиоци-тарных опухолях могут идентифицироваться антитела к о-антитрипсину, антихимотрип-сину и лизосомам. Сравнительно недавно открыто поликлональное антитело против фактора ХШа. Предполагается, что это клеточный маркер особой субпопуляции дермальных фиброгистиоцитарных клеток, называемых дермальными дендроцитами. Несмотря на то что фактор ХШа обнаруживается во многих клетках при различных типах мягкотканных опухолей, специфичным он является лишь для определенных опухолей, например для гистиоцитомы, богатой, в отличие от выбухающей дерматофибросаркомы, фактор ХIIIа-положительными клетками.
Опухоли кровеносных и лимфатических сосудов могут быть идентифицированы различными эндотелиальными маркерами. Антитела к антигену, связанному с фактором VIII используются для идентификации нормального и неопластического эндотелия, т.к. они не реагируют с тканью лимфатических капилляров, Для идентификации сосудистого эндотелия также используется Ulex Europaeus агглютинин 1. В нефиксированных замороженных срезах для различия между опухолями лимфатических и кровеносных сосудов используют EN4 и PAL-E. Лимфатические и мелкие кровеносные сосуды положительно окрашиваются на EN4. Напротив, на PAL-E могут положительно окрашиваться венулы, вены, капилляры, артериолы и артерии, а лимфатические сосуды — отрицательно,
С целью идентификации лимфом кожи и отличия их от кожных заболевании (укусов насекомых, лимфоцитомы и т.д.) используют панель лейкоцитарных маркеров; для имму-ногистохимического выявления дифференцировочных антигенов мембран опухолевых клеток используются маркеры цитокиновых рецепторов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Меня зовут Дмитрий Бейнусов, я – врач-дерматоонколог, занимаюсь лечением опухолей кожи: доброкачественных и злокачественных.

Гистологическое исследование опухолей, т. е. изучение характеристик ткани опухоли под микроскопом имеет большое, а иногда и решающее значение для лечения и прогноза. С 2011 года я направляю все удаленные образования кожи специалистам Национального центра клинической морфологической диагностики (НЦКМД); они уже почти 8 лет помогают мне с точной диагностикой.
Эту статью я написал с целью помочь своим пациентам и коллегам лучше ориентироваться в процессе гистологического исследования и понять, как это важно для лечения образований кожи.
Прочитайте эту статью до конца, и вы увидите, как в современных морфологических лабораториях максимально быстро и качественно выполняют исследования, а также сводят к минимуму вероятность человеческой ошибки.
Что такое гистологическое исследование и зачем его проводят
Согласно клиническим рекомендациям Минздрава РФ (2018), гистологическое (морфологическое) исследование – это стандарт диагностики при исследовании опухолей кожи и в первую очередь при подозрении на меланому или рак. Это обусловлено тем, что в настоящее время нет более точного метода для определения характера удаленного образования кожи.
Ни дерматоскопия, ни простой соскоб или пункция с последующим цитологическим исследованием, ни тем более простой визуальный осмотр подозрительной родинки не могут заменить гистологического исследования.
Мифы о гистологическом исследовании
Если ввести в поисковой строке слова «гистология родинки» или «гистология меланома» и посмотреть содержание первых, создается достаточно пугающее впечатление:
- здесь перепутали родинки разных людей;
- в этой лаборатории исследование делают 3 месяца;
- тут не сообщили пациенту об опасном диагнозе;
- там ошиблись с диагнозом, что закончилось печально.
К сожалению, после ознакомления с информацией в отечественном интернете создается ощущение, что в нашей стране нередко гистологические исследования образований кожи делают «на коленке» и «неизвестно кто и где».
В статье я покажу, что есть другая реальность. Кроме того, назову ошибки, которые могут возникнуть на различных этапах исследования, и, самое главное, какими способами их исключить.
Важные для пациента моменты на этапах гистологического исследования операционного и биопсийного материала кожи
Наш путь начинается в тот момент, когда удаленная опухоль кожи, например родинка, попадает в лабораторию.
Предположим, что врач сделал все правильно.
- Родинку сразу после удаления поместил в герметичный контейнер с формалином.

- Приложил к контейнеру направление на морфологическое исследование, которое поможет патоморфологу поставить точный диагноз.

Если врач все сделал именно так – смело сдаем контейнер и направление в лабораторию.

Администратор, получивший контейнер с родинкой, регистрирует ее – присваивает уникальный номер и QR-код. Эти данные, фамилию и инициалы пациента пишут на специальной кассете, в которой удаленная родинка пройдет все этапы исследования. Мне удалось заснять процесс изготовления кассет и их маркировки:
Все рабочие места врачей и лаборантов оборудованы сканерами QR-кодов. Они позволяют на любом технологическом этапе определить, кому принадлежит материал, и работать с ним. Таким образом, ошибка «перепутали родинки разных людей» в лаборатории исключена.
В Центре трепетно относятся к личным данным пациентов, поэтому Ф. И. О. на этом и других фото намеренно закрыты.

2. «Вырезка» и «фиксация»
Далее родинку внимательно осмотрят, опишут в протоколе и поместят особым образом в специальную пластиковую кассету для дальнейшего процесса. Весь процесс фиксируют на цифровую камеру. Видео понадобится в случаях неправильного расположения части родинки в кассете, когда нужно будет вернуться к этому этапу и переориентировать фрагмент.

Из промаркированного контейнера с транспортной средой извлекают родинку (невус):

Далее пигментное образование разделяют на несколько частей таким образом, чтобы для гистологического исследования были доступны все участки образования. Здесь все нужно сделать правильно, чтобы точно определить толщину меланомы по Бреслоу, состояние краев резекции кожи с опухолью – эти параметры имеют решающее значение в оценке адекватности операции и в прогнозе заболевания.
На кассете с родинкой пишут фамилию и инициалы пациента, которые были указаны на контейнере, а также QR-код и персональный числовой код.

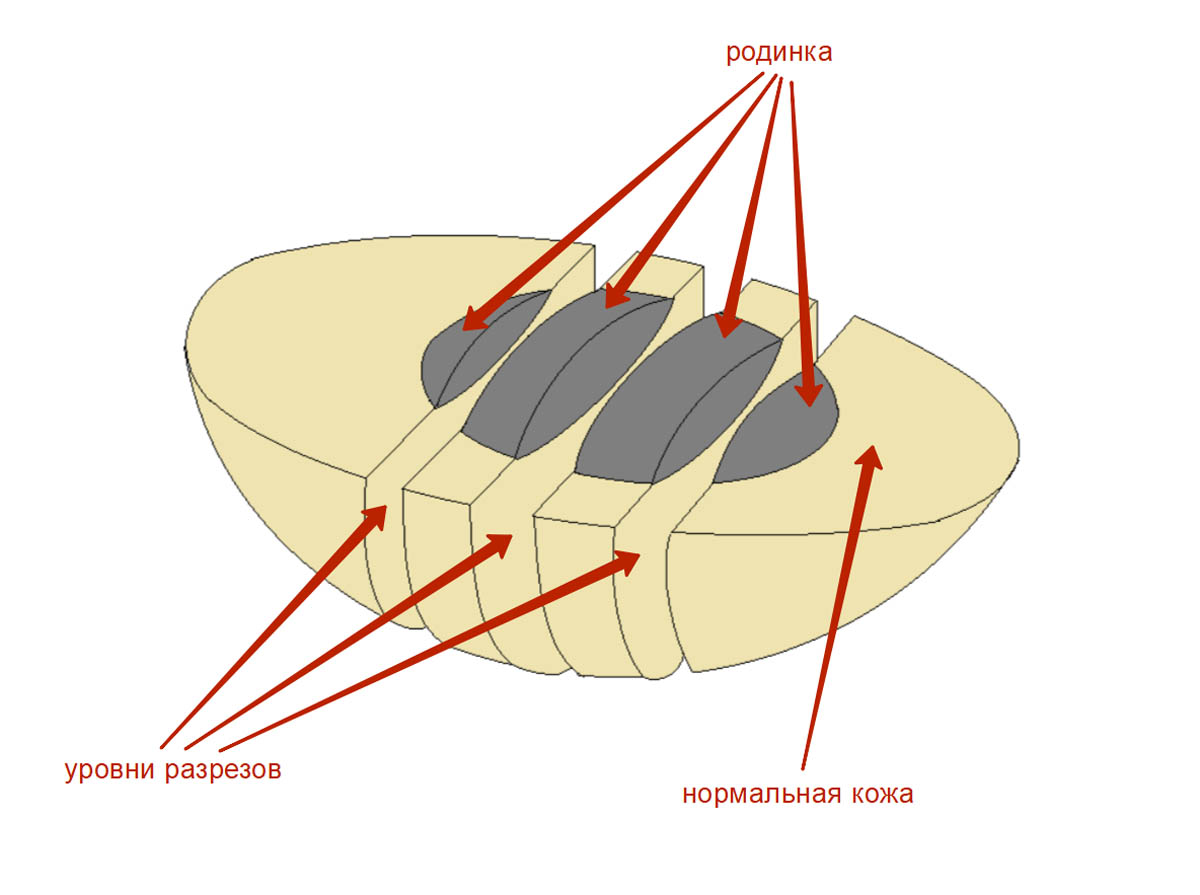
Фрагменты размещают в кассете параллельно плоскости ее дна, как показано на картинке ниже. Если фрагмент положить перпендикулярно плоскости кассеты – это может затруднить оценку краев резекции, т. е. полноты удаления родинки или меланомы.
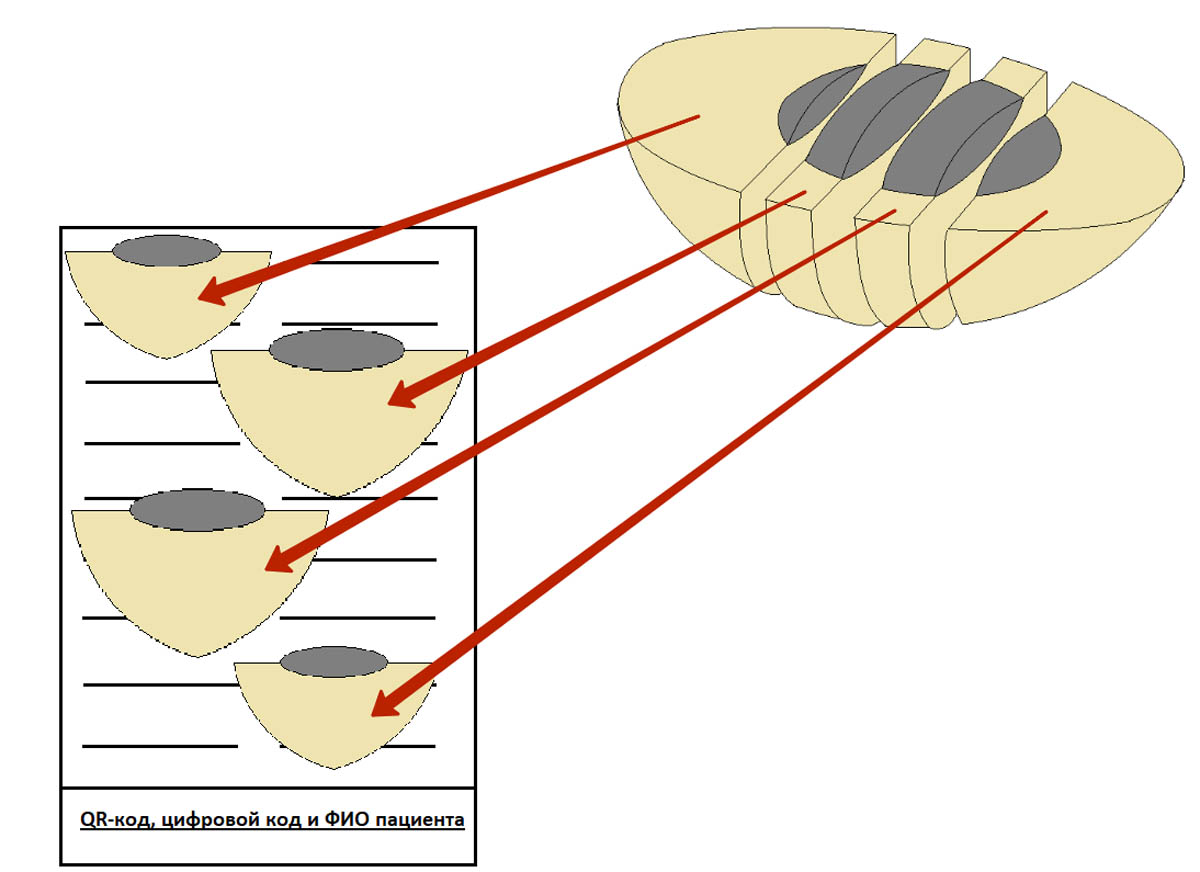
На правильном размещении фрагментов в кассете остановимся подробнее. Это очень важный момент, который позволяет избежать неинформативных срезов в будущем.
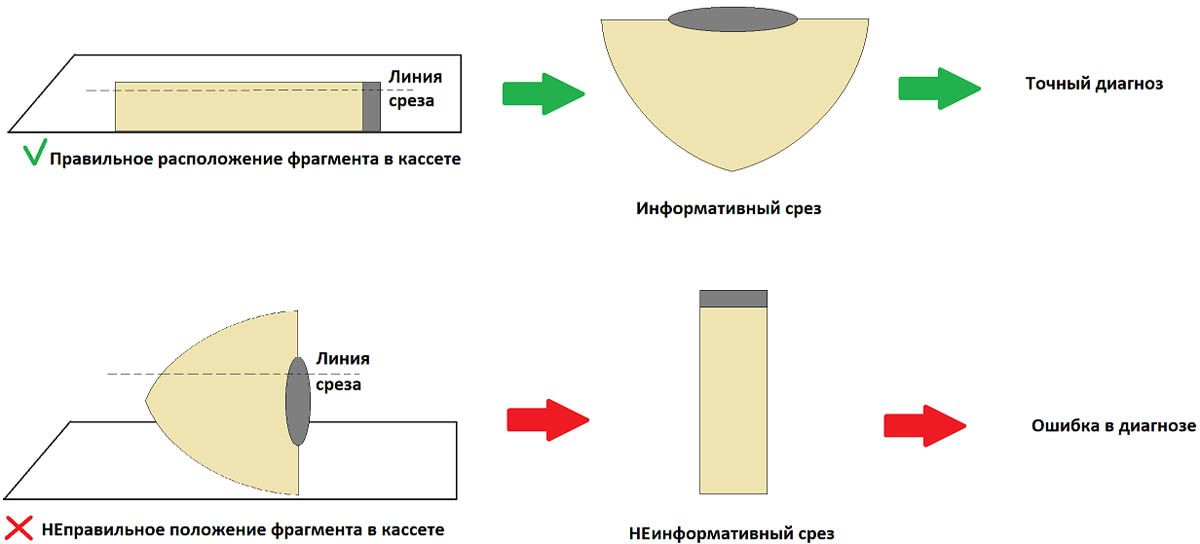
Чтобы исключить подобные ошибки, в процессе исследования используют автоматизированное оборудование.
После того как фрагмент уложат правильно, кассету плотно закрывают, что исключает утрату кусочков и переориентацию на последующем этапе 18–24-часовой фиксации операционного материала в специальном растворе (формалине).

3. Проводка
Этот этап проходит полностью в автоматическом режиме. Лаборант только загружает кассеты в гистопроцессор, выбирает программу и запускает ее.

Кассеты помещают в металлический бокс специальной камеры в верхней части аппарата.

Растворы из резервуаров в нижней части аппарата по очереди перекачиваются в камеру с кассетами. Каждая жидкость контактирует с фрагментами родинки (невуса) в течение определенного времени, после чего ее откачивают из камеры и заливают новую.

Кассета с фрагментами родинки проходит сложный процесс обезвоживания и подготовки к следующему этапу. Внешний вид ее остается прежним, но внутри происходят изменения:

После завершения этого этапа фрагменты уменьшаются, именно поэтому размеры родинки на стеклопрепарате при гистологическом исследовании примерно на 10 % меньше, чем ее реальный размер до удаления на коже.
4. Заливка парафином
Чтобы изготовить максимально тонкий срез с родинки, ее нужно надежно зафиксировать внутри плотного материала. Парафин идеально подходит для этого – он становится жидким при 56–58 градусах и быстро застывает уже при комнатной температуре.

На этом этапе, как и на предыдущем, все делает автомат, лаборант лишь загружает кассеты без парафина и достает уже готовые к получению срезов парафиновые блоки.
Автоматический процесс обеспечивает самое важное – неизменное положение фрагментов родинки (невуса) в кассете. Оно остается неизменным с момента, когда патоморфолог разделил родинку на несколько фрагментов и аккуратно уложил их в кассеты (см. раздел «Вырезка»).
Конечный продукт этого этапа – фрагмент родинки (невуса) с сохраненной исходной ориентацией и залитый парафином.

5. Приготовление срезов
Этот этап выполняет лаборант. Прибор, делающий тканевые срезы толщиной в несколько микронов, называется микротом. Срезы настолько тонкие, что разрушаются, если брать их руками. Поэтому сразу после нарезки их переносят в воду определенной температуры, а из нее – сразу на предметное стекло с персональной наклейкой с QR-кодом, числовым номером и Ф. И. О. пациента.
Конечный продукт этого этапа – НЕокрашенный срез из парафинового блока, расположенный на предметном стекле.
6. Окраска и «заключение» окрашенных срезов
На этом этапе лаборант загружает неокрашенные стекла в специальный аппарат, выбирает программу автоматической окраски и запускает ее. Вероятность любых технологических ошибок при этом сведена к нулю.
Роботизированный аппарат переносит кюретку с окрашиваемыми стеклами поочередно из одного красителя в другой, задерживаясь в одном положении в течение запрограммированного времени. После завершения окраски срезы автоматически покрываются специальной пленкой для защиты от повреждений при исследовании и последующем длительном хранении.
Вот красивый ролик о процессе с сайта производителя оборудования:
А вот небольшой фрагмент работы аппарата в лаборатории, который мне удалось заснять:
После завершения процесса из агрегата извлекают полностью готовые для последнего исследования стеклопрепараты.
8. Изучение препарата врачом-патоморфологом
Наконец родинка (невус) готова к изучению под микроскопом.
В современной лаборатории, такой как НЦКМД, на этом этапе также используются современные и высокие технологии. Но есть два момента, на которые, на мой взгляд, стоит обратить особое внимание.
Морфометрия
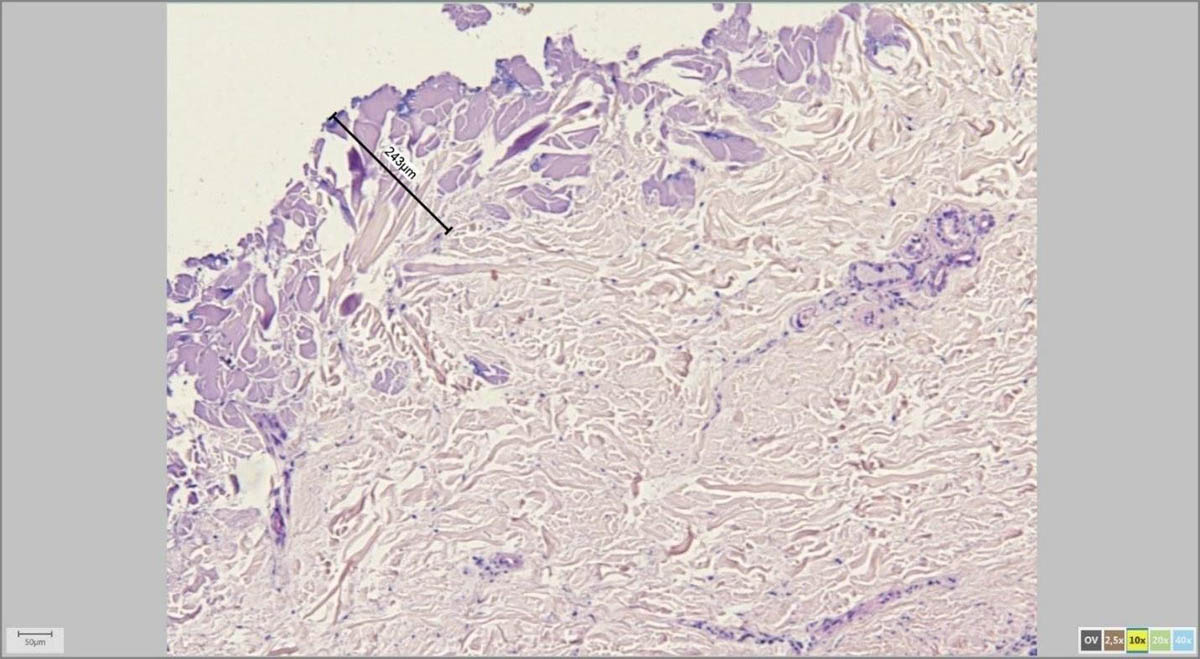
С помощью адаптера для микроскопа и специализированной программы врач-патоморфолог на экране компьютера измеряет параметры удаленной родинки в микрометрах (микронах).
Мне, как дерматоонкологу, это особенно важно для последующих измерений, к примеру, толщины по Бреслоу в случаях меланомы, а также расстояний от края опухоли до края резекции.

На картинках ниже примеры программного измерения различных участков препарата невуса кожи:
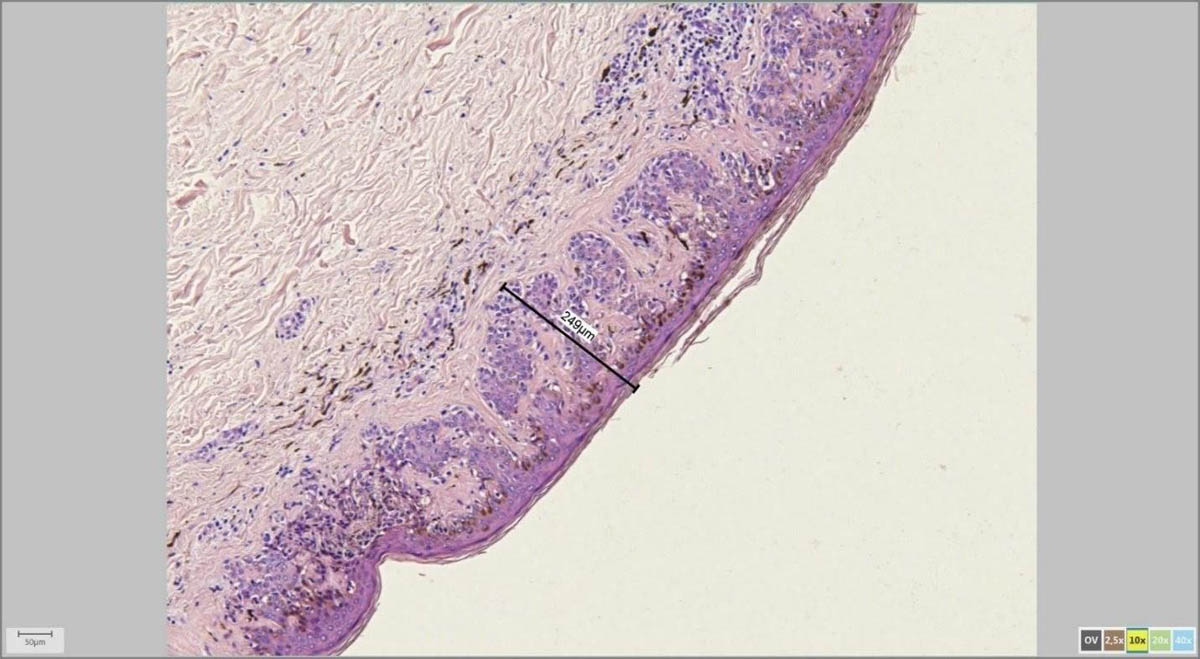
Коллегиальное мнение
До недавнего времени я не знал, что все заключения НЦКМД с диагнозом «злокачественная опухоль» выходят с подписью нескольких морфологов. Такой подход мне нравится и лишний раз подтверждает, что я не ошибся с выбором лаборатории.
Удаленные консультации
Благодаря передаче изображений препаратов на компьютер, открываются широкие возможности. На картинке ниже – специальный сканер гистологических препаратов VisionTek:

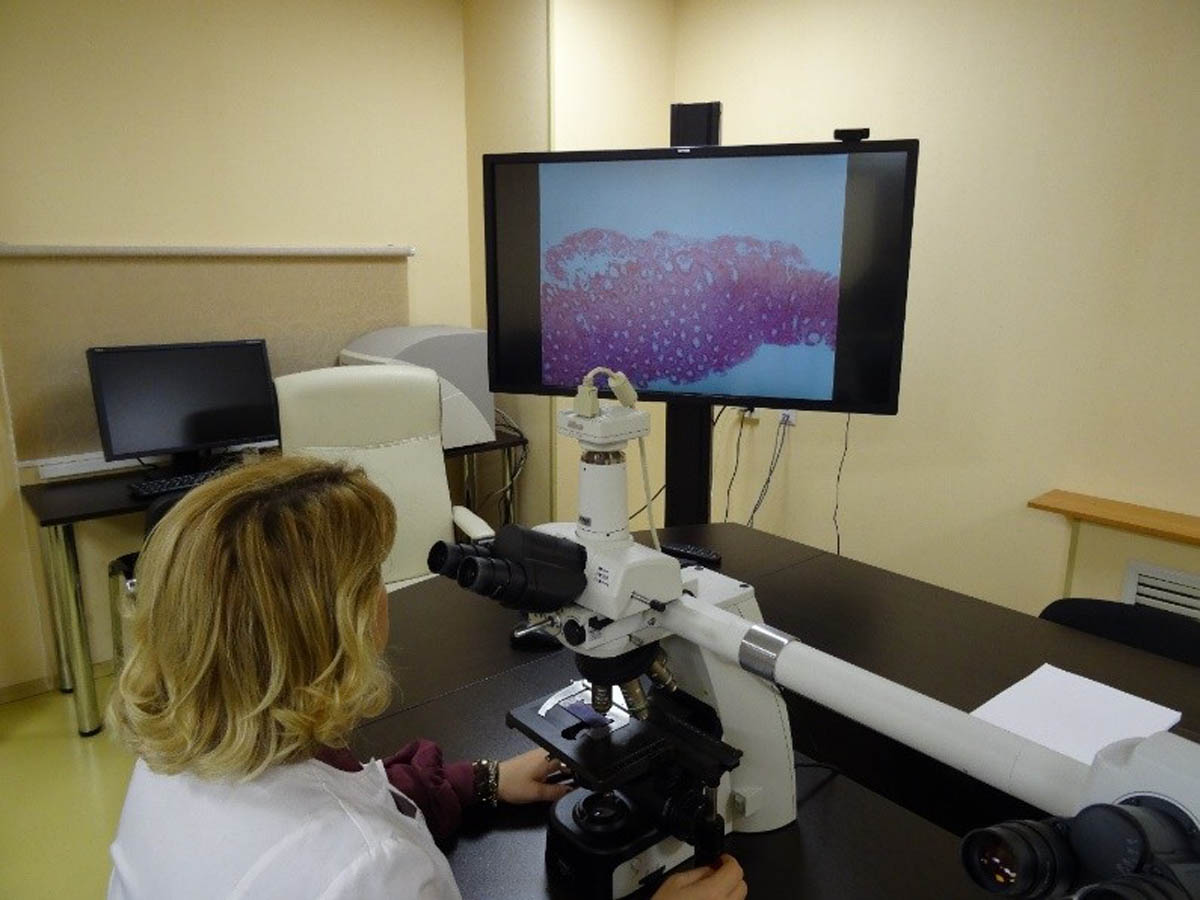
Он позволяет врачам-патоморфологам:
- Сканировать препараты в высоком разрешении, пересылать с помощью IT-технологий в другой город или страну, обсуждая результаты исследований с коллегами в нашей стране и за рубежом.

- Проводить презентации, клинические разборы и обучение, в том числе и телеконференции.

- Сохранять большое число изображений препаратов, которые не требуют физического места для хранения

9. Выдача заключения пациенту
Времена, когда гистологическое заключение выдавали в определенное время и ехать за ним нужно было через весь город, давно прошли. Сейчас результаты исследований из патоморфологической лаборатории отправляют по электронной почте сразу по мере готовности. Национальный центр клинической морфологической диагностики использует эту форму связи с медицинскими учреждениями и пациентами более 4 лет.
В заключении обязательно будут отмечены важные моменты:

- Название учреждения.
- Номер исследования.
- Патоморфологический диагноз.
- Дата исследования.
- Фамилия врача, выполнившего исследование.
Заключение
Теперь вы в деталях знаете, какой путь проходит удаленное образование кожи в современной патоморфологической лаборатории.
Коротко перечислю главные преимущества Центра, благодаря которым я сотрудничаю с этой лабораторией:
- Высокий уровень организации, автоматизации процессов регистрации и пробоподготовки операционного и биопсийного материала и адекватная подготовка лаборантов сводят вероятность ошибок к минимуму.
- Высокая квалификация врачей, возможность коллегиального мнения, в т. ч. с привлечением ведущих специалистов других учреждений, что является залогом точной диагностики.
- От момента регистрации контейнера с родинкой до отправки заключения на еmail проходит менее 48 часов, а не 7–10 дней как во многих других лабораториях.
Я, как дерматоонколог, уверен, что, отправив удаленное образование кожи в НЦКМД, гарантированно получу достоверный диагноз.
P.S. От всего сердца хочу поблагодарить сотрудников Национального центра клинической морфологической диагностики, без помощи которых я бы не написал эту статью.
В Сети огромное количество материала о раке кожи. К сожалению, информация, которая представлена не в виде научных статей и не на сайтах дерматоонкологов, не выдерживает никакой критики.
В этой статье я отвечу на многие животрепещущие вопросы: «как распознать у себя рак кожи?», «опасен ли рак кожи?», «какие варианты лечения рака кожи существуют?» и другие.
Виды рака кожи
Существует 3 вида часто встречающихся злокачественных опухолей кожи. Они различаются как по частоте заболеваемости (т. е. шансу заболеть), так и по степени опасности для жизни – базалиома, плоскоклеточный рак и меланома.
Меланома – одна из редких и опасных опухолей кожи. Она составляет всего 4 % от общего количества злокачественных образований кожи, но является причиной почти 80 % смертей при этой локализации. О меланоме можно подробно прочитать здесь.

Записывайтесь на вебинар "Канцерогены в косметике: правда, ложь и. маркетинг"
Базальноклеточный рак кожи
Базалиома – самый частый, но вместе с тем и наиболее безопасный вид рака кожи. Смерть от базалиомы возможна только в очень запущенных случаях или при агрессивных формах (базосквамозной) опухоли. Благоприятное течение базалиомы обусловлено тем, что она практически никогда не дает метастазов (всего 0,5 % случаев).
Симптомы и признаки
Наиболее часто базалиома возникает на коже носа, чуть реже на лице и значительно реже – на остальных частях тела.
Пик заболеваемости приходится на возраст старше 40 лет. Самой молодой пациентке, которой по гистологии установили диагноз базалиома, было 39 лет.
То, как выглядит базальноклеточный рак кожи, зависит от формы:
- Узловая форма (синоним нодулярная). Опухоль представлена в форме узелка. Отличить ее от других образований кожи можно по увеличенному количеству сосудов на поверхности, восковидному блеску и мелким серо-голубым включениям. Все эти признаки видны на фото.
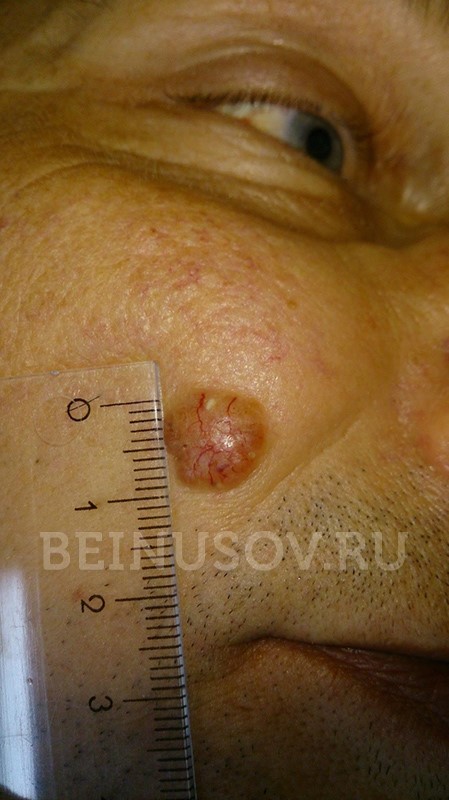
Узловая форма базалиомы
Кроме того, на поверхности узловой базалиомы может быть еще один характерный признак – изъязвление.
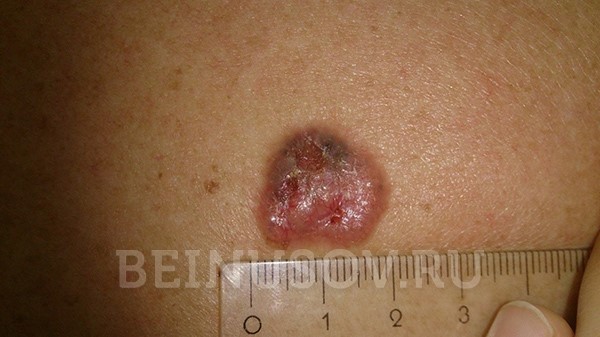
Узловая базалиома с изъязвлением
- Поверхностная форма базалиомы в большинстве случаев представлена в виде участка покраснения на коже. Возможны также элементы шелушения и уже упоминавшийся выше восковидный блеск.
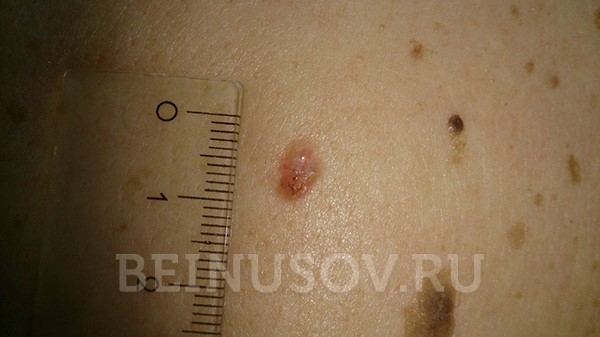
Поверхностная форма базалиомы
- Склеродермоподобная форма базалиомы – очень редкая и часто представляет трудности в диагностике. Она характеризуется более светлым и более твердым в сравнении с окружающей кожей уплотнением.
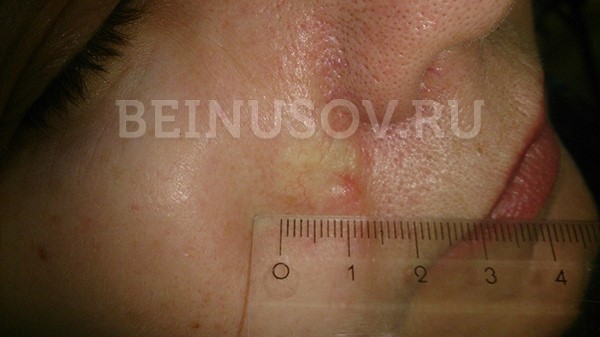
Склеродермоподобная форма базалиомы
- Пигментная форма базалиомы составляет очень малую часть от общего числа этих опухолей. Ее отличает большое количество пигмента. В связи с этим базалиому часто принимают за меланому при осмотре без дерматоскопа.
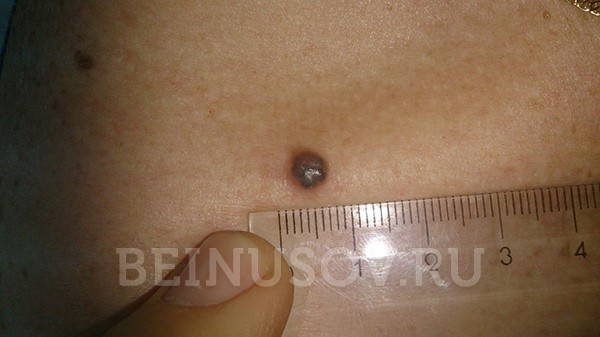
Пигментная форма базалиомы
- Язвенная форма базалиомы может достигать очень больших размеров и в запущенных случаях практически не поддается лечению.
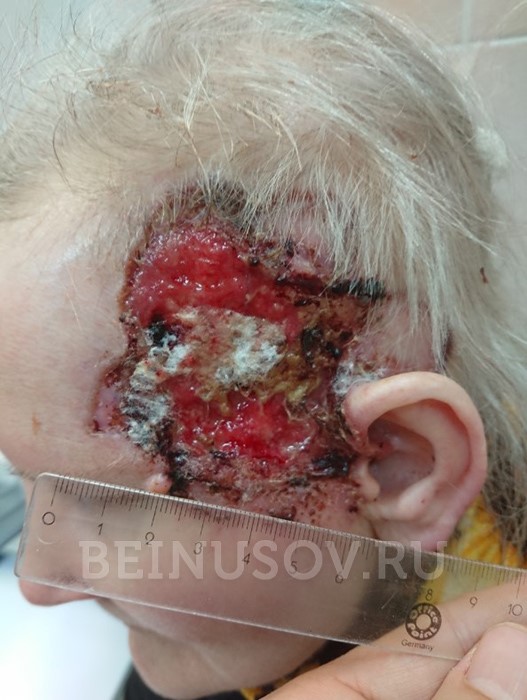
Язвенная форма базалиомы
Фото в начальной стадии
К сожалению, базальноклеточный рак кожи крайне сложно диагностировать на ранних стадиях, т. е. при минимальных размерах. Вот несколько фотографий:
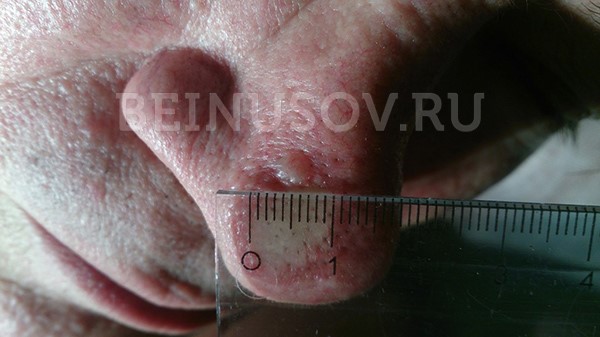
Базалиома кожи носа, узловая форма, размер 5 мм
Базалиома, узловая форма, 3 мм в диаметре
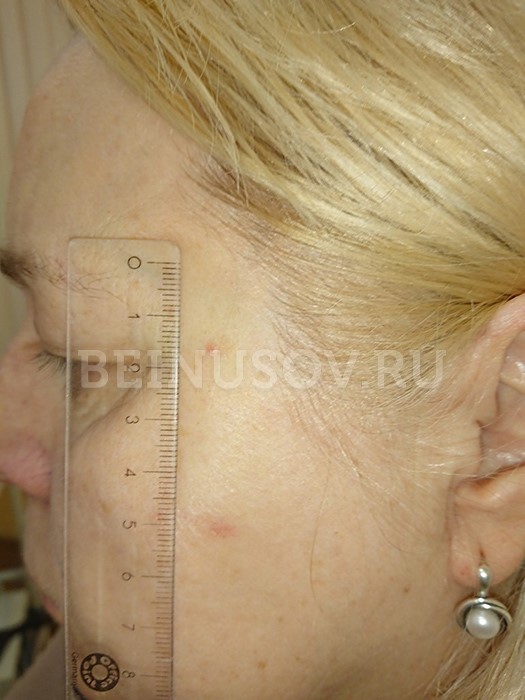
Узловая базалиома височной области, диаметр 2 мм
Диагностика базалиомы на ранних стадиях, при маленьких размерах опухоли, может представлять значительные трудности. Только сочетание комплексного осмотра всей кожи, тщательного выяснения истории существования образования и дерматоскопии поможет в установке диагноза базалиома на ранней стадии.
Базалиомы с высоким и низким риском рецидива (NCCN, 2018)
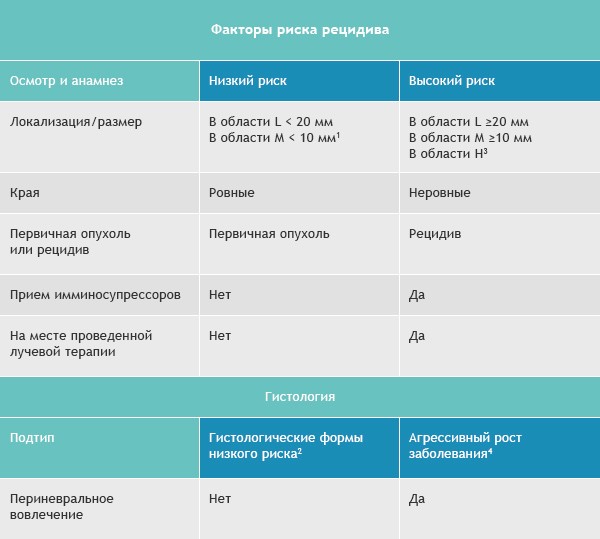
Область H: маска лица (включая веки, брови, кожа вокруг глаз, нос, губы [кожа и красная кайма губ], подбородок, нижняя челюсть, кожа/борозды перед и за ушной раковиной, виски, уши), гениталии, ладони и ступни.
Область M: щеки, лоб, волосистая часть головы, шея и голени
Область L: туловище и конечности (исключая голени, ладони, ступни, ногтевые части и лодыжки)
Примечания
- Локализация вне зависимости от размера может быть признаком высокого риска
- Гистологические формы низкого риска: узловая (нодулярная), поверхностная, кератотическая, пилоидная, с дифференцировкой в сторону придатков кожи, фиброэпителиома Пинкуса
- Область H означает высокий риск вне зависимости от размера
- Морфеаподобный, базосквамозный (метатипический), склерозирующий, смешанный инфильтративный, микронодулярный в любой части опухоли
Для присвоения опухоли статуса «высокий риск рецидива» достаточно только одного из факторов из правого или левого столбца.
Лечение базалиомы
Основной целью лечения базальноклеточного рака является полное удаление опухоли с максимальным сохранением косметических свойств и функций тех частей тела, где развилось это новообразование.
Как правило, наилучший результат обеспечивается хирургическими методами. Однако желание сохранить функциональность и косметические свойства может привести к выбору лучевой терапии в качестве основного метода лечения.
В зависимости от степени риска рецидива (см. выше) подход к лечению базалиомы может различаться.
У пациентов с поверхностной формой базалиомы и низким риском рецидива, когда хирургия или лучевая терапия противопоказаны или неприменимы, могут быть использованы следующие методы лечения:
- 5-фторурациловая мазь;
- мазь «Имиквимод» («Алдара», «Кераворт»);
- фотодинамическая терапия;
- криодеструкция.
Микрографическая хирургия по Mohs может быть рекомендована пациентам с высоким риском рецидива.
Химиотерапия при базалиоме включает препараты-ингибиторы сигнального пути hedgehog – висмодегиб (эриведж) и сонидегиб (одомзо). Эти препараты могут помочь в случае, когда хирургические методы, как и лучевая терапия, неприменимы или противопоказаны.
Что нужно знать о базалиоме?
- В подавляющем большинстве случаев базалиома не представляет угрозы для жизни.
- Если при гистологическом исследовании удаленного образования получен ответ базальноклеточный рак – ничего страшного в этом нет. Важно убедиться, что образование удалено полностью – обязательно проконсультируйтесь с онкологом.
- Если после удаления базалиомы в гистологическом исследовании есть фраза «в крае резекции опухолевые клетки» или что-то похожее – необходимо дальнейшее лечение с целью полного удаления опухоли.
- Настоятельно не рекомендую удалять базалиому без гистологического исследования, т. к. даже очень типично выглядящее образование может быть вовсе не тем, чем кажется на первый взгляд.
- Базалиому нужно лечить. Наблюдение – плохой вариант при подобном диагнозе. Лечение запущенных форм (см. фото язвенной формы) крайне трудное и дорогостоящее.
- Если у вас уже удалили базалиому, необходимо регулярно проходить осмотр всей кожи у онколога с целью возможного выявления еще одной такой опухоли.
- Вероятность метастазирования у метатипического (базосквамозного) гистологического типа выше, чем у остальных видов.
Плоскоклеточный рак
Встречается реже, чем базалиома, второй по частоте вид рака кожи и имеет чуть менее благоприятный прогноз. Однако необходимо отметить, что течение заболевания значительно менее злокачественное, чем при меланоме.
Метастазы возникают относительно редко – в среднем в 16 % случаев [1]. У больных плоскоклеточным раком кожи размером менее 2 см 5-летняя выживаемость составляет около 90 %, при больших размерах и прорастании опухоли в подлежащие ткани – менее 50 % [1].
Может возникать на любых участках тела, в том числе на гениталиях и на слизистых, однако наиболее часто – в местах, подверженных попаданию солнечных лучей.
Симптомы и признаки
То, как выглядит плоскоклеточный рак кожи, зависит во многом от клинической формы заболевания.
Ороговевающая форма – возвышение или ровная поверхность, покрытая роговыми чешуйками, которые могут нарастать и отваливаться. При повреждении может кровоточить.
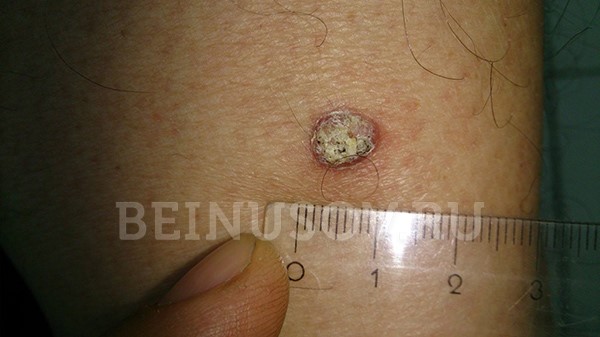
Ороговевающая форма плоскоклеточного рака кожи
Необходимо помнить, что под маской кожного рога может скрываться именно ороговевающая форма плоскоклеточного рака. В связи с этим подобные образования всегда стоит удалять только с гистологическим исследованием:

Кожный рог следует удалять с гистологией – под его маской может скрываться ороговевающая форма плоскоклеточного рака
Неороговевающая эндофитная форма (растущая в направлении окружающих тканей). Чаще всего выглядит как длительно не заживающая рана или язва, которая может со временем углубляться и расширяться.
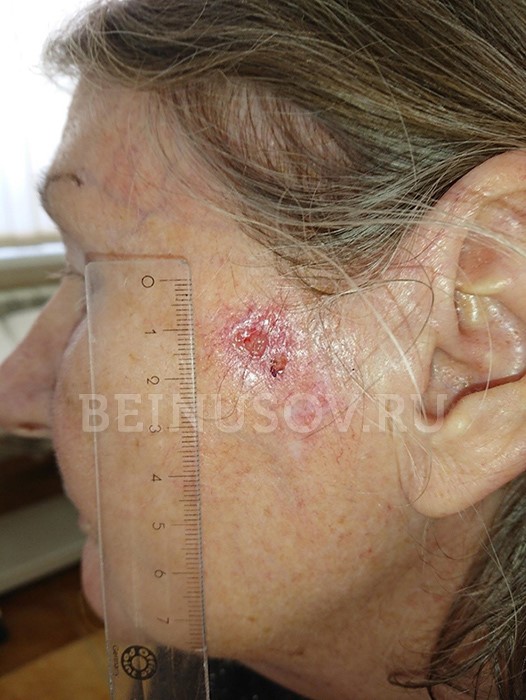
Неороговевающая эндофитная форма плоскоклеточного рака кожи
Экзофитная неороговевающая форма плоскоклеточного рака кожи выглядит как узел, возвышающийся над уровнем кожи. Поверхность узла может быть эрозирована или мокнуть.
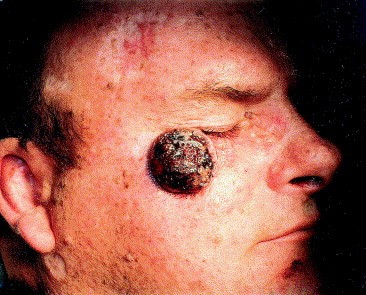
Экзофитная неороговевающая форма плоскоклеточного рака кожи
Фото в начальной стадии
Под начальной стадией плоскоклеточного рака понимается состояние, когда злокачественный процесс ограничен эпидермисом – самым верхним слоем кожи. Обозначается в диагнозе как in situ или внутриэпидермальный плоскоклеточный рак. Это заболевание не представляет опасности для жизни, если удалено полностью.
Существует 2 формы этой фазы заболевания:
Болезнь Боуэна
Чаще всего представлена одиночными плоскими бляшками, с четкими границами, асимметричной формой, неровными краями. Размер достигает 7–8 мм. Образование может постепенно увеличиваться, на поверхности часто отмечается шелушение либо образование корочек.
Цвет красный или коричневый, располагается на любых участках тела. [3]
От себя добавлю, что в моей практике гистологически подтвержденная болезнь Боуэна встретилась всего один раз. Выглядела как небольшое (3 х 4 х 3 мм) телесного цвета уплотнение с гладкой поверхностью на коже ствола полового члена у мужчины 43 лет.

Эритроплазия Кейра
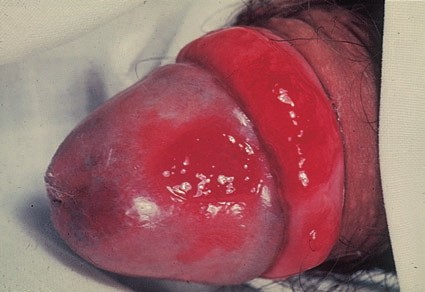
Вторая форма рака кожи начальной стадии, которая развивается наиболее часто на коже крайней плоти полового члена или головке. Значительно реже заболевание поражает женские наружные половые органы.
Наиболее частый внешний вид эритроплазии Кейра – ярко-красное пятно с четкими границами, влажной блестящей поверхностью [3].
Лечение плоскоклеточного рака кожи (NCCN, 2018)
Как и в случае с базалиомой, для плоскоклеточной карциномы выделяют группы высокого и низкого рисков рецидивирования и метастазирования.
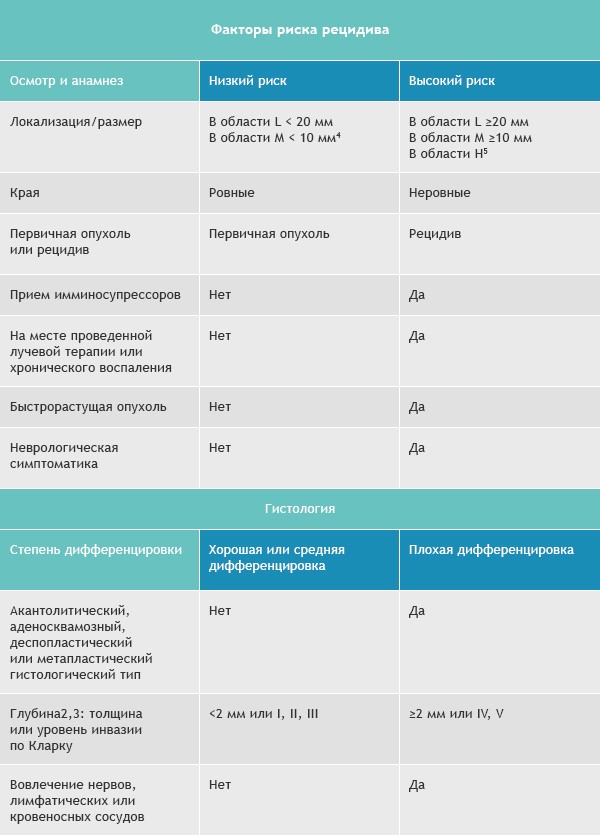
Область H: маска лица (включая веки, брови, кожа вокруг глаз, нос, губы [кожа и красная кайма губ], подбородок, нижняя челюсть, кожа/борозды перед и за ушной раковиной, виски, уши), гениталии, ладони и ступни.
Область M: щеки, лоб, волосистая часть головы, шея и голени
Область L: туловище и конечности (исключая голени, ладони, ступни, ногтевые части и лодыжки)
Примечания
- Ободок гиперемии должен быть учитываться при измерении размера.
- Эксцизионная биопсия более предпочтительна, чем инцизионная.
- Модифицированное измерение толщины по Бреслоу должно исключать паракератоз и «корочку», должно проводиться от основания язвы, если таковая имеется.
- Локализация независимо от размеров может быть признаком высокого риска.
- Область H подразумевает высокий риск вне зависимости от размера.
Основные принципы и методы лечения при плоскоклеточном раке – такие же, как и при базалиоме.
Основная цель – сохранить функциональность и косметические качества. Наиболее эффективным принято считать хирургический метод – удаление опухоли с захватом 4–6 мм здоровых тканей при низком риске рецидивирования и метастазирования. Для опухолей с высоким риском рекомендована микрографическая хирургия по Mohs либо иссечение в более широких границах, чем при низком риске.
Лучевая терапия применима в случаях, когда другие методы не могут быть использованы. При химиотерапии плоскоклеточного рака могут применяться препараты платины (цисплатин, карбоплатин), а также ингибиторы EGFR (цетуксимаб).
Как не заболеть раком кожи? Чего избегать?
Солнечный свет. Наиболее доказанной причиной появления обоих видов рака кожи, впрочем, как и меланомы, является воздействие солнечного света. Если вы любите бывать в жарких странах, у вас светлые волосы и кожа или ваша работа связана с длительным пребыванием на солнце – стоит серьезно озаботиться защитой от ультрафиолета.
Предраковые заболевания кожи – следующий фактор, который может предшествовать развитию плоскоклеточной формы: актинические (солнечные) кератоз и хейлит, лейкоплакия, папилломавирусная инфекция слизистых оболочек и гениталий. Этот вид опухоли может развиться также на фоне рубцовых изменений после ожогов или лучевой терапии.
Контакт с канцерогенами
Различные химические вещества могут приводить к развитию рака кожи: мышьяк и нефтепродукты.
Ослабленная иммунная система. Люди, принимающие иммуносупрессоры после трансплантации органов, или носители ВИЧ-инфекции имеют повышенный риск развития рака кожи плоскоклеточного типа.
Резюме
Рак кожи в подавляющем большинстве случаев – не смертельное заболевание. На ранних стадиях он лечится вполне успешно, в арсенале врачей много разных методов. В случае агрессивных форм или длительного течения без лечения рак кожи может представлять опасность для жизни.
Обследования при опухолях с неизвестной первичной локализацией
Здесь представлены лишь общие соображения, касающиеся этой трудной проблемы. Следует подчеркнуть, что для каждого пациента выбирается своя глубина обследования. При этом принимаются во внимание такие факторы, как возраст и физическое состояние больного, его психологическая готовность к процедурам, а также вероятность обнаружить курабельную опухоль.
Принятие врачом решения проводить дальнейшее обследование больного требует рассудительности и опыта. В общем, чем меньшим опытом обладает врач, тем больше он назначает различных процедур обследования. После обнаружения метастазов и исключения курабельных случаев, необходимо убедить больного в том, что дальнейшее обследование с целью выяснения локализации первичной опухоли не требуется (или не принесет ему пользы).
Гистологические исследования при опухолях с неизвестной первичной локализацией
Первый, наиболее важный этап обследования состоит в обсуждении результатов анализа биопсийного материала вместе с опытным врачом-гистологом. У гистолога могут быть предположения относительно локализации первичной опухоли, однако из-за отсутствия клинической информации он не может их подтвердить. Обычно при гистологическом исследовании обнаруживается плохо дифференцированная аденокарцинома или недифференцированная опухоль.
Использование специальных методов окраски может дать дополнительную информацию, как, например, при иммуногистохимическом окрашивании препаратов крупноклеточных лимфом. Эти опухоли часто бывает трудно отличить от анапластической карциномы, однако они обладают высокой чувствительностью к химиотерапевтическим средствам. Прокрашивание гистологических препаратов красителями на муцин позволяет обнаружить его в опухолевых клетках, что свидетельствует об их происхождении из тканей кишки, поджелудочной железы или желудка.
Определить происхождение опухолевых клеток можно с помощью моноклональных антител, специфичных к определенным белкам цитоплазмы или клеточной мембраны. В случаях недифференцированных опухолей чрезвычайно важно не пропустить крупноклеточную лимфому, и для этого обычно проводят гистологический анализ с использованием антител к общему антигену лейкоцитов, и к антигенам эпителиальных клеток, например к цитокератинам.
В таблице ниже представлены наиболее часто используемые реагенты и методы для анализа гистологических препаратов. Для одних реагентов необходимо использовать парафиновые срезы, для других — срезы замороженной ткани. Поэтому при подозрении на рак биопсийные образцы не следует фиксировать в формалине. Существуют антитела к мембранным антигенам клеток эпителия.
С их помощью можно обнаружить эпителиальные опухоли, например рак легкого, или другие плохо дифференцированные аденокарциномы. Антитела к прекератину позволяют ответить на вопрос, является ли опухоль сквамозной. Также существуют антитела к специфическому антигену меланомы. У женщин положительный тест на наличие эстрогеновых и прогестероновых рецепторов в клетках биоптатов, взятых из подмышечного или надключичного лимфатических узлов, может указывать на опухоль молочной железы.
В отдельных случаях полезно электронно-микроскопическое иесследование. Например, с помощью этого метода в клетках злокачественной меланомы можно обнаружить пре-меланосомы, а в клетках плохо дифференцированной сквамозной карциномы — существование межклеточных мостиков. Недифференцированные опухоли герминативного происхождения у больных молодого возраста относятся к числу курабельных раков, однако при обследовании их часто пропускают. В клетках этих опухолей содержится хориогонадотропин (ХГЧ) и а-фетопротеин (АФП), которые можно обнаружить при иммуногистохимическом окрашивании препаратов.

Инструментальные методы исследования при опухолях с неизвестной первичной локализацией
С помощью инструментальных методов определяют степень развития опухоли, а в отдельных случаях и локализацию ее первичного очага.
Рентгеноскопия грудной клетки является важным методом обследования и позволяет обнаружить карциному бронха, или увеличение медиастинальных лимфатических узлов, указывающее на возможность лимфомы.
При компьютерной томографии брюшной полости в 25% случаев удается обнаружить локализацию первичной опухоли. Если метастазы представляют собой аденокарциному, то часто местом ее локализации является поджелудочная железа. Диагносцирование первичной опухоли поджелудочной железы не влияет на выбор метода лечения. Обнаружение метастазов в надпочечниках позволяет предположить, что первичная опухоль локализована в легком.
При небольших размерах легочных метастазов они, вероятно, образуются из опухоли ободочной кишки, предстательной или щитовидной железы.
Для сарком характерны несколько более крупные метастазы. Кальцификация печеночных метастазов позволяет заподозрить опухоль ободочной кишки. Для дифференциальной диагностики карциномы молочной железы необходимо проводить маммографию, поскольку поражение надключичных или подмышечных лимфатических узлов не исключает возможности успешного лечения.

Гематологические и биохимические исследования исследования при опухолях с неизвестной первичной локализацией
Некоторые исследования проводят во всех случаях. К числу их относится анализ содержания щелочной фосфатазы и/или PSA в крови у мужчин старше 40 лет, позволяющий обнаружить карциному простаты. Определение уровня ХГЧ и АФП у больных молодого возраста позволяет обнаружить опухоли герминативного происхождения. Уровень АФП увеличивается также при гепатомах. При подозрении на миелому для выявления белков Бенс-Джонса необходимо провести электрофоретическое исследование плазмы крови и мочи.
При исследовании мазков крови может быть обнаружена лейкоэритробластная анемия, наиболее характерная для рака молочной железы. При карциноме почки и гепатоме отмечаются полицитемия и тромбоцитоз. Развитие гипокалиемии и гиперкальциемии свидетельствует о развитии синдрома Кушинга, который в данном случае, скорее всего, обусловлен мелкоклеточным раком легкого.
Прочие исследования
Для обнаружения эритроцитов необходимо провести анализ свежеполученных образцов мочи. Присутствие эритроцитов может указывать на карциному почки. Также могут оказаться полезными результаты определения сывороточных маркеров, однако диагностического значения они не имеют. При подозрении на карциному органов желудочно-кишечного тракта, исследуют уровень СЕА, а при подозрении на рак яичников — уровень СА-125.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

