Опоясывающий герпес и межреберная невралгия это одно и тоже
Обновлено: 17.05.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Постгерпетическая невралгия: причины появления, симптомы, диагностика и способы лечения.
Определение
Постгерпетическая невралгия - это боль или аномальные чувствительные ощущения, связанные с поражением нервной системы вирусом ветряной оспы.
Причины постгерпетической невралгии
После перенесенной ветряной оспы (ветрянки) вирус герпеса человека 3-го типа – вирус Варицелла Зостер (Varicella zoster) - из высыпаний на коже и слизистых может перемещаться в чувствительные ганглии (узлы, состоящие из скопления нейронов) спинномозговых нервов грудного, поясничного уровней или тройничного нерва. Там вирус в течение десятилетий способен оставаться в латентном (неактивном) состоянии. При снижении иммунитета (например, на фоне вирусных заболеваний, химиотерапии, онкологических заболеваний, терапии глюкокортикостероидными гормонами системных заболеваний соединительной ткани (ревматических болезней)) вирус может активироваться и вызывать развитие опоясывающего герпеса (опоясывающего лишая, Herpes zoster) или невралгии тройничного нерва.
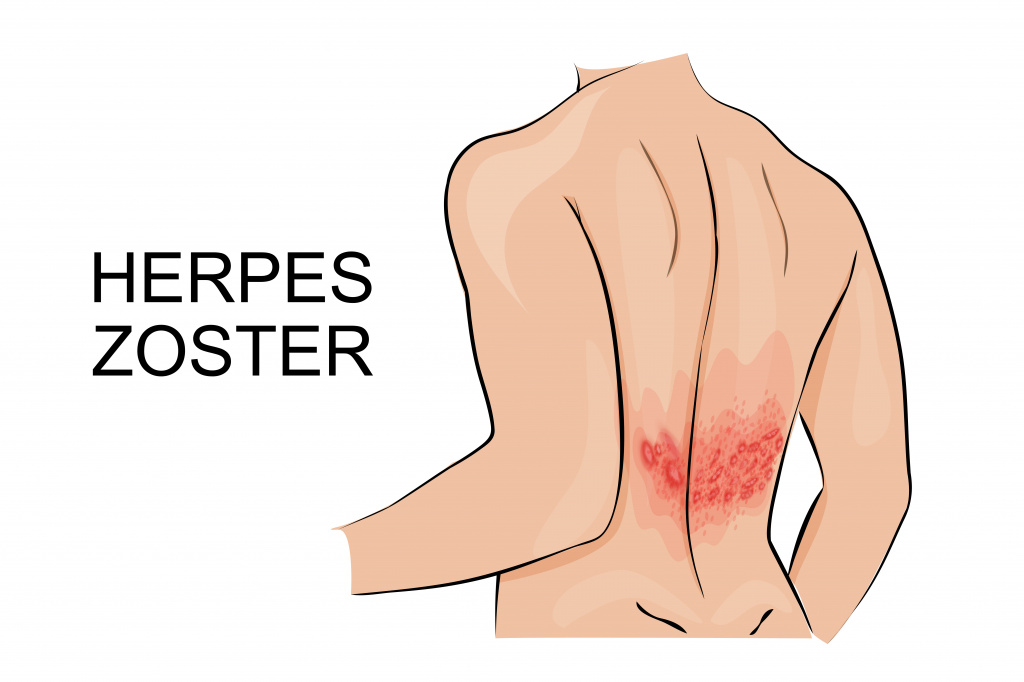
Заболевание начинается с односторонней боли, чувства жжения, повышенной кожной чувствительности, после чего, иногда спустя 1-2 недели появляется покраснение, а затем - пузырьковые высыпания на коже. У 50% больных высыпания локализуются на туловище (как правило, вдоль межреберных промежутков на уровне грудного отдела позвоночника, иногда – в области поясницы, крестца), у 20% - на голове (при поражении тройничного нерва, возможно поражение глаз, ушей), у 15% - на руках, и у 15% - на ногах. В большинстве случаев с течением времени боль проходит самостоятельно - выздоровление происходит через 2-3 недели, но иногда (примерно у 20% больных) развивается осложнение опоясывающего герпеса - постгерпетическая невралгия.
Постгерпетическая невралгия редко наблюдается у детей и молодых людей, но ее частота значительно увеличивается в пожилом возрасте.
Реальная распространенность постгерпетической невралгии неизвестна, поскольку нет единой точки зрения на временной промежуток между высыпаниями, появлением боли и продолжительностью болевого синдрома.
Классификация постгерпетической невралгии
Ряд авторов предлагают различать три временные фазы болевого синдрома, связанного с Herpes zoster.
- Острая герпетическая невралгия, при которой боль длится до 30 дней с момента появления сыпи.
- Подострая герпетическая невралгия, продолжающаяся 30-120 дней после возникновения сыпи.
- Постгерпетическая невралгия, при которой боль сохраняется более 120 дней после возникновения сыпи.
Симптомы постгерпетической невралгии
Основной жалобой пациентов является боль. Она характеризуется различной интенсивностью и частотой – от легкой до крайне мучительной, от кратковременной до постоянной. При опоясывающем герпесе болевые ощущения могут распространяться за пределы локализации высыпаний. В клинической картине постгерпетической невралгии можно выделить следующие типы боли:
- постоянная боль, которую пациенты описывают как тупую, давящую или жгучую;
- пароксизмальная (приступообразная) боль, которая возникает внезапно, острая, стреляющая, пронзающая;
- аллодиния – боль, возникающая в ответ даже на очень слабые раздражители, которые при обычных обстоятельствах боль не вызывают, – например, на легкое прикосновение холодной рукой.
Некоторые пациенты жалуются на интенсивный зуд, который локализуется, как правило, в области головы и шеи.
Диагностика постгерпетической невралгии
В начале заболевания опоясывающим герпесом, когда пациентов беспокоит только боль, врач может подозревать заболевание сердца, межреберную невралгию, остеохондроз. Однако с появлением высыпаний диагноз становится очевидным.
Инструментальная и лабораторная диагностика, как правило, не проводятся.
В нетипичных случаях может быть назначен серологический тест 256 в комплексе с тестом № 257 (IgM антитела) для диагностики ветряной оспы. Кроме того, эти исследования могут потребоваться для оценки иммунитета к вирусу.
Синонимы: Анализ крови на антитела к вирусу ветрянки; Ветряная оспа; Вирус герпеса человека 3-го типа; ВГВ-3 типа; Вирус varicellae-zoster; Опоясывающий герпес. Chickenpox; Human herpesvirus 3 IgG; Varicellazoster virus IgG; Herpeszoster IgG. Краткое описание исследования Ант.
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Доказано, что повреждение нейрональных структур начинается перед появлением кожной сыпи. При этом VZV по ходу чувствительных нервных волокон проникает в кожу, «ускользая» от факторов врожденного и приобретенного иммунитета, что в конечном итоге обусловливает возникновение односторонней везикулярной кожной сыпи, характерной для опоясывающего лишая.
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
СПИСОК ЛИТЕРАТУРЫ
Что такое межреберная невралгия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кричевцова Валерия Леонидовича, невролога со стажем в 32 года.
Над статьей доктора Кричевцова Валерия Леонидовича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Межреберная невралгия (МРН) — совокупность болевых симптомов, возникающая в результате повреждения межреберных нервов.
Межреберный нерв составляют вегетативные, чувствительные, двигательные волокна. Травматические, компрессионные, воспалительные воздействия оказывают на межреберный нерв раздражающее влияние, в итоге происходит болевой рефлекторный ответ по ходу межреберных промежутков. [1]
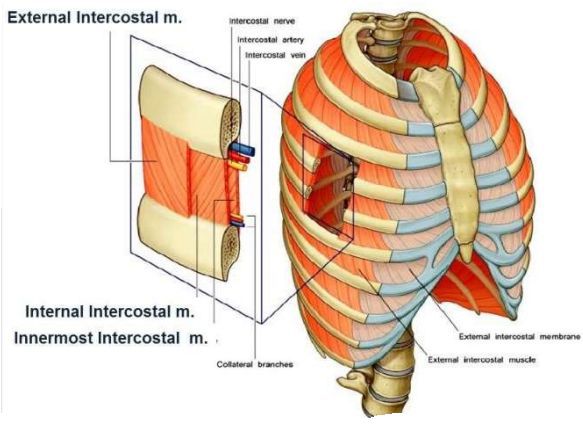
Сегодня в научной среде выделяется целый ряд причин межреберной невралгии:
- защемление нервов;
- травматическая или ятрогенная нейрома;
- постоянное раздражение нервов или опоясывающий лишай;
- дегенеративно-дистрофические заболевания позвоночника (остеохондроз, грыжи дисков, протрузии дисков, спондилолистез, травмы, остеопороз с коллапсом позвонков, артрит реберного сустава); [2]
- деформации позвоночника (сколиоз);
- локальное переохлаждение межреберных мышц или нервов;
- рассеянный склероз;
- опухоли;
- врожденные пороки развития, наследственные заболевания;
- токсические поражения;
- хронические воспаления легких, плевриты;
- ВИЧ-инфекция;
- тораколюмбарные периневральные кисты.
Существует и межреберная невралгия посттравматического характера, возникающая вследствие:
б) физической активности;
в) длительного, сильного кашля;
г) хирургических операций, которые фиксируют пациента в определенных положениях в течение длительных периодов времени;
е) травм грудной клетки и спины.
В некоторых случаях МРН возникает в результате медицинских манипуляций. Сообщается о случаях межреберной невралгии, возникающей как осложнение внутренностной радиочастотной абляции (RFA), из-за нарушения целостности изолирующей оболочки иглы RFA. [11]
Боль при МРН является результатом повреждения или воспаления межреберных нервов и локализуется в одном или нескольких местах межреберного пространства. Хотя зачастую заболевание возникает после торакотомии, сообщалось о межреберной невралгии у пациентов после грудной и абдоминальной хирургии, травм и инфекций. МРН из-за хирургического повреждения межреберного нерва традиционно трудно поддается лечению.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы межреберной невралгии
Основной симптом МРН описывается больными как «прострел, электрический ток» по ходу нерва, затем возникает боль в грудной клетке (торакалгия). Как правило, распространяясь между ребрами, от позвоночника к грудине, боль сначала не такая интенсивная, однако может усиливаться, принимая нестерпимый характер; отдает в лопатку, сердце, область эпигастрия. Болевые припадки могут длиться от нескольких секунд до двух-трех минут, появляясь вследствие неловкого движения, вздоха, кашля или смеха.
Если по ходу нерва возникает гиперемия, бледность кожи или гипергидроз, парестезии, значит поражены вегетативные волокна, входящие в состав нерва. Описанная симптоматика нередко сопровождается паническими атаками.
Герпетическая инфекция при МРН провоцирует кожные высыпания, которые возникают на второй-четвертый день, локализуясь на коже между ребрами.
Во время пальпации определенных частей тела (в области между ребрами вдоль спинальных дисков и грудной клетки) пациент может почувствовать острую боль. Кроме того, пациенты часто жалуются на боль во время активной ингаляции и выдоха, описывая свои ощущения как «перехватывает дыхание». Присутствует также «отражение» боли, которая обычно локализуется в других частях тела и может возникать под лопаткой, в спине и области паха. Характерной особенностью является также «боль в пояснице». МРН может сопровождаться не только болью и стеснением межреберного пространства, но также непроизвольным сокращением и подергиванием отдельных групп мышц. В области повреждения периферийных нервов кожа может краснеть, бледнеть или утратить чувствительность. Общие симптомы (лихорадка, одышка, потоотделение) при МРН, как правило, отсутствуют. [9]
Патогенез межреберной невралгии
В классическом варианте механизм острой межреберной невралгии связан с активацией болевых рецепторов (периферических ноцицепторов) цитокинами, выделившимися из поврежденной ткани. В результате механического действия костных структур на нерв происходит массивный выброс медиаторов воспаления (цитокинов), которые провоцируют отек и воспалительный процесс в окружающих нерв тканях. Межпозвоночные и межреберные мышцы рефлекторно спазмируются по механизму биологической обратной связи и тем самым усиливают воспаление и боль.
Но при воздействии на нерв токсических веществ, физических факторов, вирусов и бактерий, опухолей, остеобластоме, [4] глиозе спинного мозга, ВИЧ-инфекции, лучевой болезни, плеврита или пневмонии возникают схожие симптомы.
Межреберная невралгия может быть проявлением функционального заболевания нервной системы, истерии, неврастении. В исключительных случаях может возникать как следствие оперативного вмешательства на грудной клетке. [5]
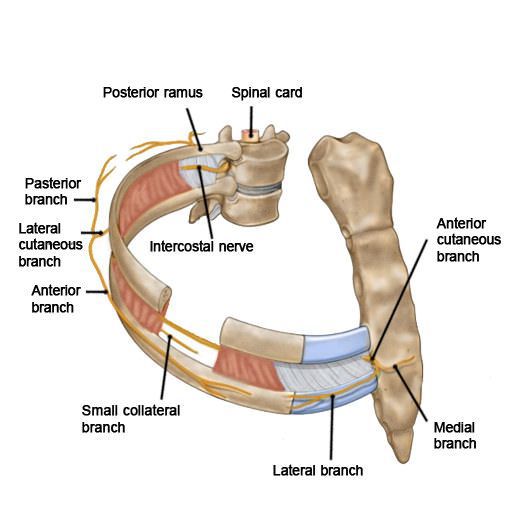
Основные проявления МРН — резкие интенсивные стреляющие боли, часто — жжение. Боль носит постоянный характер и может включать любой из межреберных нервов и нерв 12-го ребра. Болевые ощущения обычно начинаются у задней подмышечной линии и иррадируют вперед в область пораженного межреберья. Это обычно боль костно-мышечного происхождения (например, боль в суставах или перелом ребра). [1] [2] Глубокий вдох или движения грудной клетки усиливают болевые ощущения.
При МРН в грудной клетке ощущается сильная, острая, стреляющая боль, которая излучается спереди назад (или наоборот). Кожа может быть болезненной на ощупь, чувствительна к прикосновениям или наоборот — может иметь пониженную чувствительность.
Классификация и стадии развития межреберной невралгии
Специальной классификации межреберной невралгии не существует, различают отдельные формы в зависимости от причины заболевания, а также первичные и вторичные поражения.
В МКБ - 10 и выглядит как М79.2.
Осложнения межреберной невралгии
Когда говорят об осложнениях межреберной невралгии, как правило, упоминают о наиболее распространенном — постпроцедурной боли в результате интервенционного лечения. Местная боль возникает в течение нескольких дней после почти всех видов процедур. 20% пациентов, которые получали радиочастотную терапию, сообщили, что послепроцедурная боль продолжалось несколько недель. [10]
Основные осложнения межреберной блокады нерва — пневмоторакс и внутрисосудистые инъекции местных анестетиков. Для обнаружения этих осложнений необходим тщательный постпроцедурный мониторинг.
Другие редкие осложнения, связанные сблокадой межреберного нерва:
- инфекции;
- гемоторакс;
- кровохарканье;
- гематомы;
- некроз тканей;
- неврит;
- респираторная недостаточность;
- субарахноидальный блок;
- аллергическая реакция на местные анестетики. [11]
Диагностика межреберной невралгии
Физический осмотр обычно дает минимальные результаты, если только у пациента есть в анамнезе операции на грудной клетке (грудная или подреберная хирургия) или опоясывающий герпес. Предпочтительно проводить осмотр грудного отдела позвоночника с пациентом в сидячем положении и включать осмотр в покое и пальпацию позвонков и паравертебральных структур. Провокация боли путем проведения пассивных поворотов вперед, сгибание, обратное сгибание и боковые сгибания, в частности, могут указывать на то, что боль имеет спинальное происхождение. [9]
Как правило, на осмотре пациент наклоняет туловище в здоровую сторону, уменьшая таким образом давление на пораженный межреберный нерв. Если повреждено несколько нервов, невролог при осмотре может определить зону понижения или выпадения чувствительности определенных участков кожи туловища.
Если поражены нижние межреберные нервы, болевой синдром имеет сходства с заболеваниями желудочно-кишечного тракта (гастрит, язва желудка, острый панкреатит). Следует отметить, что при заболеваниях желудка боль обычно носит более длительный и менее интенсивный характер и, как правило, связана с приемом пищи. Панкреатит характеризуется опоясывающими болями двустороннего характера.
Чтобы исключить патологию органов ЖКТ, целесообразно провести дополнительные обследования: анализ панкреатических ферментов в крови, гастроскопия и пр. Если межреберная невралгия возникает как симптом грудного радикулита, то болевые пароксизмы протекают на фоне постоянных тупых болей в спине, уменьшающихся при разгрузке позвоночника в горизонтальном положении.
Для анализа состояния позвоночника проводится рентгенография грудного отдела, при подозрении на межпозвоночную грыжу — МРТ позвоночника.
МРН встречается при некоторых заболеваниях легких (атипичной пневмонии, плеврите, раке легкого).
При диагностике межреберной невралгии следует иметь в виду сирингомиелию, менингорадикулиты, интрадуральные опухоли, а также отраженные боли от внутренних органов – зоны Геда. [2]
Лечение межреберной невралгии
В остром периоде заболевания прежде всего необходимо исключить вирусную этиологию межреберной невралгии, если условия не позволяют выполнить подтверждающие исследования, противогерпетические препараты (ацикловир) следует назначить в профилактических целях.
Для купирования воспалительного процесса и боли назначают:
- глюкокортикоиды (преднизолон);
- нестероидные противовоспалительные средства (вольтарен);
- обезболивающие (прегабалин, карбамазепин);
- успокоительные (реланиум);
- витамины.
При дискогенной причине МРН показана мануальная терапия: новокаиновые блокады; физиотерапевтические процедуры.
Сама межреберная невралгия сегодня не вызывает трудностей при лечении. Проблемы случаются при герпетическом процессе, если противовирусная терапия не проводилась. В этом случае формируются поражение рецепторного аппарата кожи и вегетативных ганглиев, что дает каузалгические боли, для снятия которых применяют противосудорожные средства, [7] а в крайних случаях и наркотические.
Если межреберная невралгия не поддается лечению и носит стойкий характер, нужно пересмотреть ее происхождение и дополнительно обследовать пациента относительно наличия межпозвоночных грыж, опухолевых процессов и возможного оперативного вмешательства. [8]
Эпидуральная аналгезия рассматривается как золотой метод борьбы с болью после торакотомии. Криоанальгезия межреберного нерва может также приводить к удовлетворительным анальгетическим эффектам, но, как предполагается, увеличивает частоту хронической боли. [10] Если для межреберной блокады нерва применялись местные анестетики, то могут возникнуть осложнения: пневмоторакс, гемоторакс, кровохарканье, гематома, некроз тканей, респираторная недостаточность, субарахноидальный блок, аллергическая реакция на местные анестетики. [9]
Что такое невралгия тройничного нерва? Причины возникновения, диагностику и методы лечения разберем в статье доктора Новикова Юрия Олеговича, мануального терапевта со стажем в 41 год.
Над статьей доктора Новикова Юрия Олеговича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Невралгия тройничного нерва (НТН, Neuralgia n. trigemini, Prosopalgia) — хроническое заболевание, для которого характерны интенсивные боли стреляющего и/или жгучего характера в области лица, при этом расстройств чувствительности не выявляется.
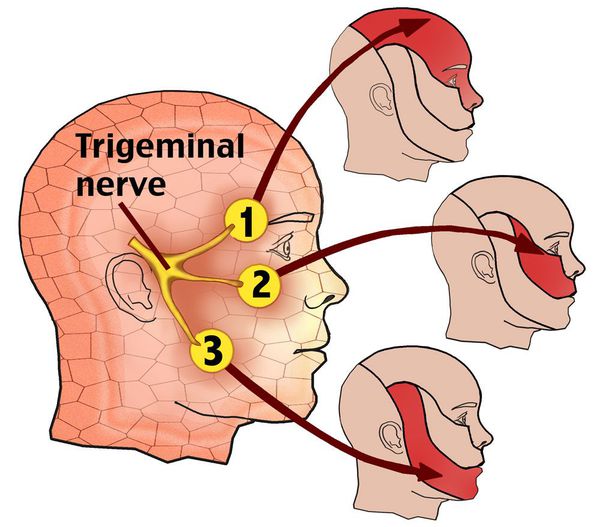
По данным Всемирной организации здравоохранения, распространённость заболевания находится в пределах 2-4 человек на 100 000 населения. Чаще встречается у женщин 50-69 лет. Преобладает правосторонняя локализация. [1] [2] Примерно в 3% случаев возможен двусторонний процесс, частота которого возрастает в ходе увеличения длительности заболевания. [3]
Причины невралгии тройничного нерва
Невралгия V нерва может быть проявлением как поражения отдельных ветвей, так и его ядер в области ствола головного мозга и продолговатого мозга.
Поражения отдельных ветвей V нерва возникают в связи с переломом черепа, менингитом или рассеянным склерозом, объёмными образованиями головного мозга, саркоидозом или аневризмами близлежащих сосудов.
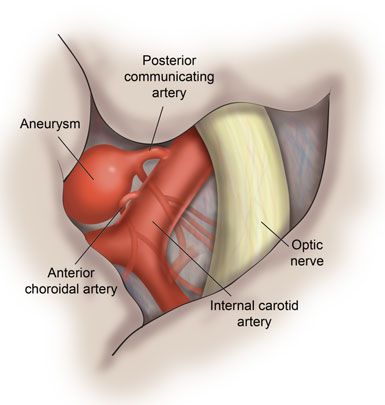
Поражение комплекса ядер также может быть связано с сосудистым процессом, объёмными образованиями, различными энцефалитами, рассеянным склерозом, сирингобульбией и сирингомиелией.
Кроме того, поражение V нерва может быть одним из признаков краниальной полиневропатии, связанной с отравлением трихлорэтиленом и другими химическими веществами, или ранним признаком некоторых заболеваний соединительной ткани, таких как склеродермия.
Некоторые проявления НТН возможны как сопутствующие признаки невропатии VII (лицевого) нерва. Это связано с единым кровоснабжением.
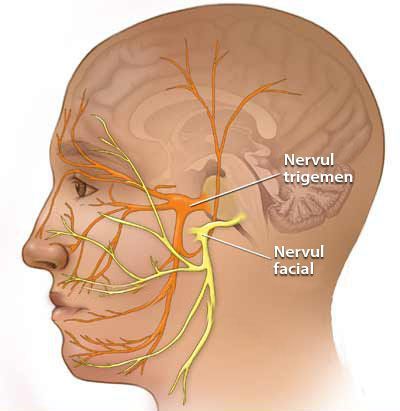
Также существует эссенциальная или идиопатическая НТН.
Факторы риска невралгии тройничного нерва
К факторам риска развития заболевания некоторые авторы относят:
- Генетический дефект в хромосоме 32Р, брахидактилию и наследственную форму гипертензии, которая передаётся от одно из родителей. Эти нарушения сочетаются с патологической извитостью или стенозом задней нижней мозжечковой или позвоночной артерий, что приводит к сдавлению переднебоковых отделов продолговатого мозга. , который снижает эластичность сосудов и увеличивает механическое воздействие пульсовой волны на корешок тройничного нерва.
- Сдавление ветвей тройничного нерва в костном канале, на месте которого повреждается оболочка, окружающая нервные волокна.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы невралгии тройничного нерва
Основной симптом невралгии тройничного нерва — это интенсивная боль в области лица. Боли при невралгии бывают двух видов:
- постоянные, тупые, периодически усиливающиеся боли без широкой иррадиации, возникающие в области распространения той или другой ветви нерва и не сопровождающиеся выраженными вегетативными реакциями;
- боли пароксизмального характера, длящиеся от нескольких минут до нескольких часов. [4][5]
Интенсивность приступов различна: от несильных, но частых, продолжающихся несколько секунд, до сильных и непереносимых, продолжающихся минутами и причиняющих сильные страдания.
Приступы нередко возникают спонтанно, без каких-либо раздражителей, либо в результате попадания твёрдой и холодной пищи в рот, прикосновений, сквозняков, переохлаждений под кондиционером, движений челюстями и т. п.
Приступ начинается обычно с болей в одной ветви нерва — месте первичного поражения, затем боль распространяется на другие ветви, нередко иррадиирует в затылок, к ушным нервам, в шею и даже в область грудных нервов.
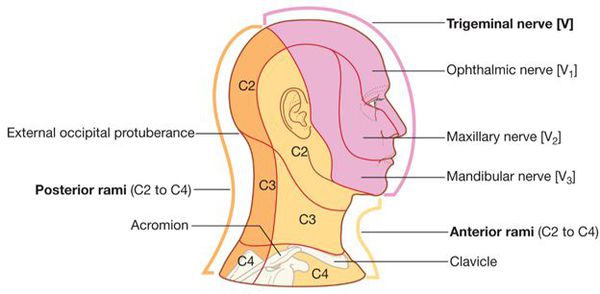
Сильные приступы обычно сопровождаются вегетативными рефлекторными реакциями: покраснением лица, слезотечением, жидкими выделениями из носа, слюнотечением, иногда отёком щеки, века, небольшим припуханием половины носа.
К симптомам воспаления тройничного нерва также относится общее беспокойство, потирание болевой зоны рукой, давление на эту зону, причмокивание. Это наслоение новых раздражений, очевидно, ускоряет момент возникновения тормозного состояния в центре болевых восприятий, которым обычно сменяется приступ.
В качестве двигательных проявлений в связи с болевым приступом возникают тикообразные подёргивания мышц или спазматические сокращения. Максимальные подёргивания или сокращения мышц соответствуют, в основном, зонам, с которых начинается боль, т. е. местам первичного поражения.
При длительном заболевании иногда отмечается поседение волос головы на поражённой стороне.
Иногда пароксизмальные невралгии сопровождаются высыпанием herpes zoster (опоясывающий герпес), располагающегося соответственно первичным поражениям тех или других ветвей, иногда поражающего слизистую роговицы.
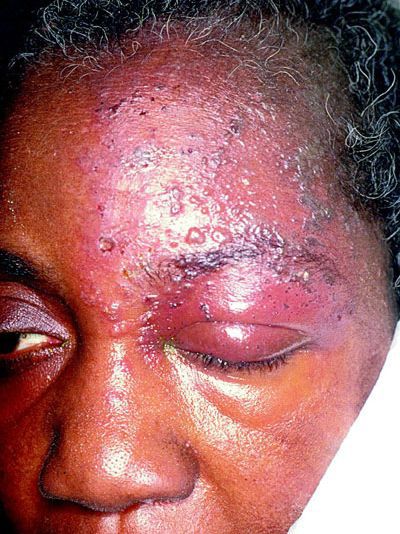
Периоды обострений могут чередоваться с периодами ремиссий, которые длятся месяцами, иногда годами.
Вне приступа обычно не наблюдается никаких расстройств: ни болевых точек, ни объективных расстройств чувствительности. Иногда можно отметить снижение болевой чувствительности главным образом в районе той ветви, которая являлась местом первичного поражения. Реже снижение чувствительности обнаруживается в области всех ветвей тройничного нерва. В отдельных случаях вне приступов больные испытывают лёгкие тупые боли. Болевые ощущения возникают в любое время, но чаще во сне. [6] [7]
Патогенез невралгии тройничного нерва
Патогенез невралгии тройничного нерва, как и локализация процесса, остаётся до конца неясным. Считается, что причиной данного страдания является сдавление корешка нерва в месте его выхода из моста изменёнными сосудами или опухолью, а причиной патологии у больных с рассеянным склерозом — образование бляшки в области чувствительного ядра тройничного нерва.
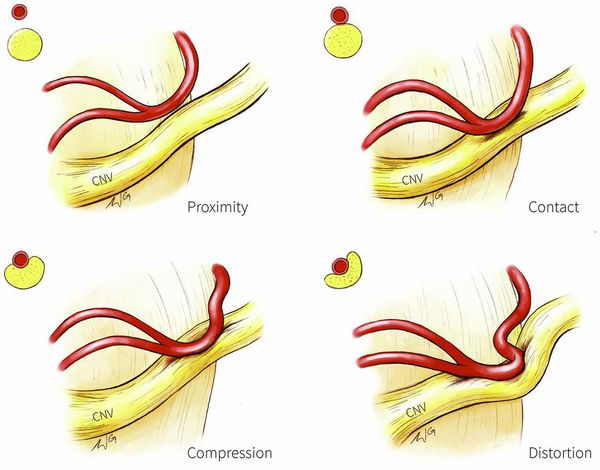
Предполагают центральную локализацию поражения на уровне понтобульбоспинальных центров, есть мнения о поражении в нисходящем корешке, связанном с ядром, или на уровне задних корешков. Имеющиеся патологоанатомические исследования, как правило, обнаруживали в гассеровых узлах изменения воспалительного или рубцового характера. Патологический очаг, изменяющий функцию узлов, влечёт за собой функциональные нарушения в расположенном выше зрительном бугре. Очаг раздражения в узле периодически под влиянием обычно внешних раздражений ведёт к возбуждению последнего с последующим возбуждением в расположенных выше центрах. Начавшись с одной точки, возбуждение затем распространяется по этим центрам. Далее сверхсильное возбуждение клеток сменяется торможением, которое распространяется в том же порядке, в каком происходила иррадиация болей. Результатом полного тормозного состояния является прекращение болей.
В этой схеме, объясняющей возникновение приступа пароксизмальной невралгии, имеется аналогия с эпилептическими припадками, только с той разницей, что реализация невралгических припадков ограничивается областью подкорки, и эти припадки никогда не ведут к последующему разлитому торможению коры головного мозга. Впрочем, это бывает иногда и при истинной парциальной эпилепсии. Если исходить из данного положения, то станет понятным, что наслаивание новых раздражений ускорит наступление тормозного состояния, т.е. конца приступа. К этим приёмам обычно и прибегают больные для купирования приступа. [8] [9]
Классификация и стадии развития невралгии тройничного нерва
Невралгия тройничного нерва бывает:
- первичной — истинной (эссенциальная или идиопатическая);
- вторичной — симптоматической:
- центральной;
- периферической (компрессионной).
Классификация по этиологическому фактору:
- травматическая НТН;
- инфекционная НТН;
- НТН в результате патологии обмена веществ в организме.
Классификация по уровню поражения:
- дентальная плексалгия;
- невралгия носоресничного нерва (синдром Чарлина);
- невралгия ушно-височного нерва (синдром Фрейя);
- синдром крылонебного узла (синдром Сладера);
- глоссофарингиальная невралгия;
- SUNCT-синдром;
- синдром поражения полулунного узла.
Классификация по нарушению функций:
- нарушение чувствительной функции тройничного нерва;
- нарушение двигательной функции тройничного нерва.
Осложнения невралгии тройничного нерва
Осложнения симптоматических вариантов НТН зависят в первую очередь от этиологии. При нейроинфекционных процессах, объёмных образованиях, аневризмах близлежащих сосудов, демиелинизирующих заболеваниях наиболее вероятны осложнения от основных заболеваний, вплоть до инвалидизации и летального исхода.
В случае идиопатической НТН чаще всего наблюдается переход в хроническую стадию: болезнь носит длительный характер, тянется непрерывно или с интервалами различной продолжительности, почти не поддаваясь окончательному излечению. Однако в некоторых случаях отмечают длительную ремиссию до 5-7 лет, но затем боли возобновляются. В периоды ремиссий типично щадящее поведение пациентов с НТН — они предпочитают жевать одной половиной рта, даже в тёплую погоду укрывают голову.
В начальных стадиях болезни, когда её причина установлена, соответствующее лечение может быстро ликвидировать воспалительный процесс без остаточных явлений в виде образования рубцов. Если рубцы образуются, рецидив болезни почти неизбежен — она приобретает хроническое течение.
В случае длительно протекающих невралгий нередки признаки нарушения трофики (питания) тканей в зоне иннервации нервного корешка, таких как сальность и истончение кожи. В случае НТН I ветви вероятны выпадение ресниц и бровей, вплоть до трофических язв роговицы. Кроме того в зоне иннервации снижается тактильная и/или температурная чувствительность.
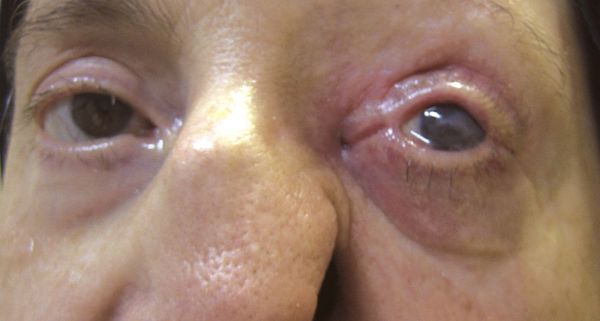
Хронические лицевые боли, обусловленные НТН, приводят к снижению порога болевой чувствительности и могут быть «маской» скрытой депрессии. И наоборот, при длительно существующей хронической боли присоединяется депрессия, вследствие общности патогенетических механизмов. [11]
Диагностика невралгии тройничного нерва
Когда следует обратиться к врачу
При НТН посетить доктора нужно как можно раньше, так как в некоторых случаях боль может быть вызвана новообразованием, инфекцией или демиелинизирующим заболеванием.
Подготовка к посещению врача
Особая подготовка не требуется. Если у пациента есть результаты нейровизуализации, то снимки стоит взять с собой.
Инструментальная диагностика
В первую очередь при подозрении на НТН необходимо выполнить магнитную томографию или компьютерную томография головы с целью исключения серьёзной патологии.
Важно дифференцировать НТН с сирингомиелией и сирингобульбией, иногда начинающихся болями в области тройничного нерва, которые могут приобрести пароксизмальный характер. Наличие характерных для сирингомиелии симптомов и дефектов физического развития позволяют установить правильный диагноз.
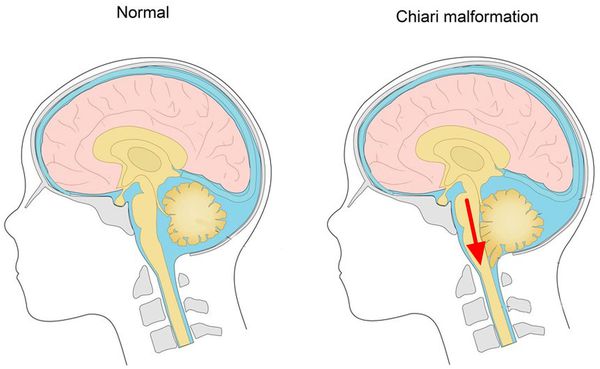
Иррадиирующие боли при заболеваниях придаточных полостей носа, зубов сравнительно легко дифференцируются от невралгии. Боли тупые, не носят пароксизмальный характер, исчезают бесследно после излечения вызвавших их заболеваний. Если после излечения боли не проходят, следует думать о невралгии. Смешение невралгии с болями, иррадиирующими из зубов, нередко ведёт к ошибочному диагнозу и удалению здоровых зубов.
Боли в районе первых ветвей тройничных нервов, наблюдаемые при тиреотоксикозах, необходимо относить к токсическим невралгиям. Они всегда двусторонние, часто сочетаются с затылочными болями, носят упорный характер. Специальное лечение обычно снимает эти боли.
Дифференциальная диагностика
Инфекционные невралгии тройничного нерва приходится дифференцировать с невралгиями неинфекционной этиологии. В пожилом возрасте такие невралгии могут быть обусловлены склеротическими изменениями отверстий, через которые проходят ветви тройничного нерва, с кровоизлияниями в нерв или гассеров узел.
Этиологический диагноз приходится ставить только на основании анамнестических данных. Клинические признаки могут быть сходны только при склеротическом поражении одной ветви, пароксизмы не так сильны и не приобретают широкой иррадиации. Невралгии, возникшие в результате оболочечных воспалительных процессов и неопластических процессов в области гассерова узла и корешков, тройничного нерва, кариозных заболеваний пирамидки распознаются сравнительно легко. При всех этих заболеваниях обычно в процесс вовлекаются другие черепные нервы: слуховой, лицевой, отводящий. [12] [13]
Лечение невралгии тройничного нерва
Медикаментозное лечение
Медикаментозное лечение включает в себя приём антиконвульсантов. Лучше всего зарекомендовал себя карбамазепин («Тегретол», «Финлепсин»), который назначают по схеме, начиная со 100 мг, постепенно увеличивая дозу до 600-800 мг в зависимости от переносимости и наличия нежелательных явлений. Приём обычно длится 1-2 недели, далее, при улучшении состояния, отменяется, постепенно снижая дозировку.
Препаратами второго ряда являются баклофен, тизанидин и антидепрессанты, которые вначале назначаются в условиях стационара, а затем применяются в амбулаторных условиях с постепенной отменой при достижении улучшения.
Также дополнительно применяют витамины группы B и сосудистые препараты.
Используют блокады анестетиками в местах выходов соответствующих ветвей тройничного нерва, акупунктуру и остеопатические методы коррекции.
Физиотерапия
Из физиотерапевтических методов в остром периоде заболевания и во время приступа местно используют умеренное тепловое и/или ультрафиолетовое воздействие. Широко применяют курсовое воздействие диадинамическими токами, которые оказывают обезболивающее и противовоспалительное воздействие. В упорных случаях возможно использование анальгетиков типа прокаин, тетракаин, эпинефрин.
В подостром периоде положительно зарекомендовал себя эндоназальный электрофорез 4% раствора прокаина и 2% раствор витамина В1.
В случае хронических форм НТН показан массаж лица, грязевые или парафин-озокеритовые аппликации на воротниковую область.
Многообещающие перспективы сосредоточены на использовании ботулинического токсина. [18]
Хирургическое лечение
При неэффективности консервативной терапии показаны нейрохирургические методы лечения:
- невротомию или нервэктомию (перерезание или удаление нерва);
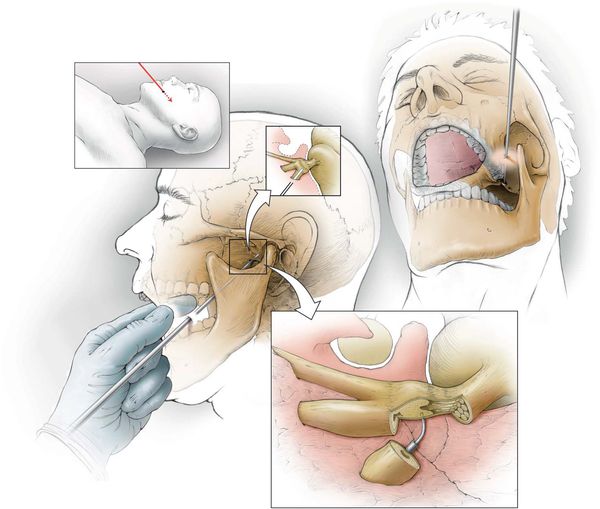
- клипирование аневризматически расширенных артерий — на мешотчатое расширение артерии накладывается металлическая скобка, прекращающая кровоток в этом расширении;
- ликвидация сдавления нерва в костных каналах внутри черепа — частично удаляются костные стенки канала;
- термическая коагуляция узла тройничного нерва;
- операции на гассеровом узле и чувствительном корешке тройничного нерва — электрокоагуляция, криодеструкция. [14][15][16][17]
Дополнительные методы лечения
Также используются когнитивно-поведенческая терапия, физические упражнения, релаксация, биологическая обратная связь, окклюзионные шины и трейнеры, массаж и многое другое как дополнительные методы помощи при хронических лицевых болях. [19]
Как снять боль при невралгии тройничного нерва
Самолечение при невралгии тройничного нерва может навредить пациенту. Уменьшить и предотвратить вероятность новых приступов можно, если своевременно лечить воспалительные и инфекционные заболевания, уменьшить психоэмоциональное перенапряжение, соблюдать режим труда и отдыха, не злоупотреблять алкоголем, острыми и горячими блюдами.
Прогноз. Профилактика
Прогноз эффективности лечения и длительности ремиссии зависит от степени нарушения тройничного нерва, своевременности начатого лечения, а также возраста пациента. Бесспорно, наилучший прогноз восстановительного лечения НТН можно ожидать при вторичных симптоматических проявлениях, когда причина не вызывает сомнения и хорошо поддаётся соответствующей терапии (например, одонтогенная или инфекционная НТН). При идиопатических НТН, этиология которых не ясна, курация наиболее затруднительна.
Профилактика прозопалгий имеет большое значение вследствие малых надежд на полное излечение хронических форм невралгий, поэтому профилактические мероприятия, в основном, сводятся к своевременному лечению заболеваний, которые могут провоцировать развитие НТН. Особое внимание необходимо уделить санации зубов, лечению ринитов и гайморита.
Важным условием профилактики является отсутствие переохлаждений и сквозняков. Необходимо избегать психотравмирующих факторов, закаляться. Немаловажная роль в профилактике принадлежит саногенезу, так как любое интеркуррентное заболевание как инфекционного, так и соматического плана, приводящее к ослаблению защитных сил организма, может привести к обострению НТН. [20] [21]
Читайте также:

