Можно применять полиоксидоний при фурункулезе
Обновлено: 21.05.2024
маннитол – 3,6 мг, повидон К 17 – 2,4 мг, масло какао – 1282,0 мг (для дозировки 12 мг).
Описание:
суппозитории торпедообразной формы, светло-желтого цвета со слабым специфическим запахом масла какао.
Суппозитории должны быть однородны. На срезе допускается наличие воздушного стержня или воронкообразного углубления.
Фармакотерапевтическая группа:
Код АТХ: [L0З]
Фармакологические свойства
Фармакодинамика
Азоксимера бромид обладает комплексным действием: иммуномодулирующим, детоксицирующим, антиоксидантным, умеренным противовоспалительным.
Основой механизма иммуномодулирующего действия Азоксимера бромида является прямое воздействие на фагоцитирующие клетки и естественные киллеры, а также стимуляция антителообразования и синтеза интерферона-альфа и интерферона-гамма.
Детоксикационные и антиоксидантные свойства Азоксимера бромида во многом определяются структурой и высокомолекулярной природой препарата.
Азоксимера бромид увеличивает резистентность организма в отношении локальных и генерализованных инфекций бактериальной, грибковой и вирусной этиологии. Восстанавливает иммунитет при вторичных иммунодефицитных состояниях, вызванных различными инфекциями, травмами, осложнениями после хирургических операций, ожогами, аутоиммунными заболеваниями, злокачественными новообразованиями, применением химиотерапевтических средств, цитостатиков, стероидных гормонов.
Азоксимера бромид блокирует растворимые токсические вещества и микрочастицы, обладает способностью выводить из организма токсины, соли тяжелых металлов, ингибирует перекисное окисление липидов как за счет перехвата свободных радикалов, так и посредством элиминации каталитически активных ионов Fe2 + . Азоксимера бромид снижает воспалительную реакцию посредством нормализации синтеза про- и противовоспалительных цитокинов.
Азоксимера бромид хорошо переносится, не обладает митогенной, поликлональной активностью, антигенными свойствами, не оказывает аллергизирующего, мутагенного, эмбриотоксического, тератогенного и канцерогенного действия.
Фармакокинетика
Азоксимера бромид в суппозиториях при ректальном введении обладает высокой биодоступностью (не менее 70 %), достигая максимальной концентрации в крови через
1 час после введения. Период полураспределения – около 0,5 часа, период полуэлиминации – 36,2 часа. В организме гидролизуется до олигомеров, которые выводятся преимущественно почками. Кумулятивный эффект отсутствует.
Показания к применению
Применяется у взрослых и детей старше 6 лет для лечения и профилактики инфекционно-воспалительных заболеваний (вирусной, бактериальной и грибковой этиологии), в стадии обострения и ремиссии.
Для лечения (в комплексной терапии):
· острых и обострения хронических рецидивирующих инфекционно-воспалительных заболеваний различной локализации, бактериальной, вирусной и грибковой этиологии;
· воспалительных заболеваний урогенитального тракта (уретрита, цистита, пиелонефрита, простатита, сальпингоофорита, эндомиометрита, кольпита, цервицита, цервикоза, бактериальных вагинозов);
· различных форм туберкулеза легких;
· аллергических заболеваний (в том числе поллиноза, бронхиальной астмы, атопического дерматита), осложненных рецидивирующей бактериальной, грибковой и вирусной инфекцией;
· ревматоидного артрита, осложненного рецидивирующей бактериальной, грибковой и вирусной инфекцией, на фоне длительного приема иммунодепрессантов;
· для активации регенераторных процессов (переломы, ожоги, трофические язвы);
· в комплексной терапии онкологических заболеваний при проведении химио- и лучевой терапии, для снижения нефро - и гепатотоксического действия лекарственных препаратов.
Для профилактики (монотерапия):
- рецидивирующей герпетической инфекции урогенитального тракта;
· обострений хронических очагов инфекций;
· гриппа и других острых респираторных инфекций в предэпидемический и эпидемический период у иммунокомпрометированных лиц;
· вторичных иммунодефицитов, возникающих вследствие старения или воздействия неблагоприятных факторов.
Противопоказания
· повышенная индивидуальная чувствительность;
· беременность, период грудного вскармливания;
· детский возраст до 6 лет;
С осторожностью
Если у Вас есть заболевания, указанные в данном разделе, обратитесь к врачу перед началом приема лекарственного препарата:
· хроническая почечная недостаточность (назначают не чаще, чем 2 раза в неделю).
Применение при беременности и в период грудного вскармливания
Противопоказано применение при беременности и в период грудного вскармливания (клинический опыт применения отсутствует).
При экспериментальном применении препарата Полиоксидоний ® у животных не выявлено эмбриотоксического и тератогенного действия, влияния на развитие плода.
Перед применением препарата Полиоксидоний ® ,если Вы беременны, или предполагаете, что Вы могли быть беременной, или планируете беременность, необходимо проконсультироваться с врачом.
В период грудного вскармливания перед применением препарата Полиоксидоний ® необходимо проконсультироваться с врачом.
Способ применения и дозы
Применяйте препарат только согласно тем показаниям, тому способу применения и в тех дозах, которые указаны в инструкции.
Если после лечения улучшения не наступает или симптомы усугубляются, или появляются новые симптомы, необходимо проконсультироваться с врачом.
Ректально и вагинально 1 раз в сутки ежедневно, через день или 2 раза в неделю.
При необходимости возможно проведение повторных курсов терапии через 3-4 месяца. При повторном назначении препарата эффективность его не снижается.
Рекомендуемые схемы применения препарата
Для лечения взрослым:
– ректально по 1 суппозиторию 1 раз в сутки после очищения кишечника;
– вагинально при гинекологических заболеваниях по 1 суппозиторию 1 раз в сутки (на ночь) вводится во влагалище в положении лежа.
- при хронических инфекционно-воспалительных заболеваниях в стадии обострения – суппозитории 12 мг 1 раз в сутки ежедневно в течение 3-х дней, затем через день. Курс лечения – 10 суппозиториев;
- при острых инфекционных процессах и для активации регенераторных процессов (переломы, ожоги, трофические язвы) – суппозитории 12 мг 1 раз в сутки ежедневно. Курс лечения – 10 суппозиториев;
- при гинекологических заболеваниях – суппозитории 12 мг 1 раз в сутки ежедневно в течение 3-х дней, затем через день. Курс лечения 10 суппозиториев;
- при обострении урологических заболеваний (уретрит, пиелонефрит, цистит, простатит) – суппозитории 12 мг 1 раз в сутки ежедневно. Курс лечения –
10 суппозиториев; - при легочной форме туберкулеза – суппозитории 12 мг 1 раз в сутки ежедневно в течение 3-х дней, затем через день. Курс лечения 20 суппозиториев. Далее возможно использование поддерживающей терапии суппозиториями 6 мг 2 раза в неделю, курсом до 2-3 месяцев;
- в комплексной терапии онкологических заболеваний при проведении химио- и лучевой терапии – суппозитории 12 мг ежедневно за 2-3 дня до начала курса химио- или лучевой терапии. Далее по 12 мг 2 раза в неделю, курсом до
20 суппозиториев; - при аллергических заболеваниях, осложненных инфекционным синдромом, – суппозитории 12 мг 1 раз в сутки ежедневно. Курс лечения – 10 суппозиториев;
- при ревматоидном артрите – суппозитории 12 мг через день. Курс лечения –
10 суппозиториев.
Для профилактики (монотерапия):
- обострений хронических очагов инфекций, рецидивирующей герпетической инфекции урогенитального тракта – суппозитории 12 мг через день.
Курс – 10 суппозиториев; - гриппа и ОРВИ – суппозитории 12 мг 1 раз в сутки. Курс – 10 суппозиториев;
- вторичных иммунодефицитов, возникающих вследствие старения – суппозитории 12 мг 2 раза в неделю. Курс – 10 суппозиториев, 2-3 раза в год.
Для лечения детям и подросткам от 6 до 18 лет:
Детям и подросткам от 6 до 18 лет суппозитории вводятся только ректально,
по 1 суппозиторию 6 мг 1 раз в сутки после очищения кишечника.
- при хронических инфекционно-воспалительных заболеваниях в стадии обострения – суппозитории 6 мг 1 раз в сутки ежедневно в течение 3-х дней, затем через день. Курс лечения – 10 суппозиториев;
- при острых инфекционных процессах и для активации регенераторных процессов (переломы, ожоги, трофические язвы) – суппозитории 6 мг 1 раз в сутки ежедневно. Курс лечения – 10 суппозиториев;
- при обострении урологических заболеваний (уретрит, пиелонефрит, цистит, простатит) – суппозитории 6 мг 1 раз в сутки ежедневно. Курс лечения –
10 суппозиториев; - при легочной форме туберкулеза – суппозитории 6 мг 1 раз в сутки ежедневно в течение 3-х дней, затем через день. Курс лечения 20 суппозиториев. Далее возможно использование поддерживающей терапии суппозитории 6 мг 2 раза в неделю, курсом до 2-3 месяцев;
- в комплексной терапии онкологических заболеваний при проведении химио- и лучевой терапии – суппозитории 6 мг ежедневно за 2-3 дня до начала курса химио- или лучевой терапии. Далее по 6 мг 2 раза в неделю, курсом до 20 суппозиториев;
- при аллергических заболеваниях, осложненных инфекционным синдромом, – суппозитории 6 мг 1 раз в сутки ежедневно. Курс лечения – 10 суппозиториев;
- при ревматоидном артрите – суппозитории 6 мг через день. Курс лечения –
10 суппозиториев.
Для профилактики (монотерапия):
· обострений хронических очагов инфекций, рецидивирующей герпетической инфекции урогенитального тракта – суппозитории 6 мг через день.
Курс – 10 суппозиториев;
· гриппа и ОРВИ – суппозитории 6 мг 1 раз в сутки, Курс 10 суппозиториев.
Для больных, длительно получающих иммуносупрессивную терапию, онкологических, подвергшихся облучению, имеющих приобретенный дефект иммунной системы – ВИЧ, показана длительная от 2-3 месяцев до 1 года поддерживающая терапия Полиоксидонием (взрослым по 12 мг, детям старше 6 лет – по 6 мг 1-2 раза в неделю).
Побочное действие
Очень редко: местные реакции в виде покраснения, отека, зуда перианальной зоны, вагинального зуда в связи с индивидуальной чувствительностью к компонентам препарата.
Если Вы заметили какие либо побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Передозировка
Взаимодействие с другими лекарственными средствами
Азоксимера бромид не ингибирует изоферменты CYP1A2, CYP2С9, CYP2С19, CYP2D6, цитохрома Р-450, поэтому препарат совместим со многими лекарственными средствами, в том числе с антибиотиками, противовирусными, противогрибковыми и антигистаминными препаратами, глюкокортикостероидами и цитостатиками.
Если Вы принимаете вышеперечисленные или другие лекарственные препараты (в том числе безрецептурные), перед началом приема Полиоксидония проконсультируйтесь с врачом.
Особые указания
При развитии аллергической реакции следует прекратить применение препарата Полиоксидоний ® и обратиться к врачу.
При необходимости прекращения терапии препаратом, отмену можно проводить сразу. В случае пропуска разовой дозы препарата необходимо принять его как можно раньше, но если наступило время приема следующей дозы, дозу на прием не увеличивать.
Не используйте препарат при наличии визуальных признаков его непригодности (дефект упаковки, изменение цвета суппозитория).
Влияние на способность управлять транспортными средствами и механизмами
Применение препарата Полиоксидоний ® не влияет на способность управления транспортными средствами, обслуживание механизмов и другие виды работ, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Суппозитории вагинальные и ректальные, 6 мг, 12 мг.
По 5 суппозиториев в контурную ячейковую упаковку из пленки поливинилхлоридной. Две контурные упаковки вместе с инструкцией по применению помещают в пачку из картона.
Срок годности
2 года. Не следует применять препарат после истечения срока годности.
Условия хранения
В сухом месте, при температуре от 2 до15 о С.
Хранить в недоступном для детей месте.
Условия отпуска
Производитель / Юридическое лицо, на имя которого выдано регистрационного удостоверение
Владелец регистрационного удостоверения и производитель:
ООО «НПО Петровакс Фарм»
Юридический адрес / Адрес для предъявления претензий потребителей:
Производство / Фасовка (первичная упаковка):
Российская Федерация, 115598, г. Москва, ул. Загорьевская, д. 10, корп. 4,
тел./факс: (495) 329-17-18.
Вторичная (потребительская) упаковка / Выпускающий контроль качества:
Российская Федерация, 142143, Московская область, Подольский район, с. Покров,
ул. Сосновая, д. 1, тел./факс: (495) 926-21-07.
Полиоксидоний суппозитории - цена, наличие в аптеках
Указана цена, по которой можно купить Полиоксидоний суппозитории в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
В настоящее время существует тенденция к росту хронических бактериальных и вирусных заболеваний, для которых характерны непрерывно рецидивирующее течение и малая эффективность антибактериальной и симптоматической терапии. Одним из таких заболеваний яв
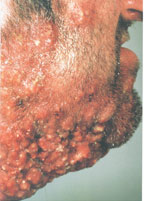
В настоящее время существует тенденция к росту хронических бактериальных и вирусных заболеваний, для которых характерны непрерывно рецидивирующее течение и малая эффективность антибактериальной и симптоматической терапии. Одним из таких заболеваний является хронический рецидивирующий фурункулез (ХРФ). Фурункул развивается в результате острого гнойно-некротического воспаления волосяного фолликула и окружающих его тканей. Как правило, фурункул является осложнением остеофолликулита стафилококковой этиологии. Фурункулы могут возникать как одиночно, так и множественно (так называемый фурункулез).
В случае рецидивирования фурункулеза диагностируется хронический рецидивирующий фурункулез. Как правило, он характеризуется частыми рецидивами, длительными, вялотекущими обострениями, толерантными к проводимой антибактериальной терапии. В зависимости от количества фурункулов, распространенности и выраженности воспалительного процесса ХРФ классифицируется по степени тяжести (Л. Н. Савицкая, 1987).
Тяжелая степень: диссеминированные, множественные, непрерывно рецидивирующие небольшие очаги со слабой местной воспалительной реакцией, не пальпируемыми или слегка определяющимися регионарными лимфатическими узлами. Тяжелое течение фурункулеза сопровождается симптомами общей интоксикации: слабостью, головной болью, снижением работоспособности, повышением температуры тела, потливостью.
Средняя степень тяжести — одиночные или множественные фурункулы больших размеров, протекающие с бурной воспалительной реакцией, с рецидивами от 1 до 3 раз в год. Иногда сопровождается увеличением регионарных лимфатических узлов, лимфангоитом, кратковременным повышением температуры тела и незначительными признаками интоксикации.
Легкая степень тяжести — одиночные фурункулы, сопровождающиеся умеренной воспалительной реакцией, с рецидивами от 1 до 2 раз в год, хорошо пальпируемыми регионарными лимфатическими узлами, без явлений интоксикации.
Чаще всего пациенты, страдающие фурункулезом, получают лечение у хирургов, в лучшем случае на амбулаторном этапе им проводится исследование крови на сахар, аутогемотерапия, некоторым назначают и иммуномодулирующие препараты без предварительно проведенного обследования, и в большинстве случаев они не получают положительного результата от проведенной терапии. Цель нашей статьи — поделиться опытом ведения больных с ХРФ.
Основным этиологическим фактором ХРФ считается золотистый стафилококк, который встречается, по разным данным, в 60–97% случаев. Реже ХРФ вызывается другими микроорганизмами — эпидермальным стафилококком (ранее считавшимся апатогенным), стрептококками групп А и В и другими видами бактерий. Описана вспышка заболеваемости фурункулезом нижних конечностей у 110 пациентов, являвшихся пациентами одного и того же педикюрного салона. Возбудителем данной вспышки являлся Mycobacterium fortuitium, причем этот микроорганизм был выявлен в ванночках для ног, используемых в салоне. В большинстве случаев ХРФ из гнойных очагов высеваются антибиотикорезистентные штаммы золотистого стафилококка. По данным Н. М. Калининой, St. aureus в 89,5% случаев резистентен к пенициллину и ампициллину, в 18,7% — резистентен к эритромицину и в 93% случаев чувствителен к клоксациллину, цефалексину и котримоксазолу. В последние годы отмечается достаточно широкое распространение метициллин-резистентных штаммов этого микроорганизма (до 25% пациентов). По данным зарубежной литературы, наличие на коже или на слизистой оболочке носа патогенного штамма St. aureus считается важным фактором развития заболевания.
ХРФ имеет сложный и до сих пор недостаточно изученный патогенез. Установлено, что дебют и дальнейшее рецидивирование заболевания обусловлены целым рядом эндо- и экзогенных факторов, среди которых наиболее значимыми считаются нарушение барьерной функции кожных покровов, патология ЖКТ, эндокринной и мочевыделительной систем, наличие очагов хронической инфекции различной локализации. По данным проведенных нами исследований, очаги хронической инфекции различной локализации выявляются у 75–99,7% пациентов, страдающих ХРФ. Наиболее часто встречаются очаги хронической инфекции ЛОР-органов (хронический тонзиллит, хронический гайморит, хронический фарингит), дисбактериоз кишечника с увеличением содержания кокковых форм. У больных хроническим фурункулезом патология ЖКТ (хронический гастродуоденит, эрозивный бульбит, хронический холецистит) определяется в 48–91,7% случаев. У 39,7% пациентов диагностируется патология эндокринной системы, представленная нарушениями обмена углеводов, гормонпродуцирующей функции щитовидной и половых желез. У 39,2% больных с упорно текущим фурункулезом имеется латентная сенсибилизация, у 4,2% — клинические проявления сенсибилизации к аллергенам домашней пыли, пыльцы деревьев и злаковых трав, у 11,1% — повышенная концентрация сывороточного IgE.
Таким образом, для большинства больных ХРФ характерны непрерывно рецидивирующее течение заболевания (41,3%) при тяжелой и средней тяжести течения фурункулеза (88%) и длительные обострения (от 14 до 21 дня — 39,3%). У 99,7% пациентов выявлены хронические очаги инфекции различной локализации. В 39,2% случаев определялась латентная сенсибилизация к различным аллергенам. Основным возбудителем является St. aureus.
В возникновении и развитии хронического фурункулеза, наряду с особенностями возбудителя, его патогенными, вирулентными и инвазивными свойствами, наличием сопутствующей патологии, большая роль отводится нарушениям нормального функционирования и взаимодействия различных звеньев иммунной системы. Иммунная система, призванная обеспечить биологическую индивидуальность организма и, как следствие, выполняющая защитную функцию при контакте с инфекционными, генетически чужеродными агентами, в силу разных причин может давать сбой, что ведет к нарушению защиты организма от микробов и проявляется в повышенной инфекционной заболеваемости.
Иммунная защита от бактерий-патогенов включает два взаимосвязанных компонента — врожденный (носящий преимущественно неспецифический характер) и адаптивный (характеризующийся высокой специфичностью к чужеродным антигенам) иммунитет. Возбудитель ХРФ при попадании в кожу вызывает «каскад» защитных реакций.
У 26–35% больных, страдающих хроническим фурункулезом, снижается количество В-лимфоцитов. При оценке компонентов гуморального иммунитета у больных фурункулезом выявляются различные дисиммуноглобулинемии. Наиболее часто встречаются снижение уровней IgG и IgM. Отмечено снижение аффинности иммуноглобулинов у больных ХРФ, причем выявлена корреляция между частотой встречаемости этого дефекта, стадией и тяжестью заболевания. Тяжесть нарушений лабораторных показателей коррелирует с тяжестью клинических проявлений фурункулеза.
Из вышесказанного следует, что изменения показателей иммунного статуса у больных ХРФ носят разноплановый характер: у 42,9% отмечено изменение субпопуляционного состава лимфоцитов, у 71,1% — фагоцитарного и у 59,5% — гуморального звена иммунной системы. В зависимости от выраженности изменений в показателях иммунного статуса больных ХРФ можно разделить на три группы: легкой тяжести, средней и тяжелого течения, что коррелирует с клиническим течением заболевания. При легком течении фурункулеза у большинства больных (70%) показатели иммунного статуса находятся в пределах нормы. При средней и тяжелой степени преимущественно выявляются изменения фагоцитарного и гуморального звеньев иммунной системы.
Диагностика и лечение ХРФ
Исходя из вышеуказанных патогенетических особенностей ХРФ алгоритм диагностики должен включать в себя выявление очагов хронической инфекции, диагностику сопутствующих заболеваний, оценку лабораторных параметров состояния иммунной системы (рис.).
В нашем институте был разработан план обследования больных ХРФ.
- Обязательное лабораторное исследование:
- клинический анализ крови;
- общий анализ мочи;
- биохимический анализ крови (общий белок, белковые фракции, общий билирубин, мочевина, креатинин, трансаминазы - АСТ, АЛТ);
- RW, ВИЧ;
- анализ крови на наличие гепатита В и С;
- посев содержимого фурункула на флору и чувствительность к антибиотикам;
- гликемический профиль;
- иммунологическое обследование (фагоцитарный индекс, спонтанная и индуцированная хемилюминесценция (ХЛ), индекс стимуляции (ИС) люминолзависимой хемилюминесценции ЛЗХЛ), бактерицидность нейтрофилов, иммуноглобулины A, M, G, аффинность иммуноглобулинов);
- бактериологическое исследование фекалий;
- анализ кала на яйца глистов;
- посев из зева на флору и грибы.
- Дополнительное лабораторное исследование:
- определение уровня гормонов щитовидной железы (Т3,Т4, ТТГ, АТ к ТГ);
- определение уровня половых гормонов (эстрадиол, пролактин, прогестерон);
- посев крови на стерильность трехкратно;
- посев мочи (по показаниям);
- посев желчи (по показаниям);
- определение базальной секреции;
- иммунологическое обследование (субпопуляции Т-лимфоцитов, В-лимфоциты);
- общий IgE.
- Инструментальные методы обследования:
- гастроскопия с определением базальной секреции;
- УЗИ органов брюшной полости;
- УЗИ щитовидной железы (по показаниям);
- УЗИ женских половых органов (по показаниям);
- дуоденальное зондирование;
- функции внешнего дыхания;
- ЭКГ;
- рентгенография органов грудной клетки;
- рентгенография придаточных пазух носа.
- Консультации специалистов: отоларинголога, гинеколога, эндокринолога, хирурга, уролога.
Тактика лечения больных ХРФ определяется стадией заболевания, сопутствующей патологией и иммунологическими нарушениями. В стадии обострения ХРФ требуется проведение местной терапии в виде обработки фурункулов антисептическими растворами, антибактериальными мазями, гипертоническим раствором; в случае локализации фурункулов в области головы и шеи или наличия множественных фурункулов — проведение антибактериальной терапии с учетом чувствительности возбудителя. В любой стадии заболевания необходима коррекция выявленной патологии (санация очагов хронической инфекции, лечение патологии ЖКТ, эндокринной патологии и т. д.). При выявлении у больных ХРФ латентной сенсибилизации или при наличии клинических проявлений аллергии необходимо в период поллинации добавлять к лечению антигистаминные препараты, назначать гипоаллергенную диету, проводить хирургическое вмешательство с премедикацией гормональными и антигистаминными препаратами.
В последнее время в комплексной терапии больных ХРФ все чаще используют препараты, оказывающие корригирующее действие на иммунную систему.
Разработаны показания к назначению иммуномодуляторов в зависимости от доминирующего типа нарушений иммунного статуса и степени заболевания. Так, в стадии обострения ХРФ рекомендовано применение следующих иммуномодуляторов.
- При наличии изменений фагоцитарного звена иммунитета целесообразно назначение полиоксидония по 6-12 мг внутримышечно в течение 6-12 дней.
- При снижении аффинности иммуноглобулинов - галавит 100 мг № 15 внутримышечно.
- При снижении уровня В-лимфоцитов, нарушении соотношения CD4/CD8 в сторону уменьшения показано применение миелопида по 3 мг в течение 5 дней внутримышечно.
- При снижении уровня IgG на фоне тяжелого обострения ХРФ при клинической неэффективности применения галавита используются препараты иммуноглобулина для внутривенного введения (октагам, габриглобин, интраглобин).
В период ремиссии возможно назначение следующих иммуномодуляторов.
- Полиоксидоний 6-12 мг внутримышечно в течение 6-12 дней - при наличии изменений фагоцитарного звена иммунитета.
- Ликопид 10 мг в течение 10 дней перорально - при наличии дефектов образования активных форм кислорода.
- Галавит 100 мг № 15 внутримышечно - при снижении аффинности иммуноглобулинов.
Применение ликопида целесообразно также при вялотекущем, непрерывно рецидивирующем фурункулезе. При упорном рецидивировании ХРФ на фоне изменений гуморального звена иммунитета показано назначение препаратов иммуноглобулина для внутривенного введения (октагам, габриглобин, интраглобин). В некоторых случаях целесообразно комбинированное применение иммуномодулирующих препаратов (например, при обострении фурункулеза возможно назначение полиоксидония, в дальнейшем, при выявлении дефекта аффинности иммуноглобулинов, добавляется галавит и т. д.).
Несмотря на значительные успехи, достигнутые в области клинической иммунологии, эффективное лечение ХРФ остается достаточно сложной задачей. В связи с этим требуется дальнейшее изучение патогенетических особенностей этого заболевания, а также разработка новых подходов к терапии ХРФ.
Неоген является синтетическим трипептидом, состоящим из L-аминокислотных остатков изолецитина, глютамина и триптофана. Неоген применялся в составе комплексной терапии, проводимой больным хроническим фурункулезом. Внутримышечные инъекции препарата неогена проводились по 1 мл 0,01% раствора 1 раз в сутки ежедневно, курс — 10 инъекций. Применение неогена в комплексной терапии больных хроническим фурункулезом на стадии ремиссии заболевания вызывает достоверную нормализацию изначально измененных иммунологических показателей (относительного и абсолютного количества лимфоцитов, относительного количества CD3 + , CD8 + , CD19 + , CD16 + -лимфоцитов, поглотительной способности моноцитов по отношению к St. aureus) и увеличение показателей спонтанной ХЛ и аффинности анти-ОАД-антител, количества HLA-DR+-лимфоцитов, а следовательно, позволяет продлить период ремиссии заболевания по сравнению с группой контроля.
Таким образом, из вышеизложенного следует, что ХРФ протекает под воздействием сложного комплекса этиологических и патогенетических факторов и его нельзя рассматривать только как местное воспаление. Больным с ХРФ необходимо проводить всестороннее обследование с целью выявления возможных очагов хронической инфекции, которые являются источником септицемии и при нарушении элиминации микробов в крови в результате снижения иммунологической реактивности организма приводят к возникновению фурункулов. Так как назначение иммунокорригирующих препаратов может вызвать обострение основного заболевания, мы считаем, что лечение больных необходимо начинать с санации выявленных очагов инфекции.
Вопрос о назначении иммунокорригирующих препаратов должен решаться индивидуально, с учетом стадии заболевания, наличия сопутствующей патологии и типа иммунологического дефекта. При выявлении у больного сенсибилизации к различным аллергенам лечение фурункулеза необходимо проводить на фоне противоаллергенной терапии.
Н. Х. Сетдикова, доктор медицинских наук
К. С. Манько
Т. В. Латышева, доктор медицинских наук, профессор
Так как элиминация любого инфекционного возбудителя является результатом синергического взаимодействия между защитными силами макроорганизма и антимикробными агентами, то лечение антибиотиками, противовирусными и противогрибковыми средствами будет малоэфф
Так как элиминация любого инфекционного возбудителя является результатом синергического взаимодействия между защитными силами макроорганизма и антимикробными агентами, то лечение антибиотиками, противовирусными и противогрибковыми средствами будет малоэффективным у лиц с исходно пониженной функциональной активностью иммунной системы. Поэтому оправдан поиск препаратов, стимулирующих иммунологическую реактивность и тем самым повышающих эффективность антимикробной терапии. Речь идет об иммуномодуляторах — лекарственных препаратах с иммунотропным действием, усиливающих эффективную иммунную защиту [9, 10, 13].
При вялотекущих, рецидивирующих, плохо поддающихся химиотерапии, имеющих тенденцию к хронизации заболеваниях целесообразно включение в комплексную терапию иммуномодулятора. Отечественный препарат последнего поколения — полиоксидоний — является иммуномодулятором первого выбора.
В условиях целостного организма полиоксидоний оказывает сложное и многогранное действие на иммунную систему. Так как развитие любого иммунного ответа начинается с клеток моноцитарно-макрофагальной системы, а цитокины, продуцируемые моноцитами/макрофагами, обладают плейотропным эффектом, то усиление под влиянием полиоксидония их функциональной активности ведет к активации и клеточного, и гуморального иммунитета. Так, в частности, при введении полиоксидония совместно с низкими дозами антигена происходит усиление синтеза антител к этому антигену в 5-10 раз по сравнению с контролем. Важно отметить, что такое усиление можно наблюдать у животных с генетически детерминированной слабой отвечаемостью на данный антиген [6]. Таким образом, полиоксидоний обладает способностью приводить в движение все факторы, защищающие организм от инфекционных агентов, причем защищающие естественным путем, так, как это происходит при развитии иммунного ответа в организме. А интенсивность иммунного ответа в большей степени зависит от исходного функционального состояния иммунной системы человека [6].
Рассмотрим, какова же клиническая и иммунологическая эффективность полиоксидония при трех основных формах иммунодефицитов.
Первичные иммунодефициты — это врожденные нарушения иммунной системы, связанные с наличием дефектов на генном уровне. Применение иммуномодуляторов при этих заболеваниях на первый взгляд кажется бесперспективным. Естественно, вылечить с помощью любого, даже самого хорошего иммуномодулятора первичный иммунодефицит невозможно, но применение этих препаратов в комплексном лечении таких состояний является обоснованным. Это связано с тем, что, согласно концепции иммунологических мобилей [4], иммунная система работает по типу весов. Наличие груза, даже очень небольшого, на одной из чашечек весов приводит в движение всю систему. Концепция иммунологических мобилей обосновывает применение иммуномодуляторов при первичных иммунодефицитах. Мы полагали, что активация, например, фагоцитарной системы у больных с дефектами в биосинтезе антител может в какой-то степени компенсировать этот недостаток и привести хотя бы к временному улучшению клинического состояния больного.
В отделении иммунопатологии нашего института полиоксидоний применялся в комплексном лечении первичного иммунодефицита — общей вариабельной иммунологической недостаточности (ОВИН) у взрослых. Это заболевание характеризуется снижением всех классов иммуноглобулинов — IgG, IgA, IgM и клинически чаще всего проявляется в виде хронических рецидивирующих заболеваний бронхолегочного аппарата. Как правило, при длительном течении ОВИН и выраженных очагах инфекции у этой категории больных формируется комбинированный клеточно-гуморальный дефект иммунитета; у многих пациентов отмечается тенденция к лейкопении, нейтропении и лимфопении.
У больных с ОВИН лечение полиоксидонием проводили по индивидуальной схеме: начинали с 12 мг, в/в, № 3 через день, а потом переводили на поддерживающую терапию по 6 мг в/м до 10 инъекций. В некоторых случаях полиоксидоний применяли в течение трех месяцев. У больных ОВИН в результате терапии полиоксидонием формула крови нормализовывалась, сокращались сроки лечения обострений, удлинялась ремиссия и в целом существенно улучшалось качество жизни.
К приобретенным иммунодефицитам относится ВИЧ-инфекция. Длительное время клинические иммунологи подвергали сомнению целесообразность применения иммуномодуляторов у больных с этой инфекцией, так как опасались активации под их влиянием Т-клеточного иммунитета и усиления размножения вируса. Однако в настоящее время накапливается положительный опыт применения иммуномодуляторов при ВИЧ-инфекции, и в частности полиоксидония. В НИИ клинической иммунологии Ростова-на-Дону применяли полиоксидоний совместно с антибиотиками (без противовирусной терапии) у больных в стадии пре-СПИДа с двусторонней очаговой пневмонией. У всех пациентов получен хороший клинический эффект, подтвержденный данными иммунологического и биохимического исследований. При применении антибиотиков и полиоксидония, по данным рентгенологического исследования, удалось на пять дней раньше ликвидировать очаги пневмонии в легких и вывести больных в состояние стойкой ремиссии по сравнению с теми, кто получал только антибиотики. У пациентов повысился уровень CD4+ T-клеток и вырос до единицы иммунорегуляторный индекс. Кроме того, улучшилась функциональная активность печени: снизился уровень билирубина и трансаминаз. Удивительным представляется факт существенного снижения вирусной нагрузки: с lg10 7 до lg10 6 . Мы полагаем, что снижение уровня ВИЧ связано со способностью полиоксидония повышать функциональную активность макрофагов и NK-клеток, осуществляющих элиминацию из организма инфицированных клеток. Мы также считаем, что включение полиоксидония в комплексную терапию больных СПИД, страдающих оппортунистическими инфекциями, является оправданным и целесообразным, так как резервные возможности организма человека очень велики и их повышение с помощью иммуномодулятора в ряде случаев может дать хороший клинический результат, пусть даже и кратковременный.
Вторичные иммунодефициты (ВИД) — это нарушения иммунной системы, развивающиеся в позднем постнатальном периоде или у взрослых и не являющиеся результатом генетических дефектов. Условно мы выделяем две формы ВИД: индуцированную и спонтанную [11]. Индуцированная форма возникает в результате конкретных причин, вызвавших ее появление: рентгеновское излучение, цитостатическая терапия, применение кортикостероидов, травмы и хирургические вмешательства. В этот перечень также входят нарушения иммунитета, развивающиеся вторично по отношению к основному заболеванию (диабет, заболевание печени, почек, злокачественные новообразования). Спонтанная форма вторичного иммунодефицита характеризуется отсутствием явной причины (хотя, без сомнения, она имеется), вызвавшей нарушение иммунной реактивности. Клинически она проявляется в виде хронических, часто рецидивирующих инфекционно-воспалительных процессов бронхолегочного аппарата, придаточных пазух носа, урогенитального и желудочно-кишечного тракта, глаз, кожи, мягких тканей, вызванных оппортунистическими (условно-патогенными) микроорганизмами. Поэтому хронические, часто рецидивирующие, вялотекущие, трудно поддающиеся лечению традиционными средствами воспалительные процессы любой локализации у взрослых рассматриваются как клинические проявления ВИД.
Наиболее ярким примером индуцированных ВИД являются хирургические инфекции. Доказана высокая клиническая эффективность полиоксидония, применяющегося как для их профилактики, так и при лечении [2]. В первом случае применение препарата перед операцией может существенно снизить развитие гнойно-септических осложнений, особенно при операциях на толстом кишечнике, когда велик риск их развития. При предоперационном применении полиоксидония почти в три раза удалось снизить частоту ампутации стопы вследствие язвенно-некротических поражений у больных сахарным диабетом [1]. Включение полиоксидония в комплексную терапию развившихся хирургических инфекций способствует более быстрому очищению раны от гнойно-некротических масс, ускоряет ее эпителизацию и заживление. Все это ведет к существенному снижению количества потребляемых антибиотиков и сокращению числа койко-дней. В силу наличия детоксицирующих и антиоксидантных свойств полиоксидоний особенно эффективен при токсико-септических состояниях; в этих случаях его целесообразно назначать капельно, внутривенно ежедневно в течение первых двух-трех дней и далее через сутки.
Как отмечалось выше, хроническое, рецидивирующее течение инфекционно-воспалительного процесса любой локализации может считаться проявлением ВИД. В этих случаях при назначении антимикробных препаратов целесообразным представляется также назначение иммуномодулятора. В нашем институте имеется положительный опыт применения полиоксидония в комплексном лечении хронического рецидивирующего фурункулеза [3] и хронического рецидивирующего герпеса.
У больных в стадии обострения фурункулеза в результате приема полиоксидония наблюдалось уменьшение признаков интоксикации, уменьшение инфильтрации фурункулов, более быстрая их регрессия. Наблюдение в течение двух лет выявило стойкую ремиссию заболевания у 44,6 % больных. Исходно у больных с хроническим рецидивирующим фурункулезом наблюдалось снижение функциональной активности фагоцитарных клеток, в частности снижение бактерицидных свойств нейтрофилов. Как правило, после применения полиоксидония у таких больных происходило восстановление их функциональной активности. Также имело место восстановление иммунорегуляторного индекса при его исходном нарушении.
При применении полиоксидония совместно с противовирусными препаратами у больных с рецидивирующим герпесом в стадии обострения острая фаза местного воспаления купировалась уже на вторые сутки, тогда как в контрольной группе везикулезные элементы сохранялись до пятого дня от начала лечения. Значительно быстрее достигалась и полная реэпитализация очагов поражения. У 95% больных, получавших полиоксидоний, длительность ремиссии составила в среднем три года. У этих больных наблюдалось повышение функциональной активности естественных киллеров и усиливался синтез α-интерферона, то есть полиоксидоний стимулировал развитие противовирусной защиты.
Таким образом, применение полиоксидония показано практически при всех формах иммунодефицитных состояний, когда возникает необходимость повысить противоинфекционную защиту организма. Это прежде всего связано с тем, что полиоксидоний повышает функциональную активность фагоцитарных клеток нейтрофилов и моноцитов/макрофагов, а элиминация возбудителя в значительной степени зависит от их «работы». Особенно велика роль в функционировании организма в целом клеток моноцитарно-макрофагальной системы. Поэтому усиление их функциональной активности дает положительный эффект при самых различных заболеваниях: туберкулезе, сахарном диабете, болезнях сердца [4], урогенитальных инфекциях [8] и др. Учитывая это, становится понятно, почему полиоксидоний характеризуется широким спектром лечебного воздействия.
Литература
1. Гришина Т. Ю., Станулис А. И., Жданов А. В., Хаев А. В. Лечение гнойно-септических осложнений у больных диабетом // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 47-48.
2. Карсонова М. И., Пинегин Б. В., Хаитов Р. М. Иммунопрофилактика и иммунотерапия хирургических инфекций // Практикующий врач. 1998. № 12. С. 9-12.
3. Латышева Т. В., Сетдикова Н. Х. Эффективность полиоксидония при некоторых формах первичных иммунодефицитов (ОВИН) и вторичных иммунодефицитных состояниях // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 41-43.
4. Лусс Л. В. Полиоксидоний в общеклинической практике // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 21-41.
5. Петров Р. В. Я или не Я. Иммунологические мобили. М.: Молодая гвардия, 1987.
6. Петров Р. В., Хаитов Р. М., Некрасов А. В. и др. Полиоксидоний - иммуномодулятор последнего поколения: итоги трехлетнего клинического применения // Аллергия, астма и клиническая иммунология. 1999. № 3. С. 3-6.
7. Пинегин Б. В. Полиоксидоний — новое поколение иммуномодуляторов с известной структурой и механизмом действия // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 27-28.
8. Полосин А. В. Иммуномодулятор полиоксидоний — перспектива в лечении хронических урогенитальных инфекций//Аллергия, астма и клиническая иммунология. 2000. № 1. С. 45-46.
9. Хаитов Р. М., Пинегин Б. В. Иммуномодуляторы и некоторые аспекты их клинического применения // Клиническая медицина. 1996. № 8. С. 7-12.
10. Хаитов Р. М., Пинегин Б. В., Андронова Т. М. Отечественные иммунотропные лекарственные средства последнего поколения и стратегия их применения // Лечащий Врач. 1998. № 4. С. 46-51.
11. Хаитов Р. М., Пинегин Б. В. Вторичные иммунодефициты: клиника, диагностика, лечение // Иммунология. 1999. № 1. С. 14-17.
12. Хаитов Р. М., Пинегин Б. В. Современные представления о защите организма от инфекции // Иммунология. 2000. № 1. С. 61-64.
13. Хаитов Р. М., Пинегин Б. В. Основные принципы иммуномодулирующей терапии // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 9-16.
14. Хоменко А. Г. Туберкулез вчера, сегодня, завтра//Проблемы туберкулеза. 1997. № 5. 9-11.
В настоящее время продолжается интенсивное изучение механизма действия и медицинского применения отечественного иммуномодулятора Полиоксидония, являющегося физиологически активным соединением с молекулярной массой 100 kD и обладающего выраженной иммуномодулирующей активностью. По своей химической структуре он являетя сополимером N-окиси 1,4-этиленпиперазина и (N-карбоксиэтил-) 1,4-этиленпиперазиния бромида с молекулярной массой 80 kD.
Полиоксидоний разрешен к медицинскому применению у детей и взрослых в двух лекарственных формах: в виде инъекций и в виде суппозиториев.
Инъекционная форма Полиоксидония нашла широкое применение в комплексном лечении при ряде хронических инфекционно-воспалительных процессов любой локализации и этиологии. Показана высокая клиническая и иммунологическая эффективность этого иммуномодулятора в лечении хирургических инфекций, инфекций урогенитального, желудочно-кишечного и бронхолегочного трактов.
Так, в частности, в нашем институте Т. В. Латышевой с соавторами (2001, 2002 гг.) показана эффективность Полиоксидония в лечении хронического рецидивирующего фурункулеза, проявляющаяся в существенном удлинении продолжительности ремиссии. А. Е. Шульженко с соавторами (2001, 2002 гг.) показана эффективность Полиоксидония в лечении хронического генитального герпеса, которая также проявлялась в существенном удлинении срока ремиссии этого (основного клинического показателя эффективности лечения любой хронической рецидивирующей инфекции). С. С. Аршиновой с соавторами. (1999, 2000, 2002 гг.) показана эффективность Полиоксидония в лечении туберкулеза легких. Это проявлялось в более быстром закрытии полостей распада, элиминации возбудителя, рассасывании инфильтратов и исчезновении интоксикации по сравнению с больными, получавшими традиционное антимикобактериальное лечение.
В подавляющем большинстве случаев целесообразно применение иммуномодуляторов в комплексном лечении при хронических инфекционно-воспалительных процессах, и мы считаем, что препаратом первого выбора в этих случаях является Полиоксидоний. Это утверждение основано на ряде положений.
Полиоксидоний хорошо взаимодействует с антибактериальными, противогрибковыми и противовирусными препаратами, а также с интерферонами и индукторами интерферонов. При совместном применении антибиотика и иммуномодулятора мы говорим о “двойном” ударе по причине заболевания. Полиоксидоний стимулирует функциональную активность клеток иммунной системы: непосредственно – нейтрофилы, моноциты/макрофаги и естественные киллеры, опосредованно – клеточный и гуморальный иммунитет, от которых в конечном итоге зависит элиминация возбудителя из организма, а антимикробный препарат убивает или понижает функциональную активность возбудителя. Но главным преимуществом Полиоксидония по сравнению с другими иммуномодуляторами является многогранность его положительного воздействия на организм человека.
Помимо иммуномодулирующего эффекта Полиоксидоний обладает детоксицирующими, антиоксидантными и мембранопротекторными свойствами, обусловленными особенностями его химической структуры. Именно наличие комплекса этих свойств обуславливает высокий клинический эффект Полиоксидония, его преимущества перед другими иммуномодуляторами и делает его препаратом первого выбора при лечении заболеваний, связанных с нарушениями иммунной системы.
Рассмотрим более подробно детоксикационные свойства инъекционной формы Полиоксидония. Эти свойства препарата хорошо демонстрируются на модели ожоговой болезни и панкреонекроза. Н. А. Гординская с соавторами (2002 г.) применяли Полиоксидоний в комплексном лечении 24 пациентов с термическими ожогами на площади от 30% до 50% поверхности тела. После курса Полиоксидония у пациентов существенно снижался уровень печеночных аминотрансфераз и среднемолекулярных пептидов. Снижалось также количество циркулирующих иммунных комплексов. Анализируя динамику концентрации токсических веществ в плазме ожоговых больных, авторы обнаружили резко повышенное содержание бактериальных липополисахаридов в период токсемии. На фоне традиционной терапии практически не регистрировалось снижение концентрации ЛПС. На фоне иммунотерапии Полиоксидонием уровень бактериальной эндотоксемии достоверно снижался.
В. Л. Аверкиев с соавторами (2002 г.) оценивали у 76 больных острым деструктивным панкреатитом в послеоперационном периоде помимо иммунного статуса состояние перекисного окисления липидов и интоксикационный синдром. У 23 больных в комплексном лечении этого заболевания был применен Полиоксидоний. В послеоперационном периоде в 1-е сутки по сравнению с дооперационным уровнем отмечается прогрессирование липопероксидации, что связано, вероятно, с наркозом, операционной травмой и с реперфузией ткани поджелудочковой железы после рассечения ее капсулы и абдоминизации. При применении Полиоксидония происходит снижение уровня малонового диальдегида и диеновых кислот. В послеоперационный период у больных происходит существенное повышение молекул средней массы (МСМ), свидетельствующее о тяжелом синдроме эндогенной интоксикации вследствие воспалительного процесса и операционной травмы. При применении Полиоксидония отмечается планомерное понижение этого показателя и к 14-м суткам уровень МСМ достигает нормы.
При анализе биохимических показателей выявлено достоверное снижение уровней билирубина, креатинина и мочевины сыворотки крови, уменьшение активности аминотрансфераз у всех больных, особенно выраженное в группе больных, получаших Полиоксидоний. Авторы полагают, что с выраженными детоксикационными свойствами Полиоксидония связано и снижение летальности (52% в контрольной и 23,1% в опытной группе) и частоты гнойно-септических осложнений (92% в контрольной и 43,9% в опытной группах). Высокая клиническая эффективность лечения Полиоксидонием четко связана и с улучшением параметров иммунного статуса.
Наряду с инъекционной формой в клиническую практику широко внедряется Полиоксидоний в виде суппозиториев. Эта форма препарата показана к применению практически при всех тех же нозологиях, что и инъекционная. На наш взгляд, особый интерес представляет применение суппозиториев для лечения хронических заболеваний урогенитального тракта.
М. Н. Шатохин с соавторами (2002 г.) показали эффективность при использовании Полиоксидония в виде суппозиториев в комплексном лечении хронического простатита. После традиционной терапии болевой синдром сохранился у 75% пациентов, дизурические расстройства наблюдались у 70% больных, простаторея и боль или дискомфорт при эякуляции остались в 40% случаев. Качество жизни практически не улучшилось.
После лечения с включением суппозиториев Полиоксидония болевой синдром купировался у всех пациентов, дизурические явления, простатоторея и дискомфорт при эякуляции сохранились лишь у 1 пациента. Качество жизни заметно улучшилось (3 балла по сравнению с 8,8 балла до лечения). При ректальном пальцевом исследовании характеристики предстательной железы улучшились: исчезла болезненность, повысился тонус. В секрете предстательной железы понизились концентрации провоспалительных цитокинов. Особенно интересными, на наш взгляд, являются данные авторов об изменениях местного иммунитета. Оказалось, что при применении суппозиториев Полиоксидония происходило снижение провоспалительных цитокинов (ФНОa, ИЛ-1b, ИЛ-6) при повышении содержания ИЛ-4 и sIgA в секрете предстательной железы.
М. Х. Коджаева с соавторами (2002 г.) применяли Полиокидоний в виде суппозиториев в комплексной терапии у 34 женщин в возрасте от 16 до 39 лет с диагнозом «хронические рецидивирующие урогенитальные инфекции». У этих женщин наблюдалось значительное улучшение клинических и лабораторных показателей. Это выражалось в увеличении количества лактобактерий, увеличении в вагинальном секрете IgA и sIgA, улучшении кольпоскопической картины, уменьшении выделений и т. д.
Л. Е. Смирновой с соавторами (2002 г.) проведена комплексная терапия 58 больных с обострением хронических воспалительных заболеваний внутренних половых органов (ХВЗВПО). Основную группу составили 36 пациенток, получавшие Полиоксидоний в виде суппозиториев на фоне базисной антибактериальной терапии. В контрольную группу вошли 22 больные, которым проводилась только базисная терапия. У больных основной группы отмечена более выраженная динамика исчезновения основных клинических симптомов, более ранняя нормализация УЗ-картины, элиминация возбудителей из слизи цервикального канала в 92% случаев по сравнению с 32% у больных контрольной группы. Также после проведенной терапии у больных основной группы, в отличие от пациенток контрольной группы, нормализовался уровень концентрации иммуноглобулинов в содержимом влагалища. Полученные данные свидетельствуют о высокой эффективности комплексной терапии ХВЗВПО в стадии обострения с применением Полиоксидония.
Полученные данные говорят о целесообразности применения Полиоксидония в гинекологической практике у женщин с длительной хронической бактериальной инфекцией.
Т. Н. Кузина и соавторы, изучали некоторые параметры местного иммунитета слизистой влагалища у 39 женщин в возрасте 19–35 лет, получавшие полиоксидоний ежедневно интравагинально, №10. Больные были разделены на две группы. Первая группа состояла из ВИЧ-серонегативных женщин (14), которые имели в качестве постоянных половых партнеров ВИЧ-инфицированных мужчин. Вторая группа – 25 ВИЧ-инфицированных женщин (стадия В по CDC). В первой группе пациенток, которые были подвергнуты катамнестическому наблюдению в течение года, ВИЧ-инфицирования женщин не регистрировалось несмотря на то, что они имели постоянные половые контакты с ВИЧ-инфицированными мужчинами, которые не пользовались презервативами.
Помимо инъекционной формы и суппозиториев разрабатываются новые перспективные способы применения Полиоксидония. В. П. Вавилова с соавторами (2002 г.) предложили интраназальную терапию Полиоксидонием детей, часто болеющих ОРВИ на фоне хронического аденоидита (40 детей в возрасте 3–6 лет) с учетом характера поражения лимфоглоточного кольца (нейтрофильно-макрофагальный вариант). У детей, страдающих хроническим аденоидитом с гнойным экссудатом, Полиоксидоний применялся местно эндоназально в течение 10 дней. Проспективное наблюдение в течение 3,5 месяцев подтвердило эффективность иммуномодулятора в плане становления местного иммунитета респираторного тракта, нормализации микробного пейзажа носоглотки и улучшения клинической картины с уменьшением размеров гипертрофированной глоточной миндалины. Представленные данные показывают перспективность создания новой лекарственной формы полиоксидония для лечения заболеваний ЛОР-органов и стимуляции местного иммунитета верхних дыхательных путей.
В целом Полиоксидоний является уникальным иммуномодулирующим препаратом, сочетающим в себе множество положительных качеств. Это, без сомнения, выдающееся достижение российских ученых. Полиоксидоний занял достойное место в арсенале отечественных лекарственных средств и среди иммуномодуляторов бесспорно является препаратом первого выбора. Без сомнения, по мере широкого медицинского применения этого препарата клинические показания для его использования будут расширяться, будут уточняться схемы и дозы его назначения, но уже сегодня можно с уверенностью сказать, что применение Полиоксидония позволило существенно повысить эффективность лечения и профилактики ряда заболеваний, связанных с нарушениями иммунной системы.
Читайте также:

