Эпителиальное образование в желудке что это
Обновлено: 17.05.2024
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»;
ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России
Классификация эпителиальных опухолей желудка ВОЗ 2019 г., 5-е издание
Журнал: Архив патологии. 2020;82(4): 58‑69
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»
Классификация эпителиальных новообразований желудка 2019 г. частично изменена по сравнению с изданием 2010 г.: выделены новые гистологические подтипы дисплазий (зубчатая дисплазия, дисплазия желудочных ямок/крипт), изменилась структура классификации доброкачественных новообразований (термин аденоматозный полип вновь вводится в обращение и представляет собой группу доброкачественных опухолей, ранее относимых к аденомам желудочного типа), раздел злокачественных эпителиальных опухолей расширен за счет карциномы из париетальных клеток, микропапиллярной и мукоэпидермоидной карцином, рака из клеток Панета. Факторы риска рака желудка разделены на две группы в зависимости от уровня доказательности их участия в канцерогенезе. Наиболее значимыми признаны: выявленная инфекция Helicobacter pylori, работа, связанная с производством резины, курение табака, рентгеновское и гамма-излучение. Изменены подходы к градации раков желудка по степени дифференцировки: подчеркивается предпочтительное использование двухступенчатой градации (low grade/ high grade). Нововведения также коснулись стадирования рака желудка. Раздел, посвященный нейроэндокринным опухолям, существенных изменений не претерпел. В целом новая классификация содержит более подробные данные по каждому из разделов, однако она не является интуитивно понятной. Пункты классификационной таблицы не соответствуют названиям разделов в тексте, что затрудняет понимание структуры и навигацию.
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»;
ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России
Дата принятия в печать:
В июле 2018 г. в Лионе состоялось заседание рабочей группы по опухолям пищеварительной системы под эгидой Международного агентства по изучению рака (International Agency for Research on Cancer, IARC). В результате классификация опухолей была пересмотрена и издана в 2019 г. в составе серии «WHO Classification of Tumors», 5-е издание [1]. Следует отметить, что разделы, посвященные отдельным локализациям, включают в себя только эпителиальные опухоли. Мезенхимальные опухоли и лимфомы представлены в виде отдельных глав. Другой особенностью новой классификации является наличие кодов классификации МКБ-11, которая официально вводится в России с 01.01.21, и отдельной главы, посвященной генетическим опухолевым синдромам желудочно-кишечного тракта. Разделы классификации 2019 г. (табл. 1) выглядят более структурированными, в каждый раздел добавлена чрезвычайно важная информация о необходимых и желательных диагностических критериях каждой конкретной опухоли, что упрощает работу с изданием для практического врача.
Таблица 1. Классификация эпителиальных опухолей желудка
Доброкачественные эпителиальные опухоли и предраковые поражения
Железистая интраэпителиальная неоплазия, low grade
Железистая интраэпителиальная неоплазия, high grade
Дисплазия зубчатая, low grade
Дисплазия зубчатая, high grade
Дисплазия кишечного типа
Дисплазия фовеолярного (желудочного) типа
Дисплазия желудочных ямок/крипт**
Аденома кишечного типа, low grade
Аденома кишечного типа, high grade
Аденома желудка кишечного типа, спорадическая
Аденома желудка кишечного типа, синдромная
Аденоматозный полип, low grade
Аденоматозный полип, high grade
Злокачественные эпителиальные опухоли
Карцинома из париетальных клеток
Папиллярная аденокарцинома NOS***
Микропапиллярная карцинома NOS***
Медуллярная карцинома с лимфоидной стромой
Карцинома клеток Панета
Плоскоклеточная карцинома NOS***
Крупноклеточная карцинома с рабдоидным фенотипом
Карцинома с остеокластоподобными гигантскими клетками
Нейроэндокринная опухоль NOS***
Нейроэндокринная опухоль, G1
Нейроэндокринная опухоль, G2
Нейроэндокринная опухоль, G3
Карциноид из энтерохромаффинных клеток
Злокачественный карциноид из ECL-клеток
Нейроэндокринная карцинома NOS***
Крупноклеточная нейроэндокринная карцинома
Мелкоклеточная нейроэндокринная карцинома
Смешанная нейроэндокринная и ненейроэндокринная опухоль (MiNEN)
Примечание. * — новые коды для МКБ-O; ** — см. пояснения в тексте статьи; *** — NOS — not otherwise specified (без дополнительных уточнений).
В 5-м издании классификации значительно увеличены разделы, касающиеся фоновых и предопухолевых поражений, а также доброкачественных эпителиальных опухолей желудка.
К фоновым состояниям относят:
— атрофию и кишечную метаплазию,
— полипы фундальных желез,
— гиперпластические полипы желудка.
Большое внимание уделяется гастриту, вызванному Helicobacter pylori, стадированию атрофических изменений по системе OLGA [2—4], а также различным видам кишечной метаплазии.
Предопухолевые изменения слизистой оболочки желудка (дисплазия /железистая интраэпителиальная неоплазия) определены как неопластические изменения эпителия слизистой оболочки без признаков стромальной инвазии. Наиболее часто дисплазия встречается в антруме, однако может наблюдаться в любых отделах желудка [5]. В 5-м издании, как и в 4-м, выделяется два основных вида дисплазии: кишечного и фовеолярного (желудочного) типа. При этом в 5-м издании выделяют также подтипы дисплазий желудка: зубчатую дисплазию высокой степени, зубчатую дисплазию низкой степени, дисплазию желудочных ямок/крипт. Однако, несмотря на то что эти подтипы вынесены в классификационную таблицу, в тексте обозначено, что их клиническое значение определено нечетко и приводятся крайне короткие описания. Таким образом, решение составителей классификации о внесении редких подтипов дисплазии с неясной клинической значимостью в основную классификационную таблицу остается труднообъяснимым.
Дисплазия/железистая интраэпителиальная неоплазия желудка может представлять собой плоский, втянутый или полиповидный участок поражения слизистой оболочки. Градация дисплазии желудка предусматривает выделение дисплазии низкой степени (low grade) и дисплазии высокой степени (high grade) [6, 7].
Дисплазия кишечного типа описывается как очаг, состоящий из тубулярных, тубулярно-ворсинчатых или ворсинчатых структур, выстланных высоким цилиндрическим эпителием с увеличенными, удлиненными, гиперхромными ядрами, расположенными в эпителиальном пласте в несколько рядов. Часто встречается терминальная дифференцировка в виде наличия бокаловидных или нейроэндокринных клеток, иногда клеток Панета. Выявляется экспрессия MUC2, CD10, CDX2 [8].
Дисплазия фовеолярного типа описывается как очаг из тубулярно-ворсинчатых и/или зубчатых железистых структур, выстланных кубическим или низким цилиндрическим эпителием, напоминающим фовеолярный эпителий. Ядра круглые или овальные, с четко различимыми ядрышками. Цитоплазма клеток бледно-эозинофильная. Выявляется положительное иммуногистохимическое окрашивание с маркерами MUC5AC, MUC6.
Дисплазия желудочных ямок/крипт. В оригинальном тексте классификации употреблен термин «ямки/крипты», в связи с чем обращаем внимание, что использование термина «крипты» для слизистой оболочки желудка не соответствует международной гистологической номенклатуре. Такой тип дисплазии наблюдается в базальных отделах желудочных ямок, где железистые структуры демонстрируют созревание до поверхностных эпителиальных клеток. В 49—72% случаев встречается по периферии традиционной неоплазии и считается независимым предиктором прогрессии в инвазивный рак [9], однако в тексте классификации не указано, чем она отличается от дисплазии фовеолярного типа.
Зубчатая дисплазия локализуется только в желудочных ямках, характеризуется наличием микропапиллярных структур, экспрессирующих MUC5AC. Подобные гистологические изменения в литературе иногда называют зубчатой аденомой желудка [10].
Классификация доброкачественных эпителиальных опухолей значительно изменена. Если ранее понятия «аденома кишечного типа» и «аденоматозный полип» являлись синонимами, то в новой редакции аденомы кишечного типа стоят особняком, а к аденоматозным полипам относят образования, ранее находившиеся в группе аденом желудочного типа (аденомы фовеолярного типа, аденомы из пилорических желез). К группе аденоматозных полипов в новой классификации также относят аденомы из кислотообразующих желез (oxyntic gland adenoma), не упоминавшиеся в предыдущей классификации. Полипы фундальных желез (fundic gland polyps) более не рассматриваются как истинные опухоли и не имеют кода МКБ-О. Итак, к доброкачественным эпителиальным опухолям относят аденомы кишечного типа и аденоматозные полипы (аденомы фовеолярного типа, аденомы из пилорических желез, аденомы из кислотообразующих желез (oxyntic gland adenoma). Причем каждая из этих категорий может сопровождаться дисплазией высокой или низкой степени. Аденомам кишечного типа соответствуют коды МКБ-О 8144/0 и 8144/2 в зависимости от степени дисплазии, а для всех разновидностей аденоматозных полипов предусмотрены единые коды 8210/0 и 8210/2.
Аденома кишечного типа является третьим по частоте встречаемости образованием среди полиповидных новообразований желудка (после гиперпластических полипов и полипов фундальных желез), локализуется преимущественно в тех отделах желудка, где распространена кишечная метаплазия (в 60% случаев поражаются дистальные отделы желудка) [11]. Пациенты обычно старше 60 лет. Аденомы кишечного типа часто сочетаются с атрофическим гастритом и выраженной кишечной метаплазией. Выделяют два подтипа аденом кишечного типа: спорадические и синдромные. Синдромные аденомы иногда являются одним из проявлений семейного аденоматозного полипоза. Размеры аденом не превышают 2 см. Гистологически аденомы кишечного типа представляют собой совокупность тубулярных структур, выстланных пролиферирующим эпителием с признаками дисплазии, которые формируют полиповидное образование. Аналогичная картина на плоской слизистой оболочке без формирования полиповидного образования обозначается как дисплазия (интраэпителиальная неоплазия). Большинство клеток имеют цилиндрическую форму, вытянутое вдоль длинной оси ядро, присутствуют бокаловидные клетки и клетки Панета. При наличии дисплазии высокой степени аденомы кишечного типа стадируются как Tis.
Аденома фовеолярного типа — доброкачественная опухоль из фовеолярного эпителия. Локализуются обычно в теле или дне желудка, развиваются без предшествующих фоновых процессов в виде гастрита или атрофии/метаплазии [12]. Спорадические опухоли крайне редки [13], обычно аденомы фовеолярного типа возникают при семейном аденоматозном полипозе и других наследственных синдромах. Гистологически опухоли состоят из сосочковых и тубулярных структур, покрытых цилиндрическим эпителием фовеолярного типа с удлиненными ядрами и признаками дисплазии (чаще всего низкой степени). Поверхностный эпителий содержит нейтральные (ШИК-позитивные) муцины, что отличает аденому фовеолярного типа от аденомы из пилорических желез. Отмечается выраженная диффузная экспрессия MUC5AC и локальная слабая экспрессия MUC6; реакции с MUC2 и CDX2 отрицательные. Однако ориентироваться при постановке диагноза необходимо в первую очередь на окраску гематоксилином и эозином и ШИК-реакцию, нежели чем на иммуногистохимию.
Аденома из пилорических желез — доброкачественная опухоль из эпителия пилорических желез, возникающая обычно в теле и дне желудка [14]. Большинство таких аденом выявляется у пациентов 60—70 лет и сочетается с атрофией/метаплазией слизистой оболочки дна и тела желудка, вызванной аутоиммунным или H. pylori-ассоциированным гастритом [14]. Размер от 0,3 до 10 см (средний — 2 см). Аденомы из пилорических желез представлены плотно лежащими железами пилорического типа, выстланными кубическим или низким цилиндрическим эпителием. Клетки со светлой или слегка эозинофильной цитоплазмой, ядра расположены базально, округлые или овоидные, со слабо различимыми ядрышками. Поверхностный эпителий не содержит нейтральные (ШИК-позитивные) муцины. В крупных опухолях железы могут быть кистозно-расширены. В 40—50% случаев в аденомах из пилорических желез встречаются дисплазия высокой степени и фокусы аденокарциномы, однако только в 10% случаев наблюдается инвазия в подслизистый слой [15]. Риск прогрессии в аденокарциному увеличивается с размером аденомы, при наличии тубуловорсинчатых структур. В связи с высоким риском прогрессии в рак желудка рекомендовано тотальное удаление образования.
Аденома из кислотообразующих желез (oxyntic gland adenoma) — доброкачественная опухоль из главных (зимогенных) и/или обкладочных (париетальных) клеток с высоким риском прогрессии в инвазивный рак. Локализуется в верхней трети желудка, точная частота встречаемости не установлена. Опухоль состоит из тубулярных структур, выстланных цилиндрическими клетками со светлой эозинофильной цитоплазмой, слабой ядерной атипией, похожих на клетки фундальных желез (преимущественно главные). Может находиться на поверхности, однако чаще встречается внутрислизистое расположение. Дифференцировку клеток можно подтвердить иммуногистохимически с помощью окраски на пепсиноген I (главные клетки) и Н+/К+ АТФазу (обкладочные клетки) [16]. Иногда в опухоли формируются солидные структуры и анастомозирующие тяжи, что может симулировать картину нейроэндокринной опухоли (NET) [17]. В таких случаях полезно определение экспрессии хромогранина А, в аденомах из кислотообразующих желез желудка данный маркер не выявляется.
Рак желудка занимает в мире 3-е место по уровню смертности [27], несмотря на снижение заболеваемости, ежегодно в мире выявляется около 1 млн новых случаев рака желудка [18, 19]. Наиболее высокий уровень заболеваемости отмечается в центральной и восточной Азии, восточной Европе и Южной Америке [18].
Рак желудка развивается под воздействием комбинации различных неблагоприятных факторов, в 90% случаев является спорадическим и только у 10% пациентов связан с наследственными/врожденными причинами. Факторы риска для развития рака желудка перечислены в табл. 2. В новом издании эти факторы разделены на две группы в зависимости от различного уровня доказательности. Следует отметить, что авторы придают большое значение инфекционным (H. pylori, вирус Эпштейна—Барр) и химическим агентам [20], а также особенностям диеты [19, 21—24], в то время как рефлюкс желчи больше не выносится как значимый фактор риска.
Таблица 2. Факторы риска возникновения рака желудка
Факторы, для которых имеются достаточные доказательства участия в канцерогенезе рака желудка у человека:
Что такое аденокарцинома желудка? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бондаренко Юлии Сергеевны, хирурга со стажем в 16 лет.
Над статьей доктора Бондаренко Юлии Сергеевны работали литературный редактор Юлия Липовская , научный редактор Вячеслав Михайличенко и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Аденокарцинома желудка (Gastric adenocarcinoma) — это злокачественная опухоль, которая развивается из железистых клеток внутренней стенки желудка — эпителиального слоя. На её долю приходится 90–95 % от всех типов рака желудка [1] .
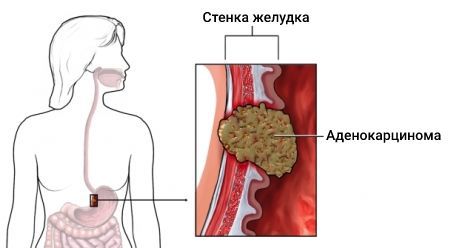
К основным симптомам аденокарциномы относятся: боль в верхних отделах живота («под ложечкой»), снижение веса, тошнота, рвота и потеря аппетита.
Причины аденокарциномы желудка
Причины заболевания окончательно не изучены. Известны только факторы риска, которые могут привести к развитию болезни. Их наличие не гарантирует, что со временем у человека сформируется рак желудка.
Различают внешние и внутренние факторы риска аденокарциномы.
Внешние факторы риска:
- нездоровый образ жизни и нерациональное питание: курение, употребление алкоголя, большого количества копчёностей, консервантов и нитритов, диета с низким содержанием овощей и фруктов; ;
- операции на желудке: ушивание прободной язвы и резекция желудка — удаление его части;
- профессиональные вредности: вдыхание угольной пыли, лаков и красок, производство резины, металлургические работы;
- инфекции, например вирус Эпштейна — Барр и Helicobacter pylori.
Внутренние факторы риска:
-
, которая развивается из-за дефицита витамина В12; ;
- аденоматозные полипы желудка;
- болезнь Мене́трие — переразвитие слизистой оболочки желудка с её последующим утолщением, появлением аденом и кист;
- наследственные факторы: мутация гена CDH1 и/или развитие рака желудка у родственника повышает вероятность образования опухоли на 80 % [1][2] .
Под влиянием этих факторов железистые клетки желудка начинают мутировать и бесконтрольно делиться, «ускользая» от иммунной системы.
Эпидемиология
Аденокарцинома желудка — наиболее распространённая злокачественная опухоль. В структуре смертности среди онкозаболеваний она занимает второе место.
Ежегодно в России регистрируют около 36 тысяч новых случаев рака желудка и более 34 тысяч человек умирают от этой болезни. Высокая смертность связана с тем, что больные обращаются за медицинской помощью уже на поздних стадиях рака.
Мужчины заболевают аденокарциномой в 1,3 раза чаще женщин. Возможно, это связано с тем, что женщины внимательней относятся к своему здоровью и раньше обращаются к врачу.
Чаще всего болезнь выявляют у людей старше 50 лет [3] . Но аденокарцинома, вызванная наследственными причинами, чаще возникает до 40 лет.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы аденокарциномы желудка
- На ранних стадиях — дискомфорт в животе, изжога, чувство переполнения и распирания вскоре после еды, иногда даже после небольшого перекуса.
- На более поздних стадиях — тошнота и боли в верхней части живота.
- Рвота съеденной пищей из-за поражения выходного отдела желудка.
- Дискомфорт за грудиной при продвижении пищи из-за поражения пищеводно- желудочного перехода.
- Рвота «кофейной гущей» и «чёрный стул» при кровотечении из опухоли желудка.
- Снижение веса, анемия, слабость и кахексия (истощение) из-за проблем с проходимостью пищи, плохого аппетита и быстрой насыщаемости на фоне растущей опухоли.
- Бледность кожи из-за присоединения анемии [2] .
Аденокарцинома желудка проявляет себя не сразу. Первым симптомом чаще всего становится быстрая насыщаемость, дискомфорт и тяжесть в верхних отделах живота. Постепенно болевой синдром прогрессирует, из-за чего снижается аппетит и вес. Признаки кровотечения и рвота также характерны для более поздних стадий болезни.
Патогенез аденокарциномы желудка
Патогенез аденокарциномы желудка до конца не изучен. Существует теория, что под воздействием агрессивных внешних факторов на слизистую оболочку желудка повреждается структура ДНК железистых клеток, которые выстилают желудочные ямки, вырабатывают слизь и гормоны простагландины. Это повреждение приводит к различным мутациям, из-за которых здоровая клетка становится злокачественной [4] .

Изначально агрессивные факторы вызывают воспаление в стенке желудка, которое затем приводит к дисплазии и метаплазии. Клетки начинают быстро делиться, становятся атипичными, из-за чего меняется структура слизистой оболочки желудка. По сути дисплазия — это предраковое состояние.
После образования аденокарцинома начинает расти либо в просвет желудка, либо прорастать во все слои его стенки, соседние ткани и органы, например в поджелудочную железу, печень, переднюю брюшную стенку и поперечный отдел толстой кишки с её брыжейкой. Также опухоль может расти вдоль пищеварительной трубки, распространяясь на пищевод и двенадцатиперстную кишку.
С током лимфы, а на поздних стадиях через кровоток, раковые клетки распространяются в организме и становятся причиной метастазов — образования вторичных очагов опухоли в других органах. Чаще всего аденокарцинома метастазирует в печень, лёгкие, головной мозг и брюшину.
Классификация и стадии развития аденокарциномы желудка
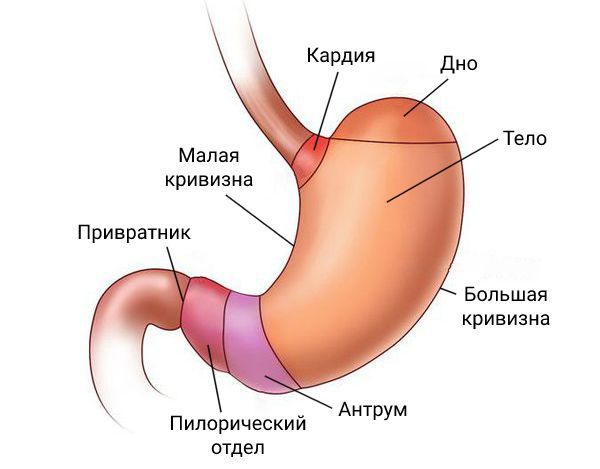
Аденокарцинома может образоваться в любой части желудка. Чаще всего её обнаруживают в пилорическом отделе, чуть реже — в кардиальном.
У каждой локализации есть свой шифр:
- C16.0 — опухоль находится в кардиальном отделе желудка;
- C16.1 — в дне желудка;
- C16.2 — в теле желудка;
- C16.3 — в антральном отделе желудка;
- C16.4 — в пилорическом отделе желудка;
- C16.5 — на малой кривизне желудка;
- C16.8 — на большой кривизне желудка;
- C16.8 — выходит за пределы перечисленных областей;
- C16.9 — опухоль неуточнённой локализации [16] .
В медицинском международном сообществе наиболее признана классификация по TNM, где:
- «T» обозначает «tumor», т. е. глубину прорастания опухоли в стенке желудка;
- «N» — «nodus», т. е. количество поражённых лимфоузлов;
- «М» — «metastasis», т. е. наличие метастазов.
Стадии аденокарциномы желудка по классификации TNM 2018 года представлены ниже в таблице [18] .
В зависимости от того, насколько опухолевые клетки похожи на здоровые, выделяют три формы опухоли:
- высокодифференцированная аденокарцинома желудка (G1) — клетки опухоли похожи на здоровую ткань, сама опухоль обычно растёт медленно, при своевременной диагностике хорошо поддаётся лечению;
- умеренно дифференцированная аденокарцинома (G2) — скорость роста и злокачественность клеток опухоли умеренные;
- низкодифференцированная аденокарцинома (G3) — клетки опухоли не похожи на какую-либо здоровую ткань, сама опухоль наиболее злокачественная, отличается быстрым ростом и метастазированием.
Отдельно стоит сказать о перстневидноклеточной аденокарциноме желудка. Это редкая низкодифференцированная опухоль, одна из самых агрессивных форм рака желудка [19] [21] . Фактически она не поддаётся химио- и лучевой терапии, наиболее эффективным методом лечения на ранних стадиях является операция. Поэтому крайне важно обращаться к врачу при появлении первых симптомов, похожих на признаки гастрита или язвы желудка, особенно если есть предрасположенность к раку желудка.
Осложнения аденокарциномы желудка
Чаще возникает кровотечение и опухолевый стеноз, реже — асцит.
Диагностика аденокарциномы желудка
Обычно пациент с аденокарциномой желудка жалуется на боли в верхней части живота (под «ложечкой»), снижение веса, непроходимость пищи, отвращение к еде, потерю аппетита, рвоту съеденной накануне пищей или кровью.
При подозрении на аденокарциному желудка назначают инструментальное обследование:
- ФГДС с биопсией — обследование пищевода, желудка и двенадцатиперстной кишки с забором и исследованием фрагмента опухоли. Выполняется в первую очередь. Позволяет отличить аденокарциному от других видов опухоли.
- КТ органов брюшной полости, грудной клетки и головы с внутривенным контрастированием — онкопоиск. Позволяет уточнить, поражены ли лимфоузлы, есть ли метастазы в других органах.
- Лапароскопия — обследование желудка с помощью видеолапароскопа. Показано пациентам, у которых по данным эндоУЗИ или КТ есть подозрение на прорастание опухоли в серозную оболочку желудка. Обязательна при тотальном и субтотальном поражении органа. Если местное распространение опухоли подтвердилось, меняется тактика лечения: таким больным сначала будет показана химиотерапия, а затем (при уменьшении опухоли) — хирургическое лечение. В сомнительных случаях в ходе лапароскопии берут смывы с желудка и брюшной полости. Это помогает обнаружить опухолевые клетки и выставить стадию рака перед началом химиотерапии.
- УЗИ брюшной полости и надключичных лимфоузлов — позволяет выявить метастазы печени, асцит и увеличение лимфоузлов (зачастую поражаются лимфоузлы над ключицами, в области яичников, прямой кишки и пупка).
Чаще всего выполняют УЗИ, КТ и ФГДС с биопсией, реже — эндоскопическое УЗИ, так как не все специалисты могут его провести. В крупных онкологических стационарах пациенты проходят все перечисленные исследования и ПЭТ КТ, так как они помогают верно подобрать тактику лечения.
При подготовке к операции обязательно назначают консультацию кардиолога. Чтобы оценить функцию сердца, по показаниям дополнительно проводят эхокардиографию и холтеровское мониторирование. Также выполняют исследование ФВД (функции внешнего дыхания) и УЗДГ вен нижних конечностей, чтобы исключить тромбозы. Иногда может потребоваться консультация эндокринолога, невролога и других врачей [6] .
Лабораторная диагностика включает:
- развёрнутый клинический и биохимический анализ крови;
- коагулограмма — исследование свёртывающей системы крови;
- определение группы крови и резус-фактора с фенотипированием;
- анализ крови на гепатиты В, С, ВИЧ-инфекцию и сифилис;
- общий анализ мочи;
- анализ крови на онкомаркеры (Са 19-9, Са 72-4 и РЭА — раковый эмбриональный антиген).
Все эти анализы также нужны для предоперационной подготовки. Если есть подозрение на аденокарциному желудка, нужно обратить внимание на количество эритроцитов и гемоглобина в общем анализе крови: их снижение может указывать на развитие анемии и внутрижелудочное кровотечение.
Лечение аденокарциномы желудка
Хирургическое лечение на ранней стадии
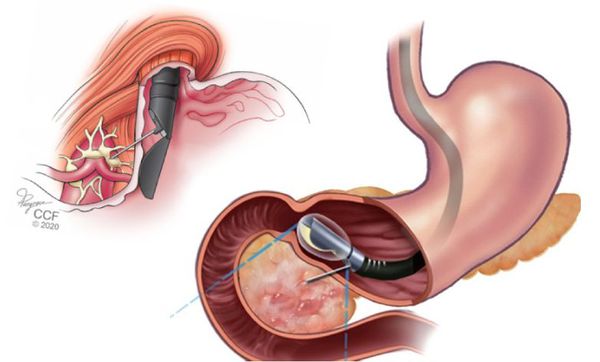
При выявлении ранних форм рака, т. е. при раке in situ, показано эндоскопическое лечение:
- резекция слизистой (EMR) — удаление опухоли вместе с частью слизистой оболочки желудка;
- диссекция в подслизистом слое (ESD) — удаление опухоли вместе с частью подслизистого слоя. Проводится при аденокарциноме до 2 см, позволяет удалить её единым блоком, без разрезов [8] .
Эти операции проводят под общим обезболиванием. Вначале определяют границы опухоли и с помощью электрокоагуляции «маркируют» (прижигают) края резекции, отступая на 3 мм от границы опухоли. Затем в подслизистый слой вводят инъекцию физраствора и Волювена (Гидроксиэтилкрахмала), чтобы отделить опухоль от мышечного слоя. Потом аденокарциному удаляют и смотрят на её «ложе»: нет ли кровотечения или перфорации, удалось ли полностью удалить опухоль. После чего удалённый фрагмент извлекают и отправляют на гистологическое исследование.
![Резекция слизистой желудка [17]](https://probolezny.ru/media/bolezny/adenokarcinoma-zheludka/rezekciya-slizistoy-zheludka-17_s.jpg)
После операции пациентов выписывают на 3–4 сутки. Эффективность лечения при соблюдении всех стандартов составляет 98 %. Рекомендуется:
- через месяц после операции, а затем каждые 3 месяца делать ФГДС;
- через полгода после операции — КТ;
- в течение месяца строго соблюдать диету — питаться жидкой протёртой пищей, исключить алкоголь и горячую еду.
Хирургическое лечение на поздних стадиях
Операция при аденокарциноме желудка проводится в несколько этапов: сначала удаляется сама опухоль, затем восстанавливается пассаж пищи [9] .
Основные радикальные операции при аденокарциноме желудка:
- гастрэктомия — полное удаление желудка;
- субтотальная проксимальная резекция — удаление верхней части желудка вместе с кардиальным отделом;
- субтотальная дистальная резекция — удаление нижних 2/3 или 3/4 желудка.
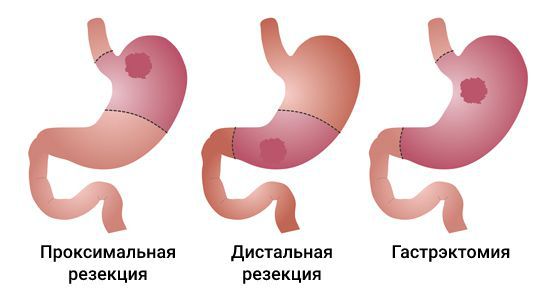
Все виды операций выполняются как «открытым» способом (лапаротомически), так и через небольшие разрезы (лапароскопически), в том числе с помощью робототехники. Выбор хирургического доступа и объёма операции зависит от распространённости процесса: степени поражения стенок желудка, вовлечения пищевода, двенадцатиперстной кишки и наличия метастазов.
После удаления опухоли часто выполняют лимфодиссекцию. Это стандартная операция по удалению лимфоузлов при раке желудка. Она проводится, чтобы снизить риск рецидива, так как аденокарцинома очень часто метастазирует лимфогенным путём , т. е. с током лимфы.
При единичных метастазах в других органах выполняют симультанные операции, т. е. сразу несколько вмешательств.
Если у пациента много отдалённых метастазов, то оперативное лечение, как правило, не проводится. Но при развитии экстренных жизнеугрожающих состояний, таких как перфорация стенки желудка, кровотечение или стеноз, операция выполняется, чтобы спасти жизнь пациента. Объём оперативного вмешательства при этом должен быть минимальным.
Химиотерапия
Основным методом лечения опухоли, которую невозможно удалить, является химиотерапия [12] . Она нужна для того, чтобы убить опухолевые клетки или значительно замедлить их рост.
Доктор может назначить монотерапию, т. е. лечение одним препаратом, или комбинированную химиотерапию с применением нескольких лекарств. Комбинированная химиотерапия позволяет усилить противоопухолевый эффект.
Комбинированные методы лечения включают:
- периоперационную химиотерапию — предпочтительный метод, проводится перед операцией, чтобы уменьшить опухоль, и после операции для борьбы с оставшимися раковыми клетками [10][11] ;
- адъювантную химиотерапию — выполняется после операции;
- адъювантную химиолучевую терапию — проводится после нерадикального удаления опухоли, т. е. когда раковые клетки остаются по краям резекции и продолжают расти.
Выбор конкретной комбинации зависит от состояния пациента, его возраста, а также тяжести и характера сопутствующих заболеваний.
Показания к химиотерапии:
- распространение аденокарциномы за пределы слизистого слоя;
- поражение лимфоузлов;
- наличие метастазов.
Пациент может отказаться от химиотерапии, но он должен понимать, что без лечения опухоль может быстро возникнуть снова и метастазировать.
Симптоматическое лечение (паллиативная помощь)
Симптоматическая терапия проводится на IV стадии рака, когда специальные методы лечения противопоказаны. Она помогает облегчить симптомы болезни с помощью адекватного обезболивания.
Рекомендуется постепенно переходить от слабых обезболивающих (например, Кетопрофена) к более сильным препаратам, вплоть до наркотических (Трамадола или Морфина). При выраженном болевом синдроме их можно использовать в среднем каждые 4 часа.
Прогноз. Профилактика
Прогноз при аденокарциноме желудка зависит от морфологического вида опухоли (дифференцированности), её размеров, наличия и количества метастазов, а также от инвазии в окружающие органы.
Зачастую пациенты с аденокарциномой обращаются к врачу уже на поздних стадиях болезни, когда опухоль проявляет себя осложнениями и её уже нельзя удалить [16] . Всё дело в том, что на ранних стадиях симптомы рака похожи на симптомы гастрита или язвы желудка. При таких проявлениях пациентам не хочется срочно делать гастроскопию. Вместо этого они идут в аптеку и покупают лекарства, после приёма которых жалобы на время стихают, однако опухоль продолжает расти. Поэтому чаще всего при аденокарциноме желудка прогноз неблагоприятный.
У пациентов, которым полностью удалили опухоль, более благоприятный прогноз:
- при первой стадии рака пятилетняя выживаемость отмечается у 80–90 % пациентов;
- при второй стадии рака — у 50–60 % пациентов;
- при третьей стадии рака — у 10–30 % пациентов [13][14] .
Пятилетняя выживаемость — это условный срок. Именно в это время зачастую развиваются рецидивы. Если в течение пяти лет после лечения опухоль не развилась повторно, то прогноз можно считать благоприятным.
Профилактика аденокарциномы желудка
Чт обы предотвратить развитие аденокарциномы, необходимо:
- правильно питаться: меньше употреблять солёных, копчёных и вяленых продуктов, больше — сезонных овощей и фруктов;
- избавиться от вредных привычек: алкоголя и курения;
- при наличии факторов риска регулярно проходить скрининг — 1 раз в год делать ФГДС;
- при появлении жалоб как можно скорее обращаться к врачу и лечить хронические заболевания желудка.
После 45–50 лет профилактически обследовать желудок нужно абсолютно всем: статистически доказано, что с возрастом риск развития аденокарциномы желудка увеличивается [15] .
Опухоли желудка – полиморфная группа новообразований, поражающих все слои желудка, имеющих различную степень пролиферативной активности и влияния на здоровье и жизнь пациента. К основным признакам онкопатологии желудка относят слабость, исхудание, дискомфорт пищеварения, потерю аппетита, анемию, депрессию и утрату интереса к жизни. Для выявления опухолей используют рентгенологические и эндоскопические методики, УЗИ, КТ и МРТ органов брюшной полости. Лечение данной патологии в основном хирургическое, при выявлении злокачественного новообразования терапия комбинированная, включает также лучевую и полихимиотерапию.

Общие сведения
Опухоли желудка могут отличаться характером опухолевого роста, происхождением, степенью дифференцировки. Среди всех новообразований желудка доброкачественные опухоли встречаются не более чем в 4% случаев, подавляющее большинство из них – полипы желудка. Среди злокачественных опухолей чаще всего выявляют рак желудка; другие виды злокачественных новообразований составляют не более 5%.
Соотношение мужчин и женщин среди пациентов с онкопатологией желудка 3:2. Возрастная планка смещена в сторону пожилых людей: более двух третей - пациенты старше 50 лет. В последние годы заболеваемость раком желудка значительно снизилась, и гастроэнтерологи связывают это со своевременным выявлением и эрадикацией хеликобактерной инфекции. Известно, что именно H.pylori принадлежит ведущая роль в формировании язвенной болезни желудка и ДПК, а длительно существующая язва способна малигнизироваться и приводить к развитию рака желудка.
Классификация опухолей желудка
По степени дифференцировки опухоли желудка делятся на доброкачественные и злокачественные. Дальнейшее разделение внутри этих групп осуществляется по типу ткани, из которой происходит данное опухолевое образование. Среди доброкачественных гастральных опухолей большая часть представлена полипами – железистыми новообразованиями, растущими в просвет желудка, имеющими округлую форму, тонкую ножку или широкое основание. По количественному критерию выделяют одиночный полип, множественные полипы, полипоз желудка (наследственное заболевание, характеризующееся поражением слизистой оболочки органов ЖКТ).
По строению полипы бывают аденоматозные (происходят из железистого эпителия желудка, в 20% случаев трансформируются в рак, особенно при размерах полипа более 15 мм); гиперпластические (развиваются на фоне атрофического гастрита, составляют более 80% всех полипов, очень редко малигнизируются); воспалительно-соединительнотканные (инфильтрированы эозинофилами, не являются истинными опухолями, но внешне очень напоминают онкологический процесс). Отдельно выделяют болезнь Менетрие – предраковое состояние, которое описывается как полиаденоматозный гастрит. Доброкачественные опухоли желудка могут происходить из различных тканей: мышечной (лейомиома), подслизистого слоя (липома), сосудов (ангиома), нервных волокон (невринома), соединительной ткани (фиброма) и др.
Большинство злокачественных опухолей желудка (более 95% случаев) представлены аденокарциномой (рак желудка эпителиального происхождения). Среди других опухолей выделяют карциноид (имеет нейроэндокринный генез, опухоль способна продуцировать гормоны), лейомиобластому (содержит в себе клетки, напоминающие как эпителиоидные, так и гладкомышечные), лейомиосаркому (состоит из трансформировавшихся гладкомышечных клеток), злокачественную лимфому (происходит из переродившейся лимфоидной ткани). Реже могут выявляться такие опухоли желудка, как фибропластическая и ангиопластическая саркома, ретиносаркома, злокачественная невринома.
Причины опухолей желудка
На сегодняшний день еще не выявлены точные причины трансформации нормальных тканей в опухоль желудка. Однако в гастроэнтерологии выделены основные предрасполагающие факторы и состояния, которые с большой вероятностью приводят к формированию онкопатологии.
Предрасполагающие факторы в основе своей одинаковы как для злокачественных, так и для доброкачественных новообразований. К ним относят хроническую хеликобактерную инфекцию, атрофический гастрит, генетическую предрасположенность (наличие онкопатологии желудка у родственников, выявление гена ИЛ-1), неправильное питание, курение и алкоголизм, проживание в зоне экологического бедствия, иммуносупрессию. К злокачественной трансформации также предрасполагает наличие полипов желудка (аденоматозных), резекция части желудка, злокачественная анемия, болезнь Менетрие.
Симптомы опухолей желудка
Доброкачественные опухоли желудка чаще всего никак не проявляются и обнаруживаются случайно во время обследования по поводу другой патологии. Полипы больших размеров могут манифестировать ноющей болью в эпигастральной области после приема пищи; тошнотой и рвотой с прожилками крови; изжогой и отрыжкой; слабостью; головокружениями (на фоне анемии, желудочного кровотечения); частой сменой запоров и поносов. Симптомы лейомиом появляются в случае некроза опухолевого узла и внутреннего кровотечения. В этой ситуации пациента беспокоят слабость, бледность, головокружения.
Признаки злокачественных опухолей желудка могут возникнуть как на фоне полного здоровья, так и сопровождать симптоматику язвенной болезни, хронического гастрита. На ранних стадиях рака желудка пациент отмечает снижение аппетита, боли и чувство перенаполнения желудка после еды, прогрессирующее исхудание, извращение вкуса и отказ от некоторых продуктов из-за этого. На поздних стадиях болезни развивается раковая интоксикация; отмечается усиление болей в животе на фоне прорастания опухолью соседних органов; рвота пищей, съеденной накануне; мелена (стул с измененной кровью); увеличение регионарных лимфоузлов.
К осложнениям доброкачественного онкопроцесса относят малигнизацию; прорастание опухолью стенки желудка с перфорацией и развитием перитонита; перекрытие просвета желудка опухолевым конгломератом с нарушением пассажа пищевого комка; изъязвление опухоли с распадом и кровотечением из опухолевого узла; миграцию полипа на ножке в двенадцатиперстную кишку с ущемлением и некрозом полипа.
Злокачественные опухоли желудка также осложняются сужением полости желудка, изъязвлением и кровотечением, перфорацией желудка. Кроме того, для злокачественных опухолей характерны метастазирование, быстрое исхудание с развитием раковой кахексии.
Диагностика опухолей желудка
В прежние годы основным методом диагностики опухоли желудка являлась рентгенография, однако сегодня на первый план выходят эндоскопические исследования. Тем не менее, нельзя отрицать информативность и широкие возможности рентгенографии – в некоторых клиниках она до сих пор остается главной диагностической методикой.
Обзорная рентгенография органов брюшной полости позволяет заподозрить опухоль благодаря деформации контуров желудка, смещению соседних органов. Для более точной диагностики используются контрастные исследования (рентгенография желудка с двойным контрастированием) – во время такого исследования выявляются различные дефекты заполнения, свидетельствующие о наличии растущей в полость органа опухоли, либо дефекты слизистой оболочки, указывающие на озлокачествление и распад новообразования.
Консультация врача-эндоскописта нужна для визуализации опухолевого процесса и назначения эзофагогастродуоденоскопии и эндоскопической биопсии. Проведение морфологического исследования позволяет установить правильный диагноз и начать своевременное лечение в 95% случаев. Для уточнения распространенности опухолевого конгломерата, степени задействованности окружающих органов и наличия метастазов возможно проведение УЗИ, КТ и МСКТ органов брюшной полости. Клинические и биохимические анализы дают возможность оценить общее состояние пациента, степень опухолевой интоксикации.

Лечение опухолей желудка
Тактика в отношении лечения доброкачественных и злокачественных опухолей желудка несколько отличается. Удаление доброкачественных опухолей желудка обычно осуществляется хирургическим путем. В отношении полипов желудка гастроэнтерологи могут занимать выжидательную тактику, хотя чаще принимается решение об удалении полипов желудка при ЭГДС с одновременным проведением интраоперационного гистологического исследования.
Выяснение морфологических характеристик удаленной доброкачественной опухоли позволяет принять решение – произвести резекцию только полипа или также прилегающей слизистой. Если во время эндоскопического исследования выявляется тотальный полипоз желудка, производится гастрэктомия. После удаления доброкачественной опухоли назначается курс лечения ингибиторами протонной помпы, антихеликобактерными препаратами.
Лечение злокачественных новообразований желудка обычно комплексное, включает оперативное вмешательство, лучевую и полихимиотерапию. На сегодняшний день наиболее эффективным методом терапии считается операция. Объем оперативного вмешательства зависит от многих факторов: типа и размеров опухоли, распространенности онкологического процесса, наличия и количества метастазов, вовлечения окружающих органов, общего состояния пациента.
При наличии злокачественного новообразования может выполняться радикальная операция либо же паллиативное вмешательство. Радикальная операция подразумевает под собой удаление опухоли, тотальную гастрэктомию, резекцию сальника (оментэктомию) и вовлеченных в процесс окружающих органов, лимфоузлов. Паллиативные операции направлены на облегчение общего состояния и обеспечение энтерального питания пациента. В комплекс лечения злокачественных новообразований обычно включают лучевую, химиотерапию для достижения наилучшего результата, предупреждения рецидивов опухоли.
Прогноз при опухолях желудка
Прогноз при выявлении доброкачественных новообразований благоприятный; однако, поскольку эти опухоли склонны к рецидивированию, пациенты находятся на диспансерном наблюдении в течение всей жизни. Установление злокачественного характера опухоли значительно ухудшает прогноз. Шансы на выздоровление намного выше при своевременной диагностике и начале лечения злокачественной опухоли. При выявлении метастазов, прорастании соседних органов прогноз для жизни значительно ухудшается.
Профилактика
Специфической профилактики опухолей желудка не существует. Для предупреждения формирования онкопроцесса следует исключить провоцирующие факторы: наладить режим питания, отказаться от вредных привычек, своевременно выявлять и лечить воспалительные заболевания желудка, регулярно проходить эндоскопическое обследование при наличии семейной предрасположенности к онкопатологии. По достижении 50-летнего возраста следует ежегодно проходить обследование у гастроэнтеролога.
Полипы желудка - доброкачественные опухолевидные выросты железистой структуры, исходящие из слизистой оболочки желудка. Полипы желудка развиваются бессимптомно, однако при достижении больших размеров могут провоцировать желудочные кровотечения, схваткообразные боли в животе, затруднение эвакуации пищи из желудка; возможна малигнизация полипов. Основу диагностики составляет фиброгастроскопия и эндоскопическая биопсия, рентгеноскопия желудка. Тактика в отношении полипов желудка может быть выжидательной (динамическое наблюдение и контроль) или активной хирургической (удаление полипов во время эндоскопии или полостной операции).



Общие сведения
Полипы желудка – опухолевые эпителиальные образования, имеющие доброкачественный характер, появляющиеся на внутренней стенке желудка. Это весьма распространенное заболевание в гастроэнтерологии, зачастую не проявляющее себя клинически и обнаруживающееся при проводимой фиброгастроскопии по поводу другой патологии. Как правило, полипы желудка характерны для пациентов среднего возраста (40-50 лет), но могут встречаться и у более молодых людей и детей. Чаще (более чем в 2 раза) полипы желудка развиваются у мужчин. В большинстве наблюдений полипы желудка располагаются в привратниковом отделе желудка, реже – в теле желудка. Одиночные полипы обнаруживаются в 47% случаев, множественные — в 52%; примерно у 1-2% больных наблюдается диффузный полипоз желудка.

Причины и классификация полипов желудка
Факторы, способствующие возникновению полипов желудка: возраст старше 40 лет; хеликобактерная инфекция (полипы часто развиваются на фоне гастритов); генетическая предрасположенность (характерна для аденоматозного полипа – заболевания, при котором полипы завиваются преимущественно в толстом кишечнике, но могут обнаруживаться и в других отделах пищеварительного тракта).

Полипы желудка делятся по морфологическим признакам на аденоматозные и гиперпластические.
Гиперпластические полипы встречаются практически в 16 раз чаще, представляют собой разрастание клеток эпителия желудка и не являются истинной опухолью. В силу своей морфологической структуры гиперпластические полипы почти никогда не озлокачествляются.
Аденоматозные полипы формируются из железистых клеток и представляют собой доброкачественные опухоли желудка с высоким риском перерождения в рак желудка (особенно это касается крупных образования, размером более двух сантиметров).
Аденоматозные полипы (аденомы желудка) в свою очередь подразделяются по гистологической структуре на тубулярные, папиллярные и папиллотубулярные опухоли (в зависимости от преобладания в опухолевой ткани трубчатых железистых, либо сосочковых структур). Помимо морфологических особенностей полипы классифицируются по количеству (одиночные и множественные) и по размеру.
Симптомы полипов желудка
Маленькие и молодые полипы, как правило, не проявляются клинически, либо отмечается симптоматика гастрита, на фоне которого развиваются полипы.
Образования крупные могут осложнятся желудочным кровотечением (и тогда обнаруживается кровь в кале – дегтеобразный стул, или рвота с кровью). Большие размеры полипа могут стать причиной затруднения проходимости желудка. Полипы на ножке могут выходить через привратник в двенадцатиперстную кишку и защемляться, вызывая острые схваткообразные боли под грудиной, иррадиирующие по всему животу.
Полипы могут способствовать развитию следующих осложнений: формирование язв и внутреннее кровотечение, затруднение эвакуации пищи из желудка в двенадцатиперстную кишку вплоть до желудочной непроходимости, ущемление полипа привратником (для полипов на длинной тонкой ножке), озлокачествление (для аденоматозных полипов).
Диагностика полипов желудка

Чаще всего полипы обнаруживают при эндоскопическом или рентгенологическом исследовании по поводу гастрита. Специфической симптоматики больные не отмечают, как правило, полипы сопровождаются хроническим воспалением слизистой желудка, поэтому на первый план выходят проявления гастрита.
Наиболее информативной методикой диагностики является гастроскопия – эндоскопическое исследование, позволяющее детально осмотреть слизистую желудка, выявить образования, оценить их размер и произвести забор биоптата для гистологического анализа. Рентгенологическое исследование желудка с контрастным веществом позволяет очертить рельеф стенок желудка и выявить наличие полипов.
Среди мер лабораторной диагностики отсутствуют специфические способы для выявления полипов желудка, но при подозрении на развитие кровотечения из полипа могут проводить исследование кала на скрытую кровь. При частых кровотечениях в общем анализе крови могут отмечать признаки анемии. Для выявления хеликобактерной инфекции проводят ПЦР-исследование и выявление антител методом ИФА.
Лечение полипов желудка

Необходимо соблюдать рекомендации и назначения гастроэнтеролога. В зависимости от размеров, количества, морфологических особенностей полипов, врач определяет лечебные мероприятия, но в любом случае оптимальной мерой лечения является удаление полипов. Небольшие полипы можно удалить при эндоскопии. Крупные полипы и образования, имеющие широкое основание требуют более серьезного хирургического вмешательства.
Иногда при гиперпластических полипах небольшого размера врач может предложить выжидательную тактику – диетическое питание и диспансерное наблюдение с регулярным обследованием (фиброгастроскопическим исследованием) желудка не менее одного-двух раз в год. Врач отмечает динамику роста полипов, характер изменения их поверхности (формирование неровностей, эрозий, изъязвлений, кровоточивость), образование новых разрастаний. Резкое ускорение роста и изменение поверхности полипа могут быть признаками его озлокачествления.
В случае развития осложнений ставится вопрос о хирургическом или, при возможности, эндоскопическом удалении полипа. После удаления полипа больные также должны проходить регулярной обследование на предмет вероятности повторного возникновения полипов.
Пациентам после эндоскопического удаления полипов (электроэксцизия или электрокоагуляция) необходимо произвести контрольную эндоскопию через 10-12 недель для уточнения полноты очистки стенок желудка от полипов. Иногда проводят доудаление остатков полипа. Окончательное заживление дефектов слизистой, образовавшихся в результате эндоскопического удаления полипов, происходит в срок от двух до восьми недель.
Стоит помнить: при регулярном эндоскопическом контроле слизистой желудка с частыми биопсиями рост полипа может ускоряться. Также эндоскопия способствует распространению злокачественного образования, склонного к метастазированию.
Резекцию желудка проводят в случае крупных полипов, множественных, часто рецидивирующих полипов, образований, осложненных массированным кровотечением, некрозом, защемлением, непроходимостью желудка, озлокачествлении (малигнизации) полипа. Специфической медикаментозной терапии полипов желудка нет, но поскольку это заболевание часто протекает на фоне гастрита, то препараты назначают в соответствии с принципами лечения этого заболевания.
Профилактика полипов желудка
Современная медицина не выделяет специфических мер по профилактике полипов желудка. Профилактические меры в основном должны быть направлены на предупреждение возникновения гастрита (либо своевременное и адекватное его лечение), поскольку именно хронический гастрит является основным фактором, способствующим возникновению и развитию полипов желудка.
Для предупреждения заболеваний желудка основными мерами являются: рациональное питание с соблюдением режима, ограничение курения и приема алкоголя, контроль над принимаемыми медикаментами (осторожное употребление гастротоксичных препаратов, в частности, обезболивающих и жаропонижающих из группы нестероидных противовоспалительных средств).
Пациентам, у которых выявлены полипы желудка, необходимо придерживаться диетического питания с исключением продуктов, раздражающих слизистую желудка (острое, соленое, кислое, жареное, копченое), а также пищи, способствующей усилению секреции соляной кислоты. От алкоголя и курения желательно полностью отказаться: алкоголь оказывает прямое повреждающее действие на слизистую, что может привести к эрозированию и изъязвлению полипа. Курение также негативно влияет на состояние стенки желудка, снижая ее защитные свойства и способствуя увеличению выработки соляной кислоты.
Препараты группы нестероидных противовоспалительных средств больным с полипами желудка противопоказаны.
Прогноз при полипах желудка
При удалении полипов прогноз благоприятен. Единственно, высока вероятность повторного возникновения, но регулярное диспансерное наблюдение позволяет выявить рецидив быстро и провести удаление новых образований на ранней стадии малоинвазивными методами. После удаления полипов восстановление трудоспособности происходит, как правило, в полном объеме. Продолжительное течение заболевания может вести к раку желудка.
Читайте также:

