Выращивают ли в ожогов
Обновлено: 30.04.2024
Категории МКБ: Последующая помощь с применением восстановительной хирургии неуточненная (Z42.9), Термический ожог 50-59% поверхности тела (T31.5), Термический ожог 60-69% поверхности тела (T31.6), Термический ожог 70-79% поверхности тела (T31.7), Термический ожог 80-89% поверхности тела (T31.8), Термический ожог 90% поверхности тела или более (T31.9)
Общая информация
Краткое описание
Приложение к приказу
Министерства здравоохранения
Республики Беларусь
24.03.2011 №293
КЛИНИЧЕСКИЙ ПРОТОКОЛ
лечения глубоких ожогов кожи методом трансплантации аутологичной (собственной, аутокожи) или донорской: консервированной кадаверной
кожи (аллокожи)
1. Кожа - самый большой орган человеческого тела и занимает около 1,6-2,2 м поверхности. Потеря значительной части кожного покрова может быть несовместимой с жизнью. Поэтому, восстановление утраченного кожного покрова является основной задачей в лечении больных с глубокими ожогами. Все другие мероприятия в комплексе общего и местного лечения направлены на подготовку к трансплантации кожи.
2. Возрастная категория: детское и взрослое население.
3. Основным юридическим документом, регламентирующим трансплантацию кожи, является Закон Республики Беларусь от 4 марта 1997 года «О трансплантации органов и тканей человека» (Ведамасщ Нацыянальнага сходу Рэспублта Беларусь, 1997 г., №9, ст.196) в новой редакции «Изменения и дополнения: Закон Республики Беларусь от 9 января 2007 г. №207-3 (Национальный реестр правовых актов Республики Беларусь, 2007 г., №15, 2/1304).
4. Выделяют 3 основных вида трансплантации кожи:
аутологичная трансплантация - трансплантация собственной кожи (далее - аутокожи);
аллогенная трансплантация - трансплантация консервированной кадаверной кожи, лиофилизированной свиной кожи (далее — аллокожи).
Выбор вида трансплантации кожи определяется конкретной клинической ситуацией.
5. Трансплантация аутокожи выполняется для восстановления кожного покрова после удаления некротического струпа и подготовки ран при ожогах ШБ - IV степени, а так же при ранах другой этиологии - после травм и гнойно-некротических процессов.
6. Трансплантация аллокожи применяется для временного закрытия ожогов ША - ШБ - IV степени после удаления ожогового струпа, ран травматического и послеоперационного происхождения, дефектов кожи после гнойно-некротических процессов, в том числе, и при дефиците собственных донорских ресурсов.
7. Трансплантация кожи на площади 5% и более поверхности тела одномоментно проводится только в специализированных отделениях.
8. Заготовка, консервация, стерилизация, лабораторный контроль качества, замораживание и хранение аллокожи производится отделом биотрансплантатов Государственной службы медицинских судебных экспертиз.
9. Консервированная аллокожа выдается по заявкам специализированных ожоговых отделений организаций здравоохранения из банка тканей отдела биотрансплантатов Г осударственной службы медицинских судебных экспертиз в стерильных герметичных пластиковых пакетах, с этикеткой на каждом пакете, с указанием номера донора, даты заготовки, толщины и площади трансплантатов.
10. Пакеты с консервированной замороженной аллокожей доставляются из отдела биотрансплантатов Государственной службы медицинских судебных экспертиз в организации здравоохранения в изотермических контейнерах не позднее одних суток до применения, хранятся в морозильных камерах бытовых холодильников.
Лечение
ПОКАЗАНИЯ К ТРАНСПЛАНТАЦИИ
АУТОКОЖИ, АЛЛОКОЖИ
11. Показаниями к трансплантации аутокожи являются:
ожоги ШБ - IV степени любой площади;
раны другой этиологии: после оперативных вмешательств, травм, гнойно-воспалительных процессов, трофические язвы.
12. Показаниями к применению трансплантации аллокожи при лечении ожогов являются:
12.1. ожоги ШБ - IV степени на площади более 10% поверхности тела при невозможности одномоментной аутотрансплантации кожи в связи с обильным кровотечением во время некрэктомии или невозможности радикальной некрэктомии.
12.2. дефицит собственных донорских ресурсов кожи;
12.3. невозможность одномоментно с некрэктомией выполнить аутотрансплантацию кожи в связи с тяжестью состояния больного;
12.4. как временное покрытие между этапами трансплантации аутокожи;
12.5. при ожогах III А степени после тангенциальных некрэктомий для ускорения эпителизации ожоговых ран;
12.6. во время подготовки гранулирующих ран к аутотрансплантации кожи у больных с вялотекущим раневым процессом со сменой аллотрансплантатов на перевязках по мере необходимости.
ПОДГОТОВКА РАН К ТРАНСПЛАНТАЦИИ КОЖИ
13. Общее состояние, возраст пострадавшего, обширность поражения и локализация ожогов, наличие донорских ресурсов кожи и состояние воспринимающего ложа имеют решающее значение при установлении сроков проведение оперативного вмешательства и способа восстановления кожного покрова.
14. Трансплантация кожи должна проводиться на раны без наличия очагов некроза и гнойного отделяемого. Это достигается проведением радикальной некрэктомии и последующим лечением и подготовкой ран.
15. Предоперационное обследование пациентов проводится в соответствии с клиническим протоколом диагностики, лечения и медицинской реабилитации пациентов с термическими поражениями и их последствиями (примечания в конце текста).
16. Проведение подготовки ран к трансплантации кожи - хирургической некрэктомии возможно при отсутствии противопоказаний. Противопоказаниями к проведению некрэктомии являются:
16.1. наличие признаков шока - гипотензия и тахикардия (с учетом возрастных норм артериального давления и частоты сердечных сокращений), анурия либо олигоурия, гипотермия, гемоконцентрация;
16.2. синдром диссеминированного внутрисосудистого свертывания крови в переходной и гипокоагуляционной стадиях (фибриноген менее 3 г/л или более 7 г/л, протромбин менее 70% или более 120%, тромбиновое время более 16 сек, антитромбин-Ш - менее 75%, АЧТВ более 37 сек);
16.3. тромбоцитопения менее 120х10 9 /л;
16.4. анемия менее 110 г/л.
17. Общая подготовка пациента к операции включает:
17.1. анальгезию и антибактериальную терапию при наличии показаний и в соответствии с клиническим протоколом диагностики, лечения и медицинской реабилитации пациентов с термическими поражениями и их последствиями (приложение 1 к приказу М3 РБ №781 от 07.08.2009);
17.2. коррекцию анемии, гемостаза, и водно-электролитного баланса - трансфузия эритроцитной массы, свежезамороженной плазмы, криопреципитата, концентрата тромбоцитов, переливание водно-электролитных растворов в необходимом количестве до достижения следующих параметров системы крови и гемостаза:
17.3. нутритивную поддержку:
энтерально, включая расширение лечебных столов дополнительным питанием до необходимого калоража; применение, при наличии показаний, питательных смесей для ожоговых больных; использование зондового питания при невозможности обеспечения приема пищи или достижения необходимого суточного калоража естественным путем;
парентерально, при наличии показаний, с учетом возрастной потребности, под контролем гликемии и потерь азота с мочой, с использованием концентрированных растворов глюкозы, растворов аминокислот, жировых эмульсий, комбинированных препаратов для парентерального питания, витаминов и микроэлементов;
17.4. комплексную терапию, направленную на устранение тканевой гипоксии и восстановление микроциркуляции в ране и окружающих тканях, включающую, при наличии показаний, применение низко- и среднемолекулярных декстранов, дезаггрегантов (учитывая возможное негативное воздействие антитромбоцитарных препаратов), гипербарическую оксигенацию.
18. При невозможности выполнения одномоментного с некрэктомией закрытия ран путем несвободной кожной пластики или трансплантации кожи проводится подготовка гранулирующих ран до появления всех доступных для оценки критериев готовности ран к трансплантации кожи. Клиническими критериями готовности гранулирующих ран к трансплантации кожи являются:
отсутствие некротических тканей на участке раны, подготовленной к трансплантации;
отсутствие выраженной экссудации - раневое отделяемое (гнойный экссудат) только на повязке;
грануляции макроскопически равномерные, мелкозернистые (отпечаток марлевой сетки на поверхности грануляционной ткани), розовые или красные, без выраженной кровоточивости;
выраженная адгезивность гранулирующих ран (прилипание к грануляциям сухого марлевого шарика);
наличие активной краевой эпителизации.
19. В процессе подготовки гранулирующих ран к трансплантации кожи проводится местная терапия в виде:
повязочного метода ведения ран с использованием растворов антисептиков, антибактериальных мазей на водорастворимой основе, кремов сульфаниламидных производных серебра, раневых покрытий. Применение того или иного антибактериального препарата производится под контролем бактериологического исследования ран с определением качественного и количественного состава микрофлоры с антибиотикограммой;
аппаратного воздействия на рану с использованием эффекта ультразвуковой кавитации и гидрохирургических систем при необходимости под общей или регионарной анестезией.
20. Перед проведением первого этапа подготовки ран к трансплантации кожи - хирургической некрэктомии необходимо:
определить сроки и объем операции (максимально допустимую в текущий момент площадь иссечения);
выбрать метод проведения некрэктомии; прогнозировать предполагаемую кровопотерю; избрать необходимые методы гемостаза;
подготовить достаточное количество трансфузионных сред для восполнения кровопотери и коррекции гемостаза;
избрать методы закрытия образовавшихся раневых дефектов в зависимости от их локализации, площади и глубины.
Предполагаемый план операции изложить в медицинской карте стационарного больного.
21. Для предотвращения интраоперационной гипотермии пациента необходимо применение систем обогрева тела пациента и инфузионных сред.
22. Некрэктомия может сопровождатся значительной кровопотерей. При ее выполнении во второй или третьей стадиях ДВС- синдрома и при тромбоцитопении величина кровопотери может достигать критических величин и являться причиной гибели пациента интраоперационно или в раннем послеоперационном периоде. С целью уменьшения объема кровопотери необходимо:
в предоперационном периоде непосредственно перед оперативным вмешательством кроме планового рассчитанного объема инфузионной терапии дополнительно провести инфузию изотонического электролитного раствора в необходимом объеме (учитывая возрастные ограничения и состояние гемодинамики) с целью гемодилюции;
выполнять некрэктомию на конечности под жгутом;
производить инфильтрацию мягких тканей в области вмешательства 0,9% раствором хлорида натрия с добавлением эпинефрина в концентрации 1 : 200 000;
при выполнении иссечения осуществлять гемостаз аппаратными методами, не допускающими образования значительного по глубине и площади коагуляционного некроза, в связи с невозможностью последующей трансплантации кожи на вновь образовавшийся коагуляционный некроз;
после иссечения остановку капиллярного кровотечения из раны осуществлять аппликацией на источник кровотечения салфеток с эпинефрином разведенным на 0,9% растворе хлорида натрия в концентрации 1 : 100 000, гемостатических препаратов и покрытий.
23. Для восполнения кровопотери наряду с инфузией растворов электролитов и синтетических коллоидов проводится трансфузия эритроцитной массы и свежезамороженной плазмы. Объем трансфузии зависит от обширности некрэктомии и величины кровопотери. Задачей восполнения кровопотери является достижение параметров системы крови и гемостаза указанных в пункте 17.2 настоящего протокола.
ТЕХНИЧЕСКОЕ ВЫПОЛНЕНИЕ ТРАНСПЛАНТАЦИИ АУТОКОЖИ
И АЛЛОКОЖИ НА РАНЫ
24. Выполнение трансплантации кожи возможно при наличии определенных условий:
25. Трансплантация аутокожи и аллокожи на раны выполняется в условиях операционной, под анестезией, метод которой определяется конкретной клинической ситуацией.
26. Для предотвращения интраоперационной гипотермии пациента необходимо применение систем обогрева тела пациента и инфузионных сред.
27. Забор аутотрансплантатов осуществляется с предварительно обработанных согласно общехирургических правил, неповрежденных или эпителизировавшихся участков кожных покровов, дерматомами с толщиной трансплантата 0,2 - 0,7 мм. Общая площадь трансплантатов должна соответствовать площади раневого дефекта подлежащего закрытию при данной операции с учетом возможностей экспансивной пластики сетчатыми трансплантатами.
28. Для уменьшения кровопотери с донорских ран при заборе трансплантатов большой площади (5 и более процентов поверхности тела) необходимо, перед срезанием кожных трансплантатов, производить инфильтрацию мягких тканей в области вмешательства 0,9% раствором хлорида натрия с добавлением эпинефрина в концентрации 1 : 200 000;
29. При аутотрансплантации на косметически и функционально важных (лицо, шея, кисти, крупные суставы, опорные поверхности стоп) областях трансплантация производится цельным неперфорированным расщепленным трансплантатом. Исключением является дефицит донорских ресурсов и тяжесть состояния пациента.
30. Донорские раны после забора аутотрансплантатов закрываются сухими асептическими повязками с целью дальнейшего ведения ран сухим полуоткрытым методом, либо повязками с антисептическими мазями или кремами, либо раневыми покрытиями, предназначенными для лечения донорских ран.
31. Размораживание аллотрансплантатов производится за 60 минут до трансплантации путем помещения пакетов на полку холодильника при температуре +4 - +8°С на 30 минут. Далее пакеты с аллотрансплантатами доставляются в операционную, вскрываются с соблюдением правил асептики. Трансплантаты извлекаются из пакетов, помещаются в стерильный сосуд и заливаются стерильным 0,9% раствором хлорида натрия комнатной температуры (+22 - +26°С) на 30 минут. При этом через 15-20 минут однократно производится замена 0,9% раствора хлорида натрия на новый раствор; размороженные аллотрансплантаты извлекаются из 0,9% раствора хлорида натрия, распластываются на стерильном столике, удаляется избыток 0,9% раствора хлорида натрия путем промокания стерильными салфетками.
32. Раны перед трансплантацией промываются растворами антисептиков, просушиваются сухими стерильными салфетками.
33. Кожные трансплантаты могут быть использованы цельными, перфорированными скальпелем для создания дренажных отверстий, сетчатыми с коэффициентом перфорации 1:1,5 - 1:2—1:3 и более (полученными при нанесении на кожный трансплантат упорядоченных отверстий с помощью аппарата для перфорации кожных трансплантатов).
34. Кожные трансплантаты свободно укладываются на подготовленные раневые поверхности, при необходимости фиксируются к краям, дну ран и между собой швами, скобами хирургического степлера.
35. Поверх трансплантатов укладываются тугие стерильные влажно-высыхающие повязки с растворами антисептиков и/или атравматические раневые покрытия с последующей фиксацией марлевыми и бинтовыми повязками.
36. После операции пациент доставляется в палату ожогового (хирургического или травматологического) отделения или (в случае тяжелого общего состояния пациента) в отделение реанимации.
ВЕДЕНИЕ ПОСЛЕОПЕРАЦИОННОГО ПЕРИОДА
37. В послеоперационном периоде пациенту проводится терапия и лабораторный мониторинг в соответствии с клиническим протоколом диагностики, лечения и медицинской реабилитации пациентов с термическими поражениями и их последствиями (приложение 1 к приказу М3 РБ №781 от 07.08.2009).
38. Нутритивная поддержка в послеоперационном периоде является важной составляющей лечения. Взрослый пациент должен получить не менее 50-60 ккал/кг массы тела, дети не менее 100 ккал/кг.
39. Для профилактики отторжения трансплантатов используются глюкокортикостероиды местно в виде аэрозоля или раствора нанесенного на повязки. При выполнении трансплантации кожи на площади 10% поверхности тела и более допустимо применение глюкокортикостероидов парентерально и/или энтерально в начальной дозе 1 мг/кг в сутки с последующим снижением до полной отмены.
40. При наличии показаний выполняется иммобилизация оперированного сегмента тела необходимым способом.
41. Сроки проведения первой и последующих перевязок индивидуальны и определяются совокупностью клинических и лабораторных данных о состоянии пациента и течении раневого процесса. При необходимости перевязка проводится в операционной или перевязочной под общей анестезией.
42. После аллотрансплантации кожи в процессе перевязок, по мере отторжения, трансплантаты удаляются, при необходимости проводится повторная аллотрансплантация, а при готовности ран и устранении дефицита донорских ресурсов выполняется аутотрансплантация кожи.
Примечание: Приложение 1 «Клинический протокол диагностики, лечения и медицинской реабилитации пациентов с термическими поражениями и их последствиями» к приказу Министерства здравоохранения Республики Беларусь от 07.08.2009 г. №781 «Об утверждении некоторых клинических протоколов».
Приказ Министерства здравоохранения Республики Беларусь от 27.01.2011 г. №69 «О внесении дополнения в приказ Министерства здравоохранения Республики Беларусь от 7 августа 2009 г. №781»
ОЖОГ (combustio) - специфическое повреждение тканей и органов, вызванное воздействием термической, химической, электрической или лучевой энергии.
Этиология. По физической природе термические агенты можно разделить на твердые, жидкие и газообразные. По виду взаимодействия с тканями пострадавшего выделяют контактные поражения (при непосредственном взаимодействии с тканями пострадавшего: пламя, горячие жидкости и т. д. ) и дистантные (без непосредственного контакта: ультрафиолетовое, инфракрасное, тепловое излучение) поражения.
Патогенез местных изменений при ожогах кожи.
Температурный оптимум для активности многих биологически важных ферментов соответствует 36-37˚С, интервал температур от 37 до 41˚С для кожи является приемлемым, дальнейшее нагревание приводит к повреждению клеток. Продолжительность существования тканевой гипертермии многократно превосходит время действия самого термического агента.
При воздействии высоких температур на поверхности тела образуются ожоги различных степеней. При перегревании тканей свыше 520С коагуляционное свертывание белков невосстановимо. Последствия ожогов зависят от размеров и глубины повреждения тканей.
Различают 3 концентрические зоны поражения при глубоких ожогах в зависимости от степени нарушения кровообращения. Центральная область раны, наиболее тесно соприкасающаяся с источником тепла, носит название зоны коагуляции. Вокруг нее располагается зона паранекроза, названная Jackson D (1953) зоной стаза (ишемическая средняя зона) и эритемная периферическая зона. При микроскопии визуализируется сосудистый тромбоз в средней и периферической зонах.
Интенсивность нагревания тканей (глубина поражения) зависит от физических характеристик термического агента (низкотемпературные, высокотемпературные), способа теплопередачи (проведение, конвекция, испарение), теплозащитных свойств одежды. Объем поражения кожи зависит не только от фактической температуры, но и от времени ее воздействия, которое удлиняется за счет того, что кожа обладает достаточно высокой теплоемкостью и теплопроводностью. Степень тканевой гипертермии прямо пропорциональна продолжительности нагревания. Краткосрочное воздействие даже очень высоких температур может не приводить к развитию ожогов. Чем выше степень перегрева тканей, тем быстрее происходит гибель клеток.
Классификация. В настоящее время в нашей стране используется классификация, принятая на XXVII Всесоюзном съезде хирургов. Выделяют следующие степени поражения (рис. 20. 1):
1 степень - поверхностный эпидермальный ожог
2 степень - ожог верхнего слоя кожи
3 степень - коагуляция и некроз всего сосочкового слоя или более глубоких слоев кожи.
3А степень - некроз эпителия распространяется на глубину эпителиального слоя до герминативного, но захватывает последний не полностью, а лишь на верхушках сосочков, сохраняются придатки кожи.
3Б степень - некроз распространяется на глубину всего эпителиального слоя и дермы.
4 степень - поражение глубжележащих тканей (подкожной клетчатки, фасций, мышц, сухожилий и костей).
За рубежом широко распространена классификация, выделяющая четыре степени поражения:
- первая степень – соответствует первой степени отечественной классификации;
- вторая поверхностная степень – соответствует II степени отечественной классификации;
- вторая глубокая степень – соответствует IIIа степени;
- третья степень – соответствует IIIб степени;
- четвертая степень – соответствует IV степени.
Клиническая картина.
Для ожоговых повреждений в зависимости от глубины (степени поражения) характерна различные местные клинические проявления (табл. 20. 1).
Ожог 1 степени характеризуются разлитой краснотой, отечностью и выраженной болезненностью кожи, местным повышением ее температуры. Термический агент за счет раздражения сосудистых нервов вызывает интенсивное расширение сосудов. Через несколько дней все проявления проходят, оставляя коричневую пигментацию кожи. Типичным примером ожога 1 степени является ожог солнечными лучами.
При ожоге 2 степени на различной глубине в толще эпидермального слоя образуются пузыри, наполненные прозрачной серозной жидкостью. Содержимым таких пузырей является бесклеточная серозная жидкость с высоким содержанием в ней белков. Заживление происходит за счет регенерации эпителия.
При ожоге 3а степени кожа местами покрыта пузырями, пятнистая, пятна бледного или темного оттенка, иногда даже черные. Нежизнеспособные ткани образуют струп, который отторгается от живых тканей с образованием демаркационной линии. Если в зоне ожога явно выражен отек, то можно рассчитывать на островковую эпителизацию и заживление без пересадки кожи. На месте ожога остаются нежные рубцы.
При ожогах 3б степени кожа поражается на всю толщину с вовлечением поверхностных слоев подкожной клетчатки. Кожа бледно-серого цвета, пятниста, чувствительность ее снижена или отсутствует. При заживлении на месте поражения образуются грубые рубцы.
Для ожогов 4 степени характерно глубокое поражение тканей, нередко их обугливание. Ткани превращаются в почерневшие ломкие массы. Самостоятельное заживление этих ожогов невозможно.
Тяжесть общего состояния больных главным образом зависит от площади обожженной поверхности и степени ожога, выраженность которых в конечном итоге и определяют прогноз заболевания. В первые дни тяжесть течения зависит в основном от площади обожженной поверхности. Глубина поражения сказывается главным образом на дальнейшем течении болезни.
Диагностика
При диагностике глубины поражения необходимо учитывать комплекс данных полученных при сборе анамнеза, осмотре пострадавшего и при проведении диагностических проб.
Анамнез позволяет установить вид и продолжительность воздействия повреждающего агента, факторы изменяющие интенсивность теплового воздействия, наличие сопутствующей патологии.
При осмотре оценивается изменение цвета эпидермиса и дермы, наличие и распространенность отека, наличие пузырей и характер их содержимого, наличие признаков нарушения кровообращения, наличие некроза тканей и его вид.
При физикальном обследование определяется состояние болевой чувствительности: уколы иглой, эпиляционный тест (выдергивание волосков), тесты с красителями.
Определение площади ожога.
Одной из важных составляющих диагноза при термической травме является определение площади поражения. Наиболее удобным является определение площади пораженной поверхности по Уоллесу (A. Wallace 1951г. ) – «правило девяток»: голова и шея - 9%, рука - 9%, нога - 18%, туловище сзади и спереди по 18%, промежность, гениталии - 1% (рис 20. 2).
Другим распространенным способом является «правило ладони». Согласно исследованиям J. Grazer (1997г. ) площадь ладони взрослого человека составляет 0, 78% от общей площади поверхности тела.
Местное лечение ожогов.
В качестве первой помощи при ожогах необходимо немедленно прекратить воздействие поражающего фактора, обеспечить доступ свежего воздуха охладить обожженные участки тела (холодная проточная вода, криопакеты «Comprigel» «Articare» и т. д. ), при обширных повреждениях ввести обезболивающие препараты (анальгин, морфин, омнопон, промедол, морадол), наложить на пораженные поверхности стерильные повязки. Следует отметить, что ключевым моментом оказания первой помощи является быстрое проведение охлаждения обожженной поверхности, правильное проведение которой снижает глубину (степень) ожога на единицу. Адекватно проведенная первая помощь на месте происшествия позволяет снизить риск ожоговой болезни и уменьшить количество осложнений.
Поверхностные ожоги не большой площади адекватно лечатся амбулаторно, поскольку в большинстве случаев, не требуют хирургического лечения. Местно применяются различные мазевые повязки, которые обладают местно охлаждающим действием, защищают раневую поверхность, стимулируют заживление, препятствуют присоединению вторичной инфекции. Наиболее часто используются мази-спреи «Олазоль», «Пантенол».
В последние годы при лечении пограничных ожогов IIIA степени и глубоких ожогов IIIБ-IV степени широко используются различные раневые покрытия, в течение многих лет успешно используется перфорированная свиная кожа - ксенокожа. Последняя помещается на ожоговые раны, обеспечивая их покой и защиту от инфекции, не препятствуя очищению ран и одновременному применению для местного лечения других препаратов.
В настоящее время существует два основных пути подготовки глубоких ожоговых ран к аутодермопластике (табл. 20. 3. ): химическая некрэктомия с отсроченной аутодермопластикой и хирургическая некрэктомия с одномоментной или отсроченной аутодермопластикой. Тактика местного лечения с использованием химической некрэктомии вполне оправдана при обширных глубоких ожогах более 40 % поверхности тела при условии крайне тяжелого общего состояния больных. Особенно при лечении больных пожилого и старческого возраста, у которых тяжелая сопутствующая патология делает оперативные вмешательства в ранние сроки невозможными.
В этих случаях с первых суток после травмы местное лечение должно быть направлено на быстрое формирование сухого ожогового струпа, профилактику инфицирования и углубления ожоговых ран. С этой целью применяют ватно-марлевые повязки с мазями на водорастворимой основе. Это способствует уменьшению потери жидкости с ожоговой поверхности, согреванию больного, формированию сухого струпа, не требует ежедневных перевязок.
В последующие дни формирование сухого ожогового струпа достигается применением влажно-высыхающих повязок. Оптимальными препаратами в этот период также являются 1 % растворы йодопирона или йодовидона, обеспечивающие высушивание струпа и обладающие широким спектром антимикробного и противогрибкового действия. Возможно также использование ватно-марлевых повязок с мазями на водорастворимой основе. Применение мази на жировой основе противопоказано.
Значительно ускоряет формирование сухого струпа лечение больного в условиях абактериальной среды. В этом случае используется открытый метод лечения с обработкой ожоговых ран два-три раза в день 1 % раствором йодопирона, йодовидона или препаратом "Наксол" и применением абактериальных изоляторов или кровати "Клинитрон". Способствует высушиванию струпа инфракрасное облучение ран. Образование сухого струпа уменьшает потери белка с ожоговой поверхности, способствует уменьшению интоксикации, улучшению общего состояния больного.
При глубоких циркулярных ожогах конечностей, когда высок риск сдавления и ишемии глубжележащих тканей формирующимся ожоговым струпом при циркулярных ожогах грудной клетки, ограничивающих еe экскурсию, в ближайшие дни после травмы показано выполнение некротомии.
После образования сухого "мумифицированного" струпа производится химическая некрэктомия с использованием 40 % салициловой мази. Толщина слоя мази должна составлять 1-2 мм. Одновременно применяется не более 200 граммов мази в связи с опасностью отравления салицилатами, уровень которых в крови может превысить допустимую норму. Через 48 часов ожоговый струп бескровно отделяется от подлежащих тканей. С учетом указанного обстоятельства химическую некрэктомию одномоментно можно осуществить на площади до 10-15% поверхности тела.
После очищения ожоговой поверхности от некроза для подготовки раны к аутодермопластике целесообразно применение мазей на водорастворимой основе, содержащих антибактериальные препараты, возможно и чередование с антисептическими растворами. Положительное влияние на раневой процесс оказывают ультрафиолетовое облучение, монохроматический красный свет лазера, низкочастотный ультразвук.
Если площадь глубоких ожогов пострадавших превышает 10-15 % поверхности тела целесообразно в это же время выполнить следующую, этапную химическую некрэктомию и подготовить гранулирующие раны к одномоментной аутодермопластике на площади до 20 % поверхности тела. Выполнение такой операции возможно только с использованием расщепленного перфорированного сетчатого кожного аутолоскута, позволяющего увеличить площадь трансплантата в соотношении 1: 2, 1: 4, 1: 6 и более.
В последние годы все большее число сторонников находит метод хирургического иссечения некротических тканей. Ведущим методом лечения является ранняя хирургическая некрэктомия ожоговых ран - радикальное иссечение всех пораженных тканей до развития воспаления и инфицирования с последующей одномоментной аутодерматопластикой кожных дефектов. Операция выполняется до 5-7 суток с момента травмы непосредственно по выведению больного из шока.
В структуре хирургических методов лечения так же применяются: раннее хирургическое очищение ожоговых ран - заведомо нерадикальное иссечение основного массива некроза с целью уменьшения интоксикации, отсроченная хирургическая некрэктомия - радикальное иссечение всех пораженных тканей при развившемся воспалении и инфицировании (выполняется на 5-14 сутки с момента травмы), поздняя хирургическая обработка раны (в т. ч. хирургическая обработка гранулирующей раны), ампутации и дезартикуляции конечностей и их сегментов.
При ожогах III степени хирургическая некрэктомия производится тангенциально (послойно) специальным инструментом (дерматом, нож Гамби) до появления мелкоточечного кровотечения из непораженного ожогом слоя кожи. При ожогах IV степени хирургическаяи некрэктомия выполняется чаще до фасции скальпелем или электроножом с последующим тщательным гемостазом. Ранняя хирургическая некрэктомия (тангенциальная или фасциальная) с одномоментной аутодермопластикой позволяет при глубоких ожогах IIIБ-IV степени восстановить целостность кожных покровов уже через 3-4 недели после травмы на площади до 20 % поверхности тела.
Следует отметить, что использование современных принципов и методов лечения тяжелой ожоговой травмы, включающих раннюю хирургическую некрэктомию с одновременной последующей аутодерматопластикой (непосредственно после выведения больного из состояния шока), позволяет у большинства пациентов избежать развития всех дальнейших периодов ожоговой болезни, либо уменьшить тяжесть ее проявлений и последствий.
В настоящее время разработан и применяется новый метод активного хирургического лечения обожженных с использованием культивированных аллофибробластов. Суть метода заключается в применении для пластического закрытия ожоговых ран искусственно выращенных в лабораторных условиях аллофибробластов - клеток соединительной ткани, определяющих активность процессов регенерации, в т. ч. эпителизации. Они могут быть получены из кожи донора или трупного материала, при культивировании неприхотливы и полностью утрачивают антигенспецифичность.
Метод предусматривает трансплантацию культивированных фибробластов на обширные ожоговые раны IIIA степени, донорские раны в т. ч. длительно не заживающие, или комбинированную аутодермопластику с использованием культуры фибробластов и сетчатых кожных аутолоскутов, перфорированных в соотношении 1: 6 и 1: 8 при глубоких ожогах IIIБ-IV степени. Операции предшествует выполнение химической или хирургической некрэктомии.
Источник: Н.А.Кузнецов в соавт. Основы клинической хирургии. Практическое руководство. Издание 2-е, переработанное и дополненное. - М.:ГЭОТАР-Медиа, 2009.

Многие из анатомии знают, что кожа выступает как «защитная оболочка» организмов людей и животных. Она состоит из двух частей – эпидермиса (верхняя многослойная поверхность эпителия) и дермы (соединительнотканная часть, которая объединяет эпидермис и мышечные ткани организма). Кожа занимает большую площадь на теле человека. У взрослых людей она достигает 1,5-2,3 м 2 . Её главная задача - в защите тела от широкого спектра внешних воздействий. Клетки кожи, как и органы дыхания, принимают внутрь кислород, которым обогащают свою деятельность в организме. При различных травмоопасных ситуациях (например, ожогах и крупных порезах) человек может лишатся своей «защитной оболочки». На заживление и восстановление кожного покрова требуется большое количество времени. Поэтому, чтобы облегчить этот процесс и помочь коже приобрести здоровый вид, учёными были разработаны варианты искусственной человеческой кожи, которая ускорит заживления на теле.
Построение искусственной кожи выглядит следующим образом – на коллагеновый гель (основу искусственной кожи), который содержит дермальные клетки – фибробласты (это аналог дермы, имеющий большое количество коллагена и фибробластов), выкладывают верхним слоем эпителиальные клетки – кератиноциты, которые точь-в-точь похожи на эпидермис – верхний слой кожи. Таким образом, искусственная кожа состоит из двух слоёв, как и настоящая человеческая кожа. На рану накладывается готовое изделие той же структуры, что и кожа пациента, и начинается процесс заживления.
Хотя сама искусственная кожа приживается лишь на время, входящие в ее состав клетки активно секретируют различные ростовые факторы, которые стимулируют собственные клетки пациента к делению и миграции в область раны. Благодаря этому рана начинает быстрее затягиваться по краям. Кожа восстанавливается. Клетки донора постепенно замещаются вновь образованными клетками самого больного. Конечно, в качестве источника кожи можно использовать и собственную кожу пациента с неповреждённых участков, но при ожогах большой площади этого, как правило, не хватает. Так как искусственная кожа по своей структуре напоминает настоящую человеческую кожу, то её также используют и для бионических протезов с сохранением чувствительности.
В России новый материал был разработан в ходе получения смеси из латекса и биоактивных растительных компонентов. Искусственная ткань плотно прилегает к ране, защищает её в дальнейшем от внешних воздействий и выполняет лечебный процесс. Учёные отмечают, что самые сложные повреждения с новой «кожей» затягиваются в течение двух дней. В Институте теоретической и экспериментальной биофизики РАН было создано идеальное раневое покрытие, которое защищает больное место от механических повреждений и вредоносных инфекций. Кроме того, искусственная кожа создает оптимальные условия для роста клеток, пропускает воздух и водные пары, чтобы рана под таким покрытием не высыхала и не мокла. Когда тончайшая пленка накладывается на рану, клетки начинают переходить в нее, смешиваясь с клетками пациента, и активизируют выработку коллагена для зарастания раны и образования рубца. Латексная «подложка» после этого просто отсоединяется, и медикам нет необходимости мучить пациентов бесконечными перевязками. Причем после выписки пациент может самостоятельно использовать лечебные мази, нанося их на латексную пленку, которая имеет микропоры, как обычная кожа.

Эксперимент с использованием 3D-биопринтера на животном
В 2019 году ученые впервые создали 3D-биопринтер, который печатает кожу в два слоя собственной кожи пациента прямо на ране. Над этим исследованием работали специалисты из Института регенеративной медицины (США). Принтер использует «чернила», которые состоят из клеток пациента, чтобы минимизировать риск отторжения. Вначале делается биопсия здоровой кожи пациента и выращивается большое количество клеток, после чего их смешивают с гидрогелем для образования "чернил" 3D-биопринтера. Точнее создаются два типа "чернил" – для внутреннего слоя (из клеток-фибропластов) и внешнего (из клеток-кератиноцитов). После удачных экспериментов, проведенных на мышах, был получен отличный результат, который в дальнейшем позволит проводить клинические испытания на людях.


3D-принтер печатает искусственную кожу с сосудами (Living Skin Can Now be 3D-Printed With Blood Vessels Included/ Теперь живую кожу можно напечатать на 3D-принтере, включая кровеносные сосуды)
После изобретения 3D-биопринтера, печатающего искусственную кожу, идентичную коже пациента, было принято решение усовершенствовать разработку, так как просто полученная кожа могла подойти не каждому пациенту. Основная причина в этом - отсутствие кровеносных сосудов, которые нужны для коммуникации трансплантированного участка с окружающими тканями. Ученые из Политехнического института Ренсселера (Нью Йорк, США) выяснили, что если в биочернила добавить эндотелиальные клетки человека, которые выстраиваются внутри кровеносных сосудов, и клетки перицита человека, обволакивающих вокруг эндотелиальных клеток, вместе с животным коллагеном и другими структурными клетками, то в течение нескольких недель они начинают формировать сосуд. Так, в ходе исследований ученые пересадили участок искусственной кожи мышке. Он удачно прижился на животном и не вызвал отторжения. Кроме того, его сосуды благополучно соединились с кровеносной системой мыши и начали снабжать клетки ткани кровью.

Искусственная кожа с эффектом чувствительности
В сентябре прошлого года исследователи Университета RMIT в Мельбурне представили электронную искусственную кожу, которая чувствует боль и прикосновения. Считается, что новая технология успешно найдет своё применение в протезировании, робототехнике и кожной трансплантации. Данное изобретение может показывать ощущение боли. Устройство имитирует почти мгновенную обратную связь и способно реагировать на боль с той же скоростью, с какой нервные сигналы поступают в мозг. Учёные отмечают, что эта разработка стала значительным прогрессом в области биомедицинских технологий и интеллектуальной робототехники следующего поколения. В будущем такая искусственная кожа может стать вариантом неинвазивных кожных трансплантатов, особенно в случаях, когда традиционный подход нежизнеспособен или не работает.
БЕСПЛАТНАЯ КОНСУЛЬТАЦИЯ: поможем врачам и владельцам клиник выбрать оборудование для лечения ожоговых рубцов
Оглавление
Ожоговые рубцы — это плотные соединительнотканные образования на коже, возникающие при нарушении нормального заживления ожоговых ран, а также при обширном и/или глубоком поражении тканей. Основную проблему для врачей и их пациентов представляют гипертрофические и келоидные ожоговые рубцы.
В нашей компании Вы можете приобрести следующее оборудование для лечения ожоговых рубцов:
По данным обследования 100 пациентов с ожогами (включая 59 детей), гипертрофические и келоидные рубцы зафиксированы в 38% случаев, включая 34% у взрослых и 41% у детей. В другом исследовании были проанализированы пациенты ожогового отделения Окружного госпиталя Солсбери — в 1968 году гипертрофические рубцы отмечены в 51% случаев, тогда как в 1984 году уже в 63% случаев.
Вероятность развития ожоговых рубцов повышают следующие факторы:
- молодой возраст;
- женский пол;
- локализация повреждения на шее и верхних конечностях;
- более одного хирургического вмешательства в травмированной области;
- трансплантация сетчатого кожного лоскута в область ожога.
Этиология и патогенез
В обычной жизни большинство ожогов происходят при температуре 100–200 °С с воздействием на кожу более 1 секунды. В горячих цехах и зонах боевых действий возможны ожоги при температуре более 1000 °С и времени воздействия менее 1 секунды. Критическим уровнем, при котором развивается термическое повреждение тканей, считается 43 °С — температура ниже этого значения не вызывает ожогов вне зависимости от длительности контакта с кожей.
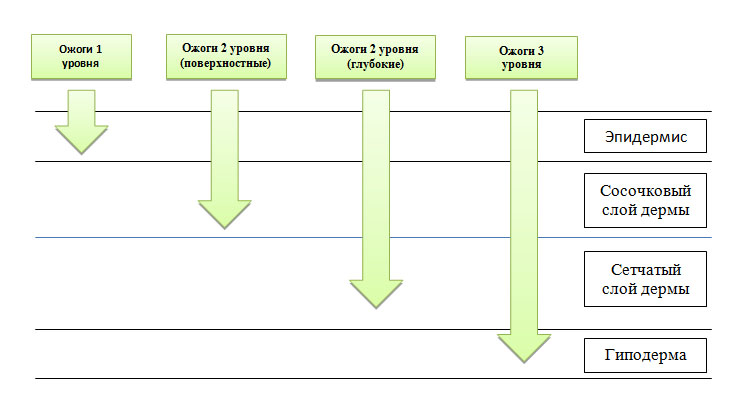
Уровень локального повышения температуры в тканях зависит от их теплопроводности — у дермы она выше, чем у подкожно-жировой клетчатки, поскольку жир является хорошим изолятором. Поэтому термическое повреждение, приводящее к полному некрозу дермы, может почти не затрагивать нижележащий липидный слой. Хотя при очень высокой температуре полностью разрушаются не только дерма и гиподерма, но также скелетные мышцы, фасции, внутренние органы и кости (рис. 1).
Волосяные фолликулы простираются глубоко в подкожно-жировую клетчатку, но это не всегда защищает их от высокой температуры. Хотя их сохранение критически важно для быстрого и качественного заживления травмированной области.
Поверхностные ожоги (первый уровень) — это термическое повреждение одного или нескольких слоев эпидермиса, за исключением базальной мембраны. Нетронутой также остается подлежащая дерма вместе с волосяными фолликулами. Заживление поверхностных ожогов обычно происходит без образования рубцов, поскольку со дна волосяных фолликулов поступает много свежих кератиноцитов, которые помогают быстро восстанавливать пораженную область.
Средние ожоги (второй уровень) — в этом случае поражается весь эпидермис и сосочковый (поверхностные ожоги 2 уровня) или сетчатый слой дермы (глубокие ожоги 2 уровня). После термического воздействия активируются макрофаги, которые начинают очищать рану от некротического мусора. Далее под отмершей тканью образуется свежая грануляционная, формируя так называемый ожоговый струп. Все это способствует восстановлению эпидермиса и образованию тонкого нормотрофического рубца.
При средних ожогах глубокие части волосяных фолликулов остаются жизнеспособными. Выстилающие их дно кератиноциты начинают активно делиться и мигрировать в пораженную область, способствуя реэпителизации. В тяжелых случаях потеря волосяных фолликулов может привести к недостаточной регенеративной активности для эффективного закрытия области повреждения. Если присоединяется инфекция, восстановление ожоговой раны затягивается и может завершаться образованием гипертрофического или келоидного рубца.
Глубокие ожоги (третий уровень) — термическое повреждение распространяется достаточно глубоко в дерму и частично в подкожно-жировую клетчатку, где полностью разрушает волосяной фолликул, включая его основание. Быстрая регенерация кожи фолликулярными кератиноцитами в этом случае невозможна — новые клетки поступают только с краев раны, поэтому такое повреждение заживает медленно. Плюс для удаления больших объемов некротизированной ткани требуется длительная работа макрофагов. В итоге растет вероятность присоединения инфекции, что еще больше осложняет и затягивает регенерацию, способствуя образованию гипертрофических или келоидных рубцов.
Основные исходы ожогов:
- Заживление ожоговой раны с полным восстановлением функции поврежденного органа или области.
- Заживление ожоговой раны с частичной утратой функции поврежденного органа или области.
- Заживление ожоговой раны со значительной утратой функции поврежденного органа или области, вплоть до ее полной потери.
- Образование гипертрофических или келоидных рубцов, сопровождающихся зудом, болезненностью, изъязвлениями и выраженным косметическим дефектом.
Рис. 1. Уровни ожогов и глубина повреждения тканей
Клинические проявления
Наиболее тяжелыми формами ожоговых рубцов являются гипертрофические и келоидные. Гипертрофические рубцы формируются в результате избыточного образования коллагена — они плотные, возвышаются над уровнем кожи, но не выходят за пределы первоначального повреждения и со временем могут подвергаться инволюции. Келоидные рубцы представляют собой опухолеподобное разрастание незрелой соединительной ткани за счет неконтролируемой пролиферации фибробластов. Их особенностью является быстрый рост, сопровождающийся парестезиями, зудом и болевыми ощущениями. Келоиды могут активно увеличиваться в размерах, выходя за пределы ожогового повреждения кожи в виде периферических тяжей. Они почти никогда не уменьшаются и не рассасываются.
Гипертрофические и келоидные рубцы обычно возникают у пациентов с серьезными (глубокими и/или обширными) ожогами (рис. 2). Отягчающим фактором является присоединение инфекции, которая значительно замедляет эвакуацию некротического содержимого и дальнейшую реэпителизацию. В области гипертрофических и келоидных рубцов часто наблюдаются нарушения пигментации — локальное потемнение или побледнение вплоть до обесцвечивания.
Ожоговые рубцы могут увеличиваться в размерах в течение нескольких месяцев, а затем постепенно регрессировать в течение нескольких лет, превращаясь в плоские рубцы без каких-либо дополнительных симптомов. Однако такой сценарий реализуется не у всех пациентов.
Точная оценка состояния ожогового рубца необходима для диагностики и выбора стратегии лечения. Среди различных классификаций, предложенных в последние годы, чаще всего используется Ванкуверская шкала оценки рубцов (Vancouver Scar Scale, VSS). В России была разработана ее модификация, представленная в табл. 1.
Табл. 1. Модифицированная Ванкуверская шкала для оценки ожоговых рубцов
При обширных ожогах возникает заболевание всего организма.
1) способствовать нормализации резко нарушенного обмена веществ, прежде всего белкового, водно-солевого, витаминного;
2) уменьшить явления интоксикации организма;
3) повысить сопротивляемость организма к инфекции;
4) способствовать восстановлению поврежденных тканей.
При ожоговой болезни потребность в пищевых веществах повышена из-за усиленного их расхода в связи с изменением обменных процессов и потерь через раневую поверхность. Организм обедневает белками, минеральными солями, жидкостью, витаминами. Может возникнуть метаболический ацидоз. Усвоение пищевых веществ ухудшается. Угнетаются функции органов пищеварения, снижается аппетит.
При тяжелой ожоговой болезни больные теряют ежедневно 0,8 — 1 кг массы тела и 100—150 г белка. Энерготраты организма больных с ожогами III—IV степени в остром периоде болезни умеренно увеличены. Расход энергии возрастает при высокой температуре, перевязках, мышечном напряжении при вынужденном положении, поэтому энергоценность рациона должна составлять 2500—2800 ккал при высоком содержании белка (110—130 г), железа и витаминов (в 1,5—2 раза выше физиологических норм). При более высокой энергоценности рациона пища потребляется не полностью и часть содержащегося в рационе белка не используется.
В первые дни болезни при тяжелом состоянии показано питание с максимальным механическим щажением по типу нулевых диет. Целесообразно полное или дополнительное зондовое питание (см. «Зондовые диеты»). Большое значение имеет включение в рацион высокопитательных специальных диетических продуктов — белкового и противоанемического энпитов, инпитана, оволакта, унипитов и др. (см. «Консервы и концентраты»). В связи с угнетением аппетита целесообразно применение веществ, улучшающих вкус и запах пищи.
После выхода из тяжелого состояния показаны диеты с умеренным механическим щажением. В основу построения рациона лучше всего положить диету № 11. В рационах, комплектующихся из обычных пищевых продуктов, уменьшают количество хлеба, крупы, макаронных изделий и увеличивают молочные продукты (творог, сыр), яйца, мясо, рыбу. Энергоценность рациона может достигать 3200—3400 ккал, а содержание белка — 130— 135 г. Такое высокое количестве белка особенно важно при лечении ожоговых больных кортикостероидными и анаболическими гормонами (см. «Особенности лечебного питания при лекарственной терапии»). В дальнейшем больных переводят на питание с обычной кулинарной обработкой продуктов, но в диете сохраняют повышенное количество белков, витаминов, железа и умеренное увеличение жиров
Читайте также:

