Вэб цмв герпес 6 типа что это
Обновлено: 18.04.2024
Исследование для выявления возбудителя герпес-вирусной инфекции 6-го типа (Human Herpes Virus 6), в ходе которого с помощью метода полимеразной цепной реакции в реальном времени (РТ-ПЦР) определяется генетический материал (ДНК) вируса в образце биоматериала.
Синонимы русские
Герпес-вирус 6-го типа, ВГЧ-6, РТ-ПЦР.
Синонимы английские
HHV-6, DNA [Real-time PCR].
Метод исследования
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Биоптат, венозную кровь, ликвор, мазок из зева (ротоглотки), слюну.
Общая информация об исследовании
6-й тип герпес-вируса человека (ВГЧ-6) впервые был определен относительно недавно, в 1986 г., в крови ВИЧ-инфицированных пациентов. К настоящему времени установлено, что инфекция ВГЧ-6 широко распространена и имеет 2 подтипа, отличающихся генетически, – А и В. В целом более распространен подтип В, однако подтип А чаще обнаруживают у пациентов с иммунодефицитами.
Полная репликация вируса происходит только в Т-лимфоцитах, но ВГЧ-6 может быть выявлен и в других клетках – моноцитах, В-лимфоцитах, а также в ткани мозга, печени, слюнных желез, в эндотелии.
Наиболее вероятный путь заражения – воздушно-капельный, со слюной, не исключена передача инфекции от матери к ребенку во время беременности.
Также существует возможность инфицирования при трансплантации органов, гемотрансфузиях, через медицинские инструменты. Наркоманы и медицинские работники могут заразиться при случайном уколе иглой шприца, содержащего кровь больного либо инфицированного.
Первый раз заражение практически всегда происходит в возрасте от 4 до 24 месяцев. В большинстве случаев ВГЧ-6 протекает бессимптомно, а если проявляется, то чаще всего как внезапная экзантема и быстро развивающаяся сильная лихорадка, продолжающаяся 3-4 дня. Через несколько часов после нормализации температуры появляются эритематозные пятна или пятнисто-папулезная сыпь. Сходство внезапной экзантемы с симптомами кори или краснухи зачастую приводит к постановке ошибочного диагноза.
В некоторых случаях бывают осложнения со стороны центральной нервной системы (судороги на фоне высокой температуры, редко энцефалит, менингоэнцефалит, серозный менингит).
Взрослые редко инфицируются ВГЧ-6, причем заражение у них может сопровождаться симптомами инфекционного мононуклеоза (вирус Эпштейна – Барр в таком случае отсутствует) или фульминантного гепатита.
ВГЧ-6 способен вызвать отторжение трансплантата у реципиентов. Осложнения вследствие активации ВГЧ-6 отмечены у пациентов после пересадки костного мозга, почек, печени, легких. В частности, пациенты после трансплантации костного мозга часто страдают от заболеваний, обусловленных HHV-6 (интерстициальная пневмония, супрессия костного мозга, менингоэнцефалит). Активация ВГЧ-6 является причиной 80 % случаев идиопатической лейкопении после трансплантации печени. К счастью, при своевременной диагностике ВГЧ-6 поддается лечению с помощью лекарственных препаратов.
ВИЧ-инфицированные составляют еще одну категорию лиц с иммунодефицитом, у которых активация ВГЧ-6 способна приводить к серьезным осложнениям (к поражениям ЦНС, к пневмонии и пр.) и прогрессированию основного заболевания. Кроме того, активный ВГЧ-6 может способствовать переходу ВИЧ из латентной в активную форму, поэтому регулярный контроль активности ВГЧ-6 у ВИЧ-положительных пациентов важен для своевременного начала антивирусной терапии.
Сегодня активно исследуется возможная роль ВГЧ-6 в развитии рассеянного склероза, синдрома хронической усталости, лимфопролиферативных заболеваний.
Так как ВГЧ-6 в латентной форме распространен практически повсеместно, очень важно вовремя устанавливать характер его течения – активный/неактивный. Активация любой вирусной инфекции начинается с размножения (репликации) вируса в клетке-хозяине. Далее в большинстве случаев клетки-хозяева погибают, а новые вирусы выходят в межклеточное пространство (внутритканевую жидкость) для заражения новых клеток. Оттуда вирусные частицы попадают в различные биологические жидкости (кровь, мочу, ликвор) и железистые секреты, где могут быть легко обнаружены с помощью ПЦР. Выявление вирусных ДНК/РНК в бесклеточных образцах биологических жидкостей или железистых секретах является однозначным указанием на активную вирусную инфекцию. Однако диагностика инфекции осложняется тем, что ВГЧ-6 после репликации в клетке-хозяине заражает другие клетки напрямую, проникая через межклеточные перегородки и избегая межклеточных пространств. Таким образом, подтверждение активности ВГЧ-6 посредством ПЦР в бесклеточных образцах биологических жидкостей и секретах удается не во всех случаях. В связи с этим возникает необходимость подтверждения активности/неактивности ВГЧ-6 с помощью серологических методов.
Когда назначается исследование?
- При дифференциальной диагностике детских инфекций, протекающих с высокой температурой и сыпью.
- При диагностике инфекционного мононуклеоза при отрицательном тесте на вирус Эпштейна – Барр.
- В комплексе обследований пациентов с лимфопролиферативными заболеваниями и гемобластозами.
- При обследовании реципиентов органов и тканей до и после трансплантации.
- При диагностике вирус-ассоциированных заболеваний у ВИЧ-инфицированных и при других иммунодефицитных состояниях (например, синдроме хронической усталости).
- При контроле за эффективностью проведенного антивирусного лечения.
Для чего используется исследование?
- Для подтверждения наличия/отсутствия инфекции.
- Для того чтобы определить характер течения инфекции – активный/неактивный.
- Для дифференциальной диагностики герпетических инфекций.
Что означают результаты?
Причины положительного результата
- Однократный положительный результат реал-тайм ПЦР однозначно свидетельствует об активной ВГЧ-6 инфекции.
Причины отрицательного результата
- Однократный отрицательный результат реал-тайм ПЦР может быть признаком отсутствия активной ВГЧ-6-инфекции и нуждается в дополнительном подтверждении с помощью ретроспективных исследований вирусоспецифических IgG-антител.
Что может влиять на результат?
Свойство ВГЧ-6 поражать другие клетки напрямую, не выходя за их пределы, способствует ложноотрицательному результату.
Важные замечания
- Лимфоциты и моноциты крови являются местом постоянного обитания и размножения ВГЧ-6 у инфицированных людей, поэтому надежным свидетельством активации/реактивации ВГЧ-6 служит обнаружение ДНК ВГЧ-6 в бесклеточных производных крови – сыворотке или бесклеточной плазме.
Также рекомендуется
Кто назначает исследование?
Аллерголог-иммунолог, акушер, гинеколог, инфекционист, педиатр, невролог, гематолог, хирург.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна–Барр: причины появления, симптомы, диагностика и способы лечения.
Вирус Эпштейна–Барр может инфицировать различные типы клеток, включая B-клетки иммунной системы (разновидность лейкоцитов – белых кровяных телец) и эпителиальные клетки слизистых оболочек.
ВЭБ является представителем ДНК-содержащих вирусов из семейства Herpesviridae (герпесвирусы), подсемейства гамма-герпесвирусов и рода лимфокриптовирусов. В процессе репликации (самокопирования) вируса экспрессируется свыше 70 различных вирусспецифических белков. В настоящее время выделены группы иммуногенных белков, определение антител к которым дает возможность дифференцировать стадию инфекции (ЕА – ранний антиген, ЕВNА-1 — ядерный антиген, VCA — капсидный антиген, LMP — латентный мембранный белок).
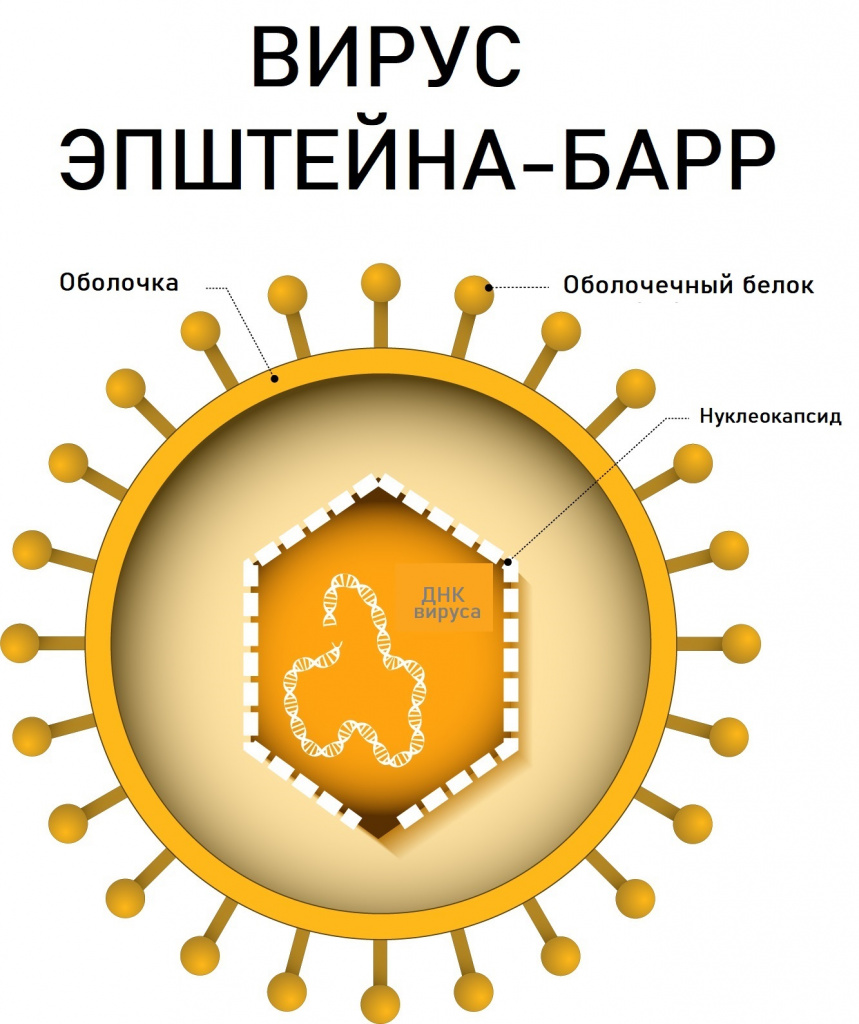
Причины появления заболеваний, вызванных вирусом Эпштейна-Барр
Вирус может распространяться от человека к человеку через биологические жидкости (воздушно-капельный путь передачи). Вот почему инфекционный мононуклеоз, одно из самых известных заболеваний, вызываемых ВЭБ, называют «болезнью поцелуев».
Другой способ заражения – контактно-бытовой (вирус передается через зубные щетки, столовые приборы, полотенца и т.д.). ВЭБ также может распространяться через кровь и сперму.
ВЭБ размножается в В-лимфоцитах и эпителиальных клетках, в связи с чем характерно многообразие клинических проявлений данной патологии. Важной отличительной чертой вируса является то, что он не тормозит и не нарушает размножение В-лимфоцитов, а, наоборот, стимулирует его. В этом заключается особенность возбудителя - он размножается в клетках иммунной системы, заставляя их клонировать свою, вирусную, ДНК.
Хронический воспалительный процесс, вызванный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии.
Классификация вируса Эпштейна-Барр
Единой классификации вирусной инфекции Эпштейна-Барр (ВИЭБ) не существует, к использованию в практической медицине предлагается следующая:
- по времени инфицирования – врожденная и приобретенная;
- по форме заболевания – типичная (инфекционный мононуклеоз) и атипичная: стертая, асимптомная, с поражением внутренних органов;
- по тяжести течения – легкая, средней степени и тяжелая;
- по продолжительности течения – острая, затяжная, хроническая;
- по фазе активности – активная и неактивная;
- смешанная инфекция – чаще всего наблюдается в сочетании с цитомегаловирусом.
- Инфекционный мононуклеоз (железистая лихорадка, болезнь Филатова) – распространенное инфекционное заболевание, основными проявлениями которого является подъем температуры до высоких значений, увеличение лимфатических узлов, воспаление слизистой оболочки глотки, увеличение печени и селезенки. ВЭБ в данном случае проникает через эпителий слизистых оболочек верхних дыхательных путей.
- Лимфогранулематоз (болезнь Ходжкина) и некоторые виды неходжкинских лимфом – группа заболеваний, объединенных злокачественной моноклональной пролиферацией лимфоидных клеток в лимфоузлах, костном мозге, селезенке, печени и желудочно-кишечном тракте.
- Синдром хронической усталости – состояние, характеризующееся длительным чувством усталости, которое не проходит после продолжительного отдыха.
- Синдром Алисы в стране чудес – состояние, клиническим проявлением которого является нарушение ощущения своего тела и отдельных его частей. Человек ощущает себя или части своего тела очень большими или очень маленькими по сравнению с действительностью.
- Гепатит, спровоцированный ВЭБ, часто является осложнением инфекционного мононуклеоза. Появляется слабость, тошнота, желтушность кожи и слизистых, увеличивается печень.
- Герпетическая инфекция в виде генитального или лабиального (на губах) поражения. Также возможен стоматит, вызванный ВЭБ. При активации инфекции появляется чувство жжения и боль, а затем множество маленьких пузырьков.
- Посттрансплантационная лимфопролиферативная болезнь – вторичное злокачественное заболевание, развивающееся после трансплантации гемопоэтических стволовых клеток (метод лечения, применяемый при онкологии, заболеваниях крови и др.), ассоциированное с ВЭБ-инфекцией.
- Рассеянный склероз – хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга. Характеризуется большим количеством симптомов и зависит от уровня поражения: часто снижается мышечная сила, угасают рефлексы, появляются параличи (обездвиженность) различных локализаций.
- Волосатая лейкоплакия – на слизистой оболочке языка по бокам, на спинке либо на его нижней части появляются белые участки с шероховатой поверхностью. Они безболезненны и не причиняют существенного дискомфорта. Основная опасность заключается в возможности озлокачествления измененных клеток слизистой.
- Назофарингеальная карцинома – злокачественное образование глотки. Среди его симптомов часто встречаются заложенность носа, потеря слуха, частые отиты, появление крови в слюне, кровянистые выделения из носа, увеличение лимфоузлов, головные боли.
- Аутоиммунный тиреоидит – хроническое заболевание щитовидной железы, при котором в организме образуются антитела к тканям щитовидной железы. При данном заболевании возможно появление зоба (увеличение щитовидной железы), развитие симптомов гипотиреоза: отеки, повышенная утомляемость, сонливость, запоры, сухость кожи, выпадение волос.
Лабораторное обследование включает:
-
вирус Эпштейна–Барр, определение ДНК в крови (Epstein Barr virus, DNA);
Определение ДНК вируса Эпштейна-Барр в крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени». Вирус Эпштейна - Барр (ВЭБ) является причиной инфекционного мононуклеоза. С вирусом Эпштейна-Барр связывают также этиологию некоторых онкологических.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Цитомегаловирус: причины появления, симптомы, диагностика и способы лечения.
Определение
Цитомегаловирус (ЦМВ, или цитомегаловирусная болезнь) – хроническое инфекционное заболевание вирусной этиологии, характеризующееся многообразием клинических форм и проявлений - от бессимптомного течения до тяжелого поражения внутренних органов и центральной нервной системы. Возбудитель ЦМВ – представитель семейства герпесвирусов (вирус герпеса человека 5-го типа).
Попадая в клетки организма, цитомегаловирус способен оставаться в них пожизненно. У лиц с нормально функционирующей иммунной системой в подавляющем большинстве случаев инфекция протекает по типу вирусоносительства. При угнетении иммунитета вирус активизируется, вызывая клинические симптомы болезни.
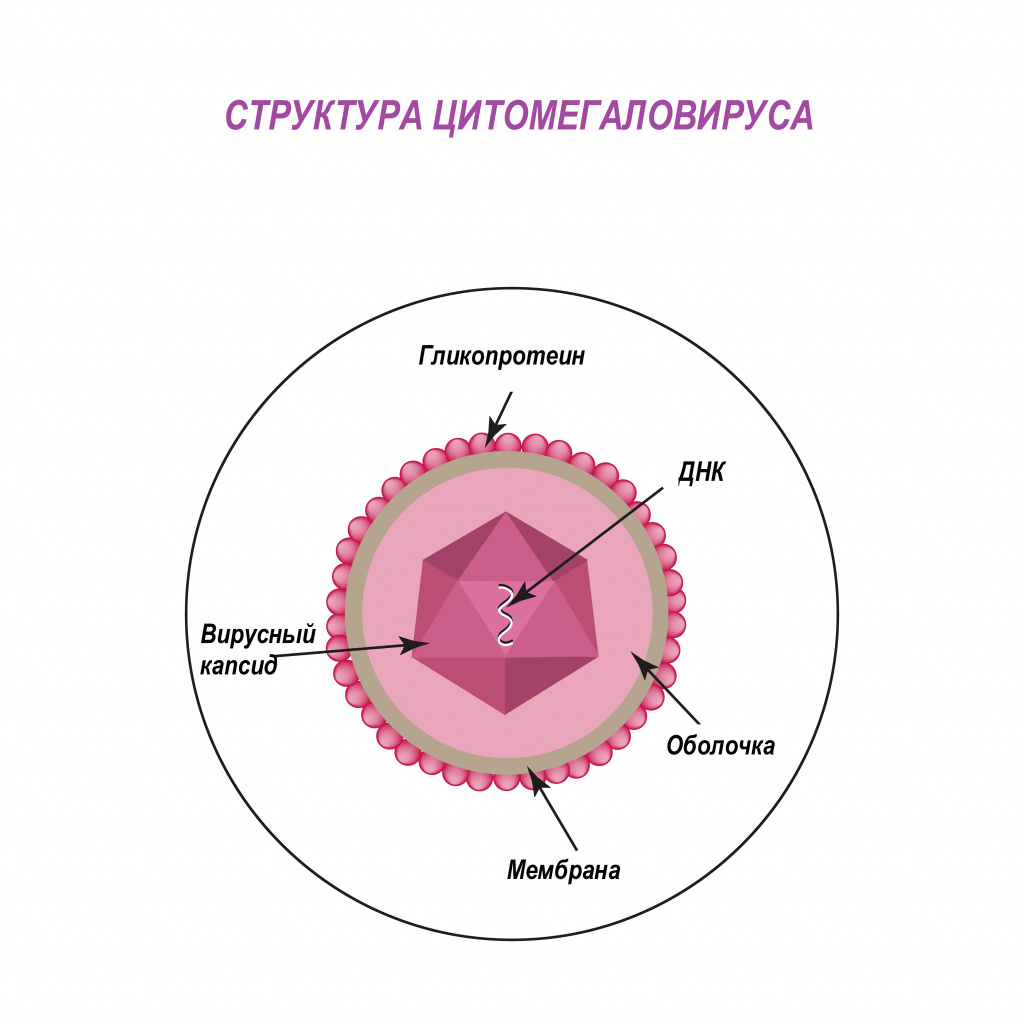
По различным данным доля носителей цитомегаловируса в России составляет порядка 73-90% - то есть именно у такого количества людей выявляются антитела к ЦМВ.
Причины появления цитомегаловирусной болезни
Цитомегаловирус передается через биологические жидкости: слюну, мочу, кровь, вагинальный секрет, слезы, сперму, фекалии, грудное молоко.
Из-за лабильности возбудителя и низкой концентрации вируса в выделениях для передачи инфекции необходим длительный, частый и тесный контакт с носителем.
Механизмы передачи вируса — воздушно-капельный (аэрозольный путь), контактный (контактно-бытовой и половой), гемоконтактный (парентеральный, а также при пересадке органов), вертикальный (от матери к плоду), фекально-оральный (алиментарный — через грудное молоко).
Заражение плода реализуется за счет трансплацентарной передачи от матери к плоду, которая возможна в течение всей беременности. Наибольшую опасность для плода представляет первичная инфекция на ранних сроках беременности, поскольку часто вызывает формирование врожденных пороков развития.
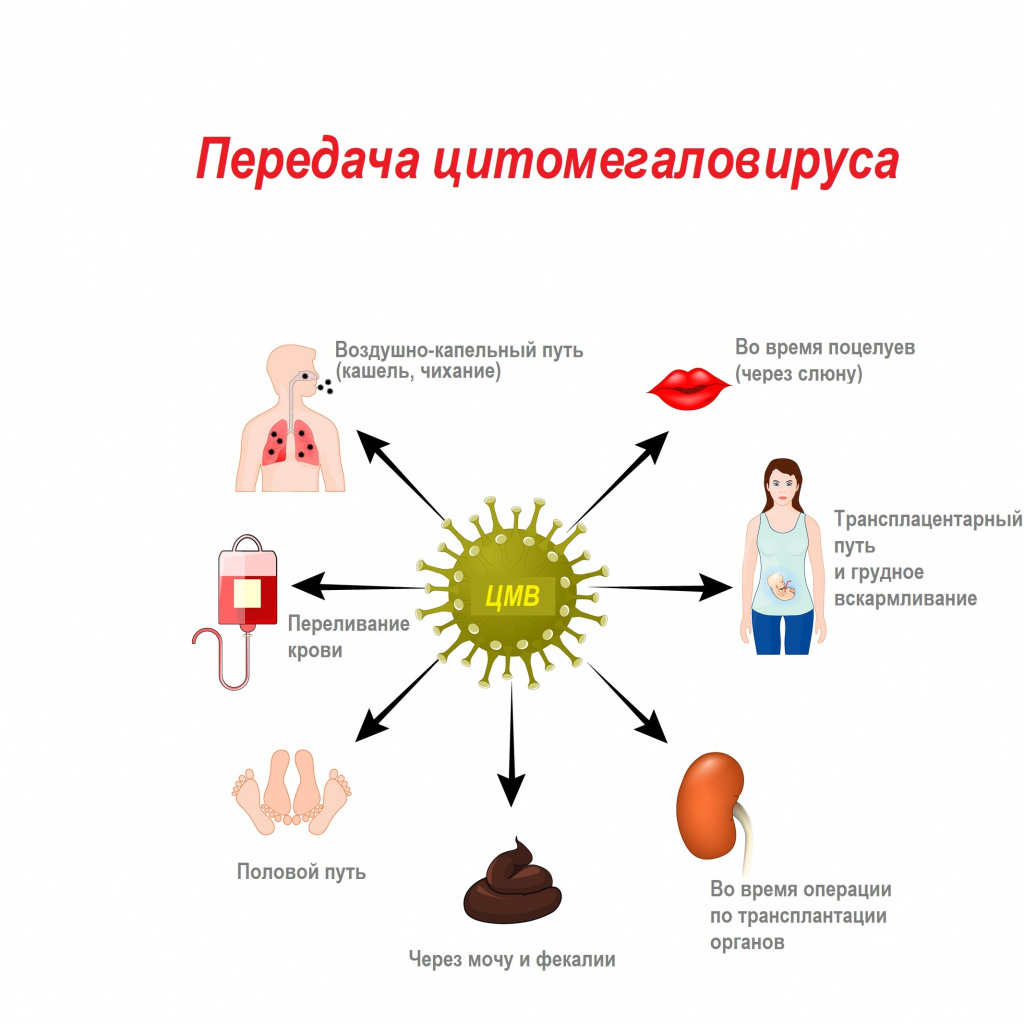
Особое свойство ЦМВ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов, в первую очередь ИНФ-α. При острой инфекции вирус поражает преимущественно эпителиальные клетки легких, печени, кишечника, почек, мочевого пузыря, молочных и слюнных желез, генитального тракта. Цитомегаловирус может инфицировать нервные клетки, клетки гладкой мускулатуры, костного мозга.
Классификация заболевания
По характеру инфицирования:
- врожденное (внутриутробное),
- постнатальное (приобретенное).
- латентная инфекция,
- персистирующая инфекция,
- активная (низкой, средней, высокой степени тяжести) инфекция.
- острая инфекция,
- реактивация вируса,
- реинфекция.
Инкубационный период цитомегаловирусной болезни составляет от 15 дней до трех месяцев (при манифестной, выраженной форме заболевания). Однако чаще первичное инфицирование протекает или бессимптомно, или по типу легкой формы ОРЗ – у пациента наблюдаются незначительная слабость, лихорадка (температура 37,1-38,0°С), дискомфорт в мышцах, першение в горле, иногда насморк, увеличение шейных лимфатических узлов, болезненность слюнных желез, головная боль, отсутствие аппетита.
У беременных острая первичная инфекция протекает, как правило, бессимптомно (25–50%) или с неспецифическими проявлениями (с лихорадкой, астенией и головной болью).
В редких случаях развиваются гепато- и спленомегалия, гепатит с минимальной степенью активности цитолитического синдрома, дерматиты, васкулиты, интерстициальный пневмонический процесс, тромбоцитоз или тромбоцитопения, лимфоцитоз.
У больных с иммунодефицитом цитомегаловирусная инфекция протекает тяжело - вирус быстро распространяется по организму и вызывает серьезные осложнения.
Диагностика цитомегаловируса
Диагностические мероприятия начинаются со сбора жалоб и анамнеза, в том числе акушерско-гинекологического анамнеза матери.
Затем врач проводит объективное обследование (физикальное, неврологическое и антропометрическое).
Лабораторные исследования - общие и специфические:
-
общий анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Метод определения Определение физико-химических параметров выполняется на автоматическом анализаторе методом «сухой химии». Аппаратная микроскопия проводится методом планарной цитометрии с использованием осевого гидродинамического фокусирования и автоматического распозна.
Синонимы: Анализ крови на антитела к цитомегаловирусу; АТ-ЦМВ-IgМ; цитомегаловирусная инфекция; ЦМВ-инфекция; специфические иммуноглобулины класса М к цитомегаловирусу. Cytomegalovirus; CMV Antibody; IgM; CMV infection; CMV-specific IgM. Краткое описание исследования Anti-CMV.
Синонимы: Анализ крови на антитела к цитомегаловирусу; АТ-ЦМВ-IgG; Цитомегаловирусная инфекция; ЦМВ-инфекция; Специфические иммуноглобулины класса G к цитомегаловирусу. Cytomegalovirus; CMV Antibody, IgG; CMV infection; CMV-specific IgG. Краткое описание исследования Anti-CMV-IgG .
Определение ДНК цитомегаловируса в крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени». Цитомегаловирус - широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латент.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирусная инфекция входит в группу репродуктивно значимых инфекций, обозначаемых как TORCH-комплекс (название образовано начальными буквами в латинских наименованиях - Toxoplasma, Rubella, Cytomegalovirus, Herpes); первичное инфицирование данными возбудителями, либо обострение .
К каким врачам обращаться
С первичными жалобами пациенты обращаются к врачу-терапевту или врачу общей практики (семейному врачу), детей ведет врач-педиатр . Могут потребоваться консультации инфекциониста - для верификации диагноза, стоматолога - при поражениях слизистой оболочки рта, кардиолога - при наличии врожденного порока сердца, нейрохирурга - при пороках центральной нервной системы, невропатолога - для оценки неврологической патологии, гематолога - при выраженных гематологических изменениях и геморрагическом синдроме, окулиста - для исследования глазного дна, отоларинголога - для исследования слухового аппарата.
Лечение цитомегаловирусной болезни
Субклинические формы ЦМВ-инфекции и латентное носительство крайне распространены, поэтому в большинстве случаев не требуют специфической терапии даже при выявлении антител. Их лечение направлено на усиление защитных сил организма при помощи иммуномодуляторов и профилактику факторов риска, которые приводят к обострению заболевания.
Для терапии клинически активных форм инфекции применяют:
- комплекс патогенетической (противовирусной) терапии, который разрабатывается профильными специалистами и включает препараты прямого противовирусного действия для минимизации риска осложнений, сокращения времени течения заболевания, а также профилактики рецидивов;
- иммунотерапию – антицитомегаловирусный иммуноглобулин назначают преимущественно детям при манифестных формах заболевания и беременным;
- дезинтоксикационную терапию, которая направлена на купирование синдрома интоксикации;
- метаболическую терапию - для восстановления обмена веществ в организме;
- симптоматическую терапию - для купирования воспалительных и токсических проявлений заболевания.
Проблема клинически выраженной инфекции актуальна для лиц, имеющих иммуносупрессию иной природы, в частности, онкогематологических пациентов, больных лучевой болезнью, лиц, длительно принимающих кортикостероидную, туберкулостатическую терапию, а также перенесших ожоговую травму.
Острое течение ЦМВ может привести к развитию гепатита с повышением уровня аминотрансфераз и атипичным лимфоцитозом.
Ученые предполагают роль цитомегаловируса как одного из кофакторов в развитии системных васкулитов, хронических диссеминированных заболеваний легких (в частности, фиброзирующего альвеолита), криоглобулинемии, опухолевых процессов (аденокарциномы предстательной железы, аденокарциномы толстой кишки, рака шейки матки), атеросклероза, кардиомиопатии, детского церебрального паралича, эпилепсии, синдрома Гийена-Барре, синдрома хронической усталости, аутизма.
Первичное инфицирование цитомагаловирусом у беременных женщин существенно повышает риск преждевременных родов, самопроизвольного выкидыша, многоводия, замершей беременности, внутриутробного инфицирования и даже гибели плода. Врожденная ЦМВ-инфекция может стать триггерным фактором развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией.
Профилактика цитомегаловирусной болезни
Женщинам, планирующим беременность, необходимо пройти обследование на наличие ЦМВ. При обнаружении вируса важно получить консультацию врача-иммунолога.
Профилактика или превентивное лечение (активный мониторинг пациентов по уровню вирусной нагрузки и назначение противовирусных препаратов пациентам с признаками инфекции) являются эффективными способами предотвращения развития цитомегаловирусной инфекции после трансплантации органов.
- Клинические рекомендации «Цитомегаловирусная болезнь у взрослых». Некоммерческая корпоративная организация «Международная ассоциация специалистов в области инфекций. Утв. Минздравом России, 2019.
- Извекова И.Я., Михайленко М.А., Краснова Е И. Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения. Лечащий врач № 4/2018. С. 90-95.
- Заплатников А.Л., Шахгильдян В.И., Подзолкова Н.М. Возможно ли предупредить последствия врожденной цитомегаловирусной инфекции? (взгляд акушера-гинеколога, инфекциониста и неонатолога). РМЖ «Медицинское обозрение» № 10 от 10.12.2018. С. 45-50.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус герпеса человека 6 типа (HHV-6, ВГЧ-6) относительно недавно был внесен в список известных человеческих инфекционных возбудителей и является серьезным претендентом на роль причинного агента таких заболеваний, как рассеянный склероз, энцефалит, лихорадка у детей с судорожным синдромом, инфекционный мононуклеоз, «внезапная экзантема». Существуют данные о том, что вирус герпеса 6 типа является кофактором СПИДа, некоторых форм карцином шейки матки и назофарингеальных карцином.
Актуальность вируса герпеса 6 типа
На сегодняшний день внимание специалистов приковано к инфекциям, вызываемым вирусами герпеса, которые являются причиной развития многих соматических и онкологических заболеваний, занимают ведущее место среди причин мертворождаемости, преждевременных родов, младенческой смертности, заболеваемости новорожденных, способствуя ранней инвалидизации детей. Это обстоятельство обусловлено рядом причин: повсеместным распространением вирусов герпеса, многообразием вызываемых заболеваний, существованием в организме человека в разных формах (острых, хронических, латентных).
Вирусы герпеса — это большое семейство ДНК-содержащих вирусов, вызывающих разнообразные болезни у человека и других млекопитающих. Различают 8 представителей семейства герпесвирусов, поражающих человека. Одним из них является вирус герпеса человека 6 типа (HHV-6).
Вирус герпеса человека 6 типа (HHV-6, ВГЧ-6) относительно недавно был внесен в список известных человеческих инфекционных возбудителей и является серьезным претендентом на роль причинного агента таких заболеваний, как рассеянный склероз, энцефалит, лихорадка у детей с судорожным синдромом, инфекционный мононуклеоз, «внезапная экзантема».
Существуют данные о том, что вирус герпеса 6 типа является кофактором СПИДа, некоторых форм карцином шейки матки и назофарингеальных карцином.
Изучалась роль вируса герпеса 6 типа в качестве причины возникновения судорог у детей. По данным зарубежных авторов, на долю судорог, обусловленных вирусом герпеса 6 типа, приходится 20–40%. В исследовании М. А. Никольского и М. В. Радыш изучалась роль вирусов герпеса 6 и 7 типа в возникновении судорог у 29 детей в возрасте от 1 мес до 7 лет, поступивших в стационар с острыми респираторными заболеваниями. По результатам исследования в 41% случаев в обследуемой группе судороги были сопряжены с вирусом герпеса 6 типа.
Эпидемиология вируса герпеса 6 типа
Вирус герпеса 6 типа впервые был обнаружен в 1986 г. у взрослых больных с гематологическими заболеваниями и зараженных вирусом иммунодефицита человека (ВИЧ).
Первые клинико-эпидемиологические исследования, проведенные в 1986 г., выявили наличие этой инфекции в зоне отдыха в штате Невада (США).

Заболевание выражалось в гриппоподобной симптоматике с повышением температуры, ночным потом, увеличением лимфатических узлов, рядом психологических симптомов (усталость, депрессия). Заболевание получило название «синдром хронической усталости». При этом у 75% больных выявлялись антитела к вирусу герпеса 6 типа.
Пути передачи вируса герпеса 6 типа
Выделение вируса герпеса 6 типа, определение вирусных белков и ДНК в образцах слюны и мокроты указывают на то, что вирус находится в организме человека в слюнных железах, а эксперименты показали, что он в латентной фазе сохраняется в моноцитах/макрофагах (главных клетках иммунной системы человека).
В естественных условиях основным путем передачи вируса является воздушно-капельный. Не исключен вертикальный путь заражения от матери ребенку: антигены вируса обнаружены в абортивном материале при спонтанных абортах. Не исключается половой путь передачи вируса.
Выявление вируса герпеса 6 типа в клетках крови внешне здоровых людей, включая доноров, является серьезным фактором риска передачи инфекции при переливании крови и ее компонентов, трансплантации органов и тканей. Экспериментальные исследования, проведенные учеными, свидетельствуют о том, что вирус герпеса 6 типа инфицирует моноциты и макрофаги разных тканей, а также стволовые клетки костного мозга, из которых впоследствии происходит его реактивация
Иммунитет у детей и взрослых
У новорожденных, при наличии материнских антител, может существовать относительная защита против вируса герпеса 6 типа.
Специфические антитела IgM появляются в течение первых пяти дней от начала клинических симптомов, в последующие 1–2 месяца IgM снижаются и в дальнейшем не определяются.
Специфические IgM могут присутствовать при реактивации инфекции и в небольшом количестве у здоровых людей. Специфические IgG повышаются в течение второй и третьей недели после инфицирования, при этом возрастает их авидность.
IgG к вирусу герпеса 6 типа определяются всю жизнь, но в более низких количествах, чем в раннем детстве. Уровни антител могут колебаться после перенесенной первичной инфекции, возможно, в результате активации латентного вируса.
Существенное возрастание уровня антител, по данным некоторых ученых, наблюдается в случае заражения другими вирусами с похожими ДНК, например, вирусом герпеса 7 типа и цитомегаловирусом. В наблюдениях исследователей указывается, что у детей в течение нескольких лет после первичной инфекции может снова происходить четырехкратное нарастание титра IgG к вирусу герпеса 6 типа, иногда вследствие острого заражения другим агентом, нельзя исключить и возможной активации латентного вируса герпеса 6 типа.
После первичной инфекции вирус сохраняется в латентном состоянии (без клинических проявления) или в виде хронической инфекции с продукцией вируса. Компоненты иммунного ответа, важного в контроле хронической инфекции, неизвестны.
Реактивация латентного вируса происходит у иммунологически ослабленных больных, но может наблюдаться и у иммунокомпетентных людей по неизвестным причинам
Диагностика вирус герпеса 6 типа инфекции
Лабораторный диагноз первичной инфекции, вызванной вирусом герпеса 6 типа, в настоящий момент устанавливается с помощью современного лабораторного оборудования.
ДНК вируса герпеса 6 типа может обнаруживаться в лимфоцитах периферической крови или в других тканях методом гибридизации (полимеразная цепная реакция, ПЦР).
ПЦР с использованием обратной транскриптазы, разработанная недавно, позволяет надежно дифференцировать латентную инфекцию ВГЧ-6 и реактивацию инфекции
Существует целый ряд серологических методов определения вируса герпеса 6 типа: иммунофлюоресцентный метод, иммуноферментный анализ (ИФА), иммуноблот, иммунопреципитация. Иммуноферментный анализ используется наиболее часто, однако серологический диагноз имеет целый ряд недостатков и редко помогает в диагностике клинической манифестации.
Определение титра специфических IgM используют для диагностики острой инфекции или реактивации, но не у всех детей, переносящих первичную инфекцию, отмечается продукция антител IgM, а приблизительно 5% здоровых взрослых имеют антитела IgM к вирусу герпеса 6 типа.
В связи с тем, что практически у всех взрослых выявляют IgG к вирусу герпеса 6 типа, обнаружение специфических антител в одном образце незначимо. К тому же повышение их титра не указывает на новую инфекцию или реактивацию. Возможно также выявление перекрестно реагирующих антител к другим ДНК вирусам, особенно вирусу герпеса 7 типа.
Доступные в настоящий момент серологические тест-системы не позволяют дифференцировать варианты А и B вируса герпеса 6 типа.
По данным литературы, реинфекция вируса герпеса 6 типа наблюдается у больных с нарушенным иммунным статусом, иммуносупрессией (трансплантация органов, СПИД и др.)
Клиника вирус герпеса 6 типа
Клинически герпес 6-го типа характеризуется полиморфизмом и может проявляться под различными масками. Обусловлено это как формой инфекции, так и штаммовыми различиями вируса
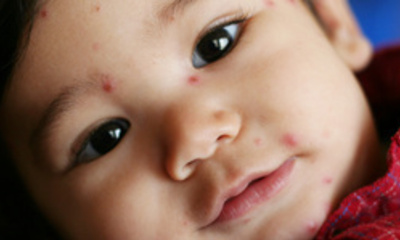
Так, к заболеваниям, ассоциированным с первичной острой вирус герпеса 6 типа инфекцией, относятся: синдром хронической усталости (миалгический энцефаломиелит); внезапная экзантема у новорожденных и более старших детей (roseola infantum exanthema subitum); судороги с фебрильной провокацией; инфекционный мононуклеоз у подростков и взрослых, не связанный с Эпштейна–Барр вирусной инфекцией (ВЭБ-инфекцией); гистиоцитарный некротический лимфаденит, некоторые заболевания центральной нервной системы (ЦНС), в частности энцефалит, ассоциированный с вирусом герпеса 6 типа и др.
Выделяют также заболевания, ассоциированные с персистентной вирусгерпеса 6 типа инфекцией, к которым относятся: лимфопролиферативные (иммунодефицит, лимфаденопатия, поликлональная лимфопролиферация); злокачественные лимфомы (неходжкинская лимфома, периферическая Т-клеточная лейкемия, В-клеточная лимфома, дерматопатическая лимфаденопатия, болезнь Ходжкина, синусоидальная В-клеточная лимфома, плеоморфная Т-клеточная лимфома).
Внезапная экзантема — это самая характерная манифестация первичной инфекции, обусловленной вирусом герпеса 6 типа. Она является, как считают большинство исследователей, главным проявлением первичной ВГЧ-6-инфекции. Типичное течение внезапной экзантемы характеризуется начальными проявлениями в виде высокой лихорадки, интоксикационного синдрома, лимфаденопатии с увеличением шейных и затылочных лимфоузлов. Сыпь появляется при снижении температуры. Иногда сыпь наблюдается перед тем, как снижается лихорадка, иногда после того, как в течение дня у ребенка отсутствовала температура.
Высыпания розовой окраски, до 2–3 мм в диаметре, они бледнеют при надавливании, редко сливаются, не сопровождаются зудом. Высыпания обычно сначала появляются на туловище с последующим распространением на шею, лицо, верхние и нижние конечности, в некоторых случаях они расположены преимущественно на туловище, шее и лице. Продолжительность высыпаний — от нескольких часов до 1–3 дней, исчезают бесследно.
По данным литературы, основными причинами поражения ЦНС в 20–27% является цитомегаловирус, в 10–15% — вирус Эпштейна–Барр, в 15–20% — вирус простого герпеса.
Известно, что герпетические поражения центральной нервной системы протекают особенно тяжело.
Болезни, обусловленные вирусом простого герпеса, занимают второе место после гриппа как причина смерти от вирусных инфекций. Анализ данных литературы последних лет, а также данных клинических наблюдений свидетельствует о том, что подавляющая часть случаев острых вирусных энцефалитов, особенно у детей, имеет герпетическую природу.
Неврологическими осложнениями вирус герпеса 6 типа инфекции, кроме фебрильных судорог, являются нейроинфекции (менингит, энцефалит), возможно развитие эпилепсии, однако данная тема является до конца не изученной.
Некоторые ученые предполагают вирус герпеса 6 типа как причину развития рассеянного склероза, синдрома полиорганной недостаточности, розового лишая, гепатита, вирусного гемофагоцитоза, идиопатической тромбоцитопенической пурпуры, синдрома чрезмерной чувствительности к лекарственным препаратам, особенно антибактериальным.
Таким образом, инфекция, обусловленная вирусом герпеса 6 типа, имеет особую актуальность на сегодняшний день. В последние годы были предприняты усилия специалистами различных медицинских профессий, как в нашей стране, так и за рубежом, по изучению строения вируса, методов диагностики инфекции, ее комбинаций с другими герпесвирусами, особенностей клинических форм и вариантов течения.
При распространении инфекции ведущая роль принадлежит ближайшему окружению. Выявлено наиболее частое сочетание вируса герпеса 6 типа с цитомегаловирусом. Актуальной является диагностика данной инфекции с преобладанием методик, основанных на выявлении ДНК вируса герпеса 6 типа в плазме и других средах организма.
Перспективно разрабатываются и другие методы диагностики (ИФА, энзимные методы и др.). Однако обязательно динамическое обследование, так как однократно взятый анализ оценить бывает трудно.
Инфекция, вызванная вирусом герпеса 6 типа, рассматривается на сегодняшний день как полиморфная. Прежде были описаны такие клинические ее проявления, как «внезапная экзантема», однако в последние годы выявлены симптомы поражения плода, различные формы поражения центральной нервной системы (менингиты, энцефалиты), длительные субфебрилитеты, респираторные формы. Однако значение вируса герпеса 6 типа в развитии гепатитов, судорожных состояний, эпилепсии и других форм у детей подлежит дальнейшему изучению.
Лечение вируса герпеса 6 типа
Сложность лечения заболеваний, вызванных вирусами герпеса, связана с генотипическими особенностями возбудителя, а также различной чувствительностью к препаратам. В последнее десятилетие исследования по изучению антивирусного действия некоторых препаратов показали, что вирусы герпеса 6,7,8 типа малочувствительны к аналогам нуклеозидов. С определенным успехом в лечении были использованы ганцикловир и фоскарнет . Однако препаратов, которые были бы достаточно эффективны в лечении инфекции, вызванной вирусами герпеса 6, 7, 8 типов, пока не найдено.
К основным этиотропным лекарственным средствам относят три группы препаратов: ациклические аналоги гуанозина, интерфероны и иммуноглобулины.
Ведущее место занимает противовирусная химиотерапия, представленная большой группой ациклических аналогов нуклеозидов. Иммунотерапия герпесвирусных инфекций, которая объединяет препараты интерферонов и иммуноглобулинов, является дополнительной, однако важной составляющей этиотропного лечения
Противовирусная химиотерапия
Обычно при инфекциях, вызванных альфа-герпесвирусами, более эффективным является ацикловир.
Бесспорными преимуществами ацикловира являются его высокая избирательность и низкая токсичность, а недостатками — неодинаковая эффективность при различных герпетических инфекциях, воздействие только на реплицирующийся вирус и возможность формирования резистентности к препарату. В порядке убывания чувствительности их можно расположить следующим образом: ВГЧ-1, ВГЧ-2, ВГЧ-3 > ВГЧ-4, ВГЧ-5 > ВГЧ-6, ВГЧ-7. Таким образом, ацикловир наиболее эффективен при инфекциях, вызванных вирусами простого герпеса 1-го и 2-го типа, а также вирусом Варицелла–Зостер (ВВЗ), а наименее — при патологии ВГЧ-6- и ВГЧ-7-этиологии. Отличия в чувствительности к ацикловиру обусловлены разным содержанием вирусной тимидинкиназы. У вирусов герпеса 6 и 7 типа количество данного фермента наиболее низкое, что обусловливает устойчивость к препарату. Ацикловир имеет ограниченную эффективность при Эпштейна –Барр вирусной инфекции и может быть полезен лишь в некоторых случаях инфекционного мононуклеоза, однако неэффективен при инфекциях, вызванных вирусом герпес 6,7 и 8 типов.
Валацикловир представляет собой L-валиновый эфир ацикловира. Препарат обычно хорошо переносится, побочные явления отмечаются редко. К валацикловиру, в отличие от ацикловира, чувствительны все виды герпесвирусов, однако наиболее высокая чувствительность — у представителей альфа-подсемейства. К недостаткам валацикловира относят отсутствие инфузионной формы препарата, что ограничивает его применение при тяжелых острых поражениях.
Ганцикловир — синтетический нуклеозидный аналог гуанозина. Механизм действия сходен с таковым у ацикловира, однако не требует активного участия вирусной тимидинкиназы, поэтому препарат применяют преимущественно при тех герпетических инфекциях, при которых недостаточно эффективен ацикловир (ВГЧ-4, ВГЧ-5, ВГЧ-6, ВГЧ-7). Существенным недостатком препарата является его сравнительно высокая токсичность, поэтому ганцикловир следует назначать строго по показаниям — при реактивированных формах указанных инфекций, которые приводят к тяжелым органным поражениям.
Новыми и многообещающими противогерпетическими химиопрепаратами являются цидофовир и бривудин. Эти лекарственные средства обладают более высокой эффективностью, чем ацикловир и ганцикловир, однако хуже переносятся, что ограничивает их широкое клиническое применение. Их следует использовать при тяжелых, угрожающих жизни формах герпесвирусных инфекций при условии известной или ожидаемой резистентности к ацикловиру и ганцикловиру.
К недостаткам противовирусной химиотерапии относится воздействие только на размножающийся вирус, невозможность полного избавления от инфекции, отсутствие эффекта последействия, ряд побочных эффектов (особенно у ганцикловира и вальганцикловира), развитие устойчивости к препарату. Причинами резистентности могут быть частое и нерациональное применение препаратов, наличие иммунодефицита, заражение устойчивым к лечению штаммом вируса. Учитывая все недостатки, монотерапия ациклическими аналогами гуанозина рекомендована только при легких формах герпесвирусных инфекций .
Среди других противовирусных препаратов наибольшую доказательную базу имеет инозин пранобекс
Иммунотерапия
Иммунотерапия не может полностью заменить противовирусную химиотерапию, однако добавление иммунотерапевтических препаратов позволяет повысить эффективность лечения, сократить курс терапии и предотвратить развитие устойчивости к ациклическим аналогам гуанозина.
Препараты бета-интерферонов показаны как средство базисной терапии при рассеянном склерозе с ремиттирующим течением. Лечение эффективно, по крайней мере, у 60% пациентов. Как известно, это аутоиммунное осложнение ассоциировано с инфекциями, вызванными вирусам Эпштейна - Барр и вирусом герпеса 6 типа. Противовирусный эффект бета-интерферонов, как минимум, в 10 раз выше, чем у альфа-интерферонов, однако более выраженный иммуносупрессивный эффект ограничивает их широкое применение. В случае нейроинфекций бета-интерфероны могут иметь определенные преимущества, поскольку снижают проницаемость гематоэнцефалического барьера.
Альтернативная терапия
Акупунктура, фитотерапия, биорезонансная терапия, ультрафиолетовое и лазерное облучение крови на сегодняшний день не имеют надлежащей доказательной базы при герпесвирусных инфекциях
Комплексное исследование, направленное на обнаружение генетического материала (ДНК) цитомегаловируса, вирус Эпштейна – Барр, вируса герпеса человека 6-го типа методом полимеразной цепной реакции в режиме реального времени.
Синонимы русские
Цитомегаловирус; ЦМВ; вирус Эпштейна – Барр; ЭБВ; герпес-вирус 6-го типа; ВГЧ-6; ДНК [полимеразная цепная реакция в режиме реального времени]; количественный анализ.
Синонимы английские
Cytomegalovirus; CMV; Epstein Barr-Virus; EBV; Human Herpes Virus 6; HHV-6; DNA [polymerase chain reaction, real-time PCR]; quantitative; qRT-PCR.
Метод исследования
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Ликвор, мазок из зева (ротоглотки), слюна, биоптат (биоптат лёгких, печени, ЖКТ), венозная кровь.
Общая информация об исследовании
Цитомегаловирус, вирус Эпштейна – Барр, вирус герпеса человека 6-го типа являются представителями семейства герпес-вирусов. Они обладают высокой патогенностью для человека, имеют способность к длительному латентному существованию, к персистенции в организме человека и могут вызывать заболевания с различными клиническими проявлениями.
Цитомегаловирус (Cytomegalovirus) относится к семейству герпес-вирусов человека, рода Cytomegalovirus и является возбудителем цитомегаловирусной инфекции. Цитомегаловирусная инфекция (ЦМВИ) – это широко распространенная инфекция человека, характеризующаяся легким, бессимптомным течением у людей в обычных условиях и с нормально функционирующей иммунной системой. Особое клиническое значение она приобретает у лиц с патологией иммунной системы, иммунодефицитными состояниями и у беременных женщин из-за риска внутриутробного инфицирования плода.
Цитомегаловирус является ДНКсодержащим вирусом, обладающим способностью к медленному распространению в культуре инфицированных клеток и приводящим к их изменению и увеличению размера (цитомегалии). Источником инфекции является человек, выделяющий вирус через различные биологические жидкости. К ним относятся кровь, слюна, моча, грудное молоко, цервикальный и вагинальный секрет, семенная жидкость, ликвор, содержимое желудочно-кишечного тракта и прочие секреты. Инфекция передается воздушно-капельным, контактным, половым путем, в результате переливания крови от инфицированного донора. Возможно также заражение при трансплантации органов и вертикальный путь передачи, от инфицированной женщины к ребенку во время беременности или родов. Длительность инкубационного периода заболевания часто установить невозможно, так как большинство клинических случаев не распознается и протекает в латентной, бессимптомной, форме.
Различают приобретенную и врождённую формы ЦМВИ. Приобретенная форма инфекции протекает в виде острого локализованного процесса, схожего по клинической симптоматике с острой респираторной вирусной инфекцией или инфекционным мононуклеозом. Отмечается повышение температуры тела, слабость, общее недомогание, боль в горле, миалгия, увеличение шейных лимфатических узлов. В редких случаях отмечаются осложнения в виде артралгий, артритов, пневмонии, цитомегаловирусного гепатита. У детей до трех месяцев жизни, а также у лиц с патологией иммунной системы (иммунодефицитными состояниями, ВИЧ-инфекцией, после трансплантации органов, лечения иммуносупрессивными препаратами, при злокачественных заболеваниях) ЦМВИ может протекать в тяжелой форме с развитием серьезных осложнений. При этом развиваются тяжелые поражения легких, почек, печени, желудочно-кишечного тракта, нервной системы с развитием вирусного энцефалита. Врождённая форма ЦМВИ возникает в результате трансплацентарной передачи инфекции от матери плоду при инфицировании женщины на ранних сроках беременности, особенно при первичном инфицировании. Развивается острая врождённая ЦМВИ, приводящая к самопроизвольному аборту или гибели эмбриона. При поражении плода на более поздних сроках беременности развивается геморрагический синдром с кровоизлияниями в кожу, внутренние органы, отмечается поражение нервной системы.
Вирус Эпштейна – Барр (EBV) относится к семейству герпес-вирусов (Herpesviridae) человека 4-й группы. Он представляет собой ДНКсодержащий лимфопролиферативный вирус. Его основной особенностью является способность реплицироваться преимущественно в В-лимфоцитах без последующего разрушения клеток.Помимо этого, вирус может инфицировать Т-лимфоциты и эпителиальные клетки.
Источником инфекции является больной человек или вирусоноситель. Путь передачи вируса – преимущественно воздушно-капельный. У 90-95 % населения некоторых стран выявляются антитела к антигенам вируса, что свидетельствует о предшествующем инфицировании вирусом. Острая инфекция обычно протекает бессимптомно у детей с нормально функционирующей иммунной системой, клинически проявляясь в виде инфекционного мононуклеоза у 30-50 % иммунокомпетентных подростков и взрослых. При патологиях иммунной системы, иммунодефицитных состояниях, при применении иммуносупрессивных препаратов возможно развитие разнообразных патологических процессов и заболеваний, вызванных вирусом Эпштейна – Барр. У таких больных присутствие вируса ассоциировано с развитием различных лимфопролиферативных нарушений и некоторых онкологических процессов, включающих лимфому Беркитта, назофарингеальную карциному, лимфогранулематоз (болезнь Ходжкина), В-клеточную лимфому. Также вирус обнаруживается у пациентов при некоторых аутоиммунных заболеваниях, синдроме хронической усталости.
Инфекционный мононуклеоз – это острое вирусное заболевание, причиной которого является вирус Эпштейна – Барр. В основном заболевание регистрируется у детей и лиц молодого возраста до 35 лет. Инкубационный период заболевания составляет в среднем 5-14 дней, иногда до 30 дней. К клиническим проявлениям заболевания относятся лихорадка, головная боль, поражение зева, нёбных, глоточных миндалин, лимфатических узлов (лимфоаденопатия), увеличение печени и селезенки. Заболевание может протекать в легкой, средней тяжести и тяжелой форме. К осложнениям инфекционного мононуклеоза относятся отиты, синуситы, паратонзиллиты, пневмонии, гепатиты. Редко могут встречаться разрывы селезенки, острая печеночная недостаточность, острая гемолитическая анемия, тромбоцитопения, миокардит, неврит, менингит, менингоэнцефалит. В редких случаях развивается хроническая активная инфекция, при которой симптомы заболевания сохраняются на протяжении более чем 6 месяцев после первичного инфицирования вирусом Эпштейна – Барр.
Вирус герпеса человека типа 6 (ВГЧ-6) представляет собой ДНКсодержащий вирус, относящийся к семейству герпес-вирусов человека. Он способен к репликации в Т-лимфоцитах, но может быть обнаружен в В-лимфоцитах, моноцитах, эндотелиальных клетках, гепатоцитах и ряде других. Источником инфекции является больной человек или вирусоноситель. Путь передачи вируса преимущественно воздушно-капельный. Возможна передача вируса вертикальным путем от матери к плоду во время беременности, при гемотрансфузиях, во время операций и при трансплантации органов.
Вирус способен проникать в лимфатическую систему и вызывать заболевания с разнообразной клинической симптоматикой. Чаще всего патологический процесс, вызванный ВГЧ-6, развивается у лиц с патологией иммунной системы, иммунодефицитными состояниями, в частности при ВИЧ-инфекции, при применении иммуносупрессивной терапии, после трансплантации органов, при аутоиммунных заболеваниях.
В большинстве случаев инфекция, вызванная ВГЧ-6, протекает бессимптомно. К основным клиническим проявлениям относятся лихорадка, экзантема в виде эритематозных пятен или пятнисто-папулезной сыпи. В некоторых случаях возможно развитие осложнений со стороны центральной нервной системы: судороги, энцефалит, менингоэнцефалит, серозный менингит. У иммунокопрометированных лиц инфекция характеризуется тяжелым течением, генерализацией процесса. Развиваются лимфаденопатии, пневмония, гепатит, энцефалит.
Диагностика вирусной инфекции, вызванной представленными вирусами, является комплексной и основана на оценке клинических проявлений заболеваний и лабораторных методов диагностики. Современные методы лабораторной диагностики играют важную роль в диагностики герпес-вирусных инфекций, особенно на ранних стадиях инфекционного процесса. К таким методам относится метод полимеразной цепной реакции в режиме реального времени. Полимеразная цепная реакция (ПЦР) – это метод молекулярной диагностики, позволяющий выявлять генетический материал возбудителя на ранних этапах заболевания. Он характеризуется высокими показателями диагностической чувствительности и специфичности, быстротой получения конечного результата и доступностью. Особенностью метода является возможность выявлять ДНК (дезоксирибонуклеиновую кислоту) бактерий даже при их малом содержании в исследуемом биологическом материале. Метод основан на многократном увеличении числа копий специфичного для данного возбудителя участка ДНК. Для диагностики может использоваться разнообразный биологический материал, взятый у детей, взрослых лиц, людей с патологией иммунной системы, беременных женщин. Метод позволяет определять количество молекул ДНК исследуемого вируса, что является важным в диагностике острой формы инфекции, реактивации персистентной инфекции, носительстве вируса, а также при контроле эффективности проводимой противовирусной терапии.
Для чего используется исследование?
- Для диагностики и подтверждения инфекционного процесса, вызванного цитомегаловирусом, вирусом Эпштейна – Барр, вирусом герпеса человека 6-го типа.
- Для диагностики острой или текущей вирусной инфекции.
- Для диагностики первичной инфекции и/или активной формы инфекции в период реактивации (обострения) персистентной инфекции.
- Для дифференциальной диагностики инфекций, вызванных герпес-вирусами.
- Для дифференциальной диагностики инфекций, протекающих с развитием ангин, тонзиллитов, высыпаниями, лихорадкой.
Когда назначается исследование?
- При диагностике и дифференциальной диагностике инфекций, вызванных герпес-вирусами.
- При клинических проявлениях заболеваний, вызванных цитомегаловирусом, вирусом Эпштейна – Барр, вирусом герпеса человека 6-го типа, или при их бессимптомном, латентном течении.
- При обследовании женщин, планирующих беременность, и женщин при патологиях имеющейся беременности.
- При комплексном обследовании пациентов с лимфопролиферативными заболеваниями и гемобластозами.
- При обследовании реципиентов органов и тканей до и после трансплантации, при проведении иммуносупрессивной терапии.
- При диагностике вирус-ассоциированных заболеваний у ВИЧ-инфицированных и при других иммунодефицитных состояниях.
- При контроле за эффективностью проведенного лечения противовирусными препаратами.
Что означают результаты?
ДНК CMV концентрация: не обнаружено.
ДНК EBV концентрация: не обнаружено.
ДНК HHV6 концентрация: не обнаружено.
* При положительном результате показатель выдается в копиях на миллилитр (копий/мл).
Причины положительного результата:
- Инфицирование цитомегаловирусом или носительство вируса.
- Инфицирование вирусом Эпштейна – Барр или носительство вируса.
- Инфицирование вирусом герпеса человека 6-го типа или носительство вируса.
Причины отрицательного результата:
- Отсутствие инфицирования цитомегаловирусом;
- Отсутствие инфицирования вирусом Эпштейна – Барр;
- Отсутствие инфицирования вирусом герпеса человека 6-го типа.
Также рекомендуется
- Cytomegalovirus, ДНК, количественно [реал-тайм ПЦР]
- Антитела к Cytomegalovirus (IgG) с определением авидности
- Определение авидности иммуноглобулинов класса IgG к капсидному антигену (VCA) вируса Эпштейна – Барр
Кто назначает исследование?
Терапевт, врач общей практики, инфекционист, аллерголог-иммунолог, акушер-гинеколог, неонатолог, педиатр, уролог, оториноларинголог, гематолог, невропатолог, хирург, онколог.
Читайте также:

