Трофические язвы на руках при диабете
Обновлено: 18.04.2024
Настоящая работа посвящена исследованию возможности повышения эффективности комплексной терапии трофических язв и послеоперационных ран нижних конечностей с помощью топического иммуномодулятора. В исследовании приняли участие 44 больных
Настоящая работа посвящена исследованию возможности повышения эффективности комплексной терапии трофических язв и послеоперационных ран нижних конечностей с помощью топического иммуномодулятора.
В исследовании приняли участие 44 больных от 30 до 81 года (30 женщин, 14 мужчин) с хроническими трофическими язвами нижних конечностей. Трофические язвы развились из-за нарушения кровообращения в нижних конечностях по причине тромбофлебита или диабетической ангиопатии. У большинства больных тромбофлебит возник как осложнение варикозной болезни. Диагноз «варикозная болезнь, посттромбофлебитический синдром (ПТФС)» был постановлен 41 больному. На момент исследования признаки острого тромбофлебита на фоне ПТФС имелись у 9 человек, признаки рожистого воспаления кожи — у 5 человек. У 1 больного трофическая язва сочеталась с остеомиелитом большой берцовой кости, у двоих — с начинающейся гангреной пальцев ноги. В анамнезе трое больных перенесли флебэктомию, 1 больная — склерозирующую терапию по поводу варикозного расширения вен.
У подавляющего большинства исследованных больных имелась 1 трофическая язва и лишь у двоих больных были 2 язвы. В большинстве случаев язвы располагались на передней, внутренней или внешней поверхности голени, у 2 больных диабетической ангиопатией язвенный процесс локализовался на стопе. Размеры трофических язв варьировали от 0,5х0,5 см до 3х4,5 см. Кратер язвы был заполнен фибринозными массами у 30 больных, фибринозно-гнойными — у 6 больных, гнойно-некротическими фрагментами ткани — у 5 пациентов. В трех случаях на момент поступления больного язва выглядела чистой, без фибринозных, гнойных или некротических масс.
У 5 больных некротически-буллезной формой рожи на коже голени были признаки острого воспаления, пузыри с серозно-гнойным содержимым. У 2 других больных отмечались признаки начинающейся гангрены: соответственно I и III пальцы правой стопы были синюшно-черного цвета.
Лечение
При лечении всех 44 больных соблюдались следующие принципы лечения:
- постельный режим с приподнятым положением больной конечности для устранения застоя крови и лимфы;
- тщательный туалет кожи вокруг язвы;
- создание тока тканевой жидкости из язвы в повязку в начале лечения. Для этой цели использовали повязки с гипертоническим раствором NaCl в сочетании со спиртовым раствором хлорофиллипта, что обеспечивало очищение язвы, улучшение питания живых тканей дна и стенок язвы;
- активация регенеративных способностей организма после очищения кратера язвы.
Все больные ПТФС получали общее и местное лечение. Общими составляющими лечения были инфузионная (реополиглюкин 200 мл + трентал 5 мл + аскорбиновая кислота 5 мл в/в капельно, через день № 5), эскузан по 15 капель 3 раза в сутки, аспирин 0,5 г — 1 раз в сутки, троксевазин по 2 капсулы 3 раза в сутки в течение 15 дней или диовенор 600 мг по 1 табл. 1 раз в сутки в течение 30 дней. В дополнение к вышеописанному лечению пациенты с признаками острого тромбофлебита получали инъекции раствора гепарина 5000 ЕД п/к 4 раза в сутки в течение 6 дней.
Местное лечение в первые дни (от 1 до 4 дней) — хлорофиллипт спиртовой в сочетании с гипертоническим раствором, перевязки делались каждый день. После очищения язвы накладывались повязки с мазью гепона или солкосерил (контрольная группа, 10 человек). Как отмечалось выше, у 3 больных язва не содержала фибринозных, гнойных или некротических элементов. У этих больных сразу начинали лечение мазью гепона — иммуномодулятора, обладающего способностью повышать эффективность иммунной защиты, а также прямым противовирусным действием.
Мазь изготавливалась непосредственно в аптеке ГКБ №1 и имела следующий состав: гепона 0,006; ланолина 10,0; масла оливкового 10,0; воды для инъекций 10,0. Готовую мазь хранили при +4°С, использовали в течение 10 дней.
Мазь наносили тонким слоем на поверхность трофической язвы, повязки с мазью гепона меняли через день. Лечение проводилось в течение 10 дней (5 перевязок).
Лечение неосложненных трофических язв
В контрольной группе 10 больных получали такую же общую терапию, но местное лечение после очищения язвы проводили мазью солкосерил. Заживление язв у больных этой группы происходило на 5–15 дней дольше, чем при применении мази гепона. У 1 больной контрольной группы в ходе лечения мазью солкосерил произошло ухудшение, развилось рожистое воспаление кожи (некротически-буллезная форма). Этой пациентке было назначено адекватное хирургическое лечение, в дополнение к общему лечению применялись антибиотик и бисептол, для местного лечения вместо солкосерила использовалась мазь гепона.
Лечение язвенных дефектов кожи после некрэктомии по поводу некротически-буллезной формы рожи
Больные с некротически-буллезной формой рожи в дополнение к инфузионной терапии получали инъекции цефазолина по 1 г в/м 3 раза в сутки в течение 7 дней, а также бисептол 480 мг по 1 табл. 3 раза в сутки в течение 10 дней. На фоне консервативного лечения проводили оперативное вмешательство — некрэктомию. Пузыри вскрывались, некротизированные ткани удалялись, открытая рана обрабатывалась раствором перманганата калия. Далее открывшиеся после некрэктомии большие дефекты кожи лечили гепоном, как трофические язвы. У всех больных отмечались хорошие результаты лечения. Через 3–4 дня после начала применения мази гепона наблюдался выраженный рост грануляционной ткани с последующим формированием соединительнотканного рубца в кратчайшие сроки.
Лечение послеоперационных ран нижних конечностей у больных диабетической ангиопатией
При лечении больных диабетической ангиопатией консервативное лечение дополняли адекватными дозами инсулина (п/к). В качестве антибиотика использовали линкомицин по 600 мг в/м 2 раза в сутки в течение 14 дней. При начинающейся гангрене пальца на фоне консервативного лечения проводили адекватное оперативное вмешательство — ампутацию или ограниченное иссечение некротизированных элементов. В послеоперационном периоде промывали рану и свищевые ходы раствором гепона (0,002 г в 10 мл физиологического раствора), а также накладывали повязки с мазью гепона, как описано выше. Результаты лечения свидетельствуют о значительной активации роста грануляционной ткани и ускоренном заживлении послеоперационной раны под влиянием гепона.
Очевидно, что применение гепона в описанных выше клинических случаях стимулировало активный рост грануляционной ткани. Обычно у больных диабетической ангиопатией проходимость капиллярного русла оказывается минимальной, во время хирургических манипуляций кровь выделяется, как правило, только из подкожных сосудов, внутренние ткани практически обескровлены, имеют бледно-розовый цвет. Рост грануляционной ткани у таких больных либо не отмечается вовсе, либо протекает очень вяло, послеоперационные раны хронически не заживают, остаются трофические язвы. Применение гепона позволило добиться ускоренного заживления послеоперационных ран и незаживающих язв у больных диабетической ангиопатией.
Литература
Клинический пример
Больная О. Л. О., 52 года (ИБ № 5039).
Диагноз при поступлении: варикозная болезнь, посттромбофлебитический синдром, трофическая язва правой голени.
Диагноз окончательный: варикозная болезнь, посттромбофлебитический синдром, трофическая язва правой голени. Рожистое воспаление правой голени (некротически-буллезная форма).
Жалобы при поступлении: боли в области правой голени, усиливающиеся при ходьбе, наличие трофической язвы на передней поверхности нижней трети правой голени.
Anamnesis morbi: считает себя больной в течение 20 лет, когда впервые появились варикозные расширения вен правой голени. Неоднократно лечилась по поводу данного заболевания у ангиохирурга по месту жительства, от оперативного лечения отказывалась. Трофическая язва появилась около месяца назад, попытки самостоятельно лечиться облегчения не принесли, обратилась в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: детских болезней не помнит, болезнь Боткина, туберкулез, наличие венерических заболеваний у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен.
Status praesens objectivus: общее состояние больной удовлетворительное, сознание ясное, положение в постели активное. Больная повышенного питания, костно-мышечная система без патологии. Кожа и видимые слизистые обычной окраски. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких дыхание везикулярное, ЧДД 16 в 1 мин. Тоны сердца ритмичные, пульс 68 уд. в 1 мин, АД 130/80 мм рт. ст. Язык влажный, розовый, живот мягкий, безболезненный, печень — по краю реберной дуги, селезенка не пальпируется, симптом «поколачивания» отрицателен с обеих сторон. Физиологические отправления в норме.
Locus morbi: правая нижняя конечность отечна, голень синюшного цвета, болезненна при пальпации. На передней поверхности нижней трети голени трофическая язва 2х2 см, края гиперемированы, в кратере фибринозное отделяемое.
Анализы: кровь на RW — отрицательная; биохимический анализ крови — белок 54 г/л, креатинин 76 мкмоль/л, мочевина 5,5 ммоль/л, остаточный азот 25 ммоль/л, диастаза 20 г/(ч/л), билирубин 16 — 4 — 12 мкмоль/л, глюкоза 3,2 ммоль/л; коагулограмма — протромбин 85%, фибриноген 3,2 мкмоль/л, время рекальцификации 90 с; общий анализ крови: Э — 5,5 млрд./мл, Л — 6,4 млн./мл, Hb — 115 г/л, цветной показатель — 0,92, СОЭ — 25 мм/ч; общий анализ мочи — норма.
Лечение: раствор гепарина по 5000 ЕД п/к каждые 6 ч, аспирин 0,25 г по 1 табл. 1 раз в день; местно трофическую язву обрабатывали спиртовым раствором хлорофиллипта, поверхность язвы 2 раза в день смазывали мазью троксевазин, на ночь — мазью солкосерил. Через 5 дней лечения общее состояние пациентки значительно ухудшилось, температура тела повысилась до 39,5°С. Кожные покровы правой нижней конечности резко гиперемированы, гипертрофированы, болезненны. Установлен диагноз: рожистое воспаление правой нижней конечности.
Коррекция лечения: цефазолин по 1 г 2 раза в сутки, бисептол 480 мг по 1 табл. 3 раза в сутки. Через двое суток в области пораженной конечности появились пузыри с серозной жидкостью, под которыми впоследствии образовались участки некроза дермы (некротически-буллезная форма рожи).
Ввиду отсутствия положительного эффекта от предшествующей терапии, у больной проведено лечение с применением гепона.
Местно — произведено рассечение пузырей, удаление некротических элементов тканей. Были назначены ванны с перманганатом калия, инфузионная терапия (реополиглюкин 200 мл + трентал 5 мл + аскорбиновая кислота 5 мл в/в капельно, через день № 5), эскузан по 15 капель 3 раза в сутки, аспирин 0,5 г — по 1 табл. 1 раз в сутки, троксевазин по 2 капсулы 3 раза в сутки в течение 15 дней или диовенор 600 мг по 1 табл. 1 раз в сутки в течение 30 дней.
Locus morbi на момент начала терапии гепоном: по передней поверхности правой голени 3 язвенных дефекта кожи 10х10 см, раны заполнены фиброзно-гнойным отделяемым. После санации раневой поверхности раствором риванола применялись повязки с гепоном. Смена повязок проводилась через день. Уже после второй перевязки появился значительный рост грануляционной ткани, к концу лечения (всего 5 перевязок в течение 10 дней) раны очистились. Проведена операция аутодермопластики марочным способом (15 марок). Гепон в виде мази продолжали применять на всей послеоперационной поверхности. На фоне применения гепона «прижились» все 15 марок, в кратчайшие сроки сформировался рубец.
Клинический пример
Больная К. Л. Н. , 78 лет (ИБ № 6784).
Диагноз при поступлении: облитерирующий атеросклероз сосудов нижних конечностей. Сахарный диабет.
Диагноз окончательный: сахарный диабет III степени. Диабетическая ангиопатия нижних конечностей. Начинающаяся гангрена III пальца (ногтевая фаланга) правой стопы.
Жалобы при поступлении на постоянные боли в нижних конечностях, особенно в области III пальца правой стопы, общую слабость, недомогание.
Anamnesis morbi: считает себя больной около 20 лет, когда впервые был обнаружен сахарный диабет. Неоднократно лечилась в эндокринологическом и хирургическом стационарах. Последнее обострение началось 3 недели назад, когда появились перечисленные выше жалобы. Попытки самостоятельного лечения оказались безрезультатными, обратилась в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: аппендэктомия в 1950 году. Болезнь Боткина, туберкулез, венерические заболевания у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен. Отмечает длительно протекающие гнойные процессы при любых незначительных травмах.
Status praesens objectivus: общее состояние средней тяжести, сознание ясное, положение в постели активное. Больная обычного питания, костно-мышечная система без патологии. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких — везикулярное дыхание, ЧДД 16 в 1 мин. Тоны сердца ритмичны, слегка приглушены, Ps 68 уд. в 1 мин, АД 130/90 мм рт. ст. Язык слегка суховат, живот правильной формы, участвует в акте дыхания, при пальпации безболезненный. Симптомы раздражения брюшины отрицательны. Печень по краю реберной дуги, селезенка не пальпируется. Симптом «поколачивания» отрицателен с обеих сторон. Физиологические отправления в норме.
Locus morbi: кожные покровы обеих нижних конечностей бледные, сухие. На стопах кожа прохладная на ощупь. Кожа III пальца правой стопы в области ногтевой фаланги синюшно-черного цвета. Движения в пальце сохранены.
Анализы: RW — отрицательная. Общий анализ крови: Э — 4,2 млрд./мл, Л — 9,2 млн./мл, Hb — 105 г/л, цветной показатель — 0,95, СОЭ — 17 мм/ч. Биохимия крови: глюкоза (при поступлении) 18,5 ммоль/л, глюкоза (после коррекции) 5,4 ммоль/л; билирубин 20,3–5,8–14,5 мкмоль/л, АЛТ — 0,43 ммоль/(ч/л), АСТ — 0,3 ммоль/(ч/л). Общий анализ мочи — норма. Коагулограмма: протромбиновый индекс 90%, фибриноген 8,8 мкмоль/л, время рекальцификации 100 с.
Лечение: инъекции инсулина (п/к) 28 ЕД утром, 16 ЕД вечером, раствора линкомицина 600 мг в/м 3 раза в сутки в течение 14 дней. Инфузионная терапия (реополиглюкин 200 мл + трентал 5 мл + актовегин 5 мл в/в капельно, через день № 5).
Местно — в III палец правой стопы под жгутом ввели линкомицин. Ночью после инъекции в области III пальца появились «дергающие» боли. Утром в области некроза кожи произведен овальный разрез длиной около 2,5 см, иссечены некротические элементы в области лизированного участка ногтевой фаланги, удалены секвестры, поставлен резиновый выпускник, наложена асептическая повязка. Со следующего дня начали накладывать повязки с мазью гепона, перевязки проводили через день №5. Во время перевязок удалялись некротические элементы до «живой» ткани. Ампутации пальца удалось избежать. Последующее лечение прошло успешно по типу лечения костного панариция. Отмечались быстрое очищение раны, энергичный рост грануляционной ткани и формирование рубца из соединительной ткани.
Клинический пример
Больная Б. Л. А., 65 лет (ИБ № 4571).
Диагноз при поступлении: диабетическая ангиопатия сосудов нижних конечностей, начинающаяся гангрена I пальца правой стопы.
Диагноз окончательный: сахарный диабет II типа средней тяжести в стадии декомпенсации. Диабетическая ангиопатия нижних конечностей. Начинающаяся гангрена I пальца правой стопы. Диабетическая нефропатия I степени.
Жалобы при поступлении: постоянные боли в области правой стопы, черный цвет кожных покровов I пальца правой стопы, общая слабость и недомогание.
Anamnesis morbi: считает себя больной около 20 лет, когда впервые был выявлен сахарный диабет. Неоднократно лечилась в эндокринологическом отделении. Перечисленные выше жалобы появились около 2 недель назад. Пыталась лечиться самостоятельно — без результата. Обратилась за помощью в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: детских болезней не помнит. Болезнь Боткина, туберкулез, венерические заболевания у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен. Периодически отмечает боли в области сердца, повышения АД.
Status praesens objectivus: общее состояние удовлетворительное, сознание ясное, положение в постели активное. Больная повышенного питания. Кожные покровы бледные, костно-мышечная система без патологии. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких — везикулярное дыхание, ЧДД 16 в 1 мин. Тоны сердца приглушены, ритмичны, Ps 82 удара в 1 мин, АД 140/80 мм рт. ст. Живот мягкий, при пальпации безболезненный. Печень по краю реберной дуги, селезенка не пальпируется. Симптом «поколачивания» с обеих сторон отрицателен. Физиологические отправления в норме.
Locus morbi: обе голени и стопы прохладные на ощупь. Пульсация на A.dorsalis pedis значительно ослаблена. I палец правой стопы в области ногтевой и средней фаланг синюшно-черного цвета, движения в пальце сохранены.
Анализы: RW — отрицательная; Э — 3,2 млрд./мл, Л — 13,5 млн./мл; Hb — 104 г/л, цветной показатель — 0,97; СОЭ — 56 мм/ч; протромбин — 100%, фибриноген 4,8 мкмоль/л, время рекальцификации 90 с: глюкоза крови 12,5 ммоль/л; общий анализ мочи — Л на все поле зрения.
Реовазография — общий кровоток правой голени снижен, левой голени достаточный. Тонус сосудов повышен. Затруднен венозный отток, больше справа.
Лечение: операция — ампутация I пальца правой стопы с головкой I плюсневой кости.
Режим II, диета 9. Инъекции инсулина (п/к) 26 ЕД утром, 16 ЕД вечером. Инъекции раствора линкомицина 600 мг в/м 3 раза в сутки в течение 14 дней. Местно — перевязки со спиртовым раствором хлорофиллипта, затем мазью левомиколь.
Locus morbi на момент начала лечения гепоном: послеоперационная рана в области I пальца правой стопы до 3 см в диаметре, имеется свищевой ход к культе плюсневой кости с гнойным отделяемым. Лечение препаратом гепон включало промывания свищевого хода и послеоперационной раны раствором гепона (0,002 г в 10 мл физиологического раствора). Процедуры с использованием гепона повторяли через день, всего 5 процедур в течение 10 дней. На 6-й день лечения гепоном из свищевого хода был извлечен секвестр. На 10-е сутки рана очистилась и уменьшилась в диаметре до 1,5 см. Края раны сцеплены лейкопластырем по типу наводящих швов. Продолжено лечение мазью гепона. К 14-му дню появилась грануляционная ткань, но из свищевого хода продолжали выделяться секвестры культи плюсневой кости. К 30-му дню рана зажила вторичным натяжением.
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
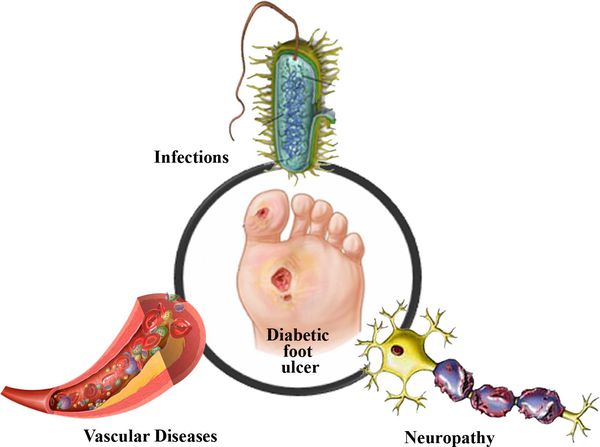
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
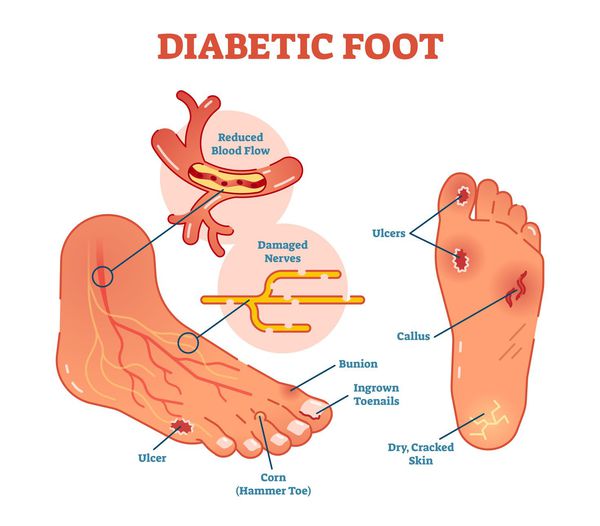
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
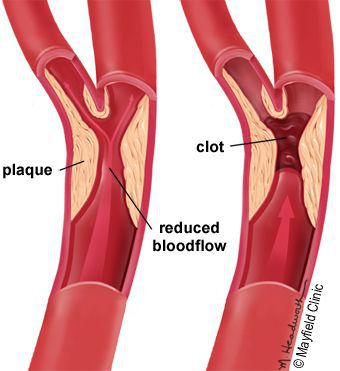
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
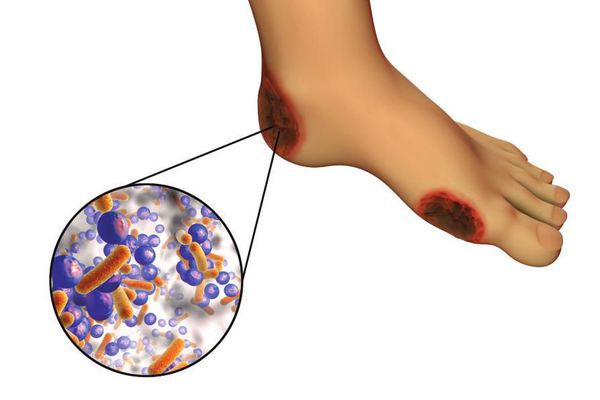
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
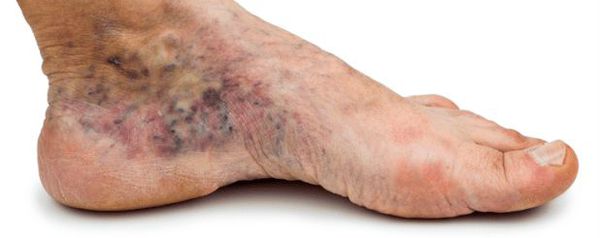
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
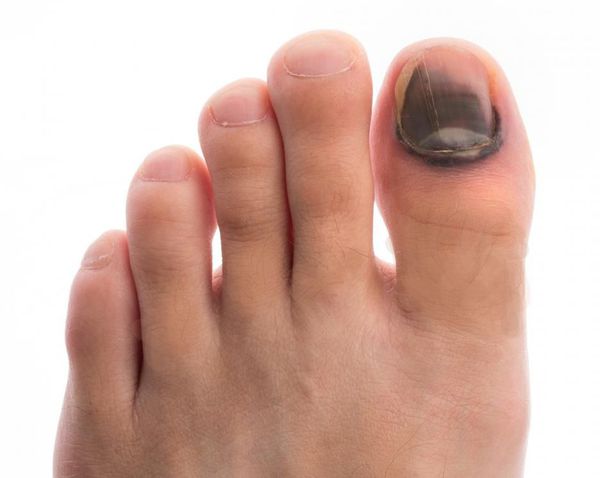
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
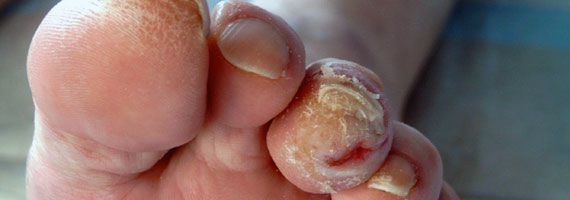
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
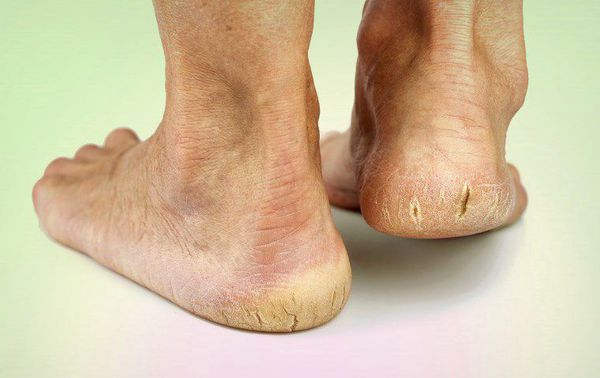
- трофические язвы, длительно не заживающие на стопах.
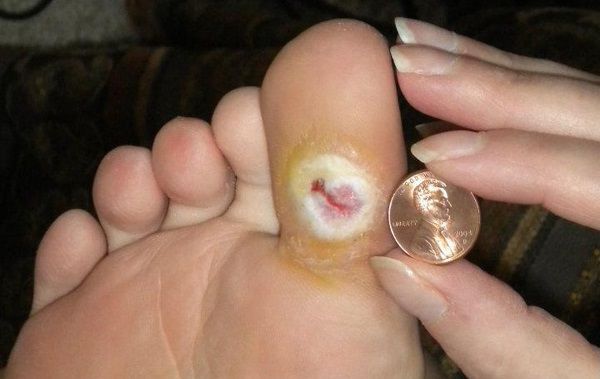
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
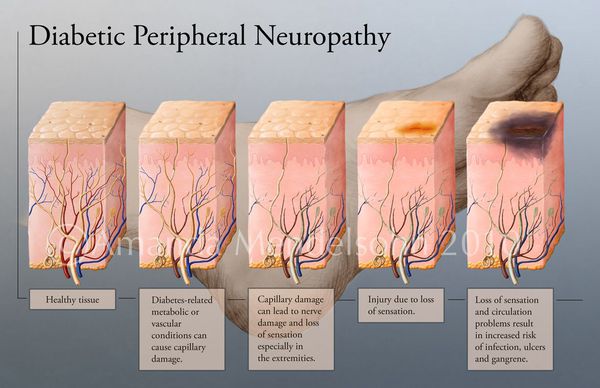
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
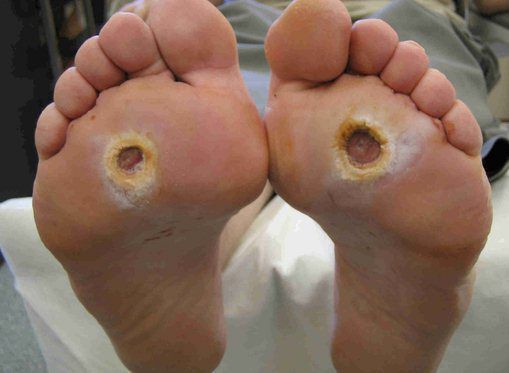
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
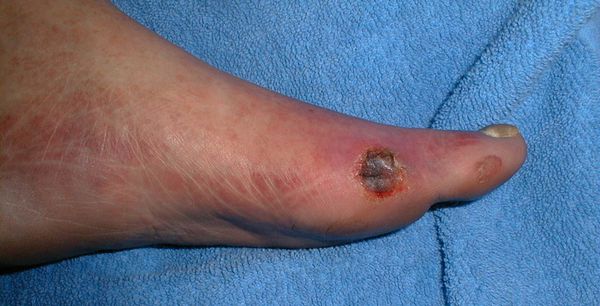
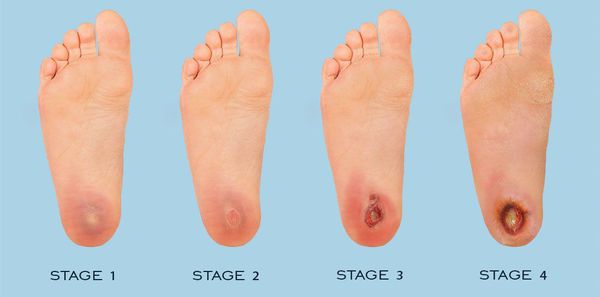
Классификация Вагнера
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.

26 Апр Трофические язвы на руках: диагностика и лечение
Трофические язвы в области верхних конечностей представляют кожный дефект различной длины и формы, возникают в результате нарушения метаболических процессов в тканях и не заживают в течение длительного времени (больше полугода).
Чаще всего данная патология развивается у лиц старшего возраста, это связано с истончением сосудистых стенок, длительным течением хронических заболеваний, сопровождаемых кожным синдромом.
Причины
Основной причиной развития таких дефектов являются не только заболевания сосудистого характера. Нередко трофические язвы возникают на фоне новообразований, локализованных в подмышечных лимфатических узлах, подключичных и средостенных. Кроме этого, травмы различного характера (колотые, резаные, рубленые, укушенные), инфекционно-воспалительные заболевания (ветряная оспа, глистные инвазии), патологии иммунной системы, системные заболевания соединительной ткани (красная волчанка, васкулиты), сепсис вызывают усугубление кожного синдрома и развитие язвенных дефектов на руках.
Механизм образования
В результате воздействия причинного фактора давление в венозных капиллярах верхних конечностей повышается, и они начинают изменять свою форму и направление. Они становятся извитыми, истонченными. Увеличивается их проницаемость, происходит отложение фибрина, кровяных сгустков между венозными сосудами. Это приводит к гипоксии (низкому уровню насыщения кислородом кровеносных сосудов). Уровень кровообращения резко снижается, вызывая ишемию (недостаточность кровообращения). Длительное отсутствие нормального кровообращения провоцирует развитие некротических процессов. На руках образуются бляшки различной формы, которые со временем либо высыхают и переходят в сухой вид некроза или начинают быстро увеличиваться, достигая больших размеров.
Клиническая картина
Основным ключевым симптомом является боль в руках в месте локализации язвы. На начальных этапах она может приносить дискомфорт, но со временем боль усиливается, становится жгучей или давящей. Кроме боли возникает зуд, покраснение и отечность. При инфекционном происхождении язвы повышается температура тела. На кожных покровах руки из-за истончения капилляров может проступать мелкая сеточка из сосудов, видимая невооруженным глазом.
Диагностика
Диагностика трофических язв на руках заключается в тщательном сборе данных о развитии основного заболевания. При осмотре врач определяет характер язвенного дефекта, связывая его с причиной его развития. После этого проводятся лабораторные и инструментальные методы исследования.
К лабораторным методам относят общий анализ крови. С его помощью определяют наличие заболеваний крови (анемии), наличие воспаления (повышается уровень лейкоцитов и скорости оседания эритроцитов), наличие онкологического очага (молодые и зрелые формы клеток крови).
Кроме общего анализа крови проводят микробиологические посевы на различные среды. Это необходимо для определения инфекционного возбудителя и назначения соответствующих антимикробных лекарственных средств.
Также при наличии иммунологических патологий проводят иммуноферментный анализ.
С его помощью определяют наличие чужеродных частиц.
К инструментальным методам относят: ультразвуковую диагностику и компьютерную томографию. С их помощью определяют ток крови в сосудах, наличие патологических новообразований и участков ишемии.
Лечение
После выявления основной причины, которая привела к развитию трофических язв на руках, осуществляют выбор адекватных терапевтических мероприятий.
С антибактериальной целью назначают антибиотики — Цефтриаксон, Амоксициллин, Тетрациклин.
Для укрепления сосудов и восстановления нарушенного кровотока используют Венарус, Детралекс.
При неглубоких / поверхностных язвенных дефектах ля местного применения рекомендовано использование заживляющих мазей. К ним относят Цинковую мазь, Аргосульфан, Солкосерил и Левомеколь.
Хирургическое лечение заключается в иссечении краев язвы, промывании антисептическими препаратами (Бетадин, Фурациллин). При наличии гнойного содержимого устанавливают дренаж.
Синдром диабетической стопы (СДС) — патологическое состояние стопы при сахарном диабете, возникающее на фоне поражения периферических нервов, кожи и мягких тканей, костей и суставов и проявляющееся острыми и хроническими язвами, костно-суставными поражениями и гнойно-некротическими процессами.
Нейроишемическая форма синдрома диабетической стопы возникает вследствие поражение артерий и нервных волокон нижних конечностей.

Рисунок 1. Синдром диабетической стопы, нейроишемическая форма. Некроз постампутационной раны левой стопы.
Поражение сосудов является причиной ранней смерти и инвалидизации среди пациентов с сахарный диабетом. Число ампутаций нижней конечности в связи с сосудистыми осложнениями сахарного диабета превышает число нетравматических ампутаций.
Так в Санкт-Петербурге, по данным «Городского центра диабетической стопы», за 2011 год у 31000 находящихся на учете пациентов выполнено 628 ампутаций. Ишемическая форма СДС, в отличие от атеросклеротического поражения сосудов, характеризуется поражением артериальных сосудов любого диаметра, в виде микро- и макроангиопатии.
Для этой формы поражения характерно сочетание 2-х патогенетических механизмов: диабетической ангиопатии и нейропатии. Соответственно, для клинической картины этой формы характерно сочетание как сосудистых, так и неврологических признаков поражения конечностей со взаимным отягощением.
Ряд авторов предлагает рассматривать всех пациентов с синдром диабетической стопы как пациентов с нейроишемической формой диабетической стопы, с преобладанием ишемического или неврологического компонента.
Снижение болевой чувствительности на фоне ангиопатии приводит к появлению очагов ишемического некроза без развития адекватного болевого синдрома. При анализе факторов, явившихся пусковыми для гнойно-некротических осложнений синдром диабетической стопы, необходимо отметить следующие:
- тривиальное повреждение кожи
- формирование микротромбов и закупорка мелких артериол
- окклюзия магистральной артерии с развитием критической ишемии.
Сочетание нейропатии и ангиопатии у пациентов с нейроишемической формой синдрома диабетической стопы делают механизмы отграничения местного инфекционного процесса несостоятельными, в связи с чем увеличивается риск прогрессирования гнойно-некротических осложнений и ампутации.

Рисунок 2. Синдром диабетической стопы, нейроишемическая форма. Окклюзия подколенной артерии справа. Обширная инфицированная рана подошвенной поверхности правой стопы.
Патогенез
Диабетическая ангиопатия, в отличие от атеросклеротичесой, характеризуется дистальным типом поражения сосудов, кроме того, окклюзии являются многосегментарными и протяженными – поражаются преимущественно артериальные сегменты ниже коленного сустава.
Морфологическая картина диабетической ангиопатии специфична, и имеет следующий вид: наличие бляшек на интиме, кальцифицирующий склероз Менкеберга, диффузный фиброз интимы.
Снижение перфузии тканей вызывает, как правило, неоангиогенез и появление коллатерального кровообращения; но у пациентов с сахарным диабетом вследствие дисфункции эндотелия развитие коллатералей недостаточно. Микроангиопатия, главным образом, проявляется поражением сосудов капиллярного русла.
Для патологической картины микроангиопатии характерны следующие особенности:
- Утолщение базальной мембраны.
- Нарушение миграции форменных элементов крови.
- Функциональная ишемия – невозможность адекватной гиперемии в ответ на поражение.
- Эндотелиальная дисфункция.
Эти изменения возникают вследствие нарушения синтеза вазоактивных веществ: эндотелина, простагландинов, простациклина и оксида азота (NO).
Наиболее значимым является NO, который влияет на гладкомышечные клетки сосудов посредством активации энзима гуанилат-циклазы, регулируя тем самым размеры просвета артерии. И в случае развития воспалительного процесса, позволяющий увеличить приток крови к очагу.
На внутриклеточном уровне в эндотелиоците происходят нарушения в механизмах активации внутриклеточных ферментов (протеинкиназы С, натрий- калиевой АТФазы, полиАДФ-рибозы полимеразы), которые наступают еще до клинического проявления сахарного диабета и связаны с инсулинорезистентностью.
Дисфункция эндотелия также является причиной тромбозов (в большей степени капиллярного русла) у пациентов с сахарным диабетом. Утолщение базальной мембраны капилляров является структурным проявлением микроангиопатии.
Данные изменения зависят от уровня и продолжительности гипергликемии. Изменение базальной мембраны сосуда приводит к нарушению миграции лейкоцитов, что проявляется в виде уменьшения эффективности воспалительной реакции в области очага повреждения.
Клиническая картина
Клиническая картина проявляется «зябкостью» и/или «усталостью» в ногах, болью в икрах. Однако болевой синдром с явлениями перемежающейся хромоты у пациентов с синдромом диабетической стопы проявляется значительно позже, по сравнению с пациентами, страдающими хронической артериальной недостаточностью нижних конечностей без сахарного диабета.
При объективном осмотре обращает на себя внимание холодность кожных покровов на ощупь. Также могут иметься трофические расстройства в виде пигментных пятен, выпадения волос на голенях, истончения кожи, язвенных дефектов разного размера, деформации ногтевых пластинок, наличия распространенного микоза стоп.

Рисунок 3. Синдром диабетической стопы, нейроишемическая форма. Окклюзия артерий левой голени. Некроз 2 пальца левой стопы.
В отличие от нейропатической формы синдрома диабетической стопы, болевой синдром может проявляться периодически и быть различной интенсивности, вплоть до нестерпимых болей, на поздних стадиях критической ишемии.
У больных с гнойно-некротическими осложнениями синдрома диабетической стопы деструктивные изменения на стопе развиваются на фоне «полного благополучия» и отсутствия жалоб.
При нарушении магистрального кровотока формируется некроз участка стопы согласно ангиосомальному принципу, предполагающему зональность кровоснабжения.
Лечение
Основной стратегией лечения гнойно-деструктивных поражений стопы у больных сахарным диабетом является мультидисциплинарный подход. В лечении пациента участвуют следующие врачи-специалисты: хирург, ангиохирург, рентген-хирург, ортопед, подиатр, кардиолог, невролог, эндокринолог, анестезиолог-реаниматолог, нефролог.
Такое количество специалистов связано с множественностью поражения органов-мишеней при сахарном диабете. Консервативная терапия ГНО СДС применяется для достижения следующих целей: компенсации сахарного диабета, улучшения перфузии мягких тканей, снижение проявлений нейропатии, разгрузки пораженной конечности, купирования явлений острого воспаления, стимуляции местных репаративных процессов.
Тактика лечения основывается на объективном состоянии пациента, характеристике гнойно-некротических осложнений и прогнозе течения заболевания. Первой необходимостью в лечении гнойно-некротических осложнений синдрома диабетической стопы является коррекция проявлений сахарного диабета, а именно гликемии; оптимальным считается показатель от 5 до 9 ммоль/л.
Высокий уровень гликемии коррелирует с увеличением послеоперационных осложнений и медленно прогрессирующим течением раневого процесса. Кроме того, кетоацидоз, как проявление декомпенсации сахарного диабета, является благоприятным фактором для диссеминации инфекции.
Важным фактором, определяющим тактику лечения, является выраженность инфекционного поражения. По тяжести течения инфекцию стопы принято разделять на легкую, умеренную и тяжелую степени.
КОНСЕРВАТИВНАЯ ТЕРАПИЯ
Противомикробная терапия
Выбор противомикробной химиотерапии должен учитывать стадию основного заболевания и степень тяжести инфекционного процесса вследствие их взаимного отягощения.
В связи с существованием в ране полимикробного пейзажа необходимо назначение как минимум одного антибиотика широкого спектра действия и химиопрепарата, воздействующего на анаэробные микроорганизмы. Антибактериальное лечение корректируется по данным микробиологического исследования и антибиотикограммы. Применяется ступенчатая терапия с переходом от парэнтерального к пероральному способу введения.
Длительность антибиотикотерапии зависит от возбудителя, реакции организма и течения заболевания. Так, при консервативном лечении хронического остеомиелита костей стопы длительность приема антибиотиков может составлять до 90 дней.
Противомикробная химиотерапия обязательно должна включать сочетание системных и местных противогрибковых препаратов в связи с наличием более, чем у половины больных сахарным диабетом микоза стоп.
Вазоактивные препараты
Для лечения явлений ишемического поражения применяются вазоактивные препараты: пентоксифилин, трентал, солкосерил, простагландин Е1, реополиглюкин. Способ введения: внутривенный или внутриартериальный селективный.
По данным международных исследований эти препараты не влияют на прогноз заболевания и имеют положительный эффект применения только лишь у 40% больных, но рекомендованы для использования при хронической артериальной недостаточности.
Разгрузка стопы
При лечении неинфекционных язвенных дефектов у пациентов с удовлетворительным парциальным давлением кислорода в тканях одна лишь разгрузка стопы позволяет добиться 80-90% заживления язвы, поэтому применение специальной обуви, ортезов, костылей, иммобилизационных повязок и т.д. является необходимым компонентом комплексной терапии.
Местное лечение
Местное лечение язвенных дефектов или ран должно быть направлено на профилактику и подавление инфекционного поражения, а так же на стимулирование репаративных процессов.
Обработка раны осуществляется на основании принципов ведения гнойных ран. Однако согласно рекомендациям по лечению гнойно-некротических осложнений у пациентов с СДС следует отдавать предпочтение более сильным антисептикам: раствор диоксидина 0,05%, раствор йод-повидона, октенисепта, пронтосана, гипохлорита.
Также важным является применение атравматических гидроколлоидных, адсорбирующих, ранозаживляющих повязок.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Тактика хирургического лечения гнойно-некротических осложнений СДС базируется на прогнозе возможного исхода. Целью хирургического лечения может быть: сохранение жизни пациента или сохранение конечности.
Принятие решения основывается как на клинических проявлениях тяжести поражения конечности, так и на стадии основного заболевания. Неблагоприятное течение ГНО СДС и тяжелое состояние пациента даже при небольшом очаге поражения зачастую заставляет применять агрессивную тактику (санационные ампутации при развитии септического процесса) (см. рисунок 4).

Рисунок 4. Санационная ампутация левой стопы при ее тотальном некрозе.
Оперативное пособие может быть выполнено в экстренном, срочном и плановом порядке. Согласно Гостищеву В. М. сроки оперативного лечения определяются показаниями, и могут быть жизненными, абсолютными и относительными.
Показаниями к экстренным оперативным (по жизненным показаниям) вмешательствам являются: влажная гангрена стопы, пальцев или голени, флегмона стопы или наличие гнойно-некротического процесса на стопе с явлениями полиорганной недостаточности. Экстренные операции имеют своей основной задачей сохранение жизни пациента за счет удаления патологического очага, поэтому достаточно часто выполняются операции ампутации.
Важным моментом является оценка системной воспалительной реакции. При наличии 2 и более баллов по уровню системной воспалительной реакции (например тахикардия и лейкоцитоз, лейкоцитоз и повышение температуры более 38) показано проведение экстренной санации гнойно-некротического очага.
Важно отметить, что в случае присутствии ишемии конечности, показано проведение реваскуляризации конечности в ближайшие часы после санационной некрэктомии (ампутации), при наличии участков конечности, которые еще возможно спасти.
Срочному оперативному (по абсолютным показаниям) лечению подвергаются пациенты с явлениями критической ишемии нижних конечностей с хроническим ранами/язвами без адекватного дренирования, с хроническим остеомиелитом и деструкцией костей, некрозами участков стопы или голени без явлений восходящего воспаления – т.е. пациенты с умеренной степенью тяжести инфекционного поражения (см. рисунок 5).

Рисунок 5. Синдром диабетической стопы, нейроишемическая форма. Окклюзия артерий правой голени. Остеомиелит костей правой голени.
Показаниями к плановым операциям являются: изменения конфигурации стопы с образованием точек избыточного давления (и развитее трофической язвы), хронический остеомиелит костей стопы, наличие обширного поверхностного дефекта мягких тканей (см. рисунок 6).

Рисунок 6. Синдром диабетической стопы, нейроишемическая форма. Окклюзия поверхностной бедренной, подколенной артерий справа. Некроз пяточной кости правой стопы.
Показаниями к ампутации являются: прогрессирующая гангрена стопы, хронический остеомиелит с обширной деструкцией костей, обширные дефекты мягких тканей, нарушение опороспособности стопы без возможности ее восстановления.
Следует отметить, что предпочтительными являются экономные ампутации на уровне стопы, так как пятилетняя выживаемость у пациентов, перенесших высокие ампутации, составляет от 28 до 32 %, а риск контралатеральной ампутации в течение 2 лет 40-52%.
В г. Санкт-Петербурге за 2011 по данным Центра Диабетической стопы (в центре наблюдается 31000 больных с СДС) выполнено 628 ампутаций, 53% из них — высокие ампутации. Перед выполнением ампутации на том или ином уровне необходима оценка поражения сосудов нижних конечностей и заключение ангиохирурга с оценкой реконструктабельности данного поражения.
При возможности производится оперативная коррекция с восстановлением магистрального кровотока к участку гнойно-некротического поражения. Восстановление артериального кровотока в очаге необходимо для заживления послеоперационной раны, так как снижение парциального давления кислорода в тканях ниже 40% (ниже 34 мм.рт.ст. по данным транскутанной оксиметрии) приводит к невозможности процессов репарации и подавления инфекции.
Поэтому уровень ампутации определяется наличием или возможностью восстановления кровотока в остающейся части нижней конечности. Выбор операции для ликвидации артериальной недостаточности нижних конечностей определяется уровнем и распространенностью поражения.
В настоящий момент времени, оперативные вмешательства на артериях нижних конечностей возможно разделить на:
- традиционные (открытые)
- эндоваскулярные оперативные вмешательства.
При поражении подвздошно-бедренного и бедренно-подколенного артериального сегмента возможно выполнение шунтирующих операций или выполнение протезирования соответствующего участка магистральной артерии.
Выбор такого оперативного пособия зависит от превалирующего поражения: наибольшая эффективность у пациентов с проксимальным поражением артериального русла нижних конечностей, то есть атеросклеротичесой ангиопатий на фоне сахарного диабета.
С другой стороны, шунтирующие операции у пациентов с синдромом диабетической стопы при периферической ангиопатии малоэффективны: восстановленный магистральный кровоток «упирается» в регидную капилярную сеть и объем кровотока уменьшается.
Положительным эффектом (в 47% случаев) обладает поясничная симпатэктомия у пациентов с атеросклеротическим поражением артерий нижних конечностей на фоне сахарного диабета. В тоже время, у пациентов с синдромом диабетической стопы и периферической ангионейропатией поясничная симпатэктомия недостаточно эффективна.
В последнее время доминирующим и эффективным методом лечения макроангиопатии у пациентов с синдромом диабетической стопы являются эндоваскулярные методы. В случае поражения сосудов на уровне щели коленного сустава и ниже, что характерно для периферической диабетической макроангиопатии, операцией выбора является транслюминальная баллонная ангиопластика.
При наличии очага гнойно-некротического поражения на стопе реваскуляризация выполняется с учетом ангиосомальных зон кровоснабжения стопы. Несмотря на обилие анастомозов между конечными отделами артерий стопы, клинические наблюдения указывают, что макроангиопатия приводит к их недостаточности
К экономным ампутациям стопы относятся ампутации пальцев стопы, трансметатарсальная ампутация стопы (см. рисунок 7), ампутация по Лисфранку и Шопару (см. рисунок 4). Зачастую операции носят характер атипичных ампутаций, сочетая в себе комбинацию оперативных приемов.

Рисунок 7. Трансметатарзальная ампутация левой стопы при синдроме диабетической стопы, нейроишемической форме.
При диабетической стопе Шарко оперативное пособие заключается в резекции участков костей, суставов, при развитии остеомиелита – остеонекрсеквестрэктомии, применение аппаратов внеочагового остеосинтеза и других видов костной иммобилизации.
К высоким ампутациям относятся ампутации на уровне бедра и голени. С учетом дистального типа поражения сосудов и атрофических изменений мягких тканей наиболее часто на голени ампутации производятся в верхней трети с формированием заднего кожно-мышечного лоскута (см. рисунок 8).

Рисунок 8. Ампутация на уровне верхней трети левой голени.
Ампутация на уровне бедра выполняется при распространенной гангрене конечности или при прогрессировании гнойно-некротического процесса с поражением голени и при развитии синдрома системной воспалительной реакции с угрозой развития септического шока.
При тяжелом общем состоянии больного выполняются так называемые санационные (они же гильотинные) ампутации, при которых производится отсечение конечности без выкраивания лоскутов, гемостаз и рана не ушивается.
Вашему вниманию хотелось бы предложить несколько клинических случаев успешного лечения синдрома диабетической стопы, нейроишемической формы.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Основное клиническое проявление хронических облитерирующих заболеваний артерий нижних конечностей - «перемежающаяся хромота» и отсутствие пульсации на артериях стоп. Артериальные трофические язвы возникают на стопе или голени после незначительных травм (потёртости, расчёсы, ссадины и др.), операций на ногах или спонтанно.
Образование артериальных трофических язв - одно из наиболее тяжёлых проявлений ишемического поражения конечности. Характерная локализация - дистальные отделы пальцев стоп, межпальцевые промежутки, тыл стопы, пяточная область, наружная и задняя поверхность голени. Отличительной чертой служат сухой некроз тканей и выраженный болевой синдром. При наличии признаков критической ишемии артериальные трофические язвы не имеют чётких границ, окружена отёчными цианотичными тканями, склонна к прогрессированию с расширением и углублением раневого дефекта. При дальнейшем развитии ишемического процесса отмечают омертвение частиноги с развитием гангрены.
Артериальные трофические язвы возникают на фоне критической нарушения крообращения, которую определяют как сосудистую недостаточность конечности, вследствие окклюзирующего поражения сосудов на финальных стадиях своего развития. При этом подразумевают, что без своевременного восстановления кровотока дальнейшее прогрессирование ишемии приведёт к необходимости высокой ампутации. Определение критической ишемии включает следующие клинические признаки:
-
ишемическую боль покоя в течение более двух недель с систолическим давлением на артериях голени
Читайте также:

