Трофическая язва при болезни рейно
Обновлено: 27.04.2024
Настоящая работа посвящена исследованию возможности повышения эффективности комплексной терапии трофических язв и послеоперационных ран нижних конечностей с помощью топического иммуномодулятора. В исследовании приняли участие 44 больных
Настоящая работа посвящена исследованию возможности повышения эффективности комплексной терапии трофических язв и послеоперационных ран нижних конечностей с помощью топического иммуномодулятора.
В исследовании приняли участие 44 больных от 30 до 81 года (30 женщин, 14 мужчин) с хроническими трофическими язвами нижних конечностей. Трофические язвы развились из-за нарушения кровообращения в нижних конечностях по причине тромбофлебита или диабетической ангиопатии. У большинства больных тромбофлебит возник как осложнение варикозной болезни. Диагноз «варикозная болезнь, посттромбофлебитический синдром (ПТФС)» был постановлен 41 больному. На момент исследования признаки острого тромбофлебита на фоне ПТФС имелись у 9 человек, признаки рожистого воспаления кожи — у 5 человек. У 1 больного трофическая язва сочеталась с остеомиелитом большой берцовой кости, у двоих — с начинающейся гангреной пальцев ноги. В анамнезе трое больных перенесли флебэктомию, 1 больная — склерозирующую терапию по поводу варикозного расширения вен.
У подавляющего большинства исследованных больных имелась 1 трофическая язва и лишь у двоих больных были 2 язвы. В большинстве случаев язвы располагались на передней, внутренней или внешней поверхности голени, у 2 больных диабетической ангиопатией язвенный процесс локализовался на стопе. Размеры трофических язв варьировали от 0,5х0,5 см до 3х4,5 см. Кратер язвы был заполнен фибринозными массами у 30 больных, фибринозно-гнойными — у 6 больных, гнойно-некротическими фрагментами ткани — у 5 пациентов. В трех случаях на момент поступления больного язва выглядела чистой, без фибринозных, гнойных или некротических масс.
У 5 больных некротически-буллезной формой рожи на коже голени были признаки острого воспаления, пузыри с серозно-гнойным содержимым. У 2 других больных отмечались признаки начинающейся гангрены: соответственно I и III пальцы правой стопы были синюшно-черного цвета.
Лечение
При лечении всех 44 больных соблюдались следующие принципы лечения:
- постельный режим с приподнятым положением больной конечности для устранения застоя крови и лимфы;
- тщательный туалет кожи вокруг язвы;
- создание тока тканевой жидкости из язвы в повязку в начале лечения. Для этой цели использовали повязки с гипертоническим раствором NaCl в сочетании со спиртовым раствором хлорофиллипта, что обеспечивало очищение язвы, улучшение питания живых тканей дна и стенок язвы;
- активация регенеративных способностей организма после очищения кратера язвы.
Все больные ПТФС получали общее и местное лечение. Общими составляющими лечения были инфузионная (реополиглюкин 200 мл + трентал 5 мл + аскорбиновая кислота 5 мл в/в капельно, через день № 5), эскузан по 15 капель 3 раза в сутки, аспирин 0,5 г — 1 раз в сутки, троксевазин по 2 капсулы 3 раза в сутки в течение 15 дней или диовенор 600 мг по 1 табл. 1 раз в сутки в течение 30 дней. В дополнение к вышеописанному лечению пациенты с признаками острого тромбофлебита получали инъекции раствора гепарина 5000 ЕД п/к 4 раза в сутки в течение 6 дней.
Местное лечение в первые дни (от 1 до 4 дней) — хлорофиллипт спиртовой в сочетании с гипертоническим раствором, перевязки делались каждый день. После очищения язвы накладывались повязки с мазью гепона или солкосерил (контрольная группа, 10 человек). Как отмечалось выше, у 3 больных язва не содержала фибринозных, гнойных или некротических элементов. У этих больных сразу начинали лечение мазью гепона — иммуномодулятора, обладающего способностью повышать эффективность иммунной защиты, а также прямым противовирусным действием.
Мазь изготавливалась непосредственно в аптеке ГКБ №1 и имела следующий состав: гепона 0,006; ланолина 10,0; масла оливкового 10,0; воды для инъекций 10,0. Готовую мазь хранили при +4°С, использовали в течение 10 дней.
Мазь наносили тонким слоем на поверхность трофической язвы, повязки с мазью гепона меняли через день. Лечение проводилось в течение 10 дней (5 перевязок).
Лечение неосложненных трофических язв
В контрольной группе 10 больных получали такую же общую терапию, но местное лечение после очищения язвы проводили мазью солкосерил. Заживление язв у больных этой группы происходило на 5–15 дней дольше, чем при применении мази гепона. У 1 больной контрольной группы в ходе лечения мазью солкосерил произошло ухудшение, развилось рожистое воспаление кожи (некротически-буллезная форма). Этой пациентке было назначено адекватное хирургическое лечение, в дополнение к общему лечению применялись антибиотик и бисептол, для местного лечения вместо солкосерила использовалась мазь гепона.
Лечение язвенных дефектов кожи после некрэктомии по поводу некротически-буллезной формы рожи
Больные с некротически-буллезной формой рожи в дополнение к инфузионной терапии получали инъекции цефазолина по 1 г в/м 3 раза в сутки в течение 7 дней, а также бисептол 480 мг по 1 табл. 3 раза в сутки в течение 10 дней. На фоне консервативного лечения проводили оперативное вмешательство — некрэктомию. Пузыри вскрывались, некротизированные ткани удалялись, открытая рана обрабатывалась раствором перманганата калия. Далее открывшиеся после некрэктомии большие дефекты кожи лечили гепоном, как трофические язвы. У всех больных отмечались хорошие результаты лечения. Через 3–4 дня после начала применения мази гепона наблюдался выраженный рост грануляционной ткани с последующим формированием соединительнотканного рубца в кратчайшие сроки.
Лечение послеоперационных ран нижних конечностей у больных диабетической ангиопатией
При лечении больных диабетической ангиопатией консервативное лечение дополняли адекватными дозами инсулина (п/к). В качестве антибиотика использовали линкомицин по 600 мг в/м 2 раза в сутки в течение 14 дней. При начинающейся гангрене пальца на фоне консервативного лечения проводили адекватное оперативное вмешательство — ампутацию или ограниченное иссечение некротизированных элементов. В послеоперационном периоде промывали рану и свищевые ходы раствором гепона (0,002 г в 10 мл физиологического раствора), а также накладывали повязки с мазью гепона, как описано выше. Результаты лечения свидетельствуют о значительной активации роста грануляционной ткани и ускоренном заживлении послеоперационной раны под влиянием гепона.
Очевидно, что применение гепона в описанных выше клинических случаях стимулировало активный рост грануляционной ткани. Обычно у больных диабетической ангиопатией проходимость капиллярного русла оказывается минимальной, во время хирургических манипуляций кровь выделяется, как правило, только из подкожных сосудов, внутренние ткани практически обескровлены, имеют бледно-розовый цвет. Рост грануляционной ткани у таких больных либо не отмечается вовсе, либо протекает очень вяло, послеоперационные раны хронически не заживают, остаются трофические язвы. Применение гепона позволило добиться ускоренного заживления послеоперационных ран и незаживающих язв у больных диабетической ангиопатией.
Литература
Клинический пример
Больная О. Л. О., 52 года (ИБ № 5039).
Диагноз при поступлении: варикозная болезнь, посттромбофлебитический синдром, трофическая язва правой голени.
Диагноз окончательный: варикозная болезнь, посттромбофлебитический синдром, трофическая язва правой голени. Рожистое воспаление правой голени (некротически-буллезная форма).
Жалобы при поступлении: боли в области правой голени, усиливающиеся при ходьбе, наличие трофической язвы на передней поверхности нижней трети правой голени.
Anamnesis morbi: считает себя больной в течение 20 лет, когда впервые появились варикозные расширения вен правой голени. Неоднократно лечилась по поводу данного заболевания у ангиохирурга по месту жительства, от оперативного лечения отказывалась. Трофическая язва появилась около месяца назад, попытки самостоятельно лечиться облегчения не принесли, обратилась в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: детских болезней не помнит, болезнь Боткина, туберкулез, наличие венерических заболеваний у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен.
Status praesens objectivus: общее состояние больной удовлетворительное, сознание ясное, положение в постели активное. Больная повышенного питания, костно-мышечная система без патологии. Кожа и видимые слизистые обычной окраски. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких дыхание везикулярное, ЧДД 16 в 1 мин. Тоны сердца ритмичные, пульс 68 уд. в 1 мин, АД 130/80 мм рт. ст. Язык влажный, розовый, живот мягкий, безболезненный, печень — по краю реберной дуги, селезенка не пальпируется, симптом «поколачивания» отрицателен с обеих сторон. Физиологические отправления в норме.
Locus morbi: правая нижняя конечность отечна, голень синюшного цвета, болезненна при пальпации. На передней поверхности нижней трети голени трофическая язва 2х2 см, края гиперемированы, в кратере фибринозное отделяемое.
Анализы: кровь на RW — отрицательная; биохимический анализ крови — белок 54 г/л, креатинин 76 мкмоль/л, мочевина 5,5 ммоль/л, остаточный азот 25 ммоль/л, диастаза 20 г/(ч/л), билирубин 16 — 4 — 12 мкмоль/л, глюкоза 3,2 ммоль/л; коагулограмма — протромбин 85%, фибриноген 3,2 мкмоль/л, время рекальцификации 90 с; общий анализ крови: Э — 5,5 млрд./мл, Л — 6,4 млн./мл, Hb — 115 г/л, цветной показатель — 0,92, СОЭ — 25 мм/ч; общий анализ мочи — норма.
Лечение: раствор гепарина по 5000 ЕД п/к каждые 6 ч, аспирин 0,25 г по 1 табл. 1 раз в день; местно трофическую язву обрабатывали спиртовым раствором хлорофиллипта, поверхность язвы 2 раза в день смазывали мазью троксевазин, на ночь — мазью солкосерил. Через 5 дней лечения общее состояние пациентки значительно ухудшилось, температура тела повысилась до 39,5°С. Кожные покровы правой нижней конечности резко гиперемированы, гипертрофированы, болезненны. Установлен диагноз: рожистое воспаление правой нижней конечности.
Коррекция лечения: цефазолин по 1 г 2 раза в сутки, бисептол 480 мг по 1 табл. 3 раза в сутки. Через двое суток в области пораженной конечности появились пузыри с серозной жидкостью, под которыми впоследствии образовались участки некроза дермы (некротически-буллезная форма рожи).
Ввиду отсутствия положительного эффекта от предшествующей терапии, у больной проведено лечение с применением гепона.
Местно — произведено рассечение пузырей, удаление некротических элементов тканей. Были назначены ванны с перманганатом калия, инфузионная терапия (реополиглюкин 200 мл + трентал 5 мл + аскорбиновая кислота 5 мл в/в капельно, через день № 5), эскузан по 15 капель 3 раза в сутки, аспирин 0,5 г — по 1 табл. 1 раз в сутки, троксевазин по 2 капсулы 3 раза в сутки в течение 15 дней или диовенор 600 мг по 1 табл. 1 раз в сутки в течение 30 дней.
Locus morbi на момент начала терапии гепоном: по передней поверхности правой голени 3 язвенных дефекта кожи 10х10 см, раны заполнены фиброзно-гнойным отделяемым. После санации раневой поверхности раствором риванола применялись повязки с гепоном. Смена повязок проводилась через день. Уже после второй перевязки появился значительный рост грануляционной ткани, к концу лечения (всего 5 перевязок в течение 10 дней) раны очистились. Проведена операция аутодермопластики марочным способом (15 марок). Гепон в виде мази продолжали применять на всей послеоперационной поверхности. На фоне применения гепона «прижились» все 15 марок, в кратчайшие сроки сформировался рубец.
Клинический пример
Больная К. Л. Н. , 78 лет (ИБ № 6784).
Диагноз при поступлении: облитерирующий атеросклероз сосудов нижних конечностей. Сахарный диабет.
Диагноз окончательный: сахарный диабет III степени. Диабетическая ангиопатия нижних конечностей. Начинающаяся гангрена III пальца (ногтевая фаланга) правой стопы.
Жалобы при поступлении на постоянные боли в нижних конечностях, особенно в области III пальца правой стопы, общую слабость, недомогание.
Anamnesis morbi: считает себя больной около 20 лет, когда впервые был обнаружен сахарный диабет. Неоднократно лечилась в эндокринологическом и хирургическом стационарах. Последнее обострение началось 3 недели назад, когда появились перечисленные выше жалобы. Попытки самостоятельного лечения оказались безрезультатными, обратилась в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: аппендэктомия в 1950 году. Болезнь Боткина, туберкулез, венерические заболевания у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен. Отмечает длительно протекающие гнойные процессы при любых незначительных травмах.
Status praesens objectivus: общее состояние средней тяжести, сознание ясное, положение в постели активное. Больная обычного питания, костно-мышечная система без патологии. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких — везикулярное дыхание, ЧДД 16 в 1 мин. Тоны сердца ритмичны, слегка приглушены, Ps 68 уд. в 1 мин, АД 130/90 мм рт. ст. Язык слегка суховат, живот правильной формы, участвует в акте дыхания, при пальпации безболезненный. Симптомы раздражения брюшины отрицательны. Печень по краю реберной дуги, селезенка не пальпируется. Симптом «поколачивания» отрицателен с обеих сторон. Физиологические отправления в норме.
Locus morbi: кожные покровы обеих нижних конечностей бледные, сухие. На стопах кожа прохладная на ощупь. Кожа III пальца правой стопы в области ногтевой фаланги синюшно-черного цвета. Движения в пальце сохранены.
Анализы: RW — отрицательная. Общий анализ крови: Э — 4,2 млрд./мл, Л — 9,2 млн./мл, Hb — 105 г/л, цветной показатель — 0,95, СОЭ — 17 мм/ч. Биохимия крови: глюкоза (при поступлении) 18,5 ммоль/л, глюкоза (после коррекции) 5,4 ммоль/л; билирубин 20,3–5,8–14,5 мкмоль/л, АЛТ — 0,43 ммоль/(ч/л), АСТ — 0,3 ммоль/(ч/л). Общий анализ мочи — норма. Коагулограмма: протромбиновый индекс 90%, фибриноген 8,8 мкмоль/л, время рекальцификации 100 с.
Лечение: инъекции инсулина (п/к) 28 ЕД утром, 16 ЕД вечером, раствора линкомицина 600 мг в/м 3 раза в сутки в течение 14 дней. Инфузионная терапия (реополиглюкин 200 мл + трентал 5 мл + актовегин 5 мл в/в капельно, через день № 5).
Местно — в III палец правой стопы под жгутом ввели линкомицин. Ночью после инъекции в области III пальца появились «дергающие» боли. Утром в области некроза кожи произведен овальный разрез длиной около 2,5 см, иссечены некротические элементы в области лизированного участка ногтевой фаланги, удалены секвестры, поставлен резиновый выпускник, наложена асептическая повязка. Со следующего дня начали накладывать повязки с мазью гепона, перевязки проводили через день №5. Во время перевязок удалялись некротические элементы до «живой» ткани. Ампутации пальца удалось избежать. Последующее лечение прошло успешно по типу лечения костного панариция. Отмечались быстрое очищение раны, энергичный рост грануляционной ткани и формирование рубца из соединительной ткани.
Клинический пример
Больная Б. Л. А., 65 лет (ИБ № 4571).
Диагноз при поступлении: диабетическая ангиопатия сосудов нижних конечностей, начинающаяся гангрена I пальца правой стопы.
Диагноз окончательный: сахарный диабет II типа средней тяжести в стадии декомпенсации. Диабетическая ангиопатия нижних конечностей. Начинающаяся гангрена I пальца правой стопы. Диабетическая нефропатия I степени.
Жалобы при поступлении: постоянные боли в области правой стопы, черный цвет кожных покровов I пальца правой стопы, общая слабость и недомогание.
Anamnesis morbi: считает себя больной около 20 лет, когда впервые был выявлен сахарный диабет. Неоднократно лечилась в эндокринологическом отделении. Перечисленные выше жалобы появились около 2 недель назад. Пыталась лечиться самостоятельно — без результата. Обратилась за помощью в хирургическое отделение 1-й ГКБ.
Anamnesis vitae: детских болезней не помнит. Болезнь Боткина, туберкулез, венерические заболевания у себя и ближайших родственников отрицает. Аллергологический анамнез не отягощен. Периодически отмечает боли в области сердца, повышения АД.
Status praesens objectivus: общее состояние удовлетворительное, сознание ясное, положение в постели активное. Больная повышенного питания. Кожные покровы бледные, костно-мышечная система без патологии. Региональные лимфатические узлы не увеличены, подвижны, безболезненны. В легких — везикулярное дыхание, ЧДД 16 в 1 мин. Тоны сердца приглушены, ритмичны, Ps 82 удара в 1 мин, АД 140/80 мм рт. ст. Живот мягкий, при пальпации безболезненный. Печень по краю реберной дуги, селезенка не пальпируется. Симптом «поколачивания» с обеих сторон отрицателен. Физиологические отправления в норме.
Locus morbi: обе голени и стопы прохладные на ощупь. Пульсация на A.dorsalis pedis значительно ослаблена. I палец правой стопы в области ногтевой и средней фаланг синюшно-черного цвета, движения в пальце сохранены.
Анализы: RW — отрицательная; Э — 3,2 млрд./мл, Л — 13,5 млн./мл; Hb — 104 г/л, цветной показатель — 0,97; СОЭ — 56 мм/ч; протромбин — 100%, фибриноген 4,8 мкмоль/л, время рекальцификации 90 с: глюкоза крови 12,5 ммоль/л; общий анализ мочи — Л на все поле зрения.
Реовазография — общий кровоток правой голени снижен, левой голени достаточный. Тонус сосудов повышен. Затруднен венозный отток, больше справа.
Лечение: операция — ампутация I пальца правой стопы с головкой I плюсневой кости.
Режим II, диета 9. Инъекции инсулина (п/к) 26 ЕД утром, 16 ЕД вечером. Инъекции раствора линкомицина 600 мг в/м 3 раза в сутки в течение 14 дней. Местно — перевязки со спиртовым раствором хлорофиллипта, затем мазью левомиколь.
Locus morbi на момент начала лечения гепоном: послеоперационная рана в области I пальца правой стопы до 3 см в диаметре, имеется свищевой ход к культе плюсневой кости с гнойным отделяемым. Лечение препаратом гепон включало промывания свищевого хода и послеоперационной раны раствором гепона (0,002 г в 10 мл физиологического раствора). Процедуры с использованием гепона повторяли через день, всего 5 процедур в течение 10 дней. На 6-й день лечения гепоном из свищевого хода был извлечен секвестр. На 10-е сутки рана очистилась и уменьшилась в диаметре до 1,5 см. Края раны сцеплены лейкопластырем по типу наводящих швов. Продолжено лечение мазью гепона. К 14-му дню появилась грануляционная ткань, но из свищевого хода продолжали выделяться секвестры культи плюсневой кости. К 30-му дню рана зажила вторичным натяжением.

Для начала разберёмся, чем болезнь Рейно отличается от синдрома Рейно.
Болезнью Рейно называют заболевание, сопровождающееся выраженным спазмом сосудов, в результате чего нарушается кровоснабжение кистей и стоп, в редких случаях - некоторых частей лица - подбородка, носа, ушей. В запущенных стадиях болезни на этих участках могут появляться трофические язвы и некрозы. Такие нарушения называются трофическими. Трофика - процесс клеточного питания тканей. При болезни происходят сбои в питании тканей дистальных участков – участков максимально удалённых от центра тела. Эти расстройства имеют периодический характер и возникают при воздействии холода или при возникновении сильного эмоционального напряжения.
Синдром Рейно является вторичным и развивается как следствие других заболеваний: ревматологической патологии, болезней щитовидной железы, остеохондроза и некоторых других.
Клинические проявления болезни и синдрома Рейно одинаковы.
Стадии болезни
Начальная стадия
При наличии раздражителей (холод и эмоциональное напряжение) временно белеет кожа на пальцах обеих рук, ощущается ломота, онемение, жжение или покалывание. Симптомы пропадают, когда пропадает раздражитель.
Более поздние стадии
Появляется сильная боль в пальцах, белёсость исчезает медленнее, кончики могут синеть. В запущенных случаях концевые фаланги пальцев чернеют, образуются длительно незаживающие трофические язвы.
Причины появления болезни Рейно до конца неизвестны, однако известны факторы, провоцирующие развитие болезни:
- отягощённая наследственность;
- стрессы;
- травмы ЦНС (центральная нервная система);
- алкоголизм, наркомания;
- патология эндокринной системы;
- частые переохлаждения – патология чаще встречается у людей, живущих в холодном климате;
- род деятельности – патология чаще отмечается у людей, чьи профессии связаны с ручным трудом: доярки, массажисты и т.д.
- половая принадлежность – патологией чаще страдают женщины.
Диагностика заболевания
- холодовая проба - погружение конечности в холодную воду с оценкой скорости восстановления нормального кровоснабжения;
- капилляроскопия – исследование капилляров мягких тканей;
- реовазография - измерение объёма и интенсивности кровотока в артериальных сосудах конечностей; артерий.
На основании результатов обследования врач назначает лечение.
Запишитесь на консультацию к нашему врачу
Консервативное лечение
Ограничение контакта с холодом, отказ от психоэмоциональных перегрузок, соблюдение режима сна и бодрствования (должен быть обеспечен полноценный 7-8 часовой ночной сон), медикаментозная терапия, направленная на уменьшение периферического сосудситого спазма и улучшающая трофику тканей (препараты из группы спазмолитиков, кальциевые блокаторы, простгландины и др.). При синдроме Рейно важно выявить болезнь, на фоне которой синдром начал развиваться. В этом случае лечение основной болезни может полностью избавить пациента от проявлений синдрома Рейно.
Хирургическое вмешательство
Симпатэктомия - операция по удалению части нервного симпатического ствола, проходящего вдоль позвоночника. Цель операции – устранить спатическое (судорожное, спазматическое) влияние симпатических нервных волокон (именно по ним приходят спазмирующие импульсы) на сосуды. В запущенных случаях пациенту может грозить ампутация пальцев. При своевременном обращении и правильном лечении болезнь и синдром Рейно — неопасные и поддающиеся лечению заболевания с медленным прогрессированием и благоприятным прогнозом.
Специалисты флебологического отделения Медицинского центра «XXI век» помогут поставить точный диагноз и подобрать консервативную терапию при этой патологии. Записаться на приём можно по телефону.
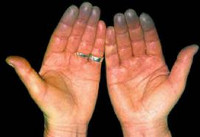
Синдром Рейно – вазоспастическое заболевание, характеризующееся пароксизмальным расстройством артериального кровообращения в сосудах конечностей (стоп и кистей) под воздействием холода или эмоционального волнения. Синдром Рейно развивается на фоне коллагенозов, ревматоидного артрита, васкулитов, эндокринной, неврологической патологии, болезней крови, профессиональных заболеваний. Клинически синдром Рейно проявляется приступами, включающими последовательное побледнение, цианоз и гиперемию пальцев рук или ног, подбородка, кончика носа. Синдром Рейно приводит к постепенным трофическим изменениям тканей. Консервативные меры включают прием вазодилататоров, хирургическое лечение заключается в симпатэктомии.
МКБ-10
Общие сведения
Синдром Рейно является вторичным состоянием, развивающимся на фоне ряда заболеваний: диффузной патологии соединительной ткани (склеродермия, системная красная волчанка), системных васкулитов, ревматоидного артрита, заболеваний симпатических ганглиев, эндокринных и гематологических нарушений, диэнцефальных расстройств, компрессии сосудисто-нервных пучков. Кроме того, синдром Рейно может быть спровоцирован воздействием профессиональных вредностей (охлаждением, вибрацией).
В патогенезе синдрома Рейно ведущая роль отводится эндогенным вазоконстрикторам – катехоламинам, эндотелину, тромбоксану А2. В развитии синдрома Рейно выделяют три последовательные фазы: ишемическую, цианотическую и гиперемическую. Фаза ишемии развивается вследствие спазма периферических артериол и полного опорожнения капилляров; проявляется локальным побледнением кожного покрова. Во второй фазе, обусловленной задержкой крови в венулах и артериовенулярных анастомозах, побледнение кожи сменяется цианозом (синюшностью). В последней фазе – реактивно-гиперемической отмечается покраснение кожи.
При отсутствии этиофакторов, характерных для синдрома Рейно, предполагают наличие болезни Рейно. В возникновении болезни Рейно установлена роль наследственности, эндокринных дисфункций, психических травм, хронической никотиновой и алкогольной интоксикации. Болезнь Рейно более распространена среди женщин 20-40 лет, страдающих мигренью.

Симптомы синдрома Рейно
Симптоматика синдрома Рейно обусловлена пароксизмальным вазоспазмом и развивающимися вследствие этого повреждениями тканей. В типичных случаях при синдроме Рейно поражаются IV и II пальцы стоп и кистей, иногда – подбородок, уши и нос. Приступы ишемии вначале кратковременны, редки; возникают под воздействием холодовых агентов, вследствие волнения, курения и т. д. Внезапно развивается парестезия, похолодание пальцев, кожа становится алебастро-белого цвета. Онемение сменяется жжением, ломящей болью, чувством распирания. Приступ завершается резкой гиперемией кожи и ощущением жара.
Прогрессирование синдрома Рейно приводит к удлинению времени приступов до 1 часа, их учащению, спонтанному возникновению без видимых провокаций. После высоты пароксизма наступает цианотическая фаза, появляется незначительная отечность тканей. В промежутки между приступами стопы и кисти остаются холодными, цианотичными, влажными. Для пароксизмов ишемии при синдроме Рейно характерно симметричное и последовательное развитие проявлений: сначала на пальцах кистей, затем - стоп. Последствиями ишемии тканей в случае длительного и тяжелого течения синдрома Рейно могут стать трофические изменения в виде плохо заживающих трофических язв, участков некрозов, дистрофических поражений ногтевых пластин, остеолиза и деформации фаланг, гангрены.
Диагностика синдрома Рейно
Пациента с синдромом Рейно направляют на консультацию ревматолога и сосудистого хирурга. При синдроме Рейно выявить изменения в дистальных отделах артерий позволяет ангиография периферического сосудистого русла, при которой определяются участки неравномерного стеноза и тотальной обструкции сосудов, отсутствие капиллярных сетей и коллатералей. При капилляроскопии ногтевого ложа и передней поверхности глаза обнаруживаются морфологические изменения микрососудистого рисунка, свидетельствующие о нарушения перфузии.
Лазерная доплеровская флоуметрия, применяемая для оценки периферической микроциркуляции, выявляет дефекты метаболической и миогенной регуляции кровообращения, снижение вено-артериальных реакций и симпатической активности. В период между приступами при синдроме Рейно спровоцировать вазоспазм и оценить состояние кровотока позволяет проведение холодовой пробы.
Лечение синдрома Рейно
Первым принципом терапии синдрома Рейно служит исключение провоцирующих моментов – курения, охлаждения, вибрации и других бытовых и производственных факторов. Проводится выявление и лечение первичного заболевания, обусловившего развитие синдрома Рейно. Среди вазодилататоров при синдроме Рейно эффективно назначение антагонистов кальция - нифедипина, алпростадила, селективных блокаторов кальциевых каналов - верапамила, никардипина дилтиазема. При необходимости применяются ингибиторы АПФ (каптоприл), селективные блокаторы HS2-серотониновых рецепторов (кетансерин).
При синдроме Рейно производится назначение антиагрегантных препаратов - дипиридамола, пентоксифиллина, низкомолекулярных декстранов (реополиглюкина). Прогрессирование и резистентность синдрома Рейно к лекарственной терапии служит показанием к проведению хирургической симпатэктомии или ганглиэктомии. При развившемся ишемическом приступе неотложными мерами является согревание конечности в теплой воде, массирование с помощью шерстяной ткани, предложение пациенту горячего питья. При затяжном приступе назначают инъекционные формы спазмолитиков (дротаверина, платифиллина), диазепама, блокады.
При синдроме Рейно используются немедикаментозные методики - психотерапия, рефлексотерапия, физиотерапия, гипербарическая оксигенация. При синдроме Рейно, обусловленном системными коллагенозами, показано проведение сеансов экстракорпоральной гемокоррекции. Новым словом в лечении синдрома Рейно является терапия с использованием стволовых клеток, направленная на нормализацию периферического кровотока. Стволовые клетки способствуют открытию новых коллатералей в сосудистом русле, стимулируют регенерацию поврежденных нервных клеток, что в итоге ведет к прекращению пароксизмов вазоконстрикции.
Прогноз и профилактика синдрома Рейно
Прогноз синдрома Рейно зависит от прогрессирования основной патологии. Течение синдрома относительно благоприятное, приступы ишемии могут спонтанно прекратиться после перемены привычек, климата, профессии, проведения санаторного лечения и т. д.
Отсутствие первичных профилактических мер позволяет говорить только о вторичной профилактике синдрома Рейно, т. е. об исключении пусковых факторов, ведущих к вазоспазму - переохлаждения, вибрации, курения, психоэмоциональных нагрузок.
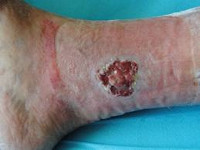
Трофическая язва – это открытая рана на коже или слизистой, возникшая после отторжения омертвевших тканей и не заживающая в течение 6 и более недель. Причина развития трофической язвы – местное нарушение кровообращения или иннервации тканей. Трофические язвы развиваются на фоне различных заболеваний, отличаются упорным длительным течением и с трудом поддаются лечению. Диагностика проводится ультразвуковыми методами (УЗДГ, УЗДС вен). Выздоровление напрямую зависит от течения основного заболевания и возможности компенсации нарушений, которые привели к возникновению язвы.
МКБ-10

Общие сведения
Трофическая язва — длительно не заживающий дефект кожи и расположенных под ней тканей. Варикозные трофические язвы чаще возникают в нижней трети голени на фоне варикозно расширенных вен. На отечной конечности появляется синюшное болезненное пятно, затем небольшие язвочки, которые постепенно сливаются в один дефект. Из язвы сочится кровянистое или гнойное отделяемое, нередко с запахом. Течение рецидивирующее, прогрессирующее, полное излечение варикозных трофических язв возможно лишь при удалении измененных вен. Диагностикой и устранением причин появления трофической язвы в таких случаях занимается клиническая флебология.

Причины
Возникновение трофических язв может быть обусловлено любым заболеванием поверхностных или глубоких вен, сопровождающимся хронической венозной недостаточностью. При постановке диагноза очень важна болезнь, которая вызвала образование язвы, поскольку тактика лечения и прогноз в значительной степени зависит от характера основной венозной патологии. К развитию трофической язвы может приводить:
- хроническая венозная недостаточность (при варикозном расширении вен, посттромбофлебитической болезни);
- ухудшение артериального кровообращения (при гипертонической болезни, сахарном диабете, атеросклерозе);
- нарушение оттока лимфы (лимфедема);
- травмы (отморожения, ожоги);
- хронические заболевания кожи (экзема и т. д.).
Трофическая язва может развиться при отравлении хромом или мышьяком, некоторых инфекционных болезнях, системных заболеваниях (васкулиты), нарушении местного кровообращения при длительной неподвижности в результате болезни или травмы (пролежни). Более 70% всех трофических язв нижних конечностей вызвано болезнями вен.
Патогенез
Нарушение венозного кровотока, вызванное заболеваниями венозной системы, приводит к депонированию крови в нижних конечностях. Кровь застаивается, в ней накапливаются продукты жизнедеятельности клеток. Питание тканей ухудшается. Кожа уплотняется, спаивается с подкожной клетчаткой. Развиваются дерматиты, мокнущая или сухая экзема.
Из-за ишемии ухудшается процесс заживления ран и царапин. В результате мельчайшее повреждение кожи при хронической венозной недостаточности может стать причиной развития длительно текущей, плохо поддающейся лечению трофической язвы. Присоединение инфекции утяжеляет течение заболевания и приводит к развитию различных осложнений.
Симптомы трофической язвы
Развитию трофической язвы венозной этиологии предшествует появление характерных признаков прогрессирующего поражения венозной системы. Вначале пациенты отмечают усиление отеков и чувства тяжести в области икр. Ночные мышечные судороги становятся более частыми. Появляется зуд, чувство жара или жжения. Усиливается гиперпигментация, ее зона расширяется. Накапливающийся в коже гемосидерин вызывает экзему и дерматит. Кожа в пораженной области приобретает лаковый вид, утолщается, становится неподвижной, напряженной и болезненной. Развивается лимфостаз, приводящий к транссудации лимфы и образованию на коже мелких капелек, по виду напоминающих росу.

Через некоторое время в центре пораженного участка появляется белесоватый очаг атрофии эпидермиса (предъязвенное состояние – белая атрофия). При минимальном повреждении кожи, которое может пройти для больного незамеченным, в области атрофии образуется мелкий язвенный дефект. В начальной стадии трофическая язва располагается поверхностно, имеет влажную темно-красную поверхность, покрытую струпом. В дальнейшем язва расширяется и углубляется. Отдельные язвы могут сливаться между собой, образуя обширные дефекты. Множественные запущенные трофические язвы в отдельных случаях могут образовывать единую раневую поверхность по всей окружности голени.
Процесс распространяется не только вширь, но и вглубь. Пенетрация язвы в глубокие слои тканей сопровождается резким усилением болей. Язвенное поражение может захватывать икроножные мышцы, ахиллово сухожилие и периост передней поверхности большеберцовой кости. Периостит, осложненный вторичной инфекцией, может перейти в остеомиелит. При повреждении мягких тканей в области голеностопного сустава возникает артрит с последующим развитием контрактуры.
Характер отделяемого зависит от наличия вторичной инфекции и вида инфекционного агента. На начальных стадиях отделяемое геморрагическое, затем – мутное с нитями фибрина или гнойное с неприятным запахом. Мацерация кожи вокруг трофической язвы нередко приводит к развитию микробной экземы.
Осложнения
При инфицировании язвы возрастает опасность возникновения осложнений. Как правило, вторичная инфекция вызывается условно патогенными бактериями. У пожилых ослабленных больных возможно присоединение грибковой инфекции, которая утяжеляет течение заболевания, становится причиной быстрого прогрессирования трофических расстройств и ухудшает прогноз.
Нередко трофические язвы сопровождаются пиодермией, аллергическим дерматитом. Может развиться лимфангит, гнойный варикотромбофлебит, рожистое воспаление, паховый лимфаденит. В отдельных случаях трофическая язва осложняется флегмоной и даже сепсисом. Рецидивирующая инфекция вызывает поражение лимфатических сосудов и приводит к развитию вторичной лимфедемы.
Диагностика
Подтверждением венозной этиологии трофической язвы является сопутствующая варикозная болезнь и перенесенный флеботромбоз. О высокой вероятности перенесенного тромбоза глубоких вен свидетельствует наличие в анамнезе заболеваний системы крови, приема гормональных препаратов, катетеризаций и пункций вен нижних конечностей, эпизодов длительной неподвижности при травмах, хронических заболеваниях и хирургических вмешательствах.
Типичная локализация венозной трофической язвы – внутренняя поверхность нижней трети голени. Кожа вокруг язвы уплотнена, пигментирована. Нередко наблюдается экзема или дерматит. При пальпации в зоне трофических нарушений могут определяться кратерообразные провалы (места, где через фасцию голени выходят измененные коммуникантные вены). Визуально выявляются варикозно расширенные вены, чаще всего расположенные по медиальной и задней поверхности голени и задней поверхности бедра.
Для оценки состояния венозной системы проводятся:
- функциональные пробы;
- УЗДГ вен нижних конечностей, ультразвуковое дуплексное исследование;
- для исследования микроциркуляции показана реовазограия нижних конечностей.
Трофические язвы венозной этиологии часто развиваются у пожилых пациентов с целым «букетом» сопутствующих заболеваний, поэтому тактика лечения должна определяться только после всестороннего обследования больного.
Лечение трофической язвы
В процессе лечения трофической язвы врач-флеболог должен решить целый комплекс задач. Нужно устранить или по возможности минимизировать проявления основного заболевания, которые стали причиной образования язвы. Следует бороться с вторичной инфекцией и проводить лечение самой трофической язвы.
Проводится общая консервативная терапия. Пациенту назначают препараты для лечения основного заболевания (флеботоники, антиагреганты и т. д.), антибиотики (с учетом чувствительности микрофлоры). Местно для очищения трофической язвы применяют ферменты, лазерную обработку; для борьбы с вторичной инфекцией – местные антисептики, после устранения воспаления – ранозаживляющие мазевые повязки. При обширных дефектах может быть показана кожная пластика трофической язвы.
Хирургическое лечение причинной патологии проводится после подготовки (заживление язвы, нормализация общего состояния больного). Выполняют операции, направленные на восстановление венозного кровотока в области поражения: шунтирование, удаление варикозно расширенных вен (минифлебэктомия, флебэктомия).
Профилактика
Профилактические меры заключаются в раннем выявлении и своевременном лечении варикозного расширения вен. Пациенты, страдающие варикозом и посттромбофлебитической болезнью, должны использовать средства эластической компрессии (лечебный трикотаж, эластичные бинты). Следует соблюдать рекомендации врача, избегать продолжительных статических нагрузок. Больным с хронической венозной недостаточностью противопоказан труд в горячих цехах, длительное переохлаждение, работа в неподвижном состоянии. Необходима умеренная физическая нагрузка для стимуляции мышечной помпы голеней.
Синдром Рейно (СР) — это эпизодическое нарушение периферической циркуляции вследствие локальной артериальной вазоконстрикции (спазм) дигитальных артерий и кожных сосудов в ответ на воздействие холода или эмоциональный стресс. Клинически синдром проявляет
Синдром Рейно (СР) — это эпизодическое нарушение периферической циркуляции вследствие локальной артериальной вазоконстрикции (спазм) дигитальных артерий и кожных сосудов в ответ на воздействие холода или эмоциональный стресс. Клинически синдром проявляется резко очерченными изменениями цвета кожи пальцев кистей. В основе повышенного спазма сосудов лежит дефект центральных и локальных механизмов регуляции вазомоторных реакций.
Распространенность СР в общей популяции составляет 3–5% и различается между отдельными климатическими зонами [1]. Заболевание начинается преимущественно в подростковом или молодом возрасте и у женщин встречается чаще, чем у мужчин. Наблюдается тенденция к семейной агрегации заболевания.
Выделяют первичный и вторичный СР. Первичный, или идиопатический, СР характеризуется спазмом пальцевых артерий и терморегуляторных сосудов кожи при воздействии холода, без каких-либо признаков поражения сосудов. При вторичном СР наблюдается сочетание синдрома Рейно с симптомами других заболеваний.
Наиболее часто при СР поражаются кисти рук. Основным клиническим признаком СР является последовательная смена окраски кожи пальцев кистей на холоде. В начале приступа вазоспазма обычно появляется бледная окраска кожи, после чего в течение нескольких минут кожа приобретает синевато-фиолетовый оттенок. Вазоспазм обычно длится 15–20 мин и завершается быстрым восстановлением кровотока, о чем свидетельствует интенсивно розовая окраска кожи (реактивная гиперемия).
У некоторых больных приступы вазоспазма сопровождаются ощущением замерзания кистей, онемением и покалыванием в пальцах, которые проходят после восстановления кровотока. В фазе реактивной гиперемии больные могут чувствовать боль в пальцах кистей.
На ранних этапах заболевания изменения цвета кожи могут наблюдаться на дистальной фаланге одного или нескольких пальцев кистей. В дальнейшем область поражения охватывает все пальцы кистей и, возможно, стоп, при этом большие пальцы обычно остаются интактными. Вазоспазму могут подвергаться также сосуды кожи лица и других участков. В этих случаях можно наблюдать характерные изменения окраски кончика носа, губ и ушных раковин, а также кожи над коленными суставами. У отдельных больных в процесс вовлекаются и сосуды языка, что проявляется дизартрией во время приступа вазоспазма. При эпизодах вазоспазма может появляться мраморный рисунок на верхних и нижних конечностях — симптом, называемый сетчатым ливедо (livedo reticularis). Частота и продолжительность эпизодов вазоспазма могут варьировать как у различных больных, так и у одних и тех же пациентов в разное время года (зимой более интенсивные, чем летом).
Трехфазная перемена окраски кожи (побеление–посинение–покраснение) выявляется не во всех случаях; у части больных наблюдается двухфазное или однофазное изменение цвета. В зависимости от количества фаз изменения цвета кожи, выделяют достоверный и вероятный СР.
- Достоверный СР — повторные эпизоды двухфазного изменения окраски кожи на холоде.
- Вероятный СР — однофазное изменение окраски кожи, сопровождающееся онемением или парестезией под воздействием холода.
- СР нет — изменения окраски кожи под воздействием холода отсутствуют.
Более чем у 80% больных выявляется первичный СР. Для верификации первичного СР применяются диагностические критерии, предложенные E. V. Allen и G. E. Brown в 1932 г. и модифицированные в последние годы. Эти критерии, разработанные с учетом клинических и некоторых лабораторных показателей, а также результатов капилляроскопии ногтевого ложа, включают [2]:
- симметричность эпизодов вазоспазма;
- отсутствие заболеваний периферических сосудов;
- отсутствие гангрены, дигитальных рубчиков или повреждения тканей;
- нормальные капилляры ногтевого ложа;
- отсутствие АНФ и нормальное значение СОЭ.
Средний возраст развития СР составляет 14 лет; только у 27% больных болезнь дебютирует в возрасте старше 40 лет [3]. При первичном СР симптомы болезни обычно умеренно выражены, и только у 12% больных наблюдаются интенсивные эпизоды вазоспазма [4]. Приблизительно у 1/4 больных СР выявляется среди родственников первой линии [5].
Вместе с тем при большом числе состояний и заболеваний, ассоциирующихся с СР, он считается вторичным (таблица).
Наиболее часто вторичный СР ассоциируется с системной склеродермией, системной красной волчанкой, другими заболеваниями соединительной ткани, гематологическими нарушениями и приемом некоторых лекарств. При длительном наблюдении за больными, которым был поставлен предварительный диагноз первичного СР, удалось выявить, что у 13% из них на определенном этапе болезни развиваются признаки системного заболевания соединительной ткани (наиболее часто — системной склеродермии) [6].
Несмотря на идентичность клинических проявлений первичного и вторичного СР, при этих двух состояниях имеются некоторые различия в отдельных признаках. На вероятность вторичного характера СР указывают следующие признаки:
- поздний возраст начала;
- мужской пол;
- болезненные эпизоды вазоспазма с признаками тканевой ишемии (изъязвления);
- асимметричный характер атак;
- наличие признаков другого заболевания;
- лабораторные признаки аутоиммунных или сосудистых заболеваний;
- выявление АНФ;
- редукция и дилатация капилляров при капилляроскопии ногтевого ложа;
- распространенный характер СР, охватывающий проксимальные по отношению к пальцам кистей и стоп участки.
Вторичный СР развивается обычно в возрасте старше 30 лет, отличается более выраженными и болезненными эпизодами вазоспазма, структурными изменениями капилляров [7]. АНФ имеет относительно низкую прогностическую ценность для заболеваний соединительной ткани (30%), тогда как выявление специфических аутоантител значительно повышает вероятность вторичного характера СР [6, 8, 9]. Приблизительно у 15–20% больных СР, у которых выявляются специфические аутоантитела и/или капилляроскопические изменения, но отсутствуют симптомы заболеваний соединительной ткани, в дальнейшем (обычно в течение двух лет) развивается то или иное заболевание соединительной ткани [10, 11].
У всех больных со впервые выявленным СР необходимо проводить специальные исследования с целью дифференциальной диагностики первичного и вторичного характера патологии.
В первую очередь следует уточнить:
- имеются ли у пациента симптомы заболеваний соединительной ткани, с которыми наиболее часто ассоциируется СР (артриты, миалгии, лихорадка, «сухой» синдром, кожная сыпь, кардиопульмональные нарушения);
- принимает ли больной на момент исследования какие-либо препараты, особенно химиотерапевтические средства;
- подвергается ли больной вибрации или другим механическим воздействиям, травмирующим кисти;
- связаны ли эпизоды синдрома Рейно с определенными позиционными изменениями.
Необходимо учитывать, что клинические признаки ассоциированного с СР заболевания могут развиться по истечении нескольких месяцев или лет после начала СР. Наиболее объективным и специфичным инструментальным методом дифференциальной диагностики первичного и ассоциированного с системными заболеваниями соединительной ткани (прежде всего с системной склеродермией) СР является капилляроскопия ногтевого ложа. В норме капилляроскопическая картина представляет собой правильный ряд равномерно распределенных по краю ногтевого ложа и одинакового размера капилляров. При системной склеродермии, с которой наиболее часто ассоциируется СР, изменения количества капилляров (редукция) и их размеров (дилатация) появляются на ранних стадиях и часто предшествуют развитию клинических признаков заболевания.
Дифференциальная диагностика СР
Повышенная чувствительность к холоду характерна для популяции в целом. Холодная кожа или неочерченная крапчатость кожи пальцев, кистей и конечностей считаются нормальным ответом на воздействие холода. У больных СР, помимо повышенной чувствительности, под влиянием холода эпизодически наблюдаются побледнение и цианоз дистальных отделов пальцев. СР следует отличать от акроцианоза — состояния, характеризующегося продолжительным цианозом кистей или стоп, который усиливается под влиянием холода.
Повышенную чувствительность к холоду могут вызвать карпальный туннельный синдром и другие невропатии. При дифференциальной диагностике следует учитывать такие состояния, как криопротеинемии, диспротеинемии, контакт с поливинилхлоридом, наличие опухоли или гипотиреоза. Если признаки заболевания проявляются асимметрично, необходимо провести исследования для выявления окклюзивных заболеваний крупных сосудов. Атеросклероз не сопровождается типичными симметричными признаками СР, но в ряде случаев проявляется перемежающейся хромотой при нагрузках, асимметричным поражением конечности, изолированной или персистирующей дигитальной ишемией. Васкулиты, эмболии или другие окклюзивные поражения сосудов могут приводить к критической ишемии, но не к развитию типичного СР. Имеются доказательства того, что СР может служить клиническим проявлением генерализованных вазоспастических заболеваний, таких как стенокардия Принцметал и мигрень [12].
Сетчатое ливедо наблюдается также при васкулитах, антифосфолипидном синдроме и окклюзивных заболеваниях периферических сосудов, при которых, в отличие от СР, этот признак имеет устойчивый характер.
На замерзание конечностей, их онемение и покалывание довольно часто жалуются больные с заболеваниями периферических сосудов, сопровождающимися снижением кровотока и ишемией. При СР, в отличие от заболеваний периферических сосудов, указанные симптомы наблюдаются только во время вазоспазма и полностью проходят после восстановления исходного кровотока.
Лечение СР
Общие рекомендации для больных первичным и вторичным СР:
- следует избегать длительного пребывания на холоде, в том числе в неотапливаемом и сыром помещении;
- необходимо носить рукавицы вместо перчаток, хуже сберегающих тепло, головной убор и теплое нижнее белье;
- следует отказаться от курения, потребления кофе и кофеинсодержащих напитков;
- необходимо овладеть приемами, с помощью которых можно уменьшить длительность эпизодов вазоспазма (согревание кистей в теплой воде или подмышечной области, быстрые круговые движения кистей и др.).
Соблюдения указанных рекомендаций часто бывает достаточно для лечения больных первичным СР.
Дигитальные артерии и терморегуляторные сосуды кожи находятся преимущественно под симпатическим адренергическим контролем. Эмоциональный стресс может спровоцировать дигитальный вазоспазм, а состояние тревоги часто усиливает индуцированные холодом атаки Рейно [13]. В таких случаях бывает полезным назначение седативных средств. Важно избегать применения препаратов, которые могут вызвать вазоконстрикцию (симпатомиметики, клонидин, эрготамин, агонисты серотониновых рецепторов и др.). Курение может редуцировать пальцевой кровоток, вследствие чего больным СР следует отказаться от этой привычки.
Медикаментозное лечение СР
В случаях частых и продолжительных эпизодов вазоспазма при первичном СР и у больных вторичным СР необходимо назначение лекарственной терапии. Для лечения СР применяют препараты с вазодилатирующим действием или средства, влияющие на реологические свойства крови.
Блокаторы кальциевых каналов
Блокаторы кальциевых каналов обладают наибольшим вазодилатационным потенциалом. Препаратами выбора являются дигидропиридиновые производные — нифедипин, амлодипин, исрадипин и фелодипин. Обладающий кратковременным действием нифедипин в разовой дозе 10–20 мг при 3-кратном ежедневном приеме значительно уменьшает частоту и выраженность, а в некоторых случаях и продолжительность эпизодов вазоспазма [15]. Однократный прием 5–20 мг нифедипина достаточно эффективно предупреждает индуцированный холодом вазоспазм при приеме за 15–20 мин до воздействия холода. При назначении нифедипина наблюдается достоверное повышение кожного и мышечного кровотока [16]. Приблизительно у 1/3 больных на фоне приема нифедипина развиваются побочные эффекты, среди них наиболее часто встречаются артериальная гипотония, головная боль, гиперемия, тахикардия, отеки голеней. Уменьшение побочных эффектов возможно при назначении ретардных форм нифедипина в суточной дозе 20–40 мг [17]. У больных первичным СР, по сравнению со вторичным, терапевтический эффект препарата обычно проявляется в большей степени. При длительном приеме нифедипина в больших дозах возможны парестезии, боли в мышцах, а также развитие толерантности и уменьшение лечебного действия препарата.
Наряду с нифедипином, в лечении СР с успехом применяются и другие производные дигидропиридина — амлодипин, исрадипин и фелодипин, которые относятся к длительно действующим препаратам [18]. Амлодипин назначается один раз в день в дозе 5 мг, при недостаточном эффекте суточная доза может быть повышена до 10 мг. Наиболее распространенным побочным эффектом амлодипина является отек лодыжек. Исрадипин назначается в дозе 2,5 мг 2 раза в день. Побочные эффекты в виде головных болей и гиперемии обычно носят умеренно выраженный характер. Фелодипин применяют в дозе 10 мг 1 раз в сут, преимущественно в виде лекарственных форм, обеспечивающих постепенное высвобождение лекарственного вещества. Блокаторы кальциевых каналов подавляют активацию тромбоцитов, что также оказывает благоприятное действие при СР [19].
При наличии противопоказаний или непереносимости блокаторов кальциевых каналов для лечения СР применяются вазодилататоры других лекарственных групп.
Назначение симпатолитических препаратов обосновано тем, что адренергическая стимуляция играет важную роль в вазоконстрикции. Празозин достоверно уменьшает выраженность и частоту вазоспазма у больных с первичным СР [20].
Простагландины оказывают комплексное физиологическое воздействие, в частности речь идет о вазодилатации, антиоксидантном действии, подавлении агрегации тромбоцитов и др.
Алпростадил (вазапростан) при ежедневных в/в инфузиях 20–40 мкг препарата в 200 мл изотонического раствора NaCl в течение 15–20 дней достоверно уменьшает как частоту, так и интенсивность вазоспазма у больных с первичным и вторичным СР [21].
Илопрост уменьшает число атак в неделю и интенсивность вазоспазма у больных первичным и вторичным (ассоциированным с системной склеродермией) СР в среднем на 39 и 35% соответственно [22].
Пентоксифиллин обладает антиагрегационным и слабым вазодилатационным действием. Назначается в комбинации с другими сосудорасширяющими препаратами на длительное время.
В лечении СР применяется ряд вазодилататоров (нитроглицерин трансдермальный, гидралазин, папаверин, миноксидил), которые могут быть эффективными у отдельных больных. Однако частое развитие побочных эффектов (системная гипотензия, головная боль) ограничивает применение этих препаратов. Результаты исследований эффективности ингибиторов ангиотензинпревращающего фермента у больных СР весьма противоречивы, в настоящее время препараты этой группы не нашли широкого применения в клинической практике.
Ксантинола никотинат назначается в таблетках по 150 мг 3 раза в день. Длительность приема, с учетом переносимости и противопоказаний к его назначению (как и других препаратов никотиновой кислоты), устанавливается индивидуально и определяется эффективностью и переносимостью средства.
Лекарственная терапия СР имеет некоторые ограничения, включая недостаточный ответ, развитие толерантности при длительном применении, развитие ряда побочных эффектов, многие из которых становятся причиной отмены того или иного препарата. При неэффективности консервативной терапии с целью уменьшения проявлений СР возможно хирургическое лечение — локальная дигитальная симпатэктомия. Однако продолжительность и ожидаемая выраженность лечебного эффекта симпатэктомии до сих пор не уточнены, в связи с чем их трудно прогнозировать. Предполагаемая эффективность симпатэктомии может быть оценена в дооперационный период с помощью фармакологической симпатэктомии.
В большинстве случаев СР представляет собой заболевание, характеризующееся благоприятным прогнозом и стабильным течением. В дебюте заболевания, особенно при наличии факторов риска вторичного характера СР, все больные СР подлежат диспансеризации и врачебному осмотру один раз в год. Пациенты должны быть предупреждены о необходимости дополнительного визита к врачу при появлении новых симптомов, указывающих на возможное развитие заболеваний, с которыми наиболее часто ассоциируется СР, прежде всего системных заболеваний соединительной ткани.
По вопросам литературы обращайтесь в редакцию.
Р. Т. Алекперов, доктор медицинских наук
Институт ревматологии РАМН, Москва
Читайте также:

