Субиктеричность кожи у новорожденных что это
Обновлено: 18.04.2024
Желтуха – это окрашивание кожи и слизистых оболочек в желтый цвет. Иногда желтушность кожи называют иктеричностью (от ikterоs - желтуха). Нередко родители слышат от лечащего врача, что у ребенка кожа и склеры глаз “иктеричны”, это значит, что они имеют желтушную окраску. Развитие желтухи связано с повышенным содержанием в крови особого вещества из группы желчных пигментов, которое называется билирубин (от bilis – желчь и rubin - красный). Этот красный желчный пигмент является главным пигментом желчи и продуктом обмена гемоглобина, именно он придает желчи характерный золотисто-желтый цвет. После отщепления молекулы железа от молекулы гемоглобина отщепляется и глобин (белковая часть вещества). Под влиянием окислителей происходит ряд биохимических реакций, в результате которых остается билирубин, который не содержит в своей молекуле белок. Такой билирубин называют непрямым, или свободным. Эта фракция билирубина попадает в плазму крови, “прикрепляется” к белку альбумину и в таком виде циркулирует в крови. Непрямой билирубин не растворяется в воде, токсичен и не проходит через почечный фильтр и почками не выделяется. В печеночной клетке к молекуле непрямого билирубина присоединяются две молекулы вещества, которое называется глюкуроновой кислотой, и образуется другая фракция билирубина – прямой билирубин, или связанный. Он не токсичен, растворяется в воде, проходит через почечный барьер и выделяется с мочой. Именно прямой билирубин хорошо проникает в ткани и обуславливает желтушное окрашивание кожи, склер, слизистых оболочек.
Различают 4 разновидности желтух: конъюгационные, гемолитические, механические (обтурационные) и печеночные (паренхиматозные). Конъюгационная (от лат. сonjugatio – соединение) желтуха связана с нарушением процессов превращения непрямого билирубина. Гемолитическая возникает вследствие интенсивного распада (гемолиза) эритроцитов. Обтурационная желтуха развивается в результате механического препятствия на пути оттока желчи в двенадцатиперстную кишку (при желчнокаменной болезни, при заболеваниях желчных путей). Печеночная (паренхиматозная) желтуха обусловлена поражением ткани печени при гепатите различной природы (вирусном, токсическом, реактивном).
Желтуха физиологическая (желтуха новорожденных) - транзиторная (временная) конъюгационная желтуха, возникающая у большинства здоровых новорожденных в первые дни жизни, вследствие того, что эритроциты плода содержат особый вид гемоглобина (гемоглобин F - фетальный) и эти эритроциты после рождения разрушаются. Кроме этого, у новорожденных имеется и дефицит специального белка, который обеспечивает перенос билирубина через мембраны печеночных клеток. Способствует избыточному накоплению билирубина запаздывание созревания ферментативных систем печени, участвующих в превращении непрямого билирубина в прямой. Еще один фактор, влияющий на скорость выведения билирубина из организма – это низкая выделительная способность печени у новорожденных детей.
Проявляется физиологическая желтуха новорожденных окрашиванием кожи в желтый цвет на 3-4-й день после рождения. Печень и селезенка не увеличиваются, признаков усиленного распада (гемолиза) эритроцитов и анемии нет. По мере улучшения работы системы выделения билирубина и исчезновения избыточных кровяных клеток из русла крови, желтуха исчезает (обычно через 1-2 недели) и не причиняет никакого вреда ребенку.
Желтуха у недоношенных детей встречается чаще, чем у доношенных, она более выражена и держится более длительно – до 3-4 недель. Уровень прямого билирубина при этой форме желтухи достигает максимума на 5-6-й день жизни ребенка. В случае интенсивной желтухи дополнительно используют медикаментозные средства и фототерапию (терапию светом от специальной лампы). Под влиянием света происходит структурная изомеризация билирубина и образуется так называемый “люмирубин”, который имеет другой путь выведения, быстро проникает в желчь и мочу.
Выраженность повышения уровня билирубина в крови у недоношенных не зависит от массы тела при рождении, а находится в прямой зависимости от степени зрелости плода и наличия заболеваний матери в период беременности.
Редко встречается желтуха, вызываемая молоком матери (ее надо отличать от желтухи при грудном вскармливании), она встречается примерно у 1% вскармливаемых грудью новорожденных со значительными проявлениями желтухи. Появляется она после 1-й недели жизни ребенка. Предполагается, что эта форма желтухи связана с содержанием в молоке матери веществ из класса жирных кислот, которые угнетают функцию печеночных клеток ребенка и снижают активность ферментов, обеспечивающих “превращение” непрямого билирубина в прямой.
Желтуха при грудном вскармливании развивается на 2-4-й день жизни, угасает на 3-4-й неделе, частота ее встречаемости - до 15 % случаев. При этом виде желтухи ребенка следует чаще кормить (можно больше 8 раз в сутки) грудным молоком, так как грудное вскармливание способствует более частому стулу и более быстрому выведению билирубина из организма. Так как у детей с повышенным уровнем билирубина часто повышенная сонливость, то их рекомендуют обязательно будить для кормления.
Прекращают грудное вскармливание у детей с желтухой только при некоторых наследственных заболеваниях, связанных с нарушением обмена веществ, например, при галактоземии.
К группе конъюгационных желтух относится конституциональная печеночная дисфункция (синдром Жильбера-Мейленграхта) – наследственное заболевание. Причиной нарушения билирубинового обмена при этой форме желтухи является изменение процессов захвата молекулы билирубина печеночной клеткой или нарушение связывания билирубина с глюкуроновой кислотой, что связано с наследственной неполноценностью ферментативных систем печени. По клинике синдром Жильбера очень сходен с транзиторной физиологической желтухой новорожденных. Печень и селезенка не увеличиваются, признаков повышенного распада эритроцитов и малокровия не наступает. Окраска кала и мочи нормальная. Лечение проводится симптоматическое. Прогноз благоприятный.
Желтуха у новорожденных может развиться при гипотиреозе - снижении функциональной активности щитовидной железы. Сочетается такая форма желтухи с другими признаками недостаточной выработки гормонов щитовидной железы: отечностью тканей, грубостью голоса, сухостью волос, повышением уровня холестерина крови, задержкой процессов окостенения и др. Возникает желтуха при гипотиреозе на 2-3-й день жизни, длится до 3-12 недель, а иногда и до 4-5 месяцев. Лечение проводят по рекомендации эндокринолога с использованием препаратов – гормонов щитовидной железы.
Желтуха детей, родившихся у матерей с сахарным диабетом, связана с незрелостью печени ребенка, если у матери тяжелое течение сахарного диабета. При очень высоких показателях уровня билирубина проводят внутривенное вливание препаратов, способствующих более быстрому выведению билирубина из организма.
Желтуха у детей с пилоростенозом и обструкцией кишечника. Причиной повышения уровня непрямого билирубина крови при этом заболевании является обратное всасывание его из кишечника. При пилоростенозе увеличенный отдел желудка (привратник) может сдавливать общий желчный проток и нарушать желчеотделение. Лечение основного заболевания приводит к нормализации пигментного обмена и исчезновению желтухи.
Гемолитическая желтуха является проявлением повышенного разрушения эритроцитов ребенка. Наиболее часто она является симптомом гемолитической болезни новорожденного (ГБН), связанной с несовместимостью крови матери и плода по группе или резус-фактору. Развиваются гемолитические желтухи также при дефиците ферментативных систем эритроцитов, при нарушении структуры гемоглобина (например, при серповидно-клеточной анемии), при нарушении формы и структуры самого эритроцита (например, микросфероцитозе – анемии Минковского-Шоффара). Патологическая желтуха проявляется в течение первых суток после рождения. Она развивается, когда чрезмерно быстро разрушается много эритроцитов. Если высвобождается очень много билирубина, это может вызвать нарушения функции головного мозга. Такое состояние называют “ядерной желтухой” или “билирубиновой энцефалопатией”, так как при этой тяжелой форме желтухи новорожденных желчные пигменты и дегенеративные изменения обнаруживают в сером веществе головного мозга (особенно в ядрах ствола). Проявляется заболевание сонливостью, плохим сосанием, изменением рефлексов. Среди поздних проявлений - глухота, параличи, умственная отсталость.
Лечение зависит от причин развития гемолитической желтухи и нередко требует проведения заменного переливания крови.
Печеночная желтуха развивается при поражении печени вирусами, бактериями, простейшими (гепатит, сепсис, цитомегаловирусная инфекция и др.). При этом состоянии происходит накопление в крови непрямого и прямого билирубина. Кожа ребенка и слизистые оболочки окрашиваются в желтый цвет с зеленоватым оттенком, происходит увеличение печени, иногда и селезенки. Стул становится слабо окрашенным, моча приобретает более интенсивную окраску. В анализах крови обнаруживают повышение показателей активности печеночных ферментов. Лечение проводят комплексное, в зависимости от причин появления паренхиматозной желтухи.
При обтурационной (механической) желтухе происходит увеличение печени и селезенки, обесцвечивание кала и усиление окраски мочи. Эта форма желтухи может развиваться при кисте желчного протока, кольцевидной поджелудочной железе, атрезии (недоразвитии) желчных ходов, при сгущении желчи на фоне гемолитической болезни, при муковисцидозе и др. Лечение зависит от причин, вызвавших механическую желтуху. При ряде патологических состояний необходимо хирургическое вмешательство.
В настоящее время известно более 50 заболеваний, которые могут проявляться желтушным окрашиванием кожи у детей в период новорожденности. Поэтому длительное сохранение желтушного окрашивания кожи у новорожденного требует обязательного определения уровня общего билирубина и его фракций в сыворотке крови, показателей функции печени, общего анализа крови, ультразвукового исследования органов брюшной полости и консультации специалистов для уточнения причины желтухи и своевременного проведения лечения.
ПАМЯТКА ДЛЯ ПАЦИЕНТОВ
Вы перенесли острый гепатит В, С, и Вам необходимо знать, что исчезновение желтухи, удовлетворительные лабораторные показатели и хорошее самочувствие не служат показателями полного выздоровления, так как полное восстановление здоровья печени наступает в течение 6 месяцев. С целью предупреждения обострения заболевания и перехода в хроническую форму важно строго соблюдать врачебные рекомендации, относящиеся к последующему наблюдению и обследованию в условиях поликлиники, режиму дня, диете, а также к условиям труда.
РЕЖИМ
Возвращение к трудовой деятельности, связанной с большим физическим напряжением или профессиональными вредностями, допустимо не ранее чем через 3-6 месяцев после выписки. До этого возможно продолжение трудовой деятельности в облегченных условиях.
После выписки из стационара следует остерегаться переохлаждения и избегать перегревания на солнце, не рекомендуют поездки на южные курорты на протяжении первых 3 месяцев. Также следует остерегаться приема медикаментов, оказывающих побочное (токсическое) влияние на печень. После нормализации биохимических показателей крови на протяжении 6 месяцев запрещается участие в спортивных соревнованиях. Переболевшие ОГВ и ОГС освобождаются от профилактических прививок на 6 месяцев. Занятия спортом ограничиваются лишь комплексом лечебной гимнастики.
ДИЕТА
На протяжении 6 месяцев после выписки необходимо обращать особое внимание на питание, которое должно быть достаточно полноценным, при полном исключении вредных для печени веществ. Алкогольные напитки (в том числе пиво) категорически запрещаются. Питаться в течение дня необходимо регулярно через каждые 3-4 часа, избегая переедания.
Разрешено
Молоко и молочные продукты во всех видах.
Отварное и тушеное мясо – говядина, телятина, куры, индейка, кролик.
Отварная свежая рыба – щука, карп, судак и морская рыба: треска, окунь, ледяная.
Овощи, овощные блюда, фрукты, квашеная капуста.
Крупяные и мучные изделия.
Супы овощные, крупяные, молочные.
Ограничено можно
Мясные бульоны и супы – нежирные, не чаще 1-2 раза в неделю.
Сливочное масло (не более 50-70 г/сутки, для детей – 30-40 грамм), сливки, сметана.
Яйца – не более 2-3 раз в неделю, белковые омлеты.
Сыр в небольшом количестве, только не острый.
Сосиски говяжьи, колбаса докторская, диетическая, столовая.
Икра лососевых и осетровых, сельдь.
Запрещено
Все виды жареных, копченых и маринованных продуктов.
Свинина, баранина, гуси, утки.
Острые приправы – хрен, перец, горчица, уксус.
Кондитерские изделия – торты, пирожные.
Шоколад, шоколадные конфеты, какао, кофе.
ВРАЧЕБНОЕ НАБЛЮДЕНИЕ И КОНТРОЛЬ
Обследование перенесших вирусные гепатиты проводят через 1,3,6 месяцев, а далее в зависимости от заключения диспансерного врача. Снятие с учета при благоприятном исходе проводят не ранее 12 месяцев после выписки из стационара.
Помните, что только наблюдение врача-инфекциониста и регулярное лабораторное обследование позволит установить факт Вашего выздоровления или перехода заболевания в хроническую форму. В случае назначения врачом противовирусного лечения Вы должны строго соблюдать режим введения препарата и регулярно приходить на лабораторный контроль показателей крови, так как это позволит максимально снизить вероятность побочного действия препарата и обеспечить контроль над инфекцией.
Явиться на лабораторное обследование нужно в строго назначенный врачом день натощак.
Ваше первое посещение КИЗ поликлиники назначает лечащий врач.
Установленные контрольные сроки повторных врачебных осмотров в поликлинике или гепатологическом центре обязательны для всех, перенесших вирусный гепатит. При необходимости Вы можете обращаться в кабинет последующих наблюдений стационаров, или гепатологический центр, или КИЗ поликлиники также и помимо этих сроков.
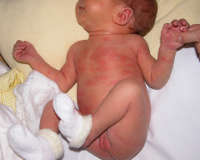
Эритема новорожденных – это транзиторное покраснение кожи, связанное с адаптацией ребенка к внеутробной жизни и сопровождающееся полиморфными высыпаниями. Основным симптомом является розово-красный цвет кожных покровов, отмечающийся в первые часы или на 2-3 сутки жизни ребенка. На фоне покраснения кожи в ряде случаев обнаруживается мелкая серо-желтая сыпь. Общее состояние, как правило, не страдает. Диагностика эритемы новорожденных основана на характерных симптомах, появляющихся в определенном возрасте (первые дни жизни), при этом клинические и лабораторные признаки воспаления и инфекций отсутствуют. Лечение обычно не требуется, по показаниям назначаются десенсибилизирующие препараты.
МКБ-10
Общие сведения
Эритема новорожденных относится к типичным адаптационным реакциям ребенка в первые дни жизни, поэтому фактически считается нормой в педиатрии. Встречается более чем у половины детей, чаще у малышей, находящихся на грудном вскармливании. Развитие эритемы в некоторой степени зависит от соматического состояния матери, поэтому можно говорить об увеличении частоты встречаемости в последние 10-20 лет в связи с ростом заболеваемости матерей сахарным диабетом, ожирением и другими социально значимыми нозологиями. Врачам следует сохранять настороженность в отношении эритемы новорожденных, особенно ее токсической формы, поскольку не исключено влияние данного состояния на дальнейшее формирование аллергического статуса ребенка.

Причины
Ведущая причина возникновения эритемы новорожденных – послеродовая адаптация организма к внешней среде, то есть к жизни вне материнской утробы. Первичные проявления во многом обусловлены разницей температур матки и окружающего воздуха, вследствие чего периферические сосуды ребенка расширяются для большего притока крови и, соответственно, согревания. Поэтому кожные покровы выглядят покрасневшими. Дальнейшее развитие эритемы новорожденных имеет аллергический генез. По большей части речь идет об алиментарном пути проникновения аллергенов, но также имеет место и контактный механизм. Определенную роль всегда играют патологии беременности – гипоксия плода, фетоплацентарная недостаточность и др.
Патогенез
После рождения ребенок впервые получает пищу через желудочно-кишечный тракт, незнакомый до настоящего момента с грудным молоком. Важно понимать, что само по себе грудное вскармливание не вызывает аллергию, но ее проявления практически неизбежны из-за огромного количества компонентов пищи, абсолютно новых для малыша. Воздушная среда тоже может оказывать раздражающее действие на кожу, но механизмы адаптации выстраиваются уже ко 2-3 дню жизни, поэтому проявления эритемы новорожденных постепенно нивелируются.
Классификация
Эритема новорожденных бывает физиологической и токсической. Классификация условна, поскольку токсическая эритема новорожденных многими специалистами не связывается с процессами адаптации ребенка в первые дни жизни, а считается отдельной нозологией. Кроме того, обе формы данного состояния требуют разной врачебной тактики.
- Физиологическая эритема. Клиническая картина обусловлена в большей степени температурным фактором.
- Токсическая эритема. Кожные проявления связаны с аллергической сенсибилизацией. Эритема может быть ограниченной, распространенной и генерализованной в зависимости от степени выраженности кожных проявлений и ухудшения общего состояния.
Симптомы эритемы новорожденных
Физиологическая эритема проявляется в первые часы жизни ребенка общим покраснением кожных покровов, больше в области ладоней и стоп. Как правило, в течение первых суток симптомы исчезают. Токсическая эритема новорожденных дебютирует обычно на 2-3 сутки (по мере формирования аллергического ответа). В отличие от физиологической эритемы, характерным признаком является сыпь. Высыпания представлены мелкими серо-желтыми бугорками с ярко-красным венчиком вокруг них. Образования всегда локализуются на ограниченном участке кожи и могут быть как единичными, так и множественными.
Общее состояние ребенка не страдает, температура может быть незначительно повышена. Генерализованная токсическая эритема новорожденных встречается относительно редко, в подобных случаях имеет место не только обильная сыпь по всему телу, но и ухудшение общего состояния – слабость, повышение температуры.
Диагностика
При постановке диагноза врач-педиатр учитывает возраст ребенка и частое сочетание с другими транзиторными состояниями: маститом новорожденных, гормональным кризом, олигурией, мочекислым инфарктом и т. д. Дифференциальная диагностика кожных элементов обычно не вызывает затруднений, поскольку характерные проявления вирусных заболеваний выглядят иначе и всегда сопровождаются другими общими симптомами. Физиологическая и токсическая эритема новорожденных различаются по времени появления и типу изменений кожи. При выраженной сенсибилизации проводится анализ крови малыша и матери на различные аллергены. Полностью исключить инфекции позволяет результат общего анализа крови ребенка.
Лечение эритемы новорожденных
В большинстве случаев состояние не требует врачебного вмешательства. Симптомы купируются в течение одного или нескольких дней. Ускорению восстановления нормального цвета кожных покровов способствуют воздушные ванны и соблюдение гипоаллергенной диеты кормящей матерью. Токсическая эритема новорожденных может потребовать назначения десенсибилизирующих препаратов (обычно в каплях) при обильных высыпаниях и беспокойстве ребенка, обычно связанном с зудом.
С целью снижения местного раздражения рекомендуется свободное пеленание. По показаниям проводится коррекция дисбиоза, поскольку большинство аллергенов попадают в организм ребенка именно алиментарным путем. Прогноз состояния благоприятный.
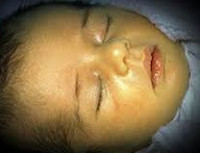
Желтуха новорожденных – физиологическое или патологическое состояние, обусловленное гипербилирубинемией и проявляющееся желтушным окрашиванием кожи и видимых слизистых у детей в первые дни их жизни. Желтуха новорожденных характеризуется повышением концентрации билирубина в крови, анемией, иктеричностью кожных покровов, слизистых оболочек и склер глаз, гепато- и спленомегалией, в тяжелых случаях – билирубиновой энцефалопатией. Диагностика желтухи новорожденных основывается на визуальной оценке степени желтухи по шкале Крамера; определении уровня эритроцитов, билирубина, печеночных ферментов, группы крови матери и ребенка и др. Лечение желтухи новорожденных включает грудное вскармливание, инфузионную терапию, фототерапию, заменное переливание крови.
Общие сведения
Желтуха новорожденных – неонатальный синдром, характеризующийся видимой желтушной окраской кожи, склер и слизистых оболочек вследствие повышения уровня билирубина в крови ребенка. По наблюдениям, на первой неделе жизни желтуха новорожденных развивается у 60 % доношенных и 80% недоношенных детей. В педиатрии наиболее часто встречается физиологическая желтуха новорожденных, составляющая 60–70 % всех случаев синдрома. Желтуха новорожденных развивается при повышении уровня билирубина свыше 80-90 мкмоль/л у доношенных и более 120 мкмоль/л у недоношенных младенцев. Длительная или выраженная гипербилирубинемия оказывает нейротоксическое действие, т. е вызывает повреждение головного мозга. Степень токсического воздействия билирубина зависит, главным образом, от его концентрации в крови и длительности гипербилирубинемии.

Классификация и причины желтухи новорожденных
Прежде всего, неонатальная желтуха может быть физиологической и патологической. По происхождению желтухи новорожденных делятся на наследственные и приобретенные. На основании лабораторных критериев, т. е. повышения той или иной фракции билирубина различают гипербилирубинемии с преобладанием прямого (связанного) билирубина и гипербилирубинемии с преобладанием непрямого (несвязанного) билирубина.
К конъюгационным желтухам новорожденных относятся случаи гипербилирубинемии, возникающие вследствие пониженного клиренса билирубина гепатоцитами:
- Физиологическую (транзиторную) желтуху доношенных новорожденных
- Желтуху недоношенных новорожденных
- Наследственные желтухи, связанные с синдромами Жильбера, Криглера-Найяра I и II типов и др.
- Желтуху при эндокринной патологии (гипотиреозе у детей, сахарном диабете у матери)
- Желтуху у новорожденных с асфиксией и родовой травмой
- Прегнановую желтуху детей, находящихся на естественном вскармливании
- Медикаментозную желтуху новорожденных, обусловленную назначением левомицетина, салицилатов, сульфаниламидов, хинина, больших доз витамина К и др.
Гемолитическая желтуха новорожденных характеризуется повышением уровня билирубина вследствие усиленного разрушения (гемолиза) эритроцитов ребенка. К такого вида гипербилирубинемиям относят:
- Гемолитическую болезнь плода и новорожденных
- Эритроцитарные ферменто- и мембранопатии
- Гемоглобинопатию (серповидно-клеточную анемию, талассемию)
- Полицитемию
Механические желтухи новорожденных обусловлены нарушением отведения билирубина с желчью по желчным путям и кишечнику. Они могут возникать при пороках (атрезии, гипоплазии) внутрипеченочных и внепеченочных протоков, внутриутробной желчнокаменной болезни, сдавлении желчных ходов извне инфильтратом или опухолью, закупорке желчных протоков изнутри, синдроме сгущения желчи, пилоростенозе, кишечной непроходимости и пр.
Желтухи смешанного генеза (паренхиматозные) возникают у новорожденных с фетальным гепатитом, обусловленным внутриутробными инфекциями (токсоплазмозом, цитомегалией, листериозом, герпесом, вирусными гепатитами А, В, D), токсико-септическим поражением печени при сепсисе, наследственных заболеваниях обмена веществ (муковисцидозе, галактоземии).
Симптомы желтухи новорожденных
Физиологическая желтуха новорожденных
Транзиторная желтуха является пограничным состоянием периода новорожденности. Сразу после рождения ребенка избыток эритроцитов, в которых присутствует фетальный гемоглобин, разрушается с образованием свободного билирубина. Вследствие временной незрелости фермента печени глюкуронилтрансферазы и стерильности кишечника связывание свободного билирубина и его выведение из организма новорожденного с калом и мочой снижено. Это приводит к накоплению лишнего объема билирубина в подкожно-жировой клетчатке и окрашиванию кожи и слизистых в желтый цвет.
Физиологическая желтуха новорожденных развивается на 2-3 сутки после рождения, достигает своего максимума на 4-5 сутки. Пиковая концентрация непрямого билирубина составляет в среднем 77-120 мкмоль/л; моча и кал имеют нормальную окраску; печень и селезенка не увеличены.
При транзиторной желтухе новорожденных легкая степень желтушности кожных покровов не распространяется ниже пупочной линии и обнаруживается только при достаточном естественном освещении. При физиологической желтухе самочувствие новорожденного обычно не нарушается, однако при значительной гипербилирубинемии может отмечаться вялое сосание, заторможенность, сонливость, рвота.
У здоровых новорожденных возникновение физиологической желтухи связывается с временной незрелостью ферментных систем печени, поэтому не считается патологическим состоянием. При наблюдении за ребенком, организации правильного вскармливания и ухода проявления желтухи стихают самостоятельно к 2-хнедельному возрасту новорожденных.
Желтуха недоношенных новорожденных характеризуется более ранним началом (1–2 сутки), достижением пика проявлений к 7 суткам и стиханием к трем неделям жизни ребенка. Концентрация непрямого билирубина в крови недоношенных выше (137-171 мкмоль/л), его прирост и снижение происходит медленнее. Вследствие более длительного созревания ферментных систем печени у недоношенных детей создается угроза развития ядерной желтухи и билирубиновой интоксикации.
Наследственные желтухи
Наиболее распространенной формой наследственной конъюгационной желтухи новорожденных является конституциональная гипербилирубинемия (синдром Жильбера). Данный синдром встречается в популяции с частотой 2-6%; наследуется по аутосомно-доминантному типу. В основе синдрома Жильбера лежит дефект активности ферментных систем печени (глюкуронилтрансферазы) и, как следствие, - нарушение захвата билирубина гепатоцитами. Желтуха новорожденных при конституциональной гипербилирубинемии протекает без анемии и спленомегалии, с незначительным подъемом непрямого билирубина.
Наследственная желтуха новорожденных при синдроме Криглера-Найяра связана с очень низкой активностью глюкуронилтрансферазы (II тип) или ее отсутствием (I тип). При I типе синдрома желтуха новорожденных развивается уже в первые дни жизни и неуклонно нарастает; гипербилирубинемия достигает 428 мкмоль/л и выше. Типично развитие ядерной желтухи, возможен летальный исход. II тип синдрома, как правило, имеет доброкачественное течение: неонатальная гипербилирубинемия составляет 257-376 мкмоль/л; ядерная желтуха развивается редко.
Желтуха при эндокринной патологии
Обычно возникает у детей с врожденным гипотиреозом в связи с дефицитом гормонов щитовидной железы, нарушающим созревание фермента глюкуронозилтрансферазы, процессы конъюгации и экскреции билирубина. Желтуха при гипотиреозе выявляется у 50-70% новорожденных; проявляется на 2-3-й сутки жизни и сохраняется до 3-5 месяцев. Кроме желтухи, у новорожденных отмечается вялость, пастозность, артериальная гипотония, брадикардия, грубый голос, запоры.
Ранняя желтуха может возникать у новорожденных, матери которых страдают сахарным диабетом, вследствие гипогликемии и ацидоза. Проявляется затяжным желтушным синдромом и непрямой гипербилирубинемией.
Желтуха у новорожденных с асфиксией и родовой травмой
Гипоксия плода и асфиксия новорожденных задерживают становление ферментных систем, следствием чего является гипербилирубинемия и ядерная желтуха. Различные родовые травмы (кефалогематомы, внутрижелудочковые кровоизлияния) могут являться источниками образования непрямого билирубина и его усиленного проникновения в кровь с развитием желтушного окрашивания кожи и слизистых. Выраженность желтухи новорожденных зависит от тяжести гипоксически-асфиксического синдрома и уровня гипербилирубинемии.
Прегнановая желтуха
Синдром Ариеса, или желтуха детей, находящихся на естественном вскармливании, развивается у 1-2% новорожденных. Может возникать на первой неделе жизни ребенка (ранняя желтуха) либо на 7-14 день (поздняя желтуха новорожденных) и сохраняться 4-6 недель. Среди возможных причин прегнановой желтухи новорожденных называют присутствие в молоке материнских эстрогенов, препятствующих связыванию билирубина; неустановившуюся лактацию у матери и относительное недоедание ребенка, вызывающие обратное всасывание билирубина в кишечнике и его поступление в кровяное русло и др. Считается, что факторами риска желтухи у новорожденных, находящихся на грудном вскармливании, служат позднее (позже 12ч жизни) отхождение мекония, задержка пережатия пуповины, стимуляция родов. Течение такого вида желтухи новорожденных всегда доброкачественно.
Ядерная желтуха и билирубиновая энцефалопатия
При прогрессирующем повышении концентрации непрямого билирубина в крови может происходить его проникновение через гематоэнцефалический барьер и отложение в базальных ядрах головного мозга (ядерная желтуха новорожденных), обусловливающее развитие опасного состояния - билирубиновой энцефалопатии.
На первом этапе в клинике преобладают признаки билирубиновой интоксикации: вялость, апатия, сонливость ребенка, монотонный крик, блуждающий взгляд, срыгивания, рвота. Вскоре у новорожденных появляются классические признаки ядерной желтухи, сопровождающиеся ригидностью затылочных мышц, спастичностью мышц тела, периодическим возбуждением, выбуханием большого родничка, угасанием сосательного и других рефлексов, нистагмом, брадикардией, судорогами. В этот период, который длится от нескольких дней до нескольких недель, происходит необратимое поражение ЦНС. В течение последующих 2-3 месяцев жизни в состоянии детей наблюдается обманчивое улучшение, однако уже на 3-5 месяце жизни диагностируются неврологические осложнения: ДЦП, ЗПР, глухота и т. д.
Диагностика желтухи новорожденных
Желтуха выявляется еще на этапе пребывания ребенка в родильном доме врачом-неонатологом или педиатром при посещении новорожденного вскоре после выписки.
Для визуальной оценки степени желтухи новорожденных используется шкала Крамера.
- I степень – желтушность лица и шеи (билирубин 80 мкмоль/л)
- II степень – желтушность распространяется до уровня пупка (билирубин 150 мкмоль/л)
- III степень - желтушность распространяется до уровня коленей (билирубин 200 мкмоль/л)
- IV степень - желтушность распространяется на лицо, туловище, конечности, за исключением ладоней и подошв (билирубин 300 мкмоль/л)
- V - тотальная желтушность (билирубин 400 мкмоль/л)
Необходимыми лабораторными исследованиями для первичной диагностики желтухи новорожденных являются: билирубин и его фракции, общий анализ крови, группа крови ребенка и матери, тест Кумбса, ПТИ, общий анализ мочи, печеночные пробы. При подозрении на гипотиреоз необходимо определение тиреоидных гормонов Т3, Т4, ТТГ в крови. Выявление внутриутробных инфекций осуществляется методом ИФА и ПЦР.
В рамках диагностики механических желтух новорожденным проводится УЗИ печени и желчных протоков, МР-холангиография, ФГДС, обзорная рентгенография брюшной полости, консультация детского хирурга и детского гастроэнтеролога.
Лечение желтухи новорожденных
Для предотвращения желтухи и уменьшения степени гипербилирубинемии все новорожденные нуждаются в раннем начале (с первого часа жизни) и регулярном грудном вскармливании. У новорожденных с неонатальными желтухами частота рекомендуемых кормлений грудью составляет 8–12 раз в сутки без ночного перерыва. Необходимо увеличение суточного объема жидкости на 10-20% по сравнению с физиологической потребностью ребенка, прием энтеросорбентов. При невозможности оральной гидратации проводится инфузионная терапия: капельное введение глюкозы, физ. раствора, аскорбиновой кислоты, кокарбоксилазы, витаминов группы В. С целью повышения конъюгации билирубина новорожденному с желтухой может назначаться фенобарбитал.
Самым эффективным методом лечения непрямой гипербилирубинемии является фототерапия в непрерывном или прерывистом режиме, способствующая переводу непрямого билирубина в водорастворимую форму. Осложнениями фототерапии могут являться гипертермия, дегидратация, ожоги, аллергические реакции.
При гемолитической желтухе новорожденных показано заменное переливание крови, гемосорбция, плазмаферез. Все патологические желтухи новорожденных требуют незамедлительной терапии основного заболевания.
Прогноз желтухи новорожденных
Транзиторная желтуха новорожденных в подавляющем большинстве случаев проходит без осложнений. Однако нарушение механизмов адаптации может привести к переходу физиологической желтухи новорожденных в патологическое состояние. Наблюдения и доказательная база свидетельствуют об отсутствии взаимосвязи вакцинации от вирусного гепатита В с желтухой новорожденных. Критическая гипербилирубинемия может привести к развития ядерной желтухи и ее осложнений.
Дети с патологическими формами неонатальной желтухи подлежат диспансерному наблюдению участкового педиатра и детского невролога.
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
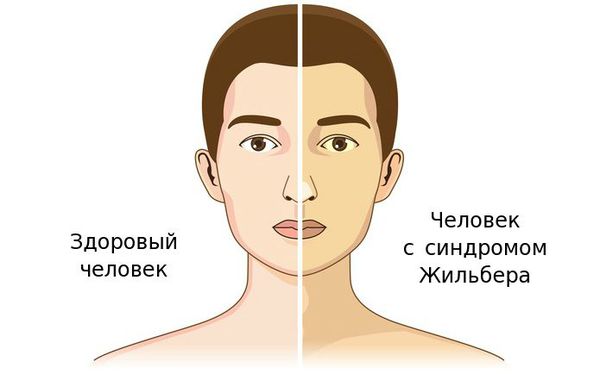
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.
К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .
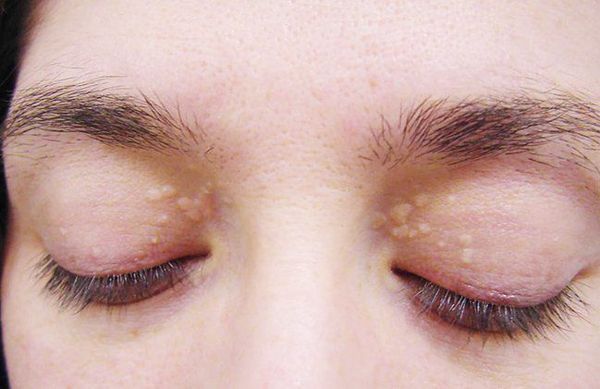
Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.
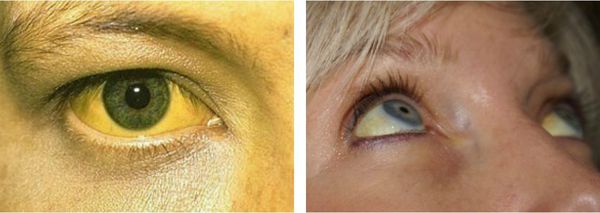
Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).
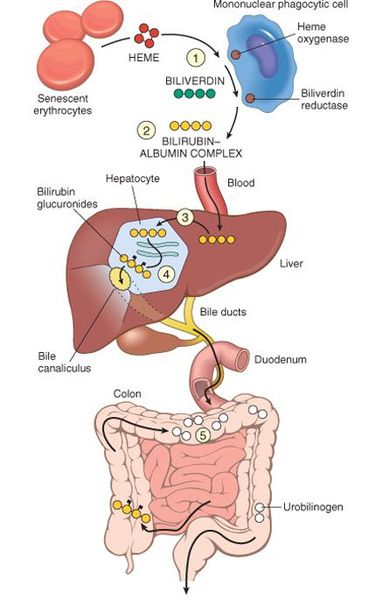
У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.
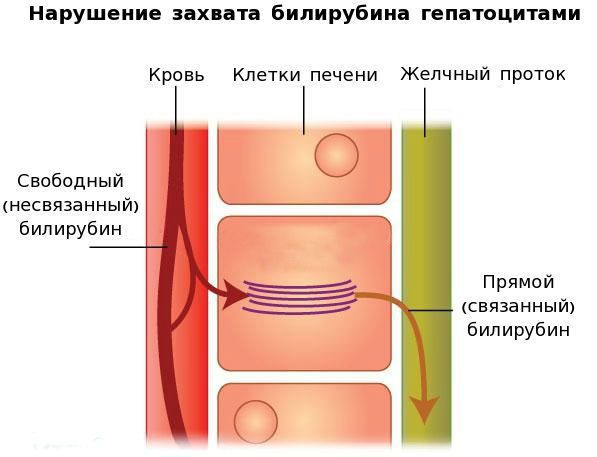
В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.
Что такое цирроз печени? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Цирроз печени (ЦП) — это хроническое дегенеративное заболевание печени, связанное с диффузным патологическим процессом, при котором нормальные клетки печени повреждаются, а затем замещаются рубцовой тканью, образуя избыточный фиброз и структурно-анатомические регенераторные узлы.
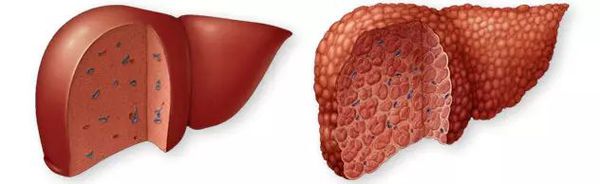
Этиология
По этиологическим характеристикам можно выделить:
- распространённые формы ЦП;
- редкие формы ЦП.
К распространённым относят вирусные (В, С, D), алкогольные и метаболические формы цирроза печени.
Редкими формами ЦП являются:
- аутоиммунные, лекарственные, токсические, первичные и вторичные билиарные циррозы;
- генетически обусловленные патологии — гемохроматоз (нарушение обмена железа), болезнь Вильсона — Коновалова, дефицит белка альфа-1-антитрипсина, гликогеноз IV типа (недостаток ферментов), галактоземия, наследственная тирозинемия и непереносимость фруктозы;
- нарушение венозного оттока из печени — венокклюзионные формы ЦП (болезнь Бадда — Киари);
- тяжёлая правожелудочковая сердечная недостаточность;
- флебопортальные циррозы (типа Банти).
Пути заражения
Заразиться циррозом печени нельзя. Однако, если он вызван вирусным гепатитом, то возбудитель может передаться через кровь, при половых контактах и от матери к ребёнку.
Основную роль в возникновении и развитии вирусного ЦП играют симптомные, малосимптомные и бессимптомные формы острого вирусного гепатита В, С, а также одновременное заболевание гепатитами В и D с последующим переходом в активный хронический вирусный гепатит. У большинства больных интервал между острым гепатитом С и клинически выраженными проявлениями ЦП превышает 30 лет. Только у мужчин, употребляющих более 50 г спирта в день, выраженные формы ЦП возникают через 13-15 лет.
Наиболее частыми причинами смерти больных ЦП является:
- большая печёночная недостаточность;
- кровотечение из варикозно расширенных вен пищевода;
- первичный рак печени;
- иммунопротективная недостаточность, влекущая за собой активизацию инфекционных (микробных) процессов, в первую очередь спонтанного бактериального перитонита и пневмонии, а также возникновение оксидативного стресса.
У больных в терминальной (заключительной) фазе заболеваний печени в основном наблюдаются декомпенсированные формы цирроза печени: асцит, варикозное расширение вен пищевода и желудка, энцефалопатия и желтуха.
Особенности цирроза печени у детей
Заболевание у детей встречается крайне редко и обычно связано:
- с аутоиммунным поражением печени;
- кардиогенными заболеваниями — лёгочной гипертензией и хронической сердечной недостаточностью;
- болезнью Бадда — Киари;
- врождёнными болезнями накопления — наследственным гемохроматозом, лизосомальными болезнями накопления, болезнью Вильсона — Коновалова;
- флебопортальным циррозом (типа Банти).
Прогноз у таких детей неблагоприятный, чаще всего они погибают, так как не успевают попасть к гепатологу и выяснить диагноз. Также они обычно страдают от множества сопутствующих болезней, в том числе от основного заболевания, ставшего причиной цирроза.
Проявления заболевания у детей и взрослых схожи. Единственный эффективный метод лечения цирроза у детей — это пересадка печени. Поэтому крайне важно вовремя диагностировать заболевание и встать в очередь на пересадку печени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цирроза печени
Цирроз печени в течение длительного времени может протекать латентно, т. е. бессимптомно.
Клиническая картина ЦП зависит от его формы и течения, активности основного заболевания, а также наличия или отсутствия печёночно-клеточной недостаточности, синдрома портальной гипертензии, холестаза и внепечёночных проявлений.
Основные общие симптомы, которые чаще всего встречаются при ЦП:
- повышенная утомляемость;
- похудение;
- нарушения сознания и поведения;
- ухудшение аппетита и чувство дискомфорта в животе;
- пожелтение кожи, белковых оболочек глаз и слизистой;
- осветление или обесцвечивание кала;
- потемнение мочи;
- болевые ощущения в животе;
- отёки;
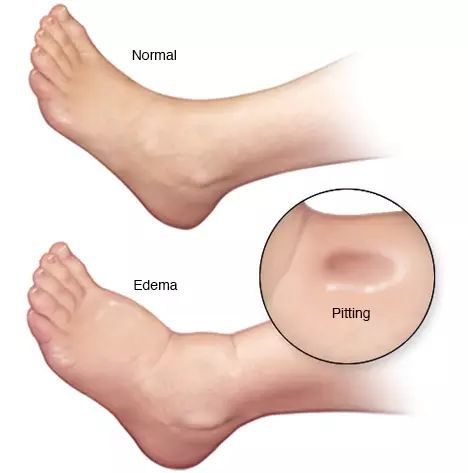
- асцит (скопление жидкости в брюшной полости);
- кровотечения из носа, желудочно-кишечного тракта, дёсен или геморроидальных узлов, а также подкожные кровоизлияния;
- часто возникающие бактериальные инфекции (например, органов дыхания);
- снижение полового влечения;
- кожный зуд.
Симптомы распространённых форм ЦП
При высокоактивном ЦП, кроме общей утомляемости, осветления стула и потемнения мочи, может возникать тупая боль в правом подреберье и вздутие живота.
Во время осмотра часто выявляют:
- субиктеричность (желтушность) склер;
- расширение вен брюшной стенки, напоминающее голову медузы;
- венозный шум при выслушивании в эпигастральной области живота (шум Крювелье — Баумгартена);
- серо-коричневатый цвет шеи;
- гинекомастию (увеличение грудных желёз);
- гипогонадизм (у мужчин);
- контрактуру Дюпюитрена (укорочение сухожилий ладоней).
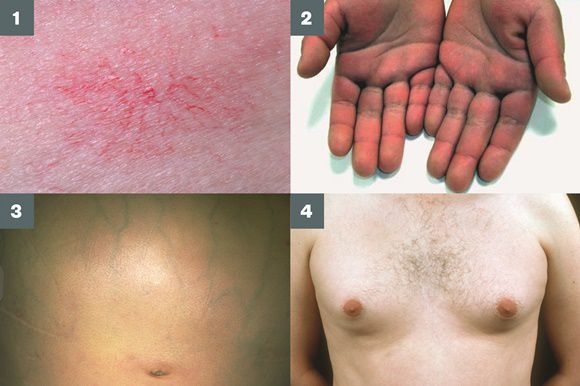
Три последних признака цирроза печени зачастую наблюдаются при алкогольных ЦП.
В области грудной клетки в 50-80% случаев наблюдаются телеангиэктазии кожи (расширения мелких сосудов), чаще при алкогольных ЦП. Пальпаторно печень отчётлива уплотнена, имеет неровный нижний край. Размеры печени различны — от значительного увеличения до уменьшения.
Часто при пальпации выявляется умеренно увеличенная селезёнка, причём её край может выступать из-под рёберной дуги на 1-3 см.
При развитии ЦП появляются симптомы белково-энергетической недостаточности, асцит, отёки, а также печёночный запах при тяжёлой печёночной недостаточности.
Симптомы при малоактивных и начальных стадиях ЦП
Данные формы ЦП зачастую протекают бессимптомно и выявляются в ходе периодических медицинских осмотров, диспансеризации, а также как случайная находка при обследовании пациента со смежной патологией или внепечёночными проявлениями.
При малоактивном ЦП, как правило, не возникают жалобы, связанные с печенью. Во время активного расспроса можно выявить весеннее снижение работоспособности, частые болезни, после которых возможны кровоточивость дёсен и потемнение мочи. Такие пациенты хуже, чем раньше, переносят длительные физические и нервно-психические нагрузки.
Желтухи и выраженного увеличения билирубина, за исключением периода интеркурентного острого гепатита, нет. Неяркая телеангиоэктазия кожи (сосудистые звёздочки) в области грудной клетки наблюдаются у 40-60% людей с ЦП.
Телеангиоэктазии кожи, плотная печень с фестончатым краем и умеренно увеличенная селезёнка — ценная клинико-диагностическая триада, которая с вероятностью 80-90% свидетельствует о ЦП или далеко зашедшем активном хроническом гепатите.
Патогенез цирроза печени
В основе патофизиологии цирроза лежит повреждение и некроз паренхимы (основной ткани) печени с деструкцией и гибелью гепатоцитов (клеток печени), а также системное поражение интерстициальной ткани.
При всех формах ЦП нарушается иммунологическое равновесие организма, преобладающими становятся аутоиммунные процессы: иммунная система человека принимает собственные клетки печени за чужеродные и повреждает их. В конечном итоге, это приводит к разрушению гепатоцитов и структуры печени в целом. Однако при этом каждая форма ЦП имеет свои патогенетические особенности:
- при вирусных гепатитах повреждающим агентом является сама вирусная частица, которая, размножаясь в клетке, разрушает её, вызывая цитолиз;
- при алкогольном ЦП прямое токсическое воздействие на мембраны гепатоцитов оказывает ацетальдегид с развитием алкогольной жировой болезни печени и алкогольного стеатогепатита;
- при метаболическом ЦП ведущую роль в патогенезе играет ожирение и сахарный диабет через стадию неалкогольного стеатогепатита с инсулинорезистентностью и последующей запрограммированной гибелью клеток печени.
В основе патогенеза более редких причин цирроза печени лежат ещё более частные механизмы развития повреждения и разрушения гепатоцитов и структуры печени:
- нарушение обмена и накопления железа при гемохроматозе;
- накопление меди при болезни Вильсона — Коновалова;
- окклюзия в системе воротной вены при гепатопортальном склерозе.
Цирроз формируется на протяжении многих лет. С течением времени происходят изменения генетического аппарата клеток печени, в результате чего появляются новые патологические клетки. Этот процесс в печени является иммуновоспалительным, он поддерживается чужеродными агентами, в роли которых могут выступать разные субстраты:
- вирус гепатита В;
- алкогольный гиалин;
- денатурированные белки;
- некоторые лекарственные средства;
- медьбелковые и железобелковые комплексы (ферритин).
В итоге повреждения паренхимы печени развивается гепатоцеллюлярная (печёночно-клеточная) недостаточность за счёт диффузного фиброза и трансформации ткани печени в анормальные узлы-регенераты. [3] [4] [5]
Классификация и стадии развития цирроза печени
В 1974 году на съезде гепатологов в Акапулько (Мексика) была принята единая морфологическая классификация, которую позже уточнили и несколько доработали эксперты ВОЗ. В настоящее время она является общепринятой.
Читайте также:

