Стероидная атрофия кожи что это
Обновлено: 19.04.2024
Московский научно-практический центр наркологии
Главный военный клинический госпиталь ФСБ России, Голицыно
Главный военный клинический госпиталь ФСБ России, Голицыно
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2012;112(10‑2): 60‑64
Полунина А.Г., Исаев Ф.В., Демьянова М.А. Стероидная миопатия. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2012;112(10‑2):60‑64.
Polunina AG, Isaev FV, Dem'ianova MA. Steroid-induced myopathy. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2012;112(10‑2):60‑64. (In Russ.).
Московский научно-практический центр наркологии
Физиологические эффекты глюкокортикоидов (ГК) включают подавление синтеза и усиление катаболизма белков в мышечных волокнах. Длительный прием высоких доз этих препаратов приводит к миопатии. Миопатические эффекты ГК проявляются как при системном, так и при ингалляционном пути введения. Наиболее часто стероидная миопатия проявляется слабостью и гипотрофией мышц ног, слабостью дыхательной мускулатуры, дисфонией. Профилактика и лечение стероидной миопатии включают сужение показаний к длительному лечению ГК, альтернирующие режимы приема данных препаратов, адекватные физические нагрузки. Существуют данные об эффективности витамина D и смесей аминокислот как метода профилактики и лечения стероидной миопатии.
Московский научно-практический центр наркологии
Главный военный клинический госпиталь ФСБ России, Голицыно
Главный военный клинический госпиталь ФСБ России, Голицыно
О неблагоприятном влиянии глюкокортикоидов (ГК) на мышечную силу и трофику мышц известно с самого начала активного использования препаратов данной группы в медицинской практике [17]. Тем не менее практические врачи до сих пор мало осведомлены о миопатических эффектах ГК.
В действительности, стероидная миопатия является одной из частых причин нарушений ходьбы у пожилых людей [1]. Миопатия усугубляет дыхательные нарушения при лечении кортикостероидами пациентов с бронхиальной астмой [2, 3, 6, 24, 40]. Длительное использование ингаляционных ГК сопряжено с развитием дисфонии в связи с формированием миопатических изменений в мышцах гортани [32]. Наконец, стероидная миопатия является причиной части случаев «миопатии критических состояний» [31]. Таким образом, стероидная миопатия является важной медицинской проблемой, требующей углубленного изучения.
Патогенетические механизмы
Физиологической функцией кортикостероидных гормонов является мобилизация ресурсов организма в условиях стресса. В стрессовых ситуациях уровень кортизола в крови повышается, а по окончании кратковременного стресса - нормализуется в течение 1-1,5 ч [23]. Важным кратковременным эффектом кортикостероидов является повышение мышечной силы [26]. В недавно опубликованном исследовании M. Minetto и соавт. [26] было показано, что введение дексаметазона (8 мг внутрь) здоровым молодым мужчинам в течение 1 нед приводит к увеличению силы мышц конечностей на 8,5%. Однако повышение «работоспособности» мышц в данном исследовании происходило на фоне снижения уровня сывороточной креатинфосфокиназы (КФК) на 50% и миоглобина на 42%, а также снижения скорости проведения по мышечному волокну на 6-10% по сравнению с периодом до исследования. Таким образом, уже через 1 нед после ежедневного приема дексаметазона исследователи наблюдали признаки снижения возбудимости сарколеммы и изменения мышечного метаболизма.
Мобилизация ресурсов организма осуществляется кортикостероидами за счет торможения гомеостатических процессов. ГК снижают скорость синтеза и усиливают процессы распада мышечных белков, что и приводит к атрофии мышц [34]. ГК подавляют транспорт аминокислот в мышцы, блокируют стимулирующие эффекты инсулина, инсулиноподобного фактора роста и аминокислот на синтез белков, подавляют миогенез за счет угнетения синтеза миогенина. Кроме того, ГК тормозят продукцию факторов роста, контролирующих на локальном уровне увеличение массы мышцы. Угнетение пролиферации и дифференциации мышц под воздействием ГК происходит вследствие увеличения продукции в мышцах миостатина. O. Schakman и соавт. [34] рассматривают стимулирующее действие ГК на продукцию миостатина как ведущий патогенетический механизм стероидной миопатии.
Даже при отсутствии клинически выраженных симптомов миопатии у пациентов, длительно получающих ГК в низких дозах, гистологические исследования выявляют увеличение концентрации гликогена в мышечных волокнах [14]. Накопление гликогена сочетается с угнетением активности основных регуляторных ферментов, контролирующих процессы деградации гликогена на фоне хронического воздействия ГК.
В целом ряде исследований было показано, что различные группы мышц имеют разную чувствительность к неблагоприятным эффектам кортикостероидов. При этом чаще всего атрофические изменения развиваются в мышцах, содержащих большое количество быстро сокращающихся волокон (волокон 2-го типа) [34]. В частности, большеберцовая мышца или разгибатели пальцев в большей степени подвержены гипотрофии при стероидной миопатии по сравнению с камбаловидной мышцей. Данные различия обусловлены минимальным содержанием волокон 2-го типа в камбаловидной мышце. В экспериментальном исследовании R. Gruener и L. Stern [18] неблагоприятное влияние дексаметазона на возбудимость мышечной мембраны у мышей также было отмечено только в мышце - длинном разгибателе пальцев при отсутствии каких-либо изменений в камбаловидной мышце. В исследовании M. Minetto и соавт. [26] после недельного приема дексаметазона здоровыми испытуемыми скорость проведения по мышечным волокнам снизилась в наибольшей степени (на 10,5%) в двуглавой мышце плеча, чуть в меньшей степени - в широкой медиальной мышце (на 10%), еще меньше - в широкой латеральной мышце (на 9%) и в наименьшей степени - в передней большеберцовой мышце (на 6%). Данная тенденция соответствует распределению волокон 2-го типа в перечисленных мышцах: 60% волокон 2-го типа содержит бицепс, 50% - широкие мышцы бедра и 30% - передняя большеберцовая мышца.
Таким образом, физиологические эффекты кортикостероидов сопряжены с угнетением нормальных гомеостатических процессов в мышечных волокнах. Соответственно, хроническое или массированное воздействие ГК облигатно приводит к дисфункции мышц с тенденцией к атрофическим изменениям в мышечных структурах.
Клинические проявления и диагностические подходы
Как клинические наблюдения, так и экспериментальные исследования на животных однозначно свидетельствуют, что высокие дозы кортикостероидов вызывают снижение мышечной массы, тонуса и силы в мышцах [34]. Подобные эффекты характерны как для случаев лечения экзогенными ГК, так и для синдрома Кушинга.
Острые формы стероидной миопатии манифестируют слабостью в проксимальной мускулатуре конечностей, миалгиями с сопутствующим повышением сывороточной КФК и креатина в суточной моче [16, 21]. У подавляющего большинства таких пациентов острое повреждение мышц развивается при повышении дозы ГК на фоне их длительного приема. Тем не менее описаны казуистические случаи острой стероидной миопатии после однократного приема ГК внутрь в относительно небольших дозах (20-24 мг метилпреднизолона) [21].
Тяжелые формы острой стероидной миопатии у пациентов с астматическим статусом могут сопровождаться рабдомиолизом с повышением уровня сывороточной КФК, миоглобинурией и развитием острой почечной недостаточности [17, 24]. В типичных случаях рабдомиолиз развивается после использования массированных доз ГК в сочетании с миорелаксантами или другими препаратами с миотоксическим эффектом (аминогликозиды и т.д.). Считается, что наиболее выраженные повреждения при острой миопатии развиваются в четырехглавых мышцах бедра [16]. Однако рабдомиолиз может затрагивать и дыхательную мускулатуру в связи с выраженной нагрузкой на данную группу мышц при астматическом статусе [37].
Стероидная миопатия может лежать в основе части случаев «резистентной» астмы [38]. В такой ситуации слабость дыхательной мускулатуры усугубляет дыхательные нарушения, при этом эффект ингаляционных ГК минимизируется в связи с неадекватным распределением препарата в дыхательных путях. Снижение дозы ГК с переходом на системные нестероидные препараты нормализует состояние таких больных. Следует подчеркнуть, что умеренно выраженная слабость дыхательной мускулатуры типична для пациентов с бронхиальной астмой, получающих ГК как системно, так и в виде ингаляций [6]. В более тяжелых случаях максимальное давление на вдохе и выдохе (PImax и PEmax) может составлять менее 40 или 50% от нормы соответственно [9]. По наблюдению M. Decramer и K. Stas [9], снижение дозы кортикостероидов в течение 3 мес приводит к улучшению дыхательных функций в виде увеличения PImax до 74% и PEmax до 92%. Следует отметить, что в экспериментах на животных была продемонстирована способность ГК индуцировать атрофические изменения в диафрагме [10]. Описаны также случаи разрыва диафрагмы на фоне обострения бронхиальной астмы и интенсивного кашля с вклинением органов брюшной полости в грудную клетку [19].
Слабость мышц ног также является частой жалобой пациентов, получающих кортикостероиды в течение длительного времени. В обследованной нами когорте пульмонологических больных (35 человек), ни один из 15 пациентов, ежедневно получавших преднизолон или ингаляционные кортикостероиды менее 8 мес, не отметил возникновения слабости в ногах при обычной ходьбе или подъеме/спуске по лестнице. В то же время 13 из 20 (65%) пациентов, получавших кортикостероиды в течение года и более длительных периодов, отметили ощущение слабости в ногах при ходьбе по плоской и/или наклонной поверхности. Многие больные указывали на выраженное ухудшение двигательных функций в периоды обострения заболевания и связанного с ним резкого увеличения дозы кортикостероидов. Следует отметить, что для пациентов, длительно получавших ГК по поводу бронхиальной астмы, но не отметивших каких-либо ощущений слабости в ногах при ходьбе, была характерна выраженная дыхательная недостаточность, ограничивавшая двигательную активность больных.
По наблюдениям M. Decramer и K. Stas [9], в случаях выраженной стероидной миопатии сила четырехглавой мышцы бедра может снижаться на 16-46%. Уменьшение дозы ГК приводило к более медленному увеличению силы в мышцах ног по сравнению с дыхательной мускулатурой. Так, через полгода после уменьшения дозы кортикостероидов сила в четырехглавой мышце бедра варьировала в пределах от 31 до 85% от нормы [27].
Целый ряд исследований посвящен функции гортанных мышц у пациентов с бронхиальной астмой, регулярно использующих ингаляторные кортикостероиды [22, 32, 35]. У таких пациентов частыми являются жалобы на дисфонию и быструю утомляемость мышц гортани в процессе речи. По данным электромиографического исследования A. Ozbilen и соавт. [32], у таких больных в наибольшей степени страдает крикотиреоидная мышца и в меньшей степени - тиреоаритеноидная мышца.
Для хронических форм стероидной миопатии характерно снижение уровня КФК и миоглобина в сыворотке крови. Так, в исследовании M. Minetto и соавт. [26] данные показатели снижались вдвое уже через 1 нед ежедневного введения дексаметазона здоровым испытуемым. Эта же исследовательская группа выявила снижение уровня КФК на 49% и снижение миоглобина на 21% у пациентов с болезнью Кушинга по сравнению с возрастной нормой [27]. Тем не менее даже при выраженных двигательных или дыхательных нарушениях уровень КФК при стероидной миопатии может оставаться нормальным [9]. Поэтому уровень креатина в суточной моче может быть более надежным маркером стероидной миопатии [11].
В подавляющем большинстве случаев стероидной миопатии у пациентов с бронхиальной астмой выявляются электрофизиологические признаки миопатии в отсутствие каких-либо изменений, характерных для нарушений нервно-мышечной передачи или полиневропатии [8, 11, 29].
Эпидемиология
Систематических исследований заболеваемости стероидной миопатией не проводилось. Относительно тяжелые формы стероидной миопатии регистрируются у 10-14% пациентов с астматическим статусом, потребовавшим искусственной вентиляции легких 6. Следует подчеркнуть, что большинство таких пациентов получали длительную терапию ингаляторными кортикостероидами в период, предшествующий декомпенсации состояния.
В поликлинической практике у 6% пожилых пациентов, требующих консультации невролога на дому в связи с подостро возникшей неспособностью ходить, можно выявить гипотрофию и слабость мышц ног вследствие хронического использования ингаляторных кортикостероидов [1, 7]. V. Mak и соавт. [25] выявили слабость четырехглавых мышц бедра у 21% пациентов с бронхиальной астмой, регулярно получавших ГК. При тщательном расспросе жалобы на регулярное ощущение слабости в ногах высказывают 65% пациентов, употребляющих кортикостероиды более 1 года. По данным A. Sinkiewicz и соавт. [35], эпизоды дисфонии отмечают до 70% пациентов с бронхиальной астмой, длительно получающих ингаляторные кортикостероиды.
Факторы риска
Длительность приема и высокие дозы ГК являются основными факторами риска развития тяжелой стероидной миопатии [16]. В нашем исследовании мы наблюдали клинические проявления стероидной миопатии только у пациентов, ежедневно использовавших ингаляционные кортикостероиды в течение как минимум 1 года.
Регулярность приема ГК также имеет существенное значение. В течение периодов лекарственных «каникул» мышечный метаболизм успевает нормализоваться, и стероидная миопатия не формируется.
Ингаляционные и системные ГК. Принято считать, что ингаляционные ГК существенно превосходят по безопасности системные ГК. Тем не менее, по данным A. Borba и соавт. [6], умеренные проявления стероидной миопатии выражены одинаково как у пациентов, получающих ГК системно, так и при использовании ингаляционных стероидов. Сходные данные продемонстрированы V. Mak и соавт. [25]. Хотя в аналогичном исследовании O. Akkoca и соавт. [2] у пациентов с бронхиальной астмой, получавших преднизолон, сила дыхательной мускулатуры была ниже по сравнению с пациентами, получавшими только ингаляции беклазона, показатели последних были ниже по сравнению со здоровыми из контрольной группы. Соответственно, результаты данного исследования указывают на дозозависимость миопатического эффекта ГК вне зависимости от пути введения препарата [9]. После отмены ГК функции мышц постепенно восстанавливались.
Пожилой возраст. В пожилом возрасте умеренно выраженная атрофия волокон 2-го типа и саркопения развиваются и в отсутствие каких-либо дополнительных миопатогенных факторов [26]. Соответственно, клинические проявления стероидной миопатии развиваются чаще у пожилых [34]. В нашей практике мы также наиболее часто наблюдаем клинические формы хронической стероидной миопатии у пациентов старше 70 лет.
Масса тела. Системные побочные эффекты ГК, по-видимому, в большей степени выражены у пациентов с небольшой массой тела. У очень тучных больных даже многолетний прием ГК может не сопровождаться ни ощущениями слабости в ногах, ни изменением объема мышц. Данная тенденция логична, поскольку в этих случаях попадающие в кровоток кортикостероиды распределяются в тканях организма в существенно меньших концентрациях. Тем не менее тучные пациенты не избавлены от таких локальных эффектов кортикостероидов, как кандидоз дыхательных путей и пищевода, дисфония и т.д.
Дыхательная недостаточность. Слабость дыхательной мускулатуры и мышц конечностей регулярно выявляется у пациентов с хронической дыхательной недостаточностью на фоне хронической обструктивной болезни легких [13, 28].
Миорелаксанты. По данным N. Behbehani и соавт. [5], использование миорелаксантов в дополнение к стероидной терапии на фоне астматического статуса является фактором риска развития тяжелой стероидной миопатии. Исследователи выявили миопатию у 30% пациентов, получавших миорелаксанты в процессе искусственной вентиляции легких. У пациентов, не получавших миорелаксанты, симптомы миопатии не наблюдались. Каждый дополнительный день миорелаксации повышал вероятность развития клинически выраженной миопатии в 2 раза.
В то же время, по данным ретроспективного исследования S. Kesler и соавт. [20], несмотря на 10-кратное снижение продолжительности миорелаксации после 1995 г. достоверного снижения заболеваемости тяжелой стероидной миопатией после астматического статуса не произошло.
Профилактика
Практические врачи должны осознавать опасность длительных курсов пероральных или парентеральных кортикостероидов и прибегать к назначению гормональной терапии только тогда, когда потенциальный лечебный эффект ГК превышает опасность развития тяжелых астматических статусов.
Лечение и прогноз
Снижение дозы или отмена ГК. Отмена кортикостероидов приводит к улучшению как двигательных функций, так и электрофизиологической картины [8, 9]. По данным W. David и соавт. [8], у пациентов с тяжелой стероидной миопатией после астматического статуса двигательные функции восстанавливаются до степени функциональной независимости в течение 1-го месяца после отмены стероидов.
Регулярная физическая активность. Данные ряда исследователей свидетельствуют, что регулярная физическая активность способна снижать миопатические эффекты кортикостероидов. Так, в экспериментальном исследовании C. Pinheiro и соавт. [33] показано, что интенсивная физическая активность (бег в течение 1 ч с периодичностью 3 раза в неделю) предотвращает гипотрофию мышц у животных, ежедневно получающих дексаметазон в течение 1 мес.
Витамин D. В целом ряде исследований были продемонстрированы достоверные корреляции между уровнем витамина D и функциональными возможностями мышц [36]. Описаны многочисленные случаи клинически выраженной миопатии, регрессирующей на фоне интенсивного лечения с использованием витамина D, в религиозных популяциях, склонных к ношению закрытой одежды в любое время года и употреблению пищи с низким содержанием животных жиров [4]. По данным исследования L. Forli и соавт. [15], более половины пульмонологических пациентов имеют дефицит витамина D (
По данным экспериментального исследования N. Miyakoshi и соавт. [30], витамин D способен предотвращать стероидную миопатию. Авторы не выявили межгрупповых различий в силе и объеме мышц между животными, получавшими преднизолон совместно с витамином D, и контрольной группой.
В то же время у животных, получавших преднизолон в течение 1 мес, были выявлены закономерные гипотрофия и снижение силы в мышцах по сравнению с контрольной группой.
Аминокислоты. Прием смесей аминокислот усиливает синтез протеинов в мышцах и снижает неблагоприятные катаболические эффекты кортикостероидов [34, 39]. По-видимому, наибольший благоприятный эффект на мышечный протеиновый синтез оказывают лейцин и глутамин.
Перспективными направлениями для дальнейших исследований профилактики и лечения стероидной миопатии могут быть: 1) стимуляция продукции факторов роста (IGF-I); 2) ингибирование продукции миостатина; 3) применение таурина, креатина и кленбутерола, способных предотвращать стероидную миопатию in vitro; 4) назначение андрогенов, способных увеличивать мышечную массу за счет стимуляции мышечных факторов роста [34].
Атрофодермия – вариант атрофии кожи, включающий в себя ряд заболеваний, в основе которых лежат дегенеративно-атрофические процессы в эпидермисе и дерме. Заболевание обладает тенденцией к затяжному течению, не имеет гендерной составляющей, внесезонное. Клиника каждой патологии, входящей в группу атрофодермии, специфична; общей чертой является образование на кожных покровах атрофических очагов. В диагностике решающее значение принадлежит гистологическому исследованию биоптата кожи. Лечение симптоматическое (витаминотерапия, физио- и бальнеотерапия), прогноз благоприятный. В течении атрофодермии есть онкологический вектор.
Общие сведения
Атрофодермия – несколько редко встречающихся хронических патологий, имеющих в своей основе комплекс дистрофических изменений кожи, занимающих промежуточное положение между классической атрофией кожи и классической склеродермией. Они могут быть врождёнными и приобретёнными, симптоматическими или выступать в качестве самостоятельного заболевания. Причины и механизм развития атрофодермии являются предметом исследования дерматологии на протяжении столетия, но до конца не выяснены и сегодня. Например, червеобразная атрофодермия была описана в конце XIX столетия при изучении фолликулярного кератоза бровей (надбровной эритемы Унна), как исход этого заболевания. Сетчатая атрофодермия известна под названием пойкилодермии Якоби с 1906 года (сетчатая эритематозная атрофодермия Мюллера, эритематозно-атрофическая пойкилодермия Милиана—Перена, атрофический дерматит Глюка, синдром Томсона, синдром Ротмунда). Ограниченная атрофодермия Пазини-Пьерини впервые описана в 1875 году, а невротическая атрофодермия - в 1864 английским хирургом Педжетом.
Клиническая картина атрофодермии в каждом отдельном случае имеет свои особенности. Поскольку точно этиология заболевания не установлена, лечение симптоматическое. Актуальность связана с возможностью перерождения пойкилодермического процесса в злокачественное новообразование.

Причины атрофодермии
Атрофодермия возникает из-за нарушения питания всех слоёв кожи в результате точно не установленных причин. Дерматологи считают, что в основе сетчатой атрофодермии (пойкилодермии) лежат сосудистые расстройства - запустевание, сужение просвета сосудов, питающих кожу - нейроэндокринного или инфекционно-токсического характера (радиационное облучение, УФО, системные дерматозы).
Червеобразная атрофодермия появляется вследствие изменения трофики кожи, деструкции её желёз из-за эндокринно-вегетативных расстройств (нарушение синтеза витамина А, сахарный диабет). Нейротическая атрофодермия – результат нарушений в центральной и периферической нервной системах, приводящих к расстройству обменных процессов (полиневриты, повреждение нерва). Ограниченная атрофодермия Пазини-Пьерини имеет в своей основе сочетание всех вышеперечисленных причин на фоне резкого ослабления общего и местного иммунитета.
Классификация атрофодермии
Классификация атрофодермии – это, скорее, количественная расшифровка заболеваний, входящих в её группу. Различают:
- Атрофодермия червеобразная – заболевание молодых, основным элементом является симметрично расположенная на щеках фолликулярная пробка с исходом в мелкий атрофический рубчик. Такая сетчатая «изъеденность» кожи напоминает кору дерева или медовые соты.
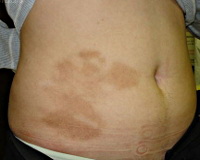
- Атрофодермия идиопатическая Пазини-Пьерини – редкое заболевание, поражает преимущественно молодых женщин. Локализуется на туловище. Первичный элемент - овальное пятно, западающее в центре, которое трансформируется в бляшку, а затем в ограниченный очаг атрофии.
- Атрофодермия невротическая – поражается кожа конечностей, нарушается трофика тканей с появлением очагов атрофо-дистрофии, истончением ногтей и выпадением волос.
- Атрофодермия сетчатая (пойкилодермия) – заболевание вне возраста и пола. Локализуется чаще всего на открытых участках кожи в виде эритемы с исходом в пигментированный очаг атрофии.
Симптомы атрофодермии
Клиника атрофодермии индивидуальна для каждого заболевания, входящего в группу этой патологии. Червеобразная атрофодермия имеет самую характерную клиническую картину: у молодых людей на щеках появляются симметрично расположенные мелкие (1-3 мм), западающие дефекты кожи причудливых очертаний глубиной до 1 мм. Это – деформированные фолликулы, заполненные, как правило, сальными пробками. Они сливаются, образуют пересекающиеся «волны», «линии», «ячейки», которые, вместе с участками нормальной кожи между ними напоминают рисунок коры дерева, изъеденной червяками, или медовых сот. С возрастом симптомы сглаживаются.
Клиника идиопатической формы напоминает ограниченный очаг поверхностной склеродермии, он вдавлен в окружающую здоровую кожу, небольшого размера (до 2 см), овальной формы, мягкий при пальпации, телесного цвета, единичный или множественный, имеет тенденцию к слиянию с образованием фестончатых форм. Располагается на животе или спине.
Невротическая форма характеризуется поражением пальцев рук и ног: кожа лоснится, напряжена, кажется, что при сгибании кисти или стопы она «лопнет», кожные покровы приобретают синюшный оттенок, как при акроцианозе, из-за недостаточного капиллярного кровоснабжения. Со временем, питание данного участка кожи практически прекращается, она становится мертвенно-бледной, истончается, в очаге атрофии наблюдаются прозрачные ногтевые пластинки и выпадение волос.
Пойкилодермия, или сетчатая атрофодермия, располагается на открытых участках кожи, в зоне декольте. Визуально выглядит, как пятнистая поверхность кожи из-за чередования атрофических, пигментированных пятен с депигментированными. Возможна трансформация в меланодермию, грибовидный микоз.
Диагностика и лечение атрофодермии
Диагностируется атрофодермия на основании клинических проявлений и результатов гистологических исследований. Потоморфологическая картина каждой патологии индивидуальна. Дифференцируют заболевание с парапсориазом, склеродермией, дерматмиозитом, лучевыми дерматитами, грибовидным микозом, меланозом, кератозом Сименса, синдромом Базекса, надбровной ульэритемой, ветрянкой, вульгарными угрями. Основа дифференциальной диагностики - клиника в сочетании с результатами биопсии кожи.
Лечение заключается в санации очагов хронической инфекции, в первую очередь, туберкулёза, сифилиса. Необходима эффективная терапия длительно существующих соматических заболеваний (сахарный диабет, заболевания щитовидной и паращитовидной железы, ревматизм, ожирение). Симптоматически применяют витаминотерапию (витамин А, наружно и внутрь, поливитамины), средства, улучшающие трофику тканей (декспантенол), препараты железа, диазепам. Эффективны тепловые процедуры, дермабразия, ванны с отрубями, морские, радоновые ванны; грязелечение (Крым, Нафталан), массаж и занятия физкультурой для улучшения питания кожи.
Профилактика атрофодермии заключается в приоритете здорового образа жизни. Прогноз благоприятен для жизни. При пойкилодермии необходимо обязательное наблюдение у дерматолога из-за возможности перерождения в ретикулосаркоматоз.
Атрофический дерматит - это процесс, при котором участки кожного покрова становятся тоньше. Кожа может истончаться вследствие различных обстоятельств. На некоторых частях тела кожа тоньше, чем на других по естественным причинам. Так, ее толщина на на веках составляет 0,5 мм, тогда как на лодыжке это 4 мм. Кожа состоит из трех слоёв, каждый из которых выполняет свои функции.
- Гиподермис - самый внутренний слой, его структурный компонент - жировая ткань. В нем залегают потовые железы,
- Дерма - средний слой, содержит нервы и кровеносные сосуды. Именно здесь развивается реакция воспаления при дерматитах,
- Эпидермис, самый внешний слой, защищает организм от грязи, бактерий и негативного влияния окружающей среды.
При атрофии кожи истончение происходит во всех слоях, но наиболее выражено в наружном.
Атрофический дерматит 9 фото с описанием
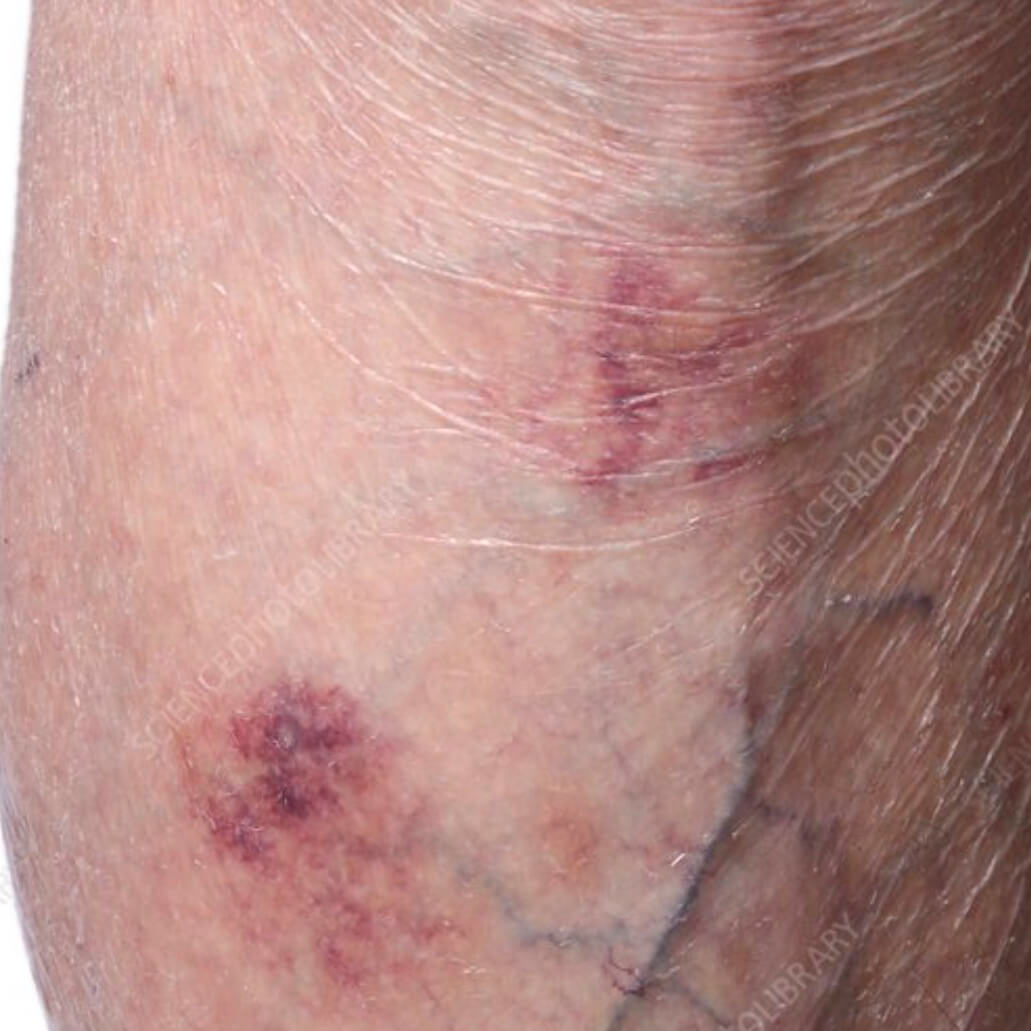
Атрофический дерматит на голени
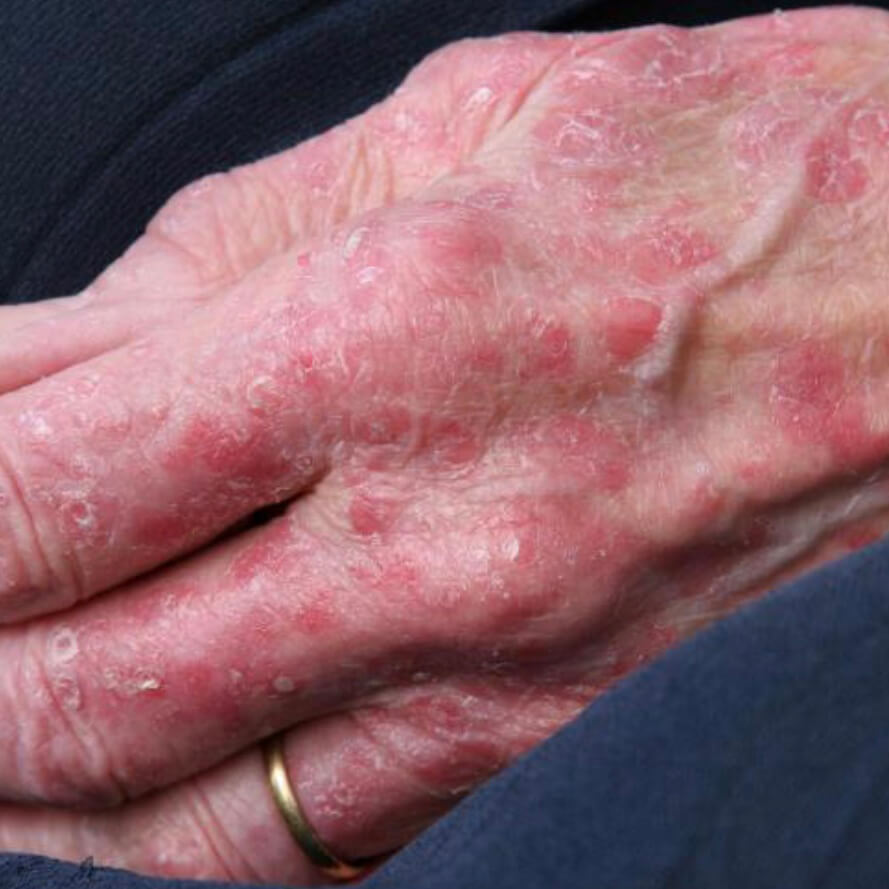
Атрофический дерматит - старение
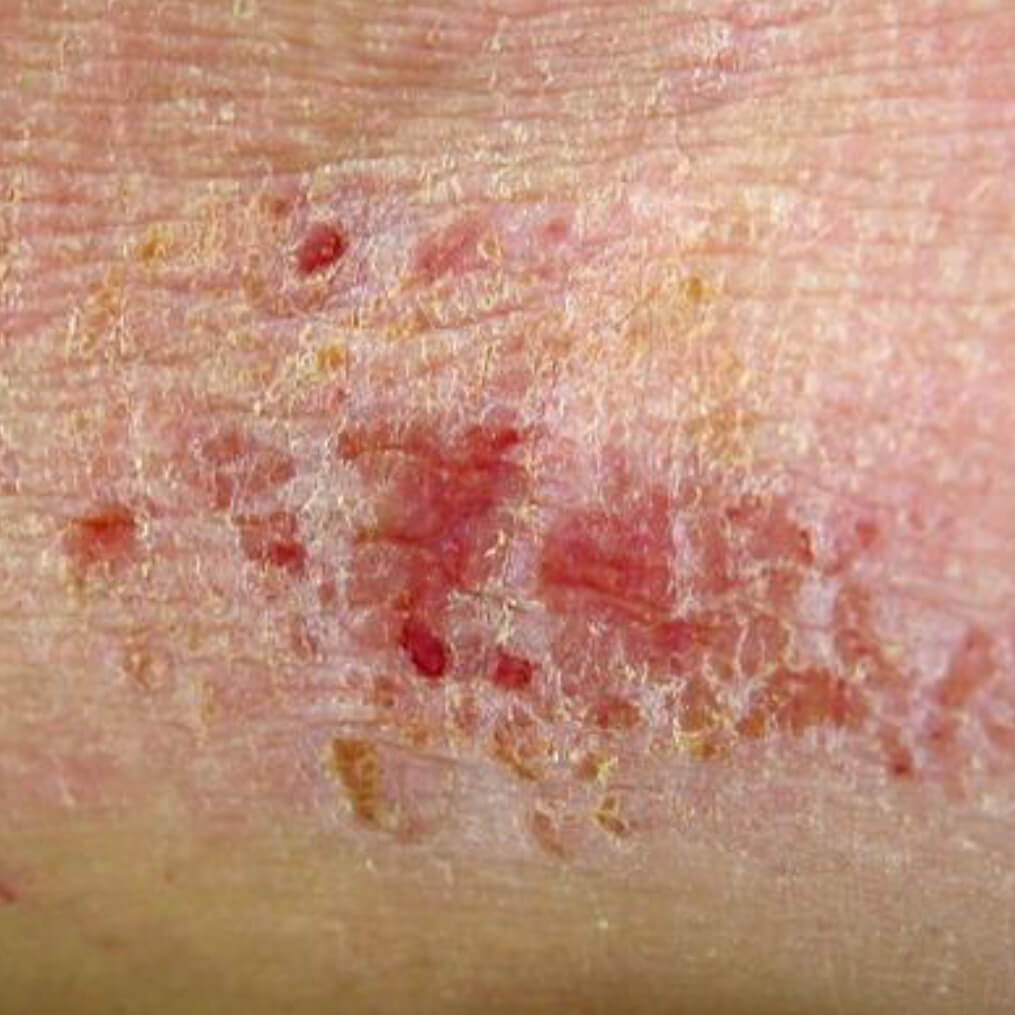
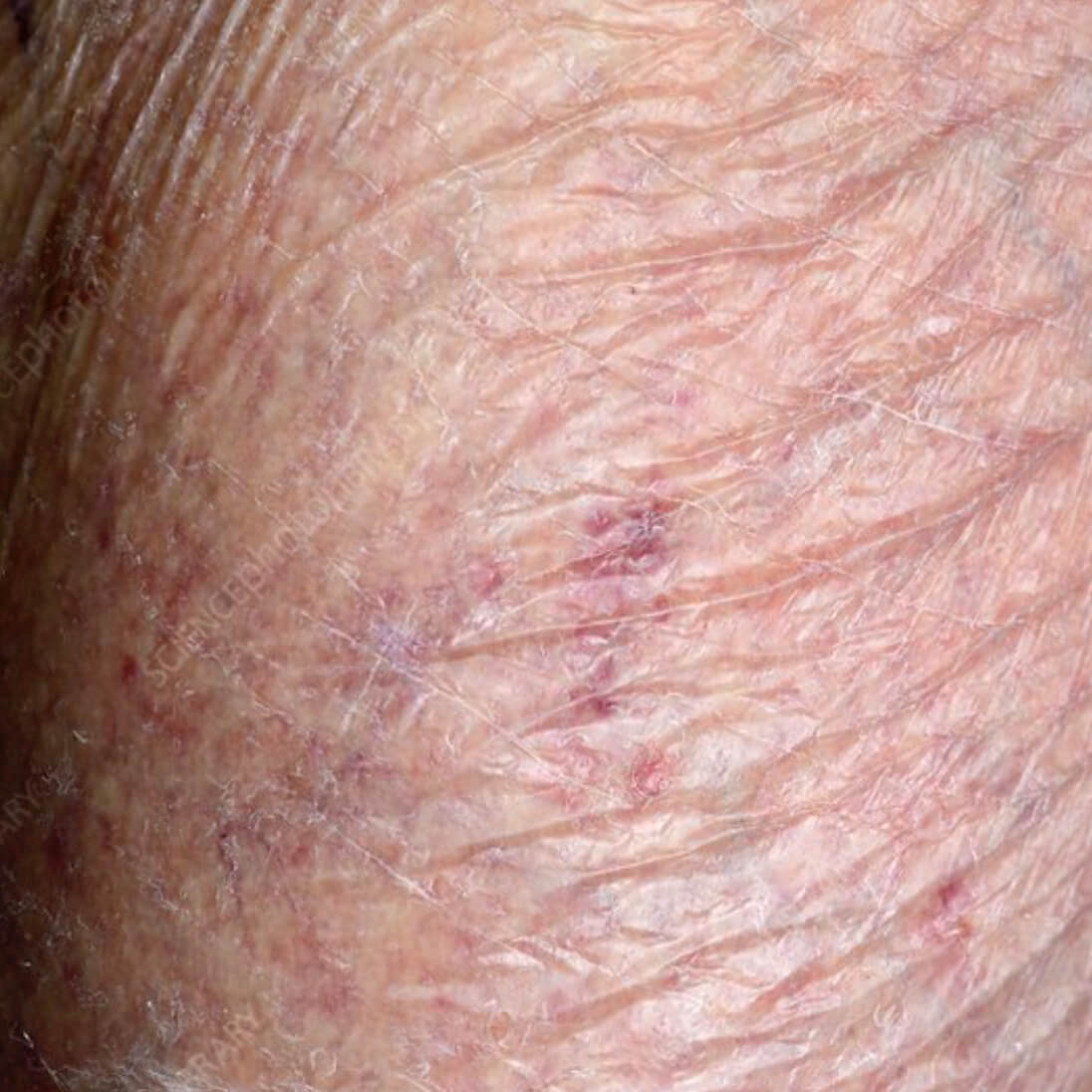
Атрофия от воздеийствия солнца
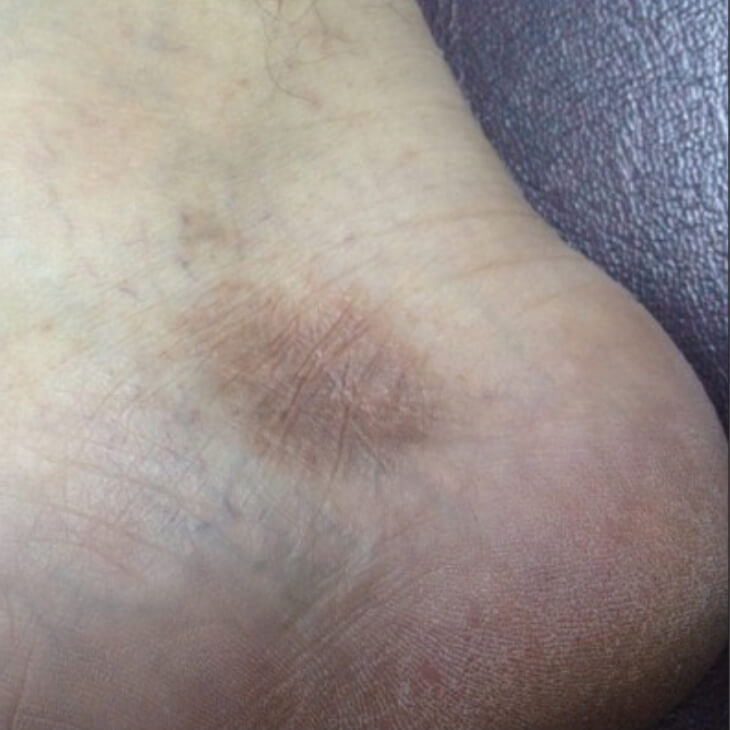
Атрофия от гормонального крема
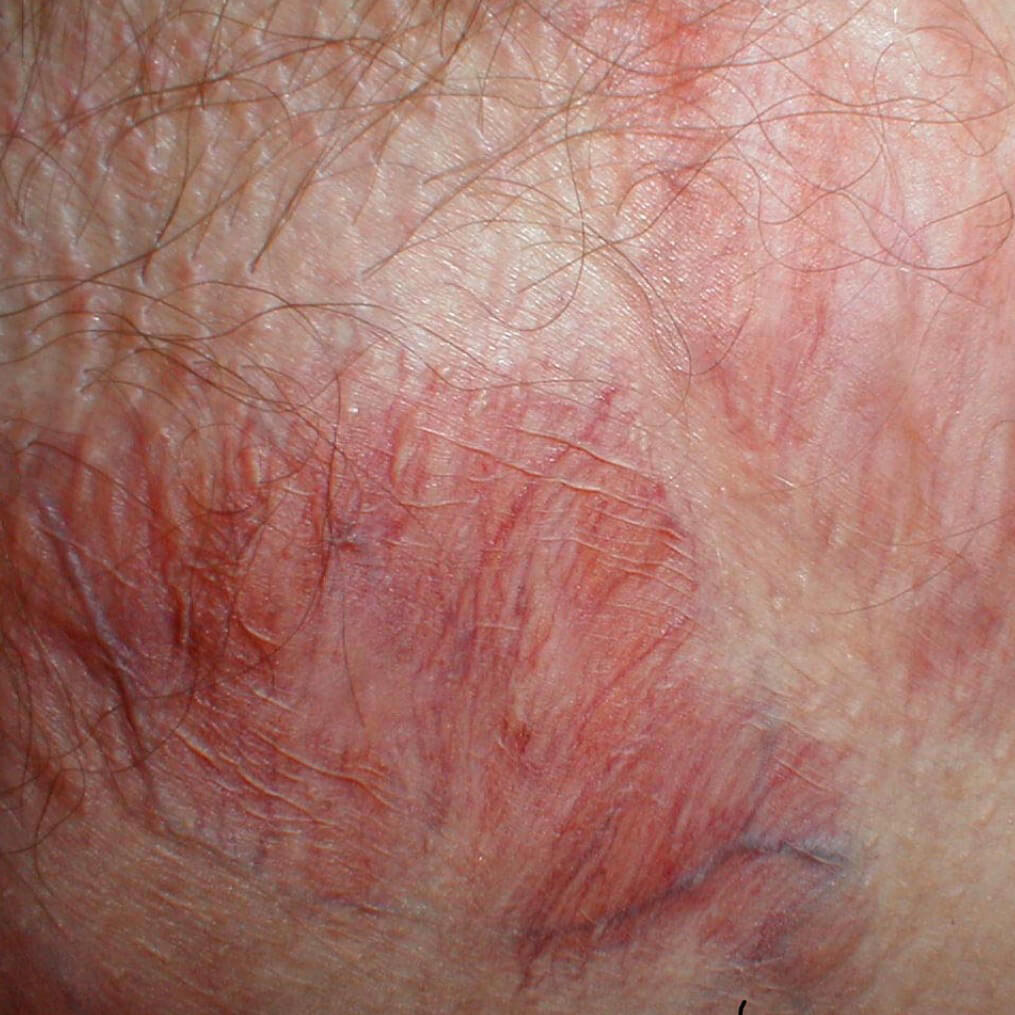
Истончение кожи от стероидов
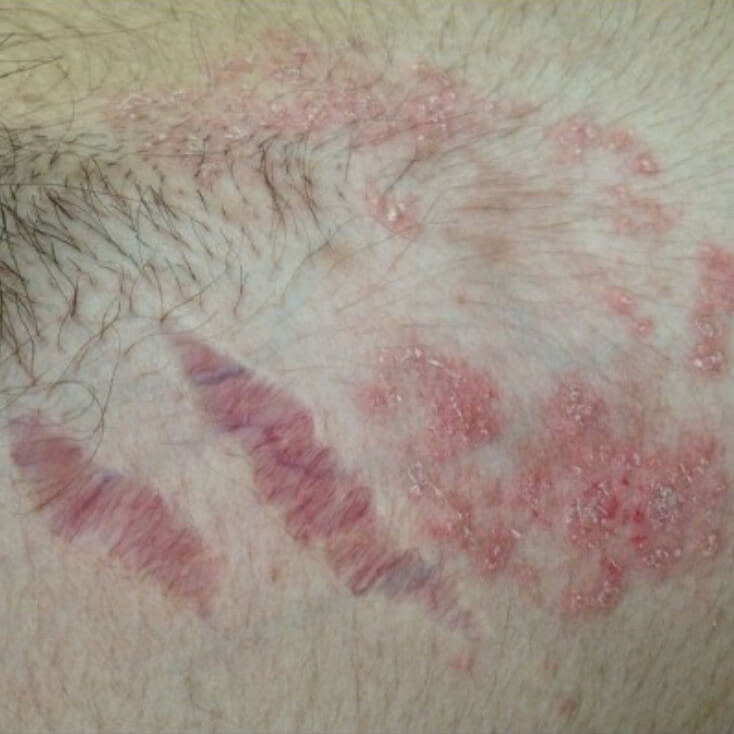
Красные стрии от стероидов
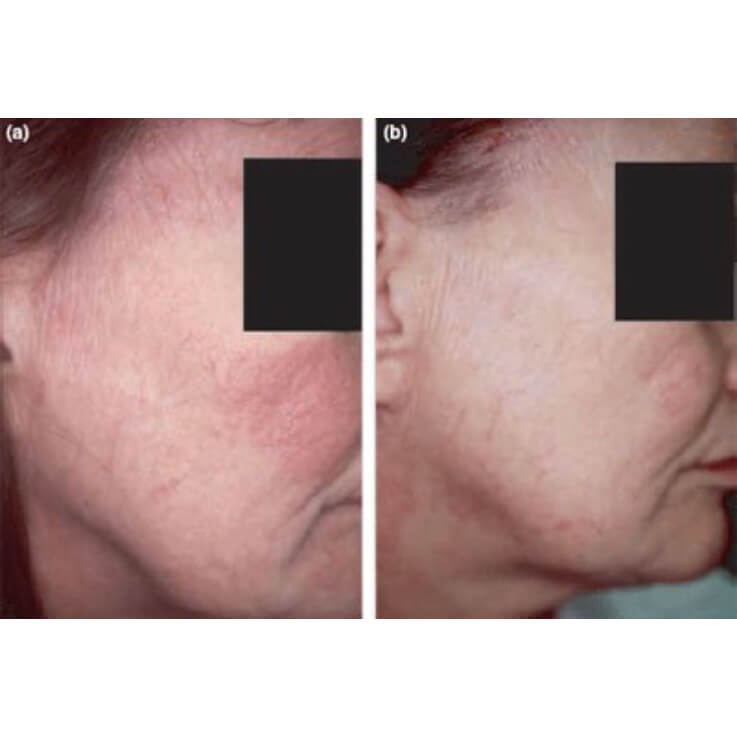
Результат лечения атрофического дерматита

Стрии от местного применения стероидов
Причины атрофического дерматита
К основным причинам атрофии относят:
- Старение - самая частая причина естественной атрофии покровов тела, это проявляется появлением морщин, потерей эластичности, сухостью и склонностью к травмам,
- Солнечный свет может приводить к атрофии. UVA и UVB лучи повреждают клетки кожи,
- Алкоголь и курение ускоряют процессы старения и приводят к истончению,
- Стероидные кремы и мази вызывают уменьшение в размерах клеток эпителия и ослабляют связи между ними.
Основной причиной атрофического дерматита является побочное действие мазей и кремов, содержащих гормоны глюкокортикостероиды. Такой эффект можно объяснить тем, что замедляется деление клеток, и разрушаются структурные белки кожи. Препараты коры надпочечников очень широко используются в дерматологии, их применяют для лечения многих патологических процессов, таких как атопический и контактный дерматит, экзема, аллергии, псориаз, а также как вспомогательные средства в терапии кожных проявлений системных заболеваний, красный волчанки, нейродермита, ревматоидного артрита.
Более слабые препараты находятся в свободной продаже, и пациенты с любой кожной проблемой могут приобрести их в аптеке и лечатся ими без контроля врача длительно. Более мощные мази, назначаемые доктором, вызывают атрофические изменения уже после двух - трёх недель использования. Наиболее сильные средства способны привести к истончению дермы после трех дней. Положительный эффект от стероидных гормонов может сводиться на нет этим побочным действием, так как значительно снижается барьерная роль эпидермиса, что приводит к большой потере жидкости, раздражению и симптомам сухой экземы.
Симптомы атрофического дерматита
Общая атрофия кожи включает в себя истончение наружного слоя - эпидермиса, а также основного слоя - дермы, уменьшение количества сальных желёз, атрофию подкожной жировой клетчатки и подлежащего мышечного слоя.
- Структурные изменения кожи, видимые невооруженным глазом: атрофированный участок выглядит сморщенным, истонченным, похож на папиросную бумагу,
- Для атрофического дерматита характерна выраженная сухость покровов,
- Пациент может ощущать жжение и покалывание, которое затем проходит вследствие спазма сосудов,
- Телеангиэктазия - это образование сосудистых звездочек в месте применения гормонов. Появление такого эффекта объясняется выработкой под влиянием глюкокортикоидов нитрита азота, который влияет на стенку сосуда, приводя к ее перерастягиванию.
- Стероидные угри, или акне, как предполагается, появляются, когда кожа вокруг волосяных фолликулов атрофируется, а также вследствие снижения местного иммунитета. К такому побочному явлению более предрасположены молодые люди, локализация преимущественно на лице и верхней части спины,
- Стероидная розацеа (розовые угри) развивается, так как стероиды стимулируют размножение микроорганизмов Propionobacterium acne и Dermodex folliculorum, которые вызывают это состояние кожи,
- Вызванная стероидами деградация белков кожи ведет к потере межклеточной субстанции. Поэтому сосуды теряют свою опору, становятся хрупкими, развивается пурпура - геморрагическая сыпь.
- Появляются тонкие бледные рубцы, вследствие нарушения кожной регенерации могут развиваться долго заживающие язвы,
- Характерная особенность атрофии кожи, вызванной стероидными гормонами - растяжки, стрии. Это разрывы глубоких слоев кожи из-за недостаточной выработки коллагена, синтез которого угнетен глюкокортикоидами. Этот симптом, в отличие от остальных, необратим, стрии остаются на коже даже после полного восстановления от атрофического дерматита.
Лечение атрофического дерматита
Атрофический дерматит приводит к изменениям, которые часто бывают необратимыми, однако во многих случаях симптомы можно уменьшить, и лечение улучшает состояние кожи, как это показано на фото.
- При атрофии, вызванной стероидами, самый главный метод терапии - отмена препарата, вызвавшего проблему. Часто одно только это мероприятие приводит к восстановлению кожных покровов.
- Увлажнение повышает сопротивление кожи внешним воздействиям, предотвращает повреждение. Назначают комплексные препараты с эмолентами.
- Необходимо ограничить контакт с жесткими химикатами, защищать кожу от механических повреждений.
- Кремы с витамином А, ретиноиды, помогают предотвратить дальнейшее истончение кожи. Они усиливают обменные процессы, способствуют обновлению эпидермиса и увеличивают скорость деления клеток.
- Несмотря на то, что средства, стимулирующие выработку коллагена не показали эффективности в клинических исследованиях, однако многие пациенты отмечают субъективное улучшение, замечают, что кожа становится толще.
- Витамин Е поддерживает эластичность кожи и препятствует атрофии. Назначают его внутрь в капсулах. Также полезно употреблять в пищу продукты , богатые витамином Е: авокадо, орехи, ростки пшеницы.
Профилактика атрофического дерматита
Все люди испытывают ту или иную степень атрофии кожи вследствие старения, и это невозможно предотвратить. Появляются мелкие линии и морщины, кожа становится тоньше и суше в связи с возрастом. Но в некоторой мере возможно уменьшить и замедлить появление видимых признаков старения. Это неспецифическая профилактика атрофического дерматита.
- Защита от ультрафиолетовых лучей значительно уменьшает скорость старения.
- Увлажнение кожи помогает защитить от потери влаги, предотвращает сухость и повреждение эпителия. Эмоленты препятствуют испарению воды, увлажненная кожа более эластичная, устойчивая и здоровая.
- Алкоголь приводит к значительной потере жидкости организмом. Для сохранения тургора кожи и профилактики атрофии спиртные напитки лучше вообще не употреблять. Если вы принимаете решение выпить алкоголь, после каждой дозы выпивайте стакан воды.
Ежедневно наносите солнцезащитное средство с фактором защиты spf30 или выше. Это предотвращает вредное воздействие и UVA, и UVB лучей.
В самые жаркие часы дня находитесь в помещении или прячьтесь в тенистое место.
Носите длинные рукава, длинные юбки или брюки, особенно в солнечные дни.
Шляпа с полями поможет защитить от солнца голову, шею и лицо.
Специфическая профилактика направлена на предотвращение стероидного атрофического дерматита. Грамотный подход к лечению любых состояний кожи гормональными мазями необходим, чтобы не развилась атрофия кожи.
- Слабые глюкокортикоиды нельзя использовать дольше месяца,
- Длительность применения более сильных гормонов ограничивается двумя неделями,
- При необходимости длительного лечения мази применяют по схеме 2-3 дня подряд с последующими тремя - четырьмя днями отдыха,
- Нельзя наносить гормональные мази на области с тонкой и чувствительной кожей - лицо, подмышечные области и промежность.
- При устойчивости кожной проблемы к лечению необходимо обратиться за помощью к лечащему врачу, который поменяет препарат или адаптирует дозу. Возможно, гормональное средство будет заменено современным негормональным.
- Во время терапии необходимо есть сбалансированную пищу с достаточным содержанием белка, который является строительным материалом для кожи. Достаточная гидратация (не менее двух литров чистой воды в день) также очень важна.
Контактный дерматит – это разновидность воспалительного заболевания кожи, возникающая как реакция на раздражитель на химическое или аллергенное вещество. К ним относятся мыло, чистящие средства, латекс, косметика (в том числе ухаживающая), металлы (никель, золото), спирт и косметика на спиртовой основе, сок растений, лекарственные препараты, чернила, краски, клей, ткани. Также контактный дерматит может проявляться под воздействием ультрафиолетовых лучей.
Существует несколько видов дерматита (атопический, контактный, аллергический и себорейный), но для всех них характерны одни и те же признаки: вздутие кожи, сыпь, зуд, жжение, шелушение кожи. Однако несмотря на схожесть симптомов, причины и механизмы появления болезни в каждом случае индивидуальны, поэтому крем или мазь от дерматита должны быть назначены врачом.
Дерматит на руках – это воспаление кожи, для которого характерны высыпания на кистях, запястьях и предплечьях (реже – плечах). Подобные высыпания чаще встречаются при контактном, аллергическом и атопическом дерматите.
Профилактические меры при дерматите направлены на продление периода ремиссии. Различают 4 разновидности этого заболевания: контактный, атопический, себорейный и аллергический дерматит. Каждый из них требует соблюдать специфические правила.
Закажите бесплатную доставку



Задайте вопрос
о заболеваниях кожи

Сергеев Юрий Юрьевич
Вопросы и ответы
посмотреть все вопросы
Здравствуйте подскажите пожалуйста год назад появилось пятно на ступни не грибок, иногда зудит и шелушится сказали экзема похоже на псориаз что делать чем лечить перепробовала все не чего не помогает пятно только становится больше
Валентина, здравствуйте! Если точный диагноз не установлен, то подбирать какое-то пробное лечение будет неправильно. Постарайтесь получить второе мнение по диагнозу у дерматолога на очной консультации, возможно, на консилиуме.
Здравствуйте! Подскажите, а какое действие имеет мазь Солантра при папуло-пустулезной розацеа? Эффективна? Чем можно лечить «розовые угри»?
Здравствуйте, Марина. Препарат обладает противовоспалительным эффектом и влияет на микрофлору кожи. В своей практике не часто назначаю этот препарат, предпочтение отдаю вариантам системной терапии (изотретиноин в малых дозах). Не занимайтесь самолечением, найдите своего врача и добивайтесь стойкой ремиссии!
Чем лечить раздражение на руке?
Здравствуйте, Ольга Игоревна. Во-первых, следует исключить провоцирующие факторы, которые вызывают воспалительную реакцию. Как лечебное средство Вы можете использовать крем «Лостерин» 2-3 раза в день – он поможет восстановить структуры кожи, уберет воспаление и безопасен для длительного применения.
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения Москвы, 119071, Москва, Российская Федерация
Стероидная розацеа как следствие применения ингаляционных глюкокортикостероидных средств
Журнал: Клиническая дерматология и венерология. 2015;14(6): 66‑68
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения Москвы, 119071, Москва, Российская Федерация
Обсуждается клиническое течение стероидной розацеа. Показано, что не только местное применение топических кортикостероидов, но и их ингаляционное введение может вызывать стероидную розацеа. Актуален вопрос о ведении пациентов, для которых ингаляционное введение кортикостероидов жизненно необходимо.
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения Москвы, 119071, Москва, Российская Федерация
Розацеа — одна из частых причин обращения к дерматологу. Заболевание характеризуется преимущественным поражением кожи лица, волнообразным течением с чередованием периодов обострений и ремиссий.
В современной классификации выделяют четыре основных типа розацеа, соответствующих эритематозной, папулопустулезной, гипертрофической стадиям и офтальморозацеа в прежних классификациях, и один вариант — гранулематозную розацеа, а также подтипы розацеа: подтип I ― эритематозно-телеангиэктатический; подтип II ― папулопустулезный; подтип III ― фиматозный (например, ринофима, гнатофима, отофима); подтип IV ― офтальморозацеа [1].
По мнению В.П. Адаскевича [2], розацеа представляет собой заболевание с характерной комбинацией кожных стигм. Если взять типологическую модель розацеа, то в ее эпицентре находятся пациенты с эритемой, телеангиэктазиями, отеком лица, папулами, пустулами, поражениями органа зрения и ринофимой. В большинстве случаев отмечается меньшее число симптомов, чем полный набор этих признаков.
Причиной заболевания является ангионевроз, который может развиваться под воздействием различных факторов: алиментарных, химических, физических [1]. Анамнестические указания на заболевание у кровных родственников, I и II тип фоточувствительности по Фитцпатрику являются бесспорными факторами риска. Интеркуррентные заболевания ― эндокринная, гастроэнтерологическая, иммунная патологии ― предопределили общеклинический характер проблемы [3, 4]. Устранение провоцирующих факторов и лечение сопутствующих заболеваний являются одним из ключевых моментов ведения пациентов с розацеа.
Кроме того, необходимо отметить распространение среди пациентов неврастении и депрессии, разнообразных эмоциональных нарушений, которые, несомненно, требуют коррекции [1].
Для общей и наружной терапии используют азелаиновую кислоту, антибиотики, ретиноиды, метронидазол [5—8].
В настоящее время топические глюкокортикоидные препараты не рекомендуются для терапии розацеа, так как их длительное использование приводит к развитию стероидной формы заболевания [9, 10]. Стероидная розацеа развивается вследствие длительного назначения топических кортикостероидов по поводу хронических дерматозов или их применения пациентами для самолечения возникших признаков розацеа. Необходимо отметить, что именно использование топических кортикостероидов является основной причиной возникновения розацеа и периорального дерматита в детском возрасте.
Клинически стероидная розацеа существенно не отличается от других форм заболевания. Помимо эритемы, телеангиэктазий, папул и пустул, при этой разновидности розацеа могут наблюдаться участки невыраженной атрофии. Другим клиническим признаком, характеризующим стероидную розацеа, является «синдром отмены», который обычно развивается после прекращения местной кортикостероидной терапии. Как правило, через 7—10 дней после применения гормонального препарата наступает резкое обострение кожного процесса. В это время отмечаются гиперемия и отечность лица, которая нередко приводит к сужению глазных щелей. Постепенно возникают папулезные и пустулезные элементы. Выраженность реакции обострения находится в прямой зависимости от продолжительности предшествующей гормональной терапии. Феномен «синдрома отмены», по-видимому, объясняется двояким характером воздействия местных кортикостероидных препаратов. С одной стороны, глюкокортикоиды способствуют стойкой дилатации мелких артериальных сосудов кожи, а также истончению последней, в результате чего формируется благоприятная почва для развития розацеа. С другой стороны, выраженный противовоспалительный эффект кортикостероидных гормонов препятствует появлению симптомов грядущего патологического процесса. Постепенно наступает толерантность к подобной терапии и постепенно нарастает симптоматика стероидной розацеа.
После применения галогенизированных топических глюкокортикоидов нередко развивается феномен «стероидной» кожи, характеризующийся субатрофией, обширной эритемой, на поверхности которой находятся телеангиэктазии и папуло-пустулезные элементы. Кортикостероидная терапия папулезной розацеа способствует переходу ее в пустулезную форму.
Помимо обычной топической стероидной терапии, к возникновению стероидной розацеа может привести ингаляционное применение кортикостероидных препаратов. Из 96 пациентов с розацеа, обследованных нами в филиале «Вешняковский» Московского научно-практического центра дерматовенерологии и косметологии, мы наблюдали стероидную розацеа, связанную с ингаляционным применением кортикостероидов, в 4 случаях. К моменту нашего обследования пациенты были в возрасте 44—52 лет, из них 2 женщины, 2 мужчин. Все 4 пациента наблюдались по поводу бронхиальной астмы в течение 18—39 лет, по поводу розацеа ― 16—28 лет; все эти больные отмечали регулярное ингаляционное применение кортикостероидов. Несмотря на отсутствие анамнестических указаний на применение топических кортикостероидов, у всех имелись вышеупомянутые клинические признаки стероидной розацеа (см. рисунок).

Стероидная розацеа.
Таким образом, стероидная розацеа, развившаяся вследствие ингаляционного введения кортикостероидов, представляет собой серьезную проблему в практике дерматовенеролога, так как отменить введение препаратов, назначаемых по жизненным показаниям, не представляется возможным, а полноценное лечение без полной отмены стероидных средств неэффективно. В подобных случаях рекомендуется применение базисных наружных средств для терапии розацеа, в частности, азелаиновой кислоты, ретиноидов для наружного применения, лазерных технологий.
"Атрофии кожи" проводится с 01 по 31 октября 2013 г.
Чтобы прислать случаи на фотосессию, выберите ее название из списка в форме "Создать наблюдение".
Рекомендуем прочесть наши советы по тому, как создать хорошее наблюдение.
Пожалуйста, подписывайте каждое фото уникальным названием (лучше всего - с указанием конкретной локализации по этому фото). Присылайте случаи по одному на одного пациента, не менее 5 фото на каждый случай. Фотографии гистологических, иммуногистохимических и иных исследований и их заключений приветствуются, заполняйте соответсвующий раздел в форме описания. Сделайте подпись к каждому фото.
Мы принимаем на фотосессию наблюдения пациентов с установленным диагнозом любого типа атрофии кожи, если термины "атрофия" или "атрофический" входят в общеупотребительное название диагноза. Список нозологий включает, но не ограничивается, следующими записями в МКБ-10:
- 90.0 Лишай склеротический и атрофический
- L90.1 Анетодермия Швеннингера-Буцци
- L90.2 Анетодермия Ядассона-Пеллизари
- L90.3 Атрофодермия Пазини-Пьерини
- L90.4 Акродерматит хронический атрофический
- L90.5 Рубцовые состояния и фиброз кожи
- Спаянный рубец (кожи)
- Шрам
- Обезображивание, вызванное рубцом
Победитель фотосессии будет определен голосованием посетителей сайта и получит много баллов рейтинга.
Дебютантам фотосессии начисляются стартовые 500 баллов.
Остальные участники получают столько же баллов, сколько голосов будет подано за их случаи.
Эти баллы Вы сможете обменять на ценные призы (книги, журналы и т.д.).Дополнительное задание
Коллективного спецзадания в этой фотосессии нет. Однако каждое представленное на конкурс наблюдение, у которого в разделе Изображения по обследованию будут фотографии гистопатологического препарата, фототрихограмма или трихоскопия, получит дополнительные 100 баллов рейтинга.
Читайте также:

