Солевые повязки при диабете гангрена
Обновлено: 15.04.2024
Пациентка А., 63 лет, впервые была осмотрена амбулаторно 16.07.14 г. в специализированном кабинете «Диабетическая стопа» ГКБ № 67 им. Л.А. Ворохобова. По результатам осмотра с учетом выявленных показаний была в плановом порядке госпитализирована и находилась на стационарном лечении во 2-ом эндокринологическом отделении с 28.07 по 15.08.2014 г. с диагнозом: Сахарный диабет 2 типа, тяжелого течения, субкомпенсация. Пролиферативная диабетическая ретинопатия, артифакия правого глаза. Субатрофия сетчатки левого глаза. Диабетическая дистальная полинейропатия. Сенсо-моторный тип. Диабетическая макроангиопатия. ХАН 2а. Варикозная болезнь обеих нижних конечностей. ХВН СЕАР 4. ИБС. Атеросклеротический кардиосклероз. НК 2А. Гипертоническая болезнь III степени. Риск 4 ССО. Дисциркуляторная энцефалопатия 2 ст., субкомпенсация. Последствия перенесенного ОНМК в 2006 г. Левосторонний гемипарез. Системная красная волчанка. Хроническое течение с полиорганным поражением: плеврит, миокардит, дерматит, анемия, иммунологические нарушения. Медикаментозный синдром Иценко-Кушинга. Системный остеопороз. Распространенный остеохондроз позвоночника. Двусторонний коксартроз. Узловой зоб. Эутиреоз. Ожирение 1 ст. Инфицированная трофическая язва левой голени смешанного генеза.
При поступлении жаловалась на наличие длительно (более 6 недель) незаживающей болезненной язвы задней поверхности левой голени со значительным гнойным отделяемым. В анамнезе сахарный диабет с 1990 г., с 2000 г. получает инсулинотерапию. Со слов пациентки суточная гликемия до 10,0 ммоль/л. Гликемия при поступлении 5,3 ммоль/л. Кетонурии не выявлено.
Общее состояние при поступлении ближе к удовлетворительному. АД – 100/80 мм.рт.ст. Периферических отеков нет. Имеется умеренная пастозность нижних конечностей, более выраженная слева. В лабораторных анализах отмечается анемия легкой степени 111 г/л. Гематокрит 33,2%. Лейкоциты 7,9 х 10 9 в л. Общий белок 72,6 г/л. Гликированный гемоглобин 8,7%.
Status localis: Левая голень и стопа пастозны. Отмечается умеренно выраженная сеть увеличенных подкожных вен до 5 мм в диаметре. На задней поверхности левой голени в средней трети имеется трофическая язва округлой формы до 3,5 см. в диаметре, глубиной до 0,5 см. Дном язвы является поверхностная фасция, покрытая плотным слоем фибрина. Грануляции на вид бледные, вялые, не кровоточат, покрывают не более 10% площади раны. Края язвы местами некротически изменены. Фибринозно-гнойное отделяемое в умеренном количестве с незначительным запахом. Явления перифокального воспаления выражены умеренно. Кожа истончена, содержит следы использования раствора марганцовокислого калия по периферии раны. Дерматита, кожных трещин нет. Движения в суставах левой нижней конечности не ограничены. Пульсация сосудов в левой паховой области отчетливая, в подколенной области снижена, дистальнее не определяется. Симптомы Хоманса и Мозеса отрицательные.
При бактериологическом исследовании раны от 23.07.14 г. выявлена смешанная микрофлора, не чувствительная к большинству тестовых антибиотиков:
Staphylococcus saprophyticus (10 5 КОЕ/мл), Escherichia coli (10 6 КОЕ/мл), Enterococcus faecalis (10 5 КОЕ/мл)
Дуплексное сканирование артерий и вен нижних конечностей: Признаков венозного тромбоза не выявлено. Признаки варикозных изменений в системе большой подкожной вены с обеих сторон. Признаки стенозирующего атеросклероза артерий обеих нижних конечностей без гемодинамических нарушений. Плече-лодыжечный индекс составил 0,75.
Начата комплексная консервативная терапия, направленная коррекцию основного заболевания и его осложнений. Назначен курс комбинированной направленной системной антибактериальной терапии (Инванз + Эдицин) с учетом высокого уровня микробной обсемененности трофической язвы смешанной микрофлорой и спектра ее чувствительности к тестовым антибактериальным препаратам.
С учетом хронического характера течения раневого процесса и наличия некротических изменений начата местная терапия с использованием повязок TenderWet ® active. Данный выбор был обусловлен основными свойствами и клинической эффективностью этих повязок, активно функционирующих благодаря свойствам суперабсорбирующего полимера (САП) - продолжительному выделению раствора Рингера и одновременной абсорбции раневого отделяемого. При этом отмечается активная регидратация и отторжение некроза, снижается уровень микробной обсемененности раны и концентрация матриксных металлопротеаз (ММП) и предотвращается разрушение экстрацеллюлярного матрикса. В результате отмечается активация местного иммунитета, сохраняются функции факторов роста, активируется воспаление, стимулируется ангиогенез и дальнейшая регенерация.
От применения эластической компрессии было решено отказаться в связи с наличием противопоказаний.

Рис. 1 Начальный вид (а) и динамика раневого заживления (б, в) трофической язвы левой голени на начальном этапе лечения повязками TenderWet ® active (plus)
Повязки TenderWet ® plus обладают более продолжительным воздействием на рану (до 72 часов), благодаря модернизации и включению в их состав полигексанида – антисептика широкого спектра действия, не токсичного в отношении тканей. Данный антисептик непосредственно связан со структурой САП в абсорбирующем элементе повязки и, не выходя на раневую поверхность, подавляет действие микроорганизмов на поверхности гранул САП, предотвращая повторное инфицирование раны в течение 72 часов. Это позволило применять повязки TenderWet ® plus для контроля над раневым процессом в выходные дни и при дальнейшем лечении, когда уровень экссудации снизился до минимума. При этом частота перевязок составляла не более 3-х раз в неделю.
К моменту выписки отмечена явная положительная динамика течения раневого процесса (рис. 1в). Язва полностью очистилась от некротических тканей, дно раны поднялось, стало вровень с кожей, покрылось хорошо выраженными грануляциями. Экссудация снизилась до уровня слабой интенсивности. Явления воспаления полностью купированы. По результатам контрольного бактериологического исследования роста микрофлоры выявлено не было. Местное лечение раны решено было продолжить повязками TenderWet ® plus в амбулаторном режиме.

Рис. 2 Дальнейшая динамика заживления язвы в начале амбулаторного лечения повязками TenderWet ® plus (а) и через 6 недель (б).
На амбулаторном этапе повязки TenderWet ® plus позволили эффективно поддерживать необходимые параметры раневой среды для создания наилучших условий для заживления хронической раны при частоте перевязок 2-3 раза в неделю (рис. 2а). Через 6 недель амбулаторного лечения язвенный дефект уменьшился в размерах и принял характер гранулирующей раны. Экссудация была минимальна по интенсивности и носила сукровичный характер (рис. 2б). Болевой синдром полностью отсутствовал как в покое, так и при смене повязки. Изменений со стороны окружающей кожи не выявлено. Было решено продолжить местное лечение с использованием губчатой повязки HydroTac ® , защищенной гидроактивным гелевым слоем, покрывающим 50% поверхности высоко гидрофильной губки. В дальнейшем, такая конструкция позволила в полной мере реализовать как высокие сорбционные, так и активные увлажняющие свойства до 5 суток. Способность поддерживать оптимальный гидробаланс раневого ложа позволила продолжать стимуляцию заживления хронических гранулирующих ран вплоть до полной их эпителизации.

Рис. 3 Динамика течения раневого процесса при амбулаторном использовании повязок HydroTac ® .
В течение двух недель амбулаторного лечения гидроактивными губчатыми повязками HydroTac ® при частоте перевязок дважды в неделю удалось поддержать прежние темпы заживления, добиться сокращения площади язвы более чем в два раза и активной эпителизации язвенной поверхности (рис. 3а). В то же время было отмечено практически полное прекращение экссудации и признаки пересыхания раневого ложа (рис. 3б). Дальнейшее применение повязок HydroTac ® не позволяло поддерживать оптимальную влажность раневого ложа и создавать условия для окончательной эпителизации трофической язвы. Поэтому рана дальше велась под прозрачной гидрогелевой повязкой Hydrosorb ® . Эта повязка обладает незначительными сорбционными свойствами. Однако ее контактный гелевый слой содержит 60% воды, способной длительно выделяться на раневую поверхность. Это позволяет, не удаляя повязки до семи суток защищать раневое ложе от пересыхания, поддерживать оптимальную концентрацию факторов роста и создавать оптимальные условия для миграции эпителиоцитов и окончательной эпителизации раневого дефекта.

Рис.4 Стимуляция эпителизации язвы с помощью прозрачной самофиксирующейся гидрогелевой повязки Hydrosorb ® comfort.
Наличие дополнительной наружной мембраны позволило отмечать периметр раны, вычислять ее площадь при каждой перевязке и сохранять данные измерения в отчетной медицинской документации (Рис. 4а,б). Начальная эпителизация язвы при использовании гидрогелевой повязки Hydrosorb ® comfort отмечалась практически по всей поверхности и была отмечена уже после двух перевязок (Рис.4в). Общий срок местного лечения язвы не превысил четырех месяцев.
Таким образом, использование метода лечения ран во влажной среде и, в соответствии с этим, последовательное использование гидроактивных повязок TenderWet ® active/plus, HydroTac ® и Hydrosorb ® (comfort) позволило добиться эпителизации раневой поверхности при местном амбулаторном лечении хронической язвы голени смешанного генеза у пациентки с сахарным диабетом и выраженной соматической полиорганной отягощенностью. При этом, как показало данное клиническое наблюдение, лечение может быть начато в условиях стационара и эффективно продолжено в амбулаторных условиях. Применение современных гидроактивных перевязочных средств позволяет достаточно надежно контролировать течение раневого процесса, препятствовать вторичному микробному обсеменению раны, уменьшить количество и болезненность перевязок и, тем самым, способствовать улучшению качества жизни пациентов с сахарным диабетом, имеющих хронические раны.
Что такое сухая гангрена? Причины возникновения, диагностику и методы лечения разберем в статье доктора Манасяна К.В., сосудистого хирурга со стажем в 10 лет.
Над статьей доктора Манасяна К.В. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Гангрена — это некроз (омертвление) тканей живого организма, связанных с внешней средой, например, кожи, лёгких, кишечника и других. С древнегреческого данный термин переводится как "разъедающая язва".
Сухая гангрена — это опасное заболевание, требующее незамедлительного лечения. При этой патологии отмирание ткани происходит без выраженного инфекционного и воспалительного процесса. Иначе такой характер течения заболевания называют мумификацией, т. е. отсыханием органа.
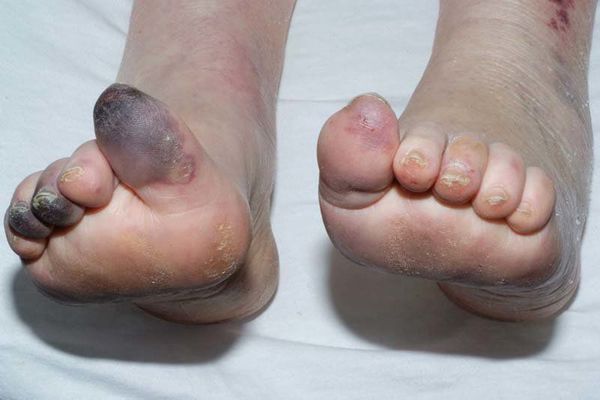
Механизмы возникновения гангрены бывают двух типов:
- прямыми (травматическими и токсическими) — появляются по причине непосредственного повреждения, иногда даже незначительного;
- непрямыми (ишемическими, аллергическими, трофоневрологическими) — происходит опосредованное отмирание тканей через анатомические каналы, в частности, при поражении сосудистой системы.
Исходя из этого факторы риска развития сухой гангрены можно также разделить на две группы:
- Внешние (экзогенные):
- переохлаждение (обмоорожение);
- химический ожог;
- удар током высокого напряжения.
- Внутренние (эндогенные): артерий нижних конечностей; ;
- курение;
- воспалительные заболевания артерий (васкулиты, в частности тромбангиит). [4][5][6]
Зачастую гангрена возникает при совокупности факторов, например, в результате механического повреждения кожи пациента с сахарным диабетом. По статистике, доля людей с мумификацией, развившейся на фоне подобных факторов и приведшей к ампутации конечности, составляет 4,2-6,4 на одну тысячу человек в год. В связи с этим люди с диабетической стопой относятся к группе риска развития гангрены. [10]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы сухой гангрены
К симптомам сухой гангрены относятся:
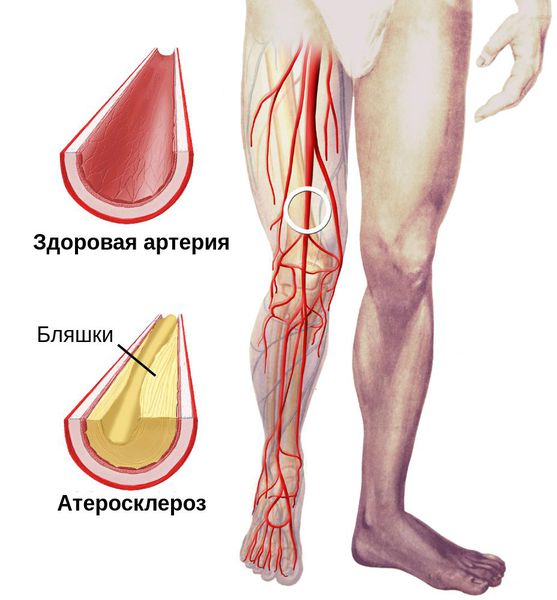
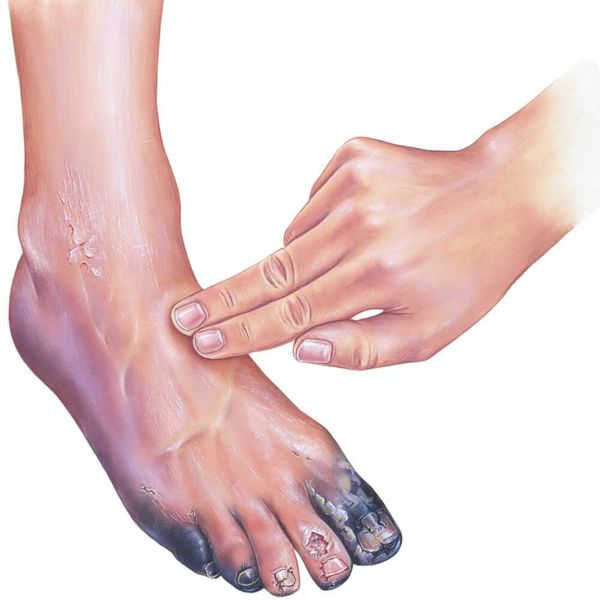
- потемнение кожного покрова (вначале кожа бледнеет, приобретает синюшный оттенок, затем постепенно становится чёрной);
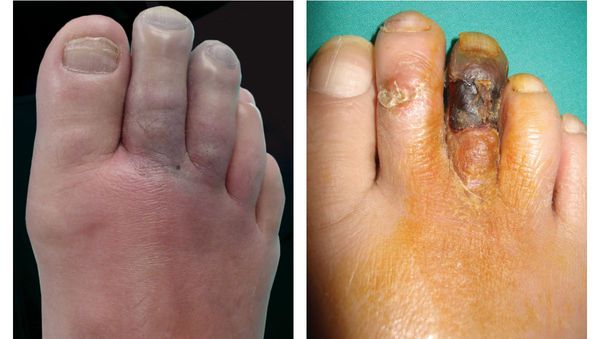
- уменьшение кожи в объёме, её высыхание, сморщивание и уплотнение;
- отслаивание эпидермального слоя кожи;
- снижение температуры конечности (зависимость от температуры окружающей среды);
- снижение чувствительности поражённых тканей (онемение);
- наличие специфического запаха отмирающего участка (хоть и не столь сильного);
- ощущение боли (простреливающие, жгучие и ноющие болевые ощущения, которые могут носить постоянный характер, а также усиливаться при минимальной нагрузке);
- покалывание, жжение или зуд в области поражения;
- нарушение функционирования конечности.
Болевой синдром отражает то, насколько сильно страдают окружающие ткани: чем сильнее боль в зоне некроза, тем больше в этой области живых клеток. Ослабление болезненных ощущений или их исчезновение указывает на прогрессирование заболевания, так как чувствительность отмирающей ткани пропадает в результате гибели нервных окончаний. В это время анатомические области, граничащие с сухой гангреной, остро нуждаются в артериальном кровотоке, которого им не хватает. В итоге в этих тканях вырабатываются продукты метаболизма и болевые импульсы.
Сухая гангрена начинается с появления небольшого очага на конечности (как правило, расположенного на пальце). Далее она распространяется на прилегающие пальцы, подошвенную и тыльную поверхность стопы, захватывая всё больше тканей конечности.
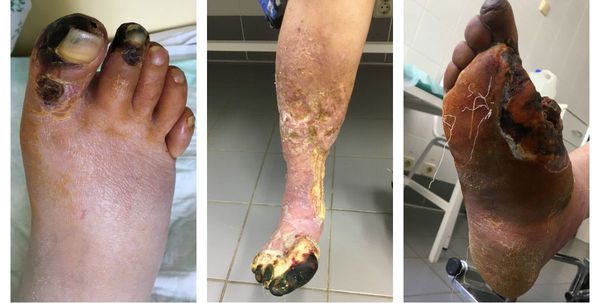
Изменения цвета отмирающих участков кожи связано с накоплением в них гемоглобина и выделением эритроцитарного железа, которое в результате соединения с сероводородом воздуха превращается в сульфид железа.
Зона, которая находится на границе гангрены и здоровой ткани называется демаркацией. Обычно она не оформлена. В исключительно редких случаях при естественном течении болезни она может самостоятельно ограничиться, что приведёт к самоампутации отмирающей конечности. [3] [5] [6]
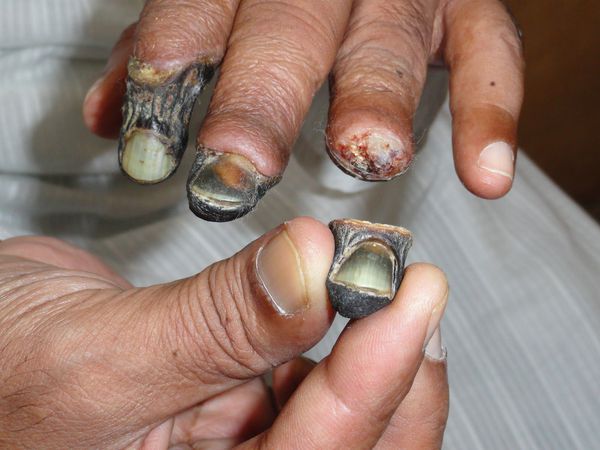
К первым признакам сухой гангрены относятся следующие состояния:
- замерзание конечности даже в тепле;
- боль в ногах и утомляемость после длительной ходьбы;
- наличие долго не заживающих ран и язв на коже конечности.
ВАЖНО: Возникновение одного из этих проявлений при наличии таких предрасполагающих факторов, как сахарный диабет или атеросклероз, — веский повод для скорейшего обращения к врачу-флебологу или хирургу. Промедление как минимум может обернуться для пациента утратой конечности.
Патогенез сухой гангрены
Процесс возникновения и развития сухой гангрены конечностей можно условно разделить на семь этапов:
При естественном течении сухой гангрены признаков инфекции не наблюдается (в отличие от влажной гангрены), однако в омертвевших тканях не исключено наличие возбудителей условно-патогенной инфекции. При этом в зонах некроза не происходит бурного развития инфекции.
Процесс развития сухой гангрены ног и рук может длится от нескольких дней до нескольких месяцев в зависимости от уровня поражения артерий и компенсаторных механизмов саморегуляции. [3] [4] [5] [6] Если некроз уже развился, то заживление без удаления некоторой части конечности невозможно.
Классификация и стадии развития сухой гангрены
В зависимости от распространения некроза на конечности можно выделить следующие виды заболевания:
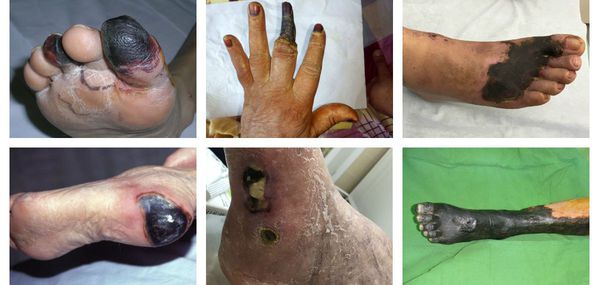
- гангрена пальцев;
- гангрена дистального сегмента стопы (кисти);
- гангрена пяточной области;
- тотальная гангрена стопы (кисти) или голени (предплечья);
- гангрена бедра (встречается крайне редко, так как пациенты просто не доживают до столь массивного гангренозного поражения). [3][5][6]
По механизму развития различают два вида гангрены:
- Первичная гангрена — это некроз, развившийся в результате ишемии тканей. Иначе говоря, она связана с нарушением проходимости артериального сосуда, кровоснабжающего определённый участок организма.
- Вторичная гангрена — это некроз тканей, возникающий в результате острого гнойного воспаления клетчаточных пространств и фасциальных футляров. Чаще всего развивается при флегмоне стопы, затрагивая пальцы, а также при или глубоком абсцессе на фоне нейроптической формы синдрома сахарного диабета.
По распространённости выделяют три степени гангрены:
- поверхностную — поражается лишь дерма;
- глубокую — проникает в сухожилия, полости суставов, фасции и кости;
- тотальную — затрагивает все отделы органа или конечности.
Помимо сухой гангрены существует ещё влажная и газовая.
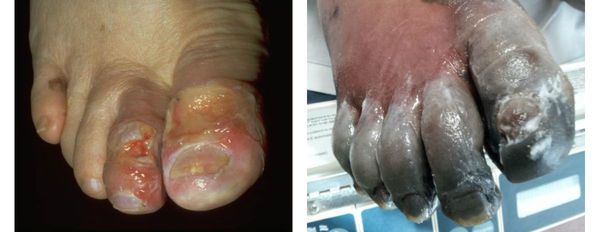
Влажная гангрена протекает с преобладанием инфекционного компонента, т. е. гнилостного расплавления. В процесс вовлекаются все без исключения ткани — кожа, подкожно-жировая клетчатка, фасции, связки, мышцы, сухожилия и кости. Кожные покровы местами приобретают багрово-синюшный, чёрный или серо-зелёный цвет. Характерно появление эпидермальный пузырей, наполненных вначале бурым, а затем зеленоватым содержимым с выраженным неприятным гнилостным запахом.
В отличие от сухой гангрены при влажной ткани не уплотняются, а распадаются, становятся рыхлыми и разжижаются. Отёк и гиперемия кожи быстро распространяются. Кожа голени может быть напряжена, лосниться. Без активного лечения демаркационная линия не появляется, так как процесс стремится к генерализации.
Газовая гангрена отличается возникновением вокруг очага некроза лёгкой крепитации газа под кожей, т. е. ощущением хруста, которое появляется из-за лопающихся пузырьков газа в тканях. Крепитация не слышна, но осязается пальцами как "скрип" крахмала или снега под ногами. Объективно газ в мягких тканях может быть обнаружен при рентгенографии конечности на достаточно "мягких" снимках. [11]
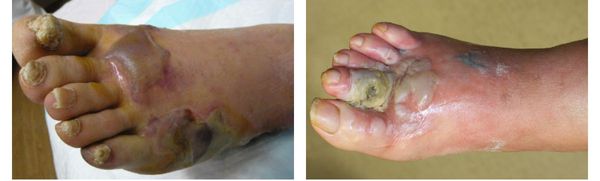
Осложнения сухой гангрены
Само по себе наличие гангрены указывает на полную нежизнеспособность и омертвление тканей, предполагая крайнюю степень патологического процесса. Поэтому отсутствие своевременного лечения может привести к потере поражённой конечности.
Сухая гангрена не может перерасти во влажную или газовую гангрену, как ошибочно утверждают многие источники, потому что изначально при возникновении некроза становится очевиден механизм развития гангрены. [1] [2] [3] [4] [7]
Редкими осложнениями сухой гангрены являются сепсис и септический шок. Они возникают в связи с токсическим действием продуктов распада при проникновении их в системный кровоток. Данные осложнения способны привести к полиорганной недостаточности и, как следствие, летальному исходу.
К проявлениям сепсиса относятся:
- ознобы;
- высокая или очень низкая температура тела (больше 38°C или меньше 36°C);
- одышка (частота дыхания более 20 в минуту);
- артериальная гипотензия (пульс более 90 ударов в минуту);
- аритмия;
- олигурия (объём мочи менее 0,5 мл/кг/ч);
- вялость, заторможенность;
- наличие различных лабораторные показания, не поддающаяся коррекции — низкий уровень белка, тромбоцитов и красных кровяных телец, а также высокий уровень билирубина, остаточного азота, мочевины, сахара в крови и ацетона в моче.
В случае септического шока давление становится крайне низким, даже на фоне интенсивного вливания внутривенных растворов. В связи с этим около 30-40 % пациентов умирает несмотря на оказываемое лечение. [12]
Диагностика сухой гангрены
Диагностика сухой гангрены достаточно проста, так как на некроз указывает внешний вид поражённого органа:
- его сухость;
- уменьшение участка кожи в объёме;
- тёмный, вплоть до чёрного, цвет кожи;
- наличие слабого неприятного запаха и болей непосредственно в мёртвом участке;
- наличие прохладных на ощупь окружающих тканей с выраженным болевым синдромом в них. [1][2][3][4][7]
При осмотре необходимо диагностировать причину сухой гангрены (например, атеросклероз артерий и тромбангиит). Для этого нужно проверить пульсацию артерий как поражённой, так и здоровой ноги на уровне паховых и подколенных областей, позади медиальной лодыжки и на тыле стопы. В дальнейшем необходимо подтвердить причинный диагноз с помощью ультразвукового исследования.
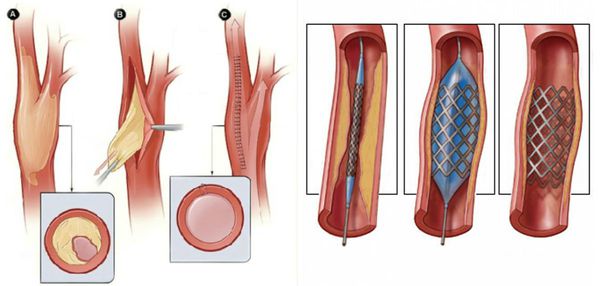
В качестве предоперационной подготовки для определения вида оперативного лечения выполняется ангиография нижних конечностей:
- при протяжённых поражениях артерий выполняется хирургическая операция — аутовенозное шунтирование;
- при коротких поражениях более предпочтительно выполнить эндоваскулярную операцию (наименее травматичное лечение). [1][2]
Для предоперационной подготовки нужно сдавать общий и биохимический анализ крови, а также бактериальный посев. Эти лабораторные исследования помогут выяснить, не является ли причиной сухой гангрены сахарный диабет.
Лечение сухой гангрены
С целью предотвращения гангрены и максимально возможного сохранения конечности требуется восстановить кровоток в тканях, окружающих гангренозный участок.
Нормализовать кровообращение в органе можно при помощи оперативного вмешательства:
- Реконструктивные операции на артериях конечности (как правило, руки):
- аутовенозное шунтирование;
- эндартерэктомия (удаление закупорки артерии) с аутовенозной пластикой;
- шунтирование артерий аорто-подвздошно-бедренного сегмента синтетичсекими протезами.
- Рентгенэндоваскулярные операции (не показаны пациентам с тромбангиитом):
- стентирование;
- баллонная ангиопластика артерий.
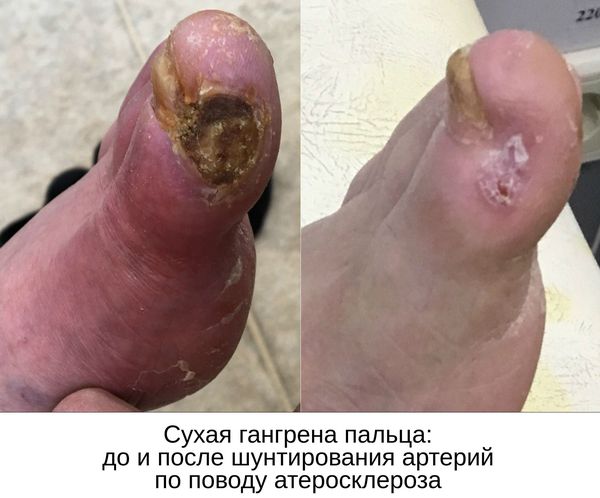
Паллиативные операции (поясничная симпатэктомия и остеотрепанация), проводящиеся для улучшения качества жизни, и другие нехирургические методы лечения (генная и физиотерапия) не способны предотвратить прогрессирование сухой гангрены.
Саму гангренозную ткань необходимо убрать. Для этого проводят:
- малые ампутации — удаление пальцев или части стопы с некрозом;
- некрэктомию — поверхностное удаление некротического струпа до пределов тканей с удовлетворительным кровотоком.
В случаях обширного гангренозного поражения с потерей опороспособной стопы прибегают к ампутации голени либо бедра. Чтобы избежать подобного печального исхода, важно при первых же признаках гангрены без промедления обратиться к врачу: потерять конечность куда страшнее, чем её лечить. Особенно это относится к людям с сахарным диабетом и атеросклерозом: нельзя ждать, когда гангрена начнёт прогрессировать, иначе удаление поражённой конечности будет неизбежным.
Если всё же обширная гангрена стопы привела к потере её опороспособности, то в таких случаях целесообразно выполнение ампутации голени на уровне границы средней и верхней трети. В дальнейшем это позволит подобрать и использовать удобный протез.
Даже после ампутации гангрены, возникшей из-за закупорки артерий ноги, необходимо выполнить реконструктивную (шунтирующую) или рентгенэндоваскулярную операцию на артериях нижней конечности. Делается это с целью обеспечения кровотока для успешного заживления постампутационной культи голени.
При физических причинах гангрены (отморожение) или химических (внутриартериальное введение синтетичсеких наркотиков) лечение заключается в нормализации вязкости крови. Для этого проводится:
- антикоагулянтная и инфузионная терапия;
- профилактика синдрома полиорганной недостаточности;
- хирургическое удаление участка, поражённого сухой гангреной. [1][2][3]
Прогноз. Профилактика
Прогноз зависит от степени гангренозного поражения:
- при гангрене пальцев или небольших участков стопы конечность можно восстановить при реставрации кровотока, удалении омертвевших тканей и создании благоприятных условий для заживления;
- при тотальной сухой гангрене стопы показана ампутация на уровне голени, но с условием, что кровоток в голени достаточен для заживления постампутационной культи;
- при обширной гангрене голени пациенту показана ампутация ноги на уровне бедра.
Пятилетняя выживаемость при сухой гангрене сравнима с выживаемостью при злокачественных новообразованиях (например, раковой опухолью кишечника): к концу первого года после подтверждения диагноза "Критическая ишемия" (критическое снижение кровоснабжения) лишь 45 % пациентов имеют шанс сохранения конечности, а около 30 % продолжают жить после ампутации бедра или голени, а 25 % — умирают.
Тем не менее число больших ампутаций остаётся высоким, а их исходы — крайне тяжёлыми. Риск смертности в течение 30 дней после таких ампутаций составляет 4-30 %, а риск развития осложнений, таких как инфаркт миокарда, инсульт, инфекция, — 20-37 %. [1] [7] [10]
Реабилитация и протезирование
Трудности в реабилитации пациентов после ампутаций и протезирования у многих пожилых пациентов отрицательно влияют на отдалённые результаты и качество их жизни.
Период реабилитации зависит от объёма гангренозного поражения, качества заживления дефекта, сопутствующих соматических заболеваний, возраста пациента и его желания вернуться к полноценной жизни. Как правило, при успешном лечении и соблюдении всех рекомендаций врача длительность реабилитации составляет 3-6 месяцев.
На качество реабилитации также влияет питание. Поэтому в период восстановления рацион должен состоять из белковой и калорийной (но не жирной) пищи: из мяса индейки, рыбы, фасоли, творога и яиц. От жирной пищи во время реабилитации лучше отказаться.
Первичный протез подбирается после заживления раны культи. Затем, когда сформирована мышца культи, пациенту подбирают вторичный протез. Этим занимается врач-реабилитолог совместно с протезистом. [7] [8] [9]
Профилактика
Для предупреждения развития гангрены у предрасположенных к этому людей (например, лиц с сахарным диабетом, атеросклерозом), важно соблюдать меры профилактики:
- отказ от курения — эта пагубная привычка может привести к ухудшению кровообращения и закупорке сосудов;
- контроль уровня сахара в крови;
- проверка тела на наличие повреждений, их лечение и ежедневное наблюдение за их заживлением;
- незлоупотребление алкоголем.
Также для профилактики гангрены нужно избегать обморожений и иных внешних причин образования некроза.
Для цитирования: Дибиров М.Д., Черкезов Д.И., Манушарова Р.А. Современные возможности консервативного и хирургического методов лечения гнойно– некротических поражений стоп у больных сахарным диабетом. РМЖ. 2005;28:1915.
При сахарном диабете малый очаг инфекции вызывает значительную гангрену стопы из–за тромбоза периферических и центральных сосудов пальцев. У 35–40% больных сахарным диабетом отмечается изолированная гангрена нескольких пальцев и у 20–25% – только одного пальца [1]. Гангрена стопы может быть сухой или с преобладанием анаэробно–неклостридиальной инфекции. У некоторых больных наблюдается некроз или гангрена отдельных участков кожи стопы или голени. Основной целью при лечении диабетической гангрены является сохранение участков влажного кожного некроза сухими. По мнению А.В. Покровского и соавт. и В.Н. Дан и соавт., консервативное лечение инфицированной диабетической стопы должно решать несколько принципиальных моментов:
– компенсация сахарного диабета – обязательная нормализация углеводного обмена;
– купирование явлений критической ишемии стопы; Работая школьным учителем, начал замечать, что меня привлекают молоденькие школьницы в форме. Постоянно пытался бороться со своими фантазиями, но они ставали все сильнее и сильее. Друг подсказал, что можно попробовать поэкспериментировать с ролевыми играми.
– подготовка микроциркуляторного русла пораженной конечности;
– профилактика инфекционных осложнений – определение вида и чувствительности флоры к антибактериальным препаратам.
Наиболее частыми и грозными осложнениями диабетической ангиопатии являются гнойно–некротические поражения нижних конечностей. При появлении гнойного очага быстро нарастает декомпенсация сахарного диабета, меняется иммунный статус, нарастает эндотоксикоз. Эти изменения, в свою очередь, усугубляют ишемию тканей и возникает синдром «взаимного отягощения», В связи с этим принимаются срочные меры: хирургическая санация очага и коррекция нарушений гомеостаза.
В основу настоящего исследования положен анализ результатов комплексного обследования и лечения 118 больных с различной стадией ишемии нижних конечностей на почве диабетической макроангиопатии. Возраст больных – от 61 до 78 лет.
Вопросы компенсации кровообращения при хронических облитерирующих заболеваниях артерий нижних конечностей занимают главное место в лечении этой категории больных. Развитие регионарного ангиоспазма, нарушение реологических свойств крови, гиперлипидемия, гиперфибриногенемия, агрегация тромбоцитов способствуют прогрессированию декомпенсации периферического кровообращения.
Больные ишемией I и II стадий лечились амбулаторно. Основу лечения составляла комплексная терапия, направленная на снятие спазма и болей, на улучшение коллатерального кровообращения, микроциркуляции, реологических свойств крови и перевода заболевания из тяжелой стадии в более легкую. Профилактику дальнейшего развития (стабилизацию) проводили путем воздействия на общее состояние больного, активизацию его защитных и компенсаторных механизмов с обязательным устранением таких факторов риска, как курение, переохлаждение и нервные стрессы, нарушение диеты.
Для оценки эффективности различных методов лечения проводилось динамическое наблюдение за больными с применением следующих методов исследования: ангиография, ультразвуковая допплерография и ангиосканирование, исследование свертывающей системы и токсичности крови, изучение иммунного, липидного спектра крови, изучалось состояние магистрального и коллатерального кровотоков.
Как уже было отмечено выше, основным при лечении диабетической макроангиопатии является:
– Лечение сахарного диабета с целью профилактики прогрессирования, обострения и, в конечном итоге, стабилизации углеводного обмена.
– Снятие сосудистого спазма и стимуляция коллатерального кровообращения.
– Улучшение центральной и регионарной гемодинамики.
Чтобы предупредить незаконное использование торговой марки компании, нужно ее зарегистрировать в патентном бюро. – Улучшение обменных процессов и микроциркуляции в ишемизированных тканях.
– Создание умеренной гипокоагуляции и улучшение реологических свойств крови.
– Профилактика и лечение гнойно–некротических осложнений.
При лечении диабета принципиально важное значение имели следующие важные моменты – питание, физическая активность, лекарства и самоконтроль. Основными целями диеты при диабете были следующие:
1. Предотвращение постпрандиальной гипергликемии.
2. Коррекция сопутствующей дислипидемии.
3. Снижение риска поздних осложнений (атеросклероз, инфаркт миокарда, гангрена, ампутация).
4. Полноценное обеспечение организма необходимыми питательными веществами, микроэлементами, витаминами.
В период обострения больные госпитализировались для проведения стационарного лечения. При этом резко ограничивали физические нагрузки. В период ремиссии мы рекомендовали больным прогулки на свежем воздухе, на природе. Ходьба должна быть щадящей, с постепенным увеличением нагрузки и длины проходимой без боли дистанции. При перемежающейся хромоте следует останавливаться до появления болей в икроножных мышцах, делать отдых на 3–5 минут, а затем продолжать прогулку.
Выбор того или иного препарата при лечении диабетической макроангиопатии зависит от стадии ишемии, тяжести трофических нарушений, механизма действия препарата, совместимости, изменений в гомеостазе, вида и тяжести сопутствующей патологии и т.д., но наиболее часто мы использовали: спазмолитики, препараты, улучшающие тканевой метаболизм, гиполипидемические препараты, ангиопротекторы, дезагреганты, реологические препараты, антиоксиданты, иммунностимуляторы, антикоагулянты, препараты, улучшающие венозный и лимфатический отток.
Спазмолитики наиболее часто использовались при ишемии I и II стадий конечности. Особенно они эффективны при преобладании спастического компонента.
Активаторы клеточного метаболизма. Препараты этой группы способствуют улучшению энергетических процессов на уровне клеток, повышают активность АТФ, стимулируют процессы заживления ран.
Гиполипидемические препараты. При длительном применении в сочетании с диетой они эффективно снижают содержание в крови холестерина и липопротеидов низкой плотности, стабилизируют липидный обмен и препятствуют прогрессированию заболевания.
Ангиопротекторы. Препараты этой группы, воздействуя на сосудистые стенки (эндотелий), улучшают их растяжимость, макро– и микроциркуляцию в тканях.
Дезагреганты.
Реологические препараты – улучшают реологические свойства крови, снижают ее вязкость, усиливают «текучесть», повышают деформируемость эритроцитов, отдачу клеткам кислорода и этим уменьшает гипоксию тканей.
Антиоксиданты – группа препаратов, которые подавляют перекисное окисление липидов. Продукты перекисного окисления липидов – альдегиды и свободные радикалы, которые при ишемии в больших количествах накапливаются в тканях и «вымываются» в кровь, вызывая адгезию и агрегацию тромбов, повреждение эндотелия, тромбозы и эндотоксикоз. К этой группе препаратов относятся: витамины Е, С, глутаминовая кислота, солкосерил, липостабил и др.
Иммуностимуляторы – наиболее часто использовались Т–активин, левомизоль, ликопид, лейкинферон, пентоглобин, гипериммунная плазма и др.
Антикоагулянты прямого и непрямого действия. Препараты, улучшающие венозный и лимфатический отток из конечности, применяются при отеке тканей, венозном застое, лимфостазе, которые часто наблюдаются при диабетической ангиопатии.
В зависимости от стадии ишемии и поставленной цели мы применяли 2–3 препарата разных лекарственных групп, а при повторных курсах назначали препараты других лекарственных групп. Наиболее часто у больных I, II и III стадии ишемии применяли сочетание следующих препаратов: папаверин, ацетилсалициловая кислота, иммунофан; тиклопидин, мексидол, симвастатин, пентоксифиллин, никошпан, доксиум; сулодексид, витамин Е, ликопид; ксантинола никотинат, фенилин, эндотелон.
При более тяжелых стадиях ишемии (III, IV) назначали внутривенные вливания следующего состава: реополиглюкина 400,0; 4–6 мл никотиновой кислоты; 5–10 мл пентоксифиллина; 1–2 мл гепарина. Такие вливания продолжали в течение 10–15 суток. Эффективными оказались внутривенные вливания солкосерила, актовегина в количестве 10–15 мл и простагландина Е1 по 40 мкг 2 ампулы в 200–250 мл физиологического раствора 2 раза в сутки в течение 10–15 дней.
В начальных стадиях макроангиопатии и в стадии ремиссии патологического процесса назначались физиотерапевтические процедуры. Наиболее эффективными из них оказались импульсные токи, магнитотерапия, лазеротерапия, диадинамические токи, которые назначались на поясничную область и по ходу сосудисто–нервного пучка на бедре и голени.
При некротических язвах проводились мероприятия, направленные на улучшение общего состояния больного, отграничение некротизированного участка от жизнеспособных тканей, улучшение кровообращения, удаление омертвевших тканей, профилактику и лечение восходящей инфекции. При влажной гангрене, с целью перевода ее в сухую, назначали антибиотики, диуретики, УФО. Некротизированные пальцы закрывали марлевой салфеткой, пропитанной 3–5% йодной настойкой, 10% раствором марганцевокислого калия, камфорным спиртом, ксероформом, настойкой календулы, 70%–ным спиртовым раствором. При быстро прогрессирующей влажной гангрене, с переходом ее на тыльную поверхность стопы или голень (особенно при выраженной интоксикации) ставился вопрос об ампутации на уровне бедра или верхней трети голени.
У больных с сухой гангреной основные мероприятия были направлены на мумификацию тканей. В этих случаях применение влажных повязок и мазей противопоказано. К пораженному участку обеспечивали доступ кислорода. Несколько раз в день область некроза обрабатывалась 70% спиртовым раствором, 3–5% йодной настойкой, настойкой бриллиантовой зелени и календулы. Быстрая мумификация и демаркация наступала при обработке места некроза 5–10% раствором марганцевокислого калия. При благоприятном течении происходило самостоятельное отторжение мумифицированного участка или производили бескровную некрэктомию по демаркационной линии.
При некрозах и язвах до очищения от гнойно–некротических тканей, перевязки проводили 1–2 раза в сутки с использованием тканевого сорбента «АУТ–М» и др.
После удаления некротических тканей рану промывали 3% раствором перекиси водорода, раствором фурацилина и накладывали повязки с протеолитическими ферментами (трипсин, химотрипсин, рибонуклеаза и др.) с водорастворимой мазью. Во время перевязок при хорошем кровоснабжении рану облучали эритемными дозами ультрафиолетовых лучей. При появлении грануляций для ускорения очищения раны проводили перевязки с ируксоловой мазью, соком каланхое, солкосериловым желе, мазью календулы. После очищения раны (язвы) и при хорошей грануляции проводили перевязки через день с использованием 10% метилурациловой мази, шиповникового (облепихового) масла, спермацетовой мази, солкосериловой мази, ванилина левомеколевой мази и т.д.
Успех в лечении трофических нарушений может быть достигнут только при условии улучшения кровообращения в конечности.
Лечение гнойно–некротических осложнений при диабетической макроангиопатии можно разделить на три этапа.
I этап включает:
1. Ликвидацию остроты гнойно–некротического процесса:
а) вскрытие и дренирование флегмон;
б) широкая некрэктомия;
в) перевод влажной гангрены в сухую;
г) достижение четкого демаркационного вала.
2. Борьбу с эндотоксикозом.
3. Нормализацию углеводного, белкового, жирового и вводно–электролитного обменов.
4 Восстановление иммунного статуса.
5. Улучшение микроциркуляции.
II этап включает восстановление или улучшение кровообращения.
III этап включает закрытие дефекта тканей после некрэктомии и восстановление функции конечности.
С соблюдением этих принципов нами в течение последних 5 лет пролечено 118 больных с гнойно–некротическими поражениями на стопе и голени. Соотношение мужчин и женщин было примерно одинаковым. Средний возраст больных – 67 лет.
Распределение больных по виду гнойно–некротического процесса представлены в таблице.
После клинического, ультразвукового и ангиографического обследования при диабетической макроангиопатии выявлена следующая локализация окклюзии:
– аорта – 12 (10%),
– подвздошные артерии – 24 (20%),
– бедренные артерии – 31 (26%),
– подколенная и берцовые артерии – 27 (23%),
– многоэтажные поражения – 25 (21%).
Таким образом, по представленному материалу только у 56% больных были «благоприятные» анатомические условия для выполнения реконструктивных операций.
Выполнены следующие операции:
Аорто–подвздошный сегмент
Аорто–бедренное бифуркационное шунтирование 16
Подвздошно–бедренное шунтирование 20
Экстраанатомическое шунтирование 20
Подключично–бедренное 8
Бедренно–бедренное 12
Бедренно–подколенной сегмент
Бедренно–проксимально–подколенное шунтирование 36
Бедренно–дистально–подколенное шунтирование 38
Подколенно–берцовый сегмент
Поясничная симпатэктомия 34
Роторная остеотрепанация 10
В результате операций у подавляющего большинства больных удалось спасти конечности.
Следует отметить, что без восстановления магистрального кровотока и улучшения микроциркуляции при гнойно–некротических осложнениях диабетической макроангиопатии выполнение этапных некрэктомий обречено на неудачу и большую летальность.
Основными причинами смерти при этом являются:
1. Полиорганная недостаточность на фоне тяжелого эндотоксикоза.
2. Сепсис.
Часто на фоне диабетической макроангиопатии жизнеспособность стопы оценивается неверно, и после выполнения этапных некрэктомий на стопе и нарушения демаркации воспалительно–некротический процесс прогрессирует в проксимальном направлении и начинается полиорганная недостаточность на фоне хронического эндотоксикоза.
Высокая ампутация, выполненная как операция отчаяния, для спасения жизни больного, усугубляет полиорганную недостаточность. Рана культи бедра при этом вторично инфицируется анаэробами, развивается септический шок с последующим летальным исходом.
Таким образом, при диабетической макроангиопатии с ишемией I–II А стадий применяется медикаментозная терапия на фоне диеты и физиотерапии.
При ишемии II–Б, III и IV стадий ставятся показания к оперативному лечению, а после ангиографии решается вопрос выбора вида оперативного лечения. При поражениях артерий голени и стопы, проходимой бедренной артерии и при плохом дистальном оттоке производится поясничная симпатэктомия. При окклюзии подвздошных и бедренных артерий выполняются реконструктивные операции.
При ишемии III–IV стадий наряду с проведением вышеуказанной терапии, при дистальных окклюзиях, эффективна внутриартериальная терапия с целью быстрейшего купирования, стихания отграничения воспалительно–некротических изменений и перевода влажной гангрены в сухую.
Местная терапия язвенных дефектов проводится согласно общепринятым правилам.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
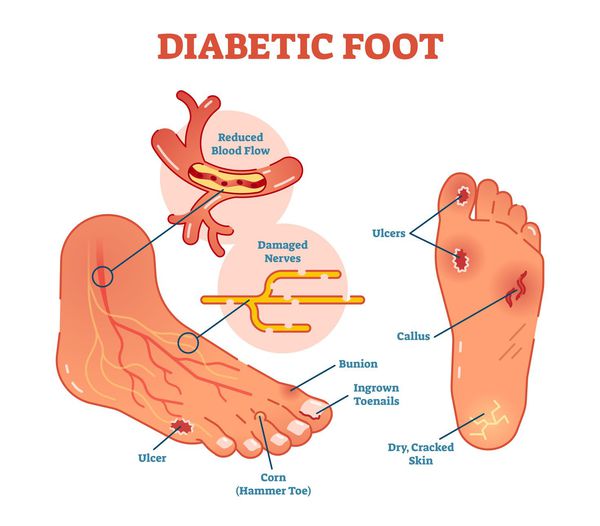
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
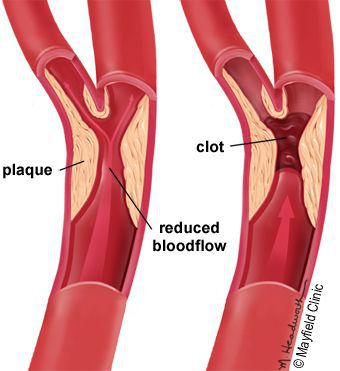
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
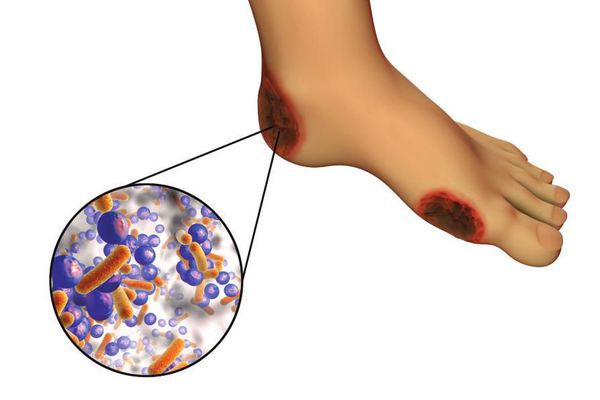
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
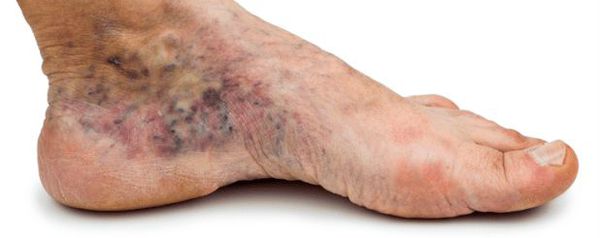
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
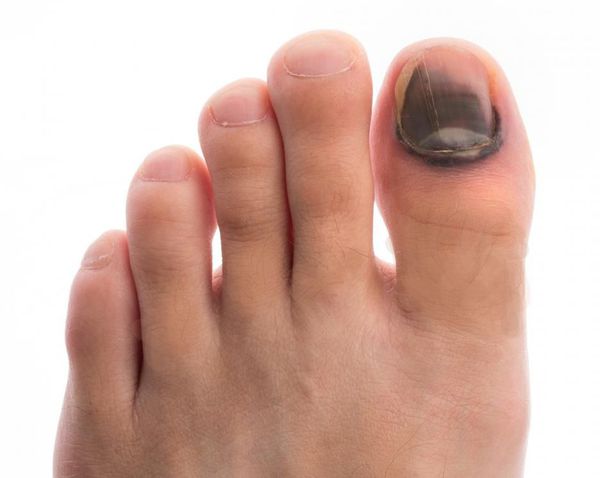
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
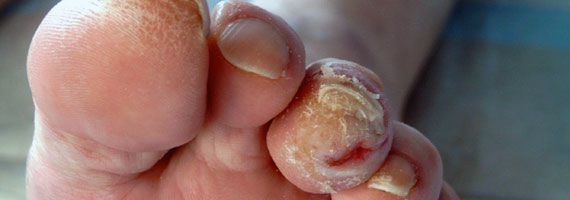
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
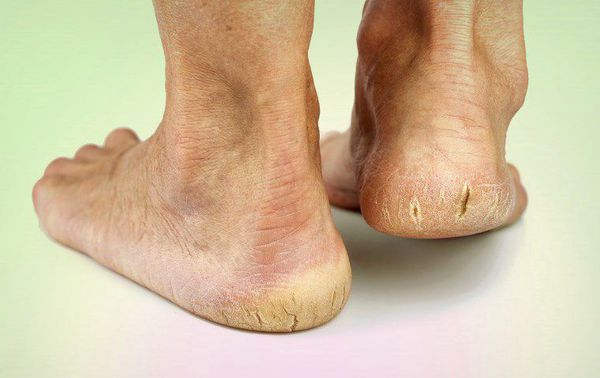
- трофические язвы, длительно не заживающие на стопах.
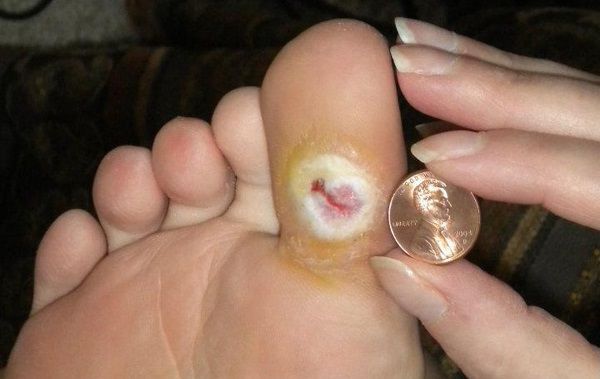
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
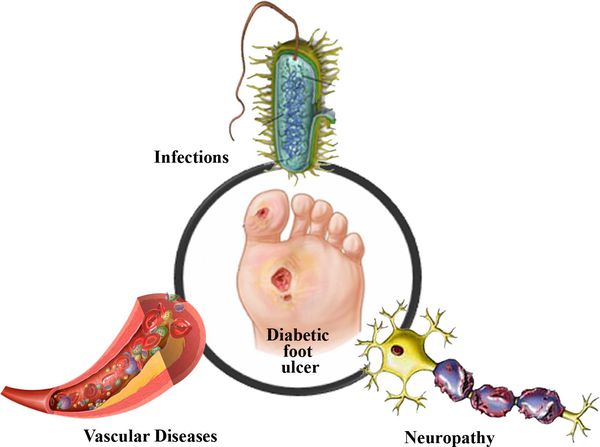
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
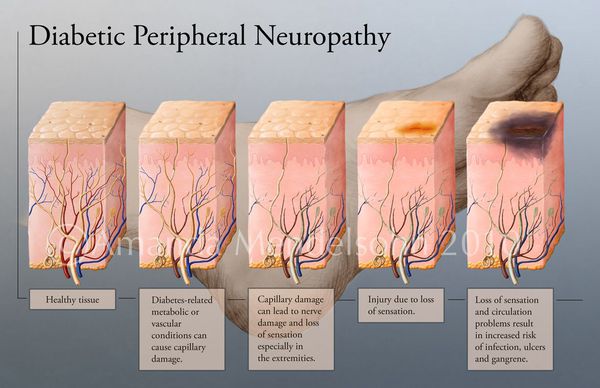
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
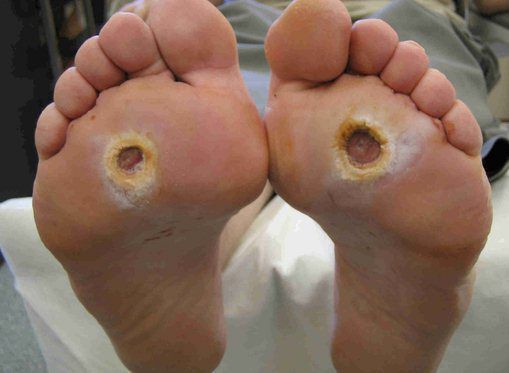
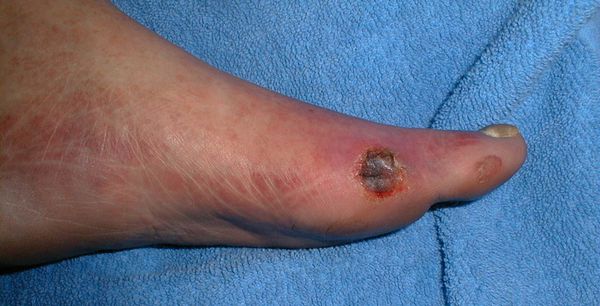
Классификация Вагнера
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
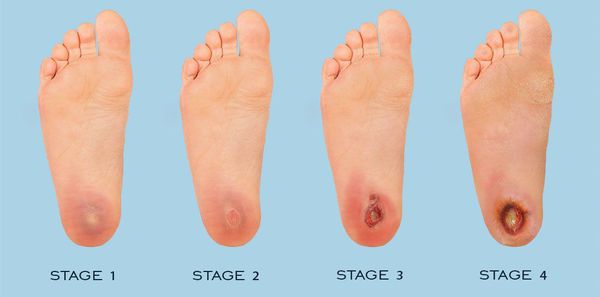
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Что такое гангрена влажная? Причины возникновения, диагностику и методы лечения разберем в статье доктора Азатяна Кярама Арутюновича, сосудистого хирурга со стажем в 7 лет.
Над статьей доктора Азатяна Кярама Арутюновича работали литературный редактор Маргарита Тихонова , научный редактор Вячеслав Подольский и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Влажная гангрена — это процесс омертвения ткани, органа или части тела, вызванный нарушением кровообращения из-за травм или патологий сосудов. Выражается в побледнении кожи, появлении длительно заживающих язв и др. Отличается обильным отделяемым из раны и отёком органа или конечности.
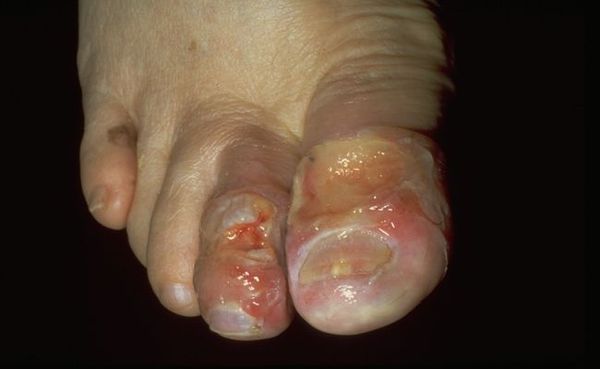
По причине возникновения патологию разделяют на две группы:
- возникшую от внутренних причин (заболеваний сосудов);
- возникшую в результате внешнего воздействия (травмы, ранения, инфекции, ожогов или обморожения).
Механизм развития гангрены связан с острой ишемией — нарушением оттока крови и/или лимфы. Это может произойти при механическом сдавлении сосудов и воспалении мягких тканей, лёгких, кишечника, кожи, матки или молочной железы. Однако основной причиной влажной гангрены является флеботромбоз — закупорка венозной системы.
Тромбоз возникает при застое крови, повреждении внутреннего слоя сосуда, тромбофилии (повышенной свёртываемости крови), сепсисе или при сочетании этих причин.
Ключевую роль в формировании тромба играет активное свёртывание крови. В ходе этого процесса образуется белок фибрин, который становится "каркасом" для строительства тромба [3] .
Развитию влажной гангрены способствуют гнилостные микроорганизмы, разлагающие и разжижающие мёртвую ткань. К таким бактериям относят анаэробы, бактероиды, дизентерийную амёбу, фузиформные бактерии, палочку путрификус, палочку спорогенес и др. Такая гангрена встречается в тканях и органах с большим содержанием крови, лимфы и тканевой жидкости [11] .
К другим факторам риска, способствующим образованию влажной гангрены, относят:
-
; ;
- декомпенсацию сахарного диабета (повышение уровня глюкозы в крови, не поддающееся коррекции);
- эндокринные и онкозаболевания; ;
- хронические заболевания вен (например, варикоз, сосудистые звёздочки, венозная мальформация);
- снижение иммунитета [11][13] .
Ежегодно острая ишемия нижних конечностей, как основная причина гангрены, развивается у 140 млн человек в мире [17] . Среди женщин такой диагноз встречается в 2 раза реже, чем среди мужчин. Причём чаще этот диагноз устанавливают мужчинам 60-64 лет и женщинам 80-84 лет. 25 % таких пациентов проводится ампутация ноги, 25 % умирают, а у оставшихся 50 % в процесс вовлекается вторая нога [12] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы влажной гангрены
Симптомы причинной болезни всегда предшествуют признакам гангрены.
Проявления тромбоза, как основной причины влажной гангрены, зависят от места расположения тромба, длительности болезни, характера и распространённости поражения венозного русла. Чаще тромб образуется в глубоких венах конечностей.
На начальных этапах тромбоза нижних конечностей симптоматика бывает стёртой или вообще не проявляется. К явным признакам болезни относят:
- отёк конечности или её части;
- синюшность кожи и выраженность подкожных вен;
- распирающую боль в ноге;
- боль по ходу магистральных сосудов [3] .
Отличительные признаки тромбоза глубоких вен верхних конечностей включают отёк руки, лица и шеи.
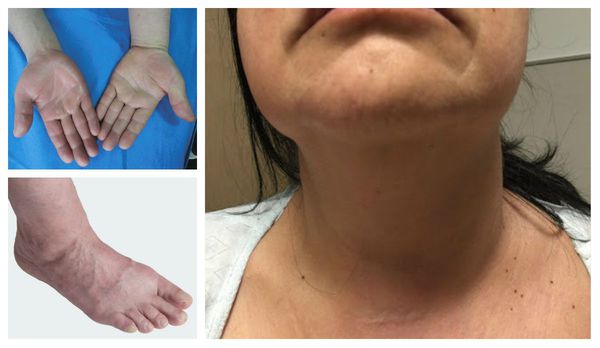
Характерные симптомы влажной гангрены:
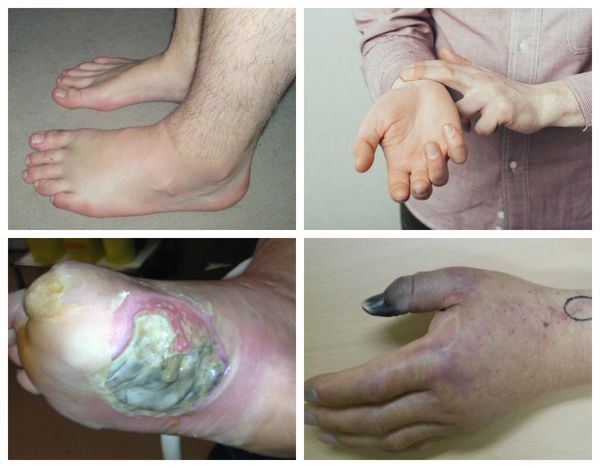
Патогенез влажной гангрены
Жизнеспособность органа и ткани зависит от работы сердечно-сосудистой системы: её основной, транспортной функции [5] .
Сердце и кровеносные сосуды снабжают организм кровью. С её притоком к органам и тканям поступает кислород и питательные вещества, а при оттоке кровь переносит углекислый газ и продукты метаболизма в лёгкие, почки, печень и другие органы-фильтры.
Нарушение транспортной функции ведёт к нарушениям микроциркуляции. Это происходит под воздействием одного или нескольких факторов. Среди них большое значение имеют:
- коллапс — внезапная сердечно-сосудистая недостаточность из-за отёка (избыточного накопления межтканевой жидкости и набухания эндотелия), повышенного слипания эритроцитов и тромбоцитов;
- образование лейкоцитарных пробок;
- повышение вязкости крови;
- формирование тромбов (сгустков крови) и эмболов (фрагментов тканей, бактерий и продуктов их жизнедеятельности);
- различные внешние факторы, например бактериальные токсины при инфицировании трофических язв.
Все эти изменения нарушают обмен веществ в органе или части тела, что ведёт к гибели клеток, некрозу (омертвению ткани) и гангрене [9] .
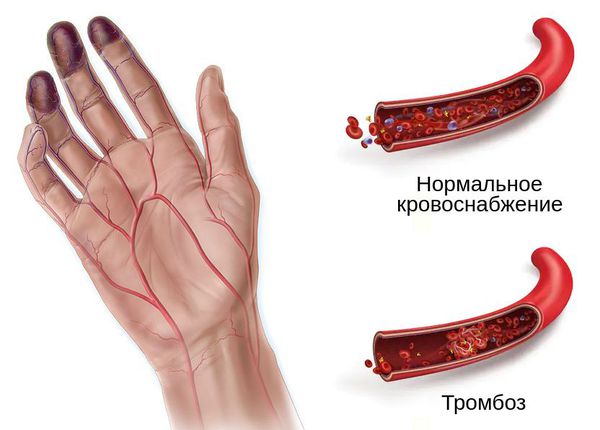
При влажной гангрене в основном нарушается механизм оттока, поэтому наблюдается отёк конечности или органа и обильные выделения из ран.
Механизм развития влажной гангрены примерно такой:
- после травмы ноги (или другого фактора) возникает тромбоз и закупорка глубоких вен, по которым кровь должна отводиться из конечности;
- возникает застой крови в ноге, отёк конечности, боль, цвет кожи или органа сначала становится бледным, потом тёмно-синим, появляются дефекты, из которых сочится жидкость, иногда присоединяется инфекция;
- отёк тканей сжимает и сдавливает артерии, нарушая приток крови и питательных компонентов;
- развивается некроз клеток, тканей и органов [6] .
Классификация и стадии развития влажной гангрены
Выделяют три типа гангрены:
-
— некроз ткани без выраженной инфекции и воспаления;
- влажная (гнилостная) — некроз с гнилостным распадом тканей;
- газовая — серьёзное осложнение, вызванное анаэробными микробами, с признаками сепсиса и интоксикации (высокой температурой и артериальным давлением, одышкой, слабостью, спутанностью сознания и др.) [2] .
Согласно классификации российского хирурга А. В. Покровского, влажная гангрена является последней стадией нарушения кровообращения конечности или органа [1] .
Фактически речь идёт о декомпенсации кровообращения, поскольку на IV стадии в поражённые ткани поступает мало кислорода, который может обеспечить нормальное потребление питательных веществ.
Классификация WIfI (Wound — язва, Ischemia — ишемия, foot Infection — инфицирование стопы) позволяет соотнести степень трофических нарушений и гангрены с ориентировочным объёмом лечения [7] .
Осложнения влажной гангрены
Влажная гангрена — опасное состояние, угрожающее жизни пациента. Промедление лечения чревато серьёзными осложнениями: увеличением раны, распространением инфекции, бактериальным эндокардитом, лёгочной недостаточностью и сепсисом.
Распространение гангрены сопровождается разрушением глубжележащих тканей. Токсины и вредные вещества, которые высвобождаются при распаде и некрозе, отравляют организм. Если процесс не остановить, пациент может лишиться конечности или органа, став инвалидом, или вовсе умереть [9] .
Тромбоз вен, как причина нарушения оттока крови, может стать причиной другого серьёзного осложнения — тромбоэмболии лёгочной артерии (ТЭЛА). Такое нарушение связано с миграцией тромба в систему лёгочных артерий. Из-за периодического изменения венозного оттока во время ходьбы, кашля или акта дефекации тромб может оторваться и закрыть просвет важных сосудов полностью или частично.
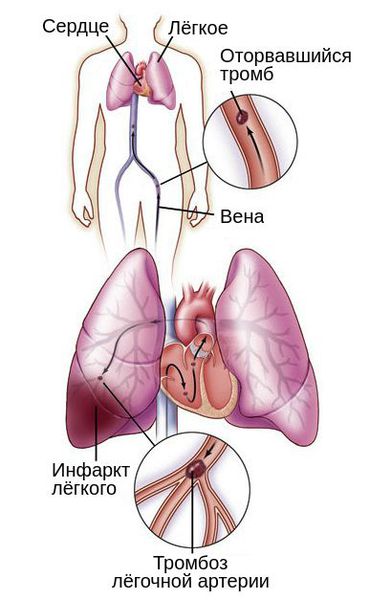
В зависимости от размера тромба закупориваются артерии различного диаметра: от сегментарных ветвей до лёгочного ствола. Тромбоз мелких веток обычно не приводит к расстройству кровообращения и дыхания, но может вызвать инфаркт участка лёгкого и пневмонию. Тромбоз лёгочного ствола заканчивается внезапной смертью.
Лёгочный инфаркт, который вызывает боль в груди, кашель, кровохарканье и образование жидкости в грудной клетке, развивается не всегда. Это осложнение относится к поздним проявлениям ТЭЛА и проявляется через несколько дней после дебюта болезни [3] .
Диагностика влажной гангрены
Диагноз влажной гангрены основывается на данных опроса, объективного осмотра, оценки распространённости процесса, состояния периферического кровотока и нервной передачи.
При опросе пациенты жалуются на длительно незаживающие раны стопы или голени с обильным выделением жидкости, образование волдырей с бурым или светлым содержимым и иногда неприятным запахом.
Важно уточнить, как давно возникли раны: они могут не заживать от нескольких недель до 2-6 лет. На скорость заживления влияют сопутствующие болезни: сердечная и дыхательная недостаточность, сахарный диабет, онкозаболевания и др. [10]
При осмотре врач обращает внимание на:
- состояние и цвет кожи (сухая или влажная, бледная, розовая или синюшная);
- объём конечностей (есть ли отёк);
- их температуру (холодные, тёплые или горячие);
- состояние ногтей — онихомикоз может являться дополнительным источником инфекции.
Периферическое кровоснабжение первично оценивается по пульсу: чем слабее удары, тем хуже состояние поражённой области.
Периферическая иннервация оценивается путём определения тактильной, вибрационной чувствительности и/или сухожильных рефлексов: чем слабее реакция пациента на раздражители, тем хуже прогноз для сохранения органа или конечности [10] .
О состоянии костных структур сложно судить без дополнительных методов исследования. Изначально можно определить только форму суставов, деформацию конечностей, объём движений и боль, возникающую в суставе.
Дополнительные методы исследования расположены в порядке значимости:
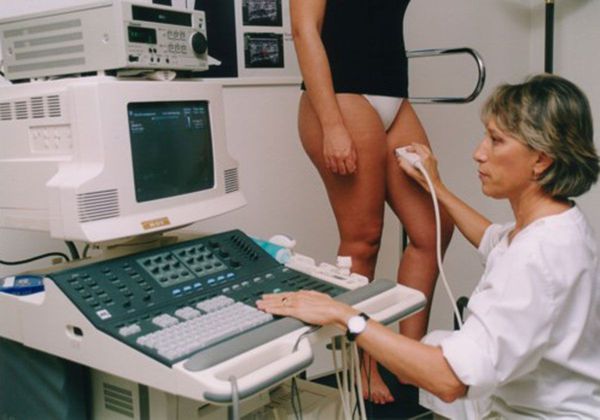
- УЗГД — ультразвуковое дуплексное сканирование артерий и вен. Безвредный метод диагностики. Позволяет выяснить, нарушено ли кровообращение в конечности или органе. Проводится в кабинете ультразвуковой диагностики. Во время процедуры пациент лежит на спине или стоит.
- Лабораторное обследование. С его помощью можно выявить системные заболевания, оценить общую тяжесть состояния и предполагаемый объём лечения. Для диагностики необходим клинический анализ крови, определение скорости оседания эритроцитов (СОЭ), развёрнутая коагулограмма (состояние свёртывающей системы крови), общий (клинический) анализ мочи и развёрнутый биохимический анализ крови. Для влажной гангрены характерны системные изменения: повышение СОЭ, лейкоцитов, D-димера и фибриногена, снижение АЧТВ, МНО, общего белка и т. д.
- Электрокардиограмма. Позволяет оценить состояние сердца. Проводится лёжа. На грудную клетку пациента накладываются специальные электроды, которые регистрируют электрическую активность сердечной мышцы — миокарда. Эта информация распечатывается на бумажной ленте в виде кардиограммы, отражающей работу сердца.
По данным этих исследований врач принимает решение о тактике лечения, его объёмах и необходимости других дополнительных методов исследования:
- МСКТ — мультиспиральная компьютерная томография. Может потребоваться для уточнения уровня и степени поражения сосудов при выявлении проблемы на УЗИ.
- Ангиография — определяет проводимость сосудов.
- Бактериологическое исследование раневой инфекции. Позволяет установить тип бактерий и их чувствительность к антибиотикам [10] .
- Рентгенография — оптимальный метод оценки состояния костей и суставов. С его помощью выявляются очаги разрушения [10] .
Дифференциальную диагностику влажной гангрены нужно проводить с другими состояниями:
- лимфатическим отёком и лимфедемой (слоновостью);
- хронической сердечной и почечной недостаточностью в стадии декомпенсации;
- острой печёночной недостаточностью и циррозом печени;
- липедемой ("жировым отёком").
Лечение влажной гангрены
Лечение влажной гангрены всегда комплексное. Оно состоит из ряда важнейших задач, которые формируются на этапах диагностики. По показаниям может потребоваться реваскуляризация — восстановление притока и оттока крови по артериям и венам. Выбор метода реваскуляризации зависит от типа сосудистой недостаточности — артериальной и/или венозной.
Одной из причин влажной гангрены является нарушение венозного оттока, а именно тромбоз глубоких вен конечности. Такая проблема чаще требует консервативной антикоагулянтной терапии — приёма таблеток, которые рассасывают тромб. Если причина в эмболизации артерий, восстановить кровоток позволяют реконструктивные операции:
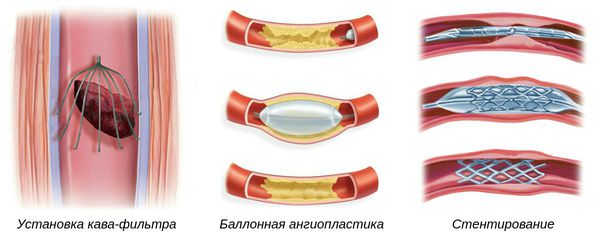
- Установка кава-фильтра — специальной системы, которая препятствует миграции тромбов из нижних конечностей к лёгким. Устанавливается в нижнюю полую вену.
- Баллонная ангиопластика — способ ликвидации суженных участков артерий, препятствующих нормальному току крови. Выполняется при помощи специальных систем.
- Стентирование — установка специальных имплантов (стентов) в область артерии, поражённой атеросклеротической бляшкой, чтобы восстановить её проходимость.
Такие операции выполняются под местной анестезией через прокол, т. е. малоинвазивным и малотравматичным способом [1] .
После восстановления кровообращения и купирования инфекционного процесса наступает восстановительный период. Он предполагает компрессионное лечение:
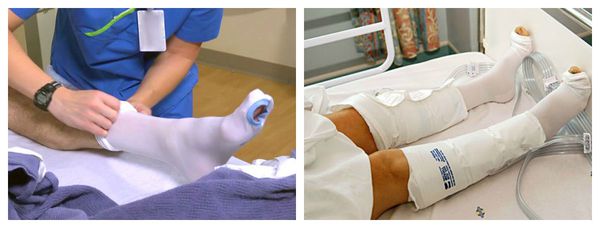
- Ношение трикотажа 2-3 класса компрессии в течение дня. Это могут быть бинты, чулки, перчатки, рукава и пр.
- Прерывистая пневмокомпрессия, или прессотерапия. Используется как противоотёчная терапия [3] . На пациента надеваются манжеты, в которые подаётся воздух. Манжеты постепенно нагнетают давление от периферии к центру, т. е. от пальцев стопы, усиливая отток лимфы.
Одновременно с перечисленными мерами проводится обработка раны. Она направлена на очищение и подготовку дефекта к заживлению.
Выбор метода обработки зависит от состояния раны и организма в целом. Возможны несколько вариантов:
- хирургический метод — иссечение омертвевших тканей;
- ферментный метод — наложение препаратов, расщепляющих омертвевшие ткани, например трипсина или химотрипсина;
- ультразвуковой метод — физический способ размельчения и удаления омертвевших тканей;
- комбинация нескольких методов очищения раны [10] .
При адекватной обработке и разгрузке поражённой конечности дефект начинает заживать в течение двух недель [10] .
Правильно выбрать повязку для раны — не менее важно. Чтобы поспособствовать заживлению, она должна отвечать четырём требованиям:
- поддерживать влажную среду в ране;
- контролировать объём воспалительного выпота;
- предотвращать повреждение краёв раны;
- хорошо фиксироваться, оставаться неподвижной.
Современные многокомпонентные повязки содержат все необходимые компоненты для заживления раны:
- гидрогели для создания оптимальной влажной среды на поверхности раны;
- альгинаты для устранения избыточной жидкости;
- гидроколлоиды для очищения раны от омертвевших тканей;
- ионы серебра для обеззараживания и т. д.
Для каждой стадии заживления раны существуют свои повязки. Они накладываются на 1-5 дней. На поверхности современных повязок имеются индикаторные метки, которые сигнализируют о том, что повязку пора сменить.
Прогноз. Профилактика
Если не лечить влажную гангрену или поздно обратиться к врачу, то в течение первого года 20 % больных умирают, 25 % пациентов проводится ампутация и лишь у 55 % больных есть шанс сохранить конечность или орган. Эти показатели отражают весь драматизм ситуации: угроза здоровью и жизни больных очень высока [8] .
Ампутация, как единственно возможный способ сохранения жизни пациента, показана при неэффективности комплексного лечения, увеличении раны, невозможности проведения операции, ухудшении состояния пациента и позднем обращении к врачу — развившейся гангрене.
Во избежание осложнений, связанных с ампутацией, операцию следует выполнять в два этапа:
- первичная ампутация — удаление омертвевших тканей, попытка восстановить кровоток и сохранить конечность;
- вторичная ампутация — проводится при неэффективности мероприятий по сохранению конечности и отсутствии положительной динамики: рана после первичной ампутации не заживает [9][14] .
При наличии гнойно-некротического очага и риске заражения крови его первичная санация должна быть выполнена до операции [10] .
Другие осложнения, связанные с лечением, возможны при критической ишемии конечности. Проводить хирургическую обработку раны в этом случае опасно: это может расширить зону некроза. Перед этим требуется провести реваскуляризацию конечности, например стентирование.
При реваскуляризации возможно развитие осложнения в виде нефропатии — нарушения работы почек. Особенно рискуют пациенты с генерализованным атеросклерозом, кальцификацией почечных артерий и хронической болезнью почек II стадии и выше [8] [15] [16] . Чтобы предупредить нефропатию, накануне и после операции пациентам из группы риска необходимо отменить метформин, петлевые диуретики и по каплям внутривенно ввести 1 л физраствора.
Профилактика влажной гангрены заключается в регулярном обследовании, контроле имеющихся заболеваний и раннем обращении к врачу при первых симптомах тромбоза или ишемии конечности. Даже небольшая на первый взгляд ранка может привести к утрате конечности.
При наследственной предрасположенности к варикозной болезни необходимо каждый год выполнять УЗИ вен нижних конечностей и консультироваться с флебологом. В профилактических целях врач может назначить ношение компрессионного белья: это позволит избежать образования тромбов и прогрессирования хронических заболеваний вен.
При сахарном диабете важно корректировать уровень глюкозы в крови, ежегодно выполнять УЗИ органов брюшной полости, артерий и вен нижних конечностей, а также правильно ухаживать за кожей ног:
Читайте также:

