Слущенный эпителий бронхов это
Обновлено: 28.04.2024
Авторы: Геппе Н.А. 1 , Озерская И.В. , Малявина У.С.
1 Клинический институт детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), Москва, Россия
Для цитирования: Геппе Н.А., Озерская И.В., Малявина У.С. Цилиарный эпителий при респираторных вирусных инфекциях у детей. Влияние лекарственных препаратов. РМЖ. 2012;24:1222.
Болезни органов дыхания относятся к числу наиболее распространенных заболеваний человека. Респираторные заболевания у детей составляют до 90% всех инфекционных болезней. Среди болезней органов дыхания львиная доля приходится на острые респираторные вирусные инфекции (ОРВИ). Наиболее высокие показатели заболеваемости отмечаются у детей раннего возраста. Дети младшего возраста в среднем болеют ОРВИ 6–8 раз в год, а 10–15% детей – не менее 12 раз в год. Высокие показатели заболеваемости ОРВИ в детском возрасте делают эту проблему крайне актуальной для педиатрии.
Таким образом, указанные изменения функции цилиарного эпителия могут поддерживать нарушения МЦК, что требует своевременной коррекции. Учитывая влияние компонентов препарата Аскорила (в частности, сальбутамола) на ЧБР цилиарного эпителия, а также влияние амброксола (как активного метаболита одного из компонентов препарата) на восстановление сурфактанта и реологию секрета дыхательных путей, можно предположить, что препарат может оказывать положительное действие на стабилизацию и восстановление МЦК при ОРВИ у детей.
Литература
1. Herzon F.S. Nasal ciliary structural pathology // Laryngoscope. 1983. Vol. 93(1). P.63–67.
2. Sleigh M.A. Movement and coordination of tracheal cilia and the relation of these to mucus transport //Cell. Motil. (Suppl.) 1982. Vol. 1. P.19–24.
3. Fawcett D.W., Porter K.R. A study of the fine structure of ciliated epithelia // J. Morphol. 1954. Vol. 94. P. 221–281.
4. Buchdahl R.M. et al. Ciliary abnormalities in respiratory disease //Archives of Disease in Childhood. 1988. Vol. 63. P. 238–243.
5. Bertrand B., Collet S., Eloy P. et al Secondary ciliary dyskinesia in upper respiratory tract //ActaOtorhinolaryngol. Belg. 2000. Vol. 54(3). P. 309–316.
6. Chilvers M.A., Rutman A., Callaghan C.O’. Functional analysis of cilia and ciliated epithelial ultrastructure in healthy children and young adults // Thorax. 2003. Vol. 58. P. 333–338.
7. Hermens W.A., Merkus F.W. The influence of drugs on nasal ciliary movement // Pharm. Res. 1987. Vol. 4(6). P. 445–449.
8. Stetinova V., Herout V., Kvetina J. In vitro and in vivo antioxidant activity of ambroxol // Clin. Exp. Med. 2004. Vol. 4(3). P. 152–158.
9. Fraschini F., Scaglione F., Scarpazza G. et al. Effect of mucolytic agent on the bioavailability of antibiotics in patients with chronic respiratory diseases // Cur. Ther. Res. 1988. Vol. 13 P. 734–742.
10. Sisson J.H., Yonkers A.J., Waldman R.H. Effects of guaifenesin on nasal mucociliary clearance and ciliary beat frequency in healthy volunteers // Chest. 1995. Vol.107(3). P. 747–751.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Изменения эпителия бронхов при бронхиальной астме.
Своеобразным вариантом эозинофильного воспаления является сочетание эозинофильного или эозинофильно-нейтрофильного воспаления с появлением в бронхиальном смыве измененного эпителия бронхов. Эпителий бронхов - одна из главных мишеней для атаки активных клеток воспаления у больных бронхиальной астмой, и изменения эпителия играют важную роль в патогенезе этого заболевания. Нами с помощью COMOD-технологии выделена группа больных с эозинофильно-нейтрофильным воспалением и наличием измененного эпителия бронхов. В эту группу входили больные бронхиальной астмой средней степени тяжести и тяжелой, у которых выявлялась колонизация бронхов непатогенной и условно-патогенной микрофлорой, вирусная инфекция, иммунные нарушения (определялись в высоком титре циркулирующие иммунные комплексы - ЦИК).
Обнаружена достоверная связь между появлением в бронхиальном смыве измененного бронхиального эпителия и показателями, характеризующими преимущественно отечный механизм нарушения бронхиальной проходимости: достоверные изменения ОФВ, после подкожной инъекции 1 мл 0,1% раствора адреналина, но не после ингаляции беротека. Важно также отметить, что у выделенных COMOD-технологией в эту группу больных преобладало нарушение бронхиальной проходимости на уровне дистальных бронхов: преимущественное снижение мгновенных скоростей воздушного потока при выдохе 50% и 75% ЖЕЛ, но не максимальной скорости воздушного потока на выдохе первой четверти ФЖЕЛ. В генезе нарушения проходимости на уровне дистальных бронхов существенную роль может играть отечный механизм. Такой механизм описан недавно, в частности у больных аспириновой бронхиальной астмы.
У больных описываемой группы выявлены нарушения обмена ККС, вероятно, связанные с вирусной инфекцией, и также, способствующие отечному механизму бронхообструкции и нарушениям микроциркуляции. У этих же больных найдено повышение уровня свободного серотонина в периферической крови, что может свидетельствовать о нарушении его инактивации эндотелием легочных сосудов и считаться маркером повреждения легочного эндотелия, наряду с таким общеизвестным показателем повреждения сосудистого эндотелия, как повышение активности фактора Виллебранда, нередко выявляемое у больных бронхиальной астмой. Повреждение эндотелия в этой группе больных может быть связано с фиксацией на нем ЦИК, о повышении которых говорилось ранее, и по крайней мере у некоторых больных нельзя исключить иммунный васкулит легочных микрососудов.
Найденные изменения укладываются в предложенные концептуальные модели нарушения микроциркуляции и иммунного васкулита у больных бронхиальной астмой и находятся в русле работ последних лет, в которых состоянию сосудов легких уделяется особое внимание, о чем писалось ранее. Таким образом, выделенная нами группа больных с эозинофильно-нейтрофильным воспалением в сочетании с появлением в бронхиальном смыве измененного эпителия бронхов относится к инфекционно-зависимому и аутоиммунному клинико-патогенетическим вариантам бронхиальной астмы. Не исключается, что выявленная у этих больных колонизация бронхов различной микрофлорой, соответствующая полученным в последнее время данным о высокой чувствительности к бактериальной адгезии вновь растущих покровых клеток, закрывающих повреждения эпителия, является толчком к развитию аутоиммунного процесса, учитывая способность некоторых бактерий и вирусов нарушать толерантность к собственным антигенам хозяина.
У некоторых больных бронхиальной астмой выделено эозинофильно-мононуклеарное воспаление: эозинофильно-макрофагальное и эозинофильно-моноцитарное (частота 0,36-0,32 среди эозинофильных вариантов воспаления в зависимости от исходной базы данных). Ранее было указано, что у многих больных бронхиальной астмой выявляется "макрофагальный дефицит"- низкое содержание макрофагов среди клеток бронхиального смыва, что может рассматриваться как проявление снижения местной защитной реакции, исходя их сложных кооперативных функций макрофагов в регуляции иммунного воспаления.
Вместе с тем, в условиях патологии, в частности при БА, альвеолярные макрофаги, составляющие 90% всех клеток дыхательных путей (около 500 млн. клеток), могут играть первичную роль в патогенезе болезни, поскольку имеют рецепторы к IgE и выделяют различные медиаторы воспаления. Д,Н. Маянский считает, что аллергическое воспалениек при бронхиальной астме проявляется преимущественно как вариант мононуклеарно-ин-фильтративного воспаления, и ведущую роль в его патогенезе играют фагоциты - эффекторы воспалительной реакции. И.Г. Даниляк указывает на важную патогенетическую роль свободных радикалов, выделяемых фагоцитами, в частности альвеолярными макрофагами, и говорит о существовании "фагоцитарно-свободнорадикального" варианта бронхиальной астмы. Другие авторы подчеркивают, что свободные радикалы после антигенного воздействия выделяют преимущественно макрофаги, а не нейтрофилы.
Увеличение содержания в бронхиальвеолярном лаваже мононуклеаров, прежде всего, лимфоцитов, по данным многих авторов, коррелирует с тяжестью течения бронхиальной астмы. Интерлейкины, выделяющиеся в зоне воспаления, и в частности ИЛ-2, связываясь с поверхностными клеточными рецепторами (IL-2R), вызывают клональную экспансию антигенстимулированных Т-лимфоцитов и играют ключевую роль в активации иммунной системы и в трансформации острого иммунного воспаления в хроническое. Л.К. Романова и соавт. выделяет особый лимфоцитар-ный вариант воспаления бронхов при бронхиальной астме. По мнению Г.Б. Федосеева и соавт. лимфоциты характеризуют хронический компонент воспаления при бронхиальной астме. Увеличение количества лимфоцитов в просвете бронхов у больных бронхиальной астмой часто сочетается с увеличением количества эозинофилов, при этом лимфоциты продуцируют провоспалительные кинины и нарушено соотношение Т и В-лимфоцитов, причем количество В-лимфоцитов увеличивается, а Т-лимфоцитов снижается.
Мононуклеары, в том числе лимфоциты, впервые появляются через 24 часа после начальной дегрануляции тучных клеток под воздействием аллергена и, следовательно, характеризуют позднюю реакцию при бронхиальной астме. При поздней аллергической реакции особенно важно взаимодействие эозинофилов и лимфоцитов.
- Вернуться в оглавление раздела "Пульмонология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Роль эпителия бронхов при воспалении.
Этот фрагмент не претендует на полноту, поскольку некоторые вопросы, рассматриваемые в других разделах сайта, в частности, роль лимфоцитов в воспалении, описывается в статьях, посвященных роли иммунной системы.
Эпителий бронхов. Большую роль в развитии воспаления бронхов играет повреждение эпителия. Функции его многообразны: во-первых, в эпителии находятся наиболее эффективные антиген-презентирующие дендритные клетки, которые после поглощения антигена мигрируют в региональные лимфоузлы, где контактируют со специфическими Т-лимфоцитами; во-вторых, клетки эпителия экспрессируют разнообразные рецепторы, благодаря которым с эпителиоцитами связываются различные БАВ, клетки воспаления, бактерии и; в-третьих, эпителиоциты активно продуцируют медиаторы, в частности, провоспалительные цитокины, поддерживающие хроническое воспаление.
Велика роль эпителия в регуляции экссудации плазмы в просвет бронхов: клетки эпителия, как и другие типы клеток, продуцируют вазоактивные медиаторы экссудации, включая различные лейкотриены (ЛТ), прежде всего ЛТД4, и фактор активации тромбоцитов (ФАТ), причем, первоначальная экссудация имеет защитное действие, поскольку плазма образует гель, который защищает обнаженную мембрану, поэтому имеется связь между степенью повреждения эпителия (аллергеном, поллютантом, бактерией) и выраженностью плазменной экссудации.
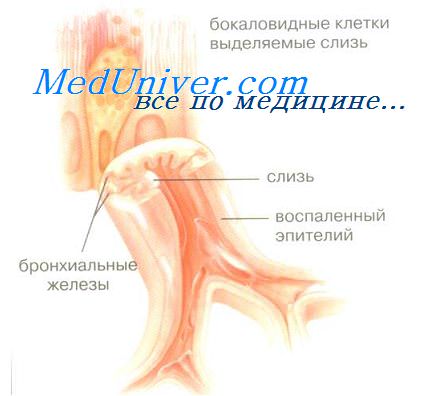
Эпителий продуцирует много провоспалительных цитокинов благодаря выраженной метаболической активности, в частности, метаболит арахидоновой кислоты 15-НЕТЕ (15-гидроксиейкозатетраеновая кислота), который стимулирует продукцию слизи и активирует 5-липоксигеназный путь обмена в тучных клетках, простагландины Е, и F2a, GM-CSP (гранулоцитарно-макрофагаяьный колониестимулируюший фактор), активирующий альвеолярные макрофаги, гранулоциты и базофилы, GCSP (гранулоцитарный колониестимулирующий фактор), интерлейкины (ИЛ), в частности ИЛ-1, ИЛ-6 и ИЛ-8 - хемоаттрактант и активатор эозинофилов и нейтрофилов. Одним из главных хемоаттрактантов, выделяемых эпителием со специфическим привлечением моноцитов - МСР-1 (моноцитарный хемоаттрактантный пептид-1). Эпителий бронхов выделяет также другие медиаторы воспаления: эндотелии-1,- активный вазо- и бронхоконстриктор и активатор фибробластов, цитокины группы RANTES из подсемейства полипептидов В или "С-С" (Regulated on Activation, Normal T-cell Expressed and Secreted), привлекающие эозинофилы, различные факторы роста (PDGE - пластиночный фактор роста, BFGF - основной фактор роста фибробластов, IGE - инсулиноподобный фактор роста),- все из них способны принимать участие в ремоделировании дыхательных путей.
В последнее время большое внимание уделяется выделению эпителием бронхов окиси азота (N0), которая обладает вазо- и бронходилатирующим действием и ее концентрация по-разному изменяется при различных легочных болезнях.
Важным в генезе воспаления является экспрессия различных молекул, прежде всего, молекул адгезии ICAM-I (intercellular adhesion molecnle-I), необходимая для транспорта нейтрофилов и эозинофилов через слизистую в просвет дыхательных путей, а также рецепторов автономной нервной системы, что указывает на влияние автономной нервной системы на функции эпителия и формирование нейрогенного воспаления. Помимо адренорецепторов, мускариновых холинорецепторов (в основном, М3), в последнее время интенсивно изучаются VIP-рецепторы (рецепторы вазоинтестинального пептида), возбудитель которых - VIP -сходен по действию с агонистами и дефицит которого может играть важную роль в патогенезе БА; тахикининовые рецепторы, которые с высокой плотностью находятся на эпителии и опосредуют действие мощных провоспалительных медиаторов - вещества П и нейрокинина А; а также большое количество медиаторных рецепторов, посредством которых различные БАВ модулируют метаболическую активность эпителиоцитов, стимулируют экспрессию других видов рецепторов или, наоборот, тормозят ее.
Таким образом, эпителиоциты действуют как трансдукторы между различными сигналами, возникающими в просвете бронха и на поверхности эпителия, и воспалительными событиями в стенке бронха, причем в нормальных условиях эпителий поддерживает баланс между про- и противовоспалительными эффектами.
При нарушении эпителиального покрова этот баланс нарушается в пользу преобладания провоспалительных эффектов, в просвет бронхов выходят клетки воспаления и жидкая часть плазмы, и при определенных условиях процесс может принять хроническое персистирующее течение.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Бронхоэктазы — это сегментарные расширения просветов бронхов, обусловленные деструкцией или нарушением нервно-мышечного тонуса их стенок вследствие воспаления, дистрофии, склероза или гипоплазии структурных элементов бронхов (И. К. Есипова, 1976). Важно
Бронхоэктазы — это сегментарные расширения просветов бронхов, обусловленные деструкцией или нарушением нервно-мышечного тонуса их стенок вследствие воспаления, дистрофии, склероза или гипоплазии структурных элементов бронхов (И. К. Есипова, 1976).
Важно разграничивать бронхоэктатическую болезнь и вторичные бронхоэктазы вследствие абсцесса легкого, туберкулезной каверны, пневмонии, инородных тел, бронхита. Наиболее обоснованным можно считать взгляд на бронхоэктатическую болезнь как на регионарное расширение бронхов обычно IV—VI порядков, превышающее просвет нормального в 2 раза и более, возникающее, как правило, в возрасте от 3 до 18 лет и проявляющееся хроническим, преимущественно эндобронхиальным нагноением.
В первые десятилетия ХХ в. было распространено мнение о преимущественно врожденной природе бронхоэктазов (F. Sauerbruch, 1927). Однако впоследствии было доказано (А. И. Струков, И. М. Кодолова, 1970), что в большинстве случаев отмечается постнатальное нарушение дифференцировки бронхиального дерева под влиянием бронхолегочной инфекции, после перенесенных в раннем детском возрасте кори, коклюша, гриппа, острых пневмоний. Подтверждением тому послужил факт расположения бронхоэктазов в тех же сегментах, что при острых пневмониях у детей.
Установлена последовательность патологического процесса — от катарального бронхита к панбронхиту, далее к перибронхиту с перибронхиальной пневмонией, затем — к деформирующему бронхиту с разрушением эластических и мышечных волокон и, наконец, к бронхоэктазам.
На основании классификации В. Р. Ермолаева (1965) различают следующие стадии заболевания: 1) легкую; 2) выраженную; 3) тяжелую; 4) осложненную. По распространенности процесса выделяют одно- и двусторонние бронхоэктазии с указанием точной локализации по сегментам. В зависимости от состояния больного, в момент обследования должна указываться фаза процесса: обострения или ремиссии. В зависимости от формы расширения бронхов, различают бронхоэктазии: а) цилиндрические; б) мешотчатые; в) веретенообразные; г) смешанные. Между ними существует много переходных форм. Кроме того, бронхоэктазии делят на ателектатические и не связанные с ателектазом, что, несомненно, удобно в практическом отношении.
Основным симптомом бронхоэктатической болезни является кашель с выделением мокроты, наиболее выраженный в утренние часы. При цилиндрических бронхоэктазах мокрота обычно отходит без затруднений, тогда как при мешотчатых и веретенообразных — нередко с трудом. При сухих бронхоэктазах, описанных С. А. Рейнбергом (1924), кашель и мокрота отсутствуют (эти бронхоэктазы проявляются лишь кровотечением, иногда угрожающим).
В период ремиссии количество слизисто-гнойной мокроты не превышает в среднем 30 мл/сут. При обострении заболевания в связи с острыми респираторными инфекциями или после переохлаждения кашель усиливается, количество мокроты увеличивается до 300 мл/сут и более, иногда достигая 1 л, она приобретает гнойный характер. Гнилостный запах мокроты не характерен для бронхоэктатической болезни и появляется лишь при абсцедировании.
Кровохарканье, по данным различных авторов, встречается у 25—34% больных. Чаще всего отмечаются прожилки крови в мокроте, но иногда возникает профузное легочное кровотечение. Считают, что источником кровохарканья и кровотечения становятся бронхиальные артерии (особенно артерии среднедолевого бронха). Кровохарканье наблюдается главным образом весной и осенью, что связывают с обострением воспалительного процесса (Д. Д. Яблоков, 1971). Обильные кровотечения могут начаться после тяжелой физической нагрузки или перегрева (А. Я. Цигельник, 1968).
Одышка и синдром бронхиальной обструкции отмечаются у 40% больных. Эти симптомы обусловлены сопутствующим хроническим обструктивным бронхитом, предшествующим образованию бронхоэктазов или возникающим вследствие нагноившихся первичных бронхоэктазов (Ю. В. Маликов и соавт., 1979). Боли в грудной клетке на стороне поражения отмечаются обычно при обострении заболевания, развитии перифокальной пневмонии и парапневмонического плеврита.
В период обострения и при тяжелом течении заболевания состояние больных значительно ухудшается. Наряду с увеличением количества гнойной мокроты, появляются признаки интоксикации: продолжительное повышение температуры тела (обычно до 38°С), потливость, слабость, недомогание. Нередко эти симптомы обусловлены перифокальной пневмонией.
При длительном течении бронхоэктатической болезни нередко наблюдаются изменения концевых фаланг пальцев рук — форма «барабанных палочек» и ногтей — форма «часовых стекол». Грудная клетка может быть деформирована вследствие пневмофиброза и эмфиземы легких.
Несмотря на яркую клиническую картину бронхоэктатической болезни, диагностировать ее удается, как правило, через много лет от начала заболевания. Больных продолжительное время лечат по поводу туберкулезной интоксикации, туберкулезного бронхоаденита и туберкулеза легких, хронической пневмонии, хронического бронхита.
Стандартное рентгенологическое исследование, дополненное иногда бронхографией, позволяет поставить правильный диагноз. В отличие от хронического бронхита, бронхоэктазы в значительной части случаев видны на обзорных рентгенограммах и томограммах. Наиболее часто бронхоэктазы встречаются в нижней доле слева и в средней доле справа.
При поражении нижней доли слева возникает характерная рентгенологическая картина (М. Г. Виннер и соавт., 1969): смещение левого корня книзу; разрежение легочного рисунка из-за вздувшейся верхней доли (компенсаторное вздутие); смещение сердца влево, сужение нижнего легочного поля; смещение книзу и кзади главной междолевой щели, что лучше видно на боковых рентгенограммах и томограммах; затемнение и уменьшение размеров самой нижней доли. При этом срединная тень сердца приобретает двойные контуры: латерально проецируется контур тени сердца, а медиально — контур уменьшенной нижней доли. Величина треугольной тени нижней доли зависит от степени ее спадения. Пятнисто-тяжистое затемнение у верхушки левого желудочка свидетельствует о наличии воспалительного процесса в нижней доле слева и язычке. При резко уменьшенной нижней доле, которая в таких случаях прячется за тенью сердца, эти патологические тени образуются воспалительным процессом в язычке. При изолированном поражении нижней доли или нижней зоны и их резком спадении, когда изображение пораженного отдела полностью располагается за тенью сердца, этих патологических изменений не видно. Также характерно затемнение в области заднего реберно-диафрагмального синуса, что видно на боковых томограммах и рентгенограммах. Этот признак является одним из самых постоянных и часто встречающихся.
При бронхографии обнаруживается, что бронхи нижней зоны или доли расширены и сближены между собой. Бронхи язычка и остальных сегментов верхней доли смещены и раздвинуты. При вовлечении в воспалительный процесс язычковых бронхов они также цилиндрически расширены и сближены между собой и с бронхами нижней доли. Бронхи верхней зоны веерообразно раздвинуты.
При поражении средней доли на обзорных рентгенограммах отчетливо определяются лишь кистовидные бронхоэктазы; другие формы отображаются в виде более или менее выраженного усиления и деформации легочного рисунка.
На томограммах в боковой или косой проекции пораженная доля бывает неоднородно затемнена, в ней наблюдаются множественные, округлые или линейные просветления, являющиеся отображением просвета расширенных бронхов в продольном, поперечном и косом сечениях.
На томограммах мешотчатые и кистовидные бронхоэктазы верхней доли отображаются в виде множественных округлых и овальных полостей с более или менее тонкими стенками, которые располагаются своей длинной осью по ходу соответствующих бронхов. В части случаев их контуры нечеткие, что обусловлено склеротическими изменениями. Иногда кистовидные бронхоэктазы сочетаются с воздушными бронхиальными кистами. Томографическая картина у них неотличима. Ценным методом, делающим возможным их распознавание, является бронхография. В отличие от воздушных бронхиальных кист, кистовидные и мешотчатые бронхоэктазы хорошо контрастируются.
При бронхоэктатической болезни важно определить истинный объем поражения, особенно при намечающейся операции. При этом бронхография обязательно должна быть двусторонней. У взрослых пациентов сделать это лучше последовательно, а у детей — одновременно, под общим обезболиванием.
Мешотчатые бронхоэктазы на бронхограммах видны в виде слепо заканчивающихся, резко расширенных бронхов IV—VI порядков, сближенных между собой и лишенных боковых ветвей (рис. 1).
Часто встречаются смешанные бронхоэктазы, когда обнаруживаются цилиндрические и мешотчатые деформации. Расположенные в верхних долях кистовидные бронхоэктазы нередко имеют туберкулезный генез и возникают в результате посттуберкулезного сужения бронха.
Бронхография, особенно в сочетании с кинематографией, позволяет выявить функциональные изменения бронхов. Нередко при этом наблюдаются парадоксальные картины: при небольших цилиндрических бронхоэктазах в части случаев видна потеря дренажной функции бронхов и, наоборот, мешотчатые полости хорошо опорожняются (Л. С. Розенштраух и соавт., 1987). Кроме того, отмечаются ригидность бронхиальных стенок, изменение углов деления и другие функциональные признаки, встречающиеся и при хроническом деформирующем бронхите, но резче выраженные.
Во время бронхоскопического исследования бронхоэктазы не видны. Бронхоскопия позволяет оценить протяженность бронхита, степень интенсивности воспаления слизистой оболочки бронхов в зависимости от стадии обострения или ремиссии бронхоэктатической болезни.
Во время бронхоскопии можно заподозрить наличие бронхоэктазов на основании признака Суля, который указывает на дистальное расширение бронхов: появление опалесцирующих пузырьков воздуха в окружности заполненных гноем устьев (рис. 2).
Для бронхоэктатической болезни в стадии ремиссии характерен частично диффузный (верхнедолевой бронх и его более мелкие ветви интактны) или строго ограниченный одно- или двусторонний бронхит I степени интенсивности воспаления (слизистая оболочка бронхов умеренно гиперемирована, отечна, секрет слизистый, жидкий или вязкий, в большом количестве).
Бронхоэктатическая болезнь в стадии обострения проявляется частично диффузным или строго ограниченным одно- или двусторонним бронхитом III степени интенсивности воспаления (слизистая оболочка бронхов ярко гиперемирована, отечна, устья сегментарных бронхов сужены до точечных, секрет гнойный, вязкий или жидкий, в очень большом количестве).
Наличие бронхоэктазов следует заподозрить на основании анамнестических сведений (кашель с выделением мокроты с детства, частые пневмонии) и выявления стойко сохраняющихся влажных хрипов в период ремиссии болезни. Однако аналогичные симптомы могут быть вызваны распространенным гнойным бронхитом или хронической пневмонией. Дифференциальная диагностика кистозных бронхоэктазов (кистозная гипоплазия) с приобретенными (мешотчатыми) бронхоэктазами, развивающимися обычно в детском возрасте, затруднительна. Обычно выделяют 3 основные группы признаков (клинико-анамнестические, рентгенологические и патоморфологические), по которым можно дифференцировать кистозную гипоплазию от сходных с нею приобретенных бронхоэктазов (Ю. Н. Левашов и соавт., 1975). О наличии ателектатических бронхоэктазов можно думать при сужении межреберных промежутков, понижении прозрачности пораженной части легкого, изменении уровня стояния диафрагмы, смещения средостения, изменения топографии междолевых щелей (Д. Л. Бронштейн, 1975). Бесспорные доказательства существования бронхоэктазов представляет, однако, лишь бронхография. При возникновении кровохарканья необходимо исключить прежде всего туберкулезный процесс, абсцесс легкого и рак бронха.
При ограниченных в пределах отдельных сегментов или даже долей бронхоэктазах без выраженного хронического обструктивного бронхита показано хирургическое лечение. Резекция легкого позволяет устранить очаг хронической инфекции, что, в свою очередь, способствует стиханию или полному разрешению хронического бронхита. Значительное улучшение состояния или выздоровление констатируют после резекции легкого у 97% больных (I. Deslauriers и соавт., 1985). Оперативное вмешательство противопоказано при хроническом обструктивном бронхите с эмфиземой легких, выраженной дыхательной и сердечной недостаточностью. Рецидивы бронхоэктазов возникают, по данным S. A. Adebonojo, O. Osinowo (1979), у 20% оперированных.
Достаточно интенсивное и своевременно начатое (особенно у детей) консервативное лечение позволяет добиться длительной ремиссии.
Методы санации бронхиального дерева принято делить на пассивные (постуральный дренаж с применением отхаркивающих средств) и активные (санационная бронхоскопия).
Обязательным считают позиционный дренаж в строгом соответствии с локализацией бронхоэктазов. При базальных бронхоэктазах секрет из бронхов удаляют путем перевешивания туловища через край кровати или значительного поднятия нижнего конца кровати. При локализации бронхоэктазов в IV и V сегментах — лежа на спине с опущенным головным концом кровати и с подложенной под больной бок подушкой.
Постуральный дренаж больным бронхоэктатической болезнью обязательно проводят по крайней мере 2 раза в день (утром после сна и вечером перед сном). При обострении болезни дренаж следует использовать многократно. Выделение мокроты значительно возрастает при сочетании перкуссии грудной клетки с постуральным дренажом. Эффект постурального дренажа может быть усилен назначением отхаркивающих средств и муколитических препаратов.
Решающее значение, однако, имеют активные методы санации бронхиального дерева. Наиболее эффективны санационные бронхоскопии.
Важное место занимает антибактериальная терапия (обязательно после бактериологического исследования с идентификацией возбудителя). Для лечения этой группы больных используют обычно полусинтетические препараты группы пенициллина, тетрациклины и цефалоспорины. Существенное значение при этом имеет путь введения антибиотика, антибактериальных средств. Принимаемые внутрь и даже вводимые парентерально препараты могут оказаться весьма эффективными при лечении перифокальной пневмонии, менее эффективными — при бронхите и вовсе неэффективными — при лечении бронхоэктазов. При бронхоэктатической болезни даже внутрибронхиальное введение антибиотика через бронхоскоп неэффективно, так как пациент откашливает его вместе с содержимым бронхиального дерева в первые же минуты после окончания бронхоскопии. В связи с этим заслуживает внимания методика интрабронхиального лимфотропного введения антибактериальных препаратов.
При двустороннем поражении на одну санацию расходуется 80—120 мл санирующего раствора, при одностороннем процессе — 60—80 мл санирующей смеси. Готовят 0,1-0,2% раствор диоксидина на 2% растворе гидрокарбоната натрия или 0,1% раствор фурагина калиевой соли на изотоническом растворе хлорида натрия. Так как у пациентов бронхоэктатической болезнью мокрота обычно очень вязкая, в санирующий раствор добавляют муколитики.
В числе первых лекарственных препаратов, влияющих на реологические свойства бронхиального секрета, применяли ферментные препараты — трипсин, химотрипсин, рибонуклеазу. В настоящее время использование протеолитических ферментов, особенно в лечении больных с хронической бронхиальной обструкцией, представляется нецелесообразным вследствие возможного развития бронхоспазма вплоть до астматического статуса, увеличения склонности к кровохарканью, аллергическим реакциям и усилению деструкции межальвеолярных перегородок при дефиците α-1-антитрипсина.
В настоящее время при заболеваниях органов дыхания, сопровождающихся образованием очень вязкой, трудно отделяемой мокроты, применяются лекарственные средства, известные как муколитики или бронхосекретолитические препараты.
Одним из наиболее распространенных препаратов этой группы является N-ацетилцистеин (флуимуцил) (Zambon Group, Италия). Свободные сульфгидрильные группы ацетилцистеина разрывают дисульфидные связи кислых мукополисахаридов мокроты. При этом происходит деполимеризация макромолекул и мокрота становится менее вязкой и адгезивной. Ацетилцистеин оказывает стимулирующее действие на мукозные клетки, секрет которых способен лизировать фибрин и кровяные сгустки.
Ацетилцистеин увеличивает синтез глутатиона, принимающего участие в процессах детоксикации. Известно, что препарат обладает определенными защитными свойствами, направленными против свободных радикалов, реактивных кислородных метаболитов, ответственных за развитие острого и хронического воспаления в легочной ткани и воздухоносных путях.
При лечебной бронхоскопии применяют 3–6 мл 5–10% раствора флуимуцила, который вводят в бронхиальное дерево в конце санации. Санационные бронхоскопии выполняют через день, 8–10 санаций на курс лечения. Желательно в год проводить 2-3 курса лечебных бронхоскопий, но уже более коротких.
Прогноз заболевания зависит от выраженности и распространенности бронхоэктазов, тяжести течения болезни и ее осложнений. Прогноз резко ухудшается при развитии у больных дыхательной недостаточности, легочной артериальной гипертензии, легочных кровотечений и особенно амилоидоза печени или почек.
Н. Е. Чернеховская, доктор медицинских наук, профессор
РМАПО, Москва
Пигментные пятна (ПП) слизистой бронхов достаточно часто встречаются в практике врача-эндоскописта. В то же время работы, посвященные ПП, немногочисленны и разноречивы. Так, частота выявления ПП при диагностических трахеобронхоскопиях колеблется
 |
Пигментные пятна (ПП) слизистой бронхов достаточно часто встречаются в практике врача-эндоскописта. В то же время работы, посвященные ПП, немногочисленны и разноречивы. Так, частота выявления ПП при диагностических трахеобронхоскопиях колеблется от 6,8 до 60% 4. Наличие ПП слизистой бронхов одни авторы считают признаком активного туберкулеза внутригрудных лимфатических узлов, в том числе “малой” его формы [1, 2], другие — “следом” перенесенного специфического процесса [5], третьи — следствием пылевого бронхита [4, 6].
Все это заставило нас провести анализ обширного клинико-эндоскопического материала, накопленного кафедрой фтизиопульмонологии РГМУ на базе ПТД №4 Москвы.
Всего за период 1990-1995 гг. было обследовано 1565 пациентов в основном в возрасте от 21 года до 70 лет, мужчин было в 1,6 раза больше, чем женщин. Показанием для трахеобронхоскопии у 66% явилось наличие активного туберкулеза легких, у 34% диагноз был неясным.
Из 1565 больных ПП были выявлены у 341 (21,8%). Следует отметить, что ПП выявлялись в 3,5 раза чаще у женщин (233 из 593 - 39%), чем у мужчин (102 из 972 - 11%) при почти полной репрезентативности возрастных групп.
У абсолютного большинства больных с ПП в анамнезе не было указаний на профессиональный контакт с пылевыми вредностями или с туберкулезными больными
Больные с ПП слизистой бронхов (341) были разделены на две группы. Первую группу составили 205 пациентов (68,4%), у которых имелись бесспорные клинико-рентгенологические признаки активного туберкулеза легких различной давности. Во вторую группу вошли 136 больных (31,6%), направленных для уточнения диагноза.
Для практического врача наибольший интерес представляет тот факт что чаще всего бронхологическое обследование проводилось с диагностической целью. У подавляющего большинства имелись жалобы, указывающие на заболевание органов дыхания.
В таблице представлены больные с различными формами туберкулеза легких в сочетании с ПП слизистой бронхов (I группа). Располагались ПП у этой группы больных, как правило, в слизистой бронхов верхней и верхушке нижней долей, пораженных туберкулезным процессом. Обычно это были долевые, сегментарные или субсегментарные бронхи. Интересно отметить, что сопоставление цитограмм из участков активного специфического процесса в слизистой бронхов и легочной ткани с цитограммами из ПП показало полную идентичность их клеточных элементов: лимфоциты, эпителиоидные клетки, клетки Пирогова — Лангxанса, дегенерированный бронхиальный эпителий, нейтрофилы.
При лечении противотуберкулезными препаратами (стрептомицин, ГИНК, рифампицин, этамбутол и др.) был отмечен параллелизм между цитологическими изменениями в ПП и специфическими очагами в легких и слизистых бронхов. Всем больным проводилось противотуберкулезное лечение в соответствии с современными общепринятыми установками.
| Пигментные пятна — нередкая находка при бронхоскопии. Чаще всего они являются признаком, иногда единственным, активного туберкулеза бронхов |
Приведенные данные убедительно доказывают, что ПП могут служить дополнительным критерием активности специфического процесса у больных туберкулезом легких.
136 больных, направленных для уточнения диагноза (II группа), объединяло наличие длительного, от шести месяцев до двух лет, субфебрилитета, синдрома интоксикации, болей в грудной клетке, упорного сухого кашля, потливости. При этом рентгенологические признаки патологии органов дыхания отсутствовали. Больные этой группы, как правило, длительно и многократно обследовались амбулаторно во многих лечебных учреждениях.
После тщательного обследования пяти больным был поставлен диагноз хронический бронхит, четырем — хроническая пневмония, двум — саркоидоз. У 18 больных обнаружились туберкулезные инфильтраты в стенках бронхов (диагноз верифицирован цитологически). У 107 больных выявлялись только ПП слизистой бронхов. По разным причинам от лечения и дальнейшего наблюдения отказались девять больных (семь с неспецифическими заболеваниями в сочетании с ПП и двое только с ПП).
Количество больных туберкулезом легких в сочетании с ПП слизистой бронхов
Больным, у которых ПП сочетались с туберкулезными инфильтратами в стенках бронхов, было назначено противотуберкулезное лечение, давшее положительный результат. Пациентам с ПП в сочетании с хроническим бронхитом проводилась терапия антибиотиками широкого спектра действия. После двух-трех месяцев лечения нормализовалось общее состояние и восстановилась трудоспособность.
У оставшихся 105 больных с ПП слизистой бронхов, несмотря на интенсивное лечение (в том числе назначение антибиотиков широкого спектра действия, ингаляции, интратрахеальные вливания), длительно, упорно сохранялся субфебрилитет, синдром интоксикации, сухой кашель, боли в груди. При повторных трахеобронхоскопиях у них продолжали определяться ПП.
Цитологическое исследование материала, взятого из ПП, обнаружило лимфоциты, эпителиоидные клетки, клетки Пирогова — Лангxанса, клеточный детрит, нейтрофилы. Клиническая картина в комплексе с цитологическими данными явилась основанием для назначения пробной противотуберкулезной терапии. Очень медленно, по мере ослабления синдрома интоксикации, отмечались качественные изменения ПП. Следует отметить, что наименьшая динамика ПП наблюдалась при упорно текущем субфебрилитете.
При сопоставлении клиники с динамическими изменениями ПП у больных обеих групп были выявлены общие закономерности, типичные для специфического процесса. Достоверные изменения ПП наблюдались только через два — шесть месяцев после начала лечения противотуберкулезными препаратами; у 7% больных они исчезли.
Через год после начала лечения исчезновение ПП было отмечено у 4% больных (Р<0,05).
Через два года лечения и наблюдения ПП исчезли у 17,5% больных. В целом почти у половины больных окраска ПП к этому времени оставалась неизменной.
У 14 больных улучшение самочувствия и общего состояния не наступило или было временным. У этих больных ПП исчезали в одних отделах бронхиального дерева и появлялись в других либо наряду с существующими появлялись новые ПП.
Важно отметить, что стихание специфического процесса и исчезновение симптомов интоксикации под влиянием противотуберкулезного лечения у больных I группы происходило быстрее по сравнению с группой II.
Таким образом, среди 1565 обследованных ПП были выявлены у 341 человека (21,8%), причем у больных с различными формами туберкулеза (205 из 1043 — 19,7%) они наблюдались реже, чем у пациентов с неясным диагнозом (136 из 522 — 26,0%, Р<0,01).
Лишь в единичных случаях (у 4 из 136) неспецифическое лечение дало положительный результат. У большинства больных этой группы цитологические данные, указывающие на туберкулезную природу ПП, подтвердились явной положительной динамикой заболевания на фоне длительной противотуберкулезной терапии, отсутствием эффекта от неспецифического лечения и в ряде случаев наличием туберкулезных инфильтратов в стенке бронхов. Таким образом, можно сделать вывод, что ПП являются проявлением (часто единственным) активного туберкулеза бронхов. Поэтому больных с ПП слизистой бронхов следует обязательно направлять на консультацию врача-фтизиатра.
Литература.
1. Бублик П. И., Васильев Н. А., Разумовская В. Ф. и др. Диагностика малых форм туберкулеза внутригрудных лимфатических узлов: Тез. докл. XI Всесоюз. съезда фтизиатров. Л., 1991, с. 100-101.
2. Бублик П. И., Разумовская В. Ф., Семиошин В. В. и др. Диагностика малых форм туберкулеза внутригрудных лимфатических узлов у лиц старше 50 лет //Сб. трудов XIX научно-практической конф. фтизиатров, Москва. М., 1992, т. LYII. С. 57-59.
3. Долгина А. Г. Эндоскопическая картина туберкулеза бронхов у больных силикотуберкулезом //Пробл. туб. 1981. №1. С. 42-45.
4. Кривонос А. П. Ранняя эндоскопическая диагностика силикотуберкулеза у горнорабочих железнорудных шахт: Автореф. канд. дис. Киев, 1988. С. 24.
5. Лавренева В. Н. Туберкулез внутригрудных лимфатических узлов у взрослых и особенности его эндоскопических осложнений: Автореф. канд. дис. М., 1982. С. 21.
6. Падерин В. Ф., Чугаев Ю. П., Теряев М. В. Сравнительная характеристика кониотуберкулеза внутригрудных лимфатических узлов профессионального и бытового генеза // Пробл. туб. 1995. №6. С. 27-29.
Читайте также:

