Синдром рейно при системной красной волчанке
Обновлено: 18.04.2024
Синдром Рейно (СР) — это эпизодическое нарушение периферической циркуляции вследствие локальной артериальной вазоконстрикции (спазм) дигитальных артерий и кожных сосудов в ответ на воздействие холода или эмоциональный стресс. Клинически синдром проявляет
Синдром Рейно (СР) — это эпизодическое нарушение периферической циркуляции вследствие локальной артериальной вазоконстрикции (спазм) дигитальных артерий и кожных сосудов в ответ на воздействие холода или эмоциональный стресс. Клинически синдром проявляется резко очерченными изменениями цвета кожи пальцев кистей. В основе повышенного спазма сосудов лежит дефект центральных и локальных механизмов регуляции вазомоторных реакций.
Распространенность СР в общей популяции составляет 3–5% и различается между отдельными климатическими зонами [1]. Заболевание начинается преимущественно в подростковом или молодом возрасте и у женщин встречается чаще, чем у мужчин. Наблюдается тенденция к семейной агрегации заболевания.
Выделяют первичный и вторичный СР. Первичный, или идиопатический, СР характеризуется спазмом пальцевых артерий и терморегуляторных сосудов кожи при воздействии холода, без каких-либо признаков поражения сосудов. При вторичном СР наблюдается сочетание синдрома Рейно с симптомами других заболеваний.
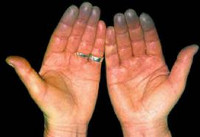
Наиболее часто при СР поражаются кисти рук. Основным клиническим признаком СР является последовательная смена окраски кожи пальцев кистей на холоде. В начале приступа вазоспазма обычно появляется бледная окраска кожи, после чего в течение нескольких минут кожа приобретает синевато-фиолетовый оттенок. Вазоспазм обычно длится 15–20 мин и завершается быстрым восстановлением кровотока, о чем свидетельствует интенсивно розовая окраска кожи (реактивная гиперемия).
У некоторых больных приступы вазоспазма сопровождаются ощущением замерзания кистей, онемением и покалыванием в пальцах, которые проходят после восстановления кровотока. В фазе реактивной гиперемии больные могут чувствовать боль в пальцах кистей.
На ранних этапах заболевания изменения цвета кожи могут наблюдаться на дистальной фаланге одного или нескольких пальцев кистей. В дальнейшем область поражения охватывает все пальцы кистей и, возможно, стоп, при этом большие пальцы обычно остаются интактными. Вазоспазму могут подвергаться также сосуды кожи лица и других участков. В этих случаях можно наблюдать характерные изменения окраски кончика носа, губ и ушных раковин, а также кожи над коленными суставами. У отдельных больных в процесс вовлекаются и сосуды языка, что проявляется дизартрией во время приступа вазоспазма. При эпизодах вазоспазма может появляться мраморный рисунок на верхних и нижних конечностях — симптом, называемый сетчатым ливедо (livedo reticularis). Частота и продолжительность эпизодов вазоспазма могут варьировать как у различных больных, так и у одних и тех же пациентов в разное время года (зимой более интенсивные, чем летом).
Трехфазная перемена окраски кожи (побеление–посинение–покраснение) выявляется не во всех случаях; у части больных наблюдается двухфазное или однофазное изменение цвета. В зависимости от количества фаз изменения цвета кожи, выделяют достоверный и вероятный СР.
- Достоверный СР — повторные эпизоды двухфазного изменения окраски кожи на холоде.
- Вероятный СР — однофазное изменение окраски кожи, сопровождающееся онемением или парестезией под воздействием холода.
- СР нет — изменения окраски кожи под воздействием холода отсутствуют.
Более чем у 80% больных выявляется первичный СР. Для верификации первичного СР применяются диагностические критерии, предложенные E. V. Allen и G. E. Brown в 1932 г. и модифицированные в последние годы. Эти критерии, разработанные с учетом клинических и некоторых лабораторных показателей, а также результатов капилляроскопии ногтевого ложа, включают [2]:
- симметричность эпизодов вазоспазма;
- отсутствие заболеваний периферических сосудов;
- отсутствие гангрены, дигитальных рубчиков или повреждения тканей;
- нормальные капилляры ногтевого ложа;
- отсутствие АНФ и нормальное значение СОЭ.
Средний возраст развития СР составляет 14 лет; только у 27% больных болезнь дебютирует в возрасте старше 40 лет [3]. При первичном СР симптомы болезни обычно умеренно выражены, и только у 12% больных наблюдаются интенсивные эпизоды вазоспазма [4]. Приблизительно у 1/4 больных СР выявляется среди родственников первой линии [5].
Вместе с тем при большом числе состояний и заболеваний, ассоциирующихся с СР, он считается вторичным (таблица).
Наиболее часто вторичный СР ассоциируется с системной склеродермией, системной красной волчанкой, другими заболеваниями соединительной ткани, гематологическими нарушениями и приемом некоторых лекарств. При длительном наблюдении за больными, которым был поставлен предварительный диагноз первичного СР, удалось выявить, что у 13% из них на определенном этапе болезни развиваются признаки системного заболевания соединительной ткани (наиболее часто — системной склеродермии) [6].
Несмотря на идентичность клинических проявлений первичного и вторичного СР, при этих двух состояниях имеются некоторые различия в отдельных признаках. На вероятность вторичного характера СР указывают следующие признаки:
- поздний возраст начала;
- мужской пол;
- болезненные эпизоды вазоспазма с признаками тканевой ишемии (изъязвления);
- асимметричный характер атак;
- наличие признаков другого заболевания;
- лабораторные признаки аутоиммунных или сосудистых заболеваний;
- выявление АНФ;
- редукция и дилатация капилляров при капилляроскопии ногтевого ложа;
- распространенный характер СР, охватывающий проксимальные по отношению к пальцам кистей и стоп участки.
Вторичный СР развивается обычно в возрасте старше 30 лет, отличается более выраженными и болезненными эпизодами вазоспазма, структурными изменениями капилляров [7]. АНФ имеет относительно низкую прогностическую ценность для заболеваний соединительной ткани (30%), тогда как выявление специфических аутоантител значительно повышает вероятность вторичного характера СР [6, 8, 9]. Приблизительно у 15–20% больных СР, у которых выявляются специфические аутоантитела и/или капилляроскопические изменения, но отсутствуют симптомы заболеваний соединительной ткани, в дальнейшем (обычно в течение двух лет) развивается то или иное заболевание соединительной ткани [10, 11].
У всех больных со впервые выявленным СР необходимо проводить специальные исследования с целью дифференциальной диагностики первичного и вторичного характера патологии.
В первую очередь следует уточнить:
- имеются ли у пациента симптомы заболеваний соединительной ткани, с которыми наиболее часто ассоциируется СР (артриты, миалгии, лихорадка, «сухой» синдром, кожная сыпь, кардиопульмональные нарушения);
- принимает ли больной на момент исследования какие-либо препараты, особенно химиотерапевтические средства;
- подвергается ли больной вибрации или другим механическим воздействиям, травмирующим кисти;
- связаны ли эпизоды синдрома Рейно с определенными позиционными изменениями.
Необходимо учитывать, что клинические признаки ассоциированного с СР заболевания могут развиться по истечении нескольких месяцев или лет после начала СР. Наиболее объективным и специфичным инструментальным методом дифференциальной диагностики первичного и ассоциированного с системными заболеваниями соединительной ткани (прежде всего с системной склеродермией) СР является капилляроскопия ногтевого ложа. В норме капилляроскопическая картина представляет собой правильный ряд равномерно распределенных по краю ногтевого ложа и одинакового размера капилляров. При системной склеродермии, с которой наиболее часто ассоциируется СР, изменения количества капилляров (редукция) и их размеров (дилатация) появляются на ранних стадиях и часто предшествуют развитию клинических признаков заболевания.
Дифференциальная диагностика СР
Повышенная чувствительность к холоду характерна для популяции в целом. Холодная кожа или неочерченная крапчатость кожи пальцев, кистей и конечностей считаются нормальным ответом на воздействие холода. У больных СР, помимо повышенной чувствительности, под влиянием холода эпизодически наблюдаются побледнение и цианоз дистальных отделов пальцев. СР следует отличать от акроцианоза — состояния, характеризующегося продолжительным цианозом кистей или стоп, который усиливается под влиянием холода.
Повышенную чувствительность к холоду могут вызвать карпальный туннельный синдром и другие невропатии. При дифференциальной диагностике следует учитывать такие состояния, как криопротеинемии, диспротеинемии, контакт с поливинилхлоридом, наличие опухоли или гипотиреоза. Если признаки заболевания проявляются асимметрично, необходимо провести исследования для выявления окклюзивных заболеваний крупных сосудов. Атеросклероз не сопровождается типичными симметричными признаками СР, но в ряде случаев проявляется перемежающейся хромотой при нагрузках, асимметричным поражением конечности, изолированной или персистирующей дигитальной ишемией. Васкулиты, эмболии или другие окклюзивные поражения сосудов могут приводить к критической ишемии, но не к развитию типичного СР. Имеются доказательства того, что СР может служить клиническим проявлением генерализованных вазоспастических заболеваний, таких как стенокардия Принцметал и мигрень [12].
Сетчатое ливедо наблюдается также при васкулитах, антифосфолипидном синдроме и окклюзивных заболеваниях периферических сосудов, при которых, в отличие от СР, этот признак имеет устойчивый характер.
На замерзание конечностей, их онемение и покалывание довольно часто жалуются больные с заболеваниями периферических сосудов, сопровождающимися снижением кровотока и ишемией. При СР, в отличие от заболеваний периферических сосудов, указанные симптомы наблюдаются только во время вазоспазма и полностью проходят после восстановления исходного кровотока.
Лечение СР
Общие рекомендации для больных первичным и вторичным СР:
- следует избегать длительного пребывания на холоде, в том числе в неотапливаемом и сыром помещении;
- необходимо носить рукавицы вместо перчаток, хуже сберегающих тепло, головной убор и теплое нижнее белье;
- следует отказаться от курения, потребления кофе и кофеинсодержащих напитков;
- необходимо овладеть приемами, с помощью которых можно уменьшить длительность эпизодов вазоспазма (согревание кистей в теплой воде или подмышечной области, быстрые круговые движения кистей и др.).
Соблюдения указанных рекомендаций часто бывает достаточно для лечения больных первичным СР.
Дигитальные артерии и терморегуляторные сосуды кожи находятся преимущественно под симпатическим адренергическим контролем. Эмоциональный стресс может спровоцировать дигитальный вазоспазм, а состояние тревоги часто усиливает индуцированные холодом атаки Рейно [13]. В таких случаях бывает полезным назначение седативных средств. Важно избегать применения препаратов, которые могут вызвать вазоконстрикцию (симпатомиметики, клонидин, эрготамин, агонисты серотониновых рецепторов и др.). Курение может редуцировать пальцевой кровоток, вследствие чего больным СР следует отказаться от этой привычки.
Медикаментозное лечение СР
В случаях частых и продолжительных эпизодов вазоспазма при первичном СР и у больных вторичным СР необходимо назначение лекарственной терапии. Для лечения СР применяют препараты с вазодилатирующим действием или средства, влияющие на реологические свойства крови.
Блокаторы кальциевых каналов
Блокаторы кальциевых каналов обладают наибольшим вазодилатационным потенциалом. Препаратами выбора являются дигидропиридиновые производные — нифедипин, амлодипин, исрадипин и фелодипин. Обладающий кратковременным действием нифедипин в разовой дозе 10–20 мг при 3-кратном ежедневном приеме значительно уменьшает частоту и выраженность, а в некоторых случаях и продолжительность эпизодов вазоспазма [15]. Однократный прием 5–20 мг нифедипина достаточно эффективно предупреждает индуцированный холодом вазоспазм при приеме за 15–20 мин до воздействия холода. При назначении нифедипина наблюдается достоверное повышение кожного и мышечного кровотока [16]. Приблизительно у 1/3 больных на фоне приема нифедипина развиваются побочные эффекты, среди них наиболее часто встречаются артериальная гипотония, головная боль, гиперемия, тахикардия, отеки голеней. Уменьшение побочных эффектов возможно при назначении ретардных форм нифедипина в суточной дозе 20–40 мг [17]. У больных первичным СР, по сравнению со вторичным, терапевтический эффект препарата обычно проявляется в большей степени. При длительном приеме нифедипина в больших дозах возможны парестезии, боли в мышцах, а также развитие толерантности и уменьшение лечебного действия препарата.
Наряду с нифедипином, в лечении СР с успехом применяются и другие производные дигидропиридина — амлодипин, исрадипин и фелодипин, которые относятся к длительно действующим препаратам [18]. Амлодипин назначается один раз в день в дозе 5 мг, при недостаточном эффекте суточная доза может быть повышена до 10 мг. Наиболее распространенным побочным эффектом амлодипина является отек лодыжек. Исрадипин назначается в дозе 2,5 мг 2 раза в день. Побочные эффекты в виде головных болей и гиперемии обычно носят умеренно выраженный характер. Фелодипин применяют в дозе 10 мг 1 раз в сут, преимущественно в виде лекарственных форм, обеспечивающих постепенное высвобождение лекарственного вещества. Блокаторы кальциевых каналов подавляют активацию тромбоцитов, что также оказывает благоприятное действие при СР [19].
При наличии противопоказаний или непереносимости блокаторов кальциевых каналов для лечения СР применяются вазодилататоры других лекарственных групп.
Назначение симпатолитических препаратов обосновано тем, что адренергическая стимуляция играет важную роль в вазоконстрикции. Празозин достоверно уменьшает выраженность и частоту вазоспазма у больных с первичным СР [20].
Простагландины оказывают комплексное физиологическое воздействие, в частности речь идет о вазодилатации, антиоксидантном действии, подавлении агрегации тромбоцитов и др.
Алпростадил (вазапростан) при ежедневных в/в инфузиях 20–40 мкг препарата в 200 мл изотонического раствора NaCl в течение 15–20 дней достоверно уменьшает как частоту, так и интенсивность вазоспазма у больных с первичным и вторичным СР [21].
Илопрост уменьшает число атак в неделю и интенсивность вазоспазма у больных первичным и вторичным (ассоциированным с системной склеродермией) СР в среднем на 39 и 35% соответственно [22].
Пентоксифиллин обладает антиагрегационным и слабым вазодилатационным действием. Назначается в комбинации с другими сосудорасширяющими препаратами на длительное время.
В лечении СР применяется ряд вазодилататоров (нитроглицерин трансдермальный, гидралазин, папаверин, миноксидил), которые могут быть эффективными у отдельных больных. Однако частое развитие побочных эффектов (системная гипотензия, головная боль) ограничивает применение этих препаратов. Результаты исследований эффективности ингибиторов ангиотензинпревращающего фермента у больных СР весьма противоречивы, в настоящее время препараты этой группы не нашли широкого применения в клинической практике.
Ксантинола никотинат назначается в таблетках по 150 мг 3 раза в день. Длительность приема, с учетом переносимости и противопоказаний к его назначению (как и других препаратов никотиновой кислоты), устанавливается индивидуально и определяется эффективностью и переносимостью средства.
Лекарственная терапия СР имеет некоторые ограничения, включая недостаточный ответ, развитие толерантности при длительном применении, развитие ряда побочных эффектов, многие из которых становятся причиной отмены того или иного препарата. При неэффективности консервативной терапии с целью уменьшения проявлений СР возможно хирургическое лечение — локальная дигитальная симпатэктомия. Однако продолжительность и ожидаемая выраженность лечебного эффекта симпатэктомии до сих пор не уточнены, в связи с чем их трудно прогнозировать. Предполагаемая эффективность симпатэктомии может быть оценена в дооперационный период с помощью фармакологической симпатэктомии.
В большинстве случаев СР представляет собой заболевание, характеризующееся благоприятным прогнозом и стабильным течением. В дебюте заболевания, особенно при наличии факторов риска вторичного характера СР, все больные СР подлежат диспансеризации и врачебному осмотру один раз в год. Пациенты должны быть предупреждены о необходимости дополнительного визита к врачу при появлении новых симптомов, указывающих на возможное развитие заболеваний, с которыми наиболее часто ассоциируется СР, прежде всего системных заболеваний соединительной ткани.
По вопросам литературы обращайтесь в редакцию.
Р. Т. Алекперов, доктор медицинских наук
Институт ревматологии РАМН, Москва
Синдром Рейно – вазоспастическое заболевание, характеризующееся пароксизмальным расстройством артериального кровообращения в сосудах конечностей (стоп и кистей) под воздействием холода или эмоционального волнения. Синдром Рейно развивается на фоне коллагенозов, ревматоидного артрита, васкулитов, эндокринной, неврологической патологии, болезней крови, профессиональных заболеваний. Клинически синдром Рейно проявляется приступами, включающими последовательное побледнение, цианоз и гиперемию пальцев рук или ног, подбородка, кончика носа. Синдром Рейно приводит к постепенным трофическим изменениям тканей. Консервативные меры включают прием вазодилататоров, хирургическое лечение заключается в симпатэктомии.
МКБ-10
Общие сведения
Синдром Рейно является вторичным состоянием, развивающимся на фоне ряда заболеваний: диффузной патологии соединительной ткани (склеродермия, системная красная волчанка), системных васкулитов, ревматоидного артрита, заболеваний симпатических ганглиев, эндокринных и гематологических нарушений, диэнцефальных расстройств, компрессии сосудисто-нервных пучков. Кроме того, синдром Рейно может быть спровоцирован воздействием профессиональных вредностей (охлаждением, вибрацией).
В патогенезе синдрома Рейно ведущая роль отводится эндогенным вазоконстрикторам – катехоламинам, эндотелину, тромбоксану А2. В развитии синдрома Рейно выделяют три последовательные фазы: ишемическую, цианотическую и гиперемическую. Фаза ишемии развивается вследствие спазма периферических артериол и полного опорожнения капилляров; проявляется локальным побледнением кожного покрова. Во второй фазе, обусловленной задержкой крови в венулах и артериовенулярных анастомозах, побледнение кожи сменяется цианозом (синюшностью). В последней фазе – реактивно-гиперемической отмечается покраснение кожи.
При отсутствии этиофакторов, характерных для синдрома Рейно, предполагают наличие болезни Рейно. В возникновении болезни Рейно установлена роль наследственности, эндокринных дисфункций, психических травм, хронической никотиновой и алкогольной интоксикации. Болезнь Рейно более распространена среди женщин 20-40 лет, страдающих мигренью.

Симптомы синдрома Рейно
Симптоматика синдрома Рейно обусловлена пароксизмальным вазоспазмом и развивающимися вследствие этого повреждениями тканей. В типичных случаях при синдроме Рейно поражаются IV и II пальцы стоп и кистей, иногда – подбородок, уши и нос. Приступы ишемии вначале кратковременны, редки; возникают под воздействием холодовых агентов, вследствие волнения, курения и т. д. Внезапно развивается парестезия, похолодание пальцев, кожа становится алебастро-белого цвета. Онемение сменяется жжением, ломящей болью, чувством распирания. Приступ завершается резкой гиперемией кожи и ощущением жара.
Прогрессирование синдрома Рейно приводит к удлинению времени приступов до 1 часа, их учащению, спонтанному возникновению без видимых провокаций. После высоты пароксизма наступает цианотическая фаза, появляется незначительная отечность тканей. В промежутки между приступами стопы и кисти остаются холодными, цианотичными, влажными. Для пароксизмов ишемии при синдроме Рейно характерно симметричное и последовательное развитие проявлений: сначала на пальцах кистей, затем - стоп. Последствиями ишемии тканей в случае длительного и тяжелого течения синдрома Рейно могут стать трофические изменения в виде плохо заживающих трофических язв, участков некрозов, дистрофических поражений ногтевых пластин, остеолиза и деформации фаланг, гангрены.
Диагностика синдрома Рейно
Пациента с синдромом Рейно направляют на консультацию ревматолога и сосудистого хирурга. При синдроме Рейно выявить изменения в дистальных отделах артерий позволяет ангиография периферического сосудистого русла, при которой определяются участки неравномерного стеноза и тотальной обструкции сосудов, отсутствие капиллярных сетей и коллатералей. При капилляроскопии ногтевого ложа и передней поверхности глаза обнаруживаются морфологические изменения микрососудистого рисунка, свидетельствующие о нарушения перфузии.
Лазерная доплеровская флоуметрия, применяемая для оценки периферической микроциркуляции, выявляет дефекты метаболической и миогенной регуляции кровообращения, снижение вено-артериальных реакций и симпатической активности. В период между приступами при синдроме Рейно спровоцировать вазоспазм и оценить состояние кровотока позволяет проведение холодовой пробы.
Лечение синдрома Рейно
Первым принципом терапии синдрома Рейно служит исключение провоцирующих моментов – курения, охлаждения, вибрации и других бытовых и производственных факторов. Проводится выявление и лечение первичного заболевания, обусловившего развитие синдрома Рейно. Среди вазодилататоров при синдроме Рейно эффективно назначение антагонистов кальция - нифедипина, алпростадила, селективных блокаторов кальциевых каналов - верапамила, никардипина дилтиазема. При необходимости применяются ингибиторы АПФ (каптоприл), селективные блокаторы HS2-серотониновых рецепторов (кетансерин).
При синдроме Рейно производится назначение антиагрегантных препаратов - дипиридамола, пентоксифиллина, низкомолекулярных декстранов (реополиглюкина). Прогрессирование и резистентность синдрома Рейно к лекарственной терапии служит показанием к проведению хирургической симпатэктомии или ганглиэктомии. При развившемся ишемическом приступе неотложными мерами является согревание конечности в теплой воде, массирование с помощью шерстяной ткани, предложение пациенту горячего питья. При затяжном приступе назначают инъекционные формы спазмолитиков (дротаверина, платифиллина), диазепама, блокады.
При синдроме Рейно используются немедикаментозные методики - психотерапия, рефлексотерапия, физиотерапия, гипербарическая оксигенация. При синдроме Рейно, обусловленном системными коллагенозами, показано проведение сеансов экстракорпоральной гемокоррекции. Новым словом в лечении синдрома Рейно является терапия с использованием стволовых клеток, направленная на нормализацию периферического кровотока. Стволовые клетки способствуют открытию новых коллатералей в сосудистом русле, стимулируют регенерацию поврежденных нервных клеток, что в итоге ведет к прекращению пароксизмов вазоконстрикции.
Прогноз и профилактика синдрома Рейно
Прогноз синдрома Рейно зависит от прогрессирования основной патологии. Течение синдрома относительно благоприятное, приступы ишемии могут спонтанно прекратиться после перемены привычек, климата, профессии, проведения санаторного лечения и т. д.
Отсутствие первичных профилактических мер позволяет говорить только о вторичной профилактике синдрома Рейно, т. е. об исключении пусковых факторов, ведущих к вазоспазму - переохлаждения, вибрации, курения, психоэмоциональных нагрузок.
Дискоидная красная волчанка – это хроническое воспалительное аутоиммунное заболевание кожи, развивающееся на фоне фотосенсибилизации (повышенной чувствительности к свету). Клинические проявления включают эритему, рубцовую атрофию кожи, фолликулярный гиперкератоз, выпадение волос, поражение ногтей. Диагноз ставится на основании симптоматики, анамнестических данных, наличия волчаночных клеток в крови, иммунологических тестов и гистологического исследования биоптата кожи. В качестве лечения применяются синтетические противомалярийные препараты, топические глюкокортикоиды, системные ретиноиды, солнцезащитные средства.
МКБ-10
Общие сведения
Дискоидная красная волчанка (ДКВ), или рубцующийся эритематоз – заболевание, относящееся к диффузным болезням соединительной ткани (коллагенозам). Данная патология является наиболее частой формой кожной красной волчанки. Средняя распространенность рубцующегося эритематоза составляет 1:100 000 человек. Чаще страдают представители европеоидной расы. Начало болезни приходится на молодой возраст (от 20 до 40 лет). Заболеваемости дискоидной волчанкой больше подвержены лица женского пола (соотношение с мужчинами 3:1). В редких случаях (1-5%) ДКВ может перейти в системную красную волчанку (СКВ).

Причины ДКВ
Эритематоз протекает по типу аутоиммунной реакции, точная причина возникновения которой неизвестна. Важное значение в развитии заболевания имеет наследственная предрасположенность, о чем свидетельствует большая встречаемость дискоидной волчанки среди близких родственников. В ходе исследований была установлена ассоциация ДКВ с антигенами тканевой совместимости HLA A1, A3, A10, A11, A18, B7, B8. Наиболее серьезным провоцирующим действием обладает ультрафиолетовое излучение.
К факторам, способствующим возникновению дискоидной волчанки, относятся постоянная травматизация кожи, хронические инфекции в организме, наличие аллергических болезней, прием лекарственных препаратов, повышающих чувствительность кожи к ультрафиолету (сульфаниламидов, тетрациклина, фторхинолонов, гризеофульвина, нейролептиков). В группе повышенного риска находятся люди, чей род деятельности связан с длительным пребыванием на открытом воздухе (работники сельскохозяйственной промышленности, строители, рыбаки). Также в группу риска входят лица с 1 фототипом кожи (кельтским) – это люди с нежной, тонкой, иногда веснушчатой кожей, имеющие светлый или рыжий цвет волос.
Патогенез
При дискоидной красной волчанке наблюдается патогенетическое сходство с СКВ, однако патологические реакции ограничиваются кожными покровами. В основе заболевания лежит аутоиммунное воспаление. Под действием ультрафиолетовых лучей в совокупности с другими провоцирующими факторами в клетках кожи нарушаются процессы метилирования ДНК (механизма регуляции транскрипции генов). Это приводит к повышению экспрессии белков, индуцирующих апоптоз (запрограммированную клеточную гибель) - p53, Fas и Fas-лиганда и гамма-интерферона.
Т- и В-лимфоциты стимулируют синтез цитокинов и антител к компонентам клеточных ядер (нуклеиновым кислотам, нуклеосомам). Образующиеся иммунные комплексы оседают на эндотелии сосудов, вызывая их повреждение. Выработку аутоантител у генетически предрасположенных лиц также способны вызывать антигены некоторых вирусов (Эпштейна-Барр, цитомегаловирус, парвовирус 19), имеющие сходную молекулярную структуру с белками клеточных мембран. Дополнительным повреждающим агентом выступает индукция свободнорадикального окисления липидов. Результатом этих процессов является массивное воспаление и разрушение клеток кожи.
Классификация
Традиционно дискоидную красную волчанку подразделяют на очаговую и диссеминированную (распространенную) – эти формы различаются количеством очагов поражения кожи и их локализацией. Также при диссеминированной форме отмечается наличие общей симптоматики (слабости, повышения температуры тела, болей в суставах) и высокого риска трансформации в СКВ. Помимо перечисленных форм, в ревматологии выделяют следующие виды ДКВ:
- Глубокая. Характерны подкожные узлы с их последующей кальцификацией.
- Папилломатозная. Патологический процесс затрагивает волосистую часть головы и кожу кистей рук. Очаги имеют вид бородавок.
- Дисхромическая. Характерны депигментация центрального участка дискоидного очага и гиперпигментация периферической зоны.
- Телеангиэктатическая. Проявляется усиленным сосудистым рисунком очагов.
- Гиперкератотическая. Роговой слой эпидермиса выражено утолщен. Очаги напоминают кожный рог. Наиболее неблагоприятная форма. Рассматривается как начальная стадия рака.
- Центробежная эритема Биетта. Проявляется высыпаниями на спинке носа и щеках, имеющими «вид бабочки».
Симптомы ДКВ
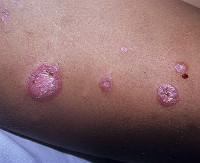
Дискоидная красная волчанка характеризуется хроническим течением, рецидивы возникают в основном летом или весной, когда длина солнечного дня максимальна. Чаще всего поражаются участки тела, подвергающиеся длительному солнечному излучению. Тремя наиболее типичными симптомами считаются эритема, фолликулярный гиперкератоз и рубцовая атрофия кожи.
Эритематоз дебютирует с появления на коже розовых, слегка возвышающихся пятен (эритем) размером 1-2 см. Пятна не сопровождаются зудом, со временем увеличиваются, на их поверхности образуются серо-белые чешуйки. Попытка удалить чешуйки вызывает боль (симптом Бенье-Мещерского). Также при снятии чешуек на месте их прикрепления к волосяным фолликулам видны участки вдавления (симптом «дамского каблучка» или «канцелярской кнопки»). По мере прогрессирования в центре дискоидных очагов кожа атрофируется. Вокруг центра формируется фолликулярный гиперкератоз вследствие закупорки фолликулов чешуйками эпидермиса, имеющий вид «гусиной кожи», по периферии очагов – эритема, зоны усиления или ослабления пигментации. Часто на коже наружного слухового прохода образуются пробки в протоках сальных желез, при этом поверхность кожи по внешнему виду напоминает наперсток.
При локализации очагов на волосистой части головы практически всегда возникает алопеция, которая оставляет после себя рубцы. При диссеминированной дискоидной волчанке очаги располагаются на груди, спине, локтях, ладонях, подошвах, обычно не имеют признаков шелушения и атрофии. Иногда поражаются ногтевые пластины. Ногти приобретают желтый цвет, становятся ломкими, деформируются. Очень редко в патологический процесс вовлекается слизистая оболочка полости рта. Очаги склонны к эрозированию, что вызывает жжение и боли во время приема пищи.
Осложнения
Серьезные осложнения дискоидной красной волчанки возникают редко. Иногда развивается вторичный гландулярный хейлит (воспаление мелких слюнных желез красной каймы губ). Диссеминированная форма ДКВ в некоторых случаях переходит в СКВ – тяжелое системное заболевание соединительной ткани, поражающее суставы и практически все внутренние органы (сердце, почки, легкие и центральную нервную систему). СКВ характеризуется упорным течением, трудно поддается терапии и имеет высокий риск летального исхода. Также может произойти трансформации стойких очагов дискоидной волчанки в плоскоклеточный рак кожи (сквамозно-клеточную карциному).
Диагностика
Пациентов с данной патологией курируют врачи ревматологи и дерматологи. При постановке диагноза дискоидной волчанки учитывается фототип кожи. На первичной консультации уточняется профессия пациента, прием фотосенсибилизирующих лекарственных средств, наличие инфекционных или аллергических заболеваний, близких родственников с ДКВ. Для диагностики проводят следующие методы исследования:
- Общие лабораторные тесты. В клиническом анализе крови отмечается увеличение скорости оседания эритроцитов, снижение уровня лейкоцитов, тромбоцитов, при инфекционных и аллергических патологиях - высокий уровень нейтрофилов и эозинофилов. При диссеминированной ДКВ возможен ложноположительный результат анализа на сифилис.
- Специальные ревматологические тесты. Примерно у 40% пациентов ДКВ обнаруживаются антинуклеарные антитела (ANA) и антитела к нуклеопротеинам (анти-Ro/SS-A, анти-La/SS-B). Волчаночные (LE) клетки встречаются у 5-7% пациентов. При реакции иммунной флюоресценции выявляются отложения иммуноглобулинов (IgG/IgM) и комплемента (положительный тест волчаночной полоски). Последний тест может быть положительным и при других заболеваниях, поэтому не является специфичным.
- Гистологическое исследование биоптата кожи. Биопсия кожи - наиболее достоверный метод для постановки диагноза. Характерны следующие признаки – атрофия эпидермиса, утолщение рогового слоя эпидермиса в устьях волосяных фолликулов, разрушение волокон коллагена, отек дермы, отложения в ней гиалина, периваскулярный лимфоцитарный инфильтрат.
Важно отличать диссеминированную форму ДКВ от системной красной волчанки, требующей более агрессивной терапии. Помощь в диагностике СКВ оказывает определение антител к двуспиральной ДНК и экстрагируемым ядерным ангигенам в крови пациента. Также дискоидную красную волчанку дифференцируют с другими формами кожной волчанки (острая, подострая), ревматологическими (дерматомиозит), дерматологическими заболеваниями (красный плоский лишай, псориаз, себорейный дерматит, экзема, фотодерматозы, эозинофильная гранулема лица, ангиолюпоид Брока-Потрие).
Лечение ДКВ
В большинстве случаев пациенты проходят лечение амбулаторно, но при тяжелом течении может потребоваться госпитализация в отделение ревматологии или дерматологии. Важным моментом является исключение приема фотосенсибилизирующих медикаментов и лечение сопутствующих аллергических или инфекционных заболеваний. Рекомендуется носить закрытую одежду, применять солнцезащитные крема или мази, содержащие вещества, которые задерживают ультрафиолетовые лучи (мексорил, двуокись титана, оксид цинка).
Основное патогенетическое лечение включает антималярийные аминохинолиновые препараты (Гидроксихлорохин), топические глюкокортикостероиды (тГКС), производные витамина А - ретиноиды (Изотретиноин, Ацитретин). Ввиду частого развития ретинопатий на фоне приема гидроксихлорохина обязателен регулярный осмотр офтальмолога. В зависимости от локализации дискоидных очагов применяются тГКС разной активности. При расположении очагов только на коже лица используют тГКС слабой и средней степени активности (Гидрокортизона ацетат, Метилпреднизолон), при поражении кожи конечностей и туловища рекомендуются тГКС сильной активности (Бетаметазон, Триамцинолон). Если дискоидные очаги имеются на ладонях и подошвах, назначаются тГКС сверхвысокой активности (Клобетазон).
Для подавления свободнорадикального повреждения клеток кожи эффективны антиоксиданты (альфа-токоферол). При неэффективности стандартного лечения прибегают к средствам, обладающим выраженным иммуносупрессивным действием – Такролимус, Метотрексат, Азатиоприн.
Прогноз и профилактика
В подавляющем большинстве случаев дискоидная волчанка имеет благоприятное течение. При грамотном подборе терапии и соблюдении всех рекомендаций наступает стойкая ремиссия. Основную проблему представляет трансформация ДКВ в более тяжелые заболевания, имеющие достаточно высокий процент летальности – СКВ и плоскоклеточную карциному. Профилактика рецидивов дискоидной волчанки заключается в ограничении времени пребывания на солнце, ношении закрытой одежды, применении солнцезащитных препаратов, исключении приема лекарств, повышающих чувствительность кожных покровов к ультрафиолетовому излучению.
1. Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 2016.
3. Федеральные клинические рекомендации по ведению больных с поражениями кожи при красной волчанке/ Самцов А.В., Чикин В.В. - 2015.
Лекарственная волчанка – обратимый волчаночноподобный синдром, вызванный приемом лекарственных препаратов. Клинические проявления лекарственной волчанки сходны с СКВ и включают лихорадку, артралгии, миалгии, полиартрит, плеврит, пневмонит, гепатомегалию, гломерулонефрит. Диагноз основывается на характерных лабораторных критериях (определении в крови антинуклеарного фактора, антинуклеарных антител, LE-клеток) и связи симптоматики с приемом определенных лекарственных медикаментов. Обычно проявления лекарственной волчанки исчезают после отмены причинно значимого препарата; в тяжелых случаях назначаются кортикостероидные препараты.
Общие сведения
Лекарственная волчанка (лекарственный волчаночный синдром) – симптомокомплекс, обусловленный побочным действием лекарственных средств и регрессирующий после их отмены. Лекарственная волчанка по своим клиническим проявлениям и иммунобиологическим механизмам сходна с системной красной волчанкой. В ревматологии лекарственная волчанка диагностируется примерно в 10 раз реже, чем идиопатическая СКВ. В большинстве случаев лекарственно-индуцированный волчаночноподобный синдром развивается у пациентов в возрасте старше 50 лет, практически с одинаковой частотой у мужчин и женщин.

Причины лекарственной волчанки
Развитие лекарственной волчанки может провоцироваться длительным применением или высокими дозировками большого круга лекарственных препаратов. К медикаментам с известным побочным эффектом относятся антигипертензивные (метилдопа, гидралазин, атенолол), противоаритмические (новокаинамид), противотуберкулезные (изониазид), противосудорожные средства (гидантоин, фенитоин), сульфаниламиды и антибиотики (пенициллин, тетрациклин), нейролептики (хлорпромазин), соли лития, золота и другие препараты. Чаще всего лекарственная волчанка возникает у пациентов, страдающих артериальной гипертензией, аритмией, туберкулезом, эпилепсией, ревматоидным артритом, инфекционными заболеваниями и принимающих перечисленные препараты. Возможно развитие волчаночноподобного синдрома у женщин, длительно применяющих оральные контрацептивы.
Патогенез лекарственной волчанки связывается со способностью названных лекарственных препаратов вызывать в организме образование антинуклеарных антител (АНА). Большую роль в предрасположенности к патологии играет генетическая детерминация, а именно – ацетилирующий фенотип пациента. Медленное ацетилирование данных препаратов ферментами печени сопровождается выработкой более высоких титров AHA и более частым развитием лекарственной волчанки. Вместе с тем, у больных с волчаночным синдромом, индуцированным новокаинамидом или гидралазином, выявляется медленный тип ацетилирования.
В целом вероятность развития лекарственной волчанки зависит от дозы препарата и длительности фармакотерапии. При продолжительном приеме лекарственного средства у 10-30% пациентов, имеющих в сыворотке крови антинуклеарные антитела, развивается волчаночноподобный синдром.
Симптомы лекарственной волчанки
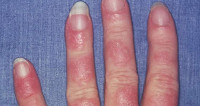
В клинике лекарственной волчанки преобладают общие проявления, суставной и кардио-пульмональный синдромы. Заболевание может манифестировать остро или постепенно с таких неспецифических симптомов, как недомогание, миалгия, лихорадка, незначительная потеря массы тела. 80% пациентов беспокоят артралгии, реже – полиартриты. У пациентов, принимающих противоаритмические средства (прокаинамид) наблюдаются серозиты (экссудативный плеврит, перикардит), тампонада сердца, пневмонит, асептические инфильтраты в легких. В ряде случаев возможно развитие лимфаденопатии, гепатомегалии, появление эритематозных высыпаний на коже.
В отличие от идиопатической системной красной волчанки, при лекарственно индуцированном синдроме редко встречаются бабочковидная эритема на щеках, язвенный стоматит, синдром Рейно, алопеция, нефротический синдром, неврологические и психические расстройства (судорожный синдром, психозы). Вместе с тем, для лекарственной волчанки, вызванной приемом апрессина, характерно развитие гломерулонефрита.
Диагностика лекарственной волчанки
От момента появления первых клинических симптомов лекарственной волчанки до постановки диагноза нередко проходит от нескольких месяцев до нескольких лет. В течение этого времени пациенты могут безрезультатно обследоваться у пульмонолога, кардиолога, ревматолога по поводу отдельных проявлений синдрома. Правильная постановка диагноза возможна при всесторонней оценке клинической симптоматики, сопоставлении признаков болезни с приемом определенных лекарственных средств, проведении иммунологических тестов.
Наиболее специфичными лабораторными критериями, указывающими на лекарственную волчанку, служит наличие в крови антинуклеарных антител (антител к гистонам), антинуклеарного фактора, антител к односпиральной ДНК, LE-клеток, снижение уровня комплемента. Менее специфичны для волчаночного синдрома, но высокоспецифичными для СКВ, являются антитела к ds ДНК, анти-Ro/SS-A, Ат к Sm-антигену, анти-La/SS-B. Дифференциальную диагностику лекарственной волчанки необходимо осуществлять с идиопатической СКВ, злокачественными опухолями легких и средостения.
Лечение лекарственной волчанки
Отмена лекарственного препарата, вызвавшего лекарственную волчанку, приводит к постепенному регрессу клинико-лабораторных признаков синдрома. Исчезновение клинической симптоматики обычно происходит в течение нескольких дней или недель после прекращения приема лекарственного средства. Антинуклеарные антитела исчезают медленнее - в течение нескольких месяцев (иногда до 1 года и дольше). С целью купирования суставного синдрома возможно назначение нестероидных противовоспалительных средств. При тяжелом течении лекарственной волчанки, длительной персистенции клинических симптомов обосновано назначение глюкокортикоидов.
Во избежание развития лекарственной волчанки не следует самопроизвольно и бесконтрольно принимать медикаменты; назначение фармакологических средств должно быть обоснованным и согласованным с лечащим врачом. Для предотвращения рецидива волчаночного синдрома необходима адекватная замена причинно значимого препарата альтернативным лекарственным средством.
Системная красная волчанка (СКВ) – аутоиммунное заболевание, этиология которого остается неизвестной. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-
Systemic lupus erythematosus: alertness in the practice of a dermatologist / M. M. Tlish, Zh. Yu. Naatyzh1, T. G. Kuznetsova, E. A. Chernenko /State Budgetary educational institution of higher professional education Kuban State Medical University of the Ministry of Healthcare of the Russian Federation, Krasnodar, Russia
Abstract. Systemic lupus erythematosus (SLE) is an autoimmune disease, the etiology of which remains unknown. Skin syndrome in SLE is often of paramount diagnostic value – skin lesion is the earliest symptom in 20-30% of cases, and in 60-70% it manifests itself at various stages of the course of the disease, which leads to the patient's primary referral to a dermatologist. Frequent diagnostic errors are due to the absence of clinical symptoms of systemic lesions in the presence of cutaneous manifestations of lupus erythematosus (LE). In this case, laboratory tests are an integral part of the algorithm for managing patients with LE at the stage of contacting a dermatologist. The most specific laboratory test is the determination of antinuclear antibodies by an indirect immunofluorescence reaction, referred to as antinuclear factor (ANF). An elevated ANF titer is included in the list of diagnostic criteria for SLE, its detection allows one to suggest a diagnosis of SLE and determine a further algorithm for the provision of medical care. The article presents two clinical cases illustrating that against the background of an isolated skin lesion and the absence of visible somatic pathology, abnormalities in immunological tests were identified. This made it possible to suspect the systemic course of the process at an early stage and refer patients to a rheumatologist's consultation, where the diagnosis of SLE was confirmed. For citation: Tlish M. M., Naatyzh Zh. Yu., Kuznetsova T. G., Chernenko E. A. Systemic lupus erythematosus: alertness in the practice of a dermatologist // Lechaschy Vrach. 2020; vol. 23 (11): 23-26. DOI: 110.26295/OS.2020.35.78.005
Согласно современным представлениям, системная красная волчанка (СКВ) – аутоиммунное заболевание неустановленной этиологии, характеризующееся гиперпродукцией органонеспецифических аутоантител с развитием иммуновоспалительного повреждения тканей внутренних органов [1]. Широкий ряд вырабатываемых аутоантител и их прямое или опосредованное воздействие на клеточные мишени обуславливают многообразие клинических проявлений при красной волчанке (КВ) [2]. СКВ может проявляться изолированным или сочетанным поражением систем и органов, включающим поражение кожи и слизистых оболочек (волчаночная бабочка, дискоидная эритема, фотосенсибилизация, алопеция, телеангиэктазии, сетчатое ливедо, язвы в полости рта), сердечно-сосудистой системы (перикардит, миокардит, эндокардит, коронарит), почек (волчаночный нефрит), центральной нервной системы (судороги, психоз), опорно-двигательного аппарата (артралгии, артриты), легких (плеврит, волчаночный пневмонит), гематологическими нарушениями (гемолитическая анемия, лейкопения, тромбоцитопения) и т. д. [3].
Ключевую роль в диагностике СКВ играет обнаружение клинических проявлений заболевания и данные лабораторной диагностики [3]. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-70% проявляется на различных этапах течения болезни, что приводит к первичному обращению больного именно к дерматологу [4]. Поражения кожи при СКВ полиморфны и представлены различными изменениями – от незначительных телеангиэктазий до буллезных поражений [2]. Выделяют волчаночно-специфичные и волчаночно-неспецифичные поражения кожи, последние встречаются в несколько раз чаще. К волчаночно-специ-фичным относят различные проявления хронической, подострой и острой КВ [5]. Группа неспецифических поражений включает: фотосенсибилизацию, лейкоцитокластический и уртикарный васкулит, телеангиэктазии, сетчатое ливедо, злокачественный атрофический папулез и синдром Рейно [5]. Широкая вариабельность клинических проявлений кожного синдрома обуславливает необходимость проведения тщательного дифференциального диагноза [1].
Важным инструментом ранней диагностики системных заболеваний является обнаружение аутоантител с помощью лабораторных тестов [3]. Наиболее специ-фичными для СКВ являются антинуклеарные антитела (АНА) – это гетерогенная группа аутоантител к компонентам клеточного ядра, среди которых выделяют антитела к двуспиральной дезоксирибонуклеиновой кислоте (ДНК), гистонам, нуклеосомам, экстрагируемым ядерным антигенам, ядрышковым антигенам и другим клеточным структурам [6]. Стандартным методом обнаружения группы АНА является непрямая реакция иммунофлюоресценции (НРИФ) с использованием линии эпителиальных клеток аденокарциномы гортани человека (HЕp-2) [7]. Определение АНА методом НРИФ принято обозначать как антинуклеарный фактор (АНФ), содержание которого оценивается по максимальному выявленному титру в сыворотке крови, с указанием интенсивности и типа флюоресценции [8]. Количественное увеличение титра свыше 1:160 входит в перечень диагностических критериев СКВ согласно рекомендациям Американской коллегии ревматологов (American College of Rheumatology, ACR) и Европейской лиги борьбы с ревматизмом (European League Against Rheumatism, ULAR) и используется для оценки активности процесса, прогноза, так как является предиктором развития СКВ на доклинической стадии [8].
Длительное формирование патогномоничного клинического симптомокомплекса СКВ, отсутствие проведения необходимых лабораторных исследований и междисциплинарного взаимодействия являются причиной частых диагностических ошибок, приводящих к отсутствию своевременной противовоспалительной и иммуносупрессивной терапии у врача-ревматолога. Учитывая вышесказанное, считаем целесообразным привести собственные клинические наблюдения.
Клиническое наблюдение № 1
Больная М., 27 лет, считает себя больной с июля 2019 г., когда после длительного отдыха на побережье появились высыпания на коже лица. Обратилась к дерматологу по месту жительства, где был выставлен диагноз: «Розацеа, папулопустулезный подтип, среднетяжелое течение». Получала курсовое лечение (доксициклин, метронидазол гель). Видимого улучшения пациентка не отмечала, процесс на коже продолжал прогрессировать, в связи с чем обратилась на кафедру дерматовенерологии ФГБОУ ВО КубГМУ Минздрава России.
Данные со стороны других органов и систем: предъявляет жалобы на ноющие боли в мелких суставах кистей и коленных суставах, чувство утренней скованности. Соматически не обследована.
Объективно: кожный патологический процесс носит ограниченный симметричный характер, локализуется на коже крыльев носа, щек, подбородка. Представлен: эритематозные пятна, чешуйки, телеангиэктазии.
На коже лица (в области крыльев носа, щек, подбородка) расположены ярко-розовые эритематозные очаги, с четкими границами, слегка инфильтрированные, правильной округлой формы, диаметром 3-4 см, покрытые небольшим шелушением в центре очагов; в периферической зоне очагов визуализируются телеангиэктазии (рис. 1). Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского).
.jpg)
Определена биодоза 20 секунд.
С предположительным диагнозом «Дискоидная красная волчанка?» больная была направлена на гистоморфологическое исследование кожи.
Результаты гистоморфологического исследования кожи из патологического очага на правой щеке: фолликулярный гиперкератоз; эпидермис с тенденцией к атрофии; вакуольная дистрофия клеток базального слоя. Под эпидермисом сосуды расширены. Во всех отделах дермы – густые диффузные и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов и плазмоцитов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина может соответствовать красной волчанке.
Данные общеклинических исследований: общий и биохимический анализ крови – показатели в пределах нормы; общий анализ мочи – показатели в пределах нормы.
Настораживающими факторами в плане трансформации кожной формы в системный процесс у пациентки М. явились: дебют заболевания в молодом возрасте, длительная инсоляция в анамнезе, II фототип кожи, биодоза 20 секунд, наличие выраженного суставного синдрома.
Для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 1:320 титр (норма менее 160); мелкогранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 53 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) – 10,13 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 12,68 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
С полученными данными больная направлена к ревматологу в Краевую клиническую больницу № 2, где был подтвержден диагноз СКВ. Больная взята на диспансерный учет ревматологом для определения дальнейшей тактики ведения и лечения.
Клиническое наблюдение № 2
Пациентка В., 66 лет, считает себя больной с апреля 2018 г., когда впервые появились высыпания на коже щек и подбородка. При сборе анамнеза установлено, что больная длительное время проживала в северном регионе и после переезда в Краснодарский край начала отмечать появление высыпаний. Самостоятельно использовала бетаметазон и декспантенол. Отмечала временное улучшение, но в весенне-летний период заболевание обострялось. Обратилась к дерматологу по месту жительства, где был выставлен диагноз «стероидпровоцированная розацеа» и назначено лечение (наружные и системные антибактериальные препараты, ангиопротекторы). Видимого улучшения не наблюдала, в связи с чем обратилась на кафедру дерматовенерологии ФГБОУ ВО КубГМУ МЗ РФ.
Объективно: кожный патологический процесс носит распространенный характер, локализован на коже лица, шеи. Представлен: пятна, телеангиэктазии, чешуйки.
На коже лица в области щек, левой околоушной области и шеи расположены отечные эритематозные очаги розовато-красного цвета, диаметром 2–3 см, преимущественно правильно-округлой формы с небольшим шелушением, визуализируются единичные телеангиэктазии. Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского) (рис. 2).
.jpg)
С предварительным диагнозом «Дискоидная красная волчанка?» пациентка направлена на гистоморфологическое исследование.
Результаты гистоморфологического исследования кожи из патологического очага: на коже левой щеки – фолликулярный гиперкератоз; участки паракератоза; эпидермис местами атрофичен; вакуольная дистрофия клеток базального слоя эпидермиса; подэпидермальные пузыри. В сосочковом слое – отек, стенки сосудов утолщены. В дерме – густые очаговые и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина больше соответствует красной волчанке.
Данные общеклинических исследований: в общем и биохимическом анализах крови выявлены следующие отклонения – лейкоциты 3,7 × 10 9 /л; холестерин 8,7 ммоль/л.
Учитывая длительность течения кожного патологического процесса, отсутствие результатов обследования смежных специалистов, для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 12 560 титр (норма менее 160); крупногранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 0,5 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) 16,65 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 14,68 МЕ/мл (референсные значения до 10 МЕ/мл – не обнаружено).
С полученными результатами лабораторных исследований больная была направленна на консультацию к ревматологу в Краевую клиническую больницу № 2, где был установлен диагноз: «СКВ, хроническое течение, 1-й степени активности, с поражением кожи (эритема по типу «бабочки»), иммунологическими нарушениями (антинуклеарный фактор на НЕр-2 клетках, положительный анализ крови на антитела к фосфолипидам IgG, IgM)». Больную госпитализировали в ревматологическое отделение на стационарное лечение.
Таким образом, иммунологические исследования и их комплексный анализ являются неотъемлемой составляющей алгоритма ведения больных с КВ уже на этапе обращения к врачу-дерматологу и способствуют высокому качеству оказания медицинской помощи данному контингенту больных.
Литература/References
- Тлиш М. М., Наатыж Ж. Ю., Сычева Н. Л., Кузнецова Т. Г., Иризелян Г. А., Псавок Ф. А. Системная красная волчанка: междисциплинарный подход к диагностике // Российский журнал кожных и венерических болезней. 2016; 19 (3): 141-147. [Tlish M. M., Naatyzh Zh. Yu., Sycheva N. L., Kuznetsova T. G., Irizelyan G. A., Psavok F. A. Sistemnaya krasnaya volchanka: mezhdistsiplinarnyy podkhod k diagnostike [Systemic lupus erythematosus: an interdisciplinary approach to diagnosis] Rossiyskiy zhurnal kozhnykh i venericheskikh bolezney. 2016; 19 (3): pp. 141-147.]
- Мазуров В. И., ред. Диффузные болезни соединительной ткани: руководство для врачей. СПб: СпецЛит, 2009. 192 с. [Mazurov V. I., red. Diffuznyye bolezni soyedinitel'noy tkani: rukovodstvo dlya vrachey. [Diffuse connective tissue diseases: a guide for physicians.] SPb: SpetsLit, 2009. P. 192.]
- Насонов Е. Л., ред. Клинические рекомендации по ревматологии. 2-е изд., испр. и доп. М.: ГЭОТАРМедиа, 2010. 429 с. [Nasonov Ye. L., red. Klinicheskiye rekomendatsii po revmatologii. [Clinical practice guidelines to rheumatology.] 2-ye izd., ispr. i dop. M.: GEOTARMedia, 2010. P. 429.]
- Романова Н. В., Шилкина Н. П. Клинико-иммуноло-гическая характеристика кожного синдрома у больных красной волчанкой // Российский журнал кожных и венерических болезней. 2005; (4): 45-48. [Romanova N. V., Shilkina N. P. Kliniko-immuno-logicheskaya kharakteristika kozhnogo sindroma u bol'nykh krasnoy volchankoy [Clinical and immunological characteristics of skin syndrome in patients with lupus erythematosus] Rossiyskiy zhurnal kozhnykh i venericheskikh bolezney. 2005; (4): pp. 45-48.]
- Тлиш М. М., Наатыж Ж. Ю., Сычева Н. Л., Кузнецова Т. Г. Системная красная волчанка в практике дерматолога // Клиническая медицина. 2018; 96 (3): 277-281. [Tlish M. M., Naatyzh Zh. Yu., Sycheva N. L., Kuznetsova T. G. Sistemnaya krasnaya volchanka v praktike dermatologa [Systemic lupus erythematosus in the practice of a dermatologist] Klinicheskaya meditsina. 2018; 96 (3): pp. 277-281.]
- Клюквина Н. Г. Клиническое значение лабораторных нарушений при системной красной волчанке // Современная ревматология. 2014; (2): 41-47. [Klyukvina N. G. Klinicheskoye znacheniye laboratornykh narusheniy pri sistemnoy krasnoy volchanke [Clinical significance of laboratory disorders in systemic lupus erythematosus] Sovremennaya revmatologiya. 2014; (2): pp. 41-47.]
- Александрова Е. Н., Новиков А. А., Насонов Е. Л. Рекомендации по лабораторной диагностике ревматических заболеваний Общероссийской общественной организации «Ассоциация ревматологов России» – 2015 // Современная ревматология. 2015; 9 (4): 25-36. [Aleksandrova Ye. N., Novikov A. A., Nasonov Ye. L. Rekomendatsii po laboratornoy diagnostike revmaticheskikh zabolevaniy Obshcherossiyskoy obshchestvennoy organizatsii «Assotsiatsiya revmatologov Rossii» – 2015 [Recommendations for laboratory diagnostics of rheumatic diseases of the All-Russian public organization «Association of rheumatologists of Russia» – 2015] Sovremennaya revmatologiya. 2015; 9 (4): pp. 25-36.]
- Александрова Е. Н., Новиков А. А., Верижникова Ж. Г., Лукина Г. В. Современный взгляд на проблемы исследования антинуклеарных антител при системной красной волчанке (обзор литературы) // Клиническая лабораторная диагностика. 2018; 63 (6): 340-348. [Aleksandrova Ye. N., Novikov A. A., Verizhnikova Zh. G., Lukina G. V. Sovremennyy vzglyad na problemy issledovaniya antinuklearnykh antitel pri sistemnoy krasnoy volchanke (obzor literatury) [Modern view on the problems of studying antinuclear antibodies in systemic lupus erythematosus (literature review)] Klinicheskaya laboratornaya diagnostika. 2018; 63 (6): pp. 340-348.]
М. М. Тлиш, доктор медицинских наук, профессор
Ж. Ю. Наатыж 1 , кандидат медицинских наук
Т. Г. Кузнецова, кандидат медицинских наук
Е. А. Черненко
ФГБОУ ВО КубГМУ Минздрава России, Краснодар, Россия
Системная красная волчанка: настороженность в практике дерматолога/ М. М. Тлиш, Ж. Ю. Наатыж, Т. Г. Кузнецова, Е. А. Черненко
Для цитирования: Тлиш М. М., Наатыж Ж. Ю., Кузнецова Т. Г., Черненко Е. А. Системная красная волчанка: настороженность в практике дерматолога // Лечащий Врач. 2020; т. 23 (11), 23-26. DOI: 110.26295/OS.2020.35.78.005
Теги: аутоиммунное заболевание, кожный синдром, алгоритм лечения
Читайте также:

